咸味作为五种基本味之一,是“百味之王”。食盐作为应用最广泛的咸味剂,具有重要的调味特性,在维持人体渗透压和保障人体机能中发挥关键作用,但摄入过量食盐会对肾脏、大脑、血管及免疫系统造成负担[1]。为了提高全民健康水平,国家卫生计生委《全民健康生活方式行动方案(2017—2025年)》中提出了“三减”政策,提出每日人均食盐摄入量为5 g,但目前我国人均每日食盐摄入量高达9.3 g,远高于推荐摄入量[2]。通过优化食盐结构与分布、金属氯化物代替钠盐以及使用风味增强剂等多种策略以减少食盐的摄入,但以上方法会造成成本增加,或者替代品带来金属味和苦味等问题。
咸味肽来源非常广泛,从天然动植物微生物中提取的咸味肽,具有广泛的应用前景和经济价值。作为一类小分子肽,咸味肽来源广泛、结构简单、分子质量小,可更好地与味觉受体进行结合,并可在没有Na+的情况下感知咸味,是一种良好的食盐替代物。其中,酵母提取物(yeast extract,YE)是许多咸味肽和咸味增强肽的主要来源,含有30多种味觉感知肽,参与鲜味和咸味的感知,且能够在不降低咸味强度的情况下抑制不良风味,达到减盐的效果[3]。但YE中蛋白质分子质量分布不均匀,小分子肽占比较少,因此可以通过酶解等手段以获更多的优良咸味肽[4],具有较大的发展空间。
许多受体或离子通道可以感知咸味,包括跨膜通道样4(transmembrane channel like 4,TMC4)蛋白模型、上皮钠通道和瞬时受体电位香草酸等[5]。其中,TMC4是一种具有8个跨膜结构域的新型氯离子通道,不仅可以响应高浓度的NaCl[6],也可激活TMC4表现出增强咸味的能力,因此,TMC4模型成为识别和筛选增强咸味物质的有力工具。为了探讨咸味肽与TMC4受体的关系,SHEN等[7]通过计算机方法构建了TMC4模型,根据变构位点和感官评价鉴定出YE中的咸味肽,包括丙氨酸-天冬酰胺(alanine-asparagine,PN)、天冬酰胺-丝氨酸-谷氨酸(asparagine-serine-glutamate,NSE)、天冬酰胺-谷氨酸(asparagine-glutamate,NE)和丝氨酸-脯氨酸-谷氨酸(serine-proline-glutamate,SPE)等。但关于特定咸味肽与TMC4相互作用的研究仍较少。因此,研究TMC4与酵母源咸味肽之间的分子相互作用,为明确咸味肽的呈味机制具有重要意义。
本研究以YE为原料,利用中性蛋白酶和风味酶两步酶解法,通过分离、纯化制备新型咸味肽,并利用TMC4模型分子对接阐明咸味肽的味觉机制,进一步结合生物信息学方法筛选咸味肽。为酵母源咸味肽筛选和开发钠盐替代品的研究提供理论基础。
1 材料与方法
1.1 材料与仪器
YE,安琪酵母股份有限公司;风味酶(30 000 U/g)、中性蛋白酶(5 000 U/g)、柠檬酸、细胞色素、抑肽酶、杆菌肽、乙氨酸-乙氨酸-酪氨酸-精氨酸、乙氨酸-乙氨酸-乙氨酸、Sephadex G-10,上海源叶生物科技有限公司;食品级味精,莲花控股股份有限公司;咖啡因,山东聚康生物科技有限公司;NaCl,中国盐业股份有限公司;NaOH、蔗糖,辽宁泉瑞试剂有限公司。
XPR205/AC分析天平,梅特勒-托利多国际有限公司;H1850R合式高速冷冻离心机,长沙湘仪离心机仪器有限公司;SHJ-4D恒温水浴锅,常州金坛良友仪器有限公司;GE5640超滤仪,吉林海普科技开发有限公司;全自动蛋白纯化系统,美国GE HealthcareL集团;SA402B型电子舌,日本Insent公司;液相色谱串联质谱系统(liquid chromatography-tandem mass spectrometry,LC-MS/MS),美国Thermo公司。
1.2 酵母咸味肽的制备与纯化
1.2.1 咸味肽的制备
根据前期实验结果,选择中性蛋白酶和风味蛋白酶采用双酶两步法酶解YE。将YE溶解于超纯水中配制成质量浓度为100 mg/mL溶液。首先在YE溶液中添加中性蛋白酶(酶与YE比为1∶150,g∶mL,pH 7)、60 ℃的条件下酶解5 h;调节pH值为6.5,再添加风味酶(酶与YE比为1∶40,g∶mL)、55 ℃酶解4 h。酶解结束后,将酶解液于95 ℃灭酶10 min,在8 000 r/min条件下离心15 min后,取酶解物上清液(enzymatic hydrolysate,EH)于4 ℃保存。
1.2.2 超滤
利用1、3、5 kDa超滤膜进行EH的超滤分级。首先,将EH通过5 kDa超滤膜,将其透过液利用脱盐柱脱盐,再分别用3、1 kDa的超滤膜进行超滤,过滤后收集得到3个组分,分别命名为UF1(3~5 kDa)、UF2(1~3 kDa)和UF3(<1 kDa)。设置转速为40 r/min,温度为40 ℃旋蒸浓缩后,冷冻干燥,于-20 ℃冷冻保存。利用感官评价选出咸味较高的组分进一步分离纯化。
1.2.3 凝胶过滤色谱分离
选择超滤后咸味分值最高的组分进行凝胶过滤色谱(gel filtration chromatography,GFC)。将上述冻干样品与超纯水配制成50 mg/mL溶液,并通过0.45 μm过滤膜。采用全自动蛋白纯化系统,配备Sephadex G-10凝胶层析柱。取1 mL过滤后的溶液加入凝胶柱中,以超纯水为洗脱液,流速0.60 mL/min,紫外检测波长220 nm进行分离。收集各个峰的组分进行冷冻干燥,于-20 ℃冷冻保存,用于感官评价和电子舌测定。
1.3 酵母咸味肽鉴定
1.3.1 分子质量分布
采用Waters 2695高效液相色谱系统,测定EH和GFC咸味值相对较高组分的相对分子质量分布。色谱条件为:TSK gel G2 kSWXL 300 mm×7.8 mm色谱柱,柱温30 ℃。流动相为乙腈∶水∶三氟乙酸=40∶60∶0.1(体积比),于紫外线220 nm检测,流速为0.5 mL/min。
1.3.2 氨基酸序列鉴定
采用ZipTip C18对GFC咸味值相对较高的组分进行脱盐、真空干燥和LC-MS/MS分析。色谱柱为PepMap RSLC C18(75 μm × 150 mm,2 μm,100 Å),流动相A为0.1%甲酸水溶液,流动相B为0.1%甲酸乙腈。进样4 μL,紫外检测波长为214 nm,流速为0.25 μL/min。洗脱梯度为:0~8 min 0%~10% B,8~33 min 10%~15% B,33~43 min 15%~28% B,43~50 min 28%~40% B,50~65 min 40%~95% B,65~70 min 95%~5% B。
采用电喷雾电离作为电离源进行质谱分析。质谱在300~1 400 m/z扫描。碰撞气体采用N2,流速250 μL/min。主质谱分辨率7×104(m/z≤200),自动增益控制目标5×104,次质谱碰撞能量12~14 eV。质谱误差容限0.05 Da,二级质谱分辨率1.75×104(m/z≤200)。使用PEAKS 12.0软件和Uniprot蛋白质组数据库(www.uniprot.org;蛋白质组UP000008827_20240125.fasta)进行数据分析,用于多肽鉴定和半定量分析。
1.4 呈味机制与咸味评价
1.4.1 TMC4模型的构建及分子对接
按照ZHAO等[8]的方法进行TMC4模型的构建与评价。利用PyMOL(https://pymol.org/2/)构建已识别肽的3D结构进行分子对接,通过Amber14分子力场优化咸味肽的三维结构,以满足最低能量构象。采用Autodock Tools软件(http://vina.scripps.edu/)对受体蛋白进行脱去蛋白结构中的结晶水分子,添加极性氢原子,修饰氨基酸以及优化能量和调整力场参数。利用PyRx软件(https://pyrx.sourceforge.io/)内部的vina进行对接,采用全局对接模式。使用Discovery Studio 2019和MOE(molecular operating environment)进行可视化分析。
1.4.2 筛选优质咸味肽
采用计算机工具鉴定具有良好安全性的候选咸味肽。topinpred工具(https://webs.iiitd.edu.in/raghava/toxinpred/index.html)用于筛选潜在毒性,pLM4Alg(https://f6wxpfd3 sh.us-east-1.awsapprunner.com)用于评估致敏性,Expasy ProtParam(https://web.expasy.org/protparam/)用于评估肽稳定性[9]。
1.4.3 感官评价
感官测试小组由10名经验丰富的成员组成(女5名,男5名,年龄22~30岁)。在实验开始前,告知小组成员告知参与评价的目标、详细的实验程序和感官要求。具体评价标准和分值情况如图1所示。
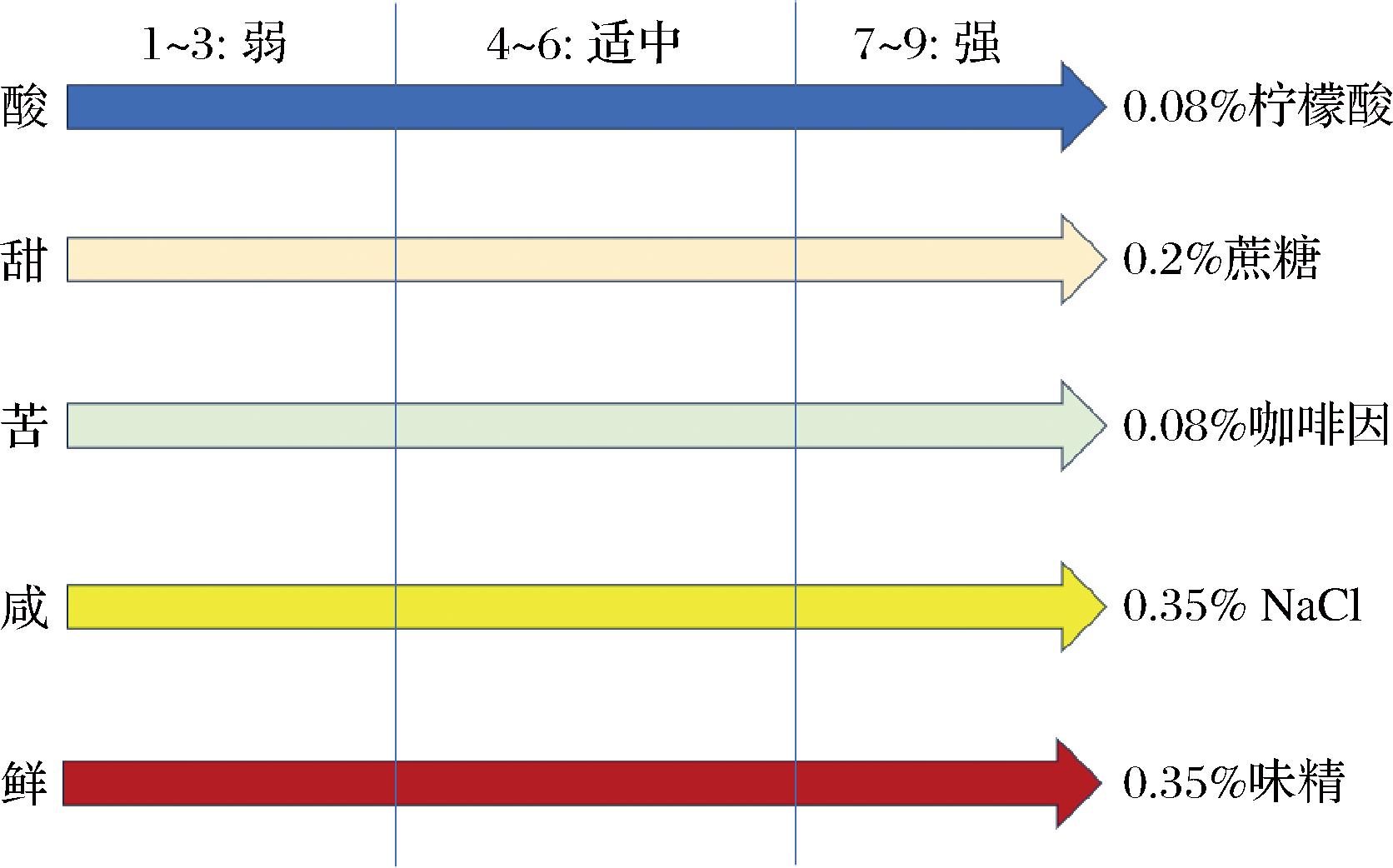
图1 感官评价标准
Fig.1 Sensory evaluation criteria
1.4.4 电子舌评价
将GFC分离后各个峰的冻干样品制备质量浓度为600 mg/L的溶液,参比溶液为30 mmol/L KCl溶液+0.3 mmol/L酒石酸溶液。将配制好的溶液倒入电子舌专用量杯中,室温下测量3次。仪器在第1次测量后稳定,最后3个信号数据点的平均值作为样品的味觉信号强度。无味点即参比溶液的输出,参比溶液由KCl和酒石酸组成味觉值,因此酸味的无味点为-13,咸味的无味点为-6,其他无味点均为0。以此为基准,当样品的味觉值低于无味点时说明样品无该味道,反之则有该味道。
1.5 数据处理
采用SPSS 25.0软件进行统计分析,使用独立样本t检测进行显著性分析,数据均采用“平均值±标准差”表示,P<0.05表示显著差异,P<0.01表示极显著差异,采用Origin 2024作图。
2 结果与分析
2.1 酶解产物分子质量分布
由表1可知,EH中绝大多数的多肽分子质量为<1 kDa,占比95.23%,显著高于3~5 kDa和1~3 kDa中的肽段含量。一般情况下,低分子质量(<1 kDa)肽中咸味肽的占比较高[10]。由于单个氨基酸的分子质量通常在100~200 Da,EH中低分子质量肽主要分布范围为180~1 000 Da,占比为52.00%,呈现较高的比例。GAO等[11]也发现,利用双酶酶解羊肚菌,可以得到较小分子质量的肽,比单酶酶解获得的小分子质量肽更多,并且两步酶解不仅可以提高咸味和鲜味,还可以降低苦味。因此,中性蛋白酶和风味酶两步酶解的更加充分。
表1 酶解产物的分子质量分布与百分比
Table 1 Molecular mass distribution and percentage of the enzymatic hydrolysis products

分子质量分布范围百分比/%>5 kDa0.093~5 kDa0.131~3 kDa4.540.5~1 kDa17.03180~500 Da34.97<180 Da43.23
2.2 超滤分离
超滤是一种膜分离技术,在多肽分离中,超滤可以有效去除不溶性底物、蛋白质和大分子质量多肽,获得分子质量较小的肽[12]。与酶解液相比,利用5 kDa超滤膜处理,截留液的色泽由深棕色转变为棕黄色,溶液更为澄清;依次利用3、1 kDa超滤膜进一步分离后,透过液的色泽为浅黄色,呈现出澄清透明的状态。超滤得到的3个组分进行感官评价,根据感官评价如图2所示,组分UF3(<1 kDa)的咸味得分高于其他组分,与ZHENG等[13]结果一致。小分子多肽之所以表现出较高的咸味,可能是由于其相对较小的分子更容易与味蕾上的咸味受体结合[14]。因此选择组分UF3进行下一步分离纯化。
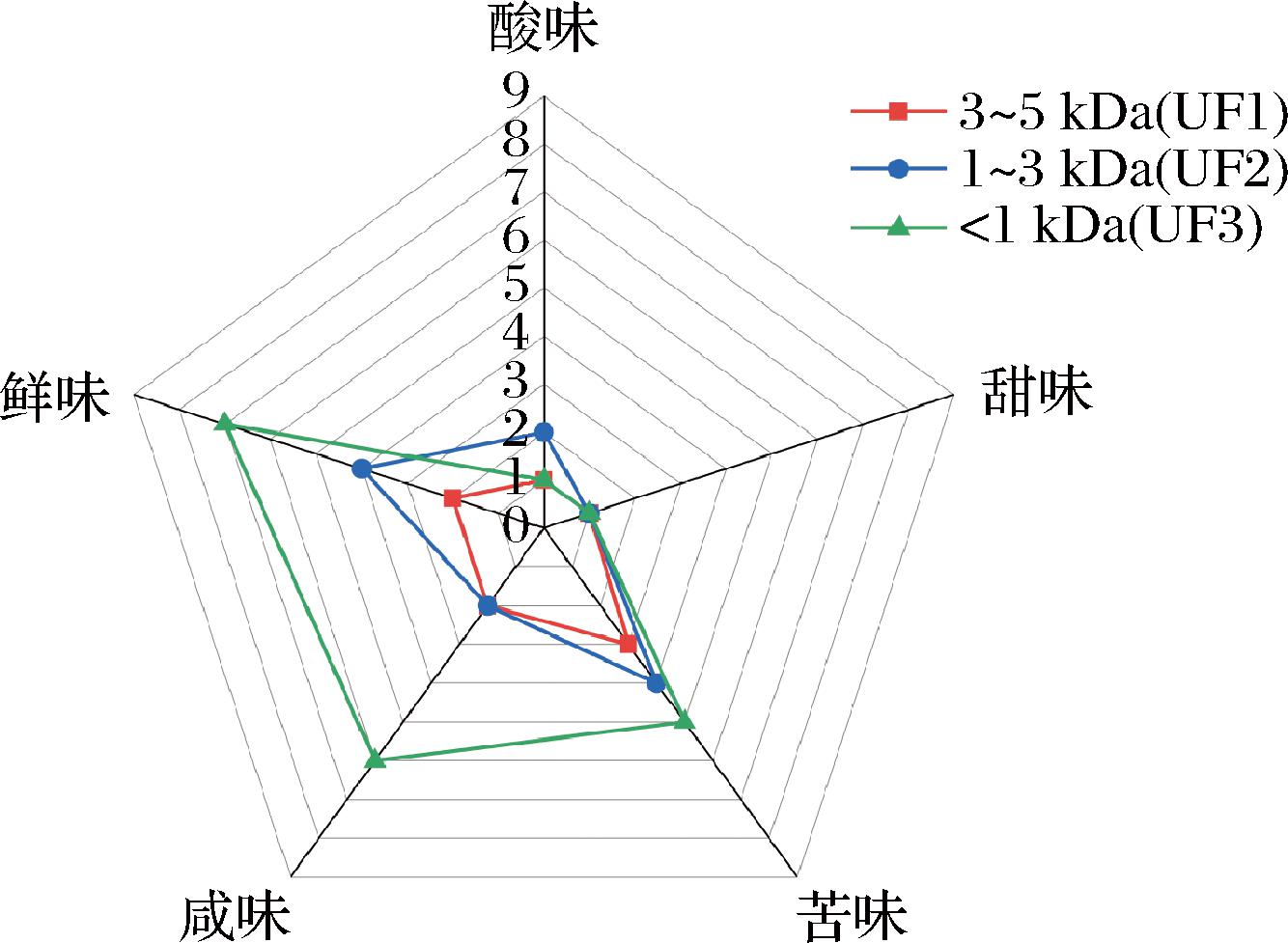
图2 超滤液的感官评价雷达图
Fig.2 Sensory evaluation radar map of UF liquid
2.3 凝胶过滤色谱分离分析
利用GFC进一步纯化咸味得分相对较强的UF3组分。由图3-a可知,在保留时间50~250 min,UF3分离得到3个组分(F1、F2和F3),各个组分的感官评价(图3-c)和电子舌分析(图3-d)结果显示,F1、F2组分咸味得分相对较高,F3组分咸味得分相对较低。此外,由图3-a可知,F1出峰时间最早,峰型窄而尖,信号值高,表明此肽段分子质量较大且纯度较高[15]。因此,本实验选择F1组分进行分子质量分布的测定。由图3-b可知,与EH相比,F1中<500 Da的多肽含量由78.20%提升至92.08%,最终选择F1组分进行氨基酸序列鉴定。
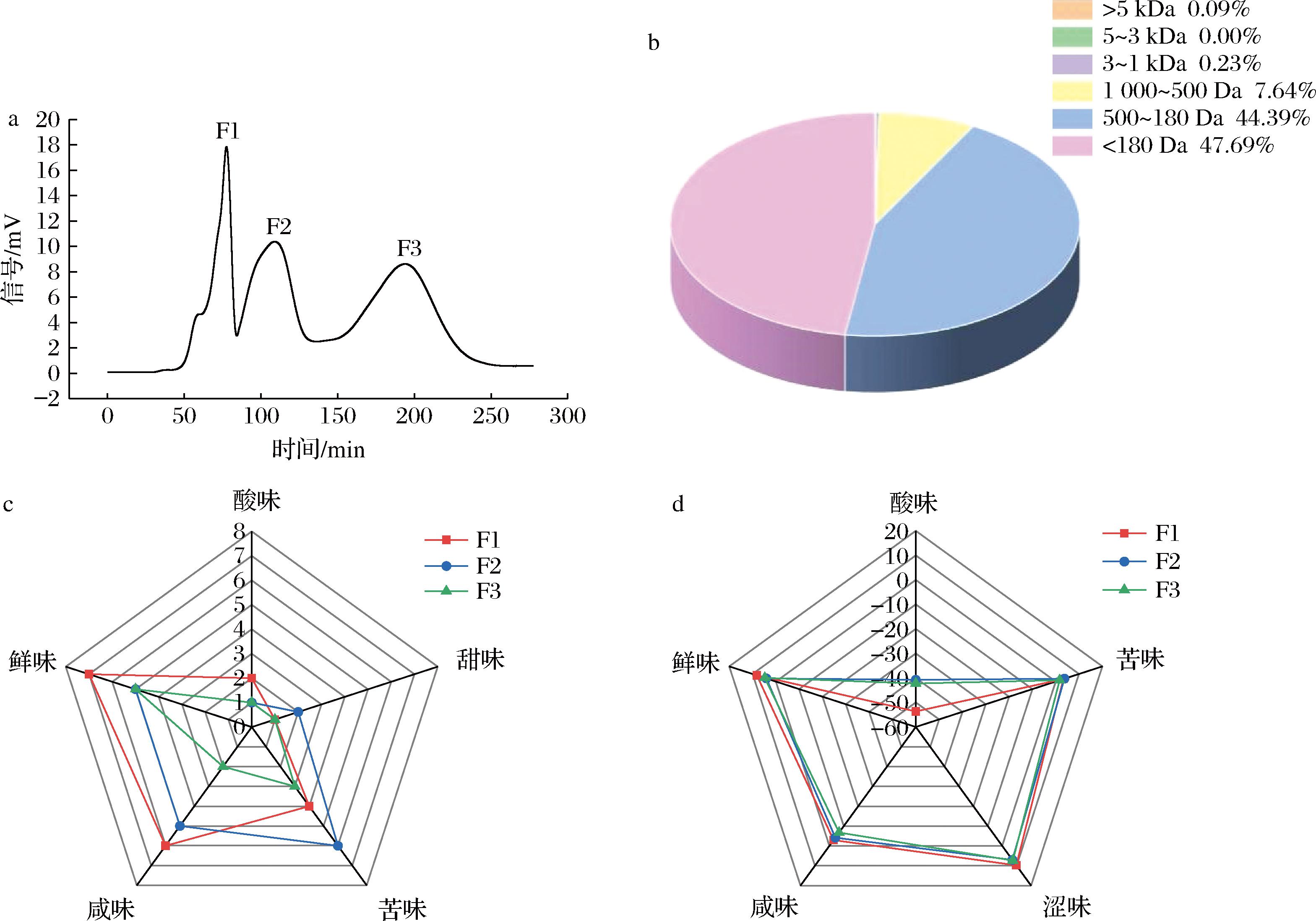
a-UF3的GFC图;b-F1的分子质量分布;c-GFC分离组分的感官评价;d-GFC分离组分的电子舌评价
图3 UF3的GFC图、F1的分子质量分布、GFC分离组分的感官和电子舌评价
Fig.3 The GFC map of UF3, the molecular mass distribution of F1, and the sensory and electronic tongue evaluation of the GFC separated components
2.4 氨基酸序列测定
采用LC-MS/MS测定F1组分的肽段序列。利用PEAKS 12.0软件进行数据库检索,共鉴定出751个肽段序列,其中最短的为4肽,最长的为10肽。由4~6个氨基酸组成占比为98.00%,其中415个为4肽。从单酶酶解物中分离纯化得到的小分子质量肽占比较低,>10肽的占66.80%[16],与本研究对比可以推测,两步酶法制备可以得到序列较短的咸味肽。
肽的咸味和强度通常受氨基酸类型、肽链长度和序列等影响[17]。研究表明,精氨酸位于C端或N端对其组成的短肽增咸效果影响显著[18]。LE等[19]也提出,Arg作为咸味增强能力的间接指标,它可能是咸味肽中的关键氨基酸。同时,鲜味氨基酸如Glu(E)和Asp(D)也可能呈现一定的咸味,咸味与鲜味之间存在正相关关系[20]。因此,根据氨基酸种类和在多肽中特定的位置、多肽得分和肽链长度,筛选59种可能的咸味肽与TMC4模型进行分子对接,结果如表2所示。
表2 组分F1的LC-MS/MS鉴定结果
Table 2 Results of LC-MS/MS identification of component F1

多肽序列多肽得分分子质量/Da多肽氨基酸数量/个多肽匹配的质量误差多肽质荷比/(m/z)多肽的电荷数/个保留时间/minKSGG26.74347.1814-1.2348.187114.057LIGV26.61400.26942.0401.277126.256GGSF26.52366.15441.1367.162115.762LFIT26.51492.29542.3493.303150.406DFGG26.46394.14940.8395.156117.408KPWEGR26.43771.40360.3386.709215.734APIGPR26.40609.36060.8305.687216.815GHRDF26.29630.28751.1316.151215.193ESAV26.28404.19144.3405.200115.639GLSP26.27372.20140.7373.208117.170VGGF26.27378.1904-0.6379.197127.976FGGA26.22350.15941.0351.167119.478LGDK26.14431.23840.7432.246116.493LPPN26.13439.24340.0440.250116.471VPYPR26.12630.34951.4316.182218.211GFSS26.02396.16540.1397.172117.377RPVPR25.98623.38750.9312.700212.988FGGR25.96435.2234-1.3436.230115.070YDGYR25.96672.28751.7337.151215.589LPWGR25.82627.34950.3314.682231.273GGFF25.81426.19041.0427.198148.234AAFP25.73404.20640.7405.214132.440KTAPGK25.65600.36061.7301.188214.736LPVGPR25.60637.39162.0319.703220.140IPPAPR25.48649.39160.7325.703216.878AGPWSR25.36672.33460.7337.175221.242DSPKYR25.29764.38261.8383.199214.116RDYR25.20608.30340.5305.159212.884GVAR25.05401.23940.6402.246114.361LHGP24.94422.22840.7423.235114.317SPFHR24.85642.32451.1322.170215.773KGAY24.77437.22740.3438.235114.298GGFG24.66336.14341.5337.151120.134VAPF24.61432.23740.7433.245139.416HVLPNR24.48734.41965.5368.219227.613KDWR24.45603.31340.8302.664215.002LPLFP24.30585.35353.2586.362152.943GPHFNP24.18667.30861.0334.662221.033KTTRR24.13660.40350.1331.209216.504HDWR24.08612.27741.5307.146216.895VAFP23.68432.23747.2433.248145.536LPKPR23.57609.39650.7305.706214.672TPKYR23.35663.3705-0.4332.692213.952TTTKR23.19605.35050.5303.68228.801GPEWR23.01643.30851.1322.662220.260GFGG22.78336.14340.4337.151115.698LPFLP22.75585.35353.2586.362152.943REYY22.67629.28140.5315.648219.069LPVPPR22.38677.42260.1339.719220.094EGFG22.30408.16541.4409.172121.349RRHR22.07623.37345.2312.695218.037
续表2
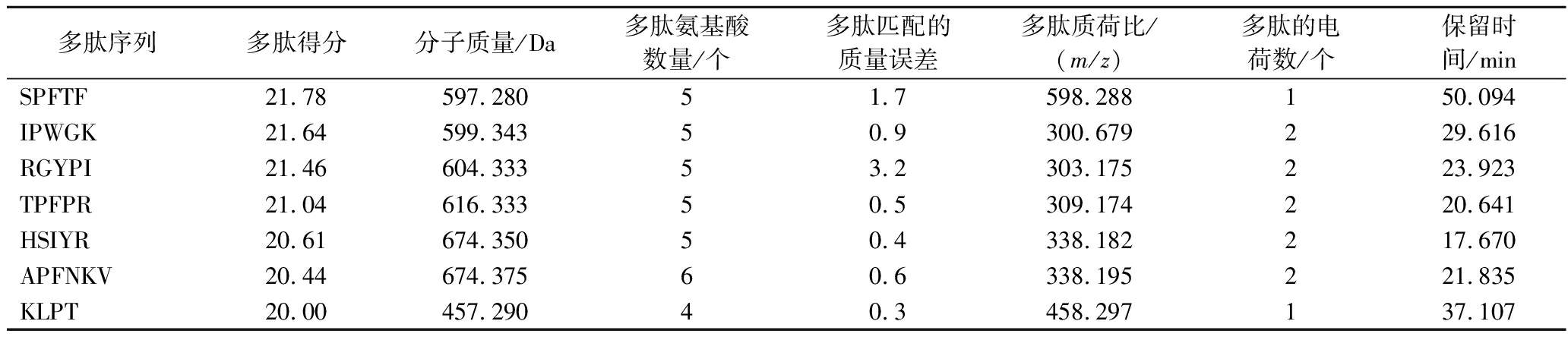
多肽序列多肽得分分子质量/Da多肽氨基酸数量/个多肽匹配的质量误差多肽质荷比/(m/z)多肽的电荷数/个保留时间/minSPFTF21.78597.28051.7598.288150.094IPWGK21.64599.34350.9300.679229.616RGYPI21.46604.33353.2303.175223.923TPFPR21.04616.33350.5309.174220.641HSIYR20.61674.35050.4338.182217.670APFNKV20.44674.37560.6338.195221.835KLPT20.00457.29040.3458.297137.107
2.5 咸味肽与TMC4的分子对接
以TMC4模型作为受体,利用深度蛋白学习模型AlphaFold2,重新构建TMC4蛋白模型,与ZHAO等[8]的TMC4模型的构建与评价结果一致(图4)。分子对接技术利用计算机模拟软件,将配体分子放置在受体的活性位点,基于几何互补和能量互补的原理,不断调整配体和受体的位置和构象等参数[21],并使用评分函数筛选最佳结合模式,主要用于预测配体与受体之间的结合方式和相互作用。常用的对接方式有刚性对接、柔性对接和半柔性对接[22],本研究采用半柔性对接技术。
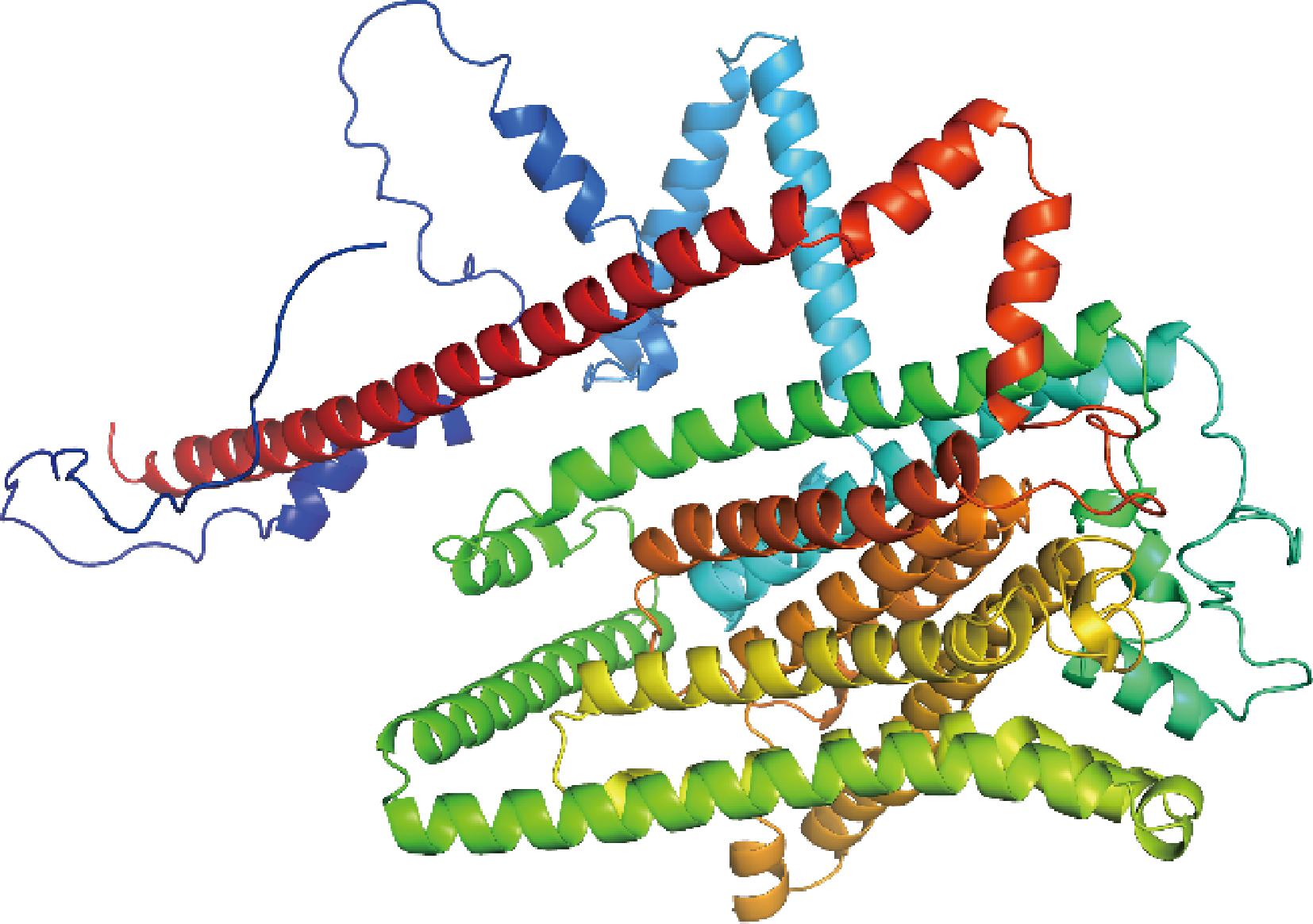
图4 TMC4模型的三维图像
Fig.4 Three-dimensional image of TMC4 model
结合能是衡量配体与受体相互作用的重要指标,结合能越低,配体与受体结合越稳定[23]。以YE中已被发现、且有效的咸味肽谷氨酸-天冬氨酸(glutamate-aspartate,ED)、苯丙氨酸-异亮氨酸(phenylalanine-isoleucine,FI)和丝氨酸-脯氨酸-谷氨酸(serine-proline-glutamate,SPE)[13]作为阳性对照,为后续选择提供参考。筛选出的59个多肽依次与咸味受体TMC4对接。通过对接得到7个结合能最低的可能咸味肽,结合能顺序为:LPWGR(-9.3 kcal/mol)
7种咸味肽与咸味受体TMC4的最佳结合构型如图5所示。其中,序列LPWGR、GPEWR、AGPWSR、IPWGK、RPVPR、TPFPR和REYY与TMC4的相互作用力总数分别为17、10、22、16、11、10和14(表3)。咸味肽与TMC4模型之间的结合相互作用包括氢键、疏水相互作用和静电相互作用[25]。其中氢键与疏水相互作用起主要作用,这与SHEN等[7]的研究结果一致。根据最佳结合模式下的相互作用力和对接位点的总结(图6),氨基酸残基如Glu531、Asp491和Leu487对氢键相互作用至关重要,而残基如Ala401和Pro409促进与TMC4模型的疏水相互作用。多肽与TMC4模型之间形成的静电相互作用主要涉及盐桥,AGPWSR与Glu531形成盐桥,IPEGK与Asp530形成盐桥。因此,咸味肽与TMC4模型的结合包括氢键、疏水作用和静电作用,这些作用力协同作用于受体,激活其功能[25]。由图6还可知,Glu531和Asp491是最常观察到的残基,而Val495、Ala401、Leu487和Asp530也是重要的结合位点。Arg151、Thr148、Tyr565、Arg424、Arg330、Tyr677和Arg580是TMC4模型与酵母提取物中的咸味肽结合的关键位点[7]。在大豆源咸味肽与TMC4模型结合中,Glu531是关键的氨基酸残基之一[8]。在本研究中,Glu531和Asp491在TMC4模型与酵母源咸味肽的结合中扮演了关键角色,与SHEN等[7]研究的结果存在差异,可能由于模型构建的模板,以及对接靶点的特殊性影响。
表3 肽与TMC4模型结合产生相互作用的类型和数量
Table 3 The type and number of interactions between peptides and TMC4 models

类型LPWGRGPEWRAGPWSRRPVPRTPFPRIPWGKREYY氢键75146587疏水相互作用7473373静电相互作用3112214
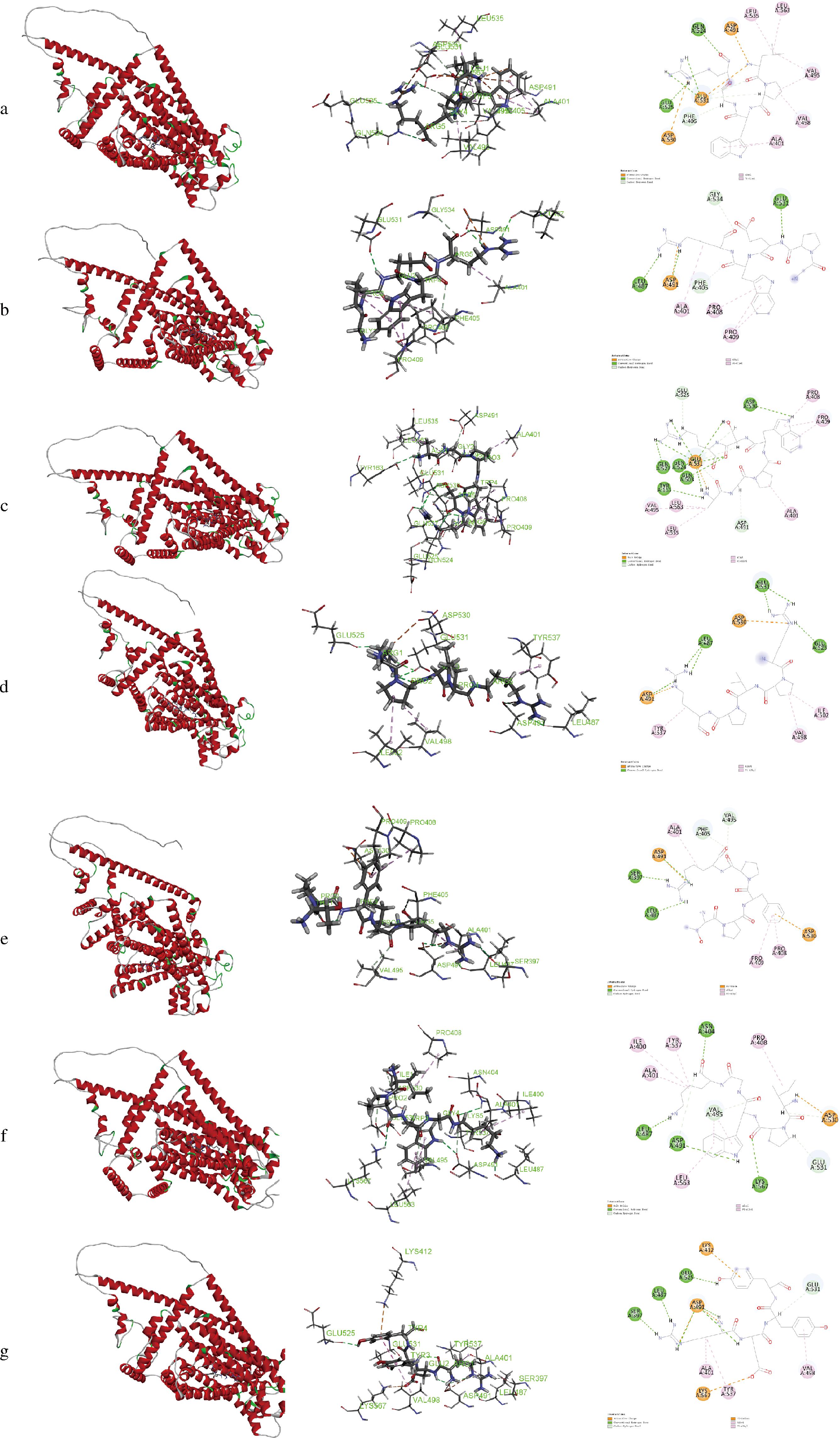
a-LPWGR;b-GPEWR;c-AGPWSR;d-RPVPR;e-TPFPR;f-IPWGK;g-REYY
图5 咸味肽与TMC4模型对接的三维和二维结构图
Fig.5 Three-dimensional and two-dimensional structure diagram of the docking between salty peptide and TMC4 model
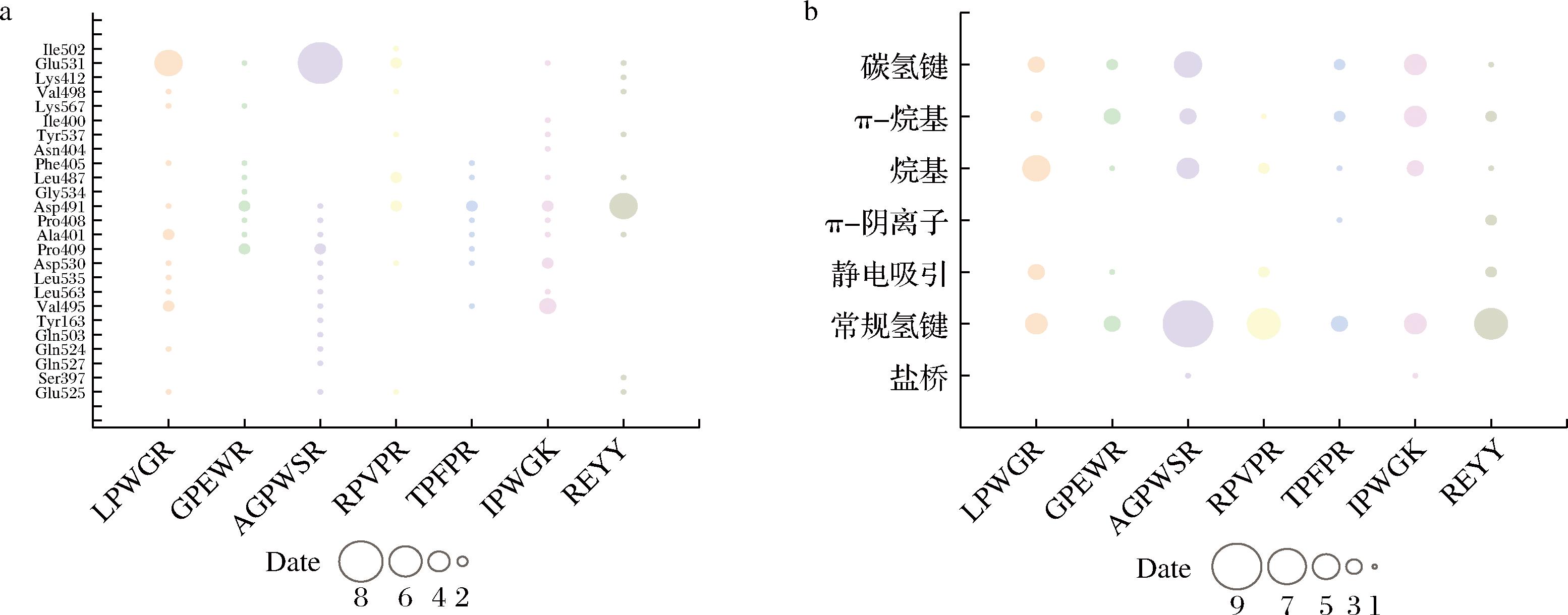
a-7种咸味肽与TMC4在单个对接位点的相互作用力总数;b-7种咸味肽与TMC4产生相互作用的类型和总数
图6 7种咸味肽与TMC4模型在单个对接位点的相互作用力总数和7种咸味肽与TMC4模型产生的相互作用的类型和总数
Fig.6 Total numbers of interactions between 7 kinds of salty peptides and TMC4 model at a single docking site and the types and total numbers of interactions between 7 kinds of salty peptides and TMC4 model
2.6 筛选和评价咸味肽
生物信息学方法可以通过开发计算机模型来预测肽和蛋白质的毒性、致敏性和稳定性。这些模型利用机器学习和定量矩阵技术,基于肽的各种特性来预测其特性。为了进一步筛选和评价优质咸味肽,本研究利用了3种计算机模型来分析这7种肽。由表4可知,LPWGER、GPEWSR、AGPWSR、IPWGK和REYY均是无毒、不致敏和稳定的咸味肽。亲水氨基酸位于C端或N端对其组成的多肽增咸效果影响显著[24],可能由于亲水性原子团在C端或N端与TMC4模型结合会产生更多数量的氢键,而氢键可能是咸味肽与TMC4模型之间重要的相互作用力[26]。从酶解豌豆蛋白得到的咸味肽YW、GEHE、ERFGP、GAGK和PGVN[27],酶解双孢菇得到的咸味肽YDPNPEK、DDWDEDAPR和DVPDGPPPE[28],以及本研究得到的7个咸味肽可以得出相同的结论,亲水氨基酸在肽段中的不同位点也影响肽段的呈味效果。与本研究得到的7个肽段的氨基酸序列相比,发酵鱼酱中分离的咸味肽RP、RA/AR、RG、RS/SR和RV/V[29],以及从牛骨中分离的咸味肽DP、DR和RE[30],这7个肽段包含已报道的咸味2肽或3肽序列,这可能是这7个肽段呈咸味的重要原因,与温青玉等[15]研究结果一致。
表4 计算机筛选咸味肽
Table 4 Computer screening for salty peptides
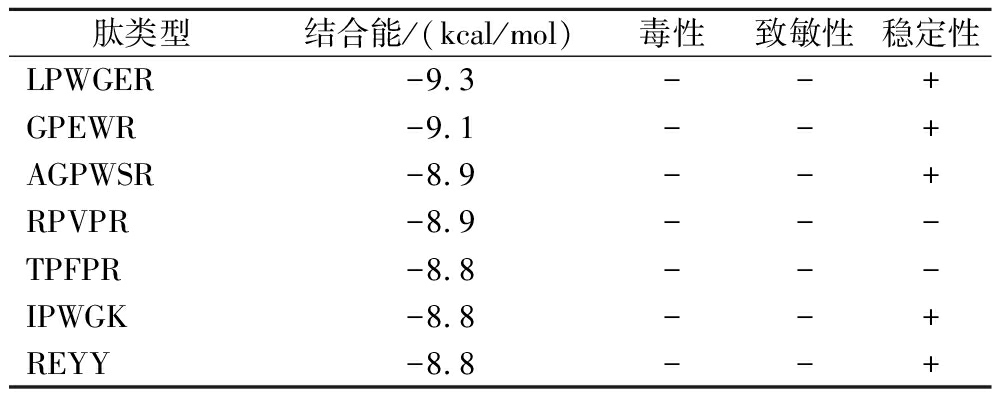
肽类型结合能/(kcal/mol)毒性致敏性稳定性LPWGER-9.3--+GPEWR-9.1--+AGPWSR-8.9--+RPVPR-8.9---TPFPR-8.8---IPWGK-8.8--+REYY-8.8--+
注:“-”表示咸味肽是通过计算机工具识别没有这种特征;“+”表示通过计算机工具鉴定出具有这些特征的咸味肽。
3 结论
本研究以YE为原料,经中性蛋白酶和风味酶两步法酶解后,通过超滤、凝胶过滤色谱和LC-MS/MS分离鉴定了YE酶解物中的咸味肽。鉴定出的751个肽段,根据筛选,最终选择59条多肽与构建的TMC4蛋白模型进行分子对接,得到7个结合能较低的肽段。对接结果表明,咸味肽与TMC4之间的结合氢键与疏水相互作用起主要作用,氨基酸残基Glu531和Asp491是最主要的结合位点。再根据生物信息学分析,最终选出LPWGER、GPEWSR、AGPWSR、IPWGK和REYY等5个无毒、无致敏性、稳定的咸味肽,此序列包含已报道的咸味2肽或3肽序列,为酵母源咸味肽与TMC4模型相互作用的研究提供了坚实的理论支撑。本研究初步探索了5个特定肽段的咸味潜力,需在复杂的食品环境体系下进行应用验证。这些研究成果不仅发现了新的咸味肽,并为咸味肽的呈味机制提供新的见解。
[1] HUNTER R W, DHAUN N, BAILEY M A.The impact of excessive salt intake on human health[J].Nature Reviews Nephrology, 2022, 18(5):321-335.
[2] GREER R C, MARKLUND M, ANDERSON C A M, et al.Potassium-enriched salt substitutes as a means to lower blood pressure:Benefits and risks[J].Hypertension, 2020, 75(2):266-274.
[3] LAO H F, CHANG J C, ZHUANG H N, et al.Novel kokumi peptides from yeast extract and their taste mechanism via an in silico study[J].Food &Function, 2024, 15(5):2459-2473.
[4] 杨文君, 段杉, 崔春.豌豆蛋白深度酶解制备咸味肽的研究[J].中国调味品, 2021, 46(8):1-5.
YANG W J, DUAN S, CUI C.Study on preparation of salty peptides by deep enzymatic hydrolysis of pea protein[J].China Condiment, 2021, 46(8):1-5.
[5] SON M, PARK T H.The bioelectronic nose and tongue using olfactory and taste receptors:Analytical tools for food quality and safety assessment[J].Biotechnology Advances, 2018, 36(2):371-379.
[6] KASAHARA Y, NARUKAWA M, ISHIMARU Y, et al.TMC4 is a novel chloride channel involved in high-concentration salt taste sensation[J].The Journal of Physiological Sciences, 2021, 71(1):23.
[7] SHEN D Y, PAN F, YANG Z C, et al.Identification of novel saltiness-enhancing peptides from yeast extract and their mechanism of action for transmembrane channel-like 4 (TMC4) protein through experimental and integrated computational modeling[J].Food Chemistry, 2022, 388:132993.
[8] ZHAO Z Y, YANG M Z, LI Z J, et al.Enzymatic preparation, identification by transmembrane channel-like 4 (TMC4) protein, and bioinformatics analysis of new salty peptides from soybean protein isolate[J].Foods, 2024, 13(17):2798.
[9] GU Y X, ZHANG J C, NIU Y J, et al.Virtual screening and characteristics of novel umami peptides from porcine type I collagen[J].Food Chemistry, 2024, 434:137386.
[10] CHEN R X, LIU X C, XIANG J Y, et al.Prospects and challenges for the application of salty and saltiness-enhancing peptides in low-sodium meat products[J].Meat Science, 2023, 204:109261.
[11] GAO J, FANG D L, MUINDE KIMATU B, et al.Analysis of umami taste substances of morel mushroom (Morchella sextelata) hydrolysates derived from different enzymatic systems[J].Food Chemistry, 2021, 362:130192.
[12] TU M L, LIU H X, ZHANG R Y, et al.Analysis and evaluation of the inhibitory mechanism of a novel angiotensin-I-converting enzyme inhibitory peptide derived from casein hydrolysate[J].Journal of Agricultural and Food Chemistry, 2018, 66(16):4139-4144.
[13] ZHENG Y Y, TANG L, YU M G, et al.Fractionation and identification of salty peptides from yeast extract[J].Journal of Food Science and Technology, 2021, 58(3):1199-1208.
[14] 张康逸, 屈凌波, 温青玉, 等.咸味肽的制备技术研究进展[J].中国调味品, 2022, 47(6):204-211.
ZHANG K Y, QU L B, WEN Q Y, et al.Research progress on the preparation technology of salty peptides[J].China Condiment, 2022, 47(6):204-211.
[15] 温青玉, 张雨, 李天齐, 等.面筋蛋白咸味肽的分离纯化及结构鉴定[J].食品科学, 2023, 44(4):194-199.
WEN Q Y, ZHANG Y, LI T Q, et al.Isolation, purification and structure identification of salty peptides from wheat gluten[J].Food Science, 2023, 44(4):194-199.
[16] CHEN D Y, CHEN W C, WU D, et al.Saltiness enhancing peptides isolated from enzymolysis extract of Lentinula edodes and their taste enhancing action mechanisms[J].LWT, 2023, 188:115430.
[17] ZHANG Y, GAO X C, PAN D D, et al.Isolation, characterization and molecular docking of novel umami and umami-enhancing peptides from Ruditapes philippinarum[J].Food Chemistry, 2021, 343:128522.
[18] PROSSER L C, TALBOTT J M, GARRITY R P, et al.C-terminal arginine-selective cleavage of peptides as a method for mimicking carboxypeptidase B[J].Organic Letters, 2023, 25(33):6206-6210.
[19] LE B, YU B B, AMIN M S, et al.Salt taste receptors and associated salty/salt taste-enhancing peptides:A comprehensive review of structure and function[J].Trends in Food Science &Technology, 2022, 129:657-666.
[20] YAO H L, LIU S P, LIU T T, et al.Microbial-derived salt-tolerant proteases and their applications in high-salt traditional soybean fermented foods:A review[J].Bioresources and Bioprocessing, 2023, 10(1):82.
[21] JORGENSEN W L, TIRADO-RIVES J.Molecular modeling of organic and biomolecular systems using BOSS and MCPRO[J].Journal of Computational Chemistry, 2005, 26(16):1689-1700.
[22] MORRIS G M, HUEY R, LINDSTROM W, et al.AutoDock4 and AutoDockTools4:Automated docking with selective receptor flexibility[J].Journal of Computational Chemistry, 2009, 30(16):2785-2791.
[23] GAO B H, HU X B, XUE H, et al.Isolation and screening of umami peptides from preserved egg yolk by nano-HPLC-MS/MS and molecular docking[J].Food Chemistry, 2022, 377:131996.
[24] NIU Y J, GU Y X, ZHANG J C, et al.Characteristics of saltiness-enhancing peptides derived from yeast proteins and elucidation of their mechanism of action by molecular docking[J].Food Chemistry, 2024, 449:139216.
[25] WANG R, FENG X R, GONG Z H, et al.Decoding of salty/saltiness-enhancing peptides derived from goose hemoglobin and the interaction mechanism with TMC4 receptor[J].Journal of Agricultural and Food Chemistry, 2024, 72(34):19107-19119.
[26] XIE X N, DANG Y L, PAN D D, et al.The enhancement and mechanism of the perception of saltiness by umami peptide from Ruditapes philippinarum and ham[J].Food Chemistry, 2023, 405:134886.
[27] XIA X, SONG S Q, ZHOU T, et al.Preparation of saltiness-enhancing enzymatic hydrolyzed pea protein and identification of the functional small peptides of salt reduction[J].Journal of Agricultural and Food Chemistry, 2023, 71(21):8140-8149.
[28] WANG Z, CHENG Y P, MUHOZA B, et al.Discovery of peptides with saltiness-enhancing effects in enzymatic hydrolyzed Agaricus bisporus protein and evaluation of their salt-reduction property[J].Food Research International, 2024, 177:113917.
[29] SCHINDLER A, DUNKEL A, ST HLER F, et al.Discovery of salt taste enhancing arginyl dipeptides in protein digests and fermented fish sauces by means of a sensomics approach[J].Journal of Agricultural and Food Chemistry, 2011, 59(23):12578-12588.
HLER F, et al.Discovery of salt taste enhancing arginyl dipeptides in protein digests and fermented fish sauces by means of a sensomics approach[J].Journal of Agricultural and Food Chemistry, 2011, 59(23):12578-12588.
[30] WANG H Y, CHEN D, LU W J, et al.Novel salty peptides derived from bovine bone:Identification, taste characteristic, and salt-enhancing mechanism[J].Food Chemistry, 2024, 447:139035.