木聚糖酶(xylanase, EC 3.2.1.8)作为糖苷水解酶(glycoside hydrolase, GH)家族中的重要成员,通过催化木聚糖主链β-1,4-糖苷键的断裂,在生物质转化、食品加工及造纸工业中具有重要的应用价值[1]。依据碳水化合物活性酶数据库(carbohydrate-active enzymes database,CAZy)分类体系,目前已表征的木聚糖酶主要属于GH10和GH11家族[2]。相较于其他家族成员,GH11家族木聚糖酶凭借其高度保守的催化结构域和底物结合口袋,展现出优异的底物特异性和催化效率,成为工业酶制剂开发的热点[3]。然而,游离态木聚糖酶在应用过程中普遍存在热稳定性差、pH耐受范围窄、无法回收使用、表达水平低及生产成本高等问题,由于工业化酶解反应往往需要在酸性或高温等苛刻条件下进行,这些性能缺陷显著制约了其规模化应用进程[4]。因此,增强酶的pH耐受性和热稳定性,已成为突破工业应用壁垒的核心方向。尽管已有研究从嗜热微生物中分离出部分耐高温的木聚糖酶,但其催化活性和表达水平仍难以满足大规模工业生产的需求[5]。基于理性设计的热稳定性改造虽能部分提升酶的耐热性能,但其高昂的成本问题仍未得到有效解决[6]。在此背景下,酶固定化技术作为一种多效性策略,可通过构建空间位阻效应,显著降低酶消耗速率与生产成本,同时提升酶分子的构象稳定性和对环境胁迫的耐受能力,因而成为解决木聚糖酶现存应用瓶颈的有效方法[7]。
当前木聚糖酶的固定化研究主要集中于物理、化学束缚策略的开发[8],如水凝胶纳米复合材料包埋[9]、戊二醛交联法固定[10]及羧基-氨基共价键合反应[11]。这些传统方法虽一定程度上提升了酶的稳定性,但仍存在载体兼容性差、酶活力降低等局限。近年来,微生物表面展示技术通过锚定蛋白-酶融合表达实现酶分子的定向固定,在利用酿酒酵母[12]、大肠杆菌[13]等宿主系统中展现出独特优势。WEE等[14]通过锚定蛋白将木聚糖酶展示在大肠杆菌表面,成功实现菠萝渣半纤维素的降解。LIANG等[15]则通过α凝集素展示系统将木聚糖酶展示在酿酒酵母表面。值得注意的是,酿酒酵母孢子固定化酶技术因其独特的孢子壁结构和抗逆性优势,正逐步成为酶固定化领域的研究热点。酿酒酵母孢子是二倍体酿酒酵母缺乏营养时通过减数分裂形成的单倍体休眠细胞,其孢子壁呈现独特的4层结构(由内而外分别为甘露糖层、葡聚糖层、壳聚糖层和二酪氨酸层)[16]。在利用孢子固定化酶分子时,通过信号肽介导的蛋白转运机制,可将目标酶牵引至孢子壁的壳聚糖层外,由于二酪氨酸层致密的网状结构形成分子筛效应,酶分子被有效截留在壳聚糖层与二酪氨酸层之间[17-18]。KONG等[19]已成功在酵母孢子中封装肌酐酶与肌酸酶,构建出具有连续转化功能的全细胞催化系统。白佳文等[18]也利用该技术实现聚对苯二甲酸乙二醇酯水解酶的孢子固定化并应用于对双-2-(羟乙基)苯二甲酸酯的降解中,这些研究表明酵母孢子作为酶固定化载体具有较好的应用潜力。
通过基因编辑技术对酿酒酵母孢子壁合成相关基因进行操作,可构建具有不同糖层构型的孢子表面展示系统。例如,敲除细胞壁甘露糖基转移酶基因OSW2后,osw2Δ孢子的二酪氨酸层交联度会下降,从而增强底物分子的扩散能力,促进酶分子与底物的接触。敲除二酪氨酸层合成基因DIT1后,dit1Δ孢子的二酪氨酸层缺失,导致壳聚糖层直接暴露于外部环境,壳聚糖通过静电吸附作用实现酶分子的固定。基于此,本研究选取3种酿酒酵母菌株(野生型AN120、孢子壁缺陷型osw2Δ和dit1Δ),构建黑曲霉来源的GH11家族木聚糖酶XynB孢子表面展示系统,并对孢子固定化木聚糖酶的酶学性质进行研究,旨在阐明孢子壁结构特性对酶分子稳定性及催化活力的影响,从而为木聚糖酶的工业应用提供新型固定化策略。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
研究中所使用和构建的菌株和质粒如表1所示,所用引物均由睿博兴科生物技术有限公司合成,引物如表2所示。
表1 本研究中所用的菌株和质粒
Table 1 Strains and plasmids used in this study

菌株描述来源HW3(dit1Δ, 二倍体)MATα/MATa ARG4/arg4-NspI his3ΔSK/his3ΔSK ho/ho LYS2/LYS2 leu2/leu2 lys2/lys2 RME1/rme1::LEU2 trp1::hisG/trp1::hisG ura3/ura3 osw2Δ::his5+/osw2Δ::his5+[20]HW83(osw2Δ, 二倍体)ho::LYS2/ho::LYS2 leu2/leu2 lys2/lys2RME1/rme1::LEU2 trp1::hisG[21]pRS424-ss-GFP-3HATRP1标记,AmpR抗性,多拷贝,含有TEF1启动子本研究pRS424-ss-GFP-xynB-3HA带有从黑曲霉中克隆得到的木聚糖酶基因xynB本研究pRS306-ss-GFP-xynB-3HAURA3标记,整合型,携带有木聚糖酶基因xynB本研究
表2 本研究使用的引物
Table 2 Primers used in this study

引物序列(5′~3′)424-xynB-F1ATCACTCTCGGCATGGACGAGCTGTACAAGGACTCTGTCGCCCAGCGTTCGGATGCCTTG424-xynB-R1GCCCGCATAGTCAGGAACATCGTATGGGTACTGAACAGTGATGGACGAAGATCCACTGCT环p-F1TACCCATACGATGTTCCTGACTATG环p-R1CTTGTACAGCTCGTCCATGCCGAGAxynB-FATGCTCACCAAGAACCTTCTCCTCTxynB-RTTACTGAACAGTGATGGACGAAGATxynB-F1-0.2kGTTCCCCACGACTCTGTCGCCCAGCxynB-F2-0.4kAGGGCTGGAACCCCGGAAGTGCGCAGGACATCACCTACAGCGGCACCTTCxynB-R1-0.2kGAAGGTGCCGCTGTAGGTGATGTCCTGCGCACTTCCGGGGTTCCAGCCCTxynB-F3AGAAGATGCGGCCAGCAAAACGACTCTGTCGCCCAGCGTTCGGATGCCTTxynB-R3TGCATTTACTTATAATACAGTTTTCTGAACAGTGATGGACGAAGATCCAC
1.1.2 培养基
YPD培养基(g/L):酵母提取物10,蛋白胨20,葡萄糖20。
色氨酸缺陷型合成葡萄糖基础培养基(synthetic drop-out medium lacking tryptophan, SD-Trp)(g/L):无氨基酸酵母氮源6.7,缺Trp的氨基酸混合物粉末2.4,葡萄糖20,琼脂粉(固体培养基)20。
尿嘧啶缺陷型合成葡萄糖基础培养基(synthetic drop-out medium lacking uracil, SD-Ura)(g/L):无氨基酸酵母氮源6.7,缺Ura的氨基酸混合物粉末2.4,葡萄糖20,琼脂粉(固体培养基)20。
酵母浸出粉蛋白胨醋酸盐培养基(yeast extract peptone acetate medium, YPAce)(g/L):酵母提取物10,蛋白胨20,乙酸钾20。
醋酸钾基础(potassium acetate, KAc)培养基(g/L):乙酸钾20。
1.1.3 其他试剂
2×Phanta Max Master Mix、lon Express Ultra One Step Cloning Kit、限制性核酸内切酶等,南京诺唯赞生物科技股份有限公司;质粒提取试剂盒、PCR产物纯化试剂盒,北京庄盟国际生物基因科技有限公司;藤黄节杆菌溶壁酶(Arthrobacter luteus lyticase),Sigma公司。
1.2 仪器与设备
荧光倒置显微镜,Nikon公司;超声波细胞粉碎机,宁波新芝生物科技股份有限公司;冷冻干燥机,EYELA公司。
1.3 实验方法
1.3.1 融合蛋白质粒构建
蛋白质和核苷酸序列参考UniProtKB登录号(http://www.uniprot.org/uniprot/)。制备来自黑曲霉的基因组DNA。以黑曲霉的基因组DNA为模板,使用2xPhanta Max Master Mix聚合酶,在Biorad的PCR仪器上使用表1中描述的特异性引物xynB-F/xynB-R进行PCR扩增得到xynB基因片段。PCR扩增参数:98 ℃预变性3 min;98 ℃变性30 s,55 ℃退火30 s,72 ℃延伸1 min;经30个循环后72 ℃延伸5 min。以纯化回收的基因片段为模板,引物xynB-F1-0.2k/xynB-F2-0.4k/xynB-R1-0.2k通过桥式PCR去除内含子与信号肽。用引物424-xynB-F1/424-xynB-R1扩增出带有GFP和pRS424载体同源臂的xynB基因,使用引物环p-F1/环p-R1进行反向PCR扩增出在GFP基因和3HA基因间切开的载体线性片段,并通过Dpn I酶去除环状质粒。通过无缝克隆法将xynB基因连接在GFP基因的C端,3HA基因的N端,同源重组质粒成环后电击转化大肠杆菌DH5α,测序验证得到重组质粒pRS424-ss-GFP-xynB-3HA。同理使用xynB-F3/xynB-R3扩增出带有pRS306载体同源臂的xynB片段,载体经单酶切线性化后,使用无缝克隆酶将基因片段连接在载体上得到重组质粒pRS306-ss-GFP-xynB-3HA。使用乙酸锂法将重组质粒转化入酿酒酵母野生型AN120感受态、酿酒酵母缺陷型osw2Δ感受态、酿酒酵母缺陷型dit1Δ感受态。随后分别在固体SD/Trp缺陷型培养基以及SD/Ura缺陷型培养基上选择阳性转化体。
1.3.2 酵母产孢与荧光定位
挑取平板上的单克隆酵母菌株,接种到5 mL缺陷型培养基中,30 ℃摇床培养过夜;将5 mL菌液转接至400 mL的YPAce培养基中诱导产孢,30 ℃摇床培养24 h;离心收集沉淀,转入400 mL KAc培养基中,于30 ℃摇床培养24~36 h诱导产孢。6 000 r/min离心10 min收集孢子。使用荧光显微镜观察蛋白在孢子中的定位。
将收集的子囊孢子重悬于少量原生质体缓冲液中(50 mmol/L pH 7.5磷酸缓冲液,1.4 mol/L山梨醇,40 mmol/L β-巯基乙醇),再加入20 μL Lyticase在37 ℃下反应2~4 h,镜检观察子囊壳裂解情况。待子囊壳裂解后,8 000 r/min、2 min收集所有处理后的孢子,去除上清液,使用原生质体缓冲液清洗2次,重悬于原生质体缓冲液中,充分混匀,超声破碎获得单个游离孢子。超声波条件为超声波功率300 W,工作1 min、停1 min,16~30个循环。单个孢子经0.5%(体积分数)Triton-X洗涤2次,梯度加入适量0.5%(体积分数)的吐温-20溶液洗涤数次,在保证裂解碎片去除干净后用超纯水洗涤3次,离心收集孢子,冷冻干燥获得单个纯化孢子,在-20 ℃条件下贮存备用。
用蛋白提取缓冲液[0.2 mol/L山梨醇,50 mmol/L Tris-HCl(pH 7.5),1 mmol/L EDTA]重悬20 mg孢子,于冰上超声波破碎,在4 000×g、15 min条件下离心取上清液进行十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis, SDS-PAGE)检测。
1.3.3 AN120、osw2Δ与dit1Δ固定化酶活力与重复使用次数的对比
孢子固定化酶活力测定:参照3,5-二硝基水杨酸(3,5-dinitrosalicylic acid, DNS)法[22],并做部分修改。取1 000 μL 10 g/L的桦木木聚糖底物,在40 ℃预热后,加入20 mg孢子固定化XynB;恒温反应30 min后加入1.5 mL DNS终止反应,沸水浴中煮沸5 min后立即置于冷水中冷却,取200 μL反应终止液于540 nm下测定吸光值,并根据相应的标准曲线计算出酶活力。一个酶活力单位U定义为每分钟从10 g/L桦木木聚糖溶液中降解释放1 μmol还原糖所需的酶量。
重复使用次数:反应结束离心后从反应溶液中回收孢子,用水洗2次后,在同样的条件下进行下一轮的反应,将第1次反应的酶活力定义为100%。
1.3.4 最适孢子质量浓度与反应时间
最适孢子浓度的测定:首先对不同孢子质量浓度进行研究,按照标准方法,以1、2、5、10、15、20、30、40 g/L不同孢子质量浓度进行反应。
最佳反应时间的测定:使用所述反应体系,在最适孢子质量浓度的条件下,分别反应10、20、30、60、120、240 min后,检测低聚木糖的产量,寻找反应最佳的孢子的反应时间。
1.3.5 最适温度和pH
最适温度的测定:0.2 mol/L pH 5.0 Na2HPO4-0.1 mol/L柠檬酸缓冲液配制桦木木聚糖底物,分别在30~90 ℃不同温度条件按照标准方法检测孢子固定化酶的酶活力,以酶活力最高点为100%。
最适pH的测定:在最适温度条件下,以0.2 mol/L Na2HPO4-0.1 mol/L柠檬酸缓冲液配制pH 2.0~8.0的底物、50 mmol/L Gly-NaOH缓冲液配制pH 9.0的底物,按照标准方法检测pH对孢子固定化酶的影响,以酶活力最高点为100%。
1.3.6 孢子固定酶和游离酶的热稳定性
将游离酶和孢子固定化酶置于不同温度(30~90 ℃)下孵育120 min,按照标准方法测定相应温度的酶活力,以未孵育的孢子固定化酶和游离酶活力为100%。
1.3.7 孢子固定酶和游离酶的pH稳定性
将游离酶和固定化酶置于不同pH缓冲液(2.0~9.0)中孵育120 min,按照标准方法测定相应pH的酶活力,以未孵育的孢子固定化酶和游离酶活力为100%。
1.3.8 游离酶和固定化酶的金属离子与有机溶剂耐受性
将游离酶和固定化酶置于不同金属离子终浓度为10 mmol/L的Mn2+、Na+、Zn2+、Mg2+、Ga2+、K+、Cu2+、Al3+及其他有机试剂[乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)、吐温-80、Triton X-100、SDS]中孵育120 min,按照标准方法测定相应金属离子与有机试剂的酶活力,以不添加上述试剂的孢子固定化酶和游离酶活力为100%。
1.3.9 孢子固定酶和游离酶的高盐耐受性
将游离酶和固定化酶置于不同质量浓度(1、5、10、15、25、30 g/100 mL)的NaCl中孵育120 min,按照标准方法测定相应金属离子与有机试剂的酶活力,以不添加NaCl的孢子固定化酶和游离酶活力为100%。
1.3.10 孢子固定化酶重复使用能力
为检测孢子固定化XynB的可重复使用性,反应结束后离心后从反应溶液中回收孢子,用水洗2次后,在同样的条件进行下一轮的反应,将第1次反应的酶活力定义为100%。重复8次。
1.3.11 孢子固定化酶底物特异性
分别取10 g/L的桦木木聚糖、榉木木聚糖、阿拉伯树胶、羧甲基纤维素、羧甲基壳聚糖、可溶性淀粉、角豆胶作为反应体系中的底物,按照标准方法检测孢子固定化XynB酶活力。
1.4 数据统计
实验数据均以“平均值±标准差”表示,采用SPSS统计学软件进行统计分析,P<0.05表示具有统计学意义,GraphPad Prism软件绘制相关图表。
2 结果与分析
2.1 孢子固定化酶的荧光定位与SDS-PAGE
为克服pRS426-ss-GFP-xynB-3HA质粒在酿酒酵母孢子表达系统中易丢失的问题,本研究先后构建了pRS426-ss-GFP-xynB-3HA质粒以及能够稳定遗传的质粒pRS306-ss-GFP-xynB-3HA,并转化至酿酒酵母。其孢子荧光结果如图1-a所示,阳性菌株的孢子出现明显的绿色荧光信号,且定位于孢子壁上,表明融合表达的GFP-xynB成功在酿酒酵母孢子中定位表达。进一步通过SDS-PAGE分析(图1-b),在分子质量约为22 kDa的位置观察到明显的特异性条带,与目标蛋白XynB的理论分子质量一致,说明目标蛋白在整合型表达系统中得到了高效且稳定的表达。综上,质粒中的绿色荧光蛋白GFP和木聚糖酶XynB在酿酒酵母孢子得到稳定表达,为孢子固定化XynB的应用提供了技术支撑。
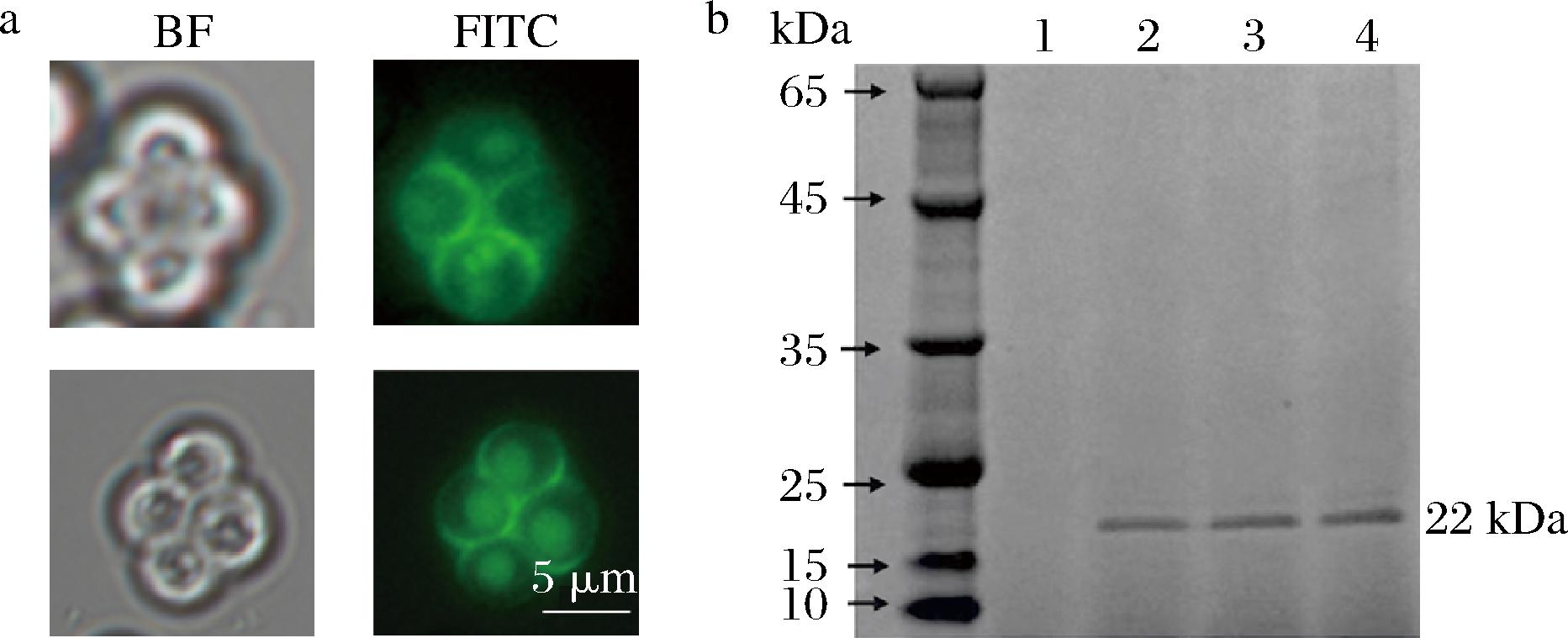
a-荧光定位;b-SDS-PAGE
图1 蛋白荧光定位与表达
Fig.1 Protein fluorescence localization and expression
注:BF表示未添加荧光剂;FITC表示异硫氰酸荧光素。
2.2 孢子固定化酶的活性与重复使用次数的对比
对3种孢子固定化酶的酶活力进行了测定,结果如图2-a所示。相较于野生型AN120孢子固定化XynB的酶活力(7.51 U/g),osw2Δ孢子(11.95 U/g)和dit1Δ孢子(12.76 U/g)的酶活力分别提升了(59.12±4.44)%和(69.91±5.25)%(P<0.05),该结果可能是由于孢子壁的结构特性和底物扩散效率的构效关系所致,相较于野生型孢子,osw2Δ孢子的二酪氨酸层交联度下降,导致二酪氨酸层结构松散孔径增加,有效减弱了分子筛效应对底物渗透的阻碍作用,而dit1Δ孢子则由于壳聚糖层直接暴露于反应体系,其表面丰富的氨基基团增强了木聚糖酶的静电吸附作用,从而使底物更易与酶结合并发生反应[23],最终表现为孢子壁缺陷型菌株固定化酶活力显著提高。
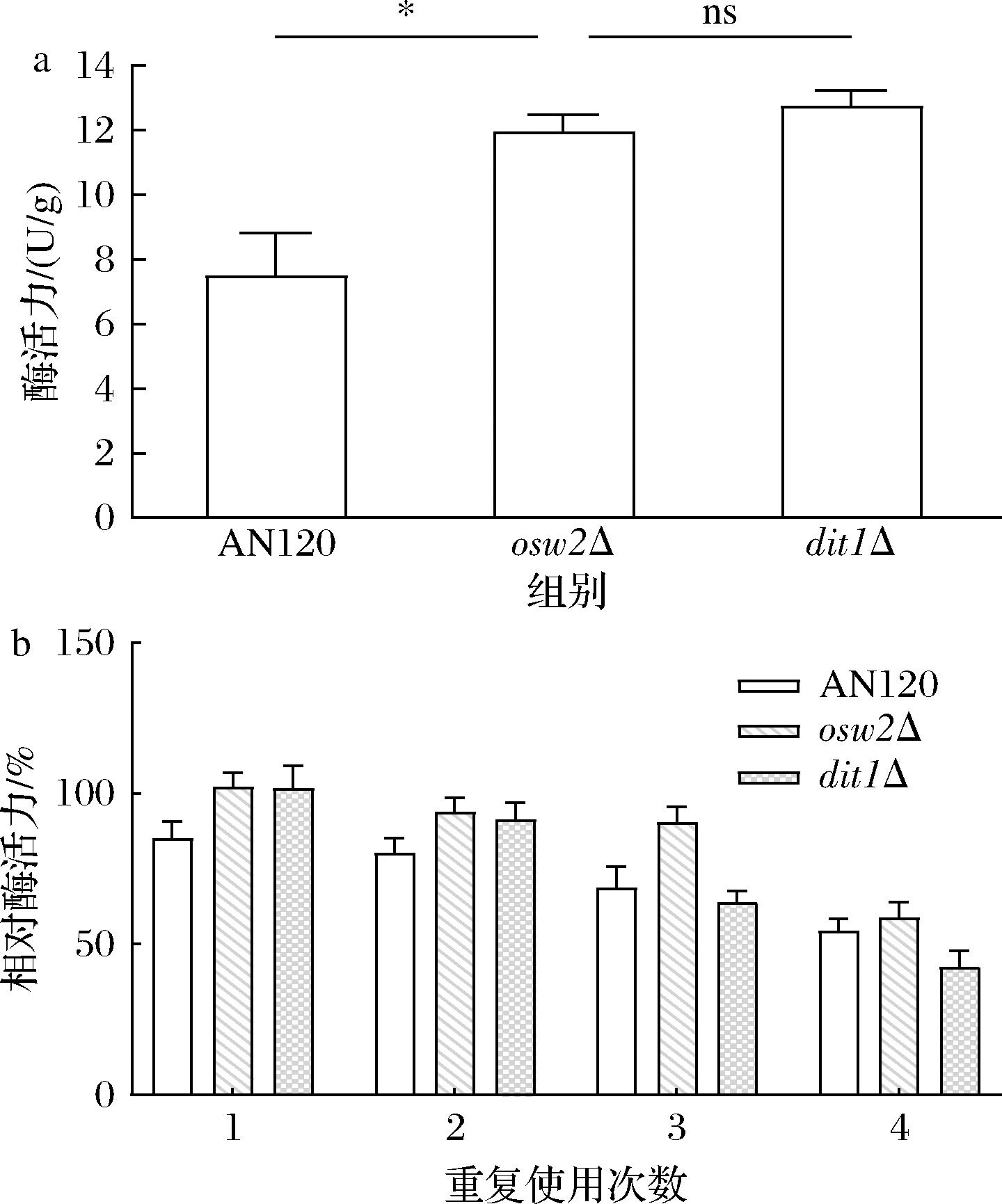
a-酶活力;b-重复使用次数
图2 固定化XynB酶活力与重复使用次数
Fig.2 Activity of immobilized XynB enzyme and the number of reuse cycles
注:*表示差异显著(P<0.05);ns表示差异不显著(P>0.05)(下同)。
为系统评价固定化酶的操作稳定性,本研究采用四循环回收-催化实验进行表征,每轮催化反应结束后,通过离心回收孢子,经去离子水洗涤后直接用于下一轮相同条件的酶解反应。如图2-b所示,dit1Δ孢子固定化XynB在前2次循环中保持(101.72±7.43)%和(91.28±5.81)%的相对酶活力,与osw2Δ孢子(102.2±4.64)%和(93.88±4.66)%相对酶活力表现相当。但从第3次循环开始,dit1Δ的相对酶活力急剧下降至初始值的(63.83±3.68)%,第4轮进一步降至(42.41±5.46)%;而osw2Δ孢子在第3轮仍保持了(90.44±5.11)%的相对酶活力,即使4轮循环后,仍保持(58.58±5.61)%的相对酶活力。这一现象可能归因于dit1Δ孢子缺乏二酪氨酸层,固定酶主要依赖静电吸附作用,这种单一作用力的结合模式具有可逆性,在重复洗涤过程中,酶分子易从孢子表面脱附。相比之下,osw2Δ孢子尽管其二酪氨酸层结构较为松散,但其网状结构仍保留空间位阻效应,不仅有效增强了底物扩散能力,也有效缓冲了催化过程中的酶构象变化[17]。综上,osw2Δ孢子是固定XynB的最优载体选择。
2.3 孢子质量浓度和反应时间对孢子固定化XynB活力的影响
在明确osw2Δ孢子作为木聚糖酶XynB固定化载体的最优选择后,本研究进一步以osw2Δ孢子固定化XynB为研究对象,开展酶学性质研究。首先梯度设置孢子质量浓度(1、2、10、15、20、30、40 g/L),在标准化反应体系下进行酶活力测定。如图3-a所示,随着孢子质量浓度不断增加,酶活力同步增加,当孢子质量浓度高于20 g/L时,相对酶活力增幅趋缓,因此,综合考虑催化效率与孢子使用量,确定20 g/L为最佳孢子反应质量浓度,并以该参数用于后续酶学性质的研究。图3-b表明,随着反应时间的延长,反应体系在初始阶段(0~30 min)相对酶活力呈指数型增长,当反应时间达到30 min后相对酶活力增长趋势变得平缓,因此将30 min设为后续固定化酶反应体系的标准反应时间。
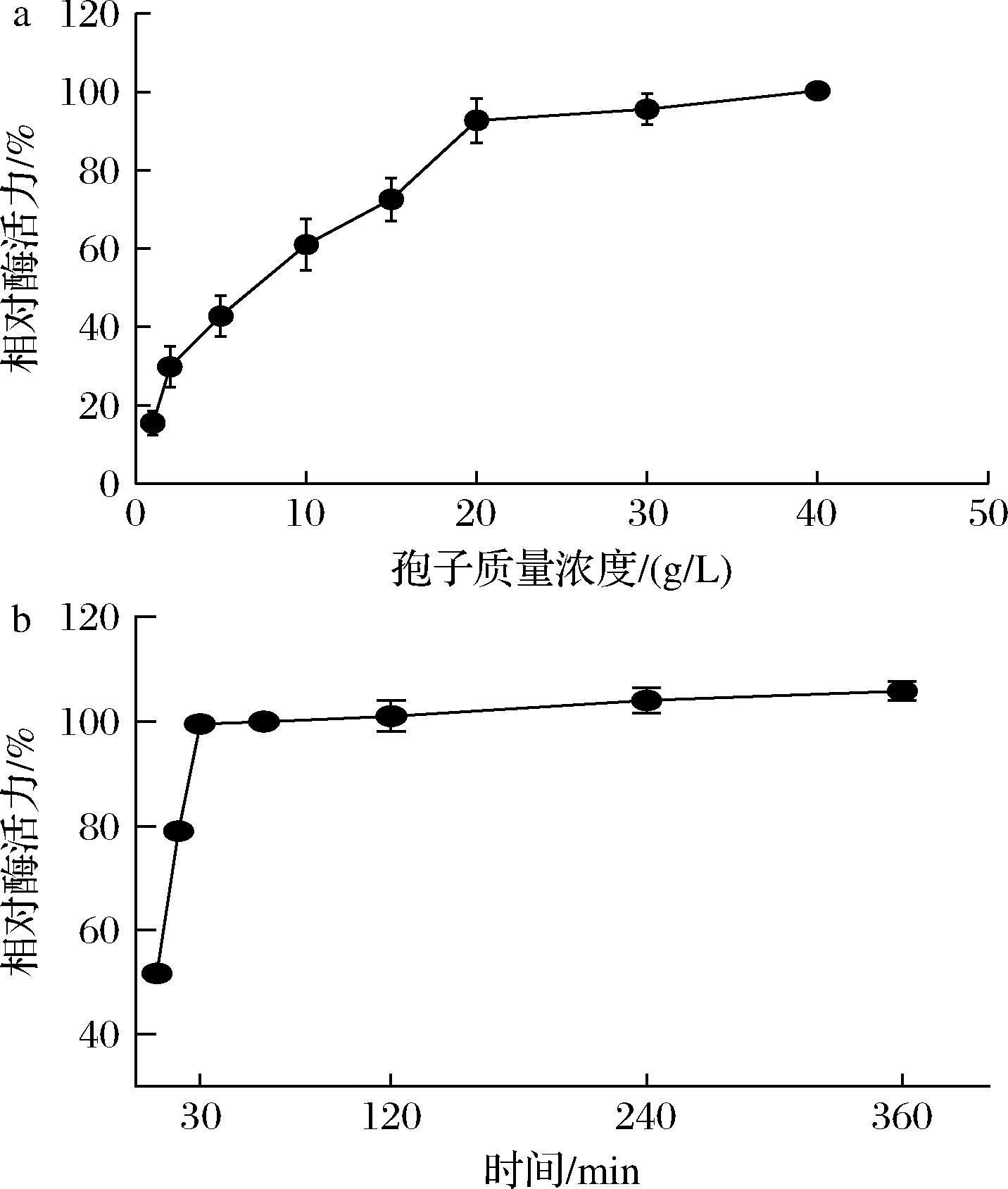
a-孢子质量浓度;b-反应时间
图3 孢子质量浓度和反应时间对孢子固定化XynB活力的影响
Fig.3 Effect of spore mass concentration and reaction time on the activity of immobilized XynB on spore
2.4 最适温度和pH
以毕赤酵母表达系统生产的游离态木聚糖酶XynB作为对照组,研究反应温度对osw2Δ孢子固定化XynB催化性能的影响。如图4-a所示,2组酶制剂均在40 ℃条件下达到峰值酶活力。当反应温度高于60 ℃时,游离XynB的酶活力迅速下降(残留活力为(58.83±1.77)%,固定化XynB仍保持(81.92±3.37)%的相对酶活力,表明在较高温度条件下,固定化酶具有更广的适用温度范围。最适pH研究表明(图4-b),2组酶制剂的最适反应pH均为5.0,与文献报道数据相符[24]。在极端pH条件(pH 2.0和pH 9.0)下,其相对酶活力较游离酶分别提升(43.59±2.40)%和(45.65±3.08)%,说明固定化酶具有更宽的pH适应范围。该结果表明独特的孢子壁结构为固定化XynB提供了良好的保护屏障,增强了目标酶作为生物催化剂的应用潜力[25]。
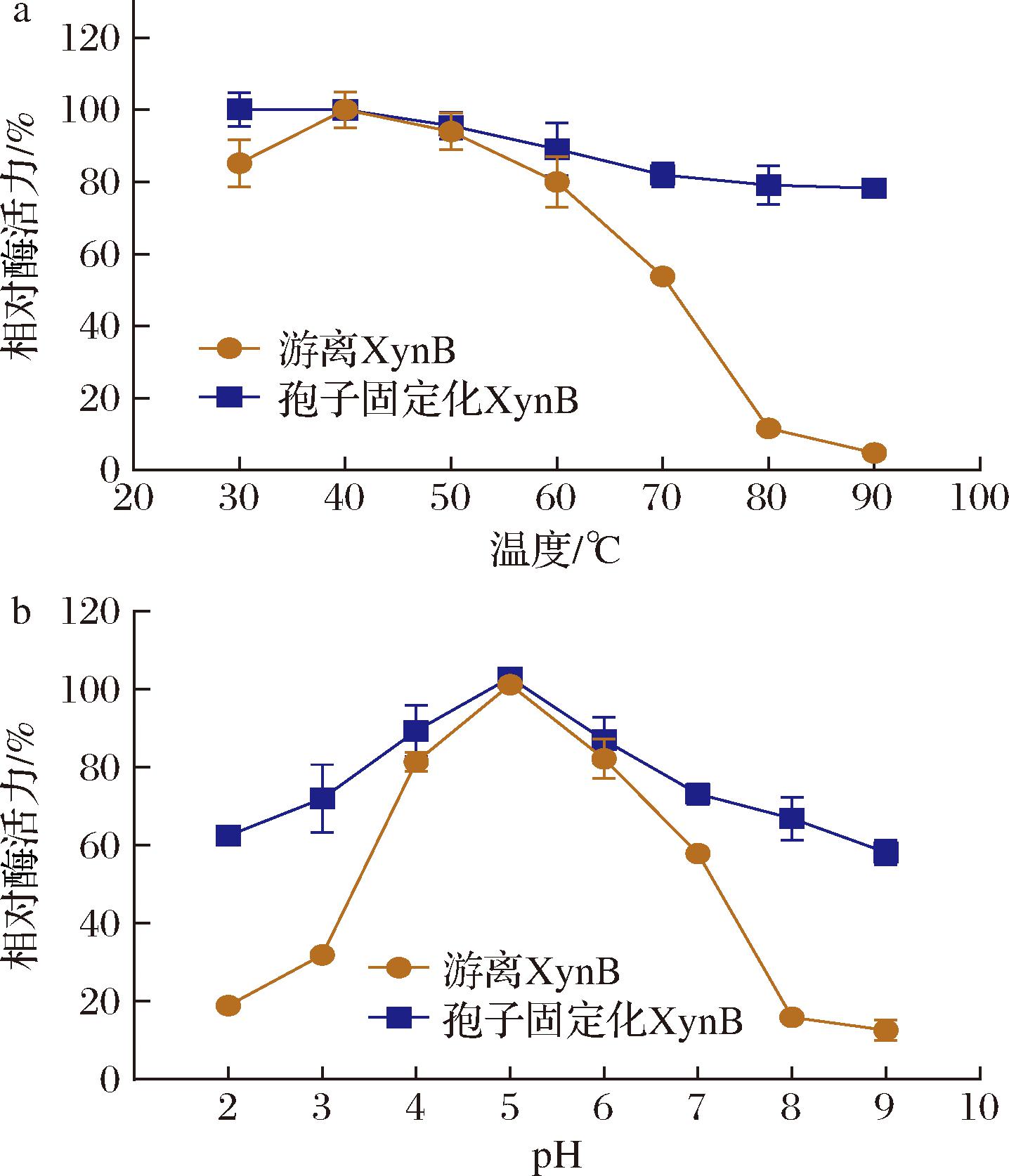
a-温度;b-pH
图4 温度和 pH 对孢子固定化XynB活力的影响
Fig.4 Effect of temperature and pH on the activity of immobilized XynB on spores
2.5 孢子固定化XynB的热稳定性以及pH耐受性
孢子固定化XynB的热稳定性如图5-a所示,在30~40 ℃条件下热处理120 min时,游离XynB展现出良好的热稳定性,酶活力为(97.03±3.83)%。当温度升至50 ℃时,游离酶活力发生显著衰减,残余酶活力为(16.31±6.35)%,60 ℃以上时完全失活。相比之下,固定化XynB在50 ℃孵育120 min后仍保留(88.26±2.05)%的酶活力,在60 ℃时保留(71.47±4.03)%的酶活力,即使在80 ℃条件下仍保留(31.07±6.09)%的残留酶活力。热稳定性的提升可能归因于酶与壳聚糖层之间形成的共价键连接,使酶分子发生热变性所需的活化能升高,从而提高了固定化酶对高温的抵抗能力[26]。
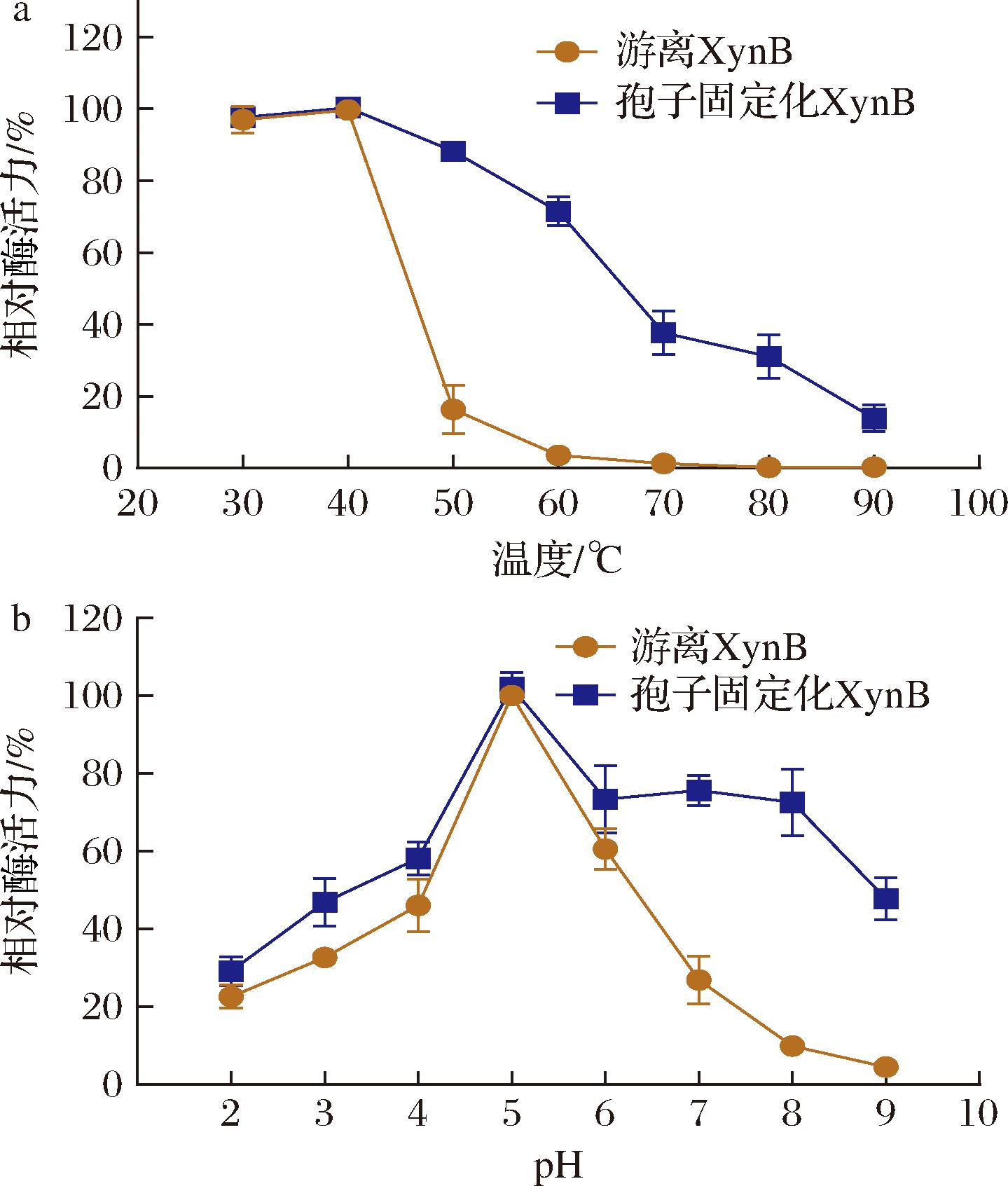
a-温度;b-pH
图5 温度和pH对孢子固定化XynB活力的影响
Fig.5 Thermal stability and pH stability of immobilized XynB on spores
pH耐受性研究结果如图5-b所示,在pH 4.0~8.0区间内,固定化酶经120 min孵育后仍保留50%以上的相对酶活力。在偏碱性(pH 8.0~9.0)及强酸性(pH 2.0~3.0)条件下,其酶活力均高于游离XynB,分别提升(43.37±3.71)%与(14.26±5.44)%,显示出优异的pH耐受性,尤其在酸性条件下具有更强的水解能力。结合热稳定性与pH耐受性的分析结果,与传统的固定化方法相比,孢子固定化XynB在极端反应条件下具有更好的催化性能,孢子固定化XynB在80 ℃孵育120 min后仍能保持约30%的初始酶活力,而采用包埋法固定的木聚糖酶,在相同条件下仅能保持初始酶活力的15%左右[27]。此外,孢子固定化XynB具有较宽的pH耐受范围,而传统固定化方法通常只能在较窄的pH范围内稳定[9]。这表明,孢子固定化木聚糖酶具有较强的热稳定性和pH耐受性,为其在复杂工业环境中应用提供了理论依据。
2.6 金属离子与不同有机试剂对游离XynB与孢子固定化XynB的影响
以游离态XynB为对照组,探究金属离子与有机试剂对osw2Δ孢子固定XynB的影响。如图6所示,在10 mmol/L浓度条件下,Mn2+、Mg2+对游离XynB酶活表现出激活效应,其中Mn2+的促进作用较为明显,酶活力提升(15.54±2.09)%。而Na+、Zn2+、Ca2+、K+等金属离子及有机试剂TritonX-100、SDS均会对游离酶活力产生不同程度的抑制作用。其中,SDS通过破坏酶蛋白空间结构,导致游离XynB的酶活力下降至(53.55±0.32)%。相比之下,金属离子与有机试剂对osw2Δ孢子固定化XynB酶活力的影响并不显著,即便在SDS存在下,固定化酶仍维持(98.38±1.12)%的催化活力,表现出对蛋白质变性剂的极强抗性。这种稳定性差异主要源于孢子壁特有的二酪氨酸交联结构,其通过形成致密的网络屏障,有效阻隔化学因子与酶分子的直接接触[28]。该结果表明osw2Δ孢子固定化策略不仅克服了游离XynB对环境敏感的局限性,更赋予酶制剂在复杂反应体系中的化学稳定性,为其在生物质转化、食品加工等领域的实际应用奠定了良好基础。
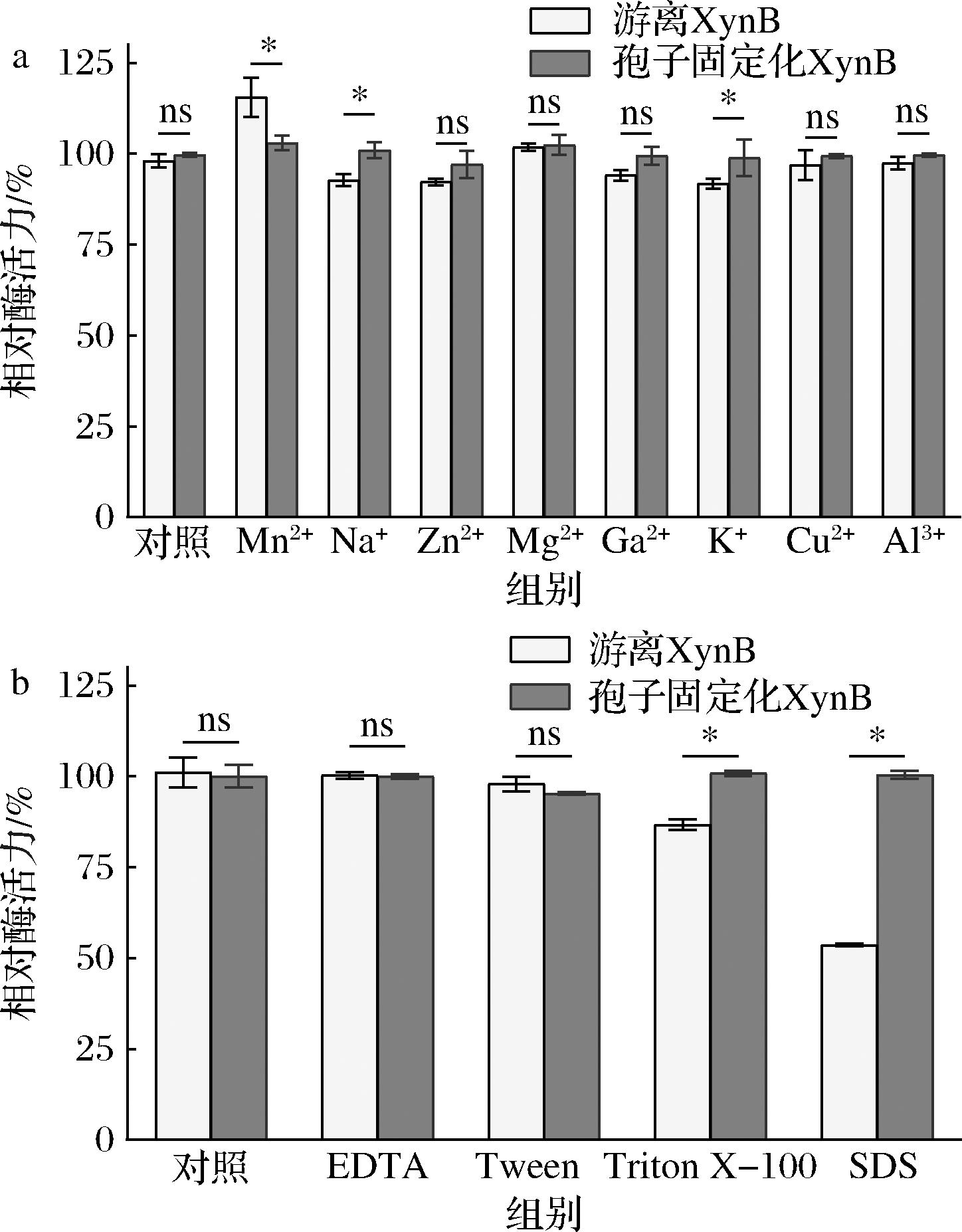
a-金属离子;b-有机试剂
图6 金属离子和有机试剂对酶活力的影响
Fig.6 Effects of metal ions and organic reagents on the enzyme’s activity
2.7 高盐体系对孢子固定化酶活力的影响
NaCl作为食品体系中的关键渗透调节物质,广泛存在于面制品、海产品、传统发酵制品等高盐基质中,此类环境对游离酶制剂的催化性能构成严峻挑战[29]。如图7所示,当NaCl质量浓度达到30 g/100 mL时,游离XynB的相对酶活力下降至(39.12±1.6)%,这可能是因为高盐缓冲体系会改变酶蛋白的部分结构,影响其与底物的结合,从而降低酶的催化活力。相比之下,孢子固定化XynB在相同盐胁迫条件下展现出优异的耐盐性能,残余酶活力维持在(84.76±1.42)%左右。该结果证明孢子固定化技术不仅能克服游离酶在高盐食品体系中的失活问题,更为其在海产品深加工、传统酿造等工业场景的应用提供了技术基础,具有广阔的产业化前景。
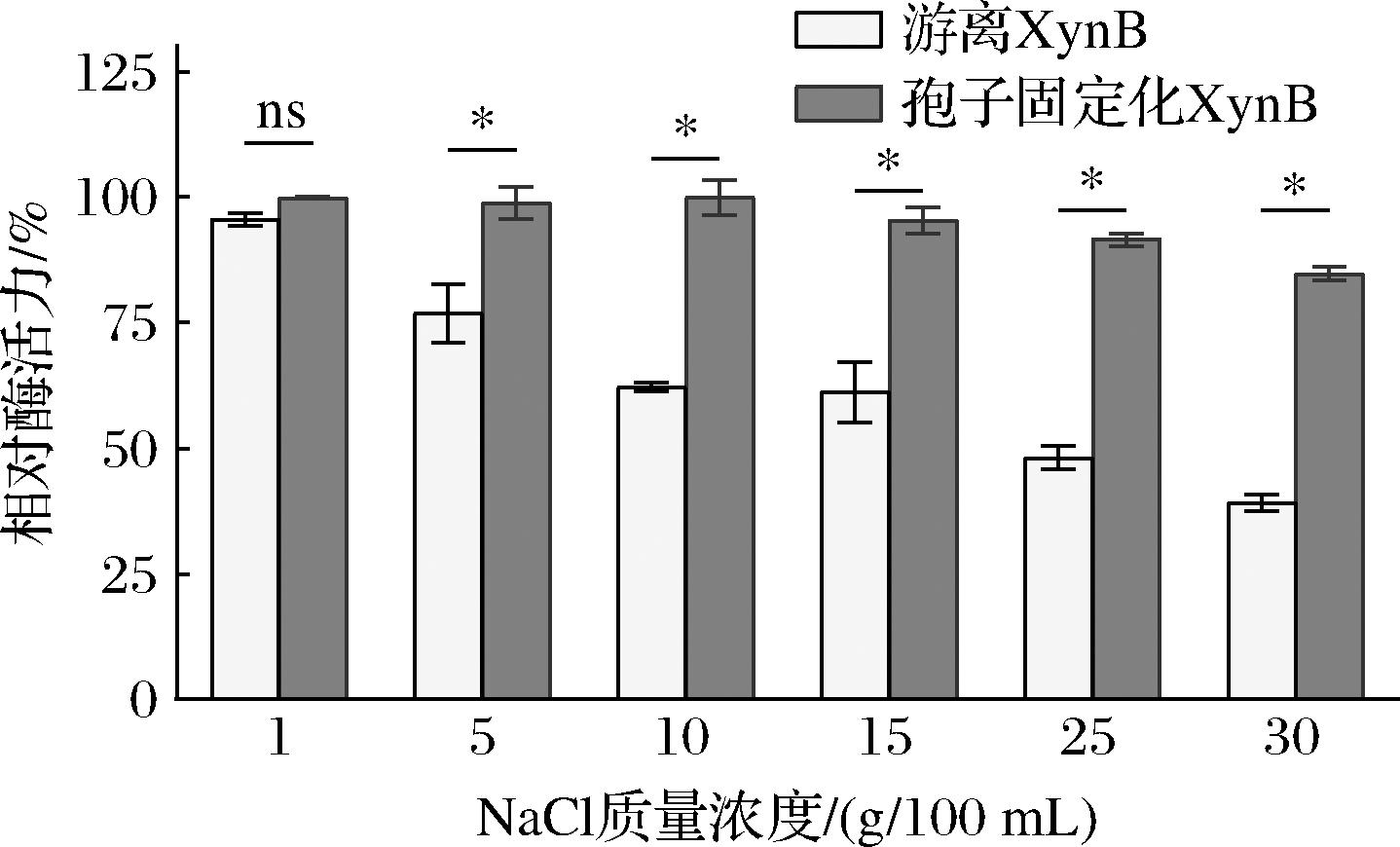
图7 NaCl质量浓度对酶活力的影响
Fig.7 Influence of salt ion concentration on enzyme activity
2.8 孢子固定化XynB的重复使用能力
为了评估孢子固定化酶的连续使用性能,进行了八循环回收-催化实验表征。图8结果表明,经5次循环使用后,固定化酶仍维持(56.10±7.13)%的初始酶活力,而采用聚合物载体固定的木聚糖酶在5次循环后仅能保留30%~40%的酶活力[30]。当使用次数增至7次时,残余酶活力仍维持在(28.14±2.22)%,显示出良好的操作稳定性,这可能是因为osw2Δ孢子壁的壳聚糖层通过静电吸附作用高效固定酶分子并维持酶构象稳定,二酪氨酸层通过交联结构有效防止酶分子浸出,导致固定化酶在重复使用过程中活力损失较小,该孢子固定化策略展现出作为长效生物催化剂的显著优势。
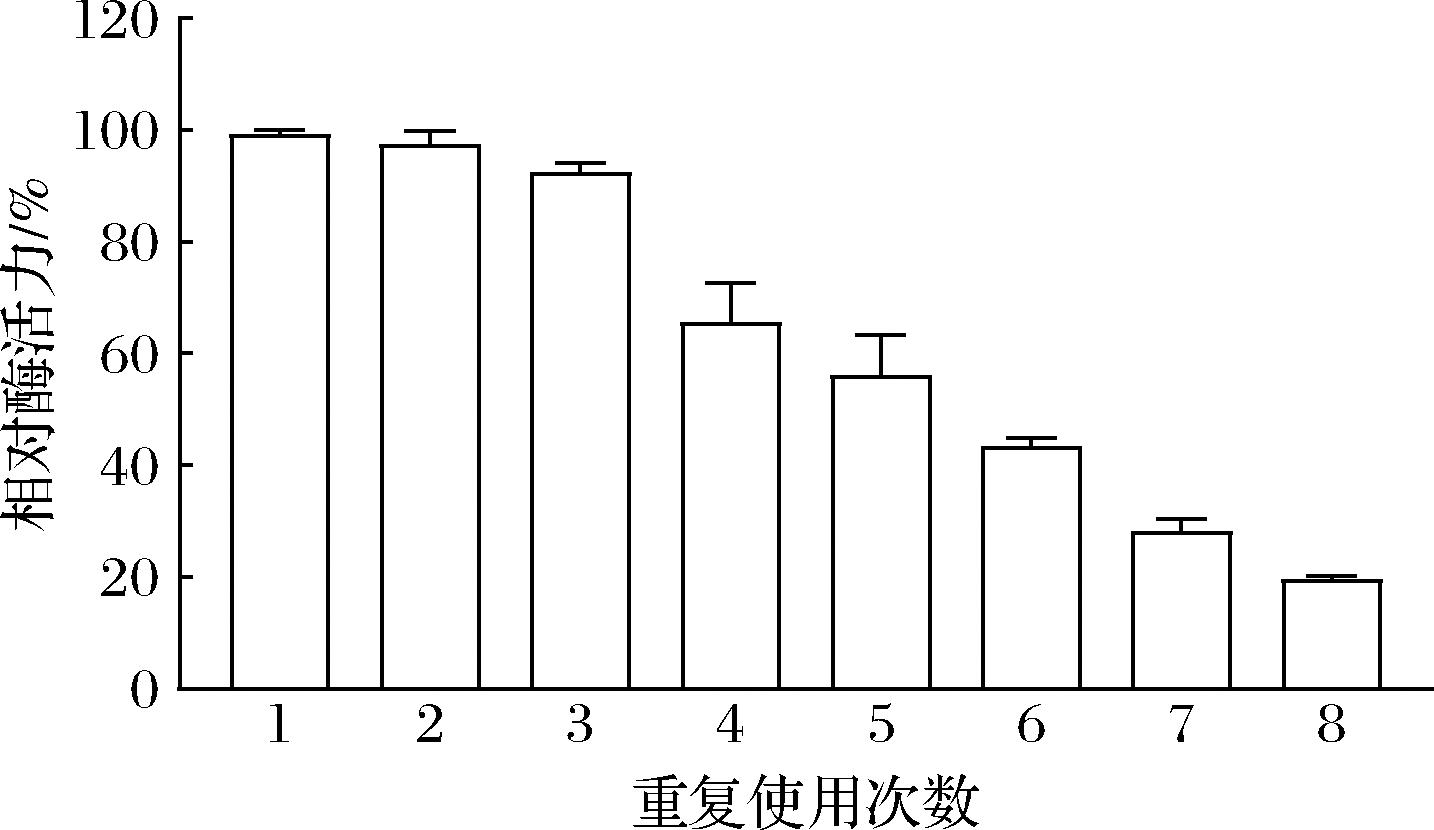
图8 孢子固定化XynB重复使用次数
Fig.8 Reusability of immobilized XynB on spores
2.9 孢子固定化XynB底物特异性分析
通过构建多底物反应体系,系统评估了游离XynB与osw2Δ孢子固定化XynB的催化特异性。结果如表3所示,2种酶制剂均特异性作用于木聚糖类底物,对山毛榉木木聚糖和桦木木聚糖展现出显著水解活力。对角豆胶、羧甲基壳聚糖、可溶性淀粉等非木聚糖底物均未检测到水解活力,表明XynB对木聚糖类底物具有高度的专一性,与其他GH11家族的木聚糖酶水解特性相似。来源于毛壳霉的木聚糖酶CsXyn11B水解榉木木聚糖产生木二糖与木三糖[31]。来源于棘孢木霉的木聚糖酶TaXyn11 A水解燕麦木聚糖、小麦阿拉伯木糖、榉木木聚糖和桦木木聚糖底物,并产生聚合度为2~6的低聚木糖[32]。本研究构建的孢子固定化XynB具有高度的木聚糖类底物特异性,显示出其在低聚木糖工业化生产中的独特优势,为木聚糖酶在功能性低聚糖开发中的应用提供了新策略。
表3 底物特异性 单位:%
Table 3 Substrate specificity

底物桦木木聚糖榉木木聚糖角豆胶阿拉伯树胶羧甲基壳聚糖羧甲基纤维素可溶性淀粉酶解得率15.49±0.1214.75±0.24NDNDNDNDND相对酶活力 100±0.7795.22±1.55-----
注:ND表示未检出。
3 结论
酿酒酵母孢子固定化技术作为微生物表面展示技术的一种,可同时实现酶的表达与固定化,它消除了对酵母表面锚定蛋白的需求,在酶分子功能与编码基因之间建立了关联,简化了传统酶制剂制备过程中繁琐的分离纯化步骤,并赋予酶分子再生能力和连续催化特性。本研究以黑曲霉来源的GH11家族低分子质量(22 kDa)木聚糖酶XynB为研究对象,通过异源表达系统将其分别固定化于3种酿酒酵母孢子表面,系统评估不同宿主体系的酶活力表现及操作稳定性,最终筛选确定osw2Δ孢子为XynB固定化的最优载体。
木聚糖酶在食品加工、造纸工业、饲料工程等领域具有广阔的应用前景,但其工业应用常受制于高温、极端pH、高盐及有机溶剂等严苛环境条件的活力衰减效应[33]。与游离XynB相比,osw2Δ孢子固定化XynB拥有更高的热稳定性和pH耐受性,同时表现出对金属离子、有机试剂及高渗透压环境的显著抗性,在保持严格底物特异性的前提下实现了良好的重复使用性能。酿酒酵母是一种低成本、易于大规模培养的微生物,其培养过程相比于合成高分子材料(如聚氨酯、聚丙烯酸酯等)更具经济效益。因此,利用酵母孢子作为固定化酶载体具有显著的经济优势。此外,与传统固定化酶方法相比,孢子固定化木聚糖酶显著降低了固定化过程中化学试剂的使用,同时减少了额外的处理步骤,从而使整体成本大大降低。这种基于酿酒酵母孢子的固定化策略不仅为低聚木糖的高效生物制备提供了理论支撑,更为开发适应复杂工业场景的稳健型酶制剂奠定了技术基础,展现出巨大的应用潜力。
[1] 张凡星, 薛嘉懿, 覃杰, 等.木聚糖酶的工业应用研究进展[J].农产品加工, 2024(24):64-68.
ZHANG F X, XUE J Y, QIN J, et al.Research progress in industrial application of xylanase[J].Farm Products Processing, 2024(24):64-68.
[2] 刘玉春, 张维清, 任菲, 等.裂褶菌极端嗜盐木聚糖酶ScXyn22的性质及对全麦面包品质的影响[J].食品科学, 2022, 43(18):127-133.
LIU Y C, ZHANG W Q, REN F, et al.Properties of extremely halotolerant xylanase ScXyn22 from Schizophyllum commune and its effect on the quality of whole wheat bread[J].Food Science, 2022, 43(18):127-133.
[3] NERI L C M, GU MUNDSSON H, MEURRENS G, et al.Identification and characterization of endo-xylanases from families GH10 and GH11 sourced from marine thermal environments[J].Enzyme and Microbial Technology, 2025, 187:110592.
MUNDSSON H, MEURRENS G, et al.Identification and characterization of endo-xylanases from families GH10 and GH11 sourced from marine thermal environments[J].Enzyme and Microbial Technology, 2025, 187:110592.
[4] 杨行, 张文娇, 闫协民, 等.嗜热拟青霉耐热阿拉伯木聚糖酶的异源表达及其对麦芽糖化的影响[J/OL].食品工业科技, 2025.DOI:10.13386/j.issn1002-0306.2024100013.
YANG X, ZHANG W J, YAN X M, et al.Heterologous expression of a thermostable arabinoxylan specific xylanase from Paecilomyces thermophila J18 in Aspergillus niger and its application in malt mashing[J/OL].Science and Technology of Food Industry, 2025.DOI:10.13386/j.issn1002-0306.2024100013.
[5] ALI S M, NOBY N, SOLIMAN N A, et al.RETRACTED ARTICLE:Isolation, expression, and in silico profiling of a thermostable xylanase from Geobacillus stearothermophilus strain NASA267:Insights into structural features and agro-waste valorization[J].Microbial Cell Factories, 2025, 24(1):69.
[6] 韩雪, 张阿娜, 王海燕, 等.基于计算设计的GH11家族木聚糖酶CDBFV的热稳定性改造及潜在机制研究[J].生物技术通报, 2024, 40(10):305-314.
HAN X, ZHANG A N, WANG H Y, et al.Computer-aided thermostability engineering and underlying mechanism investigation of the GH11 family xylanase CDBFV[J].Biotechnology Bulletin, 2024, 40(10):305-314.
[7] 杨诚睿, 姜永坤, 秦筠霞, 等.纳米磁性壳聚糖微球固定化Cellic CTec 3的制备及在玉米秸秆酶解中的应用[J/OL].吉林农业大学学报, 2025.DOI:10.13327/j.jjlau.2024.0575.
YANG C R, JIANG Y K, QIN Y X, et al.Preparation of immobilized Cellic CTec 3 by magnetic chitosan nanoparticles and its application in enzymatic digestion of corn stover[J/OL].Journal of Jilin Agricultural University, 2025.DOI:10.13327/j.jjlau.2024.0575.
[8] 李曦月, 倪孟祥.耐热木聚糖酶研究进展[J].化学与生物工程, 2023, 40(12):1-5.
LI X Y, NI M X.Research progress in thermostable xylanase[J].Chemistry &Bioengineering, 2023, 40(12):1-5.
[9] TAGHIZADEH N, ARIAEENEJAD S, GHOLLASI M, et al.Development of polyvinyl alcohol-gum Arabic hydrogel nanocomposite for xylanase immobilization and its role in poultry feed enhancement[J].Carbohydrate Polymer Technologies and Applications, 2025, 9:100722.
[10] ABD RAHMAN N H, RAHMAN R A, ILLIAS R M.Investigating glutaraldehyde cross-linked starch as a hybrid support for immobilizing pectinase and xylanase for pectic-oligosaccharides production[J].Food Bioscience, 2025, 63:105713.
[11] 李婵娟, 汪松波, 吴高兵.两种不同固定化方法对木聚糖酶Xyn11A酶学性质的影响及在低聚木糖制备中的应用[J].食品与发酵工业, 2024, 50(10):17-23.
LI C J, WANG S B, WU G B.Effects of two different immobilization methods on enzymatic properties of xylanase Xyn11A and applications in production of xylooligosaccharides[J].Food and Fermentation Industries, 2024, 50(10):17-23.
[12] ABDUL MANAF S A, MOHAMAD FUZI S F Z, LOW K O, et al.Carbon nanomaterial properties help to enhance xylanase production from recombinant Kluyveromyces lactis through a cell immobilization method[J].Applied Microbiology and Biotechnology, 2021, 105(21):8531-8544.
[13] 张谦, 王宏宇, 赵世琦, 等.木聚糖酶的大肠杆菌细胞表面展示[J/OL].微生物学通报, 2025.DOI:10.13344/j.microbiol.china.250145.
ZHANG Q, WANG H Y, ZHAO S Q, et al.Effective surface display of xylanase on the cells of Escherichia coli[J/OL].Microbiology China, 2025.DOI:10.13344/j.microbiol.china.250145.
[14] WEE M Y J, AZELEE N I W, PACHELLES S, et al.Bioconversion of pineapple pomace for xylooligosaccharide synthesis using surface display of xylanase on Escherichia coli[J].Biomass Conversion and Biorefinery, 2022, 12(12):6003-6014.
[15] LIANG H L, WANG Q, SHEN S, et al.Yeast surface displayed xylanase is an efficient strategy to induce corn defence response[J].Biotechnology &Biotechnological Equipment, 2020, 34(1):665-672.
[16] 杜祥坤, 费康清, 王亚森, 等.酿酒酵母孢子“微胶囊”表面展示乙醛脱氢酶以及检测乙醛的应用[J].食品与发酵工业, 2024, 50(22):318-326.
DU X K, FEI K Q, WANG Y S, et al.Displaying of acetaldehyde dehydrogenase on surface of “microcapsules” of Saccharomyces cerevisiae spores and applications for detection of acetaldehyde[J].Food and Fermentation Industries, 2024, 50(22):318-326.
[17] CHAO Q, LI T L, JIA J X, et al.Spore-encapsulating glycosyltransferase catalysis tandem reactions:Facile chemoenzymatic synthesis of complex human glycans[J].ACS Catalysis, 2022, 12(5):3181-3188.
[18] 白佳文, 王亚森, 杜祥坤, 等.酿酒酵母孢子固定化聚对苯二甲酸乙二醇酯水解酶的酶学性质研究[J].食品与发酵工业, 2025, 51(5):78-84.
BAI J W, WANG Y S, DU X K, et al.Enzymatic properties of polyethylene terephthalate hydrolase immobilized by yeast spores[J].Food and Fermentation Industries, 2025, 51(5):78-84.
[19] KONG J, LI Z J, ZHANG H J, et al.Consecutive hydrolysis of creatinine using creatininase and creatinase encapsulated in Saccharomyces cerevisiae spores[J].Biotechnology Letters, 2017, 39(2):261-267.
[20] BRIZA P, BREITENBACH M, ELLINGER A, et al.Isolation of two developmentally regulated genes involved in spore wall maturation in Saccharomyces cerevisiae[J].Genes &Development, 1990, 4(10):1775-1789.
[21] PAN H P, WANG N, TACHIKAWA H, et al.Osw2 is required for proper assembly of glucan and/or mannan layers of the yeast spore wall[J].Journal of Biochemistry, 2018, 163(4):293-304.
[22] KIM B S, JEONG B M, KIM D, et al.Biochemical characterization of a GH11 xylanase from xylanase-producing Trichoderma citrinoviride[J].Applied Biochemistry and Biotechnology, 2025, 197(6):3929-3945.
[23] YANG H, WANG S, CHEN M, et al.Preparation of spore-immobilized glutathione reductase and its application in inhibiting browning of pear wine[J].Journal of the Science of Food and Agriculture, 2024, 104(11):6914-6923.
[24] 覃池, 刘书亮, 李建龙, 等.重组木聚糖酶xynP N-末端对酸稳定性的影响及在苹果汁澄清中的应用[J].中国食品学报, 2024, 24(11):163-175.
QIN C, LIU S L, LI J L, et al.Effects of recombinant xylanase xynP N-terminal on acid stability and application in clarification of apple juice[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(11):163-175.
[25] YANG Y, YANG G L, LI Z J, et al.Studies on the proteinaceous structure present on the surface of the Saccharomyces cerevisiae spore wall[J].Journal of Fungi, 2023, 9(4):392.
[26] LEE-SOETY J Y, RESCH G, RIMAL A, et al.The MAPK homolog, Smk1, promotes assembly of the glucan layer of the spore wall in S.cerevisiae[J].Yeast, 2024, 41(7):448-457.
[27] KUMAR S, HAQ I, PRAKASH J, et al.Improved enzyme properties upon glutaraldehyde cross-linking of alginate entrapped xylanase from Bacillus licheniformis[J].International Journal of Biological Macromolecules, 2017, 98:24-33.
[28] 李婉杰, 王亚森, 陈洲, 等.基于壳聚糖结合模块构建新型酿酒酵母孢子表面展示系统[J].微生物学报, 2022,62(11):4431-4446.
LI W J, WANG Y S, CHEN Z, et al.Construction of a novel Saccharomyces cerevisiae spore surface display system based on chitosan-binding module[J].Acta Microbiologica Sinica, 2022, 62(11):4431-4446.
[29] 冯晓婷. 草酸青霉木聚糖酶Xyn10A在木质素上的吸附特征及弱木质素吸附的木聚糖酶构建[D].济南:山东大学, 2022.
FENG X T.The adsorption characteristics of xylanase Xyn10A from Penicillium chlorophytum onto lignin and construction of “weak lignin-adsorbed” xylanase[D].Jinan:Shandong University, 2022.
[30] AMARO-REYES A, D AZ-HERN
AZ-HERN NDEZ A, GRACIDA J, et al.Enhanced performance of immobilized xylanase/filter paper-ase on a magnetic chitosan support[J].Catalysts, 2019, 9(11):966.
NDEZ A, GRACIDA J, et al.Enhanced performance of immobilized xylanase/filter paper-ase on a magnetic chitosan support[J].Catalysts, 2019, 9(11):966.
[31] 杨行, 马俊文, 李延啸, 等.毛壳霉木聚糖酶B(CsXyn11B)的分泌表达及其在面包中的应用[J].食品工业科技, 2023, 44(4):108-113.
YANG X, MA J W, LI Y X, et al.Secretion expression of xylanase B (CsXyn11B) from Chaetomium sp.and its application in bread[J].Science and Technology of Food Industry, 2023, 44(4):108-113.
[32] 余静, 刘学强, 马俊文, 等.棘孢木霉GH11家族木聚糖酶的异源表达及酶学性质[J].食品科学技术学报, 2020, 38(6):29-38.
YU J, LIU X Q, MA J W, et al.Heterologous expression and enzymatic properties of xylanase of GH11 family from Trichoderma asperellum[J].Journal of Food Science and Technology, 2020, 38(6):29-38.
[33] 邓香连, 刘清怡, 熊海容, 等.基于酵母表面展示技术的耐热木聚糖酶全细胞催化剂的构建及酶学性质研究[J].湖北农业科学, 2021, 60(7):120-125.
DENG X L, LIU Q X, XIONG H R, et al.Construction of the thermostable xylanase whole-cell biocatalyst based on yeast cell surface display technology and enzymatic analyses[J].Hubei Agricultural Sciences, 2021, 60(7):120-125.