超氧化物歧化酶(superoxide dismutase,EC l.15.1.1,SOD)是一种广泛存在于好氧生物细胞内的金属酶,可专一性催化超氧阴离子自由基歧化生成H2O2和O2,通过清除自由基抵御氧化应激介导的细胞损伤[1];具有抗氧化、抗衰老等诸多生物学功能,目前已广泛应用于功能性食品、医药制剂及化妆品等领域。真核微生物的SOD含量明显高于原核微生物,在真核微生物中,酵母的SOD含量普遍高于丝状真菌[2]。
根据QB/T 5323—2018《植物酵素》规定,食用植物酵素是指以可用于食品加工的植物为主要原料,经微生物发酵制得的含有特定生物活性成分可供人类食用的酵素产品。植物性原料经过微生物发酵后,产生了一些新的活性物质(SOD、γ-氨基丁酸)及香气化合物,提升了原料的功能性和风味品质[3]。食用植物酵素富含功效酶、多酚类物质、有机酸及维生素等多种活性成分,因而具备维持肠道健康[4]、清除自由基、抗氧化[5]等生理功能。在食用植物酵素的发酵过程中,微生物代谢会产生多种功能性酶类,其中SOD常被作为评价酵素产品酶活力的关键指标性酶,因此,在植物酵素的加工中,筛选高产SOD的发酵菌种是目前酵素研究的重要方向之一。
酵母菌是人工接种发酵制备酵素的常用菌种,其本身富含多种人体必需氨基酸和B族维生素,在适宜条件下可产生SOD等功效酶,以及苯乙醇、异戊醇等芳香化合物[6]。LI等[7]用5种酵母菌发酵猕猴桃并对产物进行综合表征,结果表明,发酵过程中猕猴桃汁的有机酸和多酚含量显著提升,同时生成大量酯类物质,有效改善了产品的风味特征。不同酵母菌产SOD的能力不同,且受到发酵原料、发酵条件等的影响。王印壮等[8]对夏黑葡萄酵素发酵的最适酵母菌进行筛选,发现接种酿酒酵母XQ-05处理组的SOD活力在第2天达到最大值,为58.06 U/mL。刘鑫等[9]用植物乳植杆菌和酵母菌发酵蓝莓酵素,其SOD活力达到84.17 U/g。
刺葡萄[Vitis davidii (Rom.Caill.) Fo⊇x]属葡萄科葡萄属的原生葡萄品种,香气独特且营养价值高,目前多用于酿酒,但利用其进行酵素加工的研究鲜见报道。本研究以福建省农产品(食品)微生物种质资源库的菌种为基础,筛选出适于刺葡萄酵素发酵的高产SOD优良酵母,通过产酶条件优化及酶动力学研究,为高品质刺葡萄酵素研发提供理论基础,进而推动刺葡萄的多元化利用并提升其附加值。
1 材料与方法
1.1 材料与试剂
紫秋刺葡萄(福建省德化县,2024年10月采摘,树龄10年),福建省春秋农林科技有限公司;孟加拉红培养基、YPD液体培养基、麦芽汁肉汤,青岛高科技工业园海博生物技术有限公司;蛋白胨、酵母粉,北京索莱宝科技有限公司;CuSO4·5H2O、ZnSO4·7H2O、无水葡萄糖,国药集团化学试剂有限公司;总超氧化物歧化酶测定试剂盒(WST-1法),南京建成生物技术研究所;BCA蛋白浓度测定试剂盒,福建荷瑞生物技术有限公司;马克斯克鲁维酵母CSJ6,市购;其余酵母菌株,福建省农产品(食品)微生物种质资源库,菌株信息同2.1节中表2。
1.2 仪器与设备
MQD-S3R多层振荡培养箱,上海旻泉仪器有限公司;LRH-250生化培养箱,上海一恒科学仪器有限公司;GI29DS高压灭菌锅,致微仪器有限公司;Himac CR22 N高速冷冻离心机,日本日立株式会社;SCIENTZ-950E超声波细胞粉碎机,宁波新芝生物科技股份有限公司;UH5300分光光度计,日立科学仪器有限公司;Bio Tek Epoch2全波长酶标仪,美国伯腾仪器有限公司。
1.3 实验方法
1.3.1 菌株活化
取出-80 ℃超低温冰箱中保存在冻存管中的甘油酵母菌悬液,分别取200 μL涂布于孟加拉红培养基上,28 ℃恒温培养24 h,挑出单菌落接种至10 mL YPD液体培养基中,28 ℃、150 r/min振荡培养24 h;在无菌条件下,进行2次传代。
1.3.2 高产SOD酵母菌初筛
1.3.2.1 产SOD酵母菌发酵培养基
培养基配制(g/L):酵母粉5,蛋白胨10,葡萄糖40,ZnSO4·7H2O 0.5,CuSO4·5H2O 0.2。121 ℃下高温灭菌30 min。
1.3.2.2 液体培养基接种发酵
将20种不同的酵母菌活化后,按2%接种量分别接入产SOD发酵培养基中,于28 ℃、150 r/min培养24 h。
1.3.2.3 培养基发酵SOD活力的测定
参考韦琰琰[10]的方法并稍作修改,取5 mL发酵液于4 ℃、8 000 r/min离心20 min,用磷酸缓冲液(pH 7.0)将菌体清洗3次,4 ℃、8 000 r/min离心10 min,弃上清液。加入5 mL磷酸缓冲液(pH 7.0)至离心得到的湿菌体中,利用超声波细胞破碎机超声波冰浴破碎,设置超声功率400 W,超声3 s,间隔4 s,总时间30 min。4 ℃、8 000 r/min离心20 min,弃沉淀,留上清液,即为粗酶液。参照BCA蛋白定量试剂盒的说明书,制作蛋白标准曲线,测定粗酶液蛋白含量,并调整粗酶液蛋白质量浓度为(0.5±0.05) mg/mL。使用SOD测定试剂盒(WST-1法)测定SOD活力,具体方法参考说明书。
1.3.3 刺葡萄发酵高产SOD酵母菌复筛
挑选25 kg无机械伤、病害的新鲜刺葡萄,洗净、破碎,分别分装0.3 kg在灭菌后的500 mL三角瓶中,105 ℃高压灭菌15 min[11],得到发酵基质,4层纱布封口。分别收集5株酵母菌对数生长期末期的菌液,于4 ℃、8 000 r/min离心10 min。用磷酸缓冲液(pH 7.0)将菌体清洗3次,4 ℃、8 000 r/min离心10 min,弃上清液,再用与菌液同等体积的无菌水重悬酵母菌体,无菌环境下接种至刺葡萄发酵基质中,置于26 ℃恒温培养箱中发酵10 d,每隔2 d取样,测定SOD活力、多酚含量、酒精度等各项指标。
1.3.4 酵母菌发酵刺葡萄产SOD活力条件优化
1.3.4.1 单因素试验
1)发酵时间对刺葡萄SOD活力影响
在发酵温度26 ℃、克鲁维毕赤酵母JLG30201接种量为3%的条件下,分别在接种后2、4、6、8、10 d取样并测定SOD活力,以刺葡萄发酵液中SOD活力为指标,确定酵母菌发酵刺葡萄的最佳发酵时间,每个处理重复3次。
2)酵母接种量对刺葡萄SOD活力影响
在发酵温度26 ℃的条件下,将克鲁维毕赤酵母JLG30201分别以1%、2%、3%、4%、5%接种量接种于刺葡萄发酵基质中,发酵8 d取样并测定SOD活力。以刺葡萄发酵汁中SOD活力为指标,确定酵母菌发酵的最佳接种量,每个处理重复3次。
3)发酵温度对刺葡萄SOD活力影响
将克鲁维毕赤酵母JLG30201以3%接种量接种于刺葡萄发酵基质中,分别设定发酵温度为20、23、26、29、32 ℃,发酵8 d取样并测定SOD活力,以刺葡萄发酵汁中SOD活力为指标,确定酵母菌发酵的最佳温度,每个处理重复3次。
1.3.4.2 正交试验
在上述单因素试验的基础上,以发酵时间、酵母菌接种量以及发酵温度3个因素,以产酶活力为指标,设计L9(34)的正交试验,因素及水平见表1。
表1 酵母菌发酵刺葡萄正交试验因素与水平
Table 1 Factors and levels of orthogonal experiment on yeast fermentation of Vitis davidii Fo⊇x
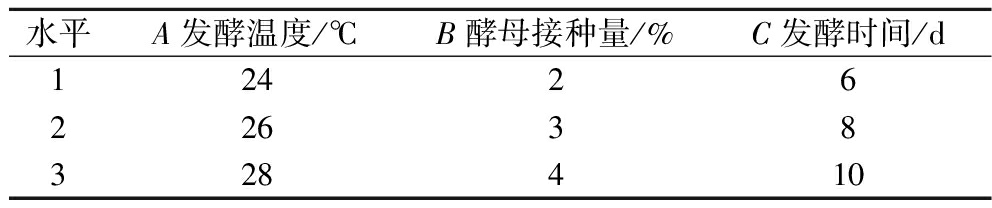
水平A发酵温度/℃B酵母接种量/%C发酵时间/d1242622638328410
1.3.5 酵母菌发酵刺葡萄产SOD动力学研究
以正交试验优化得出的工艺对刺葡萄进行接种发酵,每隔1 d取样,测定还原糖含量、SOD活力、酵母菌活菌数量。在Logistic模型、SGompertz方程以及DoseResp模型的基础上,通过测定刺葡萄在酵母菌发酵过程中发酵液的菌体浓度、底物消耗量以及产物生成量,运用Origin 2024软件进行非线性拟合,建立还原糖消耗、菌体生长、SOD生成的动力学模型[12]。
1.3.6 指标测定方法
还原糖含量参照GB 5009.7—2016《食品安全国家标准 食品中还原糖的测定》中的直接滴定法测定;酒精度参照GB 5009.225—2023《食品安全国家标准 酒和食用酒精中乙醇浓度的测定》中的方法测定;多酚含量参照GB/T 31740.2—2015《茶制品 第2部分:茶多酚》附录A规定的方法测定;SOD活力使用南京建成生物技术研究所的总超氧化物歧化酶测定试剂盒(WST-1法)测定;酵母菌活菌数参照GB 4789.15—2016《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》中的霉菌和酵母平板计数法测定。
1.4 数据处理
利用Excel对试验数据进行记录及处理,利用DPS软件对试验进行设计,并对实验结果进行分析;利用Origin 2024作图并分析。
2 结果与分析
2.1 高产SOD酵母菌初筛
不同酵母菌在培养基中发酵产生的SOD活力差异较大,其活力范围为(21.31±1.12)~(338.91±16.49) U/mg prot(表2)。产酶能力前5的酵母菌分别为:酿酒酵母JJ4、酿酒酵母J4、马克斯克鲁维酵母CSJ5、克鲁维毕赤酵母JLG30201和汉逊德巴利酵母CSJ8,其SOD酶活分别为(338.91±16.49)、(230.02±15.04)、(225.57±17.22)、(214.80±9.47)、(204.77±5.51) U/mg prot。以上5株酵母在产酶培养基中的SOD产酶能力均显著高于周湘人[13]从藏灵菇中筛选的高抗氧化活性酵母菌KM-4,SOD活力为(145.04±4.41) U/mg port。实验选用以上5株酵母菌,进一步筛选用于刺葡萄酵素发酵的高产SOD酵母菌株。
表2 酵母菌信息及培养基发酵SOD活力
Table 2 Yeast strain information and SOD activity in yeast culture medium
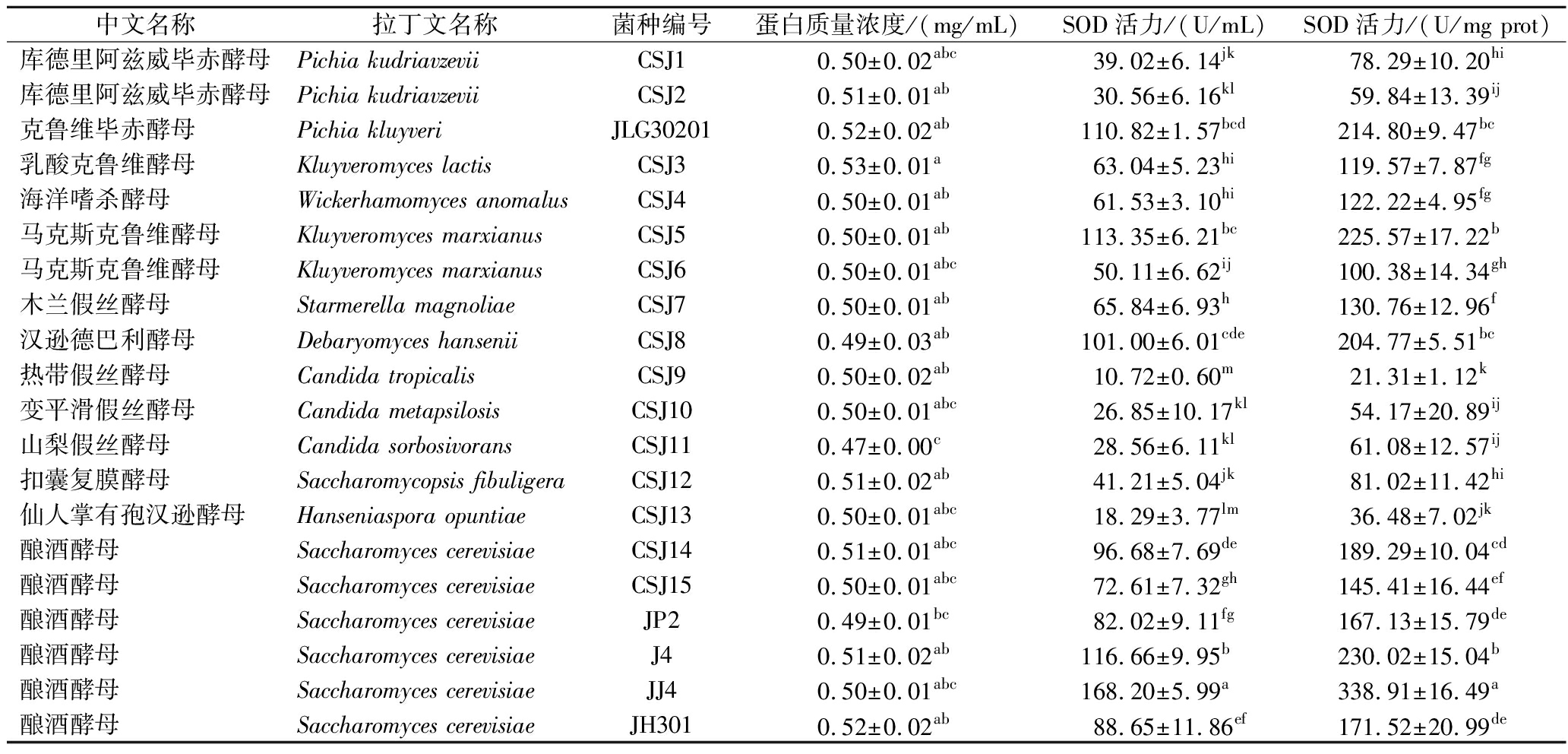
中文名称拉丁文名称菌种编号蛋白质量浓度/(mg/mL)SOD活力/(U/mL)SOD活力/(U/mg prot)库德里阿兹威毕赤酵母Pichia kudriavzeviiCSJ10.50±0.02abc39.02±6.14jk78.29±10.20hi库德里阿兹威毕赤酵母Pichia kudriavzeviiCSJ20.51±0.01ab30.56±6.16kl59.84±13.39ij克鲁维毕赤酵母Pichia kluyveriJLG302010.52±0.02ab110.82±1.57bcd214.80±9.47bc乳酸克鲁维酵母Kluyveromyces lactisCSJ30.53±0.01a63.04±5.23hi119.57±7.87fg海洋嗜杀酵母Wickerhamomyces anomalusCSJ40.50±0.01ab61.53±3.10hi122.22±4.95fg马克斯克鲁维酵母Kluyveromyces marxianusCSJ50.50±0.01ab113.35±6.21bc225.57±17.22b马克斯克鲁维酵母Kluyveromyces marxianusCSJ60.50±0.01abc50.11±6.62ij100.38±14.34gh木兰假丝酵母Starmerella magnoliaeCSJ70.50±0.01ab65.84±6.93h130.76±12.96f汉逊德巴利酵母Debaryomyces hanseniiCSJ80.49±0.03ab101.00±6.01cde204.77±5.51bc热带假丝酵母Candida tropicalisCSJ90.50±0.02ab10.72±0.60m21.31±1.12k变平滑假丝酵母Candida metapsilosisCSJ100.50±0.01abc26.85±10.17kl54.17±20.89ij山梨假丝酵母Candida sorbosivoransCSJ110.47±0.00c28.56±6.11kl61.08±12.57ij扣囊复膜酵母Saccharomycopsis fibuligeraCSJ120.51±0.02ab41.21±5.04jk81.02±11.42hi仙人掌有孢汉逊酵母Hanseniaspora opuntiaeCSJ130.50±0.01abc18.29±3.77lm36.48±7.02jk酿酒酵母Saccharomyces cerevisiaeCSJ140.51±0.01abc96.68±7.69de189.29±10.04cd酿酒酵母Saccharomyces cerevisiaeCSJ150.50±0.01abc72.61±7.32gh145.41±16.44ef酿酒酵母Saccharomyces cerevisiaeJP20.49±0.01bc82.02±9.11fg167.13±15.79de酿酒酵母Saccharomyces cerevisiaeJ40.51±0.02ab116.66±9.95b230.02±15.04b酿酒酵母Saccharomyces cerevisiaeJJ40.50±0.01abc168.20±5.99a338.91±16.49a酿酒酵母Saccharomyces cerevisiaeJH3010.52±0.02ab88.65±11.86ef171.52±20.99de
注:根据Duncan测验,同列数据字母不同表示差异显著(P<0.05)。
2.2 刺葡萄酵素发酵中高产SOD酵母菌的复筛
由图1可知,刺葡萄在5株酵母菌发酵过程中,SOD活力均处于先上升后趋于平稳或下降,其中接种JLG30201的刺葡萄发酵液的SOD活力在第8天达到最大值,故比较各酵母菌发酵8 d后刺葡萄发酵液的多酚含量、还原糖含量和酒精度。
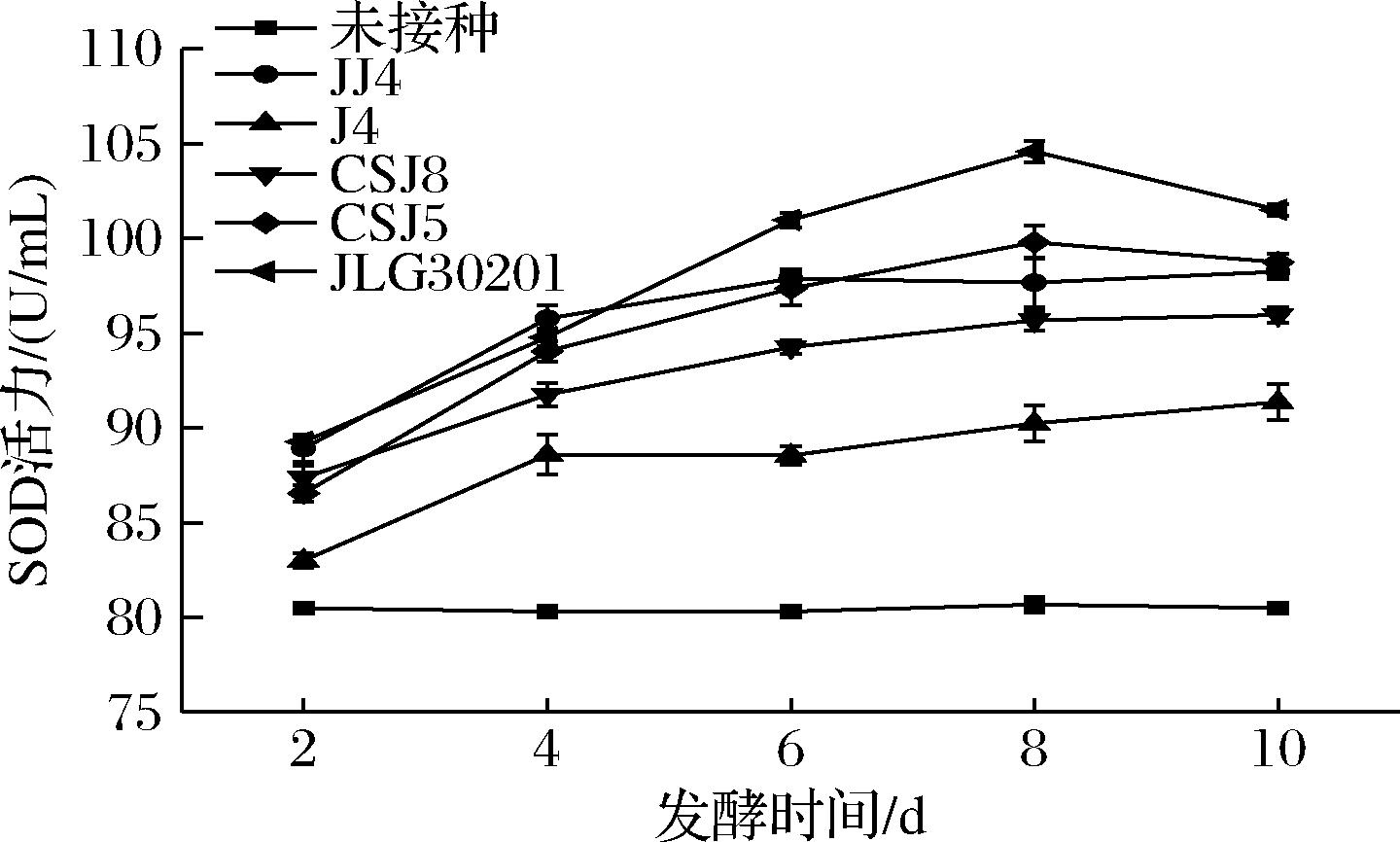
图1 五株酵母菌发酵刺葡萄发酵液中SOD活力变化
Fig.1 Changes of SOD activity in the fermentation broth of V. davidii fermented by 5 yeast strains
由表3可知,5株酵母菌发酵刺葡萄汁8 d后,各发酵组SOD活力均显著高于未接种酵母菌组,其中接种JLG30201的刺葡萄发酵液SOD活力显著高于接种其他4株酵母菌,其SOD活力为(104.6±0.46) U/mL,其次为经酿酒酵母JJ4发酵的刺葡萄发酵液,SOD活力为(97.66±1.06) U/mL。酚类物质具有较强的抗氧化性[14],5株酵母菌发酵的刺葡萄发酵液中多酚含量均显著高于未接种酵母菌的样品,这与LI等[15]的研究相似,其发现猕猴桃经过酵母菌和乳酸菌发酵前期,总酚类化合物含量显著升高。发酵时间对蓝莓酵素SOD活力影响结果大概一致;经JJ4和JLG30201发酵后,刺葡萄发酵液中多酚含量显著高于其他3株酵母菌,多酚含量分别为(1 129.47±14.10)、(1 153.09±9.41) μg/mL,毕赤酵母在发酵过程中可以产生水解酶,可能造成酚类物质的降解或转化[16]。
表3 不同酵母菌发酵8 d的刺葡萄发酵液各指标
Table 3 Various indicators in V. davidii fermentation broth fermented by different yeast strains for 8 days
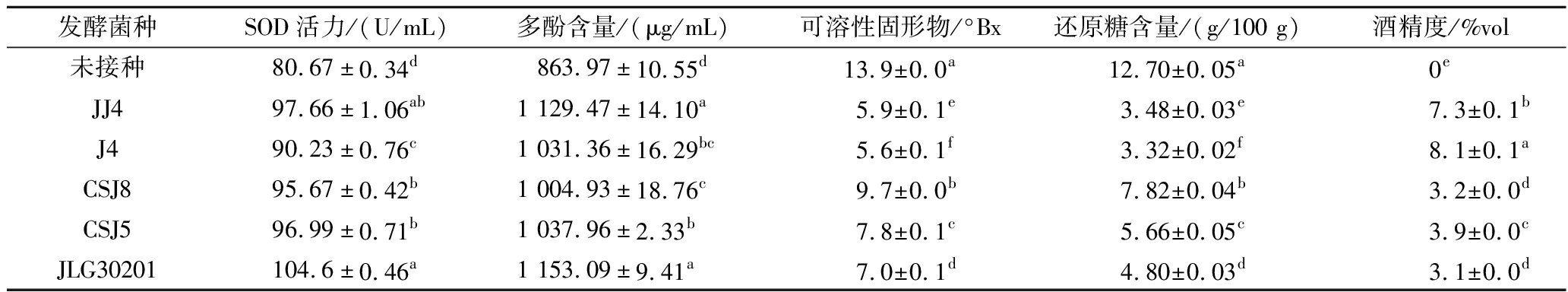
发酵菌种SOD活力/(U/mL)多酚含量/(μg/mL)可溶性固形物/°Bx还原糖含量/(g/100 g)酒精度/%vol未接种80.67±0.34d863.97±10.55d13.9±0.0a12.70±0.05a0eJJ497.66±1.06ab1 129.47±14.10a5.9±0.1e3.48±0.03e7.3±0.1bJ490.23±0.76c1 031.36±16.29bc5.6±0.1f3.32±0.02f8.1±0.1aCSJ895.67±0.42b1 004.93±18.76c9.7±0.0b7.82±0.04b3.2±0.0dCSJ596.99±0.71b1 037.96±2.33b7.8±0.1c5.66±0.05c3.9±0.0cJLG30201104.6±0.46a1 153.09±9.41a7.0±0.1d4.80±0.03d3.1±0.0d
注:根据Duncan测验,同列数据中字母不同表示差异显著(P<0.05)。
糖类物质作为酵母菌生长和代谢的核心碳源,在微生物发酵过程中发挥着关键作用。酵母菌通过糖酵解途径(EMP途径)等代谢通路,将糖类转化为丙酮酸等中间产物,进而生成酒精、CO2等多种代谢终产物;还原糖、乙醇含量的变化可以反映出微生物代谢情况并直接影响产品风味[2]。由表3可知,酿酒酵母J4与酿酒酵母JJ4耗糖能力最强;其次为克鲁维毕赤酵母JLG30201、马斯克鲁维酵母CSJ5;汉逊德巴利酵母CSJ8耗糖能力最差。经过酿酒酵母JJ4、酿酒酵母J4发酵的刺葡萄发酵液酒精度相对较高;其次为马斯克鲁维酵母CSJ5;经过克鲁维毕赤酵母JLG30201和汉逊德巴利酵母CSJ8发酵的刺葡萄发酵液酒精度较低。
结合上述实验结果可知,克鲁维毕赤酵母JLG30201发酵刺葡萄产SOD能力较强,发酵过程中酒精产量较低,同时可提高产物中多酚含量,是刺葡萄酵素发酵的优选菌种。
2.3 克鲁维毕赤酵母JLG30201发酵刺葡萄酵素工艺优化
2.3.1 单因素试验结果
SOD是食用植物酵素的功效酶之一,可催化超氧阴离子自由基歧化成分子氧和过氧化氢,在应对氧化应激中起关键作用[17]。由图2-a可知,在26 ℃下随着发酵时间的延长,克鲁维毕赤酵母JLG30201发酵刺葡萄发酵液中,SOD活力呈现出先增加后降低的趋势,降低的原因可能是在快速增殖阶段,随着菌体密度显著增加,对营养物质的竞争加剧;同时,进入衰老期的酵母为维持基本代谢活动,会大量消耗培养体系中的次级代谢产物,使得SOD活力降低[18]。在发酵时间为0~8 d内,随时间的延长,刺葡萄发酵液中SOD活力逐渐增加,于8 d时达到最大,为(104.60±0.48) U/mL,然而当发酵时间超过8 d时,刺葡萄发酵液中SOD活力开始降低。这与白琳[19]研究的发酵时间对蓝莓酵素SOD活力影响结果大概一致。因此,选择6~10 d作为正交试验的发酵时间范围。
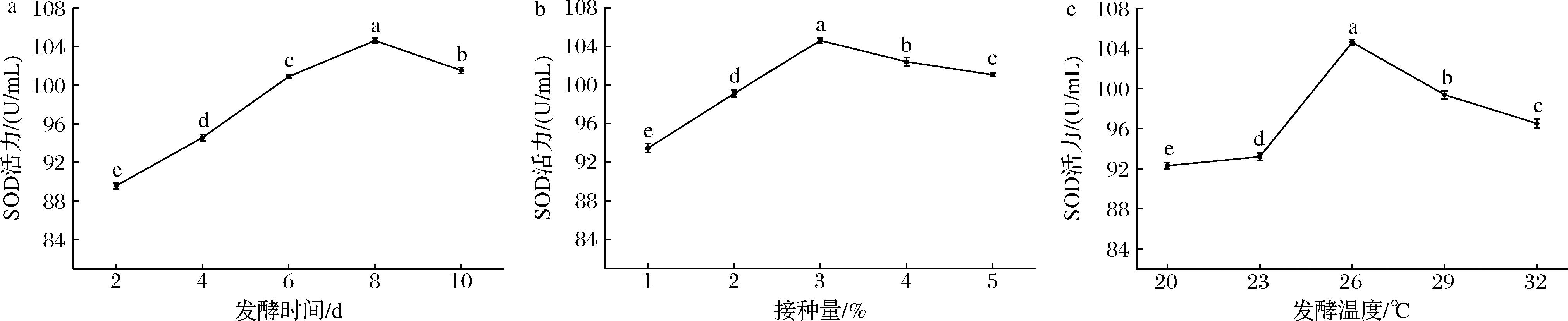
a-不同发酵时间的刺葡萄发酵液SOD活力;b-不同酵母接种量的刺葡萄发酵液SOD活力;c-不同发酵温度的刺葡萄发酵液SOD活力
图2 不同发酵时间、酵母菌接种量、发酵温度的刺葡萄发酵液SOD活力
Fig.2 SOD activity in fermentation broth of Vitis davidii Fo⊇x with different fermentation time, yeast inoculums, fermentation temperatures
注:根据Duncan测验,不同小写字母表示差异显著(P<0.05)。
如图2-b可知,将克鲁维毕赤酵母JLG30201在26 ℃温度下发酵时,当发酵基质中的营养物质一定时,接种量过小,酵母菌生长代谢缓慢,培养时间延长,代谢产物合成缓慢或降低[20];随着接种量的增大,发酵基质中营养物质不再充裕甚至匮乏,酵母菌的生长可能受到影响。当接种量为3%时,发酵液中SOD活力最高,可能是因为此接种量下,酵母菌的生长最适并合成大量SOD。因此选择2%~4%作为正交试验的酵母菌接种量。
如图2-c可知,当发酵温度为20~26 ℃时,刺葡萄发酵液SOD活力随发酵温度的升高而增加。当发酵温度为26 ℃时,刺葡萄发酵液SOD活力达到最大值,为(104.60±0.48) U/mL。但当发酵温度超过26 ℃时,刺葡萄发酵液SOD活力反而下降。这可能是因为克鲁维毕赤酵母JLG30201发酵刺葡萄的最适温度为26 ℃,当环境温度过低时,酵母菌的生理活性会受到抑制,导致其增殖速率降低,发酵周期显著延长;若温度过高,会对机体的酶及代谢活动产生不利影响[21],使得SOD活力下降。因此选择24~28 ℃进行正交试验工艺优化。
2.3.2 正交试验结果
通过单因素试验,选择对刺葡萄发酵液SOD活力影响较明显的3个因素(发酵时间、酵母接种量、发酵温度),从中选择其最优的3个水平进行正交试验,正交结果如表4所示,方差分析如表5所示。
表4 酵母菌发酵刺葡萄SOD活力正交试验结果
Table 4 Orthogonal test results of SOD activity in yeast fermentation of V. davidii
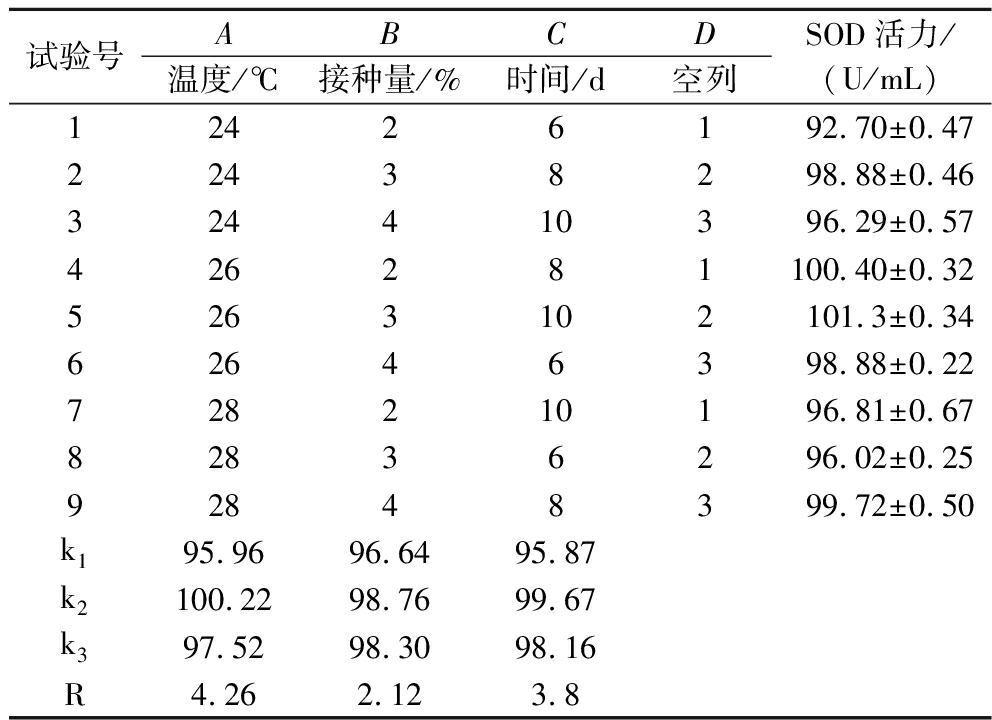
试验号ABCD温度/℃接种量/%时间/d空列SOD活力/(U/mL)12426192.70±0.4722438298.88±0.46324410396.29±0.57426281100.40±0.325263102101.3±0.3462646398.88±0.22728210196.81±0.6782836296.02±0.2592848399.72±0.50k195.9696.6495.87k2100.2298.7699.67k397.5298.3098.16R4.26 2.12 3.8
表5 正交试验方差结果分析
Table 5 Analysis of variance results of orthogonal test
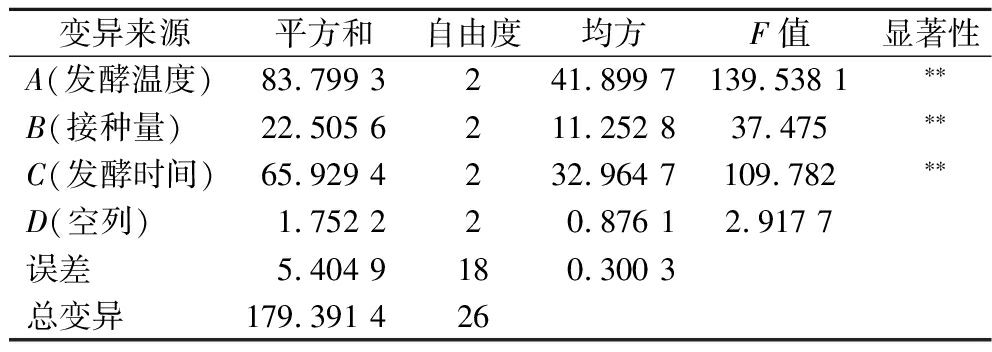
变异来源平方和自由度均方F值显著性A(发酵温度)83.799 3241.899 7139.538 1∗∗B(接种量)22.505 6211.252 837.475∗∗C(发酵时间)65.929 4232.964 7109.782∗∗D(空列)1.752 220.876 12.917 7误差5.404 9180.300 3总变异179.391 426
注:**表示差异极显著(P<0.01)。
正交试验结果表明:发酵温度、发酵时间、酵母接种量3个因素对刺葡萄酵素SOD产量的影响均达到极显著水平;影响刺葡萄发酵液SOD活力的因素顺序为发酵温度>发酵时间>酵母接种量。刺葡萄酵素酵母发酵优化组合为A2B2C2,即发酵时间8 d,发酵温度26 ℃,酵母接种量3%,在此最佳条件下得到刺葡萄发酵液SOD活力为(104.40±0.48) U/mL。
2.4 克鲁维毕赤酵母JLG30201发酵刺葡萄产发酵动力学研究
以刺葡萄为原料,克鲁维毕赤酵母JLG30201为菌种进行发酵,发酵过程中SOD活力、还原糖含量以及发酵液酵母活菌数的变化趋势如图3所示。在刺葡萄酵素发酵过程中,发酵液SOD活力、还原糖含量及酵母活菌数之间存在着一定的相互关系;酵母活菌数呈先上升后下降趋势,还原糖含量随时间延长呈下降趋势,SOD活力呈上升趋势,说明发酵液中还原糖一直在被消耗减少,这与WANG等[22]猕猴桃汁在发酵过程中还原糖含量和活力变化结果相似。实验结果表明,底物的消耗、菌体生长和产物的生成均符合微生物生长代谢规律。在发酵结束后刺葡萄发酵液中酵母活菌数为2.86×108 CFU/mL,SOD活力为(104.58±0.27) U/mL,还原糖含量为(4.80±0.03) g/100 g。
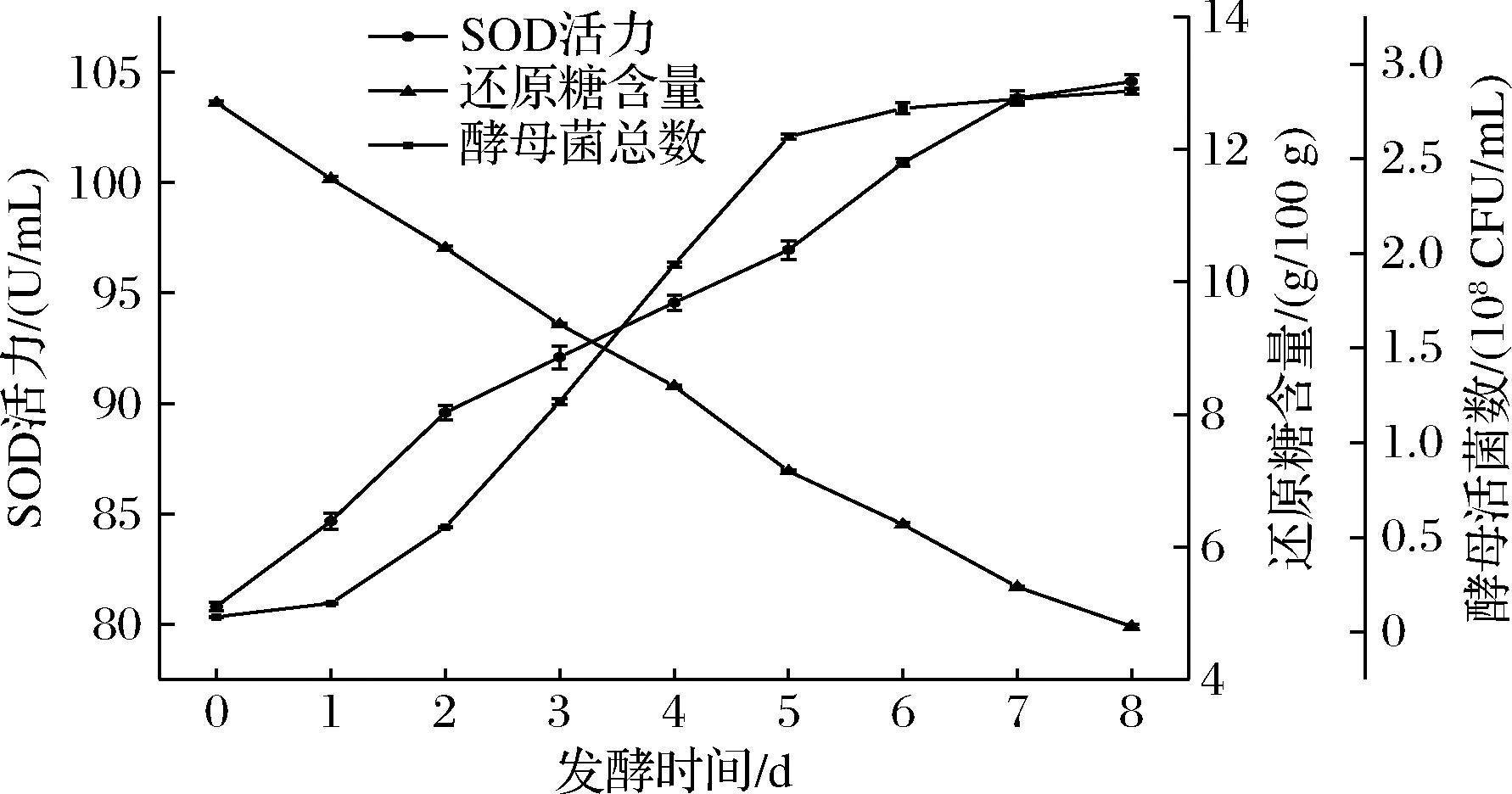
图3 发酵过程中SOD活力、还原糖含量及酵母活菌数的变化
Fig.3 SOD activity, reducing sugar content, number of viable yeast during fermentation
由图3可知,刺葡萄发酵液SOD活力在发酵过程中呈现增加趋势,因此分别用Logistic、DoseResp和 SGompertz模型进行SOD活力变化的非线性拟合,Logistic模型拟合度最高,其拟合方程为y=164.24-83.44/[1+(x/19.62)0.98],拟合相关系数R2=0.996 9,拟合曲线如图4-a所示。
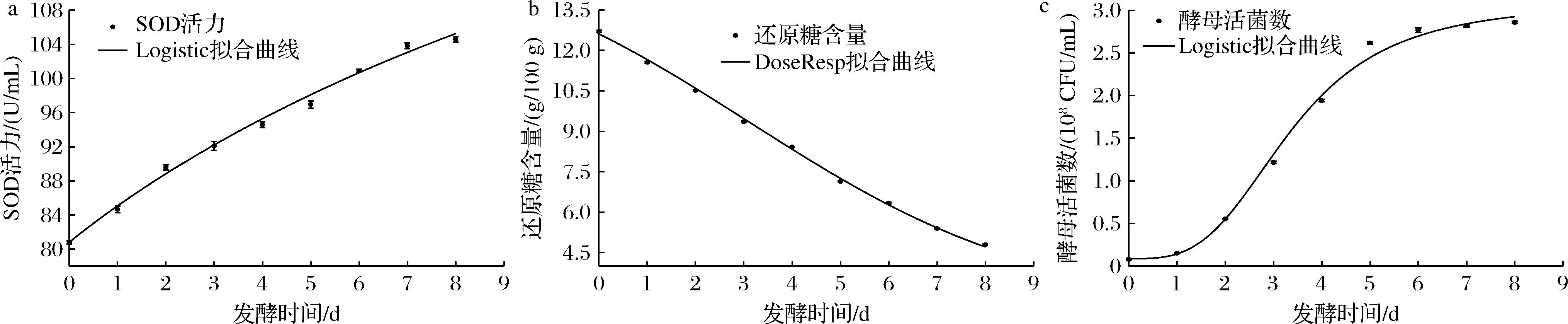
a-发酵过程中SOD活力的拟合曲线;b-还原糖含量的拟合曲线;c-酵母活菌数的拟合曲线
图4 发酵过程中SOD活力、还原糖含量、酵母活菌数的拟合曲线
Fig.4 Fitting curve of SOD activity, reducing sugar content, number of viable yeast during fermentation
糖类作为酵母菌糖代谢的底物不断被消耗,而还原糖是发酵过程中酵母菌生长繁殖的主要能量来源[23]。利用Logistic模型、DoseResp模型和Boltzmann模型对刺葡萄发酵液中还原糖含量变化进行拟合,其中DoseResp模型拟合度最高,拟合方程为y=2.36+13.96/{1+exp[(x-3.11)/3.06]},拟合相关系数R2=0.998 1,该结果与李桂峰等[24]对青枣果酒底物消耗动力学方程所建模型一致。DoseResp模型对刺葡萄酵素发酵过程中的还原糖消耗拟合曲线见图4-b。
由图3可知,酵母菌的菌体数量在发酵过程中呈现增加趋势,因此对发酵0~8 d的菌体生长情况进行非线性拟合。通过Origin软件分别用Logistic模型、DoseResp模型和SGompertz模型进行菌体数量的拟合,Logistic模型对酵母菌生长情况拟合效果最好,拟合方程为y=-9.94+22.58/[1+(x/13.01)1.22],拟合相关系数R2=0.998 0,拟合曲线如图4-c所示。
3 结论与讨论
本研究通过分析不同菌源的酵母菌在液体培养基中产SOD能力以及在刺葡萄汁中产SOD、多酚、酒精能力,筛选出适宜刺葡萄酵素发酵的高产SOD的优良酵母菌为克鲁维毕赤酵母JLG30201,其在发酵培养基和刺葡萄发酵基质中产SOD能力强,产酒精少且可提高酵素产品的多酚含量;优化了克鲁维毕赤酵母JLG30201发酵刺葡萄酵素工艺,即发酵时间8 d,发酵温度26 ℃,酵母接种量3%,在此条件下,酵素产品SOD活力达(104.60±0.48) U/mL,较发酵前增加23.42%;通过测定发酵过程中SOD活力、还原糖含量以及酵母活菌数,进行了发酵动力学分析,结果表明克鲁维毕赤酵母JLG3.0201发酵刺葡萄酵素的产SOD以及酵母活菌数运用Logistic模型的拟合度最高,而发酵中还原糖的变化运用DoseResp模型的拟合度最高。
食用植物酵素是植物性原料经过微生物发酵得到的含有特定生物活性成分的酵素产品。SOD是植物酵素中关键的抗氧化酶,且QB/T5323—2018《植物酵素》规定液态产品的SOD活力在15 U/L以上,且保存时间不少于180 d[25]。乙醇是酵母菌发酵的常见代谢产物,酵母菌在植物酵素发酵过程中,不可避免会产生乙醇,而《植物酵素》对乙醇含量有较为严格的限制,要求不能高于0.5 g/100 g,因此,筛选高产SOD且低产酒精的酵母菌作为植物酵素发酵的菌种,是生产优质植物酵素的重要前提之一。本研究筛选的酵母菌虽然低产酒精,但发酵刺葡萄酒精度也达到3.1%(体积分数),后期需要通过低温蒸馏等处理来脱去乙醇。乳酸菌和酵母菌是食用植物酵素发酵最具代表性的益生菌,由于其益生特性和发酵活性,可作为良好的发酵剂,也可用于改善食品的风味特性和营养特性[26],酵素的发酵通常采用酵母菌与乳酸菌的复合发酵工艺,酵母菌产生酶类(包括SOD)和一些芳香味物质,而乳酸菌则产生γ-氨基丁酸、有机酸等其他功能性成分[6]。本研究利用刺葡萄为发酵原料,仅对高产SOD酵母菌的筛选及发酵条件优化,后续将继续利用筛选出的酵母菌与乳酸菌复合发酵,对刺葡萄酵素的高品质加工技术进行深入研究。
[1] FATTMAN C L, SCHAEFER L M, OURY T D.Extracellular superoxide dismutase in biology and medicine[J].Free Radical Biology &Medicine, 2003, 35(3):236-256.
[2] 裴轶琨. 酵母SOD高产菌的选育及发酵条件的研究[D].吉林:吉林大学, 2006.
PEI Y K.Selection of the SOD high-producing strain from yeasts and its study on fermentaion conditions[D].Jilin:Jilin University, 2006.
[3] LI T L, JIANG T, LIU N, et al.Biotransformation of phenolic profiles and improvement of antioxidant capacities in jujube juice by select lactic acid bacteria[J].Food Chemistry, 2021, 339:127859.
[4] GAO B H, WANG J W, WANG Y H, et al.Influence of fermentation by lactic acid bacteria and in vitro digestion on the biotransformations of blueberry juice phenolics[J].Food Control, 2022, 133:108603.
[5] GHOSH K, RAY M, ADAK A, et al.Microbial, saccharifying and antioxidant properties of an Indian rice based fermented beverage[J].Food Chemistry, 2015, 168:196-202.
[6] 刘恒. 复合酵素的制备及贮藏稳定性研究[D].无锡:江南大学, 2023.
LIU H.Study on preparation and storage stability of complex Jiaosu[D].Wuxi:Jiangnan University, 2023.
[7] LI S Q, BI P F, SUN N, et al.Characterization of different non-Saccharomyces yeasts via mono-fermentation to produce polyphenol-enriched and fragrant kiwi wine[J].Food Microbiology, 2022, 103:103867.
[8] 王印壮, 丁玉峰, 段定定, 等.葡萄酵素发酵过程中的酵母菌筛选及品质变化分析[J].食品与发酵工业, 2022, 48(10):70-77.
WANG Y Z, DING Y F, DUAN D D, et al.Screening of yeast and analysis of quality changes during grape Jiaosu fermentation[J].Food and Fermentation Industries, 2022, 48(10):70-77.
[9] 刘鑫, 朱丹, 牛广财, 等.蓝莓酵素发酵工艺优化[J].中国酿造, 2018, 37(3):171-175.
LIU X, ZHU D, NIU G C, et al.Optimization of fermentation process of blueberry enzyme[J].China Brewing, 2018, 37(3):171-175.
[10] 韦琰琰. 食品中具有抗氧化活性的酵母菌的筛选及其特性的初步研究[D].武汉:华中农业大学, 2013.
WEI Y Y.Screening and study of yeasts with antioxidative activity in foods[D].Wuhan:Huazhong Agricultural University, 2013.
[11] 洪厚胜, 朱曼利, 李伟, 等.葡萄果渣酵素的发酵工艺优化及其理化特性[J].食品科学, 2019, 40(8):63-72.
HONG H S, ZHU M L, LI W, et al.Optimization of fermentation process and physicochemical properties of probiotic fermented grape pomace[J].Food Science, 2019, 40(8):63-72.
[12] 朱艳云. 杨梅渣酵素的制备及其抗氧化功能研究[D].杭州:浙江大学, 2022.
ZHU Y Y.Preparation of Chinese bayberry pomace Jiaosu and study on its antioxidant function[D].Hangzhou:Zhejiang University, 2022.
[13] 周湘人. 藏灵菇中抗氧化酵母筛选及抑制鱼肉脂质氧化研究[D].长沙:中南林业科技大学, 2022.
ZHOU X R.Study on the screening of antioxidant yeast from Tibetan kefir grain and its inhibition of lipid oxidation in fish[D].Changsha:Central South University of Forestry &Technology, 2022.
[14] LUND M N.Reactions of plant polyphenols in foods:Impact of molecular structure[J].Trends in Food Science &Technology, 2021, 112:241-251.
[15] LI Y H, WANG W J, DENG Y Y, et al.Antioxidant properties and changes in vitro digestion of the fermented kiwifruit extract prepared by lactic acid bacteria and yeasts[J].Food Chemistry, 2024, 442:138416.
[16] VIVEK K, MISHRA S, PRADHAN R C, et al.Effect of probiotification with Lactobacillus plantarum MCC 2974 on quality of Sohiong juice[J].LWT, 2019, 108:55-60.
[17] 张秋月, 黎谢飞, 曾小群, 等.产超氧化物歧化酶乳酸菌的筛选及发酵条件优化[J].中国食品学报, 2021, 21(10):143-150.
ZHANG Q Y, LI X F, ZENG X Q, et al.Screening of producing superoxide dismutase lactic acid bacteria and the optimization of fermentation conditions[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(10):143-150.
[18] 赵敏, 王瑜, 李立郎, 等.天麻酵素化过程中风味物质及抗氧化活性动态变化[J].食品与发酵工业, 2021, 47(22):92-98.
ZHAO M, WANG Y, LI L L, et al.Dynamic study on flavor components and antioxidant activity in the fermentation of Gastrodia elata[J].Food and Fermentation Industries, 2021, 47(22):92-98.
[19] 白琳. 蓝莓酵素饮料的研制及其贮藏稳定性的研究[D].乌鲁木齐:新疆大学, 2021.
BAI L.Preparation of blueberry juice and study on its storage stability[D].Urumqi:Xinjiang University, 2021.
[20] 张智慧, 庞惟俏, 徐炳政, 等.藜麦和蓝靛果发酵菌株的筛选及复合发酵工艺的优化[J].食品工业科技, 2024, 45(24):204-213.
ZHANG Z H, PANG W Q, XU B Z, et al.Screening of fermentation strains of quinoa and Lonicera caerulea and optimization of complex fermentation process[J].Science and Technology of Food Industry, 2024, 45(24):204-213.
[21] 陈秋慧, 魏建敏, 穆先, 等.刺梨果渣酵素复合发酵工艺优化[J].中国调味品, 2023, 48(9):122-130.
CHEN Q H, WEI J M, MU X, et al.Optimization of compound fermentation technology of Rosa roxburghii residue enzyme[J].China Condiment, 2023, 48(9):122-130.
[22] WANG Z N, FENG Y Z, YANG N N, et al.Fermentation of kiwifruit juice from two cultivars by probiotic bacteria:Bioactive phenolics, antioxidant activities and flavor volatiles[J].Food Chemistry, 2022, 373:131455.
[23] LI H C, HUANG J T, WANG Y Q, et al.Study on the nutritional characteristics and antioxidant activity of dealcoholized sequentially fermented apple juice with Saccharomyces cerevisiae and Lactobacillus plantarum fermentation[J].Food Chemistry, 2021, 363:130351.
[24] 李桂峰, 燕妮, 原潞, 等.青枣果酒发酵动力学模型[J].食品工业, 2021, 42(5):88-91.
LI G F, YAN N, YUAN L, et al.The fermentation kinetics of green jujube wine[J].The Food Industry, 2021, 42(5):88-91.
[25] 刘恒, 范柳萍, 张涛, 等.复合酵素的贮藏稳定性及货架期研究[J].食品与发酵工业, 2024, 50(1):59-66.
LIU H, FAN L P, ZHANG T, et al.Storage stability and shelf-life of complex Jiaosu[J].Food and Fermentation Industries, 2024, 50(1):59-66.
[26] CAI L Q, WANG W J, TONG J W, et al.Changes of bioactive substances in lactic acid bacteria and yeasts fermented kiwifruit extract during the fermentation[J].LWT, 2022, 164:113629.