窖泥在浓香型白酒酿造过程中扮演着至关重要的角色。从风味形成的角度分析,窖泥中有机酸(己酸、丁酸和乙酸等)是白酒风味酯类物质的前体物质。从微生物学的角度分析,优质窖泥纲水平微生物主要以梭菌纲(Clostridia)、拟杆菌纲(Bacteroidia)、甲烷杆菌纲(Methanobacteria)和甲烷微菌纲(Methanomicrobia)为主[1],属水平微生物主要以己小杆菌属(Caproicibacterium)、产己酸菌属(Caproiciproducens)、岩石单胞菌属(Petrimonas)、氨基酸杆状菌属(Aminobacterium)、甲烷短杆菌属(Methanobrevibacter)和甲烷杆菌属(Methanobacterium)等为主[2-6]。窖泥功能微生物主要可以分为水解和产酸发酵菌群(如己小杆菌属、产己酸菌属等)、互营短中链脂肪酸降解菌群(如乙酸共养菌属、互营单胞菌属等)和产甲烷菌群(如甲烷短杆菌属、甲烷杆菌属等)[7]。窖泥微生物多样性随着窖龄增加而增加,不同老熟程度的窖泥中微生物菌群结构存在显著差异[4]。随着组学技术的发展,人们对窖泥微生物功能的了解愈发深入。YAN等[8]在探索细菌多样性与挥发性化合物间的相关性时发现梭菌属丰度与己酸、己酸乙酯、丁酸乙酯和己醇水平强相关,嗜硫石单胞菌(Petrimonas sulfuriphila)丰度与丙酸含量强相关;TAO等[4]研究窖泥微生物过程中发现,己酸菌属、岩石单胞菌属和己小杆菌属微生物在厌氧发酵下产生有机酸;CHEN等[9]在人工窖泥培养过程中发现,梭菌属和己酸菌属丰度的增加对应的是丁酸和己酸含量的增加;WANG等[6]发现,己小杆菌属广泛分布在窖泥中,其是主要的乳酸利用型产己酸微生物;LIU等[10]在人工窖泥批次发酵过程中发现,梭菌属丰度与己酸乙酯和丁酸乙酯含量呈正相关。这些研究表明,梭菌纲、拟杆菌纲的关键菌属在窖泥中的重要作用,并为优化人工窖泥培养和白酒酿造工艺提供了科学依据。
窖泥的老熟是一个漫长的过程,通常需要20年左右,优质老窖泥资源的不足制约着优质浓香型白酒的生产[4]。自1960年起,以提高白酒质量为目的的人工窖的培养与研究逐渐深入[11]。目前,人工窖泥的制备主要依赖于2类种子源:优质老窖泥与功能微生物菌液[12]。由于优质老窖泥资源有限,人工窖泥制备时采用的老窖泥比例一般在10%左右,同时会加入己酸菌等功能菌液进行强化[13]。研究显示新制备的人工窖泥与优质老窖泥的微生物结构存在巨大差异,如在人工窖泥中芽孢杆菌纲(Bacilli)和梭菌纲(且主要是梭菌属微生物)占主导地位,而产甲烷微生物的丰度非常低[10]。适度丰度的乳酸菌可以促进窖泥中有益微生物的驯化,而过量的乳酸菌会破坏窖泥的微生态平衡[14]。REN等[15]在对比新制备的人工窖泥和老熟窖泥的微生物水平差异的研究中发现,甲烷八叠球菌属、甲烷杆菌属、甲烷囊菌属、绳菌纲(Anaerolineae)和氨基酸杆状菌属是引起风味物质产生差异的主要微生物。鉴于目前新制备的人工窖泥与老熟窖泥菌群结构差异巨大,主要原因可能为:一是优质老窖泥使用量过少,不足以提供足够的优质菌群;二是厌氧菌受到氧气影响,从老窖泥接入的厌氧功能菌无法存活;三是人工窖泥制备时使用的培养条件(如碳源、氮源)无法支持窖泥厌氧功能微生物的生长。因生产规模实验难以进行严格的对照(如做到严格可控的无氧),生产规模固态发酵传质不够均匀,这些限制条件影响了为何老窖泥微生物群落接种入新制备人工窖泥后难以生长问题的准确探究。
微宇宙也称为模型生态系统,是一种通过人工构建的小型实验系统,用于模拟自然或受干扰的生态系统的动态变化、物质循环及化学物质迁移转化规律[16]。这种生态学模型可以是自然生态系统中的一部分,也可以在实验室内模拟。微宇宙模型构建广泛应用于土壤微生态、废水厌氧消化处理、肠道微生物群落构建等领域。ZHANG等[17]使用微宇宙模型成功地模拟了南极土壤中尿素处理导致的亚硝酸盐积累现象;ATAI等[18]使用微宇宙模型研究了盐渍土壤石油烃修复过程中生物改良剂对土壤微生物群落的影响;ZHANG等[19]利用微宇宙模型探究了钙镁磷肥料的添加对籽粒中砷和镉浓度的影响。白酒发酵前期存在大量淀粉、葡萄糖等糖类,碳源作为底物被产酸微生物利用,碳源类型(葡萄糖、乳酸)对微生物群落的结构和代谢至关重要。本研究采用微宇宙模型模拟人工窖泥发酵过程,能够避免大生产水平白酒发酵过程中的O2和传质不均匀2种因素影响对结果的准确判定,为人工窖泥制作工艺的优化提供理论支撑。
1 材料与方法
1.1 材料与试剂
黄水、生土与老窖泥,甘肃某浓香型企业白酒厂;叔戊酸,美国Sigma-Aldrich试剂公司;PowerSoil DNA提取试剂盒,Qiagen公司;其余常规化学试剂购自国药集团化学试剂有限公司。
1.2 仪器与设备
Agilent 7890B气相色谱仪、Agilent 1260高效液相色谱仪、CP-WAX 57 CB气相色谱柱,美国Agilent Technology 公司;Aminex HPX-87H有机酸柱,美国Bio-Rad公司;Forma 1029厌氧培养箱、Nano Drop 8000分光光度计,美国Thermo Fisher Scientific 公司;2.5 L厌氧罐,英国 Oxoid 公司;FE20 pH计,美国Mettler Toledo公司。
1.3 实验方法
1.3.1 固态发酵实验
本实验首先精确称量预定比例的老窖泥和生土。生土的添加量决定了所需黄水的体积,以确保新泥的含水量维持在35%(质量分数)左右。黄水在添加前需进行预处理,将黄水稀释2倍并调节pH至5.5以优化发酵条件。随后,使用搅拌器将老窖泥与新泥按不同的质量比进行混合,以确保均匀性。混合后,于厌氧工作站将混合物均匀分配至12个50 mL离心管,每个离心管装载等量的混合物。实验过程中,每10 d进行1次取样,每组设置3个平行样本以增强结果的可靠性。
固态发酵实验分为4组,顺序依次为老窖泥/新泥2∶2(碳源∶黄水)组、老窖泥/新泥1∶3(碳源∶黄水)组、老窖泥/新泥2∶2(碳源∶黄水+葡萄糖)组、老窖泥/新泥1∶3(碳源∶黄水+葡萄糖)组。
1.3.2 pH测定
称取6 g的泥基质于50 mL离心管中,加入30 mL的去离子水充分涡旋均匀,4 ℃离心后取上清液,0.22 μm滤膜过膜后使用pH计直接测定。
1.3.3 短中链脂肪酸含量测定
称取6 g的泥基质于50 mL离心管中,加入30 mL的去离子水充分涡旋均匀,4 ℃离心后取上清液,0.22 μm滤膜过膜后待用。取200 μL的上清液与50 μL的叔戊酸内标充分混合均匀后置于放有内衬管的气相小瓶中待检测。检测仪器是气相色谱仪,所用色谱柱型号为CP-WAX 57 CB,升温程序为:初始温度60 ℃,保持0.5 min,以20 ℃/min速率升温到180 ℃,保持5.5 min。进样口温度为220 ℃,分流比为5∶1,氢离子火焰检测器温度为220 ℃。
1.3.4 乳酸和葡萄糖含量测定
称取6 g的泥基质于50 mL离心管中,加入12 mL的去离子水充分涡旋均匀,4 ℃离心后取上清液,0.22 μm滤膜过膜后待用。取200 μL的上清液置于放有内衬管的液相小瓶中待检测。检测仪器是HPLC,所用色谱柱为Aminex HPX-87H色谱柱,使用5 mmol/L的H2SO4作为流动相,在60 ℃的柱温和0.5 mL/min的流速条件下,通过示差折光检测器进行检测。
1.3.5 DNA提取及扩增子测序
按照PowerSoil试剂盒所提供步骤提取窖泥微生物DNA,后用分光光度计检测DNA浓度,并通过琼脂糖凝胶电泳验证DNA的完整度。采用扩增子测序检测微生物丰度变化,检测区域为16S rRNA基因的V3~V4区域,扩增引物为341 modF(5′-CCTAYGGGRBGCASCAG-3′)和806 modR(5′-GGACTACHVGGGTWTCTAAT-3′),扩增子的测序和建库在上海凌恩生物科技有限公司Illumina NovaSeq PE250测序平台完成。
1.4 扩增子数据处理
测序完成后所得原始文件利用Trimmomatic[20]进行质控,去除低质量序列,后将过滤后序列导入Qiime2[21]。使用DADA2插件进行去噪、拼接及聚类得到扩增子序列变体(amplicon sequence variant,ASV),进一步以99%一致性进行聚类,得到代表ASV,物种注释使用NCBI Taxonomy数据库(https://www.ncbi.nlm.nih.gov/guide/taxonomy/)完成。
2 结果与分析
2.1 底物类型与老窖泥接种量对窖泥微生物的底物利用与主要代谢产物产生的影响
2.1.1 pH与葡萄糖及乳酸的变化规律
白酒发酵前期存在大量淀粉、葡萄糖等碳源,同时窖泥中分离纯化的纯菌株大多能利用葡萄糖[22-25]。在此基础上,本研究通过微宇宙模拟固态发酵分析在人工窖泥制作中营养物质(葡萄糖、乳酸)对窖泥微生物生长与代谢的影响。如图1所示,4组固态发酵中葡萄糖添加与否及老窖泥和新泥不同的接种比例未影响葡萄糖的代谢速率,发酵10 d时葡萄糖含量降为0。不添加葡萄糖的2组固态发酵中乳酸均在第10天被利用完,添加葡萄糖的2组固态发酵中乳酸利用型微生物代谢水平慢于不加葡萄糖组,添加葡萄糖的老窖泥/新泥2∶2组乳酸在20 d内被利用完,而老窖泥/新泥1∶3组前期出现乳酸净生成现象。结合以上分析,初步判断葡萄糖的添加延缓了乳酸的利用速率,更高生土/黄水比例促进了乳酸的净积累。
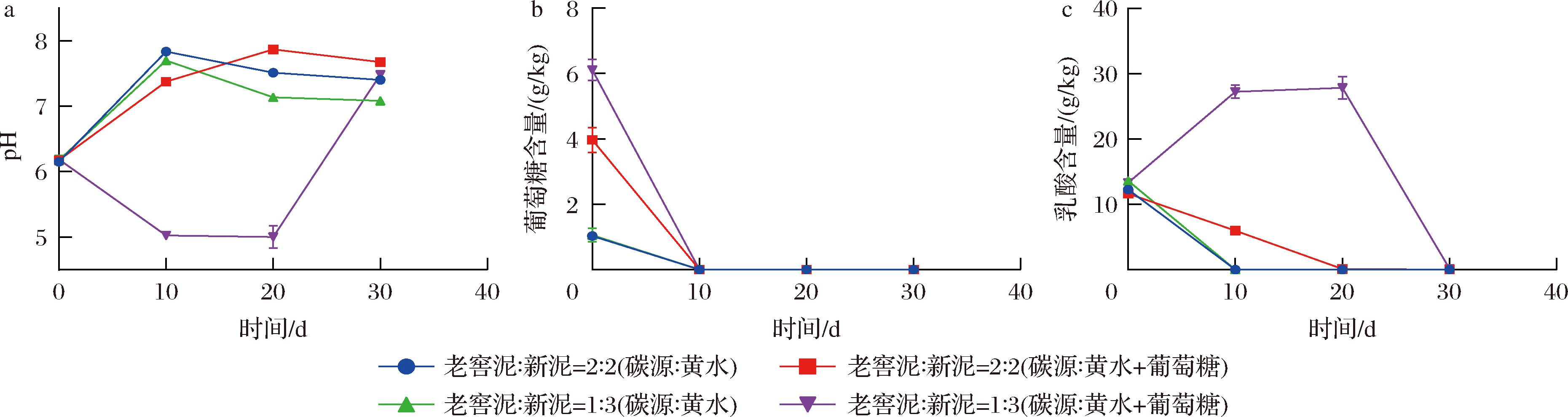
a-pH;b-葡萄糖;c-乳酸
图1 微宇宙固态发酵实验pH、葡萄糖和乳酸变化
Fig.1 pH, glucose, and lactate changes during the microcosm-solid-state fermentation system
窖泥微生物的生长代谢与pH变化息息相关。通过对比碳源含量与pH变化的趋势探索两者间的关联性。如表1所示,不添加葡萄糖的2组固态发酵中乳酸被利用发生在0~10 d且pH增幅最大;添加葡萄糖的老窖泥/新泥2∶2组乳酸被利用发生在0~20 d 且pH增加阶段在0~20 d,老窖泥/新泥1∶3组发酵前期乳酸积累且pH降低,发酵后期乳酸利用pH升高。乳酸被消耗则pH升高;乳酸生成则pH降低,碳源消耗完pH开始下降。研究表明,乳酸增加和pH下降2种现象有直接关系[5]。
表1 微宇宙固态发酵过程中葡萄糖、乳酸与pH的分阶段变化量
Table 1 Staged changes in glucose, lactate, and pH during microcosm solid-state fermentation processes
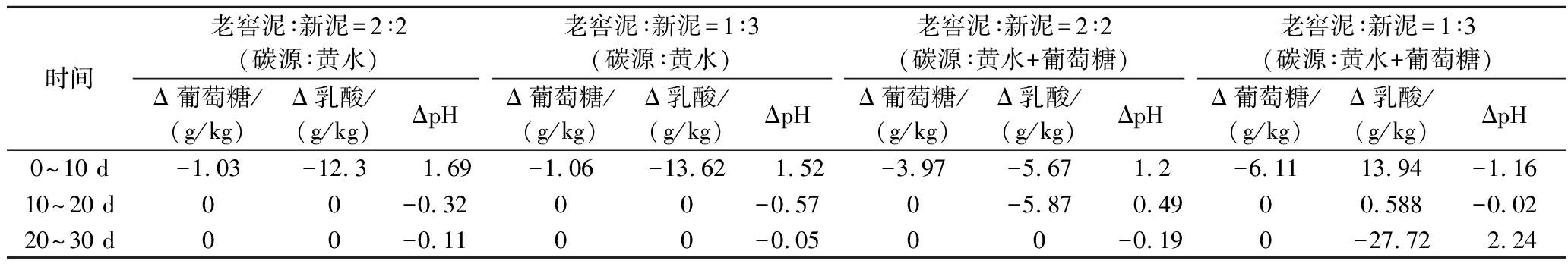
时间老窖泥∶新泥=2∶2(碳源∶黄水)老窖泥∶新泥=1∶3(碳源∶黄水)老窖泥∶新泥=2∶2(碳源∶黄水+葡萄糖)老窖泥∶新泥=1∶3(碳源∶黄水+葡萄糖)Δ葡萄糖/(g/kg)Δ乳酸/(g/kg)ΔpHΔ葡萄糖/(g/kg)Δ乳酸/(g/kg)ΔpHΔ葡萄糖/(g/kg)Δ乳酸/(g/kg)ΔpHΔ葡萄糖/(g/kg)Δ乳酸/(g/kg)ΔpH0~10 d-1.03-12.3 1.69-1.06-13.62 1.52-3.97-5.67 1.2-6.1113.94-1.1610~20 d00-0.3200-0.570-5.870.4900.588-0.0220~30 d00-0.1100-0.0500-0.190-27.722.24
注:乳酸和葡萄糖数值表示阶段发酵的净消耗量;pH数值表示阶段发酵的增加量。
2.1.2 主要挥发性短、中链脂肪酸的产生规律
由图2可知,无葡萄糖组偶数碳短、中链脂肪酸的表型变化趋势较为相似。为期30 d的发酵过程中乙酸和丁酸含量均升高,己酸含量先升高后降低。具体而言,老窖泥/新泥1∶3组的乙酸产量[(4.36±0.14) g/kg]高于老窖泥/新泥2∶2组[(2.92±0.96) g/kg];而老窖泥/新泥1∶3组的丁酸产量[(2.59±0.01) g/kg]低于老窖泥/新泥2∶2组[(4.15±0.43) g/kg]。己酸含量的增加主要发生在0~10 d,老窖泥/新泥1∶3组的己酸产量[(5.66±0.47) g/kg]高于老窖泥/新泥2∶2组[(4.85±0.22) g/kg]。
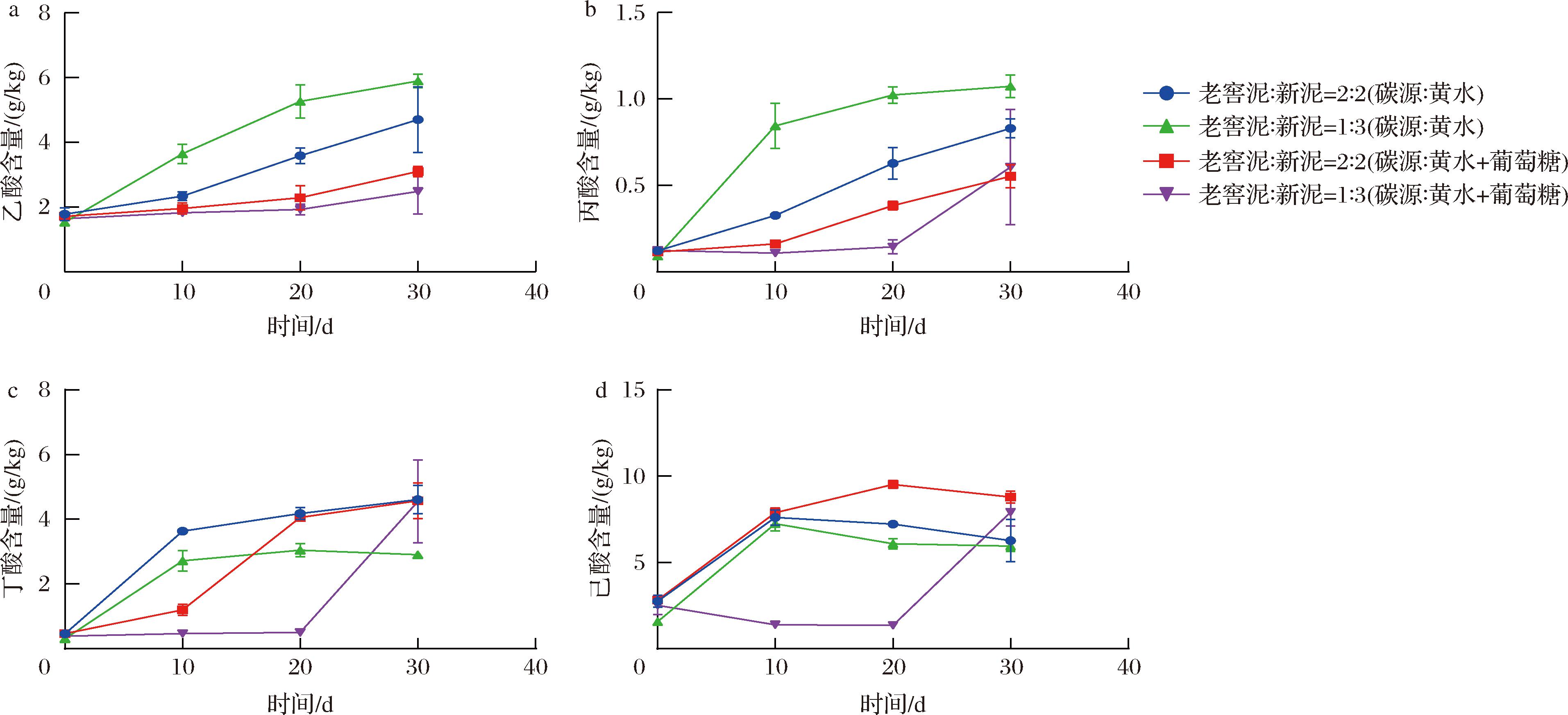
a-乙酸;b-丙酸;c-丁酸;d-己酸
图2 微宇宙固态发酵实验短、中链脂肪酸含量变化
Fig.2 Changes in concentration of short and medium chain fatty acids during the microcosm-solid-state fermentation system
添加葡萄糖组中乙酸的表型变化相近,乙酸含量均升高,其中在整个发酵过程中老窖泥/新泥2∶2组产量[(1.39±0.13) g/kg]高于老窖泥/新泥1∶3组[(0.84±0.71) g/kg]。添加葡萄糖的2组在发酵前、中期(0~20 d)丁酸和己酸的含量变化趋势不同,在老窖泥/新泥2∶2组含量变化呈现增加趋势[丁酸产量(3.59±0.09) g/kg,己酸产量(6.70±0.30) g/kg],而在老窖泥/新泥1∶3组含量未增加。老窖泥/新泥1∶3组在发酵前期主要是乳酸的生成,在发酵后期主要是短、中链脂肪酸的合成。研究表明,乳酸含量过高对细菌有毒害作用,从而影响微生物的正常代谢[26]。添加葡萄糖的2组固态发酵终点丁酸[(4.56±0.75) g/kg]和己酸产量(8.44±0.67) g/kg]相当。
丙酸是窖泥中常见的奇数碳短、中链脂肪酸,其在4组固态发酵中观察到含量增加的现象。葡萄糖添加的2组实验丙酸产量[(0.44±0.07)、(0.68±0.11) g/kg]低于无葡萄糖添加组[(0.71±0.04)、(0.98±0.07) g/kg],推测窖泥中存在利用乳酸产生丙酸的微生物。
单黄水固态发酵组在发酵第10天碳源利用完,己酸含量达到最高点,为7.24~7.61 g/kg。故以10 d为周期,计算短、中链脂肪酸的产率,比较葡萄糖添加与否的固态发酵中微生物代谢水平差异。添加葡萄糖组和不添加葡萄糖组的乙酸、丙酸和丁酸产率存在显著差异(表2)。具体表现为,添加葡萄糖组的乙酸、丙酸和丁酸产率低于不添加葡萄糖组。葡萄糖的添加影响窖泥微生物代谢水平,延缓混合泥基质中产乙酸、丙酸和丁酸微生物的代谢速率。
表2 微宇宙固态发酵前期短、中链脂肪酸产率(0~10 d) 单位:g/(kg·d)
Table 2 Yield of SCFAs at the early stage of the microcosm-solid-state fermentation system (0~10 d)
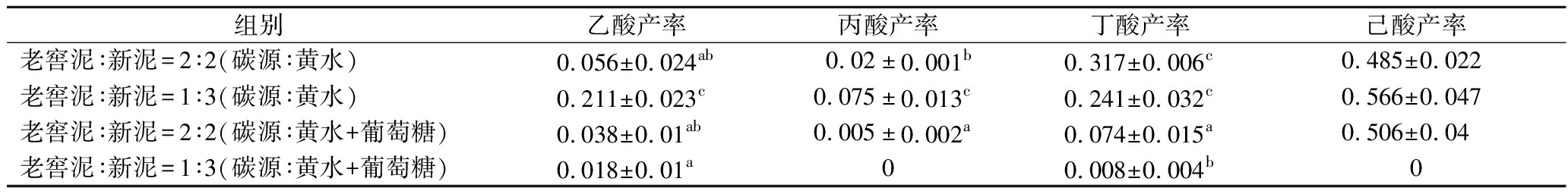
组别乙酸产率丙酸产率丁酸产率己酸产率老窖泥∶新泥=2∶2(碳源∶黄水)0.056±0.024ab0.02±0.001b0.317±0.006c0.485±0.022老窖泥∶新泥=1∶3(碳源∶黄水)0.211±0.023c0.075±0.013c0.241±0.032c0.566±0.047老窖泥∶新泥=2∶2(碳源∶黄水+葡萄糖)0.038±0.01ab0.005±0.002a0.074±0.015a0.506±0.04老窖泥∶新泥=1∶3(碳源∶黄水+葡萄糖)0.018±0.01a00.008±0.004b0
注:t-test分析组别之间的差异,字母不同表示组别之间存在显著差异(P<0.05)。
2.2 微宇宙固态发酵过程中细菌和古生菌的总体变化规律
针对不同碳源及不同老窖泥接种比例的4组发酵实验,涉及到的纲水平微生物主要有甲烷杆菌纲(Methanobacteria)、甲烷微菌纲(Methanomicrobia)、梭菌纲(Clostridia)、拟杆菌纲(Bacteroidia)、绳菌纲(Anaerolineae)、芽孢杆菌纲(Bacilli)、Tissierellia纲和互养菌纲(Synergistia)。其中甲烷杆菌纲、甲烷微菌纲、梭菌纲和拟杆菌纲微生物为老窖泥中的优势微生物[1],在发酵零时刻同样处于高丰度水平,其平均相对丰度分别是(20.12±5.20)%、(14.01±2.72)%、(31.47±3.54)%和(8.32±0.67)%。
如图3所示,为期30 d的发酵过程中,4组发酵在纲水平的相对丰度变化相似。其中甲烷杆菌纲相对丰度均呈现先升高后降低的趋势,其在发酵初时刻和末时刻相对丰度相近(20.12%~21.89%);梭菌纲在整个发酵过程中的平均相对丰度依次是(28.66±3.99)%、(29.97±2.99)%、(28.14±4.56)%和(28.51±6.05)%。梭菌纲微生物参与了乳酸、糖类、淀粉、乙醇的转化,是主要的风味物质产生微生物类群[27]。本研究的老窖泥接种比例表明,老窖泥与新泥的混合并未对梭菌纲微生物总体丰度造成过大的影响。甲烷微菌纲和拟杆菌纲相对丰度在发酵过程中整体均呈现降低趋势,甲烷微菌纲相对丰度变化依次是(11.32±0.61)%降到(5.78±0.23)%,(17.80±1.96)%降到(4.90±0.68)%,(14.09±0.36)%降到(5.52±0.10)%,(12.82±1.33)%降到(5.58±1.56)%;而甲烷杆菌纲作为主要的产甲烷菌[(21.64±5.69)%],其相对丰度在4组发酵中均未有大幅度的降低。拟杆菌纲相对丰度变化依次是从(8.57±0.49)%降到(0.39±0.14)%,从(7.84±0.83)%降到(0.40±0.002)%,从(8.40±0.89)%降到(0.37±0.10)%和从(8.47±0.48)%降到(1.45±1.16)%。这表明,新泥制作过程中,甲烷微菌纲与拟杆菌纲微生物生长相对较为困难,或相对丰度的降低仅仅是因为受到其他类型微生物的挤压。芽孢杆菌纲在发酵前期(0~10 d)相对丰度增加幅度最大,变化量依次为(24.41±4.16)%、(16.96±2.41)%、(23.66±2.48)%和(27.81±4.71)%。研究表明,在人工窖泥发酵初期同样出现芽孢杆菌纲微生物相对丰度过高的现象[10]。绳菌纲和互养菌纲相对丰度始终处于较低水平,其中互养菌纲微生物是一种典型的共生发酵微生物,该微生物可介导从乙酸降解为H2/CO2的过程,其功能不可忽略[28]。Tissierellia纲相对丰度在4组发酵过程中增加,依次变化为从(0.99±0.16)%升到(4.06±0.57)%,从(1.00±0.31)%升到(3.62±0.31)%,从(0.86±0.23)%升到(2.30±0.17)%和从(1.07±0.21)%升到(1.82±0.32)%。研究表明,Tissierellia纲微生物在厌氧消化中是主要产生挥发性脂肪酸的微生物[29]。
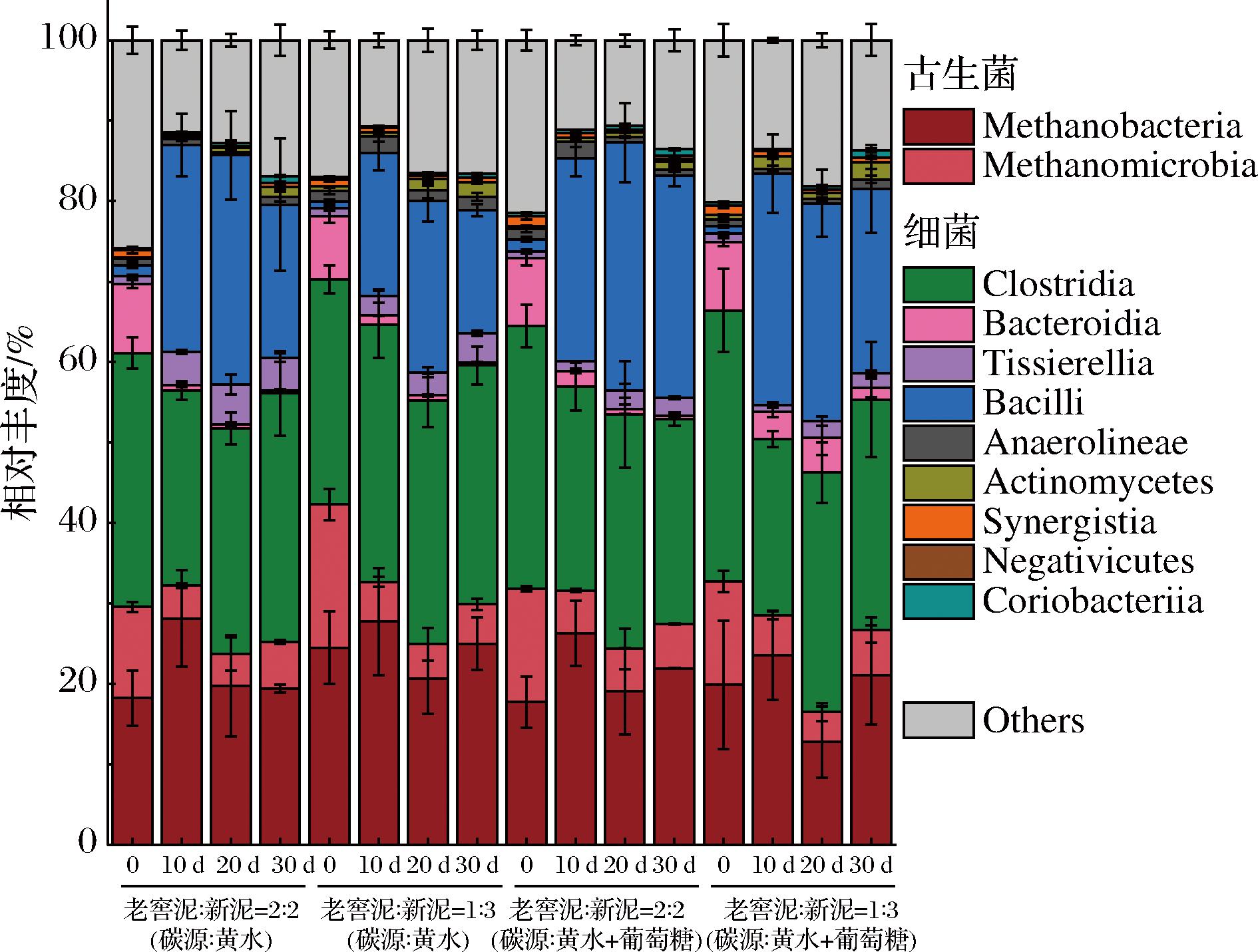
图3 微宇宙固态发酵过程中微生物在纲水平的动态变化
Fig.3 Dynamics of microbial community during the microcosm-solid-state fermentation system at class level
注:1%丰度以下的纲被合并为others。
2.3 微宇宙固态发酵过程中古生菌在属水平与种水平变化规律
如图4所示,4组固态模拟发酵过程中古菌在属水平的变化规律相似,推测在制作窖泥过程中窖泥接种比例和营养物质的不同对产甲烷微生物的生长影响较小。
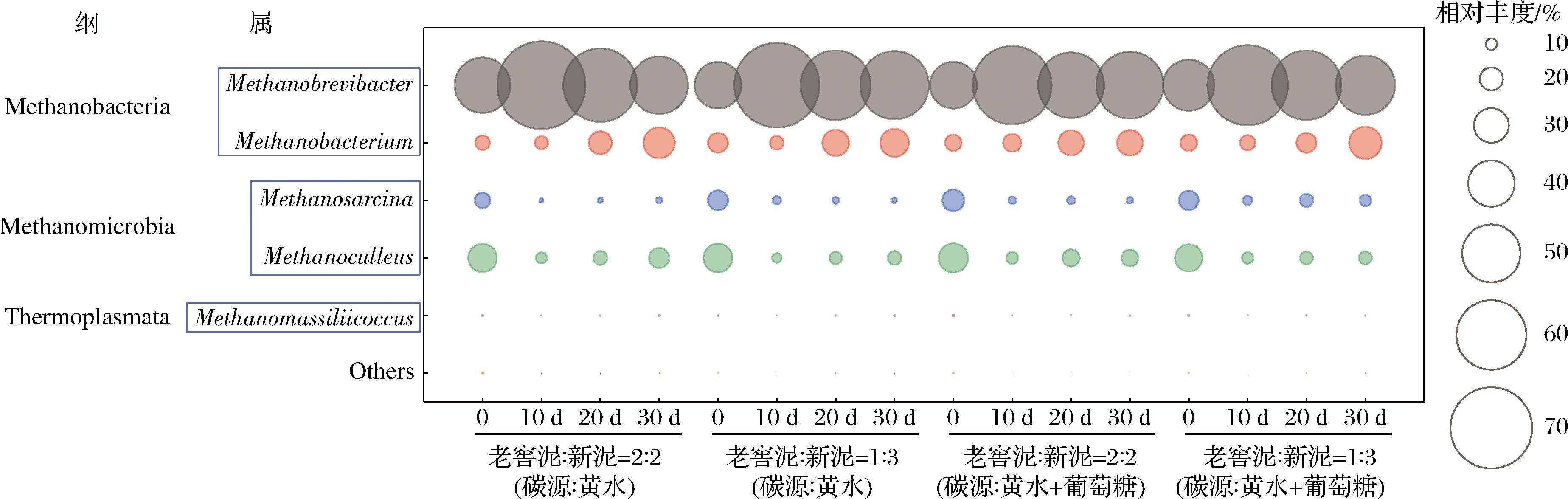
图4 微宇宙固态发酵过程中古生菌在属水平的动态变化
Fig.4 Dynamics of Archaea during the microcosm-solid-state fermentation system at genus level
注:1%丰度以下的属被合并为others(图6同)。
4组发酵甲烷短杆菌属(Methanobrevibacter)发酵初始相对丰度是(42.87±6.30)%,整个发酵过程该属所占比最高,该菌相对丰度变化趋势表现为先升高后降低。甲烷杆菌属(Methanobacterium)相对丰度在发酵前期变化幅度不大,在发酵中后期呈现升高趋势,其中刚果甲烷杆菌(Methanobacterium congolense)在发酵中后期的增加量依次为(1.63±0.59)%、(2.13±0.72)%、(0.94±0.36)%和(4.15±3.87)%(组别顺序见图4)(图5-a)。而甲烷囊菌属(Methanoculleus)相对丰度在4组发酵前期降低幅度明显,在发酵中后期呈现升高趋势,由于4组变化量接近,具体表现为布雷斯甲烷袋状菌(Methanoculleus bourgensis)和棕榈油甲烷袋状菌(Methanoculleus palmolei)的相对丰度发酵前期减少量分别为(8.52±1.98)%和(6.36±3.24)%;发酵中后期增加量分别为(1.95±1.12)%和(2.69±1.60)%(图5-b、图5-c)。甲烷八叠球菌属(Methanosarcina)相对丰度降低,变化趋势依次是从(13.31±2.54)%降到(5.36±0.32)%、从(17.03±3.28)%降到(4.54±0.32)%、从(18.62±2.50)%降到(5.57±0.28)%、从(16.80±7.63)%降到(9.81±3.80)%(组别顺序见图4)。
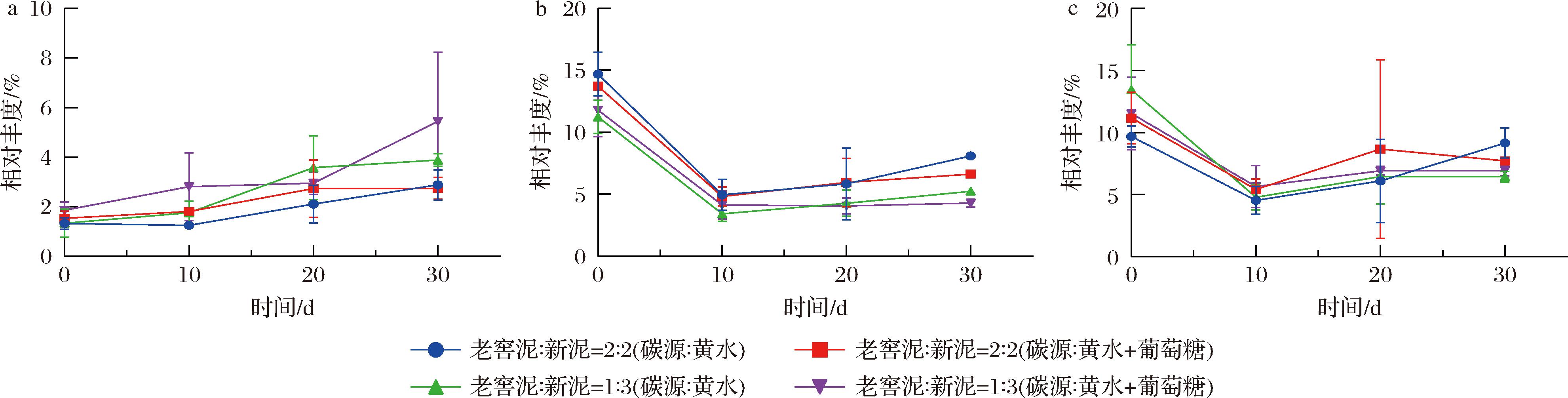
a-Methanobacterium congolense;b-Methanoculleus bourgensis;c-Methanoculleus palmolei
图5 微宇宙固态发酵过程中古生菌在种水平的动态变化
Fig.5 Dynamics of Archaea during the microcosm-solid-state fermentation system at species level
产甲烷微生物主要分为乙酸营养型和氢营养型,乙酸营养型产甲烷微生物主要以甲烷八叠球菌属为主(甲烷八叠球菌属同样也为氢营养型),完全氢营养型产甲烷微生物主要为甲烷囊菌属、甲烷短杆菌属和甲烷杆菌属,窖泥中的主要甲烷菌以氢营养型甲烷菌为主。基于发酵中后期老窖泥/新泥2∶2(碳源∶黄水)组、老窖泥/新泥1∶3(碳源∶黄水)组和老窖泥/新泥2∶2(碳源:黄水+葡萄糖)组已积累己酸和pH缓慢降低现象(图2),而乙酸和丁酸缓慢增加的趋势,且甲烷囊菌属和甲烷杆菌属相对丰度中后期增加,推测在乳酸和葡萄糖利用完后脂肪酸降解菌群正在进行链脂肪酸(己酸)的降解。
2.4 微宇宙固态发酵过程中细菌在属水平和种水平变化规律
生料黄水中含有多种营养物质,以黄水为营养源,混合生土和老窖泥的固态发酵中出现芽孢杆菌纲(Bacilli)大量生长的现象。如图6所示,在同等比例(2∶2)的老窖泥/新泥混合发酵中,相对丰度最高的芽孢杆菌是联合乳杆菌属(Ligilactobacillus),其中酸鱼联合乳杆菌(Ligilactobacillus acidipiscis)在第10天的相对丰度是35.26%~36.88%(图7-a),随着发酵时间的延长相对丰度有所降低。而随着新泥比例的增加(1∶3),2组发酵过程中酸鱼联合乳杆菌第10天的相对丰度[不添加葡萄糖组(16.36±1.34)%,添加葡萄糖组(2.49±0.92)%]低于老窖泥/新泥(2∶2)组。同时芽孢杆菌微生物生长出现差异,不添加葡萄糖组中魏斯氏菌属(Weissella)与添加葡萄糖组中片球菌属(Pediococcus)和乳杆菌属(Lactobacillus)相对丰度高于老窖泥/新泥(2∶2)组(图7-b~图7-d),与此相对应是副肠膜状魏斯氏菌(Weissella paramesenteroides)相对丰度最高可达(7.67±0.41)%,斯氏片球菌(Pediococcus stilesii)相对丰度最高可达(34.07±3.07)%,耐酸乳杆菌(Lactobacillus acetotolerans)相对丰度最高可达(2.51±0.26)%。推测生土或黄水本身所含的乳酸菌在制作窖泥中可以大量生长。
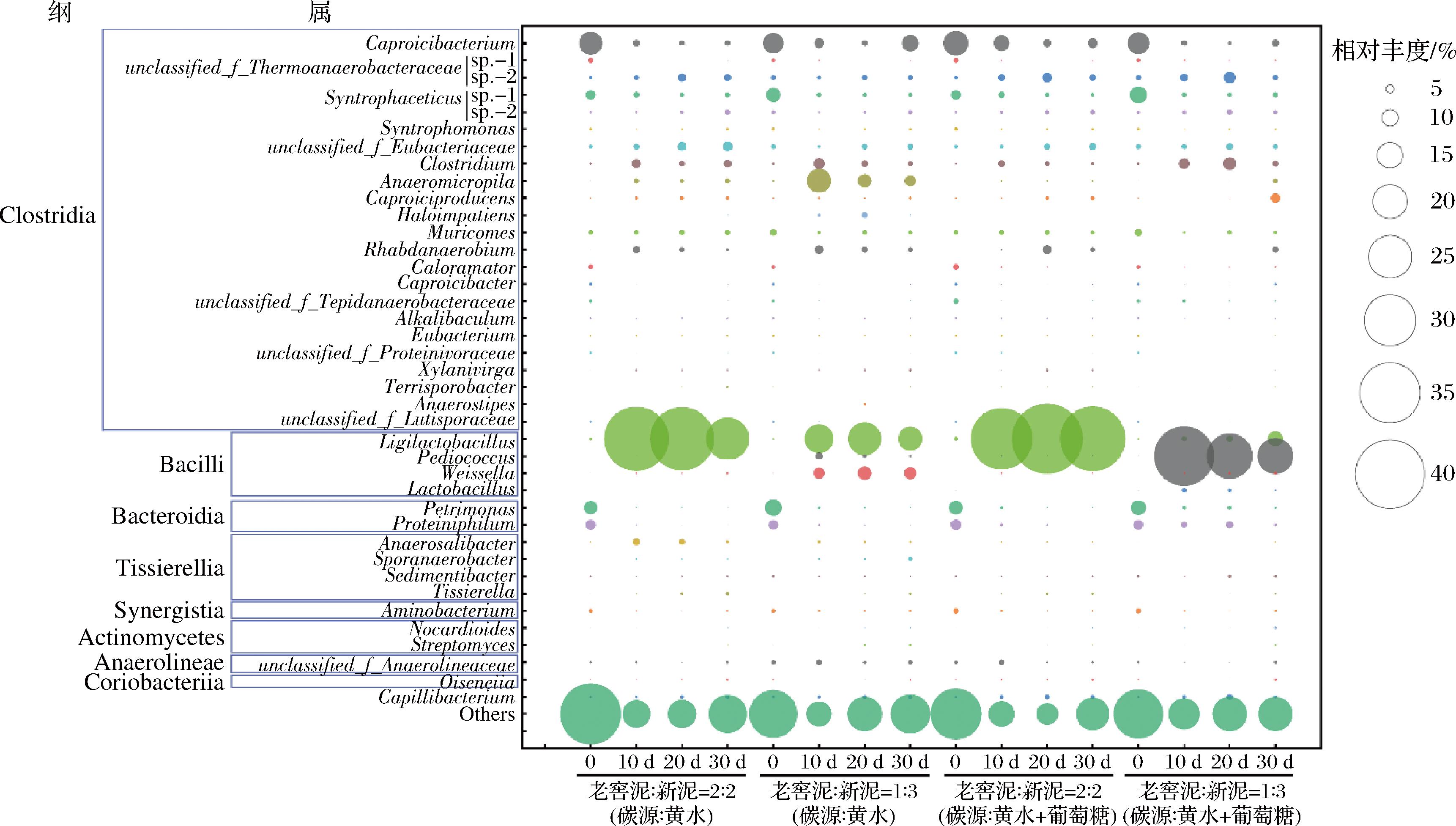
图6 微宇宙固态发酵过程中细菌在属水平的动态变化
Fig.6 Dynamics of bacteria during the microcosm-solid-state fermentation system at genus level

a-Ligilactobacillus acidipiscis;b-Weissella paramesenteroides;c-Pediococcus stilesii;d-Lactobacillus acetotolerans;e-Caproicibacterium lactatifermentans;f-Proteiniphilum propionicum;g-Petrimonas sulfuriphila;h-Clostridium cochlearium;i-Anaerosalibacter bizertensis;j-Clostridium liquoris;k-Anaeromicropila populeti;l-Sporanaerobacter acetigenes
图7 微宇宙固态发酵过程中细菌在种水平的动态变化
Fig.7 Dynamics of bacteria during the microcosm-solid-state fermentation system at species level
如图6所示,从水解和产酸发酵菌群切入,发酵零时刻己小杆菌属(Caproicibacterium)、乙酸共养菌属(Syntrophaceticus)、岩石单胞菌属(Petrimonas)和嗜蛋白菌属(Proteiniphilum)相对丰度分别为(12.74±2.12)%、(8.79±2.79)%、(8.29±1.04)%和(5.60±0.55)%。4组模拟发酵过程中己小杆菌属相对丰度先降低后升高的趋势,发酵前期(0~10 d)是变化最大阶段,减少量依次是(9.17±1.62)%、(6.10±2.31)%、(4.97±3.23)%和(9.23±1.77)%。解乳酸己小杆菌(Caproicibacterium lactatifermentans)是窖泥主体乳酸利用型产己酸微生物[6, 23],相对丰度发酵初期降低,在发酵后期相对丰度略增加(图7-e)。虽然解乳酸己小杆菌的相对丰度在前中期有较大幅度的降低,但仍然在中后期检测到相当量的己酸生成(图2),表明解乳酸己小杆菌的定殖与生长较为缓慢,但仍然可以进行有效定殖。
在4组模拟发酵过程中岩石单胞菌属和嗜蛋白菌属相对丰度均降低,岩石单胞菌属相对丰度变化依次为从(7.57±0.44)%降到(0.38±0.11)%、从(9.46±1.21)%降到(0.44±0.07)%、从(7.81±0.88)%降到(0.36±0.13)%、从(8.33±0.61)%降到(0.62±0.01)%;嗜蛋白菌属相对丰度变化依次为从(5.66±0.71)%降到(0.33±0.22)%、从(5.37±0.55)%降到(0.39±0.06)%、从(5.83±0.44)%降到(0.27±0.05)%、从(5.54±0.70)%降到(1.34±1.12)%(组别顺序见图6)。主要物种嗜硫石单胞菌(Petrimonas sulfuriphila)和嗜蛋白拟杆菌(Proteiniphilum propionicum)的代谢产物为乙酸和丙酸[24, 30]。不加葡萄糖组的匙形梭菌(Clostridium cochlearium)、Anaeromicropila populeti、比塞大厌氧耐盐杆菌(Anaerosalibacter bizertensis)和产乙酸成孢厌氧杆菌(Sporanaerobacter acetigenes)相对丰度高于添加葡萄糖组(图7-h、图7-i、图7-k、图7-l)。匙形梭菌的主要代谢产物是乙酸、丙酸和丁酸[31],Anaeromicropila populeti利用多种底物产乙酸、丁酸[32],比塞大厌氧耐盐杆菌可利用多种底物产乙酸、丙酸和丁酸[33],产乙酸成孢厌氧杆菌可利用多种底物产乙酸[34]。以上主要物种的变化解释了不加葡萄糖组的乙酸和丙酸含量高于添加葡萄糖组的原因。白酒梭菌(Clostridium liquoris)能够利用多种碳源产丁酸[25],解释了在老窖泥/新泥2∶2(碳源∶黄水+葡萄糖)组发酵中后期丁酸含量增加的现象(图7-j)。
从互营短、中链脂肪酸降解菌群切入,互营单胞菌属和乙酸共养菌属是窖泥主要互营脂肪酸降解菌群。互营单胞菌属微生物将己酸降解成乙酸,后被乙酸营养型的产甲烷微生物将乙酸降解为甲烷。乙酸共养菌属微生物能够将乙酸降解为CO2或H2,后被氢营养型的产甲烷微生物转化成甲烷。在老窖泥/新泥2∶2(碳源∶黄水)组、老窖泥/新泥1∶3(碳源∶黄水)组与老窖泥/新泥2∶2(碳源∶黄水+葡萄糖)组中互营单胞菌属和乙酸共养菌属(Syntrophaceticus sp.-2)发酵中后期相对丰度增加,其中互营单胞菌属的相对丰度变化趋势依次为从(0.57±0.08)%升到(1.62±0.19)%、从(0.56±0.10)%升到(1.43±0.21)%和从(0.89±0.07)%升到(1.45±0.06)%;乙酸共养菌属的相对丰度变化趋势依次为从(1.36±0.29)%升到(3.01±0.71)%、从(1.20±0.26)%升到(2.29±0.40)%和从(1.81±0.54)%升到(2.46±0.41)%。氢营养型产甲烷微生物甲烷囊菌属和甲烷杆菌属中后期相对丰度增加,可将乙酸共养菌属代谢所得的CO2/H2转化成甲烷,该现象主要体现在发酵中后期。而老窖泥/新泥1∶3(碳源:黄水+葡萄糖)组发酵20~30 d期间互营单胞菌属和乙酸共养菌属的相对丰度却在降低[从(1.21±0.36)%降到(0.95±0.36)%、从(2.92±1.99)%降到(2.08±0.78)%],表明葡萄糖的添加对2类微生物的生长具有负面作用。然而,乙酸共养菌属(Syntrophaceticus-1)在4组发酵过程中相对丰度降低明显,变化趋势分别为从(5.43±2.06)%降到(2.70±0.83)%、从(8.00±2.19)%降到(2.07±0.41)%、从(5.40±1.58)%降到(2.02±0.24)%和从(9.56±2.21)%降到(2.86±1.10)%,推测该微生物的变化是乙酸未出现降低趋势的原因之一。
此外,在老窖泥/新泥2∶2(碳源∶黄水)组、老窖泥/新泥2∶2(碳源∶黄水+葡萄糖)组与老窖泥/新泥1∶3(碳源∶黄水+葡萄糖)组发酵前中期热厌氧杆状菌科(unclassified_f_Thermoanaerobacteraceae sp.-2)的相对丰度均增加,变化趋势分别是从(1.70±0.24)%升到(4.52±0.96)%、从(2.03±0.35)%升到(5.47±2.01)%和从(2.84±0.36)%升到(6.72±3.11)%,在老窖泥/新泥1∶3(碳源∶黄水)组该菌的相对丰度始终保持在(2.67±0.49)%。有文献报道,热厌氧杆状菌科可参与互营代谢过程[35]。
3 结论与讨论
本研究模拟传统泥接泥的人工窖泥培养方式,通过调节不同老窖泥的接种比例及不同碳源的培养条件,探索其中微生物代谢水平和丰度变化。不同比例的老窖泥/新泥发酵实验均可观察到短、中链脂肪酸的生成,其中己酸含量最高可达(9.52±0.23) g/kg。额外葡萄糖的添加减缓短、中链脂肪酸的生成速率。新窖泥制作过程中容易产生乳酸,抑制其他己酸菌等功能微生物的生长。主体己酸菌虽然相对丰度大幅度降低,但仍然可以将乳酸转化为己酸。在老窖泥使用比例减少时,葡萄糖的额外添加会导致更多乳酸菌的生长与乳酸的产生,对己酸菌的生长产生严重抑制。短、中链脂肪酸降解关键微生物主要物种难以在窖泥中定殖与发挥短、中链脂肪酸降解作用,表明该类型菌的有效定殖与代谢是维持窖泥微生态系统稳定的关键因素。本研究通过微宇宙系统的实验室模拟固态发酵探索,表明优质老窖泥微生物的定殖受到微生物相互作用关系的影响,特别是乳酸菌的过量繁殖对窖泥微生物群落构建具有较大的负面影响。在此基础上,有针对性地优化人工窖泥制作工艺,将有望推动新型窖泥微生物应用技术的落地与应用。
[1] HU X L, DU H, REN C, et al.Illuminating anaerobic microbial community and cooccurrence patterns across a quality gradient in Chinese liquor fermentation pit muds[J].Applied and Environmental Microbiology, 2016, 82(8):2506-2515.
[2] 任海伟, 孙一帆, 王希, 等.不同窖龄及位置浓香型白酒窖泥中细菌群落结构的差异性分析[J].食品与发酵工业, 2023, 49(9):103-111.
REN H W, SUN Y F, WANG X, et al.Difference analysis of bacterial community structure in pit mud with different ages and position[J].Food and Fermentation Industries, 2023, 49(9):103-111.
[3] FANG S, WANG C X, YAN J.Comparing the differences of prokaryotic microbial community between pit walls and bottom from Chinese liquor revealed by 16S rRNA gene sequencing[J].Open Life Sciences, 2023, 18(1):20220571.
[4] TAO Y, LI J B, RUI J P, et al.Prokaryotic communities in pit mud from different-aged cellars used for the production of Chinese strong-flavored liquor[J].Applied and Environmental Microbiology, 2014, 80(7):2254-2260.
[5] ZHANG H M, MENG Y J, WANG Y L, et al.Prokaryotic communities in multidimensional bottom-pit-mud from old and young pits used for the production of Chinese Strong-Flavor Baijiu[J].Food Chemistry, 2020, 312:126084.
[6] WANG H L, GU Y, ZHOU W C, et al.Adaptability of a caproate-producing bacterium contributes to its dominance in an anaerobic fermentation system[J].Applied and Environmental Microbiology, 2021, 87(20):e0120321.
[7] 任聪, 杜海, 徐岩.中国传统发酵食品微生物组研究进展[J].微生物学报, 2017, 57(6):885-898.
REN C, DU H, XU Y.Advances in microbiome study of traditional Chinese fermented foods[J].Acta Microbiologica Sinica, 2017, 57(6):885-898.
[8] YAN S B, JIA Y L, ZHANG Q, et al.Bacterial diversity associated with volatile compound accumulation in pit mud of Chinese strong-flavor Baijiu pit[J].AMB Express, 2023, 13(1):3.
[9] CHEN S Q, HUANG J, QIN H, et al.Evolving the core microbial community in pit mud based on bioturbation of fortified Daqu[J].Canadian Journal of Microbiology, 2021, 67(5):396-405.
[10] LIU M K, TANG Y M, GUO X J, et al.Structural and functional changes in prokaryotic communities in artificial pit mud during Chinese Baijiu production[J].mSystems, 2020, 5(2).DOI:10.1128/mSystems.00829-19.
[11] DING X F, WU C D, HUANG J, et al.Eubacterial and archaeal community characteristics in the man-made pit mud revealed by combined PCR-DGGE and FISH analyses[J].Food Research International, 2014, 62:1047-1053.
[12] 张学英, 章发盛.人工窖泥的培养及应用[J].酿酒, 2011, 38(2):69-71.
ZHANG X Y, ZHANG F S.Culture and application of man-made cellar mud[J].Liquor Making, 2011, 38(2):69-71.
[13] 靳喜庆, 冯亮, 张无疾, 等.白酒人工窖泥培养方法研究进展[J].中国酿造, 2024, 43(7):7-13.
JIN X Q, FENG L, ZHANG W J, et al.Research progress on cultivation methods of artificial pit mud of Baijiu[J].China Brewing, 2024, 43(7):7-13.
[14] ZHAO Q S, YANG J G, ZHANG K Z, et al.Lactic acid bacteria in the brewing of traditional Daqu liquor[J].Journal of the Institute of Brewing, 2020, 126(1):14-23.
[15] REN D L, LIU S P, QIN H, et al.Metagenomics-based insights into the microbial community dynamics and flavor development potentiality of artificial and natural pit mud[J].Food Microbiology, 2025, 125:104646.
[16] CAO Z H, LI P, LI Z H.A latest review on the application of microcosm model in environmental research[J].Environmental Science and Pollution Research, 2021, 28(43):60438-60447.
[17] ZHANG E, WILKINS D, CRANE S, et al.Urea amendment decouples nitrification in hydrocarbon contaminated Antarctic soil[J].Chemosphere, 2024, 354:141665.
[18] ATAI E, JUMBO R B, COWLEY T, et al.Efficacy of bioadmendments in reducing the influence of salinity on the bioremediation of oil-contaminated soil[J].Science of the Total Environment, 2023, 892:164720.
[19] ZHANG T, ABU SAYEM JIKU M, LI L Y, et al.Soil ridging combined with biochar or calcium-magnesium-phosphorus fertilizer application:Enhanced interaction with Ca, Fe and Mn in new soil habitat reduces uptake of as and Cd in rice[J].Environmental Pollution, 2023, 332:121968.
[20] BOLGER A M, LOHSE M, USADEL B.Trimmomatic:A flexible trimmer for Illumina sequence data[J].Bioinformatics, 2014, 30(15):2114-2120.
[21] BOLYEN E, RIDEOUT J R, DILLON M R, et al.Reproducible, interactive, scalable and extensible microbiome data science using QIIME 2[J].Nature Biotechnology, 2019, 37(8):852-857.
[22] GU Y, ZHU X J, LIN F, et al.Caproicibacterium amylolyticum gen.nov., sp.nov., a novel member of the family Oscillospiraceae isolated from pit clay used for making Chinese strong aroma-type liquor[J].International Journal of Systematic and Evolutionary Microbiology, 2021, 71(4).DOI:10.1099/ijsem.0.004789.
[23] WANG H L, GU Y, ZHAO D, et al.Caproicibacterium lactatifermentans sp.nov., isolated from pit clay used for the production of Chinese strong aroma-type liquor[J].International Journal of Systematic and Evolutionary Microbiology, 2022, 72(1).DOI:10.1099/ijsem.0.005206.
[24] 郑慧珍, 王慧琳, 高江婧, 等.窖泥优势拟杆菌纲微生物Petrimonas sulfuriphila的分离及其功能解析[J].微生物学报, 2022, 62(9):3373-3386.
ZHENG H Z, WANG H L, GAO J J, et al.Isolation and functional analysis of the dominant Bacteroidia species Petrimonas sulfuriphila in pit mud[J].Acta Microbiologica Sinica, 2022, 62(9):3373-3386.
[25] YIN Q, TAO Y, ZHU X Y, et al.Clostridium liquoris sp.nov., isolated from a fermentation pit used for the production of Chinese strong-flavoured liquor[J].International Journal of Systematic and Evolutionary Microbiology, 2016, 66(2):749-754.
[26] JIANG B, LIU J Z, WANG J N, et al.Adaptive evolution for the efficient production of high-quality D-lactic acid using engineered Klebsiella pneumoniae[J].Microorganisms, 2024, 12(6):1167.
[27] FANG G Y, CHAI L J, ZHONG X Z, et al.Comparative genomics unveils the habitat adaptation and metabolic profiles of Clostridium in an artificial ecosystem for liquor production[J].mSystems, 2022, 7(3):e0029722.
[28] MENG X H, CAO Q, SUN Y, et al.16S rRNA genes- and metagenome-based confirmation of syntrophic butyrate-oxidizing methanogenesis enriched in high butyrate loading[J].Bioresource Technology, 2022, 345:126483.
[29] SUN Y J, SUN Y J, REN X Q, et al.Enhancement of volatile fatty acids to extremely high content in fermentation of food waste:Optimization of conditions, microbial functional genes, and mechanisms[J].Bioresource Technology, 2025, 416:131735.
[30] LIU Q J, ZHENG H Z, WANG H L, et al.Proteiniphilum propionicum sp.nov., a novel member of the Phylum Bacteroidota isolated from pit clay used to produce Chinese liquor[J].International Journal of Systematic and Evolutionary Microbiology, 2022, 72(11).DOI:10.1099/ijsem.0.005612.
[31] CIBIS K G, GNEIPEL A, KÖNIG H.Isolation of acetic, propionic and butyric acid-forming bacteria from biogas plants[J].Journal of Biotechnology, 2016, 220:51-63.
[32] UEKI A, TONOUCHI A, KAKU N, et al.Anaeromicropila herbilytica gen.nov., sp.nov., a plant polysaccharide-decomposing anaerobic bacterium isolated from anoxic soil subjected to reductive soil disinfestation, and reclassification of Clostridium populeti as Anaeromicropila populeti comb.nov[J].International Journal of Systematic and Evolutionary Microbiology, 2023, 73(1).DOI:10.1099/ijsem.0.005695.
[33] REZGUI R, MAAROUFI A, FARDEAU M L, et al.Anaerosalibacter bizertensis gen.nov., sp.nov., a halotolerant bacterium isolated from sludge[J].International Journal of Systematic and Evolutionary Microbiology, 2012, 62(Pt 10):2469-2474.
[34] HERNANDEZ-EUGENIO G, FARDEAU M L, CAYOL J L, et al.Sporanaerobacter acetigenes gen.nov., sp.nov., a novel acetogenic, facultatively sulfur-reducing bacterium[J].International Journal of Systematic and Evolutionary Microbiology, 2002, 52(Pt 4):1217-1223.
[35] ZHANG Y, LI C X, YUAN Z W, et al.Syntrophy mechanism, microbial population, and process optimization for volatile fatty acids metabolism in anaerobic digestion[J].Chemical Engineering Journal, 2023, 452:139137.