啤酒是全球最受欢迎的酒精饮料之一,近年来在我国得到了迅速发展。啤酒酵母(Saccharomyces cerevisiae)是啤酒酿造过程中不可或缺的微生物,具备独特的发酵特性和风味生成能力,是啤酒酿造中专用的菌株,对啤酒的品质及风味特征起着至关重要的作用[1]。然而,依赖单一啤酒酵母的酿造方式在一定程度上限制了啤酒风味的多样性,导致产品同质化,难以满足消费者对个性化和创新性的需求。
近年来,随着消费者对独特风味啤酒的渴求不断增长,非酿酒酵母(non-Saccharomyces)在啤酒酿造领域受到广泛关注。非酿酒酵母指除酿酒酵母属(Saccharomyces)以外的其他酵母菌种,由于其发酵性能和酒精耐受性相对较弱,且部分非酿酒酵母在代谢过程中会产生H2S、乙醛等对啤酒风味不利的化合物,传统观念认为它们并不适用于啤酒酿造。然而,随着现代研究的不断深入,人们对非酿酒酵母的认识发生了重大转变。研究发现,某些非酿酒酵母能够显著改变啤酒中风味物质的组成与含量,从而优化啤酒的口感,丰富其风味多样性,并为啤酒赋予独特的地域特色[2-3]。这一发现为啤酒酿造带来了新的思路和可能性,也为啤酒风味的创新开辟了广阔的空间。
非酿酒酵母通常具有丰富的代谢能力,能够产生多样化的风味物质,这些特性使其在啤酒增香酿造领域具有独特优势。此外,部分非酿酒酵母还能在酿造过程中产生β-葡萄糖苷酶、β-葡聚糖酶、蛋白酶等一系列生物酶,这些生物酶类在酿造过程中发挥着重要作用。其中β-葡萄糖苷酶通过酶促水解糖苷键后释放挥发性香气成分[4],蛋白酶通过将蛋白质降解为氨基酸,为合成挥发性化合物提供重要的前体物,β-葡聚糖酶则可以将β-葡聚糖降解,释放蛋白质和糖类化合物,进而产生风味物质[5]。CANONICO等[6]研究了异常威克汉姆酵母纯种发酵和混合发酵时对啤酒的影响,发现啤酒酵母与异常威克汉姆酵母混合发酵时会使啤酒中的乙醛减少,乙酸乙酯增加。HAN等[7]研究了4株非酿酒酵母在啤酒发酵中的潜力,发现光滑假丝酵母菌株纯种发酵和混合发酵的麦汁中香叶醇含量分别增加了51.5倍和11倍,且混合发酵麦汁中里那醇含量增加了1.36倍,最终啤酒产品中的酒花香气显著增强。KING等[8]研究发现,德尔布有孢圆酵母和乳酸克鲁维酵母能将橙花醇和香叶醇转化为里那醇,还能将橙花醇和里那醇转化为萜品醇。因此,非酿酒酵母和啤酒酵母混合酿造在啤酒领域的应用将有效推动啤酒风味朝着多样化和个性化方向发展,实现啤酒品质创新升级[9]。
然而,在啤酒生产中,非酿酒酵母的酿造性能受到酒精度、pH值、渗透压(糖浓度)[10]等多种外部环境因素的共同作用,使其在混合酵母发酵中难以充分表达品质,增香效果受限。因此,需要全面评估非酿酒酵母的酿造特性,筛选出适合啤酒酿造环境的优选菌株,推动啤酒混合酵母酿造技术的升级。本研究以实验室保藏的14株非酿酒酵母为出发菌株,以麦汁为培养基,从环境耐受性、产酶特性[11]和风味特性[12]方面开展研究,旨在筛选出具有显著特色风味的非酿酒酵母菌株,为啤酒品质提升提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
本实验所采用的非酿酒酵母菌种来自中国食品发酵工业研究院(表1),对菌种进行了单独编号N1~N14,对照菌株-拉格啤酒酵母W-34/70来自于弗曼迪斯酵母有限公司。
表1 实验菌种信息
Table 1 Information of experimental strains

编号菌种名称菌种拉丁文菌种来源N1葡萄汁有孢汉逊酵母Hanseniaspora uvarum中国食品发酵工业研究院N2葡萄汁有孢汉逊酵母H.uvarum中国食品发酵工业研究院N3葡萄汁有孢汉逊酵母H.uvarum中国食品发酵工业研究院N4葡萄汁有孢汉逊酵母H.uvarum中国食品发酵工业研究院N5葡萄汁有孢汉逊酵母H.uvarum中国食品发酵工业研究院N6异常威克汉姆酵母Wickerhamomyces anomalus中国食品发酵工业研究院N7库德里阿兹威毕赤酵母Pichia kudriavzevii中国食品发酵工业研究院N8库德里阿兹威毕赤酵母P.kudriavzevii中国食品发酵工业研究院N9发酵毕赤酵母Pichia fermentans中国食品发酵工业研究院N10马克斯克鲁维酵母Kluyveromyces marxianus中国食品发酵工业研究院N11乳酸克鲁维酵母Kluyveromyces lactis中国食品发酵工业研究院N12异常威克汉姆酵母W.anomalus中国食品发酵工业研究院N13异常威克汉姆酵母W.anomalus中国食品发酵工业研究院
续表1

编号菌种名称菌种拉丁文菌种来源N14白地霉Geotrichum candidum中国食品发酵工业研究院W-34/70啤酒酵母S.cerevisiae弗曼迪斯酿酒酵母有限公司
1.1.2 主要试剂
NaCl,天津大茂化学试剂厂;柠檬酸铁,西陇化工股份有限公司;NH4NO3、KH2PO4、MgSO4,北京化工厂;CaCl2,浙江兰溪城南化工厂;刚果红,广东省汕头市西陇化工厂;NaCl、无水乙醇、葡萄糖,北京博奥拓科技有限公司;盐酸,天津市恒移化工原料有限公司;七叶苷,国药集团化学试剂有限公司;对硝基苯酚,北京鼎国昌盛生物技术有限责任公司;β-葡聚糖;上海阿拉丁生化科技股份有限公司;亮氨酸,北京百灵威科技有限公司。以上实际均为分析纯。
1.1.3 培养基
YPD液体培养基(g/L):酵母浸粉10.0、葡萄糖20.0、蛋白胨20.0,115 ℃灭菌20 min。
麦汁培养基:取自产12 °P麦汁,115 ℃灭菌20 min备用,详细制备方法见1.3.1节麦汁的制备。
β-葡萄糖苷酶鉴定培养基(g/L):蛋白胨10.0、酵母粉3.0、NaCl 3.0、七叶苷1.0、柠檬酸铁0.5、琼脂粉20.0,pH 7.0,121 ℃下灭菌20 min。
β-葡聚糖酶鉴定培养基(g/L):大麦β-葡聚糖1.0、酵母浸粉5.0、刚果红0.10、蛋白胨5.0、琼脂粉20.0,pH 7.0,121 ℃下灭菌20 min。
蛋白酶鉴定培养基(g/L):干酪素5.0、牛肉膏3.0、蛋白胨 10.0、NaCl 10.0、琼脂粉20.0,pH 7.0,121 ℃下灭菌20 min。
1.2 仪器与设备
LRH-250生化培养箱,上海一恒科技有限公司;EBC标准麦芽粉碎机,德国Bauknecht公司;JJ1000电子天平,常熟市双杰测试仪器厂;QXT-1糖化仪,中国原子能科学研究院;YXQ-50G立式灭菌锅,上海博迅生物仪器股份有限公司;移液枪,德国Eppendorf公司;Clarus 680型GC-MS,美国安捷伦公司;Anton Paar啤酒分析仪,奥地利安东帕公司。
1.3 实验方法
1.3.1 麦汁及发酵液制备
麦汁制备方法参考刘皓等[1]的方法。
以制备的12 °P麦汁为培养基,分别取200 mL装入500 mL三角瓶,115 ℃灭菌20 min,冷却至10 ℃,分别接入非酿酒酵母和拉格啤酒酵母W-34/70,酵母浓度为1×107 CFU/mL,10 ℃培养,至质量恒定<0.2 g时发酵结束,制备成发酵液,放入4 ℃冰箱保存7 d后检测。
以制备的12 °P麦汁为培养基,分别取200 mL装入500 mL三角瓶,115 ℃灭菌20 min,冷却至10 ℃,同时接入非酿酒酵母和拉格啤酒酵母W-34/70,接种比例1∶10,接种酵母浓度分别为1×107、1×106 CFU/mL,10 ℃培养,至质量恒定<0.2 g时发酵结束,制备成混合发酵啤酒,放入4 ℃冰箱保存7 d后检测相关指标和感官品评。
1.3.2 菌株形态鉴定
用接种环挑取斜面非酿酒酵母菌种,分别在麦汁培养基上划线培养,在28 ℃条件下培养2 d,挑选单菌落进行形态观察。
1.3.3 菌株产酶特性的测定
1.3.3.1 菌株产β-葡萄糖苷酶的特性评价
七叶苷被β-葡萄糖苷酶水解后产生的七叶苷元可与Fe3+发生反应,而使得菌落周围培养基颜色变深。参考孔晓双等[13]的方法。β-葡萄糖苷酶粗酶液制备方法及活性测定参考付跃等[14]的方法。
1.3.3.2 菌株产β-葡聚糖酶的特性评价
β-葡聚糖酶的鉴定方法参照杨春林等[15]的方法,β-葡聚糖酶粗酶液制备方法及β-葡聚糖酶活性测定参考吕小虎等[16]的方法。
1.3.3.3 菌株产蛋白酶的特性评价
蛋白酶的鉴定及蛋白酶粗酶液制备方法参考胡连清等[17]的方法;蛋白酶活力的测定参照SB/T 10317—1999《蛋白酶活力测定法》。
1.3.4 菌株耐受性的测定
糖耐受性及pH耐受性的测定方法参考刘晓柱等[18]的方法;乙醇耐受性的测定参考熊荣园等[19]的方法。
1.3.5 啤酒风味物质分析
参照刘皓等[1]的方法稍作修改。
固相微萃取(solid-phase microextraction,SPME)香气富集:取5 mL啤酒发酵液于顶空瓶,加2.5 g NaCl和10 μL 0.082 4 g/L 2-壬醇溶液,在恒温磁力搅拌器55 ℃搅拌15 min,萃取头预先于250 ℃下老化5 min,随即插入样品瓶吸附45 min,并于进样口热解吸5 min,解析温度250 ℃,进入GC-MS分析仪进行挥发性化合物检测。
定性分析:采用NIST17质谱库检索、标准香气成分保留时间比对与手动检索矫正相结合,进行定性分析。
定量分析:将2-壬醇作为内标,采用内标-标准曲线法进行定量。按照公式(1)计算香气活度值(odor active values,OAV):
OAV=C/OT
(1)
式中:C,根据内标法计算出的该化合物的质量浓度,μg/L;OT,指香气化合物在文献中查阅到的气味阈值[20-25],μg/L。
1.3.6 感官品评
感官评定小组由10位经过培训的啤酒专业人员(5男5女,20~35岁)组成,参考曹春蕾等[25]的方法对啤酒进行的香气感官品评,标准如表2所示。
表2 啤酒感官品评标准
Table 2 Beer sensory evaluation standards

1.4 数据处理
使用Excel进行数据处理和分析,Origin 2024对实验数据进行整理和作图分析。
2 结果与讨论
2.1 菌株形态鉴定
采用麦汁培养基28 ℃培养2 d,每株菌的菌落形态如表3所示。
表3 菌株菌落形态特征
Table 3 Colony morphological characteristics of the strains
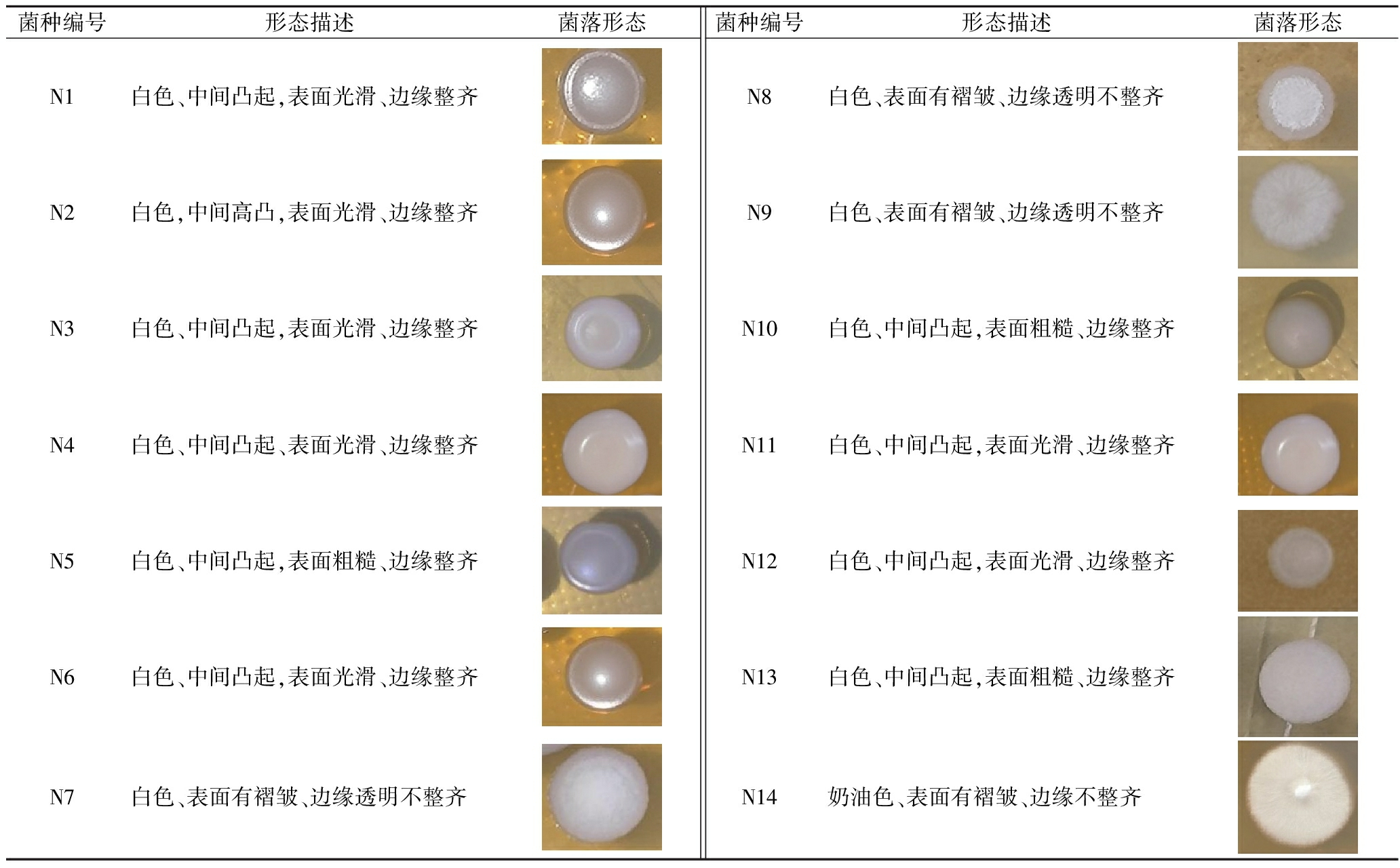
菌种编号形态描述菌落形态菌种编号形态描述菌落形态N1白色、中间凸起,表面光滑、边缘整齐N2白色,中间高凸,表面光滑、边缘整齐N3白色、中间凸起,表面光滑、边缘整齐N4白色、中间凸起、表面光滑、边缘整齐N5白色、中间凸起,表面粗糙、边缘整齐N6白色、中间凸起,表面光滑、边缘整齐N7白色、表面有褶皱、边缘透明不整齐N8白色、表面有褶皱、边缘透明不整齐N9白色、表面有褶皱、边缘透明不整齐N10白色、中间凸起,表面粗糙、边缘整齐N11白色、中间凸起,表面光滑、边缘整齐N12白色、中间凸起,表面光滑、边缘整齐N13白色、中间凸起,表面粗糙、边缘整齐N14奶油色、表面有褶皱、边缘不整齐
根据表3可以观察出酵母菌株在麦汁培养基上生长状态良好,符合酵母菌的基本形态特征[26]。大多数菌落是圆形,颜色以白色为主,表面光滑或有光泽,菌株边缘整齐,形状基本都为中部高凸起。其中,菌种N7、N8、N9、N12、N14这5株微生物的菌落边缘不整齐,N7、N8、N9、N12、N13、N14菌落表面粗糙,无光泽。
2.2 菌株产酶特性分析
非酿酒酵母较啤酒酵母可以赋予啤酒不同特征风味口感[27],主要原因是非酿酒酵母在发酵过程中可以产生多种不同酶类[28]。根据啤酒发酵过程中的酿造特点,本研究重点聚焦在蛋白酶、β-葡聚糖酶和β-葡萄糖苷酶的代谢产物[29],分析了14株非酿酒酵母的产酶特性,主要根据蛋白酶透明水解圈、β-葡聚糖酶透明水解圈以及β-葡萄糖苷酶的七叶苷培养基显色深浅来判断酵母是否具有β-葡萄糖苷酶、蛋白酶和β-葡聚糖酶3种酶的产酶能力。
2.2.1 菌株产酶特性研究
将酵母菌株接种到七叶苷培养基上,观察七叶苷培养基颜色的深浅情况,可知酵母菌株产酶特性。由图1可知,14株菌株均可以使七叶苷培养基的颜色发生变化,说明以上菌株均可以产β-葡萄糖苷酶,而使培养基颜色变深色的菌株即为高产β-葡萄糖苷酶的菌株,主要有N8、N9、N11、N13。

图1 酵母菌株在七叶苷培养基上显色结果
Fig.1 Colorimetric results of yeast strains in esculin medium
从图2的β-葡聚糖酶水解圈可以看出,14株菌株中多数非酿酒酵母可以产生β-葡聚糖酶,而仅有葡萄汁有孢汉逊酵母N1、N2、N3、N4、N5、异常威克汉姆酵母N6不能产生β-葡聚糖酶。而从β-葡聚糖酶培养基的透明圈大小可以看出,库德里阿兹威毕赤酵母N7、库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、马克斯克鲁维酵母N10、乳酸克鲁维酵母N11、异常威克汉姆酵母N13产β-葡聚糖酶的能力比较强。
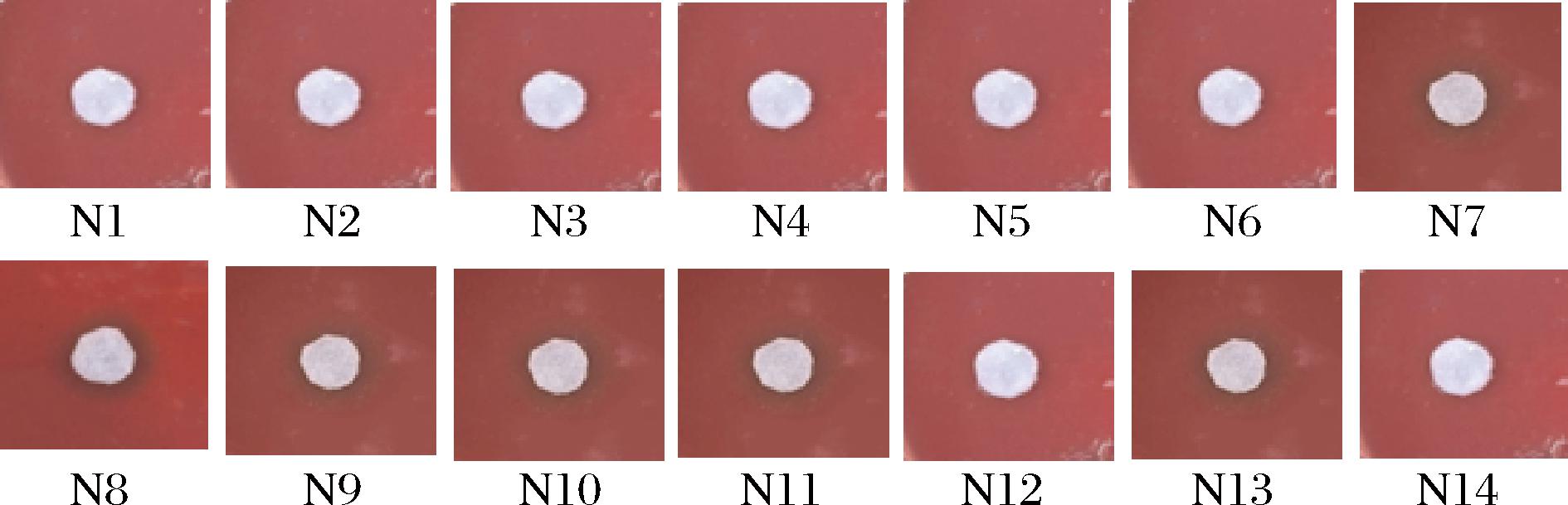
图2 酵母菌株产β-葡聚糖酶测定结果
Fig.2 Determination results of β-glucanase production by yeast strains
从图3蛋白酶透明水解圈可以看出,具有高产蛋白酶能力的非酿酒酵母菌株有:葡萄汁有孢汉逊酵母N4、葡萄汁有孢汉逊酵母N5、库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、乳酸克鲁维酵母N11、异常威克汉姆酵母N12和异常威克汉姆酵母N13,其他非酿酒酵母均未出现蛋白酶透明水解圈。

图3 酵母菌株产蛋白酶测定结果
Fig.3 Determination results of protease production by yeast strains
β-葡萄糖苷酶是一种重要的酶,能够催化糖苷水解,有效释放出游离的糖苷配体,这些配体通常具有特殊的香气和风味物质,能够为啤酒增添独特的风味特征。此外,在啤酒生产过程中,β-葡聚糖的存在会显著影响麦汁和啤酒的黏度,导致过滤困难,甚至可能引起设备堵塞,这不仅降低了生产效率,还可能影响啤酒的最终质量。因此,降低麦汁或发酵液中的β-葡聚糖含量是优化啤酒生产工艺的关键步骤之一。在啤酒酿造过程中,蛋白质不仅在形成丰富的泡沫方面起着至关重要的作用,还对啤酒的非生物稳定性产生显著影响。适量的蛋白质可以提升啤酒的口感和香气,形成持久的泡沫层,从而增强饮用体验。结果表明,14株非酿酒酵母均可以产生β-葡萄糖苷酶,库德里阿兹威毕赤酵母N7、库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、马克斯克鲁维酵母N10、乳酸克鲁维酵母N11、异常威克汉姆酵母N13可以产β-葡聚糖酶,而葡萄汁有孢汉逊酵母N4、葡萄汁有孢汉逊酵母N5、库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、乳酸克鲁维酵母N11、异常威克汉姆酵母N12和N13具有产蛋白酶的能力。
2.2.2 酶活力测定
14株菌在麦汁培养基中的产酶活力如表4所示。
表4 不同酵母菌株酶活力 单位:U/mL
Table 4 Enzyme activities of different yeast strains
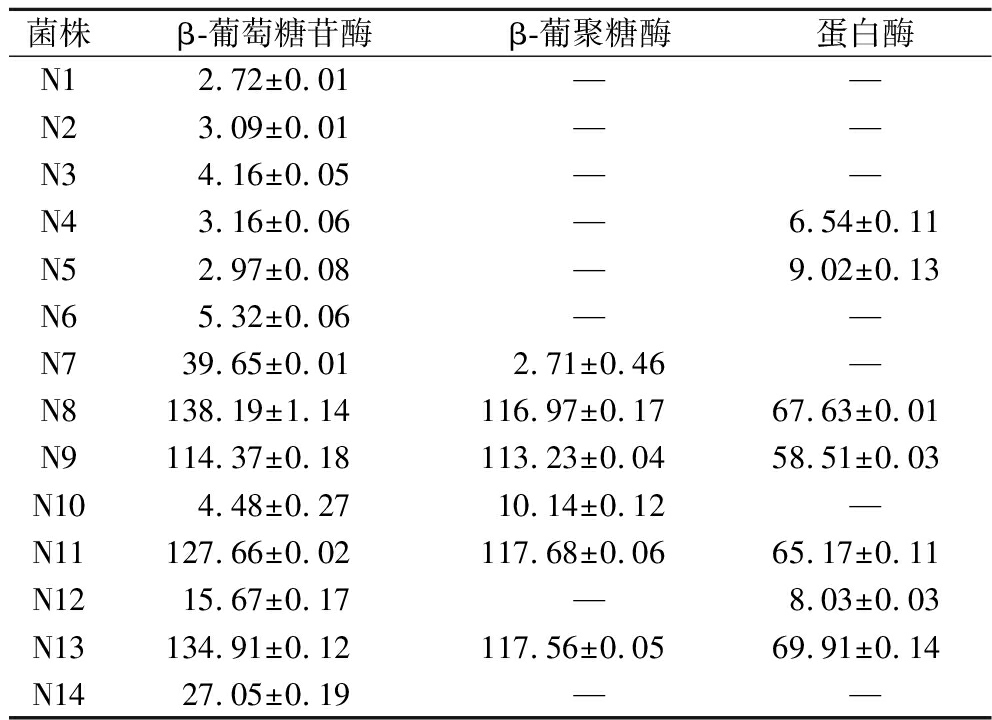
菌株β-葡萄糖苷酶β-葡聚糖酶蛋白酶N12.72±0.01——N23.09±0.01——N34.16±0.05——N43.16±0.06—6.54±0.11N52.97±0.08—9.02±0.13N65.32±0.06——N739.65±0.012.71±0.46—N8138.19±1.14116.97±0.1767.63±0.01N9114.37±0.18113.23±0.0458.51±0.03N104.48±0.2710.14±0.12—N11127.66±0.02117.68±0.0665.17±0.11N1215.67±0.17—8.03±0.03N13134.91±0.12117.56±0.0569.91±0.14N1427.05±0.19——
注:“—”表示未检出。
检测结果显示,受试非酿酒酵母菌株均可生成β-葡萄糖苷酶,其中N8、N9、N11和N13所产β-葡萄糖苷酶的活性较高,分别达到(138.19±1.14)、(114.37±0.18)、(127.66±0.02)、(134.91±0.12) U/mL,N7、N12、N14菌株所产β-葡萄糖苷酶活性在15.67~39.65 U/mL,其余菌株发酵液中的β-葡萄糖苷酶活性在10%以下。β-葡聚糖酶活性测定结果显示,仅在N7、N8、N9、N10、N11、N13菌株的发酵液中检出β-葡聚糖酶活性,其中N7、N10菌株的β-葡聚糖酶活性较低,而N8、N9、N11、N13发酵液中的β-葡聚糖酶活性较高,均大于100 U/mL。此外,在受试非酿酒酵母菌株中,有7个菌株(N1、N2、N3、N6、N7、N10、N14)的发酵液中未检测到蛋白酶活性,N8、N9、N11、N13的蛋白酶活性较高,分别为(67.63±0.01)、(58.51±0.03)、(65.17±0.11)、(69.91±0.14) U/mL。
综上,库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、乳酸克鲁维酵母N11和异常威克汉姆酵母N13具有高产β-葡萄糖苷酶、β-葡聚糖酶和蛋白酶的能力。后续研究将以此4株菌株作为研究对象进行重点研究。
2.3 菌株耐受性分析
本研究进一步探讨了库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、乳酸克鲁维酵母N11和异常威克汉姆酵母N13等4株非酿酒酵母菌株在麦汁培养基中的发酵特性,重点分析了它们对不同浓度的糖、pH值以及酒精的耐受性,以深入理解非酿酒酵母的发酵能力[29-31]。
2.3.1 菌株糖耐受性测定
高浓度糖分造成的渗透压增加会抑制酵母细胞的生长和代谢行为,导致发酵迟缓、停滞。因此在啤酒酿造过程中,需要使用具有高渗透压耐性的非酿酒酵母参与酒精发酵过程。
由图4结果可以看出,随着糖浓度的升高,非酿酒酵母的生长受到显著抑制;当葡萄糖浓度达到25%和30%时,4株菌株的生长趋势显著放缓,说明在此高糖环境中非酿酒酵母菌的生长受到明显抑制。啤酒酿造中使用的原麦汁浓度通常在25%以下,因此可以认为这4株非酿酒酵母菌在啤酒酿造的糖浓度范围内能够正常生长,并发挥一定的酿造特性。
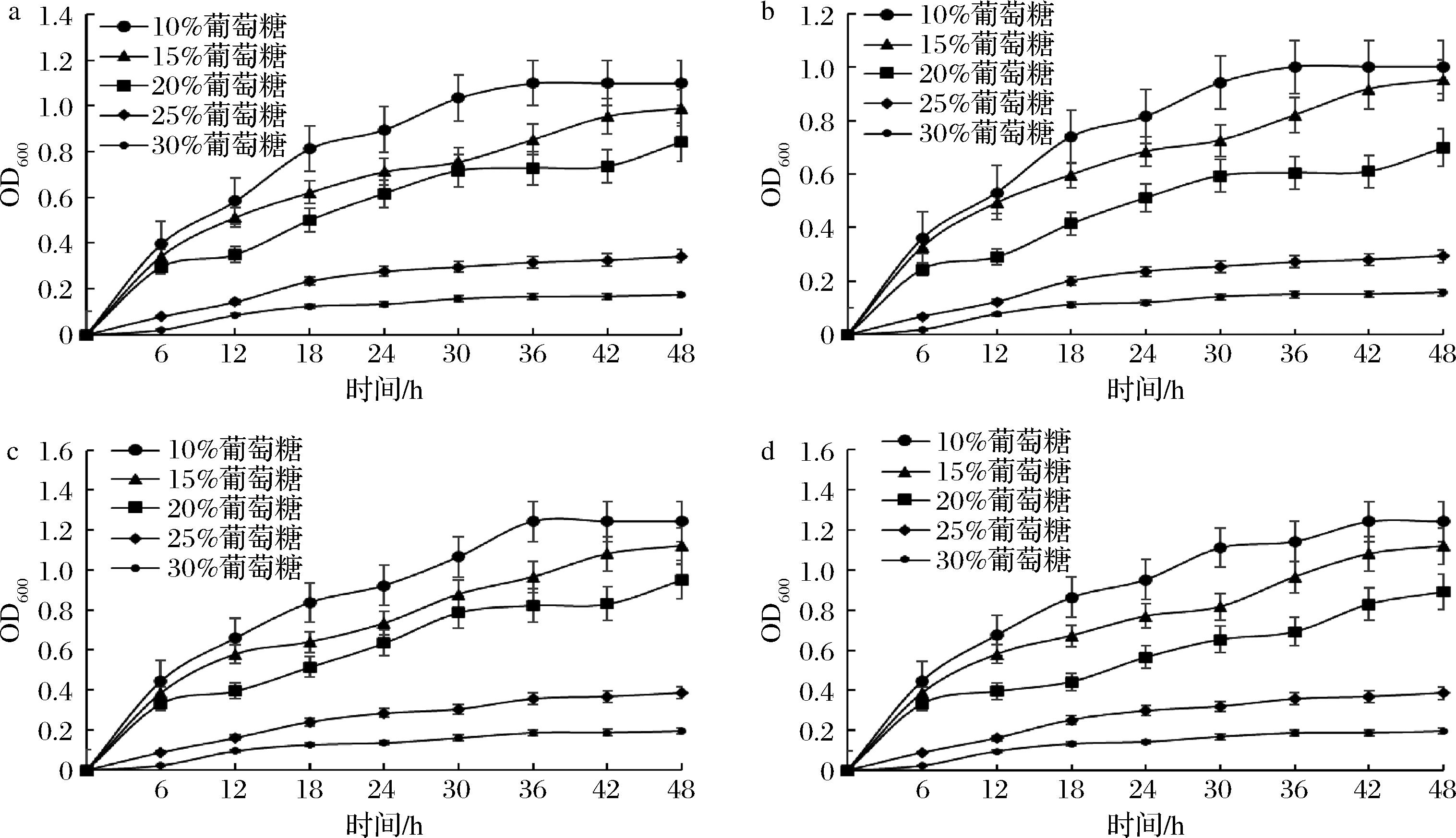
a-菌株N8;b-菌株N9;c-菌株N11;d-菌株N13
图4 酵母菌株的糖耐受能力
Fig.4 Sugar tolerance of yeast strains
2.3.2 菌株pH耐受性测定
在啤酒酿造过程中,酵母菌对酸性环境的耐受性直接影响发酵稳定性及成品品质,这是因为高酸性环境会显著抑制酵母菌的代谢活性。因此,筛选具有优异耐酸性能的非酿酒酵母菌株对确保啤酒品质至关重要[31]。
如图5所示,pH≥4时,4株非酿酒酵母均能够正常生长;pH≤3时,4株酵母的生长均受到明显抑制。此外,不同菌株的pH耐受性也表现出一定差异。其中,N13酵母在pH值为4和5的环境下具有相似的生长趋势。资料显示,啤酒的pH值一般在4~5,因此,可以认为4株酵母能够满足啤酒酿造过程中的酸度环境,可以正常进行发酵。
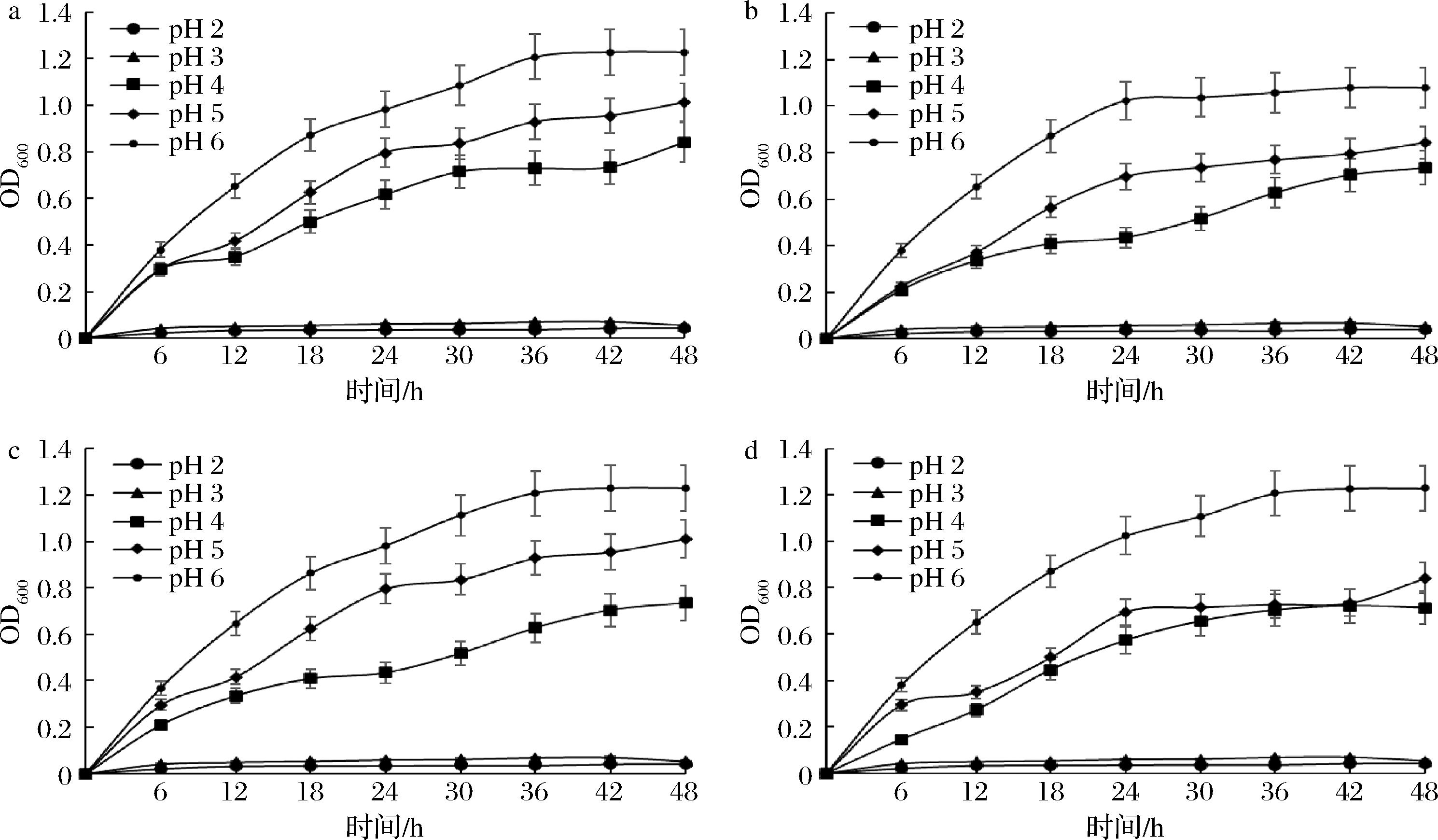
a-菌株N8;b-菌株N9;c-菌株N11;d-菌株N13
图5 酵母菌株的pH耐受能力
Fig.5 pH tolerance of yeast strains
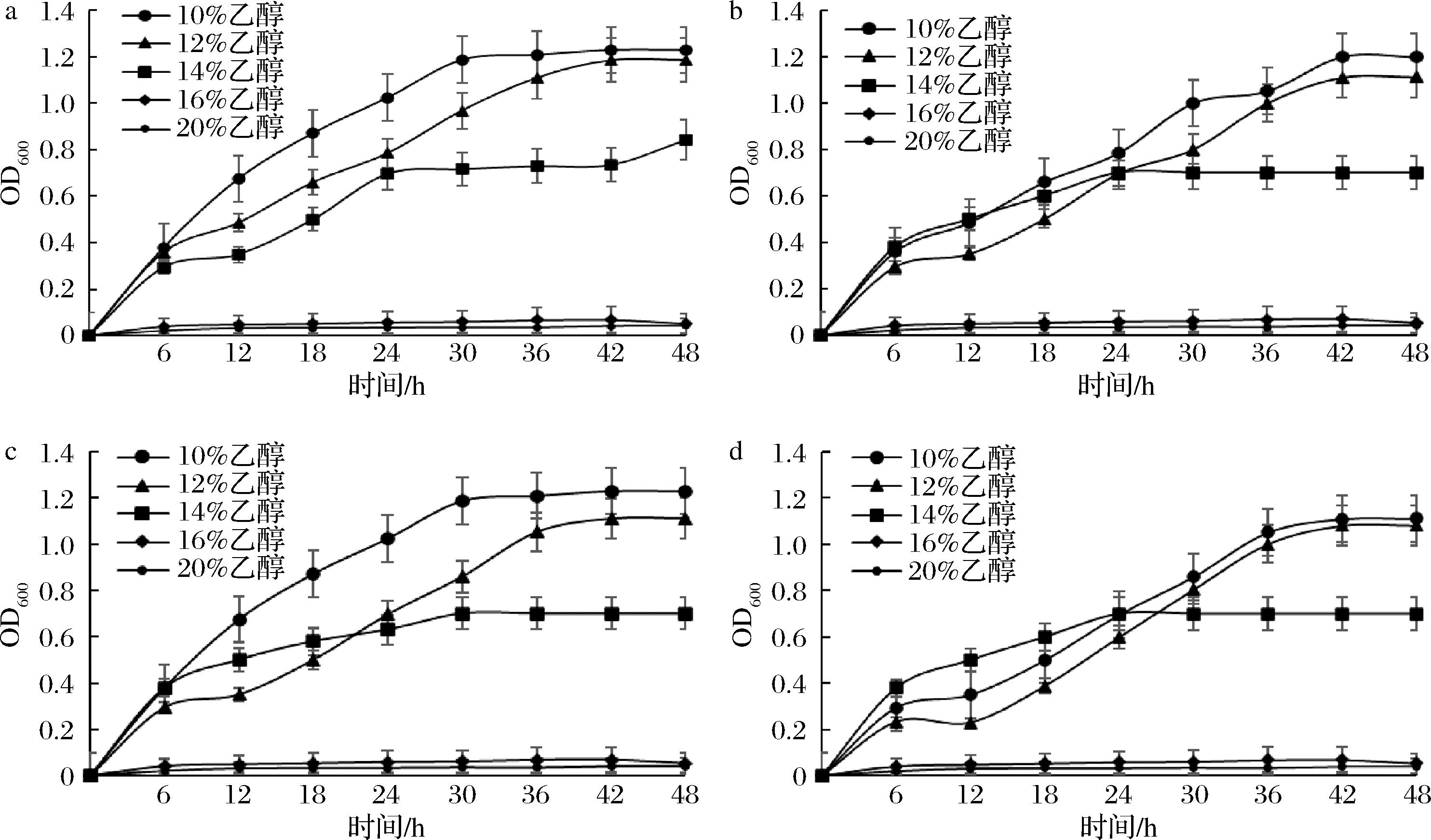
a-菌株N8;b-菌株N9;c-菌株N11;d-菌株N13
图6 酵母菌株的乙醇耐受能力
Fig.6 Ethanol tolerance of yeast strains
2.3.3 菌株乙醇耐受性测定
在啤酒酿造过程中,非酿酒酵母的乙醇耐受性较低,通常难以承受高浓度乙醇环境。因此,乙醇耐受性是非酿酒酵母参与啤酒发酵的关键因素之一。为了优化发酵过程,需要筛选具有较高乙醇耐受性的非酿酒酵母菌株,以提高发酵效率和产品质量。
如图6所示,随着乙醇体积分数的升高,酵母菌株的生长在不同程度上都受到了影响。在乙醇体积分数为10%和12%时,4株酵母均能正常生长;当乙醇体积分数为14%时,4株酵母生长均受到显著抑制;当乙醇体积分数在16%及以上时,4株酵母均不能生长。啤酒酿造过程中乙醇体积分数通常不超过12%,因此,菌株N8、N9、N11、N13能够满足啤酒发酵的乙醇耐受性要求。
因此,从4株非酿酒酵母菌株对糖、pH值和乙醇的耐受性来看,在麦汁培养基中,当糖浓度≤20%、乙醇体积分数≤12%、pH值≥4时,这些条件与啤酒酿造的实际环境基本一致。因此,菌株N8、N9、N11和N13能够满足啤酒发酵的需求。
2.4 不同非酿酒酵母发酵后啤酒风味物质分析
为了进一步评估非酿酒酵母的产香能力,本研究采用顶空固相微萃取-气相色谱质谱联用(headspace solid phase micro extraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)的方法定量对4株非酿酒酵母在麦汁发酵液中的挥发性风味化合物进行了定量分析。
2.4.1 挥发性风味化合物分析
从风味化合物种类来看,4株非酿酒酵母共检测出48种化合物,详见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.042528,下同),其中含11种酯类化合物、19种醇类化合物、2种醛类化合物、15种酸类化合物和1种萜烯类化合物,而对照啤酒酵母W-34/70仅检出了2种酯类化合物、11种醇类化合物、7种酸类化合物,2种酵母生产的醛类物质种类相似。与非酿酒酵母菌株相比,在拉格啤酒酵母纯种发酵所得的啤酒中未检出里那醇。本研究使用的4株非酿酒酵母菌株均具有较高的β-葡萄糖苷酶活性,这可促进麦芽汁及酒花中萜烯结合态糖苷的水解,释放出游离态挥发性萜烯苷元,从而提高了啤酒中萜烯类物质的产量。
由风味化合物的含量来看,4株非酿酒酵母在酯类、醇类、酸类、醛类和萜烯类化合物的含量上均显著高于纯种发酵。酯类化合物,4株非酿酒酵母产酯类化合物的含量均超过2 000 μg/L,其中乳酸克鲁维酵母N11产酯能力最高,为(4 890.12±6.32) μg/L,而拉格啤酒酵母W-34/70仅为(115.94±1.28) μg/L,非酿酒酵母产酯能力远高于拉格啤酒酵母,说明其产酯能力更强。醇类化合物,4株非酿酒酵母产醇类化合物的含量均超过780 μg/L,乳酸克鲁维酵母N11产醇类化合物总量最高(1 462.63±6.52) μg/L,对照纯种啤酒酵母为(670.39±1.99) μg/L,非酿酒酵母产醇能力显著高于拉格啤酒酵母。酸类化合物,4株非酿酒酵母酸类物质含量均超过100 μg/L,库德里阿兹威毕赤酵母N8为(196.91±3.26) μg/L,高于对照拉格啤酒酵母酸类化合物的总产量(96.96±2.11) μg/L。醛类化合物,除乳酸克鲁维酵母N11不产醛类物质外,其余3株非酿酒酵母产醛类化合物的含量均高于对照菌株。萜烯类化合物,除库德里阿兹威毕赤酵母N8不产萜烯类物质,其余3株非酿酒酵母产萜烯类化合物的含量均超过3 μg/L,对照拉格啤酒酵母未检出萜烯类物质。
综上所述,非酿酒酵母在产酯、醇、醛、酸、萜烯类等风味化合物方面的能力均高于啤酒拉格酵母。采用非酿酒酵母和啤酒酵母混合发酵酿造啤酒,具有提高啤酒的风味化合物含量,丰富啤酒的风味物质种类,提高啤酒的风味品质的潜力。
而对比分析4株非酿酒酵母的产香能力,由附表1可知,酯类化合物方面,从4株非酿酒酵母产酯类化合物的种类来看,本研究共检测出11种酯类化合物,其中N8检测出8种、N9检测出6种、N11检测出8种、N13检测出5种。从4株非酿酒酵母产酯类化合物的含量来看,乳酸克鲁维酵母N11产酯能力最高,为(4 890.12±6.32) μg/L,异常威克汉姆酵母N13产酯能力次之,为(3 266.39±4.35) μg/L。其中乳酸克鲁维酵母N11的乙酸乙酯、乙酸苯乙酯含量较高,分别为(2 274.41±3.19)、(2 547.58±2.23) μg/L。乙酸乙酯为啤酒中的主要酯类化合物,能够为啤酒带来令人愉快的果香味,本研究的4株酵母均高产乙酸乙酯,其中异常威克汉姆酵母N13的能力最强,为(3 180.55±9.86) μg/L,比其他3株非酿酒酵母高约1.5倍,其余3株非酿酒酵母能力基本相当。此外,乙酸苯乙酯具有花香和蜂蜜香气。本研究的4株酵母中,乳酸克鲁维酵母N11产乙酸苯乙酯的能力最强,为(2 547.58±2.23) μg/L,分别为其余3株非酿酒酵母N8、N9、N13的36倍、492倍和78倍。因此,产酯能力方面,4株非酿酒酵母中N8和N11的产酯类化合物的种类高于其余2株酵母,从酯类化合物含量来看,4株酵母均具有较强的产乙酸乙酯的能力,其中N13的能力最强,而N11酵母的产乙酸苯乙酯的能力最强,显著高于其余3株酵母。
醇类化合物是啤酒中重要的香气物质,从4株酵母产醇类化合物的种类来看,本研究共检测出19种醇类化合物,其中N8检出13种、N9检出14种、N11检出15种、N13检出12种,N11酵母的产醇类化合物种类高于其余3株酵母。从醇类化合物的含量来看,乳酸克鲁维酵母N11和库德里阿兹威毕赤酵母N8产醇类化合物的总量基本相当,分别为(1 462.63±6.52)、(1 434.98±5.32) μg/L,高于其余2株酵母近2倍。在2株非酿酒酵母N8和N11中3-甲基-1-丁醇、左旋薄荷醇等物质含量相对较高,显著高于其余2株酵母,其中N8酵母产苯乙醇能力高于N11酵母,而N11酵母在2-甲基-2-丙醇、3-甲基-1-丁醇、左旋薄荷醇这3种物质方面具有一定的优势。研究表明,2-甲基-2-丙醇具有特殊的醇香,3-甲基-1-丁醇带有醇香,左旋薄荷醇具有薄荷香气,苯乙醇具有玫瑰香气。因此,产醇能力来看,N8和N11酵母产醇能力相对较强,用于啤酒酿造,可以为啤酒带来薄荷香和玫瑰香等特征香气。
在本研究共检测出的15种酸类化合物中,N9检测出13种、N11和N13检测出12种、N8检测出9种。从含量上看,N8的酸类化合物含量最高,为(196.91±3.26) μg/L,显著高于其他菌株。总体而言,酸类化合物的含量相对较低,但N9、N11和N13的产酸能力较为接近。
本研究共检测出2种醛类物质,分别是苯甲醛和戊醛,但总体含量较低,其中乳酸克鲁维酵母N11中未检出醛类物质。
萜烯类化合物方面,总体含量相对偏低,但可以看到N9、N11、N13酵母均可产里那醇,可以为啤酒提供一定的特色香气。
综上所述,非酿酒酵母在产酯、醇、酸、醛、萜烯类等风味化合物方面的能力均高于拉格啤酒酵母。在4株非酿酒酵母中,N11在产酯、产醇、产酸和产萜烯类化合物方面表现最为突出,尤其是乙酸苯乙酯的生成能力显著高于其他菌株;N8在产酯和产醇方面表现优异,特别是在苯乙醇的生成上具有优势;N13在产乙酸乙酯和苯乙醇方面能力较强。因此,N11和N8酵母在啤酒酿造中具有较高的应用潜力,能够显著提升啤酒的风味多样性和品质。
2.4.2 关键挥发性风味化合物主成分分析
风味成分的贡献度由气味阈值和相对含量共同决定,低含量但低阈值的成分可能对风味有重要影响。本研究采用OAV法分析挥发性风味物质,结合气味阈值确定关键风味成分,各组关键性风味物质及对应OAV如附表2所示。
本研究的OAV分析聚焦于菌株间挥发性成分比例关系的横向比较,为了更加直观地展示本研究的5株酵母菌株挥发性香气化合物的差异,选取样品中OAV>0.1的香气物质(共8种)进行主成分分析,结果如图7所示。
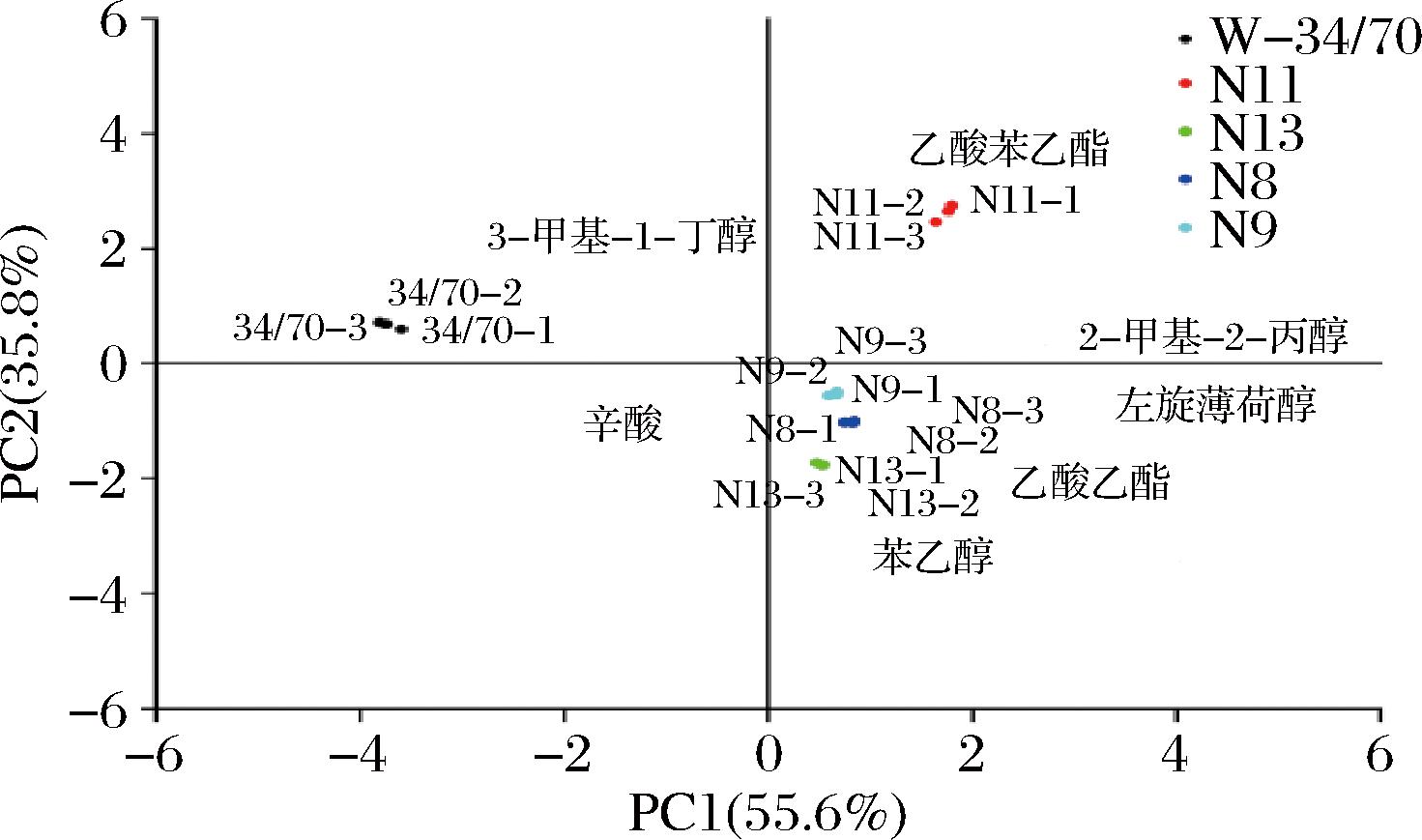
图7 不同菌株香气物质主成分分析图
Fig.7 Principal component analysis plot of aroma compounds by different strains
2个主成分(PC1和PC2)的总贡献率为91.4%,其中PC1的贡献率为55.6%,PC2的贡献率为35.8%。在主成分分析结果中,N11位于第一象限,与乙酸苯乙酯、2-甲基-2-丙醇关联性较强;W-34/70位于第二象限,与3-甲基-1-丁醇、辛酸相关性较强;N8、N9、N13位于第四象限,与乙酸乙酯、苯乙醇、左旋薄荷醇相关。主成分分析结果表明,4株非酿酒酵母与对照拉格啤酒酵母W-34/70香气差异较大,非酿酒酵母发酵液中含有呈现薄荷香特征的左旋薄荷醇、玫瑰香的苯乙醇、醇香馥郁的2-甲基-2-丙醇、水果香的乙酸乙酯、花香、蜂蜜香的乙酸苯乙酯以及具有醇厚香气的3-甲基-1-丁醇,这些独特的风味物质共同作用,极大地丰富了啤酒的香气层次,为消费者带来全新而独特的味觉体验,使啤酒在口感上更加多元和诱人。
2.5 不同非酿酒酵母与纯种啤酒酵母混合发酵后啤酒分析
本研究将获得的优良性能的产香非酵酒酵母N8、N9、N11和N13菌株应用于拉格啤酒的混菌发酵过程,非酵酒酵母N8、N9、N11和N13分别与啤酒拉格酵母W-34/70混合发酵麦汁,对混合发酵啤酒样品和拉格啤酒酵母纯种发酵啤酒样品进行评价。
2.5.1 常规理化指标分析
采用啤酒分析仪对啤酒发酵液的常规理化指标(原麦汁浓度、酒精度、真正浓度和真正发酵度)进行检测,如表5所示。发酵度范围保持在65.15%~66.48%,主要可能是酵母菌以及发酵方式对发酵度产生了一定的影响,因此也对应地体现在酒精度和真正浓度上。通过常规理化指标可知,根据不同接种策略接种酵母后,均能够顺利完成发酵,没有表现出发酵异常或中止的情况。
表5 啤酒常规理化指标测定结果
Table 5 Results of routine physicochemical indexes of beer

指标发酵菌株N8+W-34/70N9+W-34/70N11+W-34/70N13+W-34/70W-34/70原麦汁浓度/°P12.97±0.2312.64±0.2312.71±0.1812.65±0.212.52±0.19酒精度/%vol5.32±0.155.40±0.155.53±0.235.43±0.165.56±0.22真正浓度/°P4.52±0.154.27±0.184.26±0.234.36±0.224.23±0.15真正发酵度/%65.15±0.2265.43±0.2166.48±0.1765.53±0.2266.21±0.18
2.5.2 感官品评分析
感官品评是评估啤酒质量的最直观方法。本研究选择非酿酒酵母菌株N8、N9、N11和N13,分别与啤酒拉格酵母W-34/70混合发酵麦汁,并从外观、香气、口感和综合评价等方面对发酵啤酒样品进行品评(图8)。结果显示,使用N11和N13非酿酒酵母混合发酵的啤酒在感官综合评价中表现优于其他组。其中,N11的感官评分最高,其次是N13,主要优势体现在香气方面。N11和N13显著增强了啤酒的酯香和醇香特性,使香气更为浓郁且持久。此外,在口感方面,N11和N13酿造的啤酒表现出纯正柔和的风味,酒体协调性更好,整体风味更加平衡。
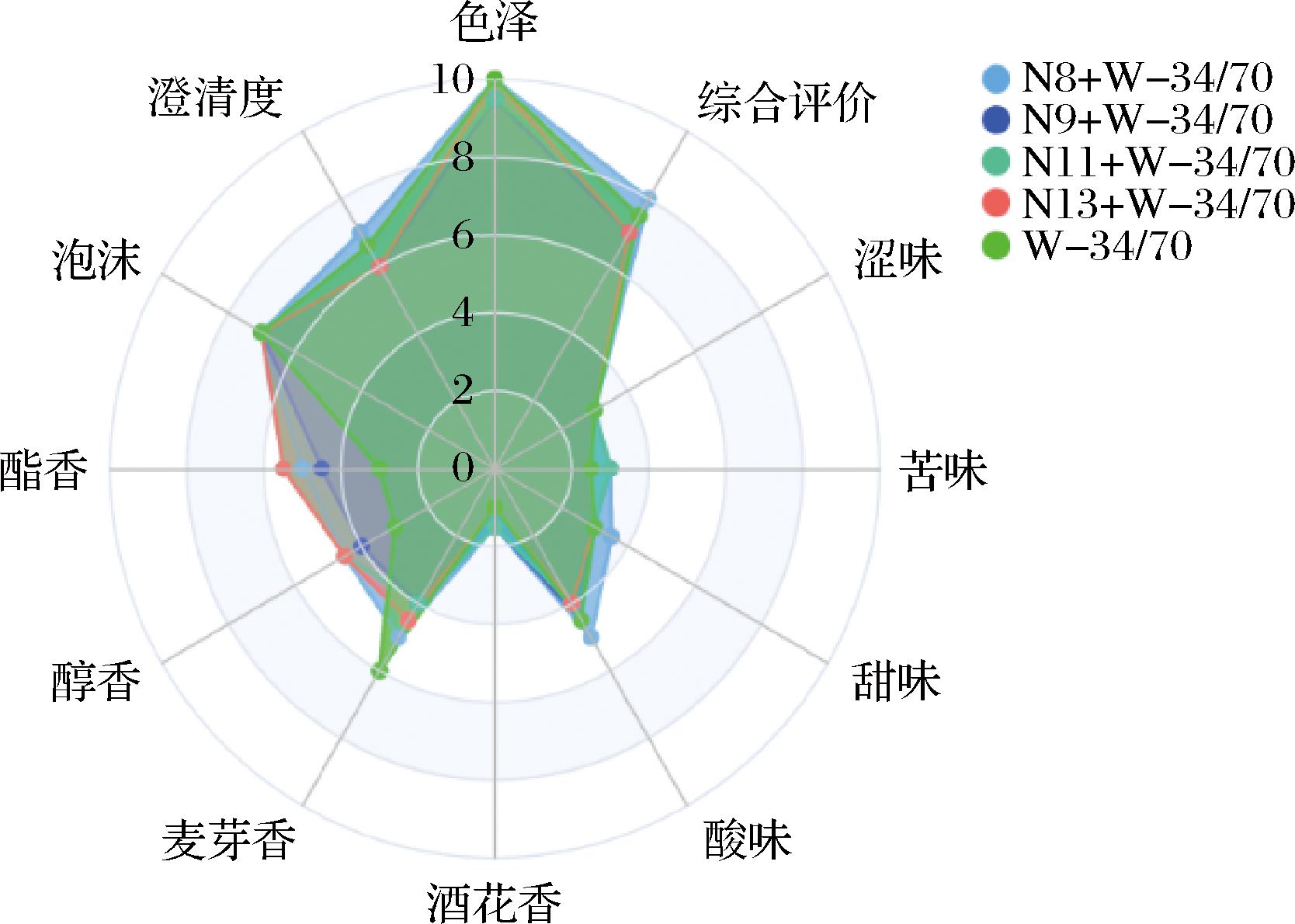
图8 发酵啤酒样品感官品评结果
Fig.8 Sensory evaluation results of fermented beer samples
3 结论
研究表明,库德里阿兹威毕赤酵母N8、发酵毕赤酵母N9、乳酸克鲁维酵母N11和异常威克汉姆酵母N13均表现出良好的产酶活性,能够产生β-葡萄糖苷酶、β-葡聚糖酶和蛋白酶,且酶活性较高。这些酶在啤酒酿造过程中能够有效促进风味物质的生成。在耐受性方面,这4株酵母菌株普遍表现出良好的糖、pH和乙醇耐受性,尽管不同菌株在不同条件下的耐受性存在差异,但总体而言,它们均能满足啤酒酿造的基本要求。因此,这些菌株具备作为啤酒酿造用菌株的潜力。
从风味化合物的生成来看,非酿酒酵母在产酯、醇、醛、酸、萜烯类等风味化合物的种类和含量方面均优于啤酒酵母。4株非酿酒酵母均表现出较强的乙酸乙酯生成能力,其中乳酸克鲁维酵母N11在产酯、产醇、产酸和产萜烯类化合物方面表现最为突出,尤其在乙酸苯乙酯的产量上显著高于其他3株酵母。此外,库德里阿兹威毕赤酵母N8也表现出较强的产酯能力,而异常威克汉姆酵母N13在乙酸乙酯和苯乙醇的生成上表现优异。
在特征风味方面,4株非酿酒酵母与啤酒拉格酵母存在显著差异。乳酸克鲁维酵母N11与乙酸苯乙酯和2-甲基-2-丙醇关联性较强,可能会赋予啤酒花香和蜂蜜香的风味特征;而N8、N9和N13与乙酸乙酯、苯乙醇和左旋薄荷醇关联性较强,可能会赋予啤酒玫瑰花香、果香以及薄荷的风味特征。
感官品评结果表明,采用N11和N13与啤酒拉格酵母混合发酵啤酒样品,感官品评综合评价分数最高,从香气上和口味上优于纯种啤酒拉格酵母发酵样品,香气更为纯正、典型,口感更为柔和协调。
综上所述,非酿酒酵母在啤酒酿造中展现出显著的风味提升潜力。它们不仅能够产生丰富的风味化合物,还能为啤酒带来独特的香气层次和风味体验,为酿造不同风格的啤酒提供了更多选择。
[1] 刘皓, 陈烨, 曾英杰, 等.不同比例黑青稞麦芽汁中酵母的发酵性能及啤酒品质[J].现代食品科技, 2024, 40(3):74-82.
LIU H, CHEN Y, ZENG Y J, et al.Fermentation performance of yeast in malt wort with different proportions of black highland barley and the resulting beer quality[J].Modern Food Science and Technology, 2024, 40(3):74-82.
[2] 于亚敏, 李霞, 唐国冬, 等.两种酿酒酵母混合发酵对赤霞珠干红葡萄酒香气成分的影响[J].中国酿造, 2018, 37(4):121-126.
YU Y M, LI X, TANG G D, et al.Effects of mixed fermentation with two kinds of Saccharomyces cerevisiae on aroma components of Cabernet Sauvignon dry red wine[J].China Brewing, 2018, 37(4):121-126.
[3] YANG X S, ZHAO F Q, YANG L, et al.Enhancement of the aroma in low-alcohol apple-blended pear wine mixed fermented with Saccharomyces cerevisiae and non-Saccharomyces yeasts[J].LWT, 2022, 155:112994.
[4] ENGLEZOS V, RANTSIOU K, CRAVERO F, et al.Starmerella bacillaris and Saccharomyces cerevisiae mixed fermentations to reduce ethanol content in wine[J].Applied Microbiology and Biotechnology, 2016, 100(12):5515-5526.
[5] 刘晓燕, 赵晓敏, 张小月, 等.混菌顺序发酵对赤霞珠干红葡萄酒品质的影响[J].中国酿造, 2022, 41(4):65-72.
LIU X Y, ZHAO X M, ZHANG X Y, et al.Effects of mixed yeasts sequential fermentation on quality of Cabernet Sauvignon dry red wine[J].China Brewing, 2022, 41(4):65-72.
[6] CANONICO L, GALLI E, CIANI E, et al.Exploitation of three non-conventional yeast species in the brewing process[J].Microorganisms, 2019, 7(1):11.
[7] HAN X Y, QIN Q X, LI C Y, et al.Application of non-Saccharomyces yeasts with high β-glucosidase activity to enhance terpene-related floral flavor in craft beer[J].Food Chemistry, 2023, 404:134726.
[8] KING A, RICHARD DICKINSON J.Biotransformation of monoterpene alcohols by Saccharomyces cerevisiae, Torulaspora delbrueckii and Kluyveromyces lactis[J].Yeast, 2000, 16(6):499-506.
[9] 王笑语, 陈晶瑜, 马长伟.非酿酒酵母在多元化啤酒酿造应用中的研究进展[J].食品与发酵工业, 2024, 50(10):362-370.
WANG X Y, CHEN J Y, MA C W.Application of non-Saccharomyces in diversified beer brewing:A review[J].Food and Fermentation Industries, 2024, 50(10):362-370.
[10] 徐晓裕, 吴慧敏, 王鑫炜, 等.蟠桃表皮产酶非酿酒酵母的分离鉴定及发酵特性研究[J].中国食品添加剂, 2023, 34(6):48-57.
XU X Y, WU H M, WANG X W, et al.Isolation, identification and fermentation characteristics of enzymeproducing non-Saccharomyces cerevisiae from the epidermis of flat peach[J].China Food Additives, 2023, 34(6):48-57.
[11] 李婷, 陈景桦, 马得草, 等.优选非酿酒酵母与酿酒酵母在模拟葡萄汁发酵中生长动力学及酯酶活性分析[J].食品科学, 2017, 38(22):60-66.
LI T, CHEN J H, MA D C, et al.Growth kinetics and esterase activities of selected non-Saccharomyces yeast and Saccharomyces cerevisiae in the fermentation of model grape juice[J].Food Science, 2017, 38(22):60-66.
[12] POSTIGO V, O’SULLIVAN T, ELINK SCHUURMAN T, et al.Non-conventional yeast:Behavior under pure culture, sequential and aeration conditions in beer fermentation[J].Foods, 2022, 11(22):3717.
[13] 孔晓双, 黄新新, 董应宏, 等.一株产β-葡萄糖苷酶甘草内生菌的筛选、全基因组分析及产酶优化[J].微生物学通报, 2024, 51(1):279-294.
KONG X S, HUANG X X, DONG Y H, et al.Screening, whole genome analysis, and fermentation condition optimization of a β-glucosidase-producing endophyte from Glycyrrhiza uralensis Fisch[J].Microbiology China, 2024, 51(1):279-294.
[14] 付跃, 李书安, 石娟娟, 等.杂色曲霉β-葡萄糖苷酶分离纯化及酶学性质研究[J].中国饲料, 2024(13):48-54.
FU Y, LI S A, SHI J J, et al.Isolation, purification and enzymatic properties of β-glucosidase from Aspergillus versicolor[J].China Feed, 2024(13):48-54.
[15] 杨春林, 李洪浩, 胡强, 等.高产β-葡聚糖酶木霉菌诱变育种及对黄瓜枯萎病的生防效果[J].中国瓜菜, 2023, 36(11):64-70.
YANG C L, LI H H, HU Q, et al.Mutation breeding of Trichoderma harzianum strain for β-Glucanase production and biocontrol effect on cucumber Fusarium wilt[J].China Cucurbits and Vegetables, 2023, 36(11):64-70.
[16] 吕小虎, 曹贵东.高产葡聚糖酶微生物的分离筛选[J].天津农业科学, 2022, 28(10):24-28.
LÜ X H, CAO G D.Isolation and screening of glucanase producing microorganisms[J].Tianjin Agricultural Sciences, 2022, 28(10):24-28.
[17] 胡连清, 刘雯雯, 刘婉茹, 等.糯红高粱中产蛋白酶内生酵母筛选鉴定及发酵特性研究[J].食品与发酵工业, 2023, 49(5):74-80.
HU L Q, LIU W W, LIU W R, et al.Screening, identification, and fermentation properties of protease-producing endophytic yeasts from waxy sorghum[J].Food and Fermentation Industries, 2023, 49(5):74-80.
[18] 刘晓柱, 赵湖冰, 李银凤, 等.一株刺梨葡萄汁有孢汉逊酵母的鉴定及酿酒特性分析[J].食品与发酵工业, 2020, 46(8):97-104.
LIU X Z, ZHAO H B, LI Y F, et al.Identification and oenological properties analysis of a strain of Hanseniaspora uvarum from Rosa roxburghii[J].Food and Fermentation Industries, 2020, 46(8):97-104.
[19] 熊荣园, 王黎明, 魏玲, 等.柑橘及桑葚中优质酵母菌的筛选及鉴定[J].中国酿造, 2023, 42(4):163-167.
XIONG R Y, WANG L M, WEI L, et al.Screening and identification of high-quality yeasts from citrus and mulberry[J].China Brewing, 2023, 42(4):163-167.
[20] 周文杰, 张芳, 王鹏, 等.基于GC-MS/GC-O结合化学计量学方法研究库尔勒香梨酒的特征香气成分[J].食品科学, 2018, 39(10):222-227.
ZHOU W J, ZHANG F, WANG P, et al.GC-MS/GC-O combined with chemometrics for the screening and identification of aroma characteristics of Korla pear wine[J].Food Science, 2018, 39(10):222-227.
[21] 焦红茹, 刘爱国, 谢春梅, 等.宁夏产区不同陈酿年份霞多丽干白葡萄酒香气成分研究[J].保鲜与加工, 2019, 19(4):167-175;183.
JIAO H R, LIU A G, XIE C M, et al.Analysis on aroma composition of chardonnay dry white wine in different aging years from Ningxia Region[J].Storage and Process, 2019, 19(4):167-175;183.
[22] 李涛, 司梦鑫, 李冲, 等.顶空固相微萃取-气质联用(HS-SPME-GC-MS)技术分析浓香型竹酒中香气成分[J].四川师范大学学报(自然科学版), 2020, 43(3):364-372.
LI T, SI M X, LI C, et al.Analysis of aroma components in Luzhou-flavor bamboo wine by headspace solid phase microextraction-gas chromatography-mass spectrometry(HS-SPME-GC-MS)[J].Journal of Sichuan Normal University (Natural Science), 2020, 43(3):364-372.
[23] 张倩, 李沁娅, 黄明泉, 等.2种芝麻香型白酒中香气活性成分分析[J].食品科学, 2019, 40(14):214-222.
ZHANG Q, LI Q Y, HUANG M Q, et al.Analysis of aroma active components in two sesame-flavor liquor[J].Food Science, 2019, 40(14):214-222.
[24] 易封萍, 马宁, 朱建才.基于GC-O、OAV及Feller加和模型对酱香型习酒特征香气成分的分析[J].食品科学, 2022, 43(2):242-256.
YI F P, MA N, ZHU J C.Identification of characteristic aroma compounds in soy sauce aroma type Xi Baijiu using gas chromatography-olfactometry, odor activity value and feller’s additive model[J].Food Science, 2022, 43(2):242-256.
[25] 曹春蕾, 余培斌, 吴殿辉, 等.几株啤酒酵母的筛选及发酵性能比较[J].中国生物工程杂志, 2022, 42(7):45-53.
CAO C L, YU P B, WU D H, et al.Screening of several strains of brewer’s yeast strains and comparison of their fermentability[J].China Biotechnology, 2022, 42(7):45-53.
[26] 孙传伯, 段文昌, 朱雪琦, 等.一株艾尔型啤酒酵母的选育及发酵性能研究[J].中外酒业·啤酒科技, 2017(13):31-35.
SUN C B, DUAN W C, ZHU X Q, et al.Breeding of an Al-type beer yeast and its fermentation performance[J].Global Alcinfo, 2017(13):31-35.
[27] NYHAN L, SAHIN A W, ARENDT E K.Co-fermentation of non-Saccharomyces yeasts with Lactiplantibacillus plantarum FST 1.7 for the production of non-alcoholic beer[J].European Food Research and Technology, 2023, 249(1):167-181.
[28] RUSSO P, ENGLEZOS V, CAPOZZI V, et al.Effect of mixed fermentations with Starmerella bacillaris and Saccharomyces cerevisiae on management of malolactic fermentation[J].Food Research International, 2020, 134:109246.
[29] HU K, JIN G J, XU Y H, et al.Enhancing wine ester biosynthesis in mixed Hanseniaspora uvarum/Saccharomyces cerevisiae fermentation by nitrogen nutrient addition[J].Food Research International, 2019, 123:559-566.
[30] KOCHL
 OV
OV T, KIJ D, KOPECK
T, KIJ D, KOPECK J, et al.Non-Saccharomyces yeasts and their importance in the brewing industry.Part II[J].Kvasny Prumysl, 2016, 62(7-8):206-214.
J, et al.Non-Saccharomyces yeasts and their importance in the brewing industry.Part II[J].Kvasny Prumysl, 2016, 62(7-8):206-214.
[31] 黄倩, 蔡建, 高秀, 等.羊奶果果酒专用本土非酿酒酵母的筛选、鉴定及特性研究[J].中国酿造, 2024, 43(6):156-161.
HUANG Q, CAI J, GAO X, et al.Screening, identification, and characterization of indigenous non-Saccharomyces cerevisiae for Elatagnus sarmentosa Rehd.fruit wine[J].China Brewing, 2024, 43(6):156-161.