酸笋是以新鲜麻竹笋为原料,采用盐水腌制发酵生产的传统发酵蔬菜,因其独特的风味和鲜香脆爽的口感而深受消费者喜爱。目前酸笋的生产主要是以自然发酵为主,但存在风味较单一、生产周期长、产品质量不稳定等问题,接种发酵技术可有效解决这些问题。接种发酵作为一种现代发酵技术,通过引入特定的微生物群体来主导发酵过程,以实现对微生物群落的调控。植物乳植杆菌作为蔬菜发酵领域中应用最广泛的菌种之一[1],在酸笋接种发酵过程中,会产生更高含量的乳酸等有机酸以及更多种类的代谢物[2],赋予酸笋多种风味,同时提升保质期和安全性。因此,研究不同发酵方式下酸笋的代谢产物差异变化,对于提升酸笋的风味品质具有重要意义。
近年来,非靶向代谢组学已经成为研究蔬菜发酵期间代谢物变化的重要手段,它能够客观、全面地反映代谢物的组成和含量变化,并发现一些未知的或潜在的生物标志物。研究表明,植物乳植杆菌接种发酵泡菜中鸟氨酸含量高于自然发酵[3],抗炎性更强[4];ZHANG等[5]基于液相色谱-质谱联用技术,分析了自然发酵和乳酸菌接种发酵酸菜的差异,结果表明氨基酸、肽和类似物、碳水化合物和碳水化合物衍生物是2种发酵酸菜产生的主要差异代谢物种类。但是,目前基于非靶向代谢组学研究自然发酵和接种发酵酸笋代谢差异方面鲜有报道。因此,本文利用液相色谱-质谱联用技术,以自然发酵酸笋(naturally fermented Suansun, NFS)和植物乳植杆菌接种发酵酸笋(Lactiplantibacillus plantarum-inoculated fermented Suansun, LPS)为原料,结合京都基因和基因组百科全书数据库进行代谢通路富集分析,探究在不同发酵方式下酸笋代谢物及代谢通路的差异,旨在为酸笋品质评估和调控提供理论参考。
1 材料与方法
1.1 材料与试剂
新鲜麻竹笋,重庆市北碚区天生桥农贸市场;植物乳植杆菌(Lactiplantibacillus plantarum)SS0831,保藏于中国典型培养物保藏中心,保藏编号为CCTCC NO:M 20242877;腌制盐,重庆合川盐化工业有限公司;甲醇、乙腈、甲酸、丙醇(均为色谱纯),美国赛默飞生物科技有限公司;L-2-氯苯丙氨酸,上海泰坦科技股份有限公司。
1.2 仪器与设备
超高效液相色谱串联傅里叶变换质谱,美国赛默飞生物科技有限公司;HSST3色谱柱(100 mm×2.1 mm,1.8 μm),美国沃特世公司;JXDC-20型氮气吹扫仪,上海净信实业发展有限公司;LNG-T88型台式快速离心浓缩干燥器,太仓市华美生化仪器厂;Wonbio-96c型高通量组织破碎仪,上海万柏生物科技有限公司;SBL-10DT型超声波清洗机,宁波新芝生物科技股份有限公司;Centrifuge5430R型高速冷冻离心机,德国艾本德公司。
1.3 实验方法
1.3.1 NFS和LPS的制备
参考GUAN等[6]的方案,将植物乳植杆菌SS0831接种到MRS肉汤中并在37 ℃下培养24 h。然后将培养物转移到新的MRS肉汤中,并在30 ℃下再培养12 h。将培养物在4 ℃下以6 000 r/min离心2 min,用8.5 g/L无菌盐水洗涤2次,然后重新放置在8.5 g/L新鲜无菌盐水中,以获得7 lg CFU/mL植物乳植杆菌作为发酵剂接种。
将新鲜的麻竹笋清洗晾干,切成笋片,于沸水浴中漂烫15 min后捞出冷却。一部分笋片按照固液比2∶3(g∶mL)加入6%(质量分数,下同)的盐水,密封发酵,将自然发酵酸笋命名为NFS。另一部分按照相同固液比,加入6%的盐水,同时按100 g酸笋接种1 mL菌液的接种量投入已活化的植物乳植杆菌,密封保存,将植物乳植杆菌接种发酵酸笋命名为LPS。在室温下对NFS和LPS进行腌制,14 d后微生物代谢达到最高水平,进行取样。每组各取6次样品,以保证实验数据的可靠性与准确性。
1.3.2 NFS和LPS代谢物的提取
根据HU等[7]的方法并加以改进进行酸笋代谢物的提取。准确称取(50±5) mg固体样品于2 mL离心管中,加入一颗直径6 mm的研磨珠,使用0.02 mg/mL L-2-氯苯丙氨酸作为内标物的提取溶剂[甲醇∶水=4∶1(体积比)],共加入400 μL提取液。在-10 ℃和50 Hz下,置于冷冻组织研磨仪中处理样品6 min,然后在5 ℃和40 kHz下超声波提取30 min。在-20 ℃下静置30 min后,于4 ℃,13 000×g离心15 min,移取上清液至带内插管的进样小瓶中上机分析。另外,为了进行质量控制,每个样本分别移取20 μL上清液,混合后制成3个质控(quality control, QC)样本。
1.3.3 液相色谱-质谱联用技术条件
液相色谱条件:3 μL样本经HSST3色谱柱(100 mm×2.1 mm,1.8 μm)分离后进入质谱检测。流动相A为95%水和5%乙腈(含0.1%甲酸),流动相B为47.5%乙腈、47.5%异丙醇和5%水(含0.1%甲酸),以上均为体积分数;流速0.40 mL/min;柱温40 ℃。
质谱条件:样品经电喷雾电离,分别采用正、负离子扫描模式采集质谱信号,质量扫描范围为70~1 050 m/z。氮气流速为50 psi,辅助气流速为13 psi,辅助气加热温度为425 ℃,正模式离子喷雾电压设置为3 500 V,负模式离子喷雾电压设置为-3 500 V,离子传输管温度为325 ℃,归一化的碰撞能为20-40-60 V循环碰撞能。一级质谱分辨率60 000,二级质谱分辨率7 500,采用DDA模式采集数据。
1.4 数据处理与分析
使用美吉云平台对数据进行可视化处理,所有样品均一式三份,代谢物分析结果取其平均值。使用R软件绘制主成分分析(principal component analysis, PCA)图和最小偏二乘判别分析(partial least squares-discriminant analysis, PLS-DA)图;采用Origin 2021软件、京都基因与基因组百科全书数据库(Kyoto encyclopedia of genes and genomes, KEGG)(http://www.genome.jp/kegg/pathway.html)、人类代谢组数据库(human metabolome database, HMDB)(http://hmdb.ca/ metabolites)进行代谢途径富集分析。
2 结果与分析
2.1 NFS和LPS代谢产物的PCA和PLS-DA
PCA评估了NFS和LPS样本在酸笋发酵过程中的代谢物差异。由图1-a可知,2组样品均位于置信区间内,组内样品聚集,差异不明显,2种发酵方式下各组酸笋样本具有稳定性和均一性;NFS和LPS沿着PC1方向明显分离,样本间存在显著差异,表明在不同发酵方式下酸笋具有独特的代谢特征;QC样本在图中紧密聚集,与NFS和LPS样本的距离都较远,说明本次代谢组学检测方法稳定可靠,并进一步说明植物乳植杆菌显著改变原有微生物发酵菌群,NFS和LPS产生的代谢物存在显著差异。
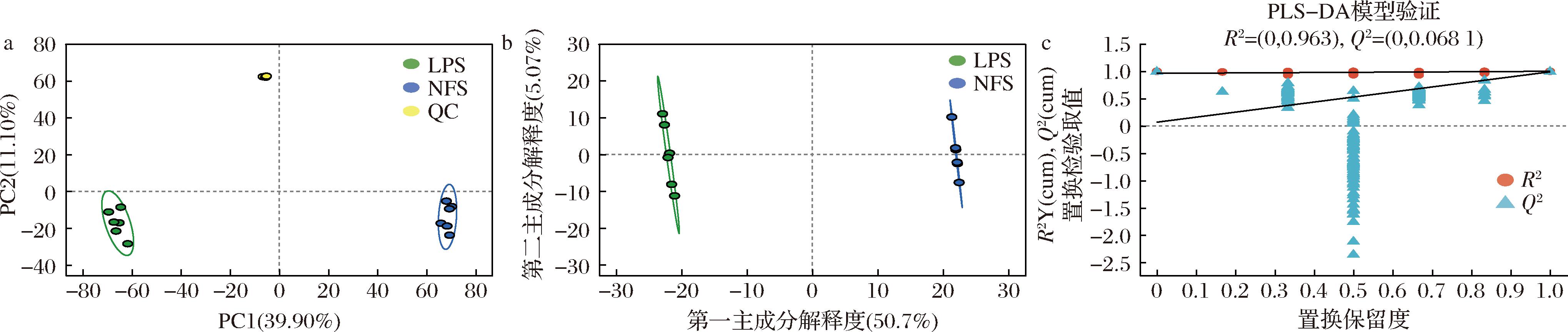
a-NFS、LPS和QC的PCA得分图;b-NFS和LPS代谢产物的PLS-DA得分图;c-NFS和LPS代谢产物的PLS-DA置换检验结果
图1 NFS和LPS样本比较分析图
Fig.1 Comparative analysis chart of NFS and LPS samples
为最大程度地查看NFS和LPS样品组间差异,降低组内差异,建立PLS-DA模型。如图1-b所示,NFS和LPS样品分离效果明显,与PCA结果相似,说明2组代谢物质确实存在显著性差异。为了确保结果的可靠性,对PLS-DA模型进行200次置换检验分析,由图1-c可知,随着置换保留度的下降,R2和Q2下降,回归线呈上升的趋势,表明模型可靠、不存在过拟合现象,准确地反映出NFS和LPS之间的代谢物差异。综上,NFS和LPS的微生物发酵菌群存在显著不同,代谢物层面具有显著差异,为后文NFS和LPS差异代谢物的深入分析提供理论支撑。
2.2 NFS和LPS总代谢物注释信息
为快速了解NFS和LPS代谢物组成,基于其特有或共有代谢物用于后续深入分析NFS和LPS差异代谢物,建立韦恩图。由图2-a可知,NFS和LPS共有代谢物9 688种。表明NFS和LPS仍具有高度相似性,可能是酸笋发酵过程中的基础代谢,不受发酵方式的影响。NFS特有代谢物87种,LPS特有代谢物116种,是NFS和LPS主要的差异代谢物,也是导致NFS和LPS在酸笋风味、品质和感官评价等方面差异的主要原因。NFS和LPS特有代谢物种类都主要是氨基酸、肽及其类似物,这是因为植物乳植杆菌分泌的蛋白酶会将酸笋中的蛋白质分解成氨基酸和小肽,同时这些小分子易被人体吸收利用,提高营养价值[8]。在LPS中,植物乳植杆菌大量繁殖,始终在发酵过程中占据主导地位,在NFS初期乳酸菌较少,植物乳植杆菌在发酵中期成为优势菌株,含量相比LPS较低[9],因此氨基酸、肽及其类似物在LPS中种类更丰富,表明在不同发酵方式下酸笋的微生物群落结构会发生改变,引起代谢差异。
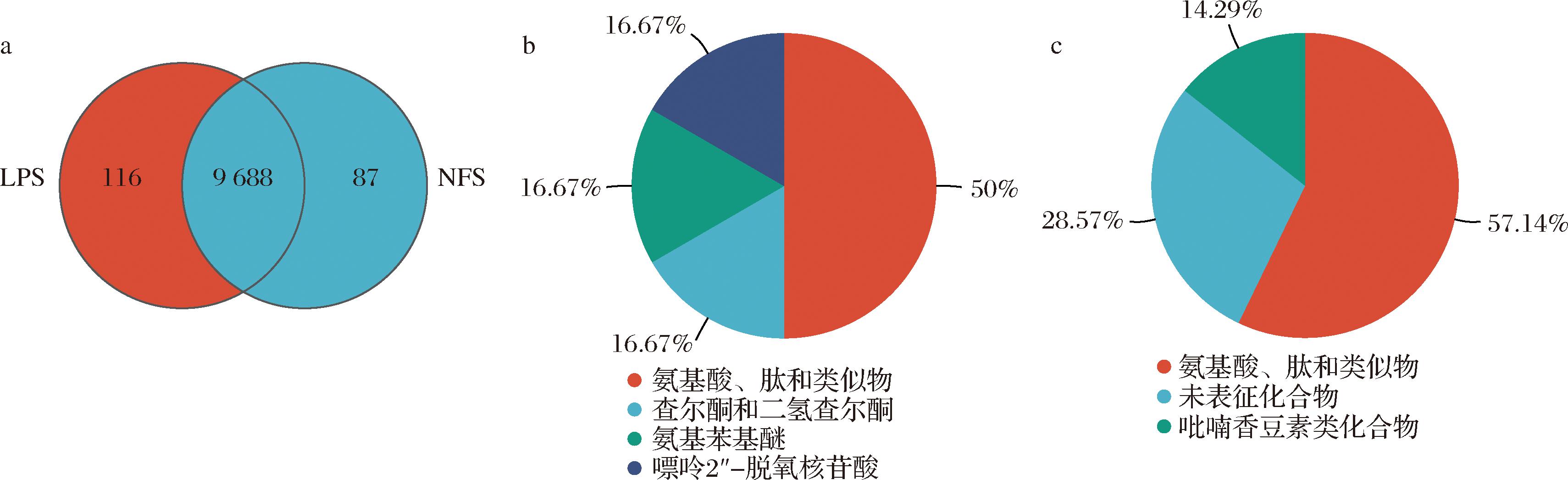
a-NFS和LPS的韦恩图;b-NFS特有代谢物饼图;c-LPS特有代谢物饼图
图2 NFS和LPS特有代谢物注释
Fig.2 Annotations on metabolites unique to NFS and LPS
将代谢物与KEGG功能通路进行比对,由图3可知,NFS和LPS中总代谢物共注释1 031条通路,与细胞过程对应的化合物数量最多,其次是生物体系统,而遗传信息处理代谢物数量最少,表明在不同发酵方式下,微生物在酸笋发酵过程中的核心都主要围绕细胞过程展开,基本不会发生遗传信息变异,稳定性较好。NFS和LPS总代谢物的代谢通路主要包括氨基酸代谢、其他次生代谢物的生物合成、生物降解和代谢、脂质代谢和化学结构转换。其中,氨基酸代谢是最富集的通路,会对酸笋风味产生一定的影响。一方面,许多氨基酸本身具有呈味特性,在酸笋发酵过程中,多种呈味氨基酸协同作用,构成酸笋独特的风味;另一方面,氨基酸是许多风味化合物的前体[10],例如氨基酸会发生脱氨、脱羧反应,生成相应的醇类,或者通过Ehrlich途径转化为醛类,都是酸笋风味的重要组成部分。因此,NFS和LPS风味来源都主要是由于氨基酸代谢。
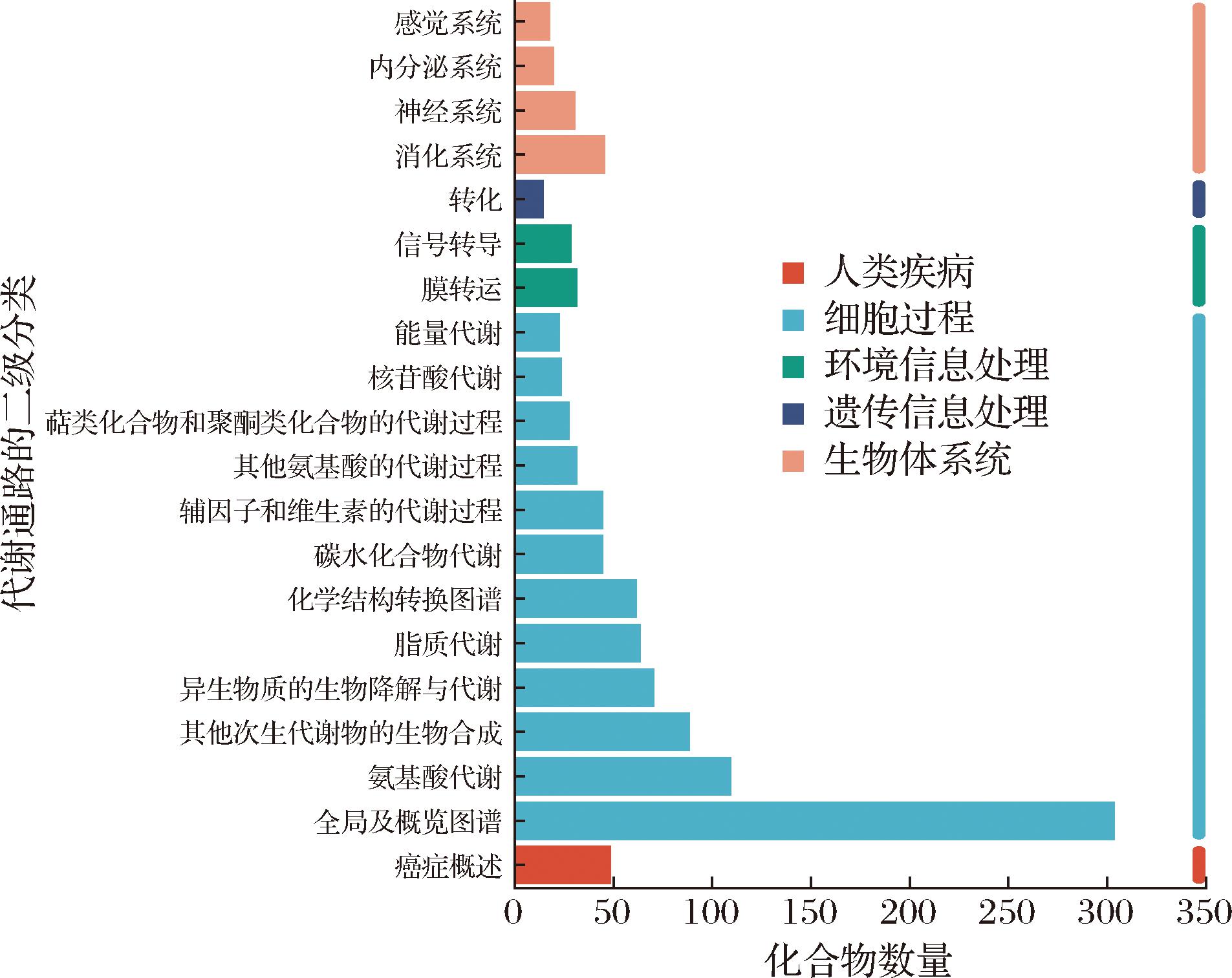
图3 NFS和LPS的KEGG通路统计柱状图
Fig.3 Bar charts for KEGG pathway statistics of LPS and NFS
2.3 LPS和NFS差异代谢物的火山图分析
在本实验中,使用单变量统计分析联合多元统计分析以及倍数变化值(fold change, FC)共同筛选差异代谢物,筛选条件为P<0.05,log2FC>1或log2FC<-1且变量投影重要性(variable importance projection,VIP)>1。由图4可知,LPS和NFS共筛选出差异代谢物523种,在阳离子模式下,上调93种,下调105种;在阴离子模式下,上调191种,下调134种,总体而言,LPS比NFS表现出更复杂、活跃的代谢方式。植物乳植杆菌作为一种益生菌,能够通过特定的代谢途径和酶系,将发酵底物转化为更多的代谢产物[11],从而增加上调代谢物的数量。值得注意的是,L-精氨酸显著下调,已有研究证明植物乳植杆菌具备通过精氨酸二氢解酶途径降解精氨酸的能力,此途径是细菌生长的重要能量来源,同时也可以保护生物体免受酸性损伤[12],在LPS中植物乳植杆菌含量显著高于NFS[9],因此L-精氨酸的显著下降可能是LPS显著抑制细菌生长,延长保质期的重要原因。
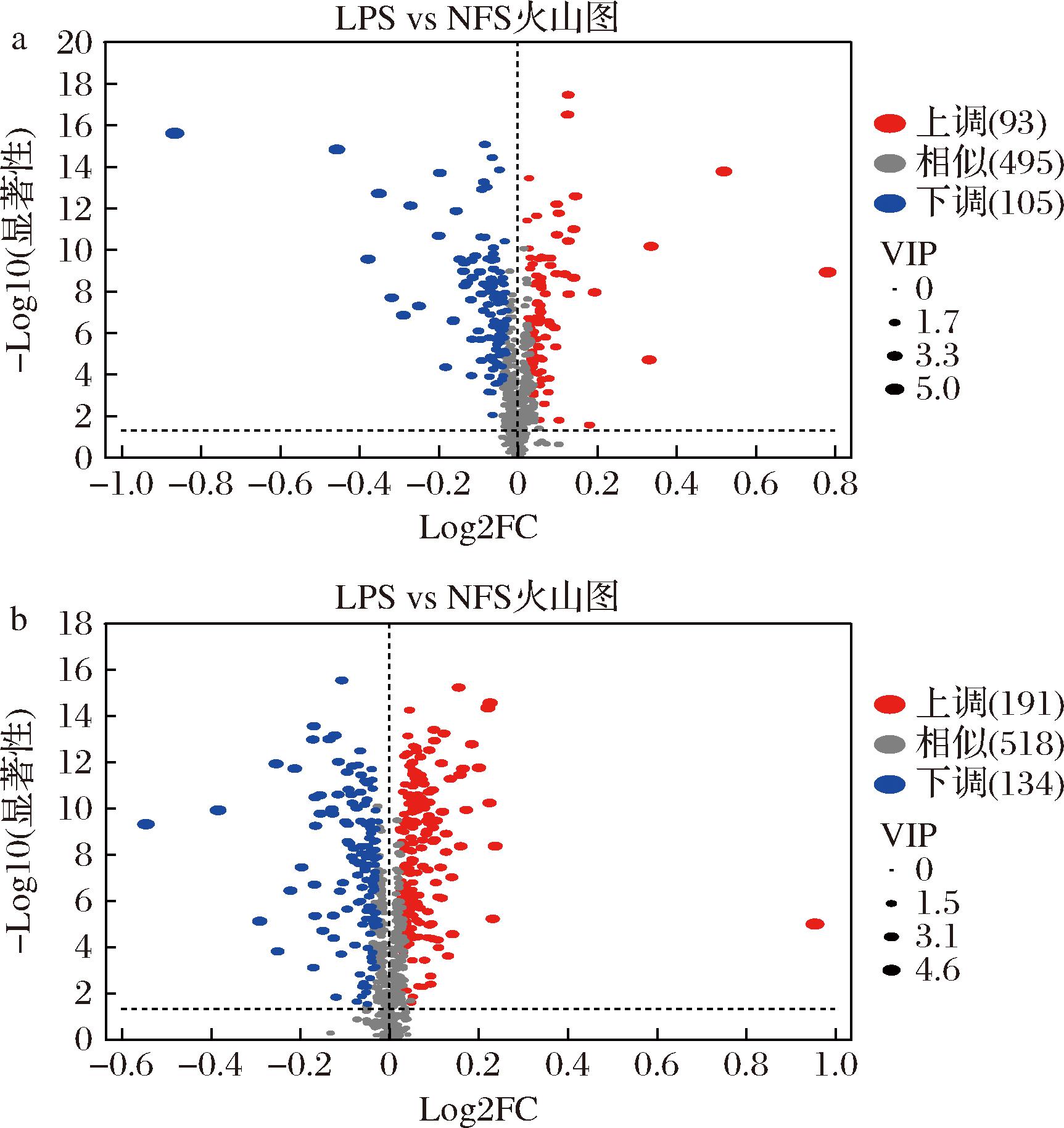
a-阳离子表;b-阴离子表
图4 NFS和LPS差异代谢物的火山图
Fig.4 Volcano plot for differential metabolites between LPS and NFS
2.4 LPS和NFS差异代谢物的筛选、分类和鉴定
采用多维统计VIP>1和单变量统计P<0.05进行差异代谢物的筛选。如图5所示,在差异代谢物中,有机酸及其衍生物(organic acids and derivatives)占19.5%,是造成酸笋酸味的主要来源[13];有机杂环化合物(organoheterocyclic compounds)占18.55%,大多数有机杂环化合物如吲哚、吡咯、呋喃等会赋予酸笋独特风味[14];脂质及类脂质分子(lipids and lipid-like molecules)占11.85%;苯丙烷类化合物和聚酮化合物占10.71%;有机含氧化合物(organic oxygen compounds)占10.52%;苯类化合物(benzenoids)占9.18%,能为酸笋带来独特的香气,是气味成分的主要贡献者[15]。上述显著差异代谢物种类,表明NFS和LPS发酵微生物的差异,具体体现在酸笋的风味、质地和香气方面。其中,有机酸及其衍生物是富集数量最多的代谢物种类,可作为NFS和LPS标志性差异代谢物种类区分2组样本。植物乳植杆菌能够利用酸笋中的碳水化合物,进一步代谢产生乳酸等有机酸。有机酸的富集使pH值快速下降,产生独特风味的同时抑制有害微生物的生长,因此在工业上可利用接种植物乳植杆菌缩短酸笋发酵时间,提高生产效率,这与BOTTHOULATH等[16]的研究结果一致。
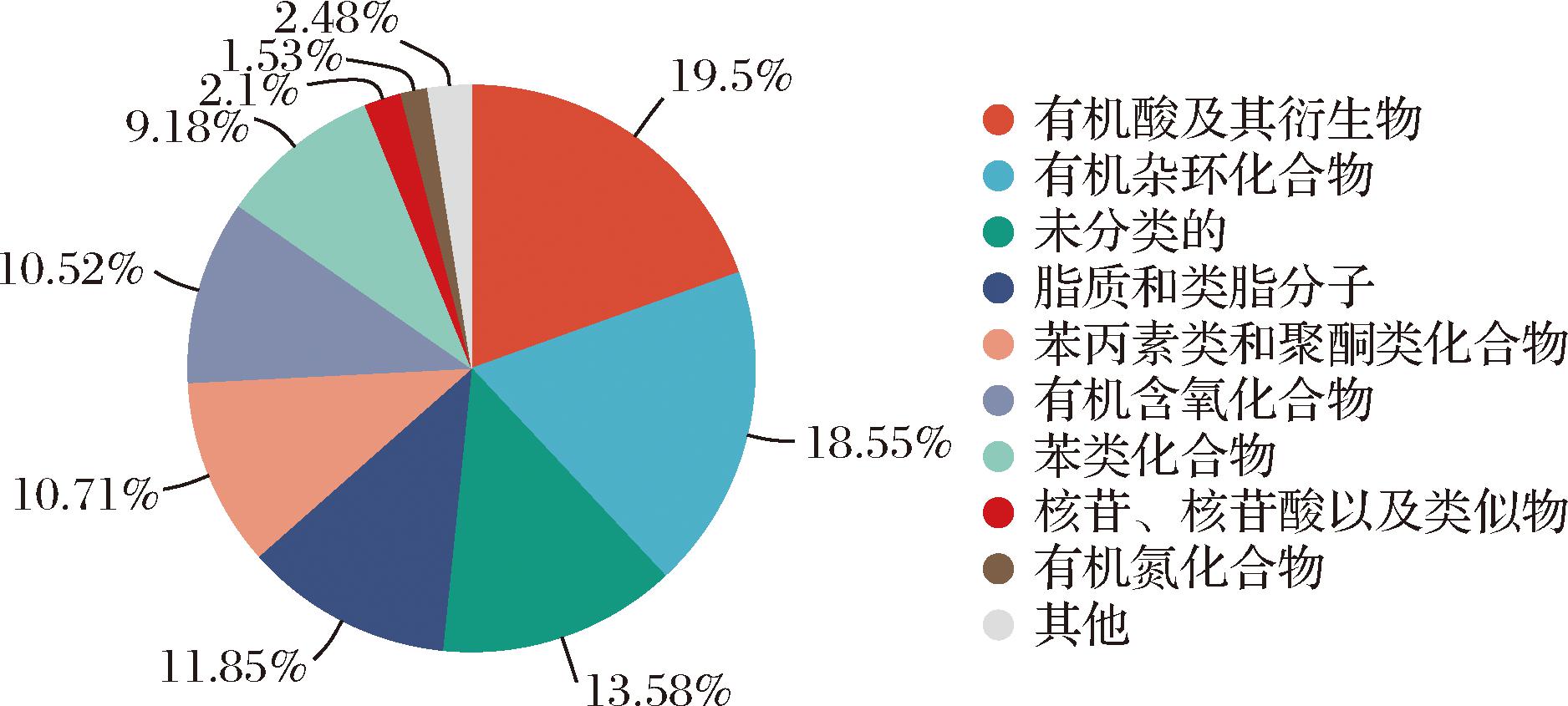
图5 NFS和LPS差异代谢物的类别
Fig.5 Categories of differential metabolites between LPS and NFS
基于PLS-DA模型,筛选出排名前30的差异代谢物,对其进行聚类分析。结果如图6所示,NFS和LPS显著差异代谢物主要分为杂环有机化合物、苯丙素类化合物和聚酮类化合物、有机酸及其衍生物、苯类化合物、脂类及类脂质分子。α-D-葡萄糖(VIP=5.73)、D-3-苯乳酸(VIP=5.73)、甲基-6-O-没食子酰-β-D-葡糖吡喃苷(VIP=5.72)在LPS中显著上调。植物乳植杆菌细胞膜上的磷酸烯醇式丙酮酸-磷酸转移酶系统可高效地将胞外的α-D-葡萄糖转运至胞内[17],提高酸笋的甜味;植物乳植杆菌在发酵过程中分泌大量D-3-苯乳酸,属于低分子质量抗真菌化合物,抗菌谱较广[18],抑制了酸笋在储存过程中的腐败变质。甲基-6-O-没食子酰-β-D-葡糖吡喃苷属于酚类化合物,与多酚氧化酶等酶类相互作用,抑制酶促褐变反应的发生,保持酸笋的色泽稳定[19]。因此,植物乳植杆菌的接种可提高酸笋的保质期和感官评价,使酸笋更具市场竞争力。下调的化合物主要为亮氨酸(VIP=5.74)、原儿茶酸(VIP=5.74)和苯甲醛(VIP=5.67)。亮氨酸和原儿茶酸都具有微苦的风味特性;苯甲醛主要以苷的形式存在于酸笋中,具有霉味和苦杏仁味[20],表明植物乳植杆菌与原有微生物菌群相互作用,可能会抑制产生苦味的微生物生长或代谢活动,从而抑制发酵酸笋中苦味物质的产生,改善酸笋风味特性。
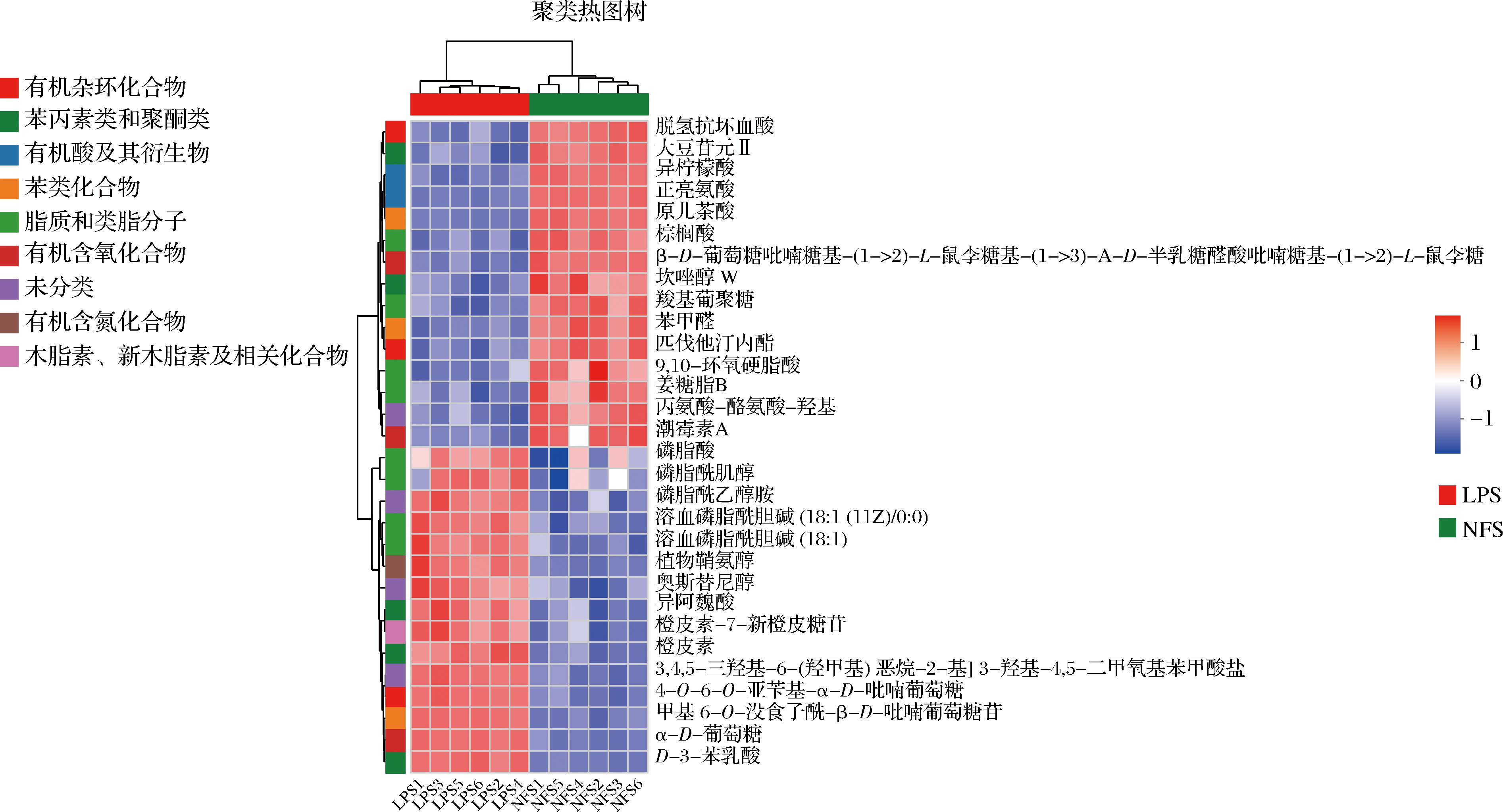
图6 NFS和LPS差异代谢物聚类热图
Fig.6 Heatmap for clustering differential metabolites between NFS and LPS
为探究NFS和LPS的代谢机制,通过KEGG数据库对所有显著差异的代谢物进行通路富集分析。共获得240种差异代谢通路,其中排在前20的代谢通路如图7所示。差异代谢物富集最多的通路是植物次生代谢物的生物合成、辅因子的生物合成、苯丙烷类化合物的生物合成和腺苷三磷酸结合盒转运蛋白(ATP-binding cassette,ABC)转运蛋白,表明这些代谢通路在酸笋发酵过程中具有重要的作用,可以通过调控这些代谢途径来调控酸笋发酵,对于深入研究酸笋发酵调控机制具有重要意义。苯丙烷类化合物的生物合成通路主要产物是部分酚类化合物和香豆素等苯丙烷类化合物,这些苯丙烷类化合物具有抗氧化、抗炎、抗菌等活性,酸笋通过植物乳植杆菌的发酵,其生物活性得到了一定提升[21];植物乳植杆菌发酵酸笋通过影响ABC转运蛋白的表达和活性,影响酸笋中多酚、黄酮等物质的运输和积累,同时植物乳植杆菌本身产生的一些代谢产物,如乳酸、乙酸等,也影响ABC转运蛋白的表达和活性,综合作用影响了酸笋的口感和营养价值[22]。
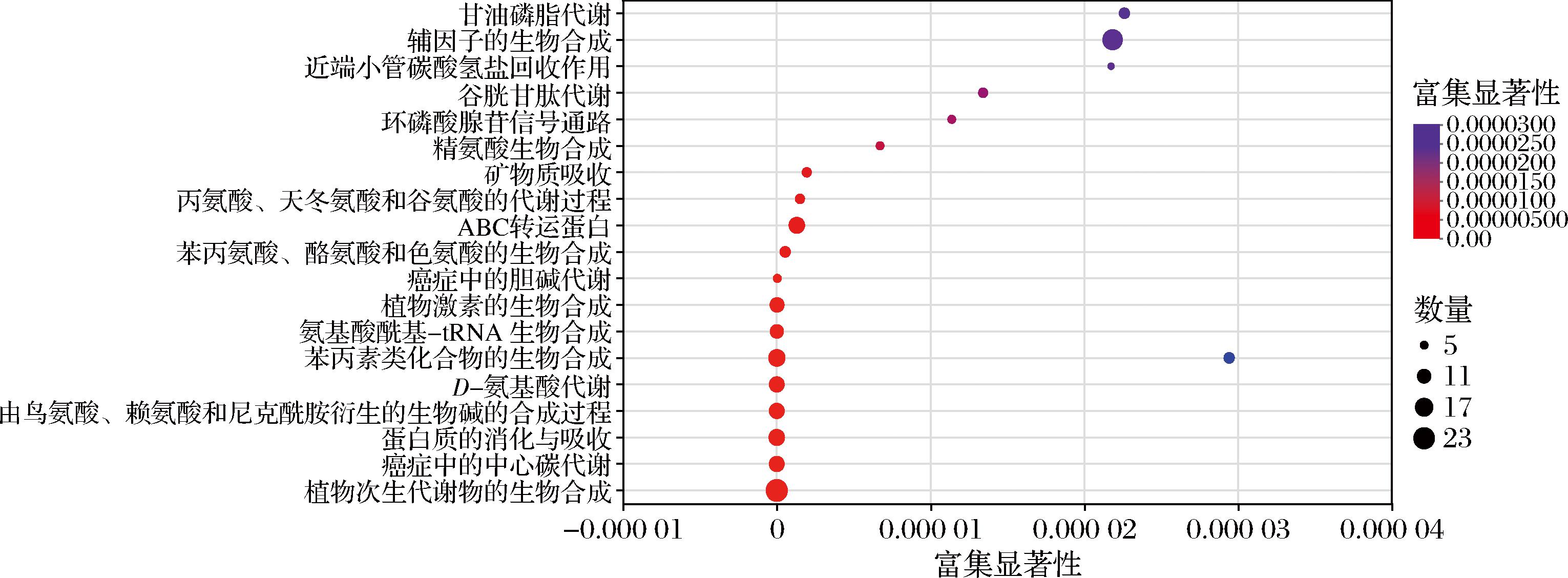
图7 NFS和LPS差异代谢物KEGG富集图
Fig.7 KEGG enrichment diagram of differential metabolites between LPS and NFS
其中植物次生代谢物的生物合成不仅是差异代谢物富集最多的通路,也是富集显著性P值最小的通路,对其通路所富集到的差异代谢物进行数据挖掘,并通过VIP评分对代谢产物进行鉴别。结果如表1所示,在此通路中,上调的有苹果酸(VIP=2.89)、苯丙酮酸(VIP=1.69)、L-鸟氨酸(VIP=1.61)、L-半胱氨酸(VIP=1.51)等共10种代谢物。下调的有L-丝氨酸(VIP=2.03)、L-赖氨酸(VIP=1.95)、2-氨基-3-甲基丁二酸(VIP=1.88)、异柠檬酸(VIP=1.51)等共13种代谢物。苹果酸能赋予酸笋愉快的酸味但略带苦味,已有研究表明酸笋中植物乳植杆菌与苹果酸的产生呈正相关[23]。L-丝氨酸和L-赖氨酸分别是甜味氨基酸和鲜味氨基酸。异柠檬酸具有柔和的酸味,是三羧酸循环中的重要组成成分,为细胞提供充足能量。在三羧酸循环中,异柠檬酸在异柠檬酸脱氢酶的作用下,发生氧化脱羧反应,生成α-酮戊二酸作为氨基基团受体[24],利用氨基转移酶转氨反应生成苯丙酮酸,提高苯乳酸的产量[25],抑制多种食源性致病菌且对酸热较稳定,因此植物乳植杆菌的接种可减少酸笋制备过程中化学防腐剂的含量并延长保质期[26]。
表1 LPS和NFS显著差异代谢通路中的代谢物
Table 1 Metabolites in the significantly different metabolic pathways between LPS and NFS
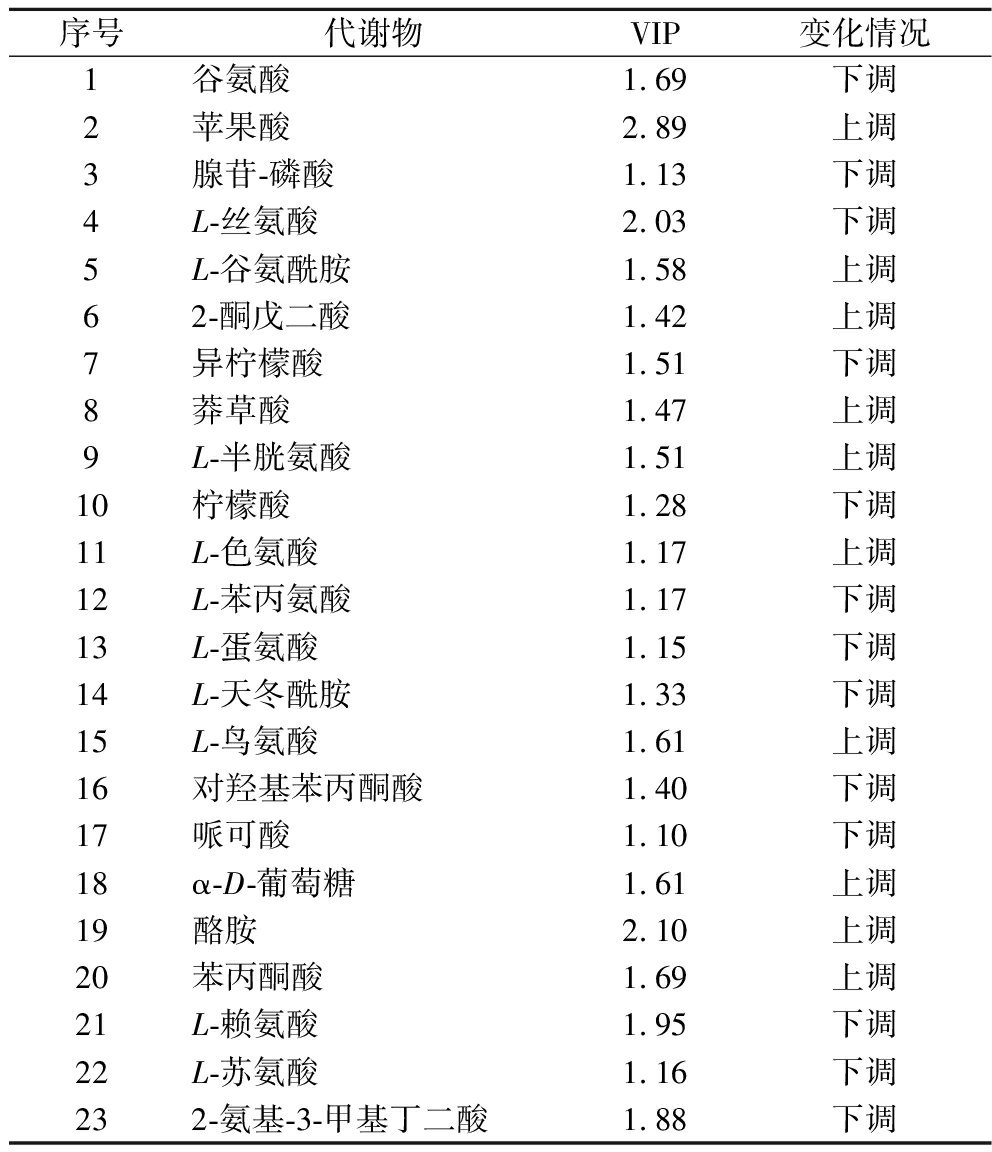
序号代谢物VIP变化情况1谷氨酸 1.69下调2苹果酸 2.89上调3腺苷-磷酸 1.13下调4L-丝氨酸 2.03下调5L-谷氨酰胺 1.58上调62-酮戊二酸 1.42上调7异柠檬酸 1.51下调8莽草酸 1.47上调9L-半胱氨酸 1.51上调10柠檬酸1.28下调11L-色氨酸1.17上调12L-苯丙氨酸 1.17下调13L-蛋氨酸 1.15下调14L-天冬酰胺 1.33下调15L-鸟氨酸 1.61上调16对羟基苯丙酮酸 1.40下调17哌可酸 1.10下调18α-D-葡萄糖 1.61上调19酪胺 2.10上调20苯丙酮酸 1.69上调21L-赖氨酸 1.95下调22L-苏氨酸 1.16下调232-氨基-3-甲基丁二酸1.88下调
利用KEGG拓扑学分析代谢物在代谢通路中的作用大小,由图8可知,磷壁酸生物合成通路颜色较深,相对重要性最大为1,表明磷壁酸生物合成途径在NFS和LPS之间存在显著差异,且在代谢网络中具有非常重要的地位,丰富了不同发酵方式下对酸笋差异代谢途径的认识[27]。植物乳植杆菌作为革兰氏阳性菌,细胞壁含有磷壁酸,在接种发酵过程中,植物乳植杆菌大量繁殖,磷壁酸合成通路活跃,磷壁酸可以维持细胞结构稳定,调节细胞内外物质交换,抵御外界不利因素,这可能是LPS具有良好发酵耐受性[28]。丙氨酸、天冬氨酸和谷氨酸代谢相对重要性较大,甘氨酸、丝氨酸和苏氨酸代谢的富集显著性最大,说明其在2组样本间也存在一定差异。植物乳植杆菌通过影响原有微生物种类和数量,使微生物发酵利用氨基酸偏好不同,导致2种氨基酸代谢通路成为主要作用部分。综上,植物乳植杆菌影响原有微生物代谢途径,对上述3条通路作用最大,在NFS和LPS代谢差异中具有重要作用。
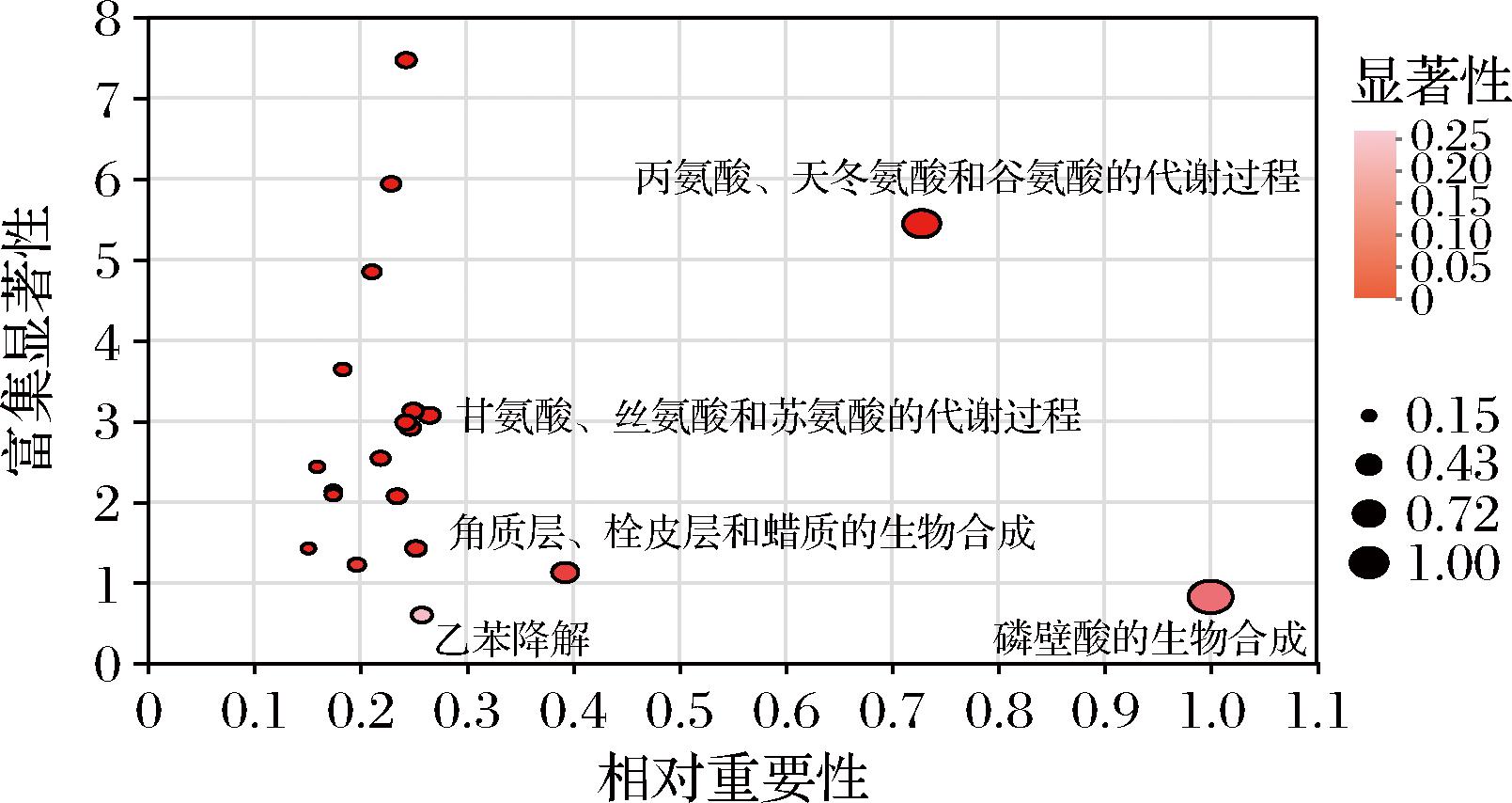
图8 NFS和LPS差异代谢物的KEGG拓扑学分析图
Fig.8 KEGG topological analysis diagram for differential metabolites between LPS and NFS
将KEGG拓扑学分析中所富集到的化合物与表1进行对比,结果如表2所示。NFS和LPS中重要差异代谢物主要集中在丙氨酸、天冬氨酸和谷氨酸代谢,甘氨酸、丝氨酸和苏氨酸代谢通路中,表明氨基酸代谢途径是NFS和LPS主要差异代谢途径,植物乳植杆菌主要通过影响氨基酸代谢途径,引起代谢物差异。上调的分别为L-谷氨酰胺、L-色氨酸、2-酮戊二酸和L-半胱氨酸。植物乳植杆菌可分泌大量的芳香氨基酸氨基转移酶和吲哚脱氢酶,通过这些酶的作用,使色氨酸代谢生成一系列吲哚化合物,作为酸笋中含量最高的挥发性风味物质之一[29];L-半胱氨酸含有巯基,在微生物酶的作用下,会生成多种含硫香气化合物。下调的是谷氨酸、L-丝氨酸、L-天冬酰胺、L-苏氨酸、2-氨基-3-甲基丁二酸和柠檬酸。谷氨酸是酸笋呈现鲜味的关键物质,下降原因可能是由于植物乳植杆菌分泌谷氨酸脱氢酶使谷氨酸分解产生γ-氨基丁酸[30];L-天冬酰胺可水解生成具有一定鲜味的天冬氨酸,而柠檬酸能赋予酸笋清爽、开胃的口感。综上,LPS具有更丰富的香气和风味,但是其鲜味及风味丰富度较NFS有所降低,在工艺上生产LPS,可以对上述代谢物进行合成途径优化,赋予酸笋多种风味。
表2 NFS和LPS中重要代谢物
Table 2 Important metabolites in NFS and LPS
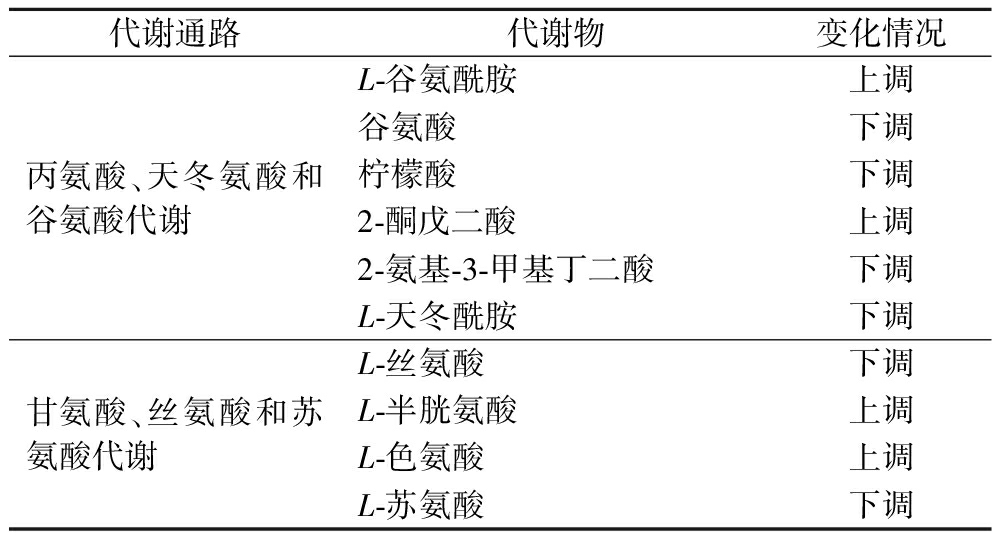
代谢通路代谢物 变化情况丙氨酸、天冬氨酸和谷氨酸代谢L-谷氨酰胺 上调谷氨酸 下调柠檬酸 下调2-酮戊二酸 上调2-氨基-3-甲基丁二酸 下调L-天冬酰胺 下调甘氨酸、丝氨酸和苏氨酸代谢L-丝氨酸 下调L-半胱氨酸 上调L-色氨酸 上调L-苏氨酸 下调
3 结论
本研究利用液相色谱-质谱联用技术研究NFS和LPS差异代谢物及代谢通路。研究表明,NFS和LPS特有代谢物种类都主要是氨基酸、肽及其类似物。氨基酸代谢是NFS和LPS总代谢物富集数量最多的通路,赋予酸笋独特的风味。LPS与NFS相比,差异代谢物共523种,显著差异代谢物主要是α-D-葡萄糖、D-3-苯乳酸、亮氨酸、苯甲醛,提高了LPS的感官质量。根据KEGG功能通路进行NFS和LPS差异代谢物通路分析,L-半胱氨酸、谷氨酸、L-丝氨酸、2-氨基-3-甲基丁二酸是NFS和LPS差异代谢物的关键调控点,通过对上述代谢物进行控制,为酸笋的品质调控提供理论基础。
[1] WANG D W, WANG Y, LAN H B, et al.Enhanced production of γ-aminobutyric acid in litchi juice fermented by Lactobacillus plantarum HU-C2 W[J].Food Bioscience, 2021, 42:101155.
[2] 李昕诺, 吴宇辉, 吴良如, 等.基于宏基因组学揭示自然发酵与植物乳杆菌接种发酵酸笋中微生物代谢及关键风味基因[J].食品与发酵工业, 2025, 51(7):167-176.
LI X N, WU Y H, WU L R, et al.Revealing microbial metabolism and key flavor genes in natural fermented and Lactobacillus plantarum inoculated fermented Suansun based on macrogenomics[J].Food and Fermentation Industries, 2025, 51(7):167-176.
[3] HWANG H, LEE J H.Characterization of arginine catabolism by lactic acid bacteria isolated from kimchi[J].Molecules, 2018, 23(11):3049.
[4] LE B, ANH P T N, YANG S H.Enhancement of the anti-inflammatory effect of mustard kimchi on RAW264.7 macrophages by the Lactobacillus plantarum fermentation-mediated generation of phenolic compound derivatives[J].Foods, 2020, 9(2):181.
[5] ZHANG W J, YU X C, XIN L Y, et al.Effect of rapid fermentation on the quality of northeastern sauerkraut analyzed based on HSSPME-GC-MS and LC-MS[J].LWT, 2024, 198:116005.
[6] GUAN Q Q, ZHENG W D, MO J L, et al.Evaluation and comparison of the microbial communities and volatile profiles in homemade Suansun from Guangdong and Yunnan provinces in China[J].Journal of the Science of Food and Agriculture, 2020, 100(14):5197-5206.
[7] HU T, ZHU J H, CHAI Y H, et al.Characterization of microbial diversity and important off-odor compounds in fermented Ma bamboo shoots (Dendrocalamus latiflorus Munro)[J].LWT, 2023, 188:115378.
[8] QIN X Y, XIONG T, XIONG S J, et al.Metatranscriptomics unravel the formation mechanism of key flavors during the natural fermentation of Suansun, a Chinese traditional fermented bamboo shoot[J].Food Bioscience, 2024, 57:103436.
[9] XUE B J, YOU Y M, DU M Y, et al.Metagenomic analysis of Lactobacillus plantarum DACN768 inoculation effects on volatile flavor compounds, microbial succession, and flavor metabolic network in Suansun[J].Food Research International, 2025, 199:115382.
[10] CHEN C X, CHENG G G, LIU Y P, et al.Correlation between microorganisms and flavor of Chinese fermented sour bamboo shoot:Roles of Lactococcus and Lactobacillus in flavor formation[J].Food Bioscience, 2022, 50:101994.
[11] DA SILVA SABO S, VITOLO M, GONZ LEZ J M D, et al.Overview of Lactobacillus plantarum as a promising bacteriocin producer among lactic acid bacteria[J].Food Research International, 2014, 64:527-536.
LEZ J M D, et al.Overview of Lactobacillus plantarum as a promising bacteriocin producer among lactic acid bacteria[J].Food Research International, 2014, 64:527-536.
[12] ARENA M E, SAGUIR F M, MANCA DE NADRA M C.Arginine dihydrolase pathway in Lactobacillus plantarum from orange[J].International Journal of Food Microbiology, 1999, 47(3):203-209.
[13] SINGHAL P, BAL L M, SATYA S, et al.Bamboo shoots:A novel source of nutrition and medicine[J].Critical Reviews in Food Science and Nutrition, 2013, 53(5):517-534.
[14] GUO R C, YU F T, WANG C H, et al.Determination of the volatiles in fermented bamboo shoots by head space-solid-phase micro extraction (HS-SPME) with gas chromatography-olfactory-mass spectrometry (GC-O-MS) and aroma extract dilution analysis (AEDA)[J].Analytical Letters, 2021, 54(7):1162-1179.
[15] MARTIN V, GIORELLO F, FARI A L, et al.De novo synthesis of benzenoid compounds by the yeast Hanseniaspora vineae increases the flavor diversity of wines[J].Journal of Agricultural and Food Chemistry, 2016, 64(22):4574-4583.
A L, et al.De novo synthesis of benzenoid compounds by the yeast Hanseniaspora vineae increases the flavor diversity of wines[J].Journal of Agricultural and Food Chemistry, 2016, 64(22):4574-4583.
[16] BOTTHOULATH V, DALMACIO I F, ELEGADO F B.Physico-chemical and functional properties of the Lao fermented bamboo shoots (Nor Mai Som) inoculated with potential probiotic bacteria, Pediococcus pentosaceus BBS1 and Lactiplantibacillus plantarum BBS13[J].Food Chemistry Advances, 2024, 5:100803.
[17] KLEEREBEZEM M, BOEKHORST J, VAN KRANENBURG R, et al.Complete genome sequence of Lactobacillus plantarum WCFS1[J].Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(4):1990-1995.
[18] PREMA P, SMILA D, PALAVESAM A, et al.Production and characterization of an antifungal compound (3-phenyllactic acid) produced by Lactobacillus plantarum strain[J].Food and Bioprocess Technology, 2010, 3(3):379-386.
[19] CHUNGSATAPATHCHAI J, JIRAPAKKUL W.Changes in browning, phenolic, quinone and lignin contents during storage of fermented bamboo shoot in different packagings[J].Environmental Science, Agricultural and Food Sciences, 2008, 136999464.
[20] 朱照华. 酸笋的营养成分检测及其主要风味物质的研究[D].南宁:广西大学, 2014.
ZHU Z H.Study on fermented bamboo shoot nutrition and flavor components[D].Nanning:Guangxi University, 2014.
[21] 叶峥, 张江宁.基于非靶向代谢组学探究不同菌种发酵骏枣汁的代谢差异分析[J].食品与发酵工业, 2025, 51(11):81-89.
YE Z, ZHANG J N.Non-targeted metabolomics analysis on metabolic differences among Ziziphus jujuba Mill.juices fermented by different strains[J].Food and Fermentation Industries, 2025, 51(11):81-89.
[22] ZHANG H H, ZENG N D, FENG Q R, et al.New mechanistic insights into PAHs transport across wheat root cell membrane:Evidence for ABC transporter mediation[J].Science of The Total Environment, 2023, 859:160251.
[23] 马艺荧. 东北酸菜发酵过程中细菌多样性及有机酸的变化规律[D].哈尔滨:东北农业大学, 2019.
MA Y Y.Changes of bacterial diversity and organic acids during fermentation of Northeast sauerkraut[D].Harbin:Northeast Agricultural University, 2019.
[24] YU S H, JIANG H Y, JIANG B, et al.Characterization of D-lactate dehydrogenase producing D-3-phenyllactic acid from Pediococcus pentosaceus[J].Bioscience, Biotechnology, and Biochemistry, 2012, 76(4):853-855.
[25] 李兴峰, 江波, 潘蓓蕾, 等.苯丙氨酸及苯丙酮酸对Lactobacillus sp.SK007合成苯乳酸的影响[J].过程工程学报, 2007, 7(6):1202-1206.
LI X F, JIANG B, PAN B L, et al.Effects of phenylalanine and phenylpyruvic acid on biosynthesis of phenyllactic acid with Lactobacillus sp.SK007[J].The Chinese Journal of Process Engineering, 2007, 7(6):1202-1206.
[26] ZHANG J M, ZHANG C C, LEI P, et al.Isolation, purification, identification, and discovery of the antibacterial mechanism of ld-phenyllactic acid produced by Lactiplantibacillus plantarum CXG9 isolated from a traditional Chinese fermented vegetable[J].Food Control, 2022, 132:108490.
[27] WU Y H, YOU Y M, WU L R, et al.Integrated metagenomics and metatranscriptomics analyses reveal the impacts of different Lactiplantibacillus plantarum strains on microbial communities and metabolic profiles in pickled bamboo shoots[J].Food Chemistry, 2025, 464:141772.
[28] LU H H, HUANG C J, YU K N, et al.Effects of mixed inoculation of Leuconostoc citreum and Lactobacillus plantarum on Suansun (Sour bamboo shoot) fermentation[J].Food Bioscience, 2022, 47:101688.
[29] PAN T, PEI Z M, FANG Z F, et al.Uncovering the specificity and predictability of tryptophan metabolism in lactic acid bacteria with genomics and metabolomics[J].Frontiers in Cellular and Infection Microbiology, 2023, 13:1154346.
[30] ZHAO N, ZHANG C C, YANG Q, et al.Selection of taste markers related to lactic acid bacteria microflora metabolism for Chinese traditional Paocai:A gas chromatography-mass spectrometry-based metabolomics approach[J].Journal of Agricultural and Food Chemistry, 2016, 64(11):2415-2422.