作为白酒酿造过程中的核心因素,大曲不仅富含多样化的微生物群落、高效的功能性酶系统和丰富的风味前体物质,而且对酿造的启动和顺利进行起着重要作用[1]。细菌群落作为大曲体系不可或缺的组成部分,其功能特性一直是研究者们关注的焦点。例如,LIU等[2]使用自主分离的枯草芽孢杆菌(Bacillus subtilis)D39进行强化大曲的制作发现,大曲的糖化能力、液化能力和纤维素酶活性显著提高。MI等[3]对从浓香大曲中分离出的菌株进行功能性筛选,结果发现大肠杆菌(Escherichia coli)S16具有良好的产酯和抗氧化活性,B. subtilis在发酵过程中增加了酯类物质的含量,包括乙酸乙酯、辛酸乙酯等。由此可见,细菌类群对大曲的理化特性及风味物质具有显著影响。温度是细菌群落演替的主要驱动因素,根据发酵的峰值温度,大曲被划分为低温大曲(40~50 ℃)、中温大曲(50~55 ℃)、中高温大曲(55~60 ℃)和高温大曲(60~70 ℃)共4种类型[4]。不同类型大曲之间,细菌群落的组成存在显著差异[5-6],这种差异进一步导致了白酒风格的多样化。因此,深入探究大曲的细菌群落结构特征,对于实现大曲标准化生产以及提升白酒品质至关重要。
在这个高通量测序时代,使用多样化测序技术已成为探索白酒酿造过程中微生物结构的主流方式。PacBio单分子实时(single molecule real-time, SMRT)测序技术因其准确性和长读长测序等多种优势[7]而被广泛用于全面评估复杂酿造体系的微生物群落结构。例如ZHANG等[8]对不同等级高温大曲微生物群落结构进行研究发现,普通等级大曲组鸡葡萄球菌(Staphylococcus gallinarum)和大曲岩石芽孢杆菌(Scopulibacillus daqui)的相对丰度显著高于优等大曲组(P<0.05),而洋葱伯克霍尔德菌(Burkholderia cenocepacia)的相对丰度显著低于优等大曲组(P<0.05)。XIANG等[9]对不同地区低温大曲微生物群落结构进行研究发现,柠檬明串珠菌(Leuconostoc citreum)和扣囊复膜孢酵母(Saccharomycopsis fibuligera)是山西省太原市低温大曲的生物标志物,融合魏斯氏菌(Weissella confusa)和嗜热子囊菌(Thermoascus aurantiacus)是湖北省随州市低温大曲的生物标志物。HAN等[10]对不同类型大曲细菌群落进行研究发现,低温大曲组以成团泛菌(Pantoea agglomerans,15.92%)和S. gallinarum(15.17%)为主,中温大曲以粘质沙雷氏菌(Serratia marcescens,20.14%)和S. gallinarum(17.41%)为主,高温大曲以大曲慢生芽孢杆菌(Lentibacillus daqui,16.23%)和Oceanobacillus caeni(10.48%)为主。这些研究表明,PacBio SMRT测序技术可以帮助揭示大曲种水平的微生物群落组成。
现有研究虽已解析多地大曲细菌群落结构,但针对山东省德州市大曲细菌多样性的研究仍显不足。德州市地处鲁西北平原,京杭大运河畔,属温带季风气候,独特的地理位置和气候条件可能赋予当地大曲细菌群落独特的地域特征。基于此,本研究从山东省德州市某酒厂收集了10份大曲样品,包括2种主要类型(中高温大曲和高温大曲)。首先,利用PacBio SMRT测序技术对大曲样品宏基因组的16S全长序列进行测序,并基于SILVA数据库,揭示2种类型大曲的细菌物种差异。其次,采用微生物纯培养技术对大曲样品的可培养微生物进行分离保藏,基于GenBank数据库,揭示2种类型大曲可培养微生物的差异。本研究深入解析了不同类型大曲细菌群落结构的差异,以期为驱动不同类型白酒独特风味特征的形成提供数据支持。
1 材料与方法
1.1 材料与试剂
TGuide S96磁珠法土壤/粪便基因组DNA提取试剂盒,天根生化科技(北京)有限公司;引物16S-F/16S-R,北京百灵克生物科技有限责任公司;Agencourt AMPure XP核酸纯化试剂盒,贝克曼库尔特生物科技(苏州)有限公司;MRS(de Man,Rogosa and Sharpe)培养基、营养琼脂(nutrient agar, NA)培养基,北京奥博星生物技术有限责任公司;引物27F/1495R,武汉天一辉远生物科技有限公司。
1.2 仪器与设备
BF-10小型高速粉碎机,河北本辰科技有限公司;8411型电动振筛机,绍兴市上虞星星仪器设备有限公司;QYC-2102C全温培养摇床,上海新苗医疗器械制造有限公司;DG250厌氧工作站(80% N2、10% H2和10% CO2),英国Don Whitley公司;KENT-N电热恒温培养箱,广州市康恒仪器有限公司;Veriti 96-Well梯度基因扩增仪,美国Applied Biosystems公司;R930机架式服务器,美国DELL公司。
1.3 实验方法
1.3.1 中高温和高温大曲样品采集和制备
样本采集地点位于山东省德州市(东经115°45′—117°36′、北纬36°24′25″—38°0′32″),本研究选取了该地区某知名酒厂的2种类型大曲:中高温和高温大曲。具体而言,从成品曲曲房四周及中心5个点各选取1个完整曲块样品,总共收集了5个中高温大曲和5个高温大曲,分别标记为ZGW1~5和GW1~5。所有样品被立即运送到实验室并进行粉碎处理,过40目筛混匀后,贮存在-20 ℃冰箱以进行下一步分析。
1.3.2 PacBio SMRT测序
根据制造商的说明,使用TGuide S96磁珠法土壤/粪便基因组DNA提取试剂盒从10份大曲样品中提取总DNA。参考DU等[11]的方法,使用含有Barcode的16S全长引物对16S-F(5′-AGRGTTTGATYNTGGCTCAG-3′)与16S-R(5′-TASGGHTACCTTGTTASGACTT-3′)对目标区域进行PCR,扩增产物经Agencourt AMPure XP试剂盒纯化后,由北京百迈客生物科技有限公司进行PacBio SMRT测序。
1.3.3 生物信息学分析
首先,使用SMRT-Link分析软件对原始数据进行环形一致性序列(circular consensus sequencing, CCS)的筛选,去除正向和反向引物后,依据长度和平均质量对序列进行过滤和修剪,从而获得高质量序列。在100%序列同一性条件下,使用PyNAST工具对高质量序列进行比对,以获得代表性序列。随后,采用UCLUST算法,以97%的相似性将代表性序列进行操作分类单元(operational taxonomic units, OTU)划分,并使用Chimera Slayer工具去除代表性OTU中的嵌合体序列。基于SILVA数据库,依据伯杰氏分类法,在界、门、纲、目、科、属和种水平上对每个OTU代表序列的分类信息进行注释,分类阈值最低为80%。基于QIIME软件,使用多样性插件计算大曲样本的α和β多样性指数。采用克鲁斯卡尔-沃利斯检验(Kruskal-Wallis test)确定不同分组α多样性指数是否存在显著差异,基于加权和非加权Unifrac距离评估β多样性,并通过主成分坐标分析(principal coordinates analysis, PCoA)进行可视化,采用置换多元方差分析(permutational multivariate analysis of variance, PERMANOVA)确定不同分组β多样性指数是否存在显著差异。最后,使用PICRUSt软件结合UniRef 90数据库进行代谢途径的注释,并利用直系同源蛋白数据库(clusters of orthologous groups of proteins, COG)进行细菌基因功能的注释。
1.3.4 可培养细菌的分离和保藏
将10 g大曲粉末样品与90 mL无菌0.85%(质量分数)生理盐水溶液充分均质30 min后,吸取1 mL所得匀浆进行10倍梯度稀释,至稀释度达到10-6。取0.1 mL稀释度为10-6~10-3的稀释液,使用涂布棒涂布于NA和MRS固体培养基上,分别置于30 ℃培养箱和37 ℃厌氧工作站中培养48~72 h。选取具有不同菌落形态的单菌落,在NA和MRS固体培养基上进行传代培养,经3次纯化后,挑取单菌落使用30%(体积分数)的甘油进行保藏。
1.3.5 可培养细菌分离株的鉴定
参考TIAN等[12]的方法,使用十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide, CTAB)方法提取细菌菌株的DNA。使用通用引物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1495R(5′-ACGGTTACCTTGTTACGACTT-3′)进行PCR,扩增产物由上海赛恒生物科技有限公司进行测序。将返回的测序结果与国家生物技术信息中心(National Center for Biotechnology Information, NCBI)的GenBank序列数据库进行BLAST比对搜索。最后通过MEGA 7.0软件,使用邻接法(neighbor-joining method)绘制系统发育树,以确定分离株的分类学地位。
1.3.6 数据处理
使用MEGA 7.0结合R软件包“treeio”和“ggtree”进行系统发育树的绘制;使用R软件包“VennDiagram”进行OTU韦恩图的绘制;使用Prism软件进行α多样指数、差异物种和差异功能类群柱形图的绘制;使用R软件包“ggplot2”进行PCoA图的绘制;使用Origin 2018软件进行优势门、属、种和分离株多样性柱形图的绘制;使用R软件包“microeco”进行线性判别分析(linear discriminant analysis effect size, LEfSe)柱形图的绘制;使用R软件包“psych”结合Gephi软件进行共现性网络图的绘制;使用R软件包“corrplot”进行差异代谢通路热图的绘制。
2 结果与分析
2.1 中高温和高温大曲样品细菌多样性分析
基于处理后的106 366条高质量16S序列,本研究首先对2种类型大曲的细菌多样性进行了对比分析,结果如图1所示。
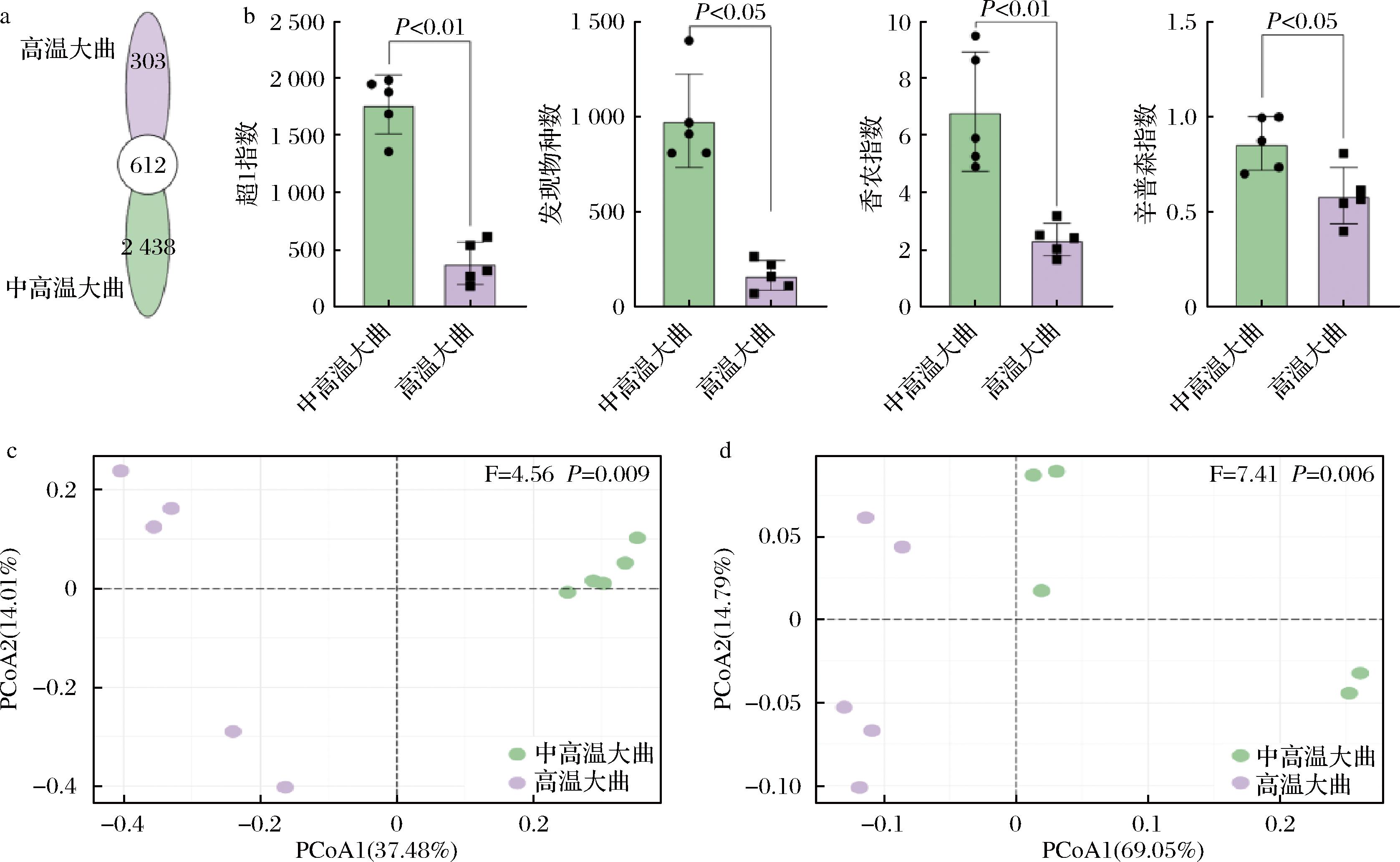
a-OTU韦恩图;b-α多样指数性分析;c-非加权Unifrac的PCoA结果;d-加权Unifrac的PCoA结果
图1 中高温和高温大曲细菌群落多样性分析
Fig.1 Analysis of bacterial community diversity in medium-high- and high-temperature Daqu
以相似度≥97%对10个大曲样品的16S序列进行OTU聚类,共获得3 353个OTU。由图1-a可知,中高温大曲组中存在2 438个独特OTU,高温大曲组中存在303个独特OTU,表明2种类型大曲的细菌群落结构存在明显差异,且中高温大曲物种更丰富。由图1-b可知,采用α多样性指数对2类大曲群落丰富度和多样性差异进行验证发现,中高温大曲细菌群落的平均超1指数和发现物种数分别为1 773和977,显著高于高温大曲的382和166(P<0.05),同时中高温大曲细菌群落的香农和辛普森指数分别为6.85和0.86,显著高于高温大曲的2.35和0.59(P<0.05),表明中高温大曲具有更高的细菌群落丰富度和多样性。由图1-c可知,采用基于加权和非加权Unifrac距离的PCoA对2类大曲群落结构差异进行验证发现,中高温和高温大曲组呈现显著的空间分离(P<0.01),表明两者细菌群落结构存在显著差异。作为白酒酿造过程中的唯一发酵剂,大曲通常以小麦为原料,在开放环境中通过固态自发发酵过程生产,因此环境条件(如温度、湿度、氧气浓度等)的变化能够显著影响大曲中微生物群落的多样性[13]。
2.2 中高温和高温大曲样品细菌门、属和种水平群落组成
经SILVA数据库比对后,将平均相对含量>1%的门、属和种,定义为优势门、属和种,将其他平均相对含量<1%的物种归类为“others”,未鉴定到具体分类的物种被定义为“unclassified”,基于门、属和种水平对2种类型大曲样品的细菌菌群结构分析结果如图2所示。
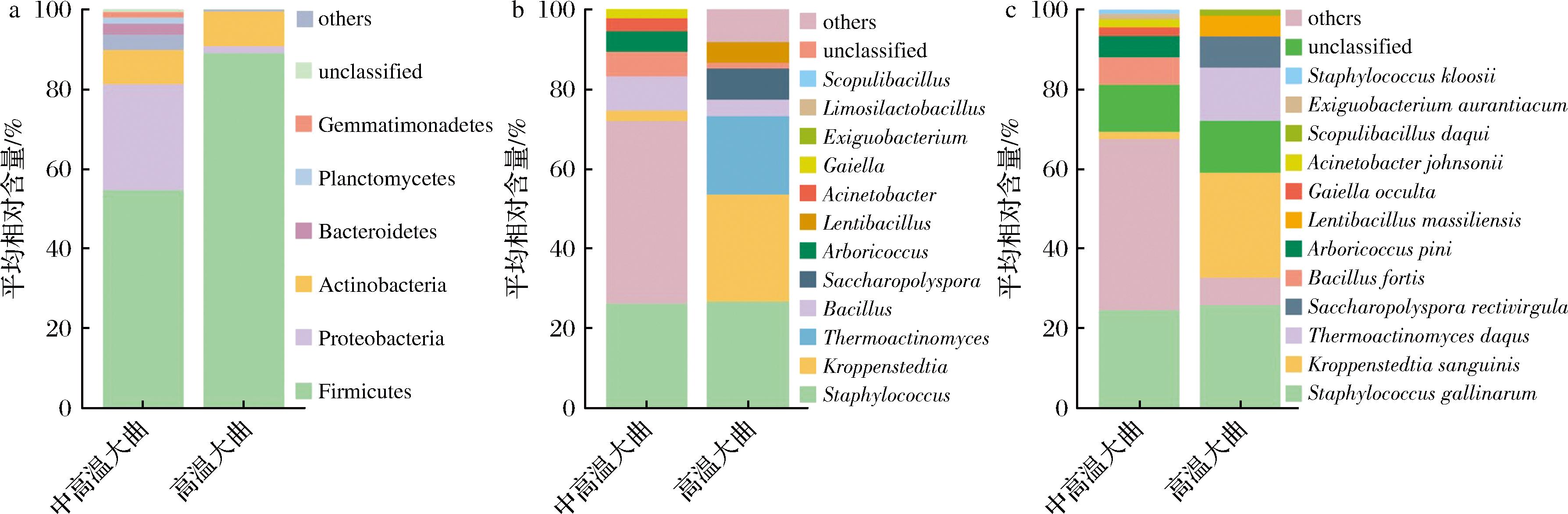
a-门水平;b-属水平;c-种水平
图2 中高温和高温大曲细菌群落结构分析
Fig.2 Analysis of bacterial community structure in medium-high- and high-temperature Daqu
由图2-a可知,在门水平上,高温大曲组样品中优势细菌门有3个,分别为厚壁菌门(Firmicutes,88.98%)、放线菌门(Actinobacteria,8.62%)和变形菌门(Proteobacteria,1.80%)。中高温大曲组样品中优势细菌门有6个,与高温大曲相比,中高温大曲明显增加的优势细菌门包括变形菌门(Proteobacteria,26.59%)、拟杆菌门(Bacteroidetes,2.67%)、浮霉菌门(Planctomycetes,1.68%)和芽单胞菌门(Gemmatimonadetes,1.24%),而厚壁菌门(Firmicutes,54.63%)、放线菌门(Actinobacteria,8.55%)的平均相对含量均明显偏低。由图2-b可知,在属水平上,中高温大曲组样品主要以葡萄球菌属(Staphylococcus)和芽孢杆菌属(Bacillus)为主,其平均相对含量分别为26.43%和8.54%,高温大曲组样品主要以克罗彭斯特菌属(Kroppenstedtia)、Staphylococcus、高温放线菌属(Thermoactinomyces)为主,其平均相对含量分别为26.81%、26.78%和19.72%。
由图2-c可知,在种水平上,中高温大曲组样品中共检测出8个优势细菌种,其中S. gallinarum是该组样品中的优势丰富细菌种,平均相对含量为24.70%。作为大多数传统发酵食品中较为常见的细菌微生物之一,S. gallinarum是不同类型大曲中常见的菌种[14-15]。韩培杰[16]对采集自52个酒厂的296份大曲样品细菌群落结构进行研究发现,S. gallinarum位列第一,平均相对含量为11.05%。侯议轲[17]对汾酒大曲细菌群落结构进行研究亦发现,S. gallinarum为优势菌种(2%~9%)。罗美燕等[18]对从虾酱中分离的S. gallinarum FELA3进行研究发现,S. gallinarum具有产脂肪酶能力,同时使用该菌株制备的发酵液中共检测到94种挥发性风味物质,相较于空白发酵液,这些挥发性风味物质的含量显著上升了655.25 ng/mL。WANG等[19]对不同类型大曲研究发现,S. gallinarum与酯化力、芳香类化合物含量呈显著正相关(P<0.05)。高温大曲组样品中共检测出7个优势细菌种,其中血液克罗彭施泰特氏菌(Kroppenstedtia sanguinis)是该组样品中的优势丰富细菌种,平均相对含量为26.39%。熊盈盈[20]对采集自贵州茅台镇某酱香型白酒企业的高温大曲进行研究发现,K. sanguinis为主要菌种,平均相对含量为49.53%。作为大曲中的核心功能细菌,K. sanguinis隶属于高温放线菌科(Thermoactinomycetaceae)下的Kroppenstedtia菌属,其最佳生长温度相对较高,为45 ℃ 或50 ℃[21]。据报道,Kroppenstedtia能够表达和分泌淀粉酶,同时在风味物质的产生方面,任婷婷等[22]研究发现,Kroppenstedtia与苯乙醇、乙酸苯乙酯和2-十一烯醛呈极显著正相关(P<0.001);WANG等[23]研究发现,Kroppenstedtia与酯、酸和吡嗪呈正相关。综上可知,中高温和高温大曲细菌群落结构存在明显差异。S. gallinarum和K. sanguinis作为各自组别中的优势细菌种,不仅在大曲中普遍存在,而且与风味的形成密切相关。然而,目前关于大曲中S. gallinarum 和K. sanguinis的功能性研究仍为空白,因此其对大曲及白酒品质的贡献值得进一步探索。
值得一提的是,无论是在属还是种水平上,中高温大曲组样品中others的平均相对含量均显著较高,超过了40%。这一数据表明,纳入本研究的酒厂所生产的中高温大曲含有更多的低丰度细菌类群,进一步证实了中高温大曲细菌群落多样性和丰富度更高。究其原因,这可能与中高温大曲(55~60 ℃)和高温大曲(60~65 ℃)发酵温度的差异密切相关。在中高温大曲的发酵过程中,通常会经历翻曲和开关门窗等操作,这一方面有效调节了发酵的温度和湿度,为微生物的生长提供了一个更加适宜的发酵环境;另一方面,大曲能够捕获更多周围环境中的微生物资源,增加了群落多样性[24]。然而,相较于中高温大曲,高温大曲为了维持高温的发酵环境,翻曲和开窗次数则有所减少。这种条件下,大曲表面会被烤焦,导致曲皮硬度增加[4],这不仅使得氧气难以进入大曲内部,同时还阻碍了水分和生物热等的排出,不利于微生物的生长和繁殖,最终导致高温大曲的细菌类群数量减少。尽管本研究选取了相对具有代表性的中高温和高温曲块,但原料批次、制作时间、空间异质性等因素会对大曲的细菌群落结构产生影响,因此未来研究中可适当增加采集时间梯度与重复样本数,以全面解析德州地区大曲的细菌多样性。
2.3 中高温和高温大曲样品生物标志物分析
本研究进一步采用LEfSe分析(LDA阈值为3.5)筛选不同类型大曲细菌群落的显著差异物种(P<0.05),结果如图3所示。
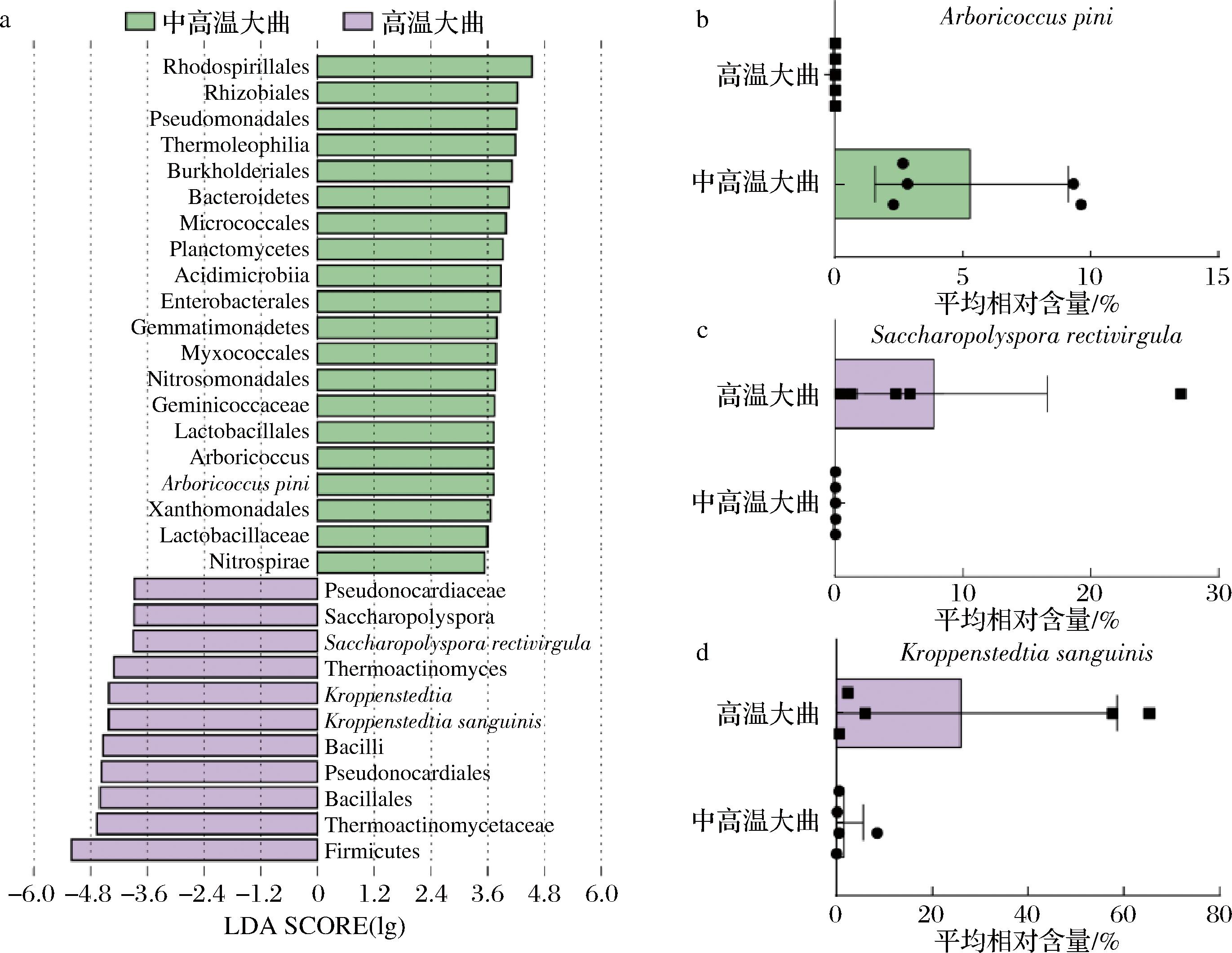
a-LEfSe分析柱形图;b~d-差异物种柱形图
图3 中高温和高温大曲细菌物种差异分析
Fig.3 Analysis of bacterial species differences in medium-high- and high-temperature Daqu
由图3-a可知,2种类型大曲样品共识别出31个差异物种,中高温和高温大曲组分别识别出20和11个显著差异物种。此外,差异物种中共发现3个种水平的细菌生物标志物,分别为Arboricoccus pini、直杆糖多孢菌(Saccharopolyspora rectivirgula)和K. sanguinis。由图3-b~图3-d可知,A. pini在中高温大曲中显著富集,S. rectivirgula和Kroppenstedtia sanguinis在高温大曲中显著富集。因此,根据LDA值的大小,可以分别将A. pini和K. sanguinis分别作为纳入本研究中高温和高温大曲的生物标志物。
2.4 中高温和高温大曲样品共现性网络分析
本研究进一步采用共现性网络分析对不同温度变化下细菌群落间的复杂程度与稳定性进行了探究,结果如图4所示。
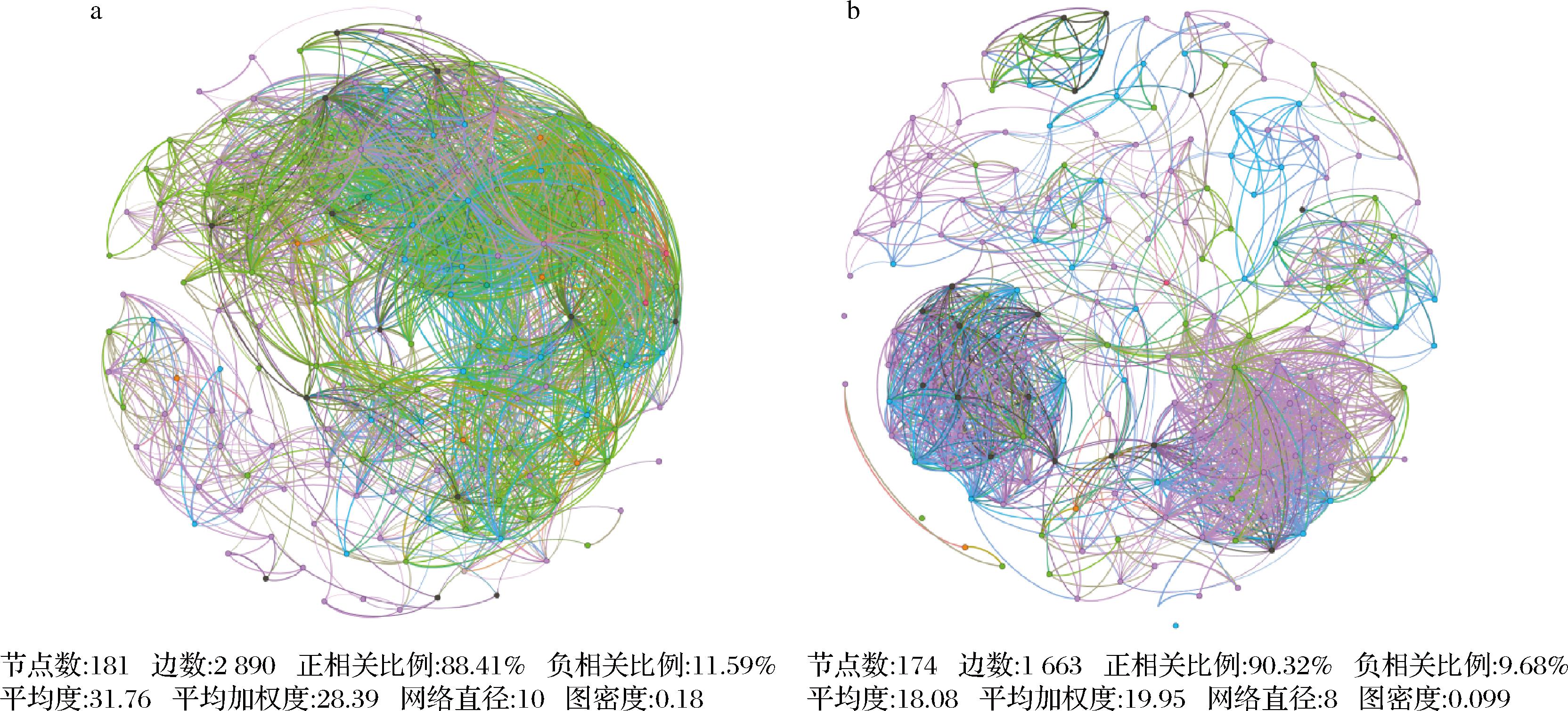
a-中高温大曲;b-高温大曲
图4 中高温和高温大曲细菌共现性网络分析
Fig.4 Analysis of co-occurrence network of Daqu bacteria at medium-high- and high-temperature Daqu
由图4可知,网络拓扑学参数分析表明,中高温大曲组在节点数、边数、平均度、平均加权度、网络直径和图密度指标上均明显高于高温大曲组,说明中高温大曲组细菌群落间复杂程度更高。这种复杂的微生物网络结构不仅提升了细菌群落中资源和信息的传递效率,加快了底物的转化与利用,还增强了微生物群落对环境干扰的耐受力和稳定性[25]。由图4亦可知,中高温大曲组细菌网络的负相关比例高于高温大曲组,表明中高温大曲细菌物种之间可能存在着更大的竞争。究其原因,可能与中高温大曲在相对较低的发酵环境温度下具有更高的细菌多样性和丰富度密切相关。这种条件下物种的重叠导致营养物质竞争加剧,竞争可能进一步通过“竞争排斥-生态位分化”机制促进群落的共振荡,从而有助于形成动态稳定的生态系统[26]。赵慧君等[27]研究发现,高温大曲真菌菌群之间的稳定性弱于中温大曲;ZONG等[28]的研究也证实发酵环境会对微生物之间的相互作用产生影响。然而,环境的变化可以被调节,促进有益微生物的生长和代谢。因此,未来在大曲的发酵过程中,应更加重视发酵条件对大曲微生物群落结构和微生态系统稳定性的影响,以强化功能菌群的适配性,减少环境胁迫对大曲微生态稳定性的消极影响,从而保障白酒品质的稳定性。
2.5 中高温和高温大曲样品COG功能和代谢通路预测
由图5-a~图5-c COG功能注释结果可知,中高温大曲组中,染色体结构与动力学,细胞壁/膜/质膜形成,翻译后修饰、蛋白质周转、伴侣蛋白,信号转导机制,细胞内运输、分泌和囊泡运输这5个功能基因的表达更为显著(P<0.05),这些功能更多地与微生物的生长繁殖相关,亦证明中高温大曲中细菌群落的竞争更大[29]。高温大曲组中,氨基酸转运与代谢、碳水化合物转运与代谢这2个功能基因的表达更为显著(P<0.05),表明高温大曲微生物群在原料降解和风味合成方面具有潜力[30]。由图5-d可知,代谢通路注释结果显示,高温大曲细菌在PWY-5101(L-异亮氨酸生物合成Ⅱ)、PWY-6126(腺苷核苷酸从头生物合成Ⅱ的超途径)等氨基酸合成功能以及TCA(TCA循环Ⅰ)、PWY-6969(TCA循环Ⅴ)等碳水化合物代谢相关的丰度显著高于中高温大曲(P<0.05),这一结果与COG功能注释结果相互验证。
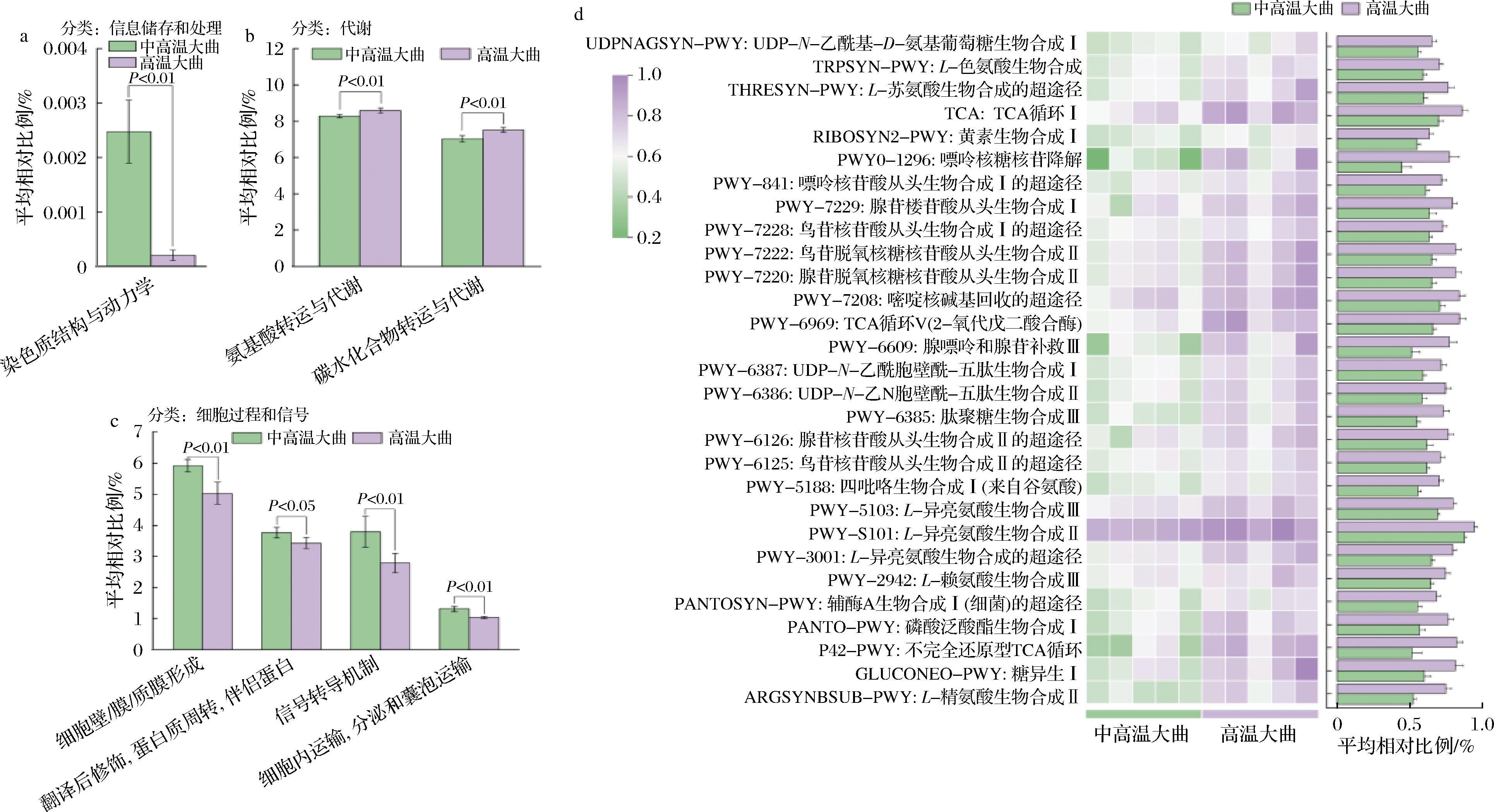
a、b、c-COG功能预测;d-平均相对含量>6%的差异代谢通路
图5 中高温和高温大曲细菌功能预测
Fig.5 Prediction of bacterial function in medium-high- and high-temperature Daqu
2.6 中高温和高温大曲样品可培养微生物的差异性分析
白酒的酿造过程是一个繁复的自然发酵体系,鉴于此,研究人员积极利用现代生物技术手段,以期选育功能微生物,进而提升酒曲的发酵效能与风味特性。因此,本研究进一步采用微生物纯培养技术对中高温和高温大曲样品可培养微生物进行了分离,通过16S rRNA序列对比结果构建系统发育树,结果如图6所示。
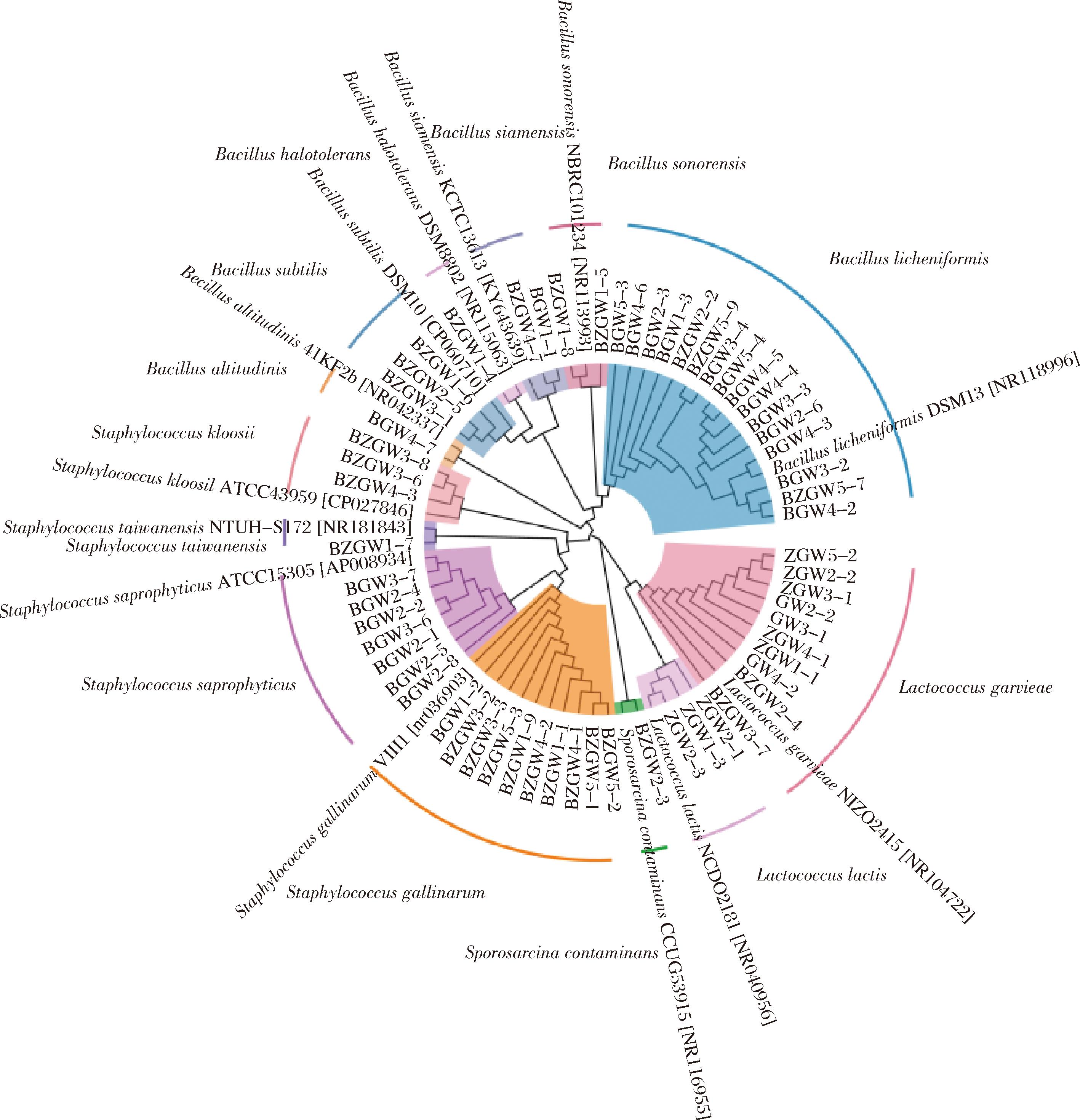
图6 中高温和高温大曲细菌分离株系统发育树
Fig.6 Phylogenetic tree of medium-high- and high-temperature Daqu bacterial isolates
由图6可知,10份大曲样品中共得到60个分离株。经16S rRNA序列鉴定后,隶属于4个属,13个种,包括暹罗芽孢杆菌(Bacillus siamensis)、地衣芽孢杆菌(Bacillus licheniformis)、高地芽孢杆菌(Bacillus altitudinis)、环状芽孢杆菌(Bacillus halotolerans)、索诺拉沙漠芽孢杆菌(Bacillus sonorensis)、Bacillus subtilis、格氏乳球菌(Lactococcus garvieae)、乳酸乳球菌(Lactococcus lactis)、克氏葡萄球菌(Staphylococcus kloosii)、Staphylococcus gallinarum、Staphylococcus taiwanensis、腐生葡萄球菌(Staphylococcus saprophyticus)、污染物芽孢八叠球菌(Sporosarcina contaminans)。为分析不同类型大曲样品可培养微生物的多样性和丰富度,本研究进一步统计了不同样品中分离得到的微生物种类和数量,对不同菌种的相对含量进行了计算,结果如图7所示。
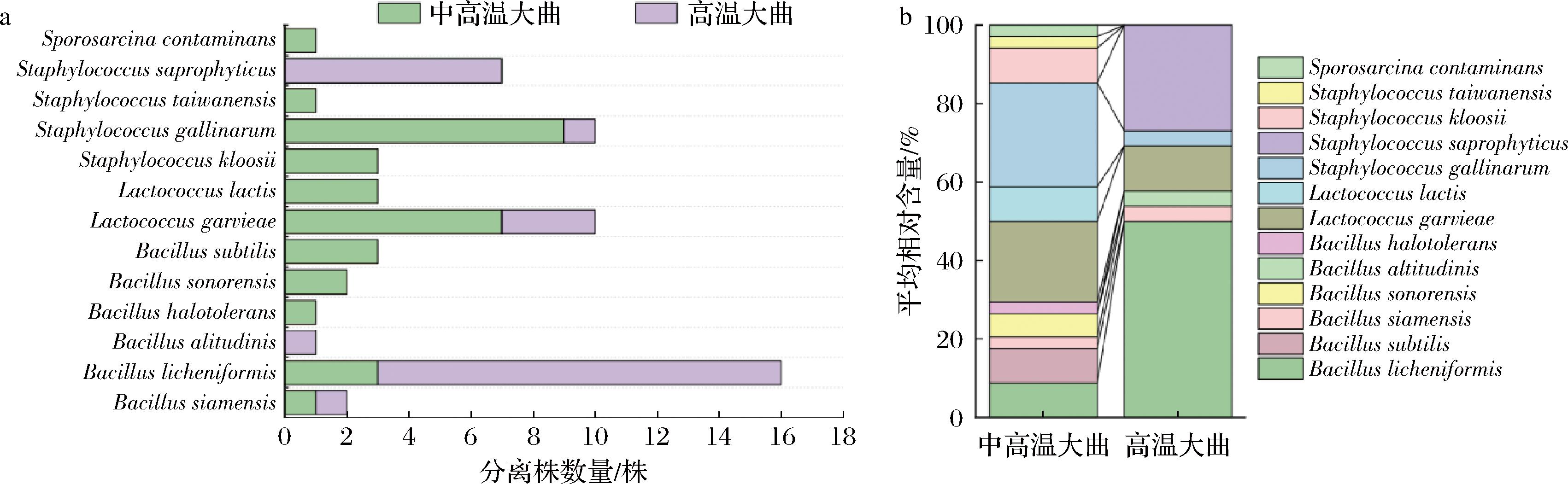
a-分离株物种多样性分析;b-中高温和高温大曲可培养细菌多样性分析
图7 大曲细菌分离株多样性分析
Fig.7 Diversity analysis of Daqu bacterial isolates
由图7-a可知,优势菌种为B. licheniformis,共16株,占总分离株的26.67%,其次为L. garvieae和S. gallinarum,均占总分离株的16.67%。作为一个重要的风味产生类群,B. licheniformis能够合成各种参与发酵的酶,如α-淀粉酶、葡糖淀粉酶、蛋白酶等。QIN等[31]研究发现,接种B. licheniformis CGMCC 20675显著增加了中温大曲碳水化合物代谢、氨基酸代谢和酯类物质生物合成的潜力。WANG等[32]研究发现,接种B. licheniformis CGMCC 3963影响了大曲发酵中微生物群落,同时提高了芳香族化合物和吡嗪类化合物的含量。这进一步凸显了B. licheniformis对提升白酒品质的重要意义,因此,在未来可以进一步通过强化大曲的制作,筛选出具有特定功能的B. licheniformis菌株。由图7-b的菌群结构分析可知,从中高温大曲样品中分离的物种多样性高于高温大曲,且2种类型大曲中可培养微生物菌群结构存在明显差异。例如,B. halotolerans、B. sonorensis、B. subtilis、L. lactis、S. kloosii、S. taiwanensis和S. contaminans这7个菌种仅在中高温大曲中分离得到,B. altitudinis和S. saprophyticus这2个菌种仅在高温大曲中分离得到,同时中高温大曲的乳酸菌含量高于高温大曲,造成这种差异的原因可能与2种类型大曲的发酵温度不同有关。此外,中高温大曲优势可培养细菌为S. gallinarum,相对含量为26.47%,与测序结果一致。高温大曲优势可培养细菌为B. licheniformis,相对含量为50.00%,基于前面关于B. licheniformis功能性的讨论,亦证明高温大曲在风味合成方面可能具有巨大潜力。值得一提的是,中高温和高温大曲的发酵条件较为严苛,而本研究纯培养分离设置的温度条件为30 ℃ 和37 ℃,培养基条件为NA和MRS培养基,与大曲内微生物实际的生态条件存在差异,这可能会影响最终分离得到的细菌物种。因此,未来研究中可适当优化细菌分离条件,以期为强化大曲菌株的选择提供更多可能性。
3 结论
德州地区中高温和高温大曲在细菌群落结构、多样性、功能和可培养微生物等方面存在显著差异。具体而言,中高温大曲优势菌种为S. gallinarum,其群落复杂程度、稳定性、微生物生长合成速率和可培养细菌多样性均明显偏高;而高温大曲优势菌种为K. sanguinis,其氨基酸和碳水化合物的转运与代谢功能明显偏高。本研究阐明了德州地区中高温和高温大曲细菌群落结构和多样性的差异,以期为大曲品质的提升提供理论依据。
[1] LI H D, LIU S Y, LIU Y B, et al.Functional microorganisms in Baijiu Daqu:Research progress and fortification strategy for application[J].Frontiers in Microbiology, 2023, 14:1119675.
[2] LIU Y B, LI H D, LIU W X, et al.Bioturbation analysis of microbial communities and flavor metabolism in a high-yielding cellulase Bacillus subtilis biofortified Daqu[J].Food Chemistry:X, 2024, 22:101382.
[3] MI R Y, LU W, ZHANG X, et al.Screening and identification of strains for high quality and antioxidant activity of Baijiu from strong-flavor Daqu and analysis of microbial synergistic effects[J].PLoS One, 2025, 20(3):e0319616.
[4] LEI Y, CAI W C, WANG Y R, et al.Elucidating the physicochemical parameters, bacterial community structure, and correlation characteristics of medium-high temperature Daqu[J].Food Bioscience, 2024, 58:103679.
[5] ZHENG X W, YAN Z, ROBERT NOUT M J, et al.Characterization of the microbial community in different types of Daqu samples as revealed by 16S rRNA and 26S rRNA gene clone libraries[J].World Journal of Microbiology and Biotechnology, 2015, 31(1):199-208.
[6] SHANG C H, LI Y J, ZHANG J, et al.Analysis of bacterial diversity in different types of Daqu and fermented grains from Danquan distillery[J].Frontiers in Microbiology, 2022, 13:883122.
[7] MOU C Y, LI Q, HUANG Z P, et al.PacBio single-molecule long-read sequencing provides new insights into the complexity of full-length transcripts in oriental river prawn, Macrobrachium nipponense[J].BMC Genomics, 2023, 24(1):340.
[8] ZHANG Y D, DING F, SHEN Y, et al.Characteristics of the microbiota and metabolic profile of high-temperature Daqu with different grades[J].World Journal of Microbiology and Biotechnology, 2022, 38(8):137.
[9] XIANG F S, CAI W C, HOU Q C, et al.Comparative analysis of the microbial community structure in light-flavor Daqu in Taiyuan and Suizhou regions, China[J].LWT, 2023, 177:114599.
[10] HAN P J, SONG L, WEN Z, et al.Species-level understanding of the bacterial community in Daqu based on full-length 16S rRNA gene sequences[J].Food Microbiology, 2024, 123:104566.
[11] DU Z M, SUN L, LIN Y L, et al.Using PacBio SMRT sequencing technology and metabolomics to explore the microbiota-metabolome interaction related to silage fermentation of woody plant[J].Frontiers in Microbiology, 2022, 13:857431.
[12] TIAN F, LIAO X F, WANG L H, et al.Isolation and identification of beneficial orchid mycorrhizal fungi in Paphiopedilum barbigerum (Orchidaceae)[J].Plant Signaling &Behavior, 2022, 17(1):2005882.
[13] DENG J, ZHENG J, HUANG D, et al.Characterization of physicochemical properties, volatile compounds and microbial community structure in four types of Daqu[J].LWT, 2023, 184:115064.
[14] MU Y, YAO S J, HUANG Y, et al.Unveiling the metabolic heterogeneity and formation mechanism in Chinese typical Daqu based on Qu-omics[J].Food Research International, 2025, 202:115735.
[15] 黄魏, 李浪金, 谢丹, 等.3种高温大曲发酵过程中细菌群落结构演替规律[J].食品研究与开发, 2023, 44(22):155-162.
HUANG W, LI L J, XIE D, et al.Investigation of bacterial community structure succession during the fermentation of three types of high-temperature Daqu[J].Food Research and Development, 2023, 44(22):155-162.
[16] 韩培杰. 中国白酒大曲微生物多样性研究[D].福州:福建农林大学, 2023.
HAN P J.Study on microbial diversity of Chinese Baijiu Daqu[D].Fuzhou:Fujian Agriculture and Forestry University, 2023.
[17] 侯议轲. 清香型白酒酿造微生物菌群快速检测方法的研究与应用[D].太原:山西大学, 2023.
HOU Y K.Research and application of rapid detection method for microbial flora in Fen-flavor liquor[D].Taiyuan:Shanxi University, 2023.
[18] 罗美燕, 刘唤明, 香江, 等.虾酱中风味菌株的筛选及其发酵性能分析[J].广东海洋大学学报, 2022, 42(2):79-87.
LUO M Y, LIU H M, XIANG J, et al.Isolation of flavor strains in shrimp paste and analysis of fermentation characteristic[J].Journal of Guangdong Ocean University, 2022, 42(2):79-87.
[19] WANG Y R, HOU Q C, NI H, et al.Multi-method joint analysis reveals differences in the quality and microbial composition of high-temperature and medium-high-temperature Daqu[J].LWT, 2024, 209:116804.
[20] 熊盈盈. 第三代测序技术和培养法联合使用对酱香大曲细菌多样性及其功能的研究[D].贵阳:贵州大学, 2021.
XIONG Y Y.Research on the bacterial diversity and functions of jiang-flavor Daqu based on the application of third-generation sequencing technology and cultivation methods[D].Guiyang:Guizhou University, 2021.
[21] SHI W, CHAI L J, ZHAO H, et al.Deciphering the effects of different types of high-temperature Daqu on the fermentation process and flavor profiles of sauce-flavor Baijiu[J].Food Bioscience, 2024, 61:104917.
[22] 任婷婷, 晏培, 山其木格, 等.控温控湿高温大曲在制酒生产过程中的应用[J].食品科学, 2025, 46(7):151-161.
REN T T, YAN P, SHAN Q M G, et al.Application of high-temperature Daqu with controlled temperature and humidity in Baijiu brewing[J].Food Science, 2025, 46(7):151-161.
[23] WANG W H, FAN G S, LI X T, et al.Application of Wickerhamomyces anomalus in simulated solid-state fermentation for Baijiu production:Changes of microbial community structure and flavor metabolism[J].Frontiers in Microbiology, 2020, 11:598758.
[24] 李学思, 侯小歌, 王蕴哲, 等.不同储存期宋河中高温大曲霉菌的分离及鉴定[J].中国酿造, 2023, 42(6):91-96.
LI X S, HOU X G, WANG Y Z, et al.Isolation and identification of mould from Songhe medium-high temperature Daqu with different storage periods[J].China Brewing, 2023, 42(6):91-96.
[25] 马世源, 李子健, 罗惠波, 等.酿酒酵母对浓香型白酒酒醅微生物群落结构及功能的影响[J].中国食品学报, 2024, 24(2):71-82.
MA S Y, LI Z J, LUO H B, et al.Effects of Saccharomyces cerevisiae on microbial community structure and function of Nong-flavour fermented grains[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(2):71-82.
[26] 张梅婷, 刘晋仙, 苏嘉贺, 等.苦草叶表附生和水体浮游细菌群落多样性格局及其影响因素[J].环境科学, 2023, 44(1):252-261.
ZHANG M T, LIU J X, SU J H, et al.Diversity patterns and influencing factors of epibiotic in Vallisneria natans and planktonic bacteria communities[J].Environmental Science, 2023, 44(1):252-261.
[27] 赵慧君, 王玉荣, 侯强川, 等.滨州地区高温和中温大曲真菌类群解析及其感官品质关联性分析[J].食品工业科技, 2025,46(11):163-173.
ZHAO H J, WANG Y R, HOU Q C, et al.Analysis of fungal communities of high-temperature and medium-temperature Daqu in Binzhou region and their correlation with sensory quality[J].Science and Technology of Food Industry, 2025,46(11):163-173.
[28] ZONG E X, BO T, DANG L, et al.Different functions can be provided by low temperature Daqu with different appearance features due to variations in the microbial community structure during fermentation[J].LWT, 2024, 193:115763.
[29] 侯强川, 王玉荣, 王文平, 等.茅台和尧治河高温大曲细菌群落结构差异及功能预测[J].食品与发酵工业, 2022, 48(1):36-44.
HOU Q C, WANG Y R, WANG W P, et al.Difference of bacterial community structure and functional prediction in high-temperature Daqu of Maotai and Yaozhihe[J].Food and Fermentation Industries, 2022, 48(1):36-44.
[30] WANG Y, ZHOU W, TAO Y, et al.Profiling the global map of ester-producing metabolism and the response patterns of key genes to environmental factors during medium-high temperature Daqu production[J].Food Bioscience, 2024, 62:105462.
[31] QIN H, ZHANG S Y, WANG C, et al.Revealing the influence of exogenously inoculated Bacillus spp.on the microbiota and metabolic potential of medium-temperature Daqu:A meta-omics analysis[J].Food Research International, 2024, 182:114152.
[32] WANG P, WU Q, JIANG X J, et al.Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].International Journal of Food Microbiology, 2017, 250:59-67.