支链氨基酸(branched chain amino acids,BCAAs),包括缬氨酸、亮氨酸和异亮氨酸,是生物体蛋白质合成的基本单元,在多种细胞生理功能中发挥关键作用[1-2]。BCAAs的生物合成起始于糖酵解产物丙酮酸或苏氨酸代谢物2-酮丁酸,在乙酰乳酸合酶(acetyl lactate synthase,ALS)的催化下生成乙酰乳酸或乙酰羟基丁酸,乙酰乳酸和乙酰羟基丁酸分别经过异构化、脱氢与转氨等一系列生物化学反应,形成缬氨酸、亮氨酸或异亮氨酸[1-2]。可见,乙酰乳酸合酶是支链氨基酸生物合成与供给的关键酶系,并由此决定了细胞生理代谢的相关行为与表型特征。
为解析生物体BCAAs的生物合成过程并创新其高效生物制备高产菌株及制备技术,大肠杆菌乙酰乳酸合酶获得了较为深入的研究。作为BCAAs生物合成的起始酶,大肠杆菌中的ALS酶系包括至少3种同工酶,分别为ALS Ⅰ、ALS Ⅱ和ALS Ⅲ,三者由不同的基因簇编码[3-4],对三者生理功能的研究已揭示其具有差异性。有研究显示,ALS Ⅰ由ilvB和ilvN基因编码,主要负责亮氨酸的生物合成,并在支链氨基酸匮乏的情况下优先表达[5-6];ALS Ⅱ由ilvG和ilvM基因编码,参与缬氨酸和异亮氨酸的合成,且在部分大肠杆菌菌株中由于基因突变而失活[7-8];ALS Ⅲ由ilvI和ilvH基因编码,主要在异亮氨酸的代谢中发挥作用[9-10]。除了作用于BCAAs的生物合成,大肠杆菌ALS还具有非天然底物之外的广谱底物特性,在生物炼制、生物化工与合成生物学等方面同样具备重要研究与生物工具价值[11-12]。
大肠杆菌作为一种模式菌株,在基础生物学研究中被广泛应用为生物研究材料,并由此获得清晰遗传背景、成熟遗传操作技术以及丰富工程放大创新技术体系,是生物工程研究、多种工业菌种创建以及合成生物学领域的重要工业平台菌株[13-15]。基于其快速增殖、代谢灵活性强以及能够高效表达外源基因等优越特性,大肠杆菌已被成功开发用于合成多种平台化合物及高附加值化学品,如氨基酸、维生素、有机酸、生物燃料等,为可持续的工业生物制造提供有效解决方案[15-17]。进一步开展相关高效菌株创建的基础生物学特征、遗传与代谢模块、新型代谢控制节点与控制策略研究,不仅可提升工业菌种与生物制造技术水平,也可为未来生物菌种创新与工业控制提供新的研究策略。
本研究就大肠杆菌B0013菌株中ALS酶系组成及其功能进行系统分析,通过基因删除与遗传互补等技术,在获得相应基因突变体的基础上,详细分析与研究其功能呈现与细胞增殖的相互关系,以期为通过BCAAs生物合成调控细胞增殖的新型调控策略建立技术基础,同时为工业微生物菌种的高效工程改良与优化提供新的理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株、质粒与引物
本研究所使用的菌株和质粒见表1。大肠杆菌B0013菌株是早期从自然界分离获得的、应用于生物燃料生物制造的底盘菌株[18-19],用作本研究的分子克隆基因供体;大肠杆菌LG101菌株为L-乳酸单体生产菌株,由大肠杆菌B0013经多重遗传修饰与基因表达等获得[20]并进一步删除pflC/D、pflE/F、tdcE、aceA等基因。本研究使用的寡核苷酸引物序列见表2,委托生工生物工程(上海)股份有限公司经化学合成方法获得。
表1 本研究中所用的菌株和质粒
Table 1 Strains and plasmids used in this study

菌株和质粒有关特性来源菌株E.coli JM109克隆宿主[21]LG101L9KH, ΔpflE/F, ΔpflC/D, ΔtdcE本课题组前期构建并保存LG201LG101, ΔilvI/H本研究构建LG202LG101, ΔilvG/M本研究构建LG203LG101, ΔilvB/N本研究构建LG204LG201, ΔilvB/N本研究构建LG205LG202, ΔilvI/H本研究构建LG206LG203, ΔilvG/M本研究构建LG207LG206, ΔilvI/H本研究构建LG207(pHC18-ilvB/N)LG207, pHC18-ilvB/N本研究构建LG207(pHC18-ilvI/H)LG207, pHC18-ilvI/H本研究构建LG207(pHC18-ilvG/M)LG207, pHC18-ilvG/M本研究构建质粒pHC18Apr;temperature-condition-al replicon本课题组前期构建并保存pSKsymApr;克隆质粒[22]pSKsym-difEryApr;Eryr;dif-Ery-dif本课题组前期构建并保存pSKsym-ilvG/M::difEryApr;Eryr;ilvG/M::difEry本课题组前期构建并保存pSKsym-ilvI/H::difEryApr;Eryr;ilvI/H::difEry本课题组前期构建并保存T-ilvB/N::difEryApr;Eryr;ilvB/N::difEry本课题组前期构建并保存pHC18-ilvB/NApr;temperature-condition-al replicon, ilvB/N本研究构建pHC18-ilvI/HApr;temperature-condition-al replicon, ilvI/H本研究构建pHC18-ilvG/MApr;temperature-condition-al replicon, ilvG/M本研究构建
表2 本研究中所用引物
Table 2 Primers used in this study
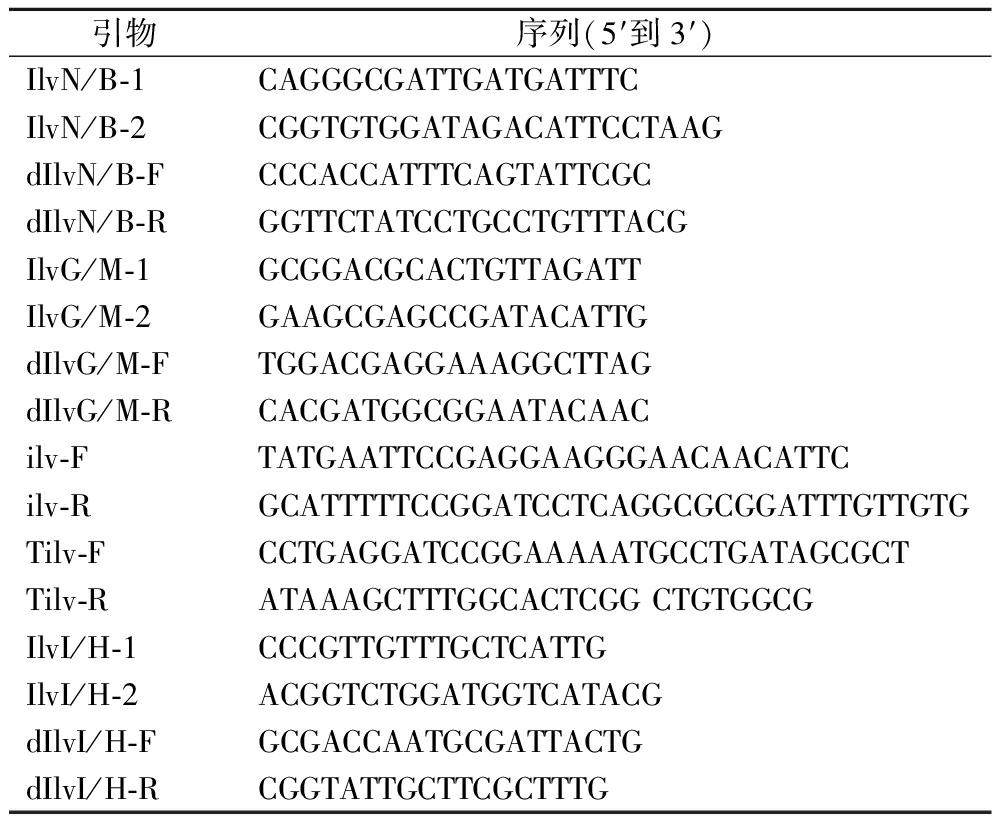
引物序列(5′到3′)IlvN/B-1CAGGGCGATTGATGATTTCIlvN/B-2CGGTGTGGATAGACATTCCTAAGdIlvN/B-FCCCACCATTTCAGTATTCGCdIlvN/B-RGGTTCTATCCTGCCTGTTTACGIlvG/M-1GCGGACGCACTGTTAGATTIlvG/M-2GAAGCGAGCCGATACATTGdIlvG/M-FTGGACGAGGAAAGGCTTAGdIlvG/M-RCACGATGGCGGAATACAACilv-FTATGAATTCCGAGGAAGGGAACAACATTCilv-RGCATTTTTCCGGATCCTCAGGCGCGGATTTGTTGTGTilv-FCCTGAGGATCCGGAAAAATGCCTGATAGCGCTTilv-RATAAAGCTTTGGCACTCGG CTGTGGCGIlvI/H-1CCCGTTGTTTGCTCATTGIlvI/H-2ACGGTCTGGATGGTCATACGdIlvI/H-FGCGACCAATGCGATTACTGdIlvI/H-RCGGTATTGCTTCGCTTTG
1.1.2 主要试剂
质粒小量提取试剂盒、限制性内切酶、T4 DNA连接酶等,宝生物工程有限公司;小量DNA纯化试剂盒,北京庄盟国际生物基因科技有限公司;氨苄青霉素、红霉素,生工生物工程(上海)股份有限公司;其他化学试剂均为国产分析纯。
1.1.3 培养基
本研究使用的LB培养基、M9培养基和改良M9液体培养基,均按照文献[23]方法配置。必要时在培养基中添加质量浓度为100 μg/mL氨苄青霉素或160 μg/mL红霉素。
1.2 基因克隆与删除
分子克隆、体外重组、转化、DNA纯化及PCR基因扩增等实验步骤,均按照实验室常规方法进行[24]。大肠杆菌的基因删除采用此前报道的Red/Xer重组系统,进行无痕基因敲除[21, 25]。主要操作步骤为:以大肠杆菌B0013基因组DNA为模板,通过PCR扩增获得待删除基因ilvG/M、ilvI/H或ilvB/N片段;将PCR产物克隆入质粒pSKsym获得相应的重组质粒,进一步在目的基因的中间克隆difEry片段[26],创建完成突变盒;通过PCR扩增构建突变盒ilvG/M::difEry、ilvI/H::difEry、ilvB/N::difEry,并采用电击转化方法[26-27],将突变盒依次转入目标菌株;通过诊断PCR进行验证,确定获得突变菌株的基因型正确性,并用于后续实验。
1.3 生长特征评价
固体平板上突变株的营养特征分析按照文献[24]方法进行。基本步骤为:在基本补充培养基M9中补加200 mg/L缬氨酸、亮氨酸、异亮氨酸或其组合形式,制备平板后通过划线接入相应待试突变株,置于30 ℃下培养一定时间后,观察并记录突变株的生长状况。液体摇瓶培养在250 mL三角瓶中进行,培养液体积为50 mL[21]。主要步骤为:将培养24 h的单个菌落接种到50 mL的LB液体培养基中,置于30 ℃、200 r/min下培养10 h;以0.5%的接种量将培养物转接到含有5 g/L葡萄糖的50 mL改良M9培养基中,在30 ℃、200 r/min下进行好氧培养,定期取样测定菌体密度(OD600),用于评价菌体的生长情况。菌体密度按照实验室常规方法用分光光度计进行测定[24]。
1.4 模拟分子对接
使用Autodock Vina软件[28],对ALS的3种同工酶与底物丙酮酸以及2-酮丁酸的结合能进行预测。
2 结果与讨论
2.1 大肠杆菌BCAAs合成途径解析与ALS同工酶基本组成特征
基于已有大肠杆菌基因组相关信息,对其BCAAs(包括L-缬氨酸、L-亮氨酸和L-异亮氨酸)的合成途径组成及特征进行了分析,重点考察了其乙酰乳酸合酶的相关生物信息特征分析,结果如图1和表3所示。大肠杆菌BCAAs的合成依赖于乙酰乳酸合酶从丙酮酸催化生成乙酰乳酸或从2-酮丁酸催化生成乙酰羟基丁酸的经典路径,其乙酰乳酸合酶具有3种同工酶ALS Ⅰ、ALS Ⅱ和ALS Ⅲ,分别为如下基因编码:ALS Ⅰ由ilvB和ilvN基因编码,ALS Ⅱ由ilvG和ilvM基因编码,ALS Ⅲ则由ilvI和ilvH基因编码。由NCBI网站(https://www.ncbi.nlm.nih.gov)查询获得3种同工酶的编码基因编号(表3)。通过EcoCyc网站(https://www.ecocyc.org)查询可知,3种同工酶的辅因子均为FAD和ThDP;支链氨基酸生物合成途径的最终产物均抑制ALS Ⅲ活性,但缬氨酸的抑制作用最为显著,ALS Ⅰ和ALS Ⅲ均受缬氨酸抑制,但ALS Ⅱ对缬氨酸不敏感,ALS Ⅱ在支链氨基酸的生物合成中可能具有更显著作用。分子对接结果显示,相比底物丙酮酸,ALS Ⅰ、ALS Ⅱ和ALS Ⅲ 3种同工酶均对底物2-酮丁酸具有更高的亲和性。
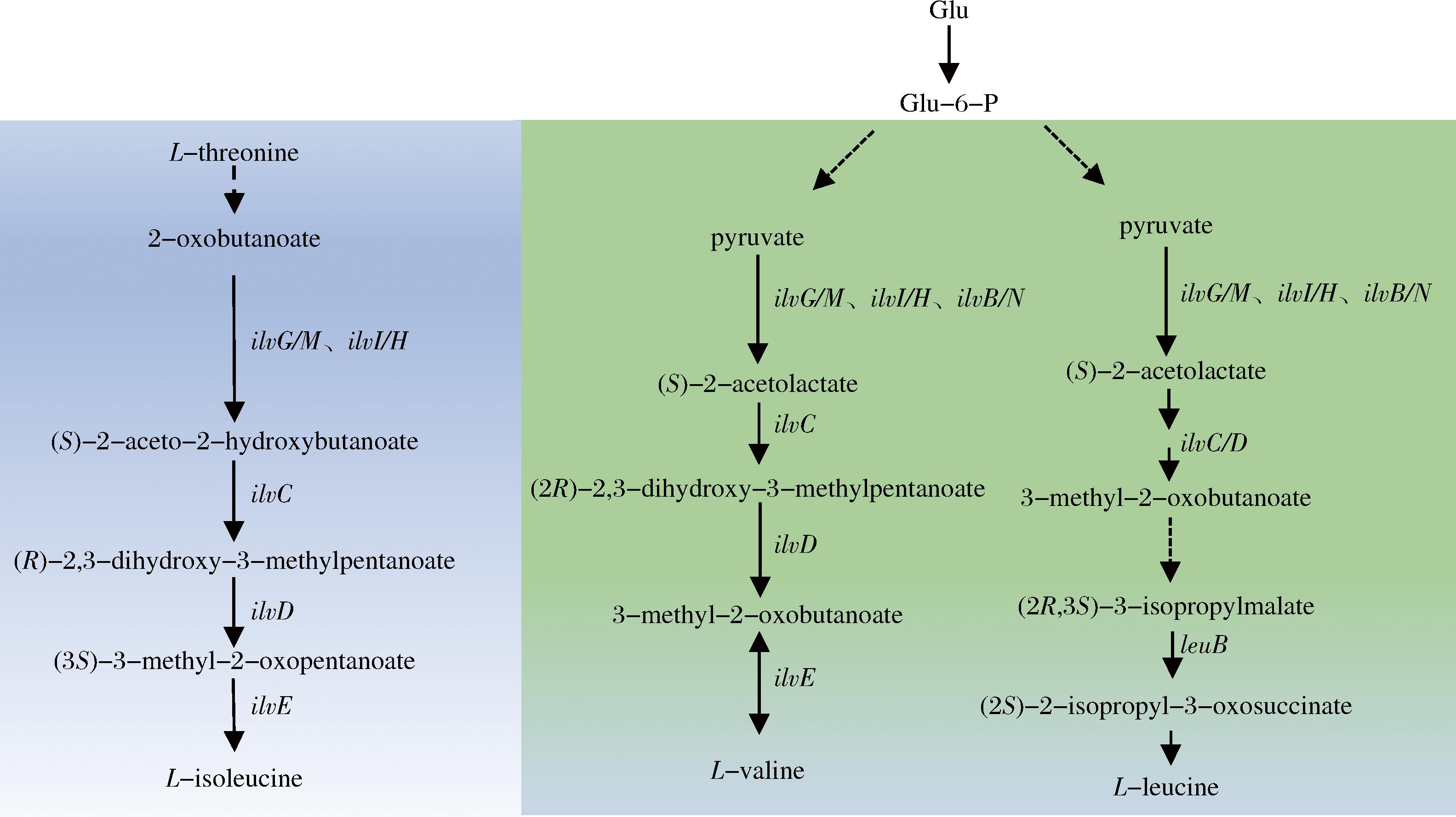
图1 大肠杆菌L-异亮氨酸、L-缬氨酸、L-亮氨酸生物合成途径
Fig.1 Biosynthetic pathways of L-isoleucine, L-valine, and L-leucine in E.coli
表3 乙酰乳酸合酶的相关生物信息特征分析
Table 3 Analysis of relevant biological information characteristics of acetyllactate synthase
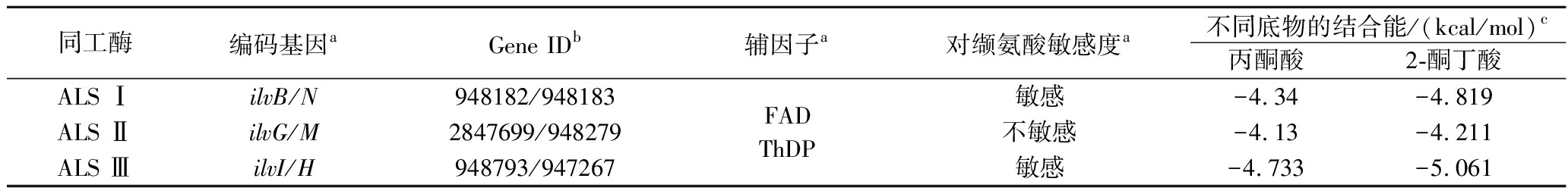
同工酶编码基因aGene IDb辅因子a对缬氨酸敏感度a不同底物的结合能/(kcal/mol)c丙酮酸2-酮丁酸ALS ⅠilvB/N948182/948183ALS ⅡilvG/M2847699/948279ALS ⅢilvI/H948793/947267FAD ThDP敏感-4.34-4.819不敏感-4.13-4.211敏感-4.733-5.061
注:a-数据检索自EcoCyc网站;b-数据检索自NCBI网站;c-数据使用Autodock Vina软件分析获得。
2.2 大肠杆菌LG101中乙酰乳酸合酶与BCAAs生物合成相关关系
2.2.1 ALS编码基因ilvG/M、ilvI/H和ilvB/N突变株的选育
运用无痕殊位重组技术对菌株LG101基因组中乙酰乳酸合酶编码基因ilvG/M、ilvI/H和ilvB/N进行了单点和组合敲除,并经诊断PCR扩增确认,共计选育出7株突变株,结果汇总于图2。单基因突变中,突变株LG201中的ilvI/H获得突变,突变后形成了1.7 kb大小的突变条带(野生型为2.3 kb);突变株LG202中ilvG/M突变后从基因组中删除了该基因中间300 bp编码序列,在诊断PCR实验中形成了1.9 kb大小的突变条带(野生型为2.2 kb);突变株LG203中ilvB/N突变后形成1.3 kb大小的突变条带(野生型为1.6 kb)。进一步在单基因突变株获得的基础上进行组合突变,获得4株组合突变株,其中突变株LG204中ilvI/H和ilvB/N同时发生突变,形成了1.7 kb ilvI/H突变条带和1.3 kb ilvB/N突变条带;突变株LG205中ilvG/M和ilvI/H同时发生突变,出现1.9 kb ilvG/M突变条带和1.3 kb ilvB/N突变条带;突变株LG206中ilvB/N和ilvG/M皆发生突变,形成1.3 kb ilvB/N突变条带和1.9 kb ilvG/M突变条带;突变株LG207中ilvB/N、ilvG/M和ilvI/H皆形成正确突变,产生1.3 kb ilvB/N突变条带、1.9 kb ilvG/M突变条带和1.7 kb ilvI/H突变条带。至此,本研究成功完成了对大肠杆菌LG101菌株中3个L-乙酰乳酸合成酶编码基因的单一和全部组合形式的基因敲除并获得相应的突变株。
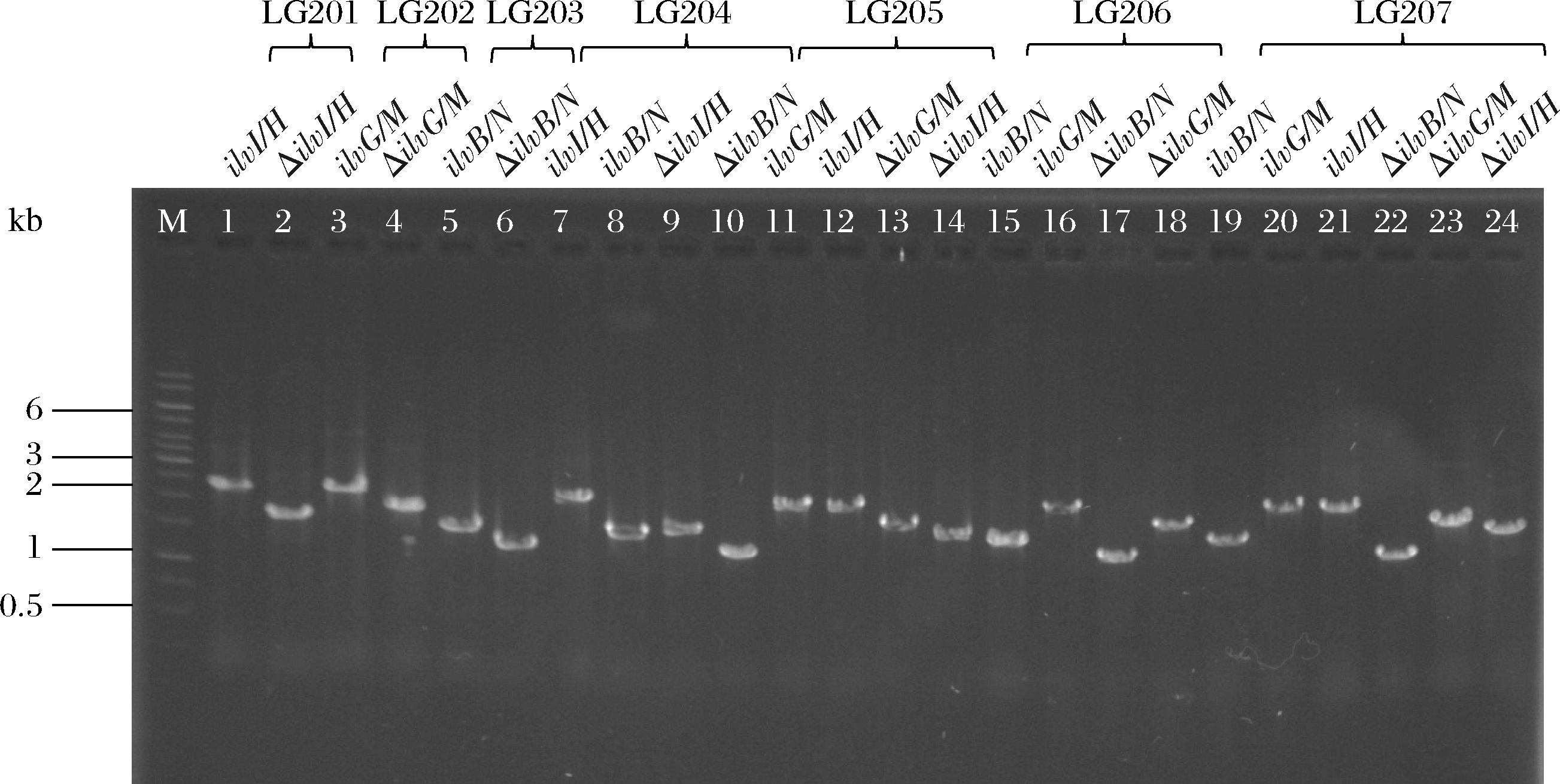
M-DL10 000 DNA Marker;泳道1、2-突变株LG201中ilvI/H发生突变;泳道3、4-突变株LG202中ilvG/M发生突变;泳道5、6-突变株LG203中ilvB/N发生突变;泳道7~10-突变株LG204中ilvI/H、ilvB/N发生突变;泳道11~14-突变株LG205中ilvG/M、ilvI/H发生突变;泳道 15~18-突变株LG206中ilvB/N、ilvG/M发生突变;泳道19~24-突变株LG207中ilvB/N、ilvG/M、ilvI/H同时发生突变。
图2 大肠杆菌LG101中ilvG/M、ilvI/H和ilvB/N删除突变及突变株的诊断PCR检验
Fig.2 Diagnostic PCR tests of ilvG/M, ilvI/H, and ilvB/N deletion mutations and mutant strains in LG101
2.2.2 ALS突变株营养需求表型变化分析
在固体培养基上评价ALS突变株对3种支链氨基酸的营养需求,结果如图3所示。本研究出发菌株LG101能够在基本固体培养基上正常生长(图3-a),所构建的各突变株在基本固体培养基上均未见生长(图3-b)。单基因突变株LG201和LG202在补充L-异亮氨酸后,各自生长均能恢复(图3-c、图3-d),两者营养型均表现为Leu+Val+Ilv-;单基因突变株LG203在补充亮氨酸后恢复生长(图3-e),其营养型表现为Leu-Val+Ilv+。双基因突变株中,LG204在同时补充L-亮氨酸和L-异亮氨酸后恢复生长(图3-f),其营养型表现为Leu-Val+Ilv-;LG205在同时补充L-缬氨酸和L-异亮氨酸后恢复生长(图3-g),其营养型表现为Leu+Val-Ilv-;LG206在同时补充L-亮氨酸和L-异亮氨酸后恢复生长(图3-h),其营养型表现为Leu-Val+Ilv-。在三基因突变株LG207的培养基中同时补加缬氨酸、亮氨酸和异亮氨酸,使其恢复生长(图3-i),其营养型表现为Leu-Val-Ilv-。结果表明,上述突变株中相应ALS同工酶编码基因的删除均产生对应支链氨基酸营养缺陷型特征,3种同工酶ALS Ⅰ、ALS Ⅱ和ALS Ⅲ均为出发菌株LG101正常生长所必需。
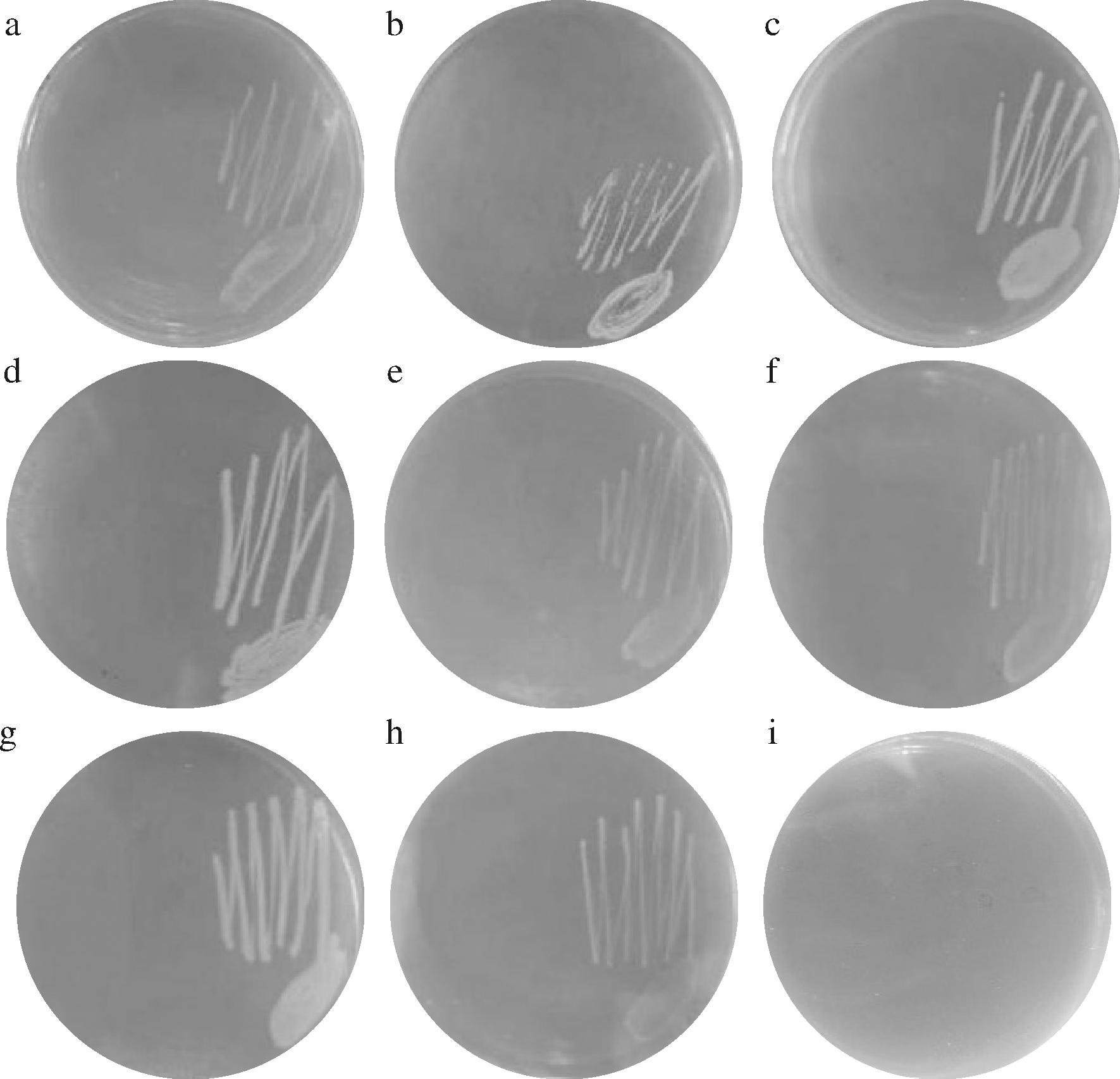
a-出发菌株LG101在基本培养基上生长情况;b-各突变株在基本培养基上生长情况;c-突变株LG201在外加L-异亮氨酸的情况下生长情况;d-突变株LG202在外加L-异亮氨酸的情况下生长情况;e-突变株LG203在外加L-亮氨酸的情况下生长情况;f-突变株LG204在外加L-亮氨酸、L-异亮氨酸的情况下生长情况;g-突变株LG205在外加L-缬氨酸、L-异亮氨酸的情况下生长情况;h-突变株LG206在外加L-亮氨酸、L-异亮氨酸的情况下生长情况;i-突变株 LG207在外加L-亮氨酸、L-异亮氨酸、L-缬氨酸的情况下生长情况
图3 突变菌株在固体培养基上的生长特征
Fig.3 Growth characteristics of mutant strains on solid mediums
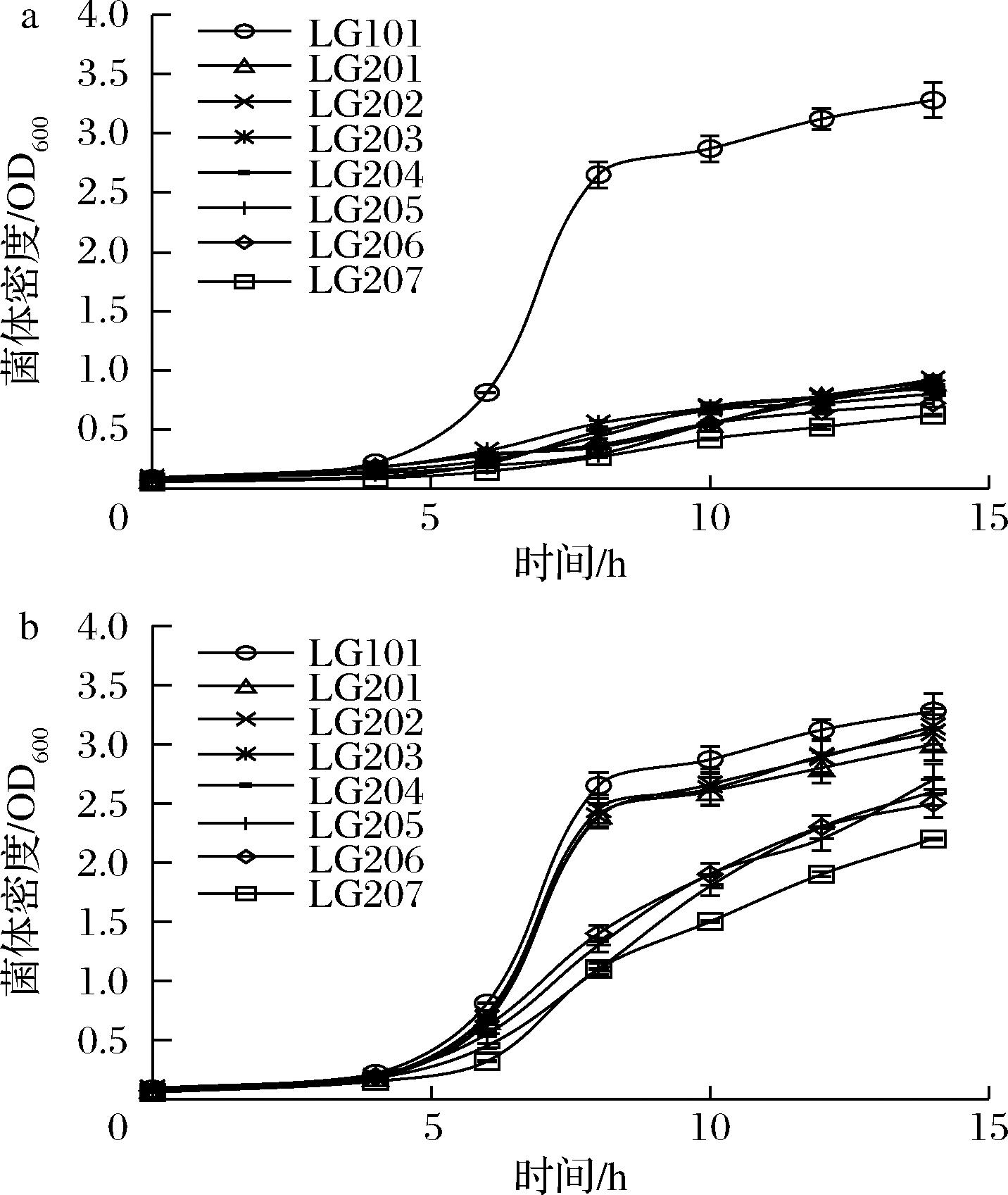
a-M9基本液体培养基中各菌株的生长特征;b-M9基本液体培养基补充相应氨基酸后各菌株的生长特征
图4 突变菌株在基本和补充液体培养基中的生长特征
Fig.4 Growth characteristics of mutant strains in basic and supplementary liquid mediums
2.2.3 ALS突变株在液体培养基中的细胞增殖特征
进一步在摇瓶液体培养基中评价ALS突变株的细胞增殖变化特征,结果见图4。在M9基本培养基中培养14 h(图4-a),出发菌株LG101展现出典型的指数增长曲线,菌体密度达3.28;3种单基因突变菌株菌体密度为0.85~0.92;3种双基因突变菌株菌体密度为0.72~0.88;三基因突变株LG207菌体密度为0.60。可见,ALS编码基因的删除显著影响菌体在基本培养基中的增殖能力,基因的叠加删除会进一步增大此影响。
在M9基本培养基中补充加入特定氨基酸培养上述突变株的结果见图4-b。摇瓶培养14 h,在分别加入相应单种氨基酸的条件下,3种单基因突变株菌体密度为3.02~3.15;在分别加入相应2种氨基酸的条件下,3种双基因突变株菌体密度为2.52~2.70;三基因突变株LG207在外加亮氨酸、异亮氨酸和缬氨酸条件下,菌体密度为2.25。可见,相应外源氨基酸的加入可显著促进各突变株生长,外源氨基酸和突变株的生长可能存在剂量-效应相关关系,需要后续进一步研究。
2.3 通过遗传互补可以恢复ALS突变株的支链氨基酸原养型表型
扩增并体外编辑大肠杆菌ilvB/N、ilvI/H及ilvG/M操纵子序列并克隆入表达质粒pHC18中,获得相应重组表达质粒pHC18-ilvB/N、pHC18-ilvI/H和pHC18-ilvG/M,进一步将所获得的重组表达质粒转化入突变株LG207中,获得重组菌株LG207(pHC18-ilvG/M)、LG207(pHC18-ilvB/N)和LG207(pHC18-ilvI/H)。以此为基础,评价经遗传互补方式恢复ALS突变株的支链氨基酸原养型表型的可行性及其特征,结果如图5所示。
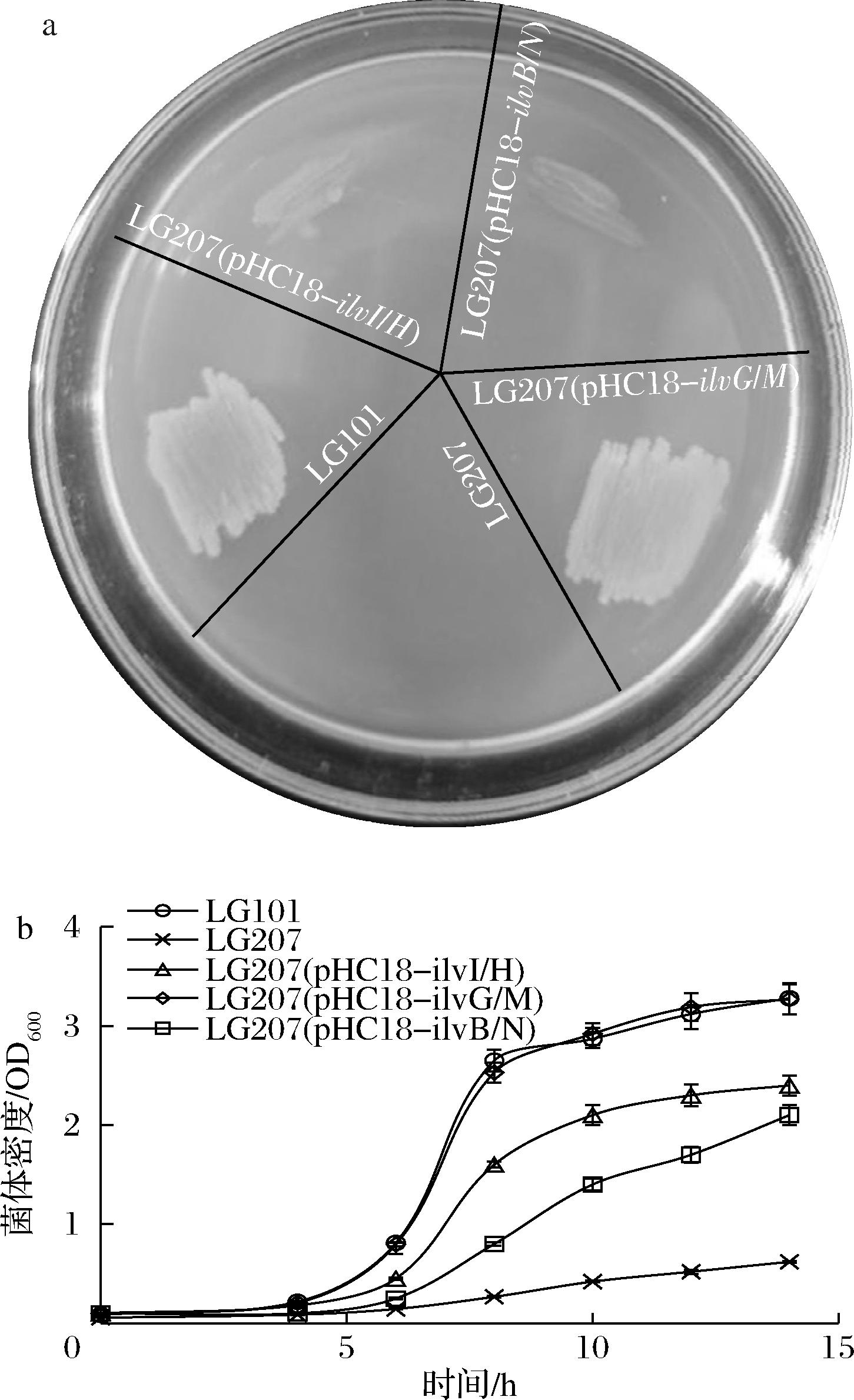
a-遗传互补突变株在基本固体培养基中的生长特征;b-遗传互补突变株在基本液体培养基中的生长特征
图5 遗传互补突变株在基本固体培养基和液体培养基中的生长特征
Fig.5 Growth characteristics of genetic complementation mutant strains in basic solid medium and liquid medium culture
各突变菌株在基本固体培养基中的培养结果见图5-a。在基本固体培养基中培养24 h,三基因突变株LG207不生长,表现出亮氨酸、异亮氨酸和缬氨酸3种氨基酸完全营养缺陷表型;遗传互补突变株LG207(pHC18-ilvG/M)与出发菌株LG101生长特征相似,表型恢复效果明显;遗传互补突变株LG207(pHC18-ilvB/N)和LG207(pHC18-ilvI/H)可以生长,但与出发菌株LG101相比,生长特征不佳,菌株生长缓慢,表型恢复效果一般。可见,在突变株LG207中恢复ALS Ⅱ编码基因ilvG/M功能,可能使其恢复为支链氨基酸原养型。
各突变菌株在基本液体培养基中的培养结果见图5-b。各菌株在基本液体培养基中摇瓶培养14 h,LG207生长微弱,菌体密度低于0.70;遗传互补突变株LG207(pHC18-ilvG/M)呈现出典型指数生长特征,生长曲线与出发菌株LG101相似,培养14 h菌体密度达3.27,与出发菌株LG101接近。遗传互补突变株LG207(pHC18-ilvI/H)和LG207(pHC18-ilvB/N)培养14 h菌体密度分别为2.42和2.11,培养过程中生长速率显著低于LG101和LG207(pHC18-ilvG/M),但生长速率及最终菌体密度均显著高于LG207。3株遗传互补突变株均具有一定的表型恢复效果,相比之下,使用ALS Ⅱ编码基因ilvG/M效果最为显著,相应构建的遗传互补突变株LG207(pHC18-ilvG/M)生长特征接近原养型。
3 结论
通过基因敲除研究,发现大肠杆菌LG101中乙酰乳酸合酶3种同工酶ALS Ⅰ、ALS Ⅱ和ALS Ⅲ均为菌株正常生长所必需,其编码基因的删除产生对应支链氨基酸营养缺陷型特征,且编码基因删除对菌株生长的影响具有叠加效应。通过遗传互补研究,发现3种同工酶编码基因的遗传互补突变株生长性能均有一定程度恢复,其中同工酶ALS Ⅱ编码基因ilvG/M效果最为显著,相应遗传互补突变株生长性能接近原养型。上述发现丰富了大肠杆菌BCAAs代谢调节的研究成果,为未来工业生产中通过控制BCAAs代谢调节优化细胞增殖和代谢产物合成提供了技术基础。
[1] NEINAST M, MURASHIGE D, ARANY Z.Branched chain amino acids[J].Annual Review of Physiology, 2019, 81:139-164.
[2] BO T, FUJII J.Primary roles of branched chain amino acids (BCAAs) and their metabolism in physiology and metabolic disorders[J].Molecules, 2024, 30(1):56.
[3] KOUHEN O M, JOSET F.Biosynthesis of the branched-chain amino acids in the Cyanobacterium synechocystis PCC6803:Existence of compensatory pathways[J].Current Microbiology, 2002, 45(2):94-98.
[4] 赵婷,黄礼清,金紫阳,等.重组大肠杆菌产乙酰乳酸合成酶发酵条件优化[J].食品与发酵工业, 2020, 46(14):156-162.
ZHAO T, HUANG L Q, JIN Z Y, et al.Fermentation optimization of acetolactate synthetase in recombinant Escherichia coli[J].Food and Fermentation Industries, 2020, 46(14):156-162.
[5] QIAO Q Q, NING S Z, WANG R R, et al.Efficient expression regulation of acetohydroxyacid synthase for production of branched-chain amino acids in Corynebacterium glutamicum[J].Chinese Journal of Biotechnology, 2024, 40(9):3114-3126.
[6] 刘宁,徐建中.改造乙酰羟酸合成酶提高L-亮氨酸产量[J].食品与生物技术学报, 2023, 42(9):45-55.
LIU N, XU J Z.Improvement of L-leucine production by modifying acetohydroxy acid synthase[J].Journal of Food Science and Biotechnology, 2023, 42(9):45-55.
[7] LAWTHER R P, CALHOUN D H, GRAY J, et al.DNA sequence fine-structure analysis of ilvG (IlvG+) mutations of Escherichia coli K-12[J].Journal of Bacteriology, 1982, 149(1):294-298.
[8] LU M F, UMBARGER H E.Effects of deletion and insertion mutations in the ilvM gene of Escherichia coli[J].Journal of Bacteriology, 1987, 169(2):600-604.
[9] RICCA E, LIMAURO D, LAGO C T, et al.Enhanced acetohydroxy acid synthase Ⅲ activity in an ilvH mutant of Escherichia coli K-12[J].Journal of Bacteriology, 1988, 170(11):5197-5199.
[10] REIFENBERG P, ZIMMER A.Branched-chain amino acids:Physico-chemical properties, industrial synthesis and role in signaling, metabolism and energy production[J].Amino Acids, 2024, 56(1):51.
[11] LIU Y D, LI Y Y, WANG X Y.Acetohydroxyacid synthases:Evolution, structure, and function[J].Applied Microbiology and Biotechnology, 2016, 100(20):8633-8649.
[12] ZHANG Y Y, LI Y, LIU X, et al.Molecular architecture of the acetohydroxyacid synthase holoenzyme[J].Biochemical Journal, 2020, 477(13):2439-2449.
[13] LEE S Y, KIM H U.Systems strategies for developing industrial microbial strains[J].Nature Biotechnology, 2015, 33(10):1061-1072.
[14] CHOI K R, JANG W D, YANG D, et al.Systems metabolic engineering strategies:Integrating systems and synthetic biology with metabolic engineering[J].Trends in Biotechnology, 2019, 37(8):817-837.
[15] CHEN X Z, ZHOU L, TIAN K M, et al.Metabolic engineering of Escherichia coli:A sustainable industrial platform for bio-based chemical production[J].Biotechnology Advances, 2013, 31(8):1200-1223.
[16] LEE S Y, KIM H U, CHAE T U, et al.A comprehensive metabolic map for production of bio-based chemicals[J].Nature Catalysis, 2019, 2(1):18-33.
[17] SANTOS C N S, XIAO W H, STEPHANOPOULOS G.Rational, combinatorial, and genomic approaches for engineering L-tyrosine production in Escherichia coli[J].Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(34):13538-13543.
[18] 孙金凤, 徐敏, 张峰, 等.利用木糖和葡萄糖合成乙醇的新型重组大肠杆菌的研究[J].微生物学报, 2004, 44(5):600-604.
SUN J F, XU M, ZHANG F, et al.Novel recombinant Escherichia coli producing ethanol from glucose and xylose[J].Acta Microbiologica Sinica, 2004, 44(5):600-604.
[19] 孙金凤, 田康明, 沈微, 等.底物选择性大肠杆菌共发酵葡萄糖和木糖产生乙醇[J].食品与发酵工业, 2018, 44(12):1-7.
SUN J F, TIAN K M, SHEN W, et al.Ethanol production from mixed glucose and xylose by substrate-selective Escherichia coli strains[J].Food and Fermentation Industries, 2018, 44(12):1-7.
[20] NIU D D, TIAN K M, PRIOR B A, et al.Highly efficient L-lactate production using engineered Escherichia coli with dissimilar temperature optima for L-lactate formation and cell growth[J].Microbial Cell Factories, 2014, 13(1):78.
[21] 周丽, 牛丹丹, 李宁, 等.基于Red重组系统和Xer重组系统的大肠杆菌多基因删除方法[J].微生物学通报, 2010, 37(6):923-928.
ZHOU L, NIU D D, LI N, et al.Multiple gene inactivation approach in Escherichia coli mediated by a combination of Red recombination and Xer recombination[J].Microbiology China, 2010, 37(6):923-928.
[22] 周丽, 田康明, 左志锐, 等.大肠杆菌琥珀酸和乙酸合成途径的删除及其重组菌株的D-乳酸发酵[J].生物工程学报, 2011, 27(1):31-40.
ZHOU L, TIAN K M, ZUO Z R, et al.Elimination of succinate and acetate synthesis in recombinant Escherichia coli for D-lactate production[J].Chinese Journal of Biotechnology, 2011, 27(1):31-40.
[23] ZHOU L, NIU D D, TIAN K M, et al.Genetically switched d-lactate production in Escherichia coli[J].Metabolic Engineering, 2012, 14(5):560-568.
[24] 诸葛健, 王正祥.工业微生物实验技术手册[M].北京:中国轻工业出版社, 1994.
ZHUGE J, WANG Z X.Manual of Industrial Microbiological Experiment Techniques[M].Beijing:China Light Industry Press, 1994.
[25] 王正祥. 微生物遗传育种[M].北京:高等教育出版社, 2020.
WANG Z X.Genetic Breeding of Microorganisms[M].Beijing:Higher Education Press, 2020.
[26] 韩梦圆, 王萌, 高明亮, 等.大肠杆菌LG101生物合成L-丙氨酸特征及作为细胞增殖调控节点的研究[J].微生物学通报, 2025, 52(3):980-991.
HAN M Y, WANG M, GAO M L, et al.Biosynthetic pathways of L-alanine and their role in the regulation of cell proliferation in Escherichia coli LG101[J].Microbiology China, 2025, 52(3):980-991.
[27] ZHOU L, ZUO Z R, CHEN X Z, et al.Evaluation of genetic manipulation strategies on d-lactate production by Escherichia coli[J].Current Microbiology, 2011, 62(3):981-989.
[28] EBERHARDT J, SANTOS-MARTINS D, TILLACK A F, et al.AutoDock vina 1.2.0:New docking methods, expanded force field, and Python bindings[J].Journal of Chemical Information and Modeling, 2021, 61(8):3891-3898.