小米是最早的谷类食品,谷子因其高度耐旱,在我国北方广泛种植[1]。在现代,小米可以提供大量营养并带来许多健康益处。小米是一种全谷物,富含多种营养素,包括蛋白质、脂肪、膳食纤维、维生素和矿物质等。这些营养素对维持身体健康起到了至关重要的作用[2]。蛋白质是小米中的主要营养成分,含量为11.2%~13.5%。小米的品质、口感由蛋白质的含量决定。此外,小米蛋白质中含有大量氨基酸,能够满足人体的基本营养需求。小米中的维生素B1与维生素E具有抗氧化功能,可以帮助身体抵抗自由基的侵害,减少细胞受损,降低癌症风险。在许多国家,小米是一种未被充分利用的粮食资源,因此小米作为人类食品和饮料的原材料有着巨大的潜力。
随着社会的迅速进步,人们对饮食结构提出了更高的要求,饮食习惯逐渐向合理的膳食结构以及具有保健功能的食品转变。其中,益生菌发酵食品在功能性食品行业中占比最大且增长最快,占整个功能性食品市场的60%~70%[3]。益生菌既能改善食品的风味和品质、延长食品的保质期,还可以调节肠道菌群平衡、降低胆固醇、预防便秘、延缓衰老等。据报道,发酵食品在发展中国家大约占饮食的60%,而谷物发酵饮料市场随着发酵食品市场的增加也有扩大趋势[4]。发酵食品在中国已有数千年历史,它的作用是可以通过调节肠道菌群对健康产生有益影响。发酵食品含有益生菌、必需氨基酸和生物营养素,以及重要的具有生物活性或有益健康的化合物[5]。
发酵饮料中蛋白质含量尤其重要,蛋白质在发酵过程中分解产生的氨基酸和多肽,能够增强饮料的鲜味和风味复杂性。蛋白质同时可以增加饮料的黏度和顺滑度,使其口感更加浓郁和饱满。高蛋白饮料符合现代消费者对健康食品的需求,尤其是针对健身人群、素食者或需要补充蛋白质的消费者。
本文选用不同工艺处理后的小米作为原料,通过研究不同工艺处理过的小米粉代替培养基中的主要碳源对益生菌增殖的影响,筛选小米粉熟化方式以及发酵菌种;以蛋白含量为响应值,通过单因素试验和响应面法优化小米发酵饮料的最佳配方,并检测发酵饮料的菌落总数以及发酵前后的氨基酸组成和挥发性物质,为新型发酵饮料的开发与利用提供新思路。
1 材料与方法
1.1 材料和设备
1.1.1 材料与试剂
小米,山西汾都香开发股份有限公司;鼠李糖乳酪杆菌(Lacticaseibacillus rhamnosus)、罗伊氏粘液乳杆菌(Limosilactobacillus reuteri)、嗜酸乳杆菌(Lactobacillus acidophilus),本实验室保存;α-淀粉酶、复合蛋白酶、糖化酶、果胶、羧甲基纤维素钠、甲醇、丙酮、石油醚、盐酸标准溶液、NaOH,国药集团化学试剂有限公司;MRS培养基,北京索莱宝科技有限公司。
1.1.2 仪器与设备
BrabenderKETSE20/40双螺杆挤压膨化机,德国杜伊斯堡布拉本德公司;IKA MultiDrive研磨机、RV8旋转蒸发仪,艾卡广州仪器有限公司;InfiniteM200PRO全波长多功能微孔板检测仪,上海帝肯贸易有限公司;7890A-5975C型气质联用仪,美国安捷伦科技有限公司;Biochrom30+全自动氨基酸分析仪,英国百康公司。
1.2 实验方法
1.2.1 小米粉不同预处理工艺
选用晋谷21号小米,取颗粒饱满的小米,磨粉过筛,备用。
1.2.1.1 挤压膨化处理
小米粉含水量为15%,前段温度60 ℃,中段温度150 ℃,后段温度110 ℃,螺杆转速为30 r/min,进料速度2.4 kg/h。挤压膨化后磨粉过80目筛。
1.2.1.2 湿热高压处理
将小米粉配制成0.1 g/mL的悬浊液,130 ℃,0.169 MPa压热处理30 min后取出冻干粉碎并过80目筛。
1.2.1.3 微波处理处理
将厚度小于0.2 cm的小米粉均匀放置在平板上,放入微波炉中,设置火力大小为中火,微波3 min,取出备用。
1.2.2 不同预处理后小米粉的持水性、持油性、吸水指数与水溶性指数
1.2.2.1 持水性
将样品和水(按1∶20,g∶mL)加入离心管中,25 ℃放置2 h,10 000 g离心10 min去除上清液,称量残留物的质量。持水性按公式(1)计算。
持水性![]()
(1)
式中:m1,样品的原始质量,g;m2,残留物的质量,g。
1.2.2.2 持油性
将0.1 g样品分别与2 mL玉米油混合,放入离心管中,25 ℃下放置2 h,10 000 g离心10 min去除上清液。持油性按公式(2)计算[6]。
持油性![]()
(2)
式中:m1,样品的原始质量,g;m2,残留物的质量,g。
1.2.2.3 吸水指数与水溶性指数
将2 g样品分散于25 mL蒸馏水中,30 ℃水浴30 min,5 000 r/min离心15 min,将上清液转移到铝容器中,105 ℃干燥至恒重取出。吸水指数与水溶性指数分别按公式(3)和公式(4)计算。
吸水指数![]()
(3)
水溶性指数![]()
(4)
式中:m3,沉淀物的质量,g;m4,干燥样品的质量,g;m5,溶解在上清液中固体的质量,g。
1.2.3 不同预处理小米粉替代碳源对益生菌的影响
采用原粉、挤压膨化、湿热高压、微波处理后的小米粉,将小米粉替代葡萄糖配制成MRS液体培养基,其中小米粉的量分别为碳源的25%、50%、100%、150%、200%。分别培养鼠李糖乳酪杆菌、罗伊氏粘液乳杆菌、嗜酸乳杆菌,采用稀释涂布的方法测量益生菌的生长量,以lg CFU/mL表示。
1.2.4 小米发酵饮料的制备及其优化
1.2.4.1 小米发酵饮料工艺流程
![]() 接种→均质→杀菌→成品
接种→均质→杀菌→成品
1.2.4.2 小米发酵饮料工艺优化
如表1所示,设料液比、接种量、发酵时间分别为A、B、C,并对其进行优化。将小米粉原料加水溶解,料液比(g∶mL)分别为1∶20、1∶10、1∶6.7、1∶5、1∶4。添加α-淀粉酶进行酶解,加酶量为10 U/mL,55 ℃水浴45 min后[7],将物料快速冷却,添加糖化酶80 U/mL以及复合蛋白酶40 U/mL在60 ℃进行复合酶解45 min,迅速冷却,过100目筛备用。酶解后原浆中益生菌的接种量分别设定为1%、2%、3%、4%、5%,在37 ℃下发酵;发酵时间分别为4、6、8、10、12 h。得到的小米发酵饮料在30 MPa条件下均质2次,进行巴氏杀菌。采用BCA试剂盒方法检验发酵液中蛋白含量。
表1 单因素试验设计方案
Table 1 Single-factor experimental design plan
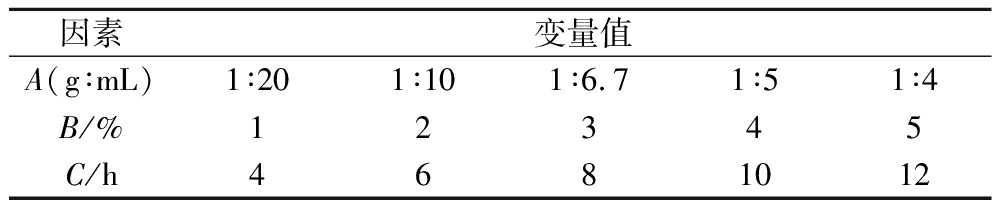
因素变量值A(g∶mL)1∶201∶101∶6.71∶51∶4B/%12345C/h4681012
1.3 小米发酵饮料响应面试验
依据Box-Behnken实验设计原则,结合单因素试验结果,料液比(A)、接种量(B)和发酵时间(C)各选取3个水平,进行三因素三水平实验,经统计分析后得到最优工艺。分析试验设计见表2。
表2 三因素三水平响应曲面分析试验设计表
Table 2 Three-factor three-level response surface analysis experimental design table

因素水平-101A(g∶mL)1∶201∶101∶6.7B/%234C/h81012
1.4 蛋白质量浓度模型建立
对实验数据进行回归方程分析,将响应变量与实验变量联系起来。遵循二阶多项式方程:对响应曲面优化蛋白质量浓度实验数据运用Design-expert 10.0.7数据分析软件对实验数据进行多元回归拟合,设料液比、接种量、发酵时间分别为A、B、C,以蛋白质量浓度为响应值进行多元回归拟合[8]。
1.5 微生物指标的测定
菌落总数测定,参照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》;大肠菌群测定,参照GB 4789.3—2025《食品安全国家标准 食品微生物学检验 大肠菌群计数》;金黄色葡萄球菌测定,参照GB 4789.10—2016《食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验》;霉菌和酵母菌测定,参照GB 4789.15—2016《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》。
1.6 氨基酸分析
取样品100 mL加入4 mL盐酸,放入氮吹仪中吹N2 15 min。再放入110 ℃的烘箱中进行24 h水解,取出并冷却。吸取试样2 mL,置于60 ℃中并在氮吹仪中脱酸,并通过0.22 μm的过滤小柱[9]。
色谱柱规格:200 mm×4.6 mm的色谱柱为阳离子树脂层析柱、紫外检测器、茚三酮为显色剂、钠盐为缓冲液、层析柱的温度55 ℃、反应温度138 ℃。脯氨酸检测波长440 nm,其他氨基酸检测波长570 nm[10]。
1.7 挥发性性成分分析
1.7.1 样品处理
称取8 mL样品加入顶空瓶中,于70 ℃下顶空萃取40 min;于250 ℃解吸5 min[11]。
1.7.2 仪器条件
色谱柱为DB-WAX(30.0 m×250 μm,0.25 μm);开始温度40 ℃,最终升至240 ℃并保持10 min。升温速度为:10 ℃/min。气化室温度为250 ℃;传输线温度240 ℃;载气气体为He;载气流量1.0 mL/min;不分流。
质谱条件:EI源;电子能量70 eV;四极杆150 ℃;离子源温度230 ℃;扫描模式Scan;扫描范围29~500 u。
1.8 数据处理
所有实验重复3次,结果均采用“平均值±标准差”的表示方法。数据统计使用Excel 2010软件进行,图形绘制使用Origin 2024软件,采用SPSS 25.0软件进行数据显著性分析(P<0.05)。
2 结果与分析
2.1 预处理小米粉的吸水指数与水溶性指数以及持水性持油性变化
由表3可知,小米原粉吸水指数最低,挤压膨化的吸水指数最高,蛋白质和淀粉与吸水指数高度相关。随着熟化过程中温度不断升高,蛋白质减少和淀粉增加,吸水指数增加。而经过湿热高压处理过的小米粉,其水溶性指数明显高于其他3种小米粉,原因可能是在蒸煮过程中,淀粉中的支链淀粉受到极大的破坏,导致了水溶性指数的增加[12]。可以看到挤压膨化和湿热高压处理后的小米粉持水性显著增加,湿热高压处理过的小米粉持油性显著升高。挤压膨化处理后的小米粉有较好的持水性以及持油性,良好的持水性在防止食品脱水与收缩方面有较强作用,高持油性的好处为降低脂质在肠道内的吸收。
表3 不同加工小米粉吸水指数、水溶性指数、持水性、持油性变化
Table 3 Effects of processing methods on water absorption index, water solubility index, water-holding, and oil-holding capacity of millet flour
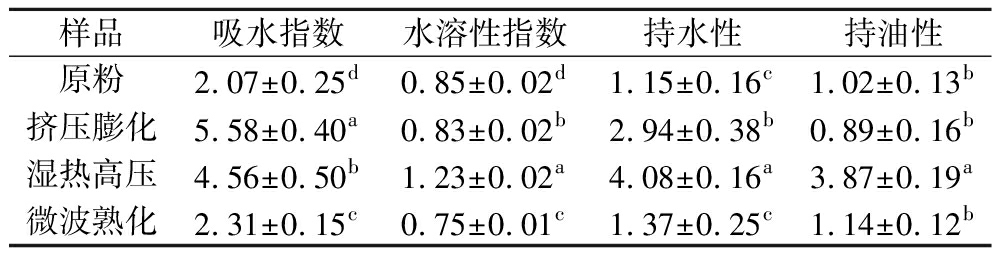
样品吸水指数水溶性指数持水性持油性原粉2.07±0.25d0.85±0.02d1.15±0.16c1.02±0.13b挤压膨化5.58±0.40a0.83±0.02b2.94±0.38b0.89±0.16b湿热高压4.56±0.50b1.23±0.02a4.08±0.16a3.87±0.19a微波熟化2.31±0.15c0.75±0.01c1.37±0.25c1.14±0.12b
注:同列不同小写字母表示差异显著(P<0.05)(下同)。
2.2 预处理小米粉对乳杆菌增殖的影响
由表4~表6可知,经不同处理的小米粉对乳杆菌增殖的影响存在显著差异,其中小米原粉相比于其他3种方式熟化的小米粉替代碳源对乳杆菌增殖效果一般。挤压膨化处理的小米粉随着添加量的增加,乳杆菌增殖量逐渐增多,由于挤压膨化产生高温和高压环境,小米的内部水分瞬间蒸发,从而形成压力差,并导致小米以多孔结构膨胀,淀粉糊化,小分子可溶性物质增加,同时大分子结构被破坏,由于糊化的淀粉更容易被微生物利用[13]。由表4可知,在促进嗜酸乳杆菌增殖上,其中挤压膨化处理后的小米粉在不同比例的添加量下的增殖效果显著高于其他处理方式。由表5可知,其鼠李糖乳酪杆菌在挤压膨化的小米粉作为主要碳源时,生长效果最好。湿热高压处理以及微波处理后的小米粉替代碳源对鼠李糖乳酪杆菌增殖效果接近。4种不同的小米粉随着样品添加量的增加,其对乳杆菌的增殖效果也越好。在这3种乳杆菌中,其鼠李糖乳酪杆菌在挤压膨化处理过的小米粉替代培养基中主要碳源制成的培养基中增殖效果最好,挤压膨化处理过的小米粉替代碳源的量为200%时,鼠李糖乳酪杆菌的增殖量为(9.48±0.10) lg CFU/mL,增殖量最大,最终在小米发酵饮料的选择鼠李糖乳酪杆菌作为小米饮料的发酵菌种,挤压膨化处理为小米粉的熟化方式。
表4 不同比例小米粉替代碳源对嗜酸乳杆菌增殖的影响 单位:lg CFU/mL
Table 4 Effect of replacing carbon source with different proportion of foxtail mille flour on the proliferation of L.acidophilus
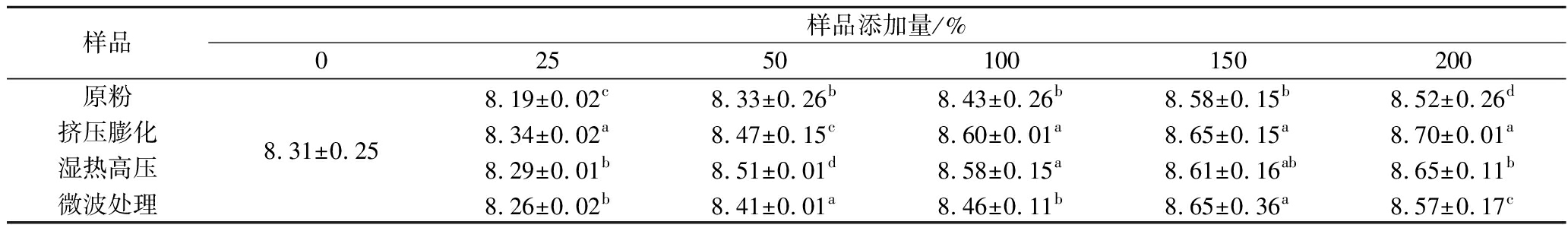
样品样品添加量/%02550100150200原粉挤压膨化湿热高压微波处理8.31±0.258.19±0.02c8.33±0.26b8.43±0.26b8.58±0.15b8.52±0.26d8.34±0.02a8.47±0.15c8.60±0.01a8.65±0.15a8.70±0.01a8.29±0.01b8.51±0.01d8.58±0.15a8.61±0.16ab8.65±0.11b8.26±0.02b8.41±0.01a8.46±0.11b8.65±0.36a8.57±0.17c
表5 不同比例小米粉替代碳源对鼠李糖乳酪杆菌增殖的影响 单位:lg CFU/mL
Table 5 Effect of different proportion of foxtail mille flour to replace carbon source on the proliferation of L.rhamnosus
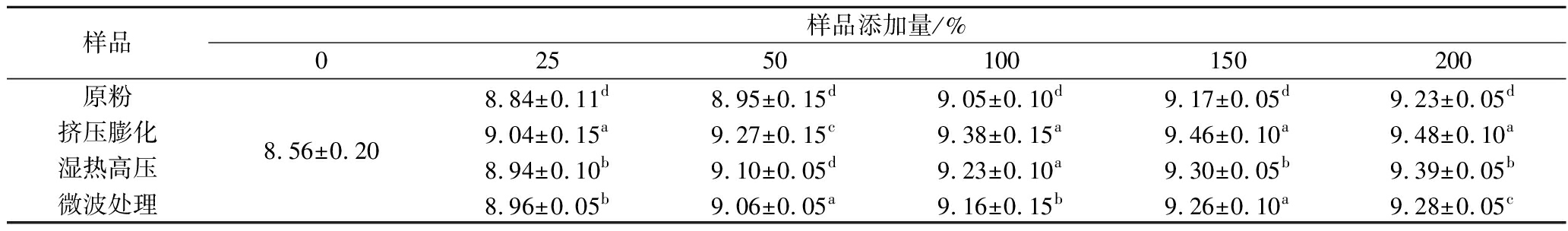
样品样品添加量/%02550100150200原粉挤压膨化湿热高压微波处理8.56±0.208.84±0.11d8.95±0.15d9.05±0.10d9.17±0.05d9.23±0.05d9.04±0.15a9.27±0.15c9.38±0.15a9.46±0.10a9.48±0.10a8.94±0.10b9.10±0.05d9.23±0.10a9.30±0.05b9.39±0.05b8.96±0.05b9.06±0.05a9.16±0.15b9.26±0.10a9.28±0.05c
表6 不同比例小米粉替代碳源对罗伊氏粘液乳杆菌增殖的影响 单位:lg CFU/mL
Table 6 Effect of replacing carbon sources with different proportions of foxtail mille tflour on the proliferation of L.reuteri
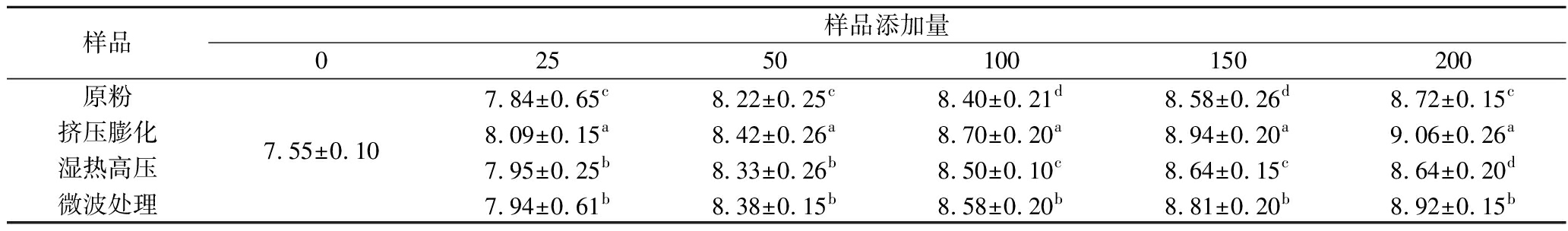
样品样品添加量02550100150200原粉挤压膨化湿热高压微波处理7.55±0.107.84±0.65c8.22±0.25c8.40±0.21d8.58±0.26d8.72±0.15c8.09±0.15a8.42±0.26a8.70±0.20a8.94±0.20a9.06±0.26a7.95±0.25b8.33±0.26b8.50±0.10c8.64±0.15c8.64±0.20d7.94±0.61b8.38±0.15b8.58±0.20b8.81±0.20b8.92±0.15b
2.3 发酵工艺的单因素试验
由图1可知,当料液比1∶10(g∶mL)时、接种量为3%、发酵时间为8 h,发酵后饮料中蛋白含量最高,由于料液比的增加,可能由于酶解时间的限制,当料液比在高于10%时,由于酶解作用增强从而饮料中的蛋白含量下降[14]。由图2可知,料液比为1∶10(g∶mL)、接种量为3%、发酵时间为8 h时、小米发酵饮料中的蛋白含量最高,为(6.94±0.25) mg/mL。由图2和图3可知,当料液比为1∶10(g∶mL)时、接种量为3%、发酵时间为10 h,饮料中的蛋白含量最高,蛋白质量浓度为(7.25±0.25) mg/mL。
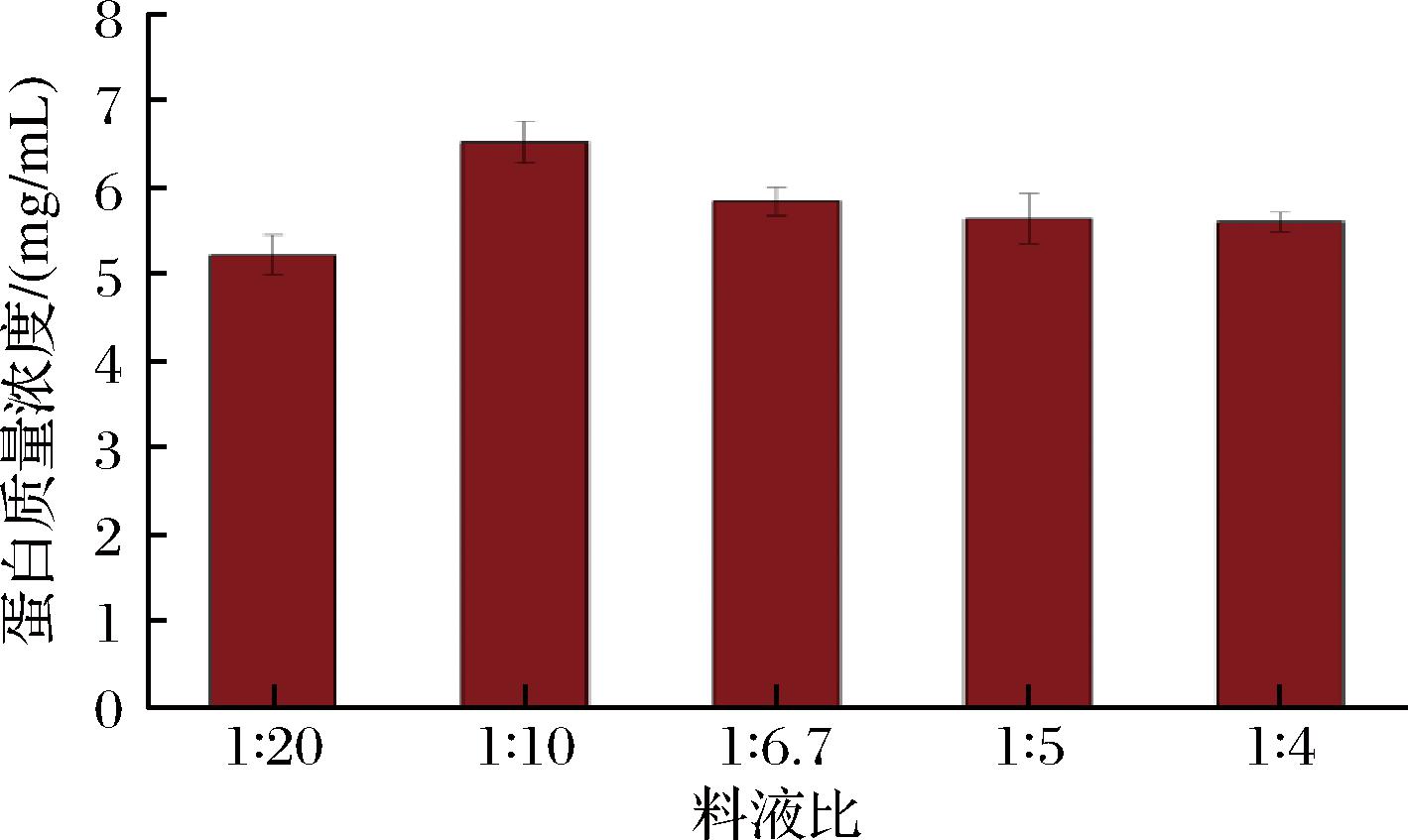
图1 料液比对发酵饮料蛋白含量的影响
Fig.1 Effect of solid-liquid ratio on protein content of fermented beverage
注:不同小写字母表示差异显著(P<0.05)(下同)。
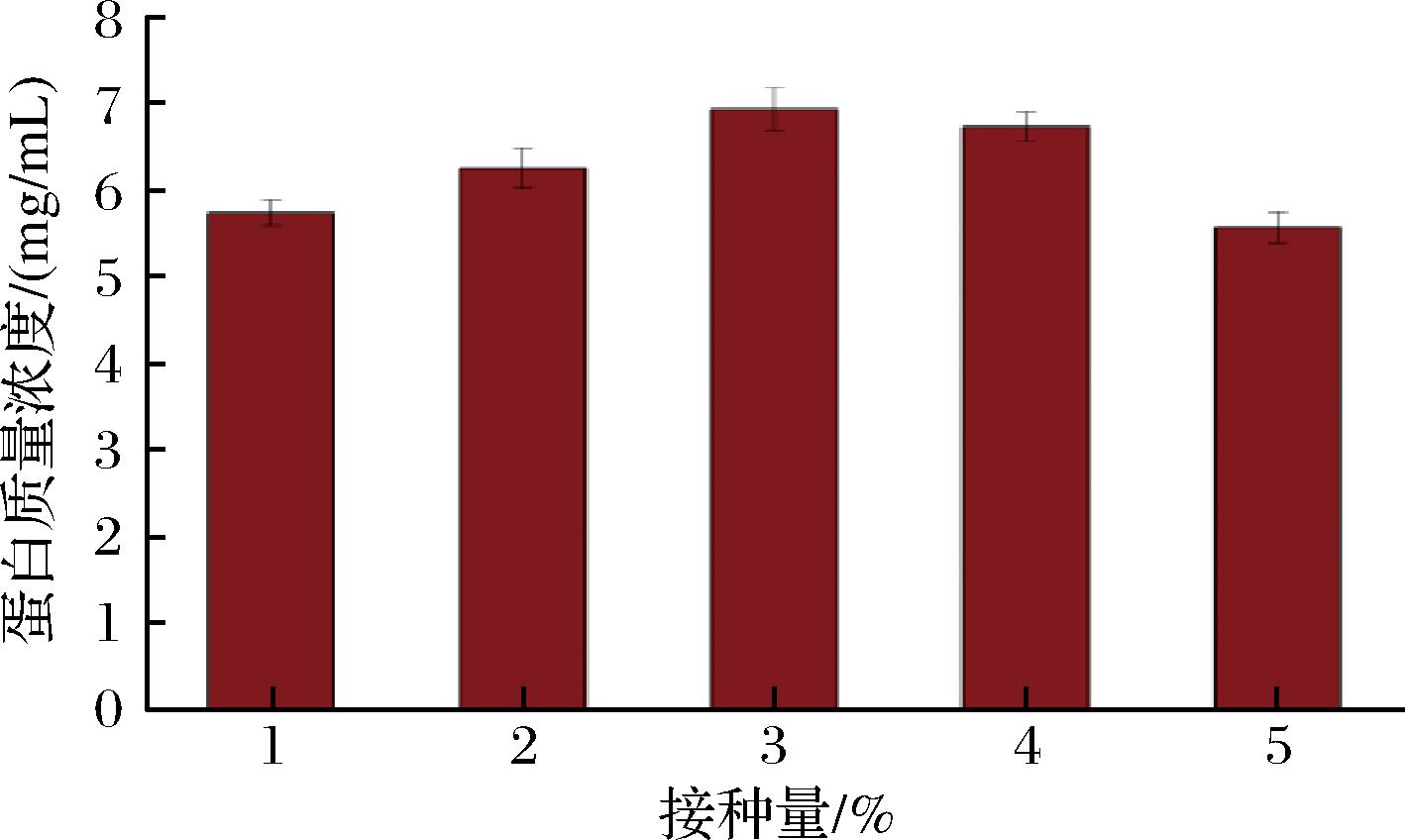
图2 接种量对发酵饮料蛋白含量的影响
Fig.2 Effect of inoculation amount on protein content of fermented beverage
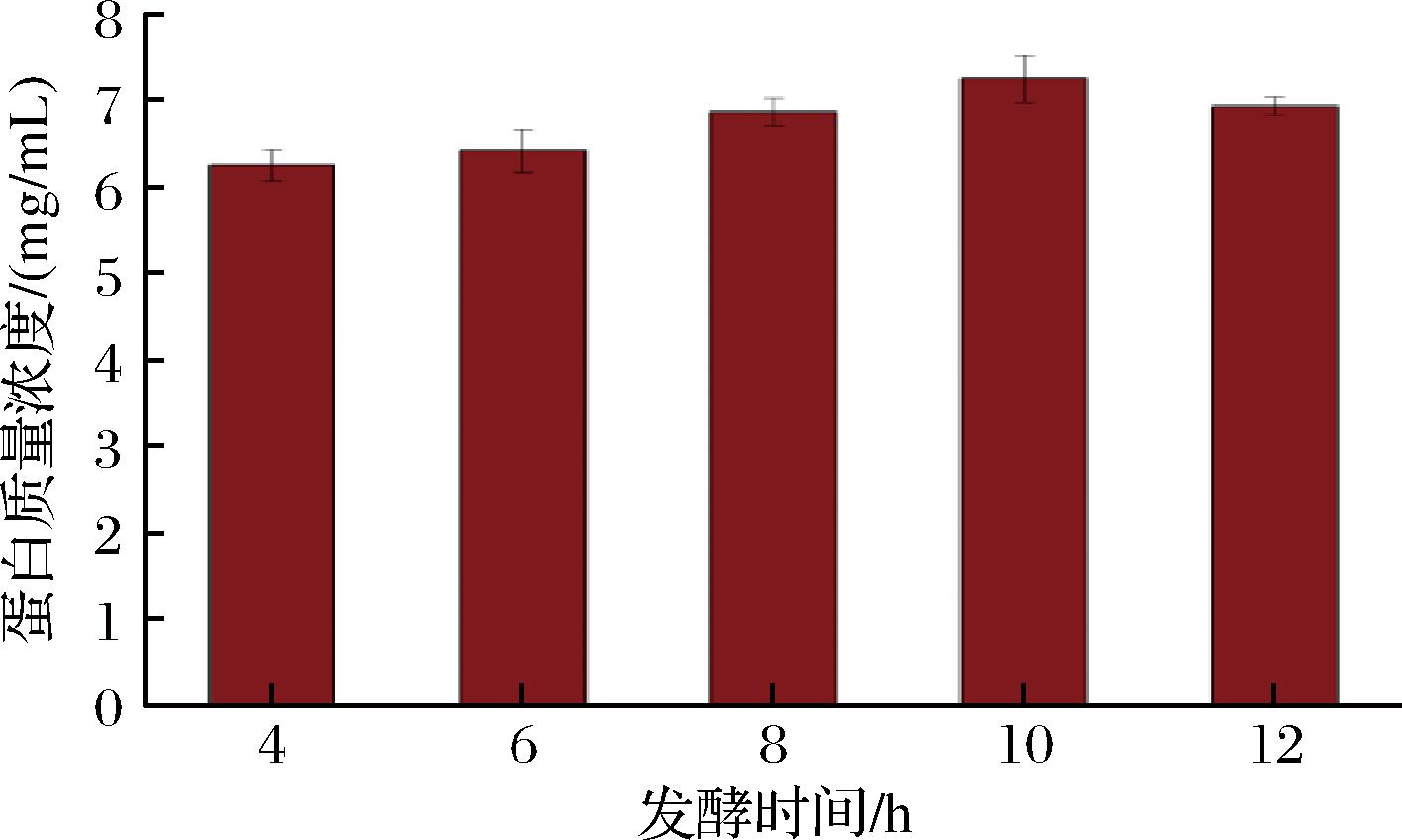
图3 发酵时间对发酵饮料蛋白含量的影响
Fig.3 Effect of fermentation time on protein content of fermented beverage
2.4 Box-Behnken试验结果与分析
2.4.1 模型的建立及方差分析
根据单因素试验结果,以小米发酵饮料中的蛋白含量为响应值,将料液比(A)、接种量(B)、发酵时间(C)这3个因素作为考察因素,进行Box-Behnken试验,其设计及结果见表7,实验方差分析见表8。
表7 响应曲面试验设计与结果
Table 7 Response surface test design and results
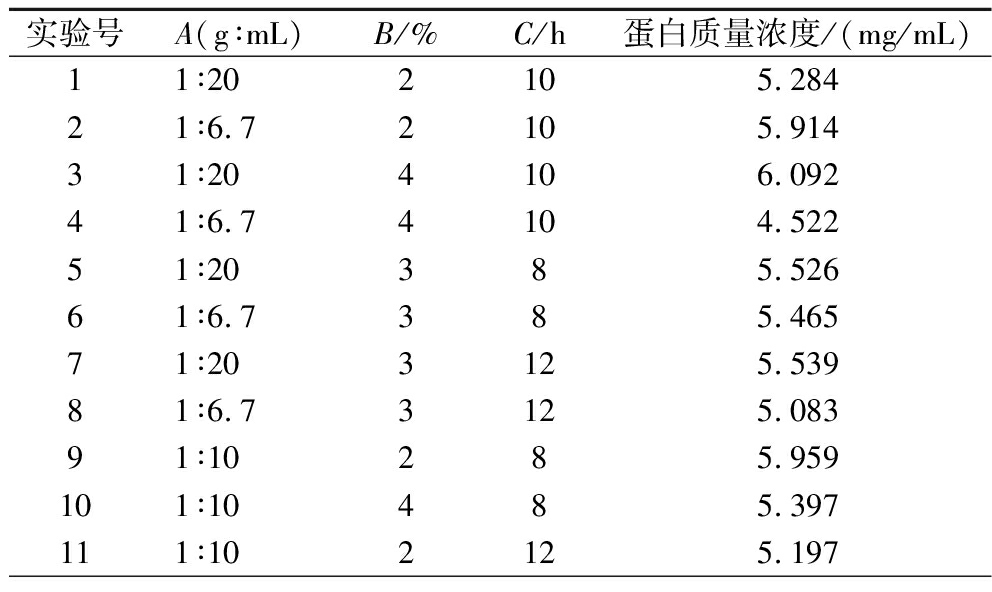
实验号A(g∶mL)B/%C/h蛋白质量浓度/(mg/mL)11∶202105.28421∶6.72105.91431∶204106.09241∶6.74104.52251∶20385.52661∶6.7385.46571∶203125.53981∶6.73125.08391∶10285.959101∶10485.397111∶102125.197
续表7
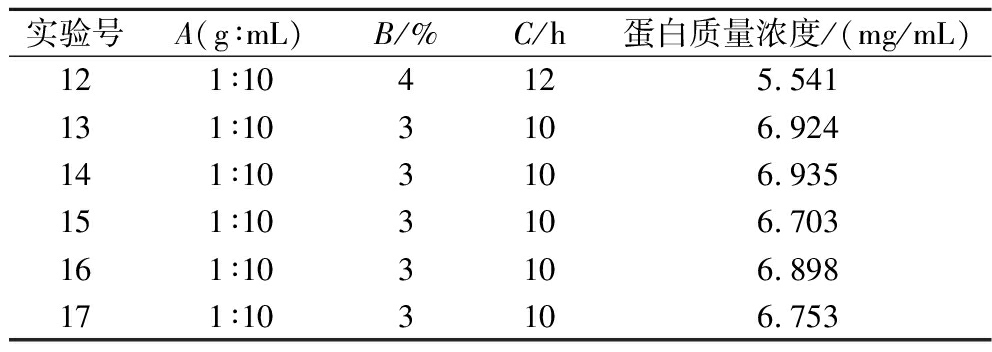
实验号A(g∶mL)B/%C/h蛋白质量浓度/(mg/mL)121∶104125.541131∶103106.924141∶103106.935151∶103106.703161∶103106.898171∶103106.753
表8 蛋白质量浓度模型及回归系数的回归分析结果
Table 8 Results of regression analysis of protein concentration model and regression coefficient
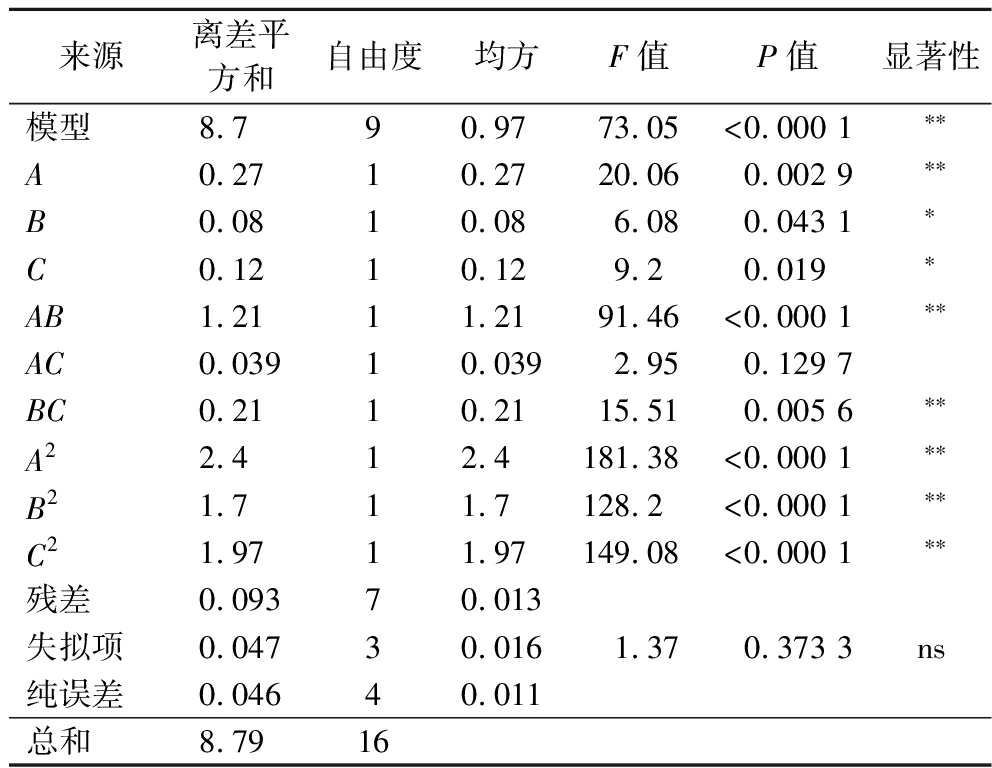
来源离差平方和自由度均方F值P值显著性模型8.7 90.97 73.05<0.000 1∗∗A0.2710.2720.060.002 9∗∗B0.0810.086.080.043 1∗C0.1210.129.20.019∗AB1.2111.2191.46<0.000 1∗∗AC0.03910.0392.950.129 7BC0.2110.2115.510.005 6∗∗A22.412.4181.38<0.000 1∗∗B21.711.7128.2<0.000 1∗∗C21.9711.97149.08<0.000 1∗∗残差0.09370.013失拟项0.04730.0161.370.373 3ns纯误差0.04640.011总和8.7916
注:P<0.01为极显著,用**表示;P<0.05为显著,用*表示;P>0.05为不显著,用ns表示;![]()
以蛋白质量浓度为响应值进行多元回归拟合,得到方程:Y=6.84-0.18A-0.1B-0.12C-0.55AB-0.099AC-0.23BC-0.75A2-0.63B2-0.68C2,进一步对该模型及回归系数进行回归分析,从表8可以看出该回归模型P<0.000 1(极显著),其失拟项P=0.373 3>0.05(不显著),进而表明模型拟合程度良好,可以对回归方程相应回归值进行预测,同时模型回归系数R2=0.989 5,调节后的R2=0.975 9,说明97.59%的数据可解释该模型,进而说明方程可靠性程度较高。
F值是方差分析中的重要指标,F值可以评价各变量对响应值的影响程度,F值越大,表明有关模型分量对响应影响贡献度越高。当显著性检验概率P<0.05时,表明该变量对响应值影响非常显著,具有数理统计意义。通过相关数据的分析可以表明,一次项料液比对蛋白质量浓度具有极显著影响(P<0.01),接种量、发酵时间对蛋白质量浓度具有显著影响(P<0.05),进而得到结论主效应关系为:A>C>B,即料液比>发酵时间>接种量。进而分析二次项交互作用AB、BC对小米发酵饮料蛋白质量浓度具有极显著的影响(P<0.01),而AC对饮料中的蛋白质量浓度的影响不显著(P>0.05)。
2.4.2 各因素的交互作用
使用Design-Expert10.0.7软件对实验结果构建响应面图,料液比(A)、接种量(B)、发酵时间(C)对蛋白质量浓度的影响见图4~图6。
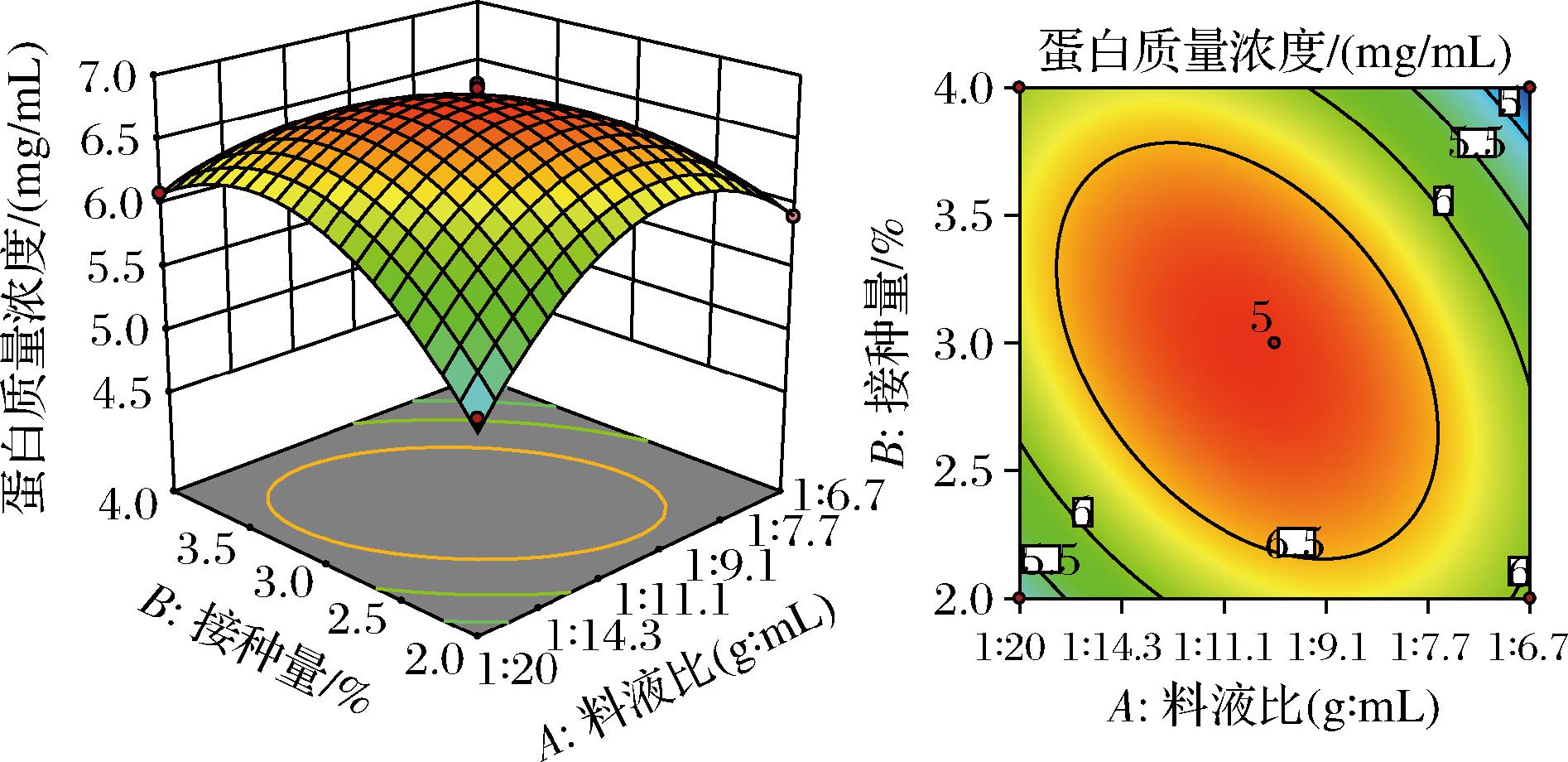
图4 AB交互作用对蛋白含量的影响
Fig.4 Effect of AB interaction on protein content
AB交互作用如图4所示,AB的交互曲面中伴随着接种量的不断增加,饮料中的蛋白质量浓度呈先增加后降低的趋势。仅考虑二者交互作用的条件下,当料液比为1∶14.3~1∶9.1(g∶mL)水平、接种量在2.5%~3.5%水平范围内时,蛋白质量浓度达到最大值。
AC交互作用如图5所示,AC交互曲面中料液比、发酵时间的增量带来蛋白质量浓度的变化坡度呈先增加后降低的趋势,仅考虑二者交互作用的条件下,当料液比为1∶14.3~1∶7.7(g∶mL)水平范围内、发酵时间为9~11 h时,蛋白质量浓度逐渐达到最大值。
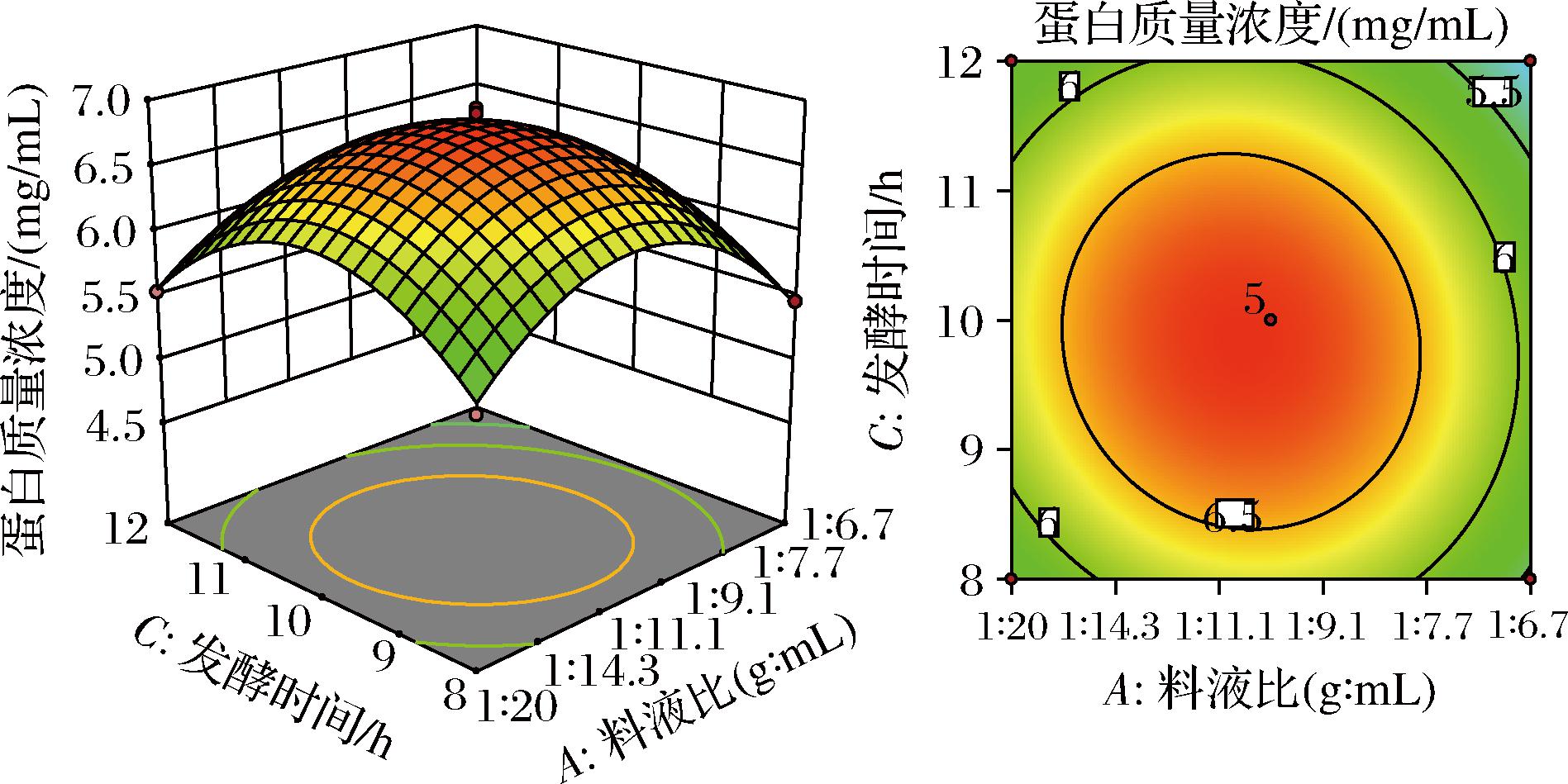
图5 AC交互作用对蛋白含量的影响
Fig.5 Effect of AC interaction on protein content
BC交互作用如图6所示,BC交互曲面中,蛋白质量浓度的变化坡度随发酵时间和接种量的增加呈先增加后降低的趋势,仅考虑二者交互作用的条件下,在接种量为2.5%~3.5%水平范围内、发酵时间为9~11 h时,其蛋白质量浓度取得最大值,曲面图与表8方差分析的结果也是相符合的。
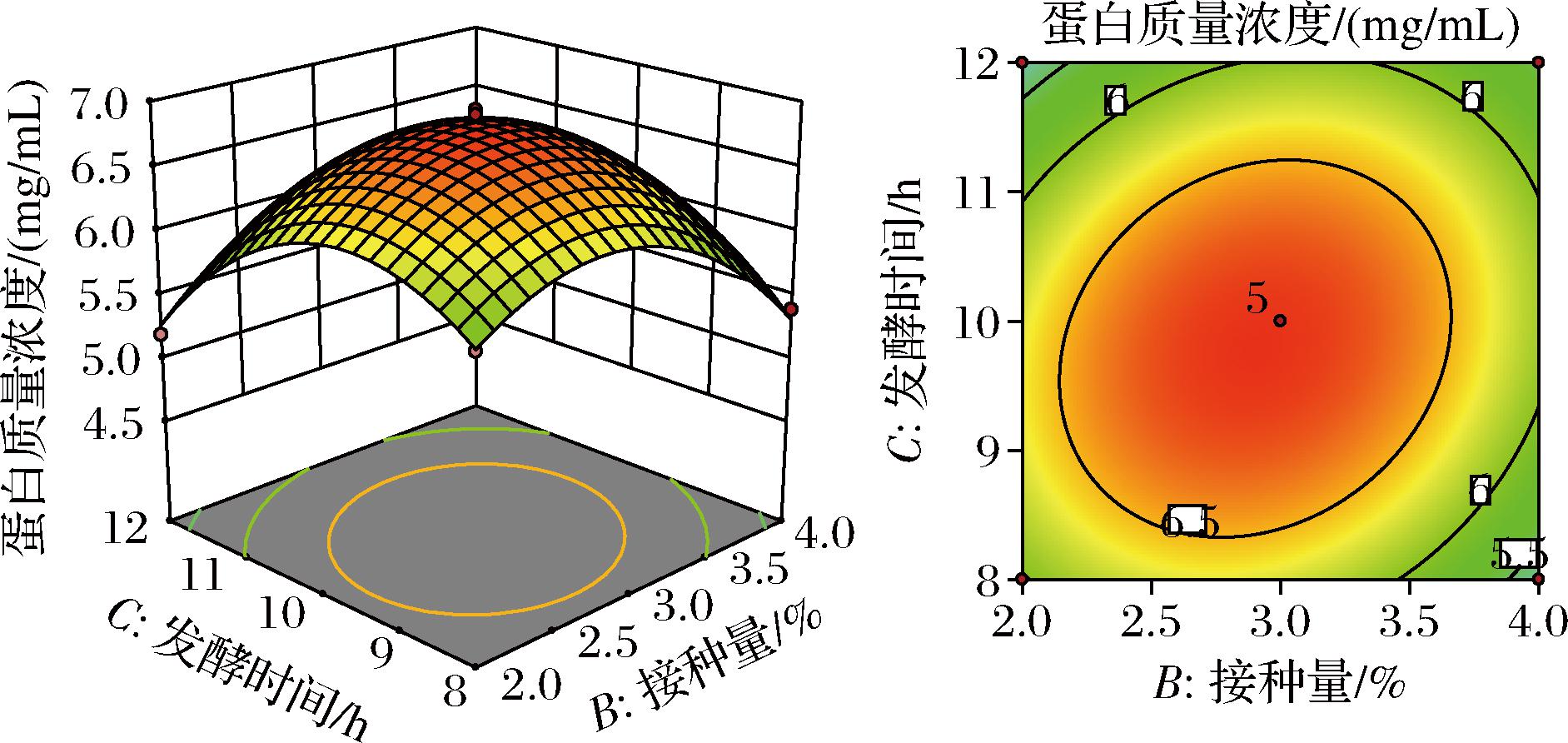
图6 BC交互作用对蛋白含量的影响
Fig.6 Effect of BC interaction on protein content
2.4.3 验证实验结果
根据回归方程模型,以蛋白质量浓度最大值为优化目标,得到预测的最优条件为:料液比为1∶10.49(g∶mL)、接种量为2.946%、发酵时间为9.814 h,根据实验实际条件,将条件修正为料液比为1∶10.49(g∶mL)、接种量为3.0%、发酵时间为9.8 h,在此最优条件下经3组平行实验,得到发酵饮料的蛋白质量浓度为(6.824±0.127) mg/mL,与预测值总蛋白质量浓度为6.860 mg/mL相差在5%范围内,证实了预测值和实验值之间的良好相关性。
2.5 小米发酵饮料成品的检验结果与分析
2.5.1 小米发酵饮料的微生物指标测定
由表9可知,分别参照国家标准测定了小米发酵饮料中的菌落总数、大肠杆菌、金黄色葡萄球菌,以及霉菌和酵母菌,其中菌落总数的检测结果为<10,符合国家标准,其余菌均未在小米发酵饮料中检出。其微生物指标与国家规定的安全标准相符。
表9 小米发酵饮料微生物指标测定 单位:CFU/mL
Table 9 Determination of microbiological index of millet fermented beverage
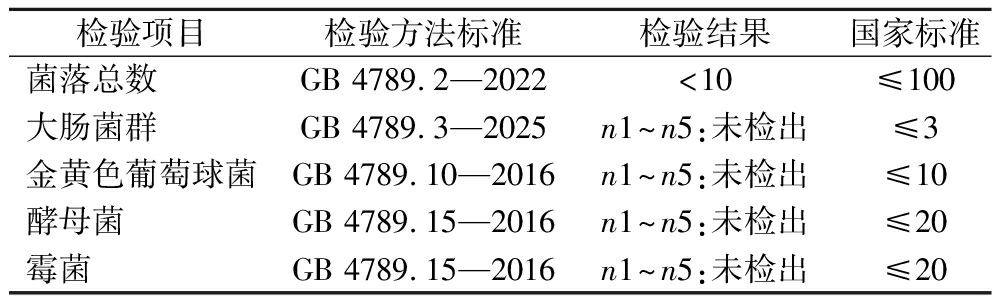
检验项目检验方法标准检验结果国家标准菌落总数GB 4789.2—2022<10≤100大肠菌群GB 4789.3—2025n1~n5:未检出≤3金黄色葡萄球菌GB 4789.10—2016n1~n5:未检出≤10酵母菌GB 4789.15—2016n1~n5:未检出≤20霉菌GB 4789.15—2016n1~n5:未检出≤20
2.5.2 氨基酸分析结果
由表10可知,小米发酵饮料中总游离氨基酸含量(5.852±0.001) mg/mL,而发酵后的总游离氨基酸增加到(6.558±0.021) mg/mL,总游离氨基酸含量升高12.06%,同时发酵前必需游离氨基酸含量是(1.976±0.002) mg/mL,而发酵后的必需游离氨基酸增加到(2.201±0.015) mg/mL,必需游离氨基酸含量升高11.39%,在发酵后的饮料中必需游离氨基酸占游离氨基酸总量的33.5%。证明该饮料含有大量的游离氨基酸[15]。含有6种人体必需游离氨基酸,以及幼儿体内不能合成的精氨酸和组氨酸。发酵后的饮料总游离氨基酸升高,必需游离氨基酸含量升高,人体必需的氨基酸含量升高,必需游离氨基酸占游离氨基酸总量的33.5%,其中含量最高的是亮氨酸,亮氨酸可以促进生长发育,提高免疫力,保护肝脏等功能[16]。游离氨基酸中的呈味氨基酸谷氨酸、酪氨酸含量的增加,可以给发酵饮料提供更丰富的味觉感受。
表10 小米饮料发酵前和发酵后的氨基酸结果 单位:mg/mL
Table 10 Amino acid results of millet beverage before and after fermentation
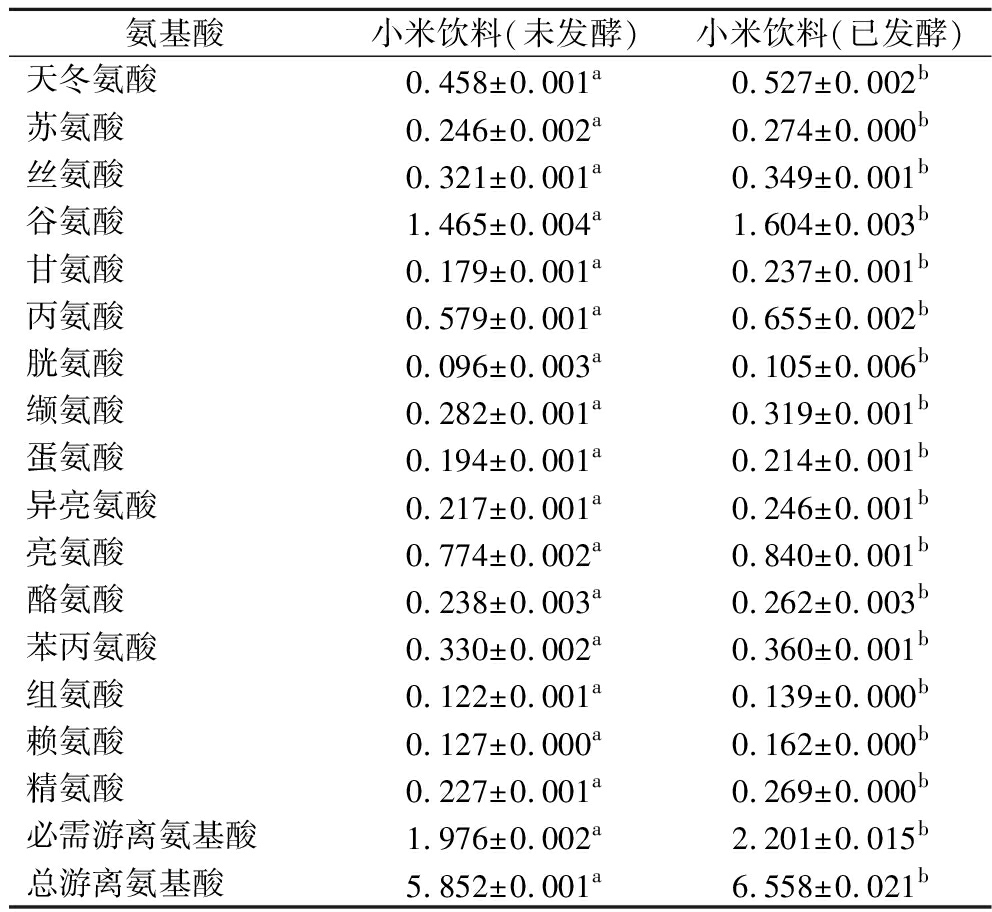
氨基酸小米饮料(未发酵)小米饮料(已发酵)天冬氨酸0.458±0.001a0.527±0.002b苏氨酸0.246±0.002a0.274±0.000b丝氨酸0.321±0.001a0.349±0.001b谷氨酸1.465±0.004a1.604±0.003b甘氨酸0.179±0.001a0.237±0.001b丙氨酸0.579±0.001a0.655±0.002b胱氨酸0.096±0.003a0.105±0.006b缬氨酸0.282±0.001a0.319±0.001b蛋氨酸0.194±0.001a0.214±0.001b异亮氨酸0.217±0.001a0.246±0.001b亮氨酸0.774±0.002a0.840±0.001b酪氨酸0.238±0.003a0.262±0.003b苯丙氨酸0.330±0.002a0.360±0.001b组氨酸0.122±0.001a0.139±0.000b赖氨酸0.127±0.000a0.162±0.000b精氨酸0.227±0.001a0.269±0.000b必需游离氨基酸1.976±0.002a2.201±0.015b总游离氨基酸5.852±0.001a6.558±0.021b
注:同行不同小写字母表示差异显著(P<0.05)。
2.5.3 挥发性物质分析
由电子版增强出版附表1(https://doi.org/10.13995/jcnki.11-1802/ts.042095)可知,小米饮料样品发酵前后共检测到165种挥发性风味物质,其中包括醇类物质39种,醛类化合物26种、酮类化合物19种、酸类化合物17种、酯类物质4种、烯烃类化合物19种、烷烃类化合物16种以及其他类化合物25种。
挥发性风味物质含量顺序为:发酵后小米饮料平行样品>发酵前小米饮料平行样品,发酵后小米饮料的各个挥发性风味物质含量相比发酵前均有提升,表明发酵工艺有利于增加小米饮料挥发性风味物质含量[17]。
酸类物质在发酵后小米饮料风味中占主体地位,其次为醛类、醇类、酮类和酯类物质,其中在酸类物质中己酸占比最高,约为27.8%,其次为乙酸和戊酸,含量分别为1.66%和1.17%。酸类是一种重要风味物质,游离脂肪酸就是酸类中的一类代表性风味成分,酸性物质带来不同的风味。己酸是己酸乙酯的前体物质。研究表明在发酵过程中,己酸菌使醇类和醋酸经过酪酸生成己酸,己酸经酯化反应生成己酸乙酯,该反应又可逆向水解将己酸乙酯还原为己酸,故而发酵过程中的己酸与己酸乙酯含量是不断变化的,在各种因素影响下最终达到动态平衡,己酸的味觉阈值为8.6 mg/L,在食品的有机酸中属于中等偏上,呈味特点为“酸味较柔和”,而戊酸的特征风味为酿香、奶酪和果香[18]。
发酵后小米饮料风味的醛类物质中己醛、2,4-癸二烯醛和2-辛烯醛占比较高,含量分别为4.37%、5.69%和2.18%,醛类化合物是一种阈值低的挥发性化合物,对风味的贡献较大。己醛具有草香味,而2,4-癸二烯醛和2-辛烯醛具有清香味的物质,一定程度上能作为提高小米饮料的主要香味来源[19]。
醇类物质的气味阈值较高,对风味的贡献不是特别明显,其中随着浓度与碳链长度的增加,可产生一类香气为脂肪香和清木香,这两种风味物质可以在风味的改良上起到积极作用。醇类物质不仅可以助香,并可以作为前体物质在合成酯类物质上,其中在发酵后的小米饮料中醇类物质1-己醇和1-戊醇占比最高,分别为7.85%和1.93%。1-己醇和1-戊醇主要表现出柔和的刺激感和微甜、浓厚,但作为短链醇的挥发性较强,稳定性不高[20]。
一般而言,酮被认为是理想的挥发性成分,并有助于产生甜味和果香味。小米饮料发酵后新产生了3-辛烯-2-酮,3-辛烯-2-酮具有酮香、甜香和干草香,其中发酵后的小米饮料的3-辛烯-2-酮含量相比发酵前提升了0.66%。小米饮料发酵后新产生的2,3-丁二酮有强烈的奶油香味、发酵香味、乳脂香味、甜香味等[21]。其中发酵后的小米饮料2,3-丁二酮含量相比发酵前提升了7.13%。
脂质氧化产生的游离脂肪酸与醇类物质发生酯化反应从而形成酯类物质,短链酯类阈值较低但其挥发性较强,产生的香味与类似水果和酒类相近,对风味的贡献较大。发酵后小米饮料中的正己酸乙烯酯含量最高,约为2.23%,正己酸乙烯酯作为一种无色液体,可以作为风味增强剂,为食品增添特定的香气[22]。其挥发性的特点使其能够迅速扩散到空气中。
其他类化合物中值得关注的是发酵后的小米饮料中出现了乙偶姻,其含量为1.18%,其是乳酸菌的一种特殊发酵产物。
综上,经过发酵工艺后的小米饮料可以有效增加小米饮料中的挥发性风味物质,从而提升小米饮料的品质。
3 结论
小米发酵饮料的最佳制作流程为选取挤压膨化方式熟化后的小米粉,使用鼠李糖乳酪杆菌进行发酵;最佳条件为料液比1∶10.5(g∶mL)、接种量为3.0%、发酵时间9.8 h,在此最优条件下经3组平行实验,得到发酵饮料的蛋白质量浓度为(6.824±0.127) mg/mL,与预测值相差在5%范围内,从而证明预测值和实验值之间良好的相关性。该条件下得到的小米发酵饮料色泽呈金黄色,甜度适中。小米饮料中总游离氨基酸含量5.852 mg/mL,含有6种人体必需游离氨基酸,包括婴幼儿体内不能自我合成的精氨酸与组氨酸。发酵后的饮料总游离氨基酸升高,必需游离氨基酸含量升高,人体必需的氨基酸含量升高,必需游离氨基酸占游离氨基酸总量的33.5%。小米饮料样品发酵前后共检测到165种挥发性风味物质,酸类物质在发酵后小米饮料风味中占主体地位,其次为醛类、醇类、酮类和酯类物质,其中在酸类物质中己酸占比最高,约为27.8%,其次为乙酸和戊酸,含量分别为1.66%和1.17%。酸类是一种重要风味物质,游离脂肪酸就是酸类中的一类代表性风味成分,酸性物质带来不同的风味。本研究所得到的新型小米发酵饮料为杂粮类发酵饮料的开发与利用提供了新的思路。本研究有助于开发出新型发酵保健食品,为新型小米发酵饮料的进一步开发和有效利用提供了科学依据及数据支持。
[1] 刘俊英, 谢国莉, 危晴, 等.小米中脂肪酸的GC-MS法测定及营养价值分析[J].食品研究与开发, 2012,33(2):165-168.
LIU J Y, XIE G L, WEI Q, et al.Determination on fatty acids of millet through GC-MS and analysis on nutritional value[J].Food Research and Development, 2012,33(2):165-168.
[2] 许寅生, 郭亚丽, 王玉祥, 等.谷子的营养价值及产品开发[J].农业科技通讯, 2018(3):152-155.
XU Y S, GUO Y L, WANG Y X, et al.Nutritional value and product development of millet[J].Bulletin of Agricultural Science and Technology, 2018(3):152-155.
[3] 熊凤麒, 袁吕江.高效液相色谱法测定小米维生素E含量研究[J].西南农业大学学报, 1992,14(6):525-527.
XIONG F L, YUAN L J.Determination of vitamin e in millef grain by high performance liquid chromatography[J].Journal of Southwest Agricultural University, 1992,14(6):525-527.
[4] 赵闪闪, 张一凡, 肖志刚, 等.辽宁地区小米矿物元素与母壤矿物质的相关性研究[J].食品工程, 2016(1):15-19.
ZHAO S S, ZHANG Y F, XIAO Z G, et al.The correlation study between Liaoning regional mineral elements of millet and it’s parent soil[J].Food Engineering, 2016(1):15-19.
[5] 赵宇晗, 张嘉欣, 葛晓欣, 等.猴头菇小米饮料的制备工艺[J].食品工业, 2022,43(5):76-81.
ZHAO Y H, ZHANG J X, GE X X, et al.Production of Hericium erinaceus and millet beverage[J].The Food Industry, 2022,43(5):76-81.
[6] 王晨, 吴卫国, 赵俊杰, 等.螺杆转速与加水量对方便粥品质的影响[J].中国食品学报, 2023,23(8):296-305.
WANG C, WU W G, ZHAO J J, et al.Influence of screw speed and water addition amount on the quality of instant porridge[J].Journal of Chinese Institute of Food Science and Technology, 2023,23(8):296-305.
[7] 左旭, 吴兴壮.益生菌发酵谷物饮料研究进展[J].农产品加工, 2024(15):100-104;107.
ZUO X, WU X Z.Research progress of probiotic fermented cereal beverage[J].Farm Products Processing, 2024(15):100-104;107.
[8] 代亚西. 鲜食玉米乳酸菌发酵工艺优化及产品开发[D].长春:吉林大学, 2024.
DAI Y X.Optimisation of fermentation process and product developmentof lactic acid bacteria from fresh corn[D].Changchun:Jilin University, 2024.
[9] 葛家驹, 王贵一, 周畅, 等.发酵芒果饮料的开发及其挥发性香气、氨基酸的测定[J].食品工业, 2023,44(11):309-316.
GE J J, WANG G Y, ZHOU C, et al.Development of fermented mango beverage and determination of its volatile and amino acid components [J].The Food Industry, 2023,44(11):309-316.
[10] 陈金华, 王英姿, 黄建安, 等.茶饮料中游离氨基酸总量测定方法的改进[J].食品工业, 2019,40(10):191-195.
CHEN J H, WANG Y Z, HUANG J A, et al.Determination methods improvement of the amino acid total quantity in tea beverages[J].The Food Industry, 2019,40(10):191-195.
[11] 移兰丽. 荔枝风味物质分析及其乳酸菌发酵饮料的研发[D].南昌:江西农业大学, 2016.
YI L L.Litchi flavor analysis and the development of lactic acid bacteria fermented litchi beverage[D].Nanchang:Jiangxi Agricultural University, 2016.
[12] 黄美香, 林河通, 李辉, 等.龙眼果实加工技术研究进展[J].包装与食品机械, 2012,30(2):48-52;56.
HUANG M X, LIN H T, LI H, et al.Advances in the researches of processing technologies of Longan fruits[J].Packaging and Food Machinery, 2012,30(2):48-52;56.
[13] BENHUR D R, BHARGAVI G, KALPANA K, et al.Development and standardization of sorghum Pasta using extrusion technology[J].Journal of Food Science and Technology, 2015, 52(10):6828-6833.
[14] 龚菲菲, 阎光宇.玉米淀粉发酵饮料的工艺流程优化及其影响因素研究[J].工业微生物, 2024,54(5):10-12.
GONG F F, YAN G Y.Optimization and influence factors of the process of corn starch fermented beverages [J].Industrial Microbiology, 2024,54(5):10-12.
[15] BONKE A, SIEUWERTS S, PETERSEN I L.Amino acid composition of novel plant drinks from oat, lentil and pea[J].Foods, 2020, 9(4):429.
[16] POVEDA J M.Biogenic amines and free amino acids in craft beers from the Spanish market:A statistical approach[J].Food Control, 2019, 96:227-233.
[17] 费永涛, 黄一鹤, 屈春云, 等.覆盆子乳酸菌饮料发酵工艺优化及挥发性风味物质分析[J].中国酿造, 2023,42(7):214-220.
FEI Y T, HUANG Y H, QU C Y, et al.Optimization of fermentation process and volatile flavor substances of raspberry lactic acid bacteria beverage[J].China Brewing, 2023,42(7):214-220.
[18] BAI S, YOU L Q, JI C, et al.Formation of volatile flavor compounds, Maillard reaction products and potentially hazard substance in China stir-frying beef Sao zi[J].Food Research International, 2022, 159:111545.
[19] LI S Q, BI P F, SUN N, et al.Effect of sequential fermentation with four non-Saccharomyces and Saccharomyces cerevisiae on nutritional characteristics and flavor profiles of kiwi wines[J].Journal of Food Composition and Analysis, 2022, 109:104480.
[20] 崔香香, 白飞荣, 于学健, 等.谢瓦散囊菌CICC 41584产香特性及在浓香型白酒大曲生产中的应用[J].食品与发酵工业, 2019,45(21):60-67.
CUI X X, BAI F R, YU X J, et al.Aroma characteristics of Eurotium chevalieri CICC 41584 and its application in aroma Baijiu Daqu production[J].Food and Fermentation Industries, 2019,45(21):60-67.
[21] 袁辛锐, 杨其长, 王芳,等.紫胡萝卜复合发酵饮料的研制及其挥发性风味物质分析[J].食品工业科技, 2024,45(2):201-209.
YUAN X R, YANG Q C, WANG F, et al.Development and volatile flavor substances analysis of purple carrot compound fermented beverage[J].Science and Technology of Food Industry, 2024,45(2):201-209.
[22] LIU X, XU S J, WANG M K, et al.Effect of mixed fermentation with Pichia fermentans, Hanseniaspora uvarum, and Wickeramomyces Anomala on the quality of fig (Ficus carica L.) wines[J].Journal of Food Processing and Preservation, 2021, 45(2):e15169.