红糖是以甘蔗为原料,经过压榨、澄清、熬煮等工艺制作而成的一种重要的调味品,在食品加工和烹饪中应用广泛[1]。由于红糖未经分蜜处理,其很好地保留了蔗汁中的营养成分,富含蛋白质、氨基酸、维生素、微量元素及多种生物活性成分,在我国也被当作保健食品[2-4]。然而,传统红糖风味单一,主要作为糖源用于食品加工领域,不能充分发挥红糖自身营养保健的优势。随着我国经济社会持续发展,消费者的需求发生转变,将红糖进行深加工,开发具有明确功效的健康食品,对于满足人民日益增长的对美好生活的需要具有重要意义。
乳酸菌是代谢碳水化合物后主要产物为乳酸的一类细菌的总称[5-6]。乳酸菌发酵可赋予食物特有风味,同时可以提升食物营养价值、延长食物保藏时间,已成为一种安全、经济且技术成熟的工艺,并广泛应用于乳制品、果蔬及粮食等食品的精深加工[7]。近年来,许多研究聚焦于利用植物乳植杆菌、副干酪乳酪杆菌等乳酸菌对各种植物基原料的发酵,与未发酵相比,乳酸菌发酵可显著提升植物基原料的酸味,其中酚类、酸类和酮类物质含量均提高,且新增了醛类和含硫物质,极大地丰富了植物基原料的风味物质,在改善感官特性的同时,也提升了食品的营养价值[8-11]。
本研究以红糖为原料,开展鼠李糖乳酪杆菌NM-94和嗜酸乳杆菌TYCA06复合发酵红糖发酵工艺技术研究,通过液态发酵技术制备发酵红糖液。依据发酵红糖液pH及DPPH自由基清除率优化发酵工艺参数,综合感官评价结果和抗氧化功效制定发酵红糖饮品的配制方案,为拓宽红糖原料的深加工途径、提高红糖原料的经济附加值、创制新型功能性红糖产品提供一定的科学依据。
1 材料与方法
1.1 材料与试剂
红糖,中国糖类酒业集团有限公司;DPPH、ABTS,北京博奥拓达科技有限公司;无水乙醇,福晨(天津)化学试剂有限公司;鼠李糖乳酪杆菌NM-94,北京科拓恒通生物技术股份有限公司;嗜酸乳杆菌TYCA06,Bioflag锦旗生物集团。
1.2 仪器与设备
FOX4000电子鼻,Alpha M.O.S公司;TS-5000Z电子舌,Insent公司;手持pH计,梅特勒-托利多仪器有限公司;DL-CJ-2 ND-I型洁净工作台,北京东联哈尔仪器制造有限公司;SPX-150BⅢ生化培养箱,天津市泰斯特仪器有限公司。
1.3 实验方法
1.3.1 发酵红糖液的制备
本实验发酵红糖液的制备方法是建立在笔者前期开展的发酵菌种筛选及双联复配发酵实验基础上。称取一定量的红糖,加入去离子水溶解,得到质量浓度为150 g/L的红糖原液。将红糖原液加热灭菌,得到灭菌红糖原液。将一定量复配菌粉(鼠李糖乳酪杆菌∶嗜酸乳杆菌=1∶1)投入降温后的灭菌红糖原液中混匀,经一定条件发酵后得到发酵红糖液。
1.3.2 发酵工艺参数优化的单因素试验
分别进行发酵时间、发酵温度、接菌量的单因素试验,通过测定发酵红糖液pH及DPPH自由基清除率确定各个单因素的最佳范围。
在发酵温度为37 ℃、复配菌粉添加总量为0.2 g/L时,测定发酵时间分别为12、24、36、48、72 h时制备发酵红糖液pH及DPPH自由基清除率。
在发酵时间为36 h、复配菌粉添加总量为0.2 g/L时,测定发酵温度分别为27、32、37、42、47 ℃时制备发酵红糖液pH及DPPH自由基清除率。
在发酵时间为36 h、发酵温度为37 ℃时,测定复配菌粉添加总量分别为0.05、0.1、0.2、0.5、1 g/L时制备发酵红糖液pH及DPPH自由基清除率。
1.3.3 响应面法试验设计
在上述单因素试验结果的基础上,进一步使用Box-Behnken响应面法以确定制备发酵红糖液的最优参数,试验设计各因素水平如表1所示。而DPPH自由基清除率是衡量发酵红糖液功效的重要指标,DPPH自由基清除率越高,发酵红糖液的抗氧化能力越强,故以发酵时间、发酵温度以及复配菌粉添加总量为自变量,发酵红糖液的DPPH自由基清除率为响应值,进行3因素3水平响应面试验分析。
表1 响应面试验设计因素水平
Table 1 Response surface experimental design factors and levels

水平因素发酵时间/h发酵温度/℃菌粉添加总量/(g/L)-124320.1036370.2148420.3
1.3.4 发酵红糖液pH值测定方法
参考GB 5009.237—2016《食品安全国家标准 食品中pH值的测定》,将发酵完成的红糖液从培养箱取出,在超净台内搅拌均匀,无菌取样,使用pH计测定样品的pH值。
1.3.5 DPPH自由基清除率检测方法
按需配制0.1 mmol/L的DPPH溶液。按表2加入样品和试剂,摇匀,37 ℃反应30 min。以体积分数80%乙醇调零,517 nm处测定吸光度。
表2 DPPH自由基清除能力反应体系
Table 2 DPPH free radical scavenging ability reaction system

编号样品反应体系A21.5 mL 80% 乙醇+30 μL样品A11.5 mL 0.1 mmol/L 的DPPH溶液+30 μL样品A01.5 mL 0.1 mmol/L的DPPH溶液+30 μL 80%乙醇
DPPH自由基清除率计算如公式(1)所示:
清除率![]()
(1)
式中:A1、A2、A0分别为表2对应体系517 nm处吸光度值。
1.3.6 发酵红糖液电子感官评价
在1.3.1节所述工艺基础上,优化发酵工艺条件并制备发酵红糖液,同时增加稀释处理,对所得不同浓度的优化发酵红糖液进行电子鼻和电子舌评价。
1.3.6.1 电子鼻参数设置
电子鼻FOX4000含有3个高效传感器室,共18根传感器。
Sensors chamber 1:LY2、LG、LY2/G、LY2/AA、LY2/GH、LY2/gCTl、LY2/gCT
Sensors chamber 2:T30/1、P10/1、P10/2、P40/1、T70/2、PA/2
Sensors chamber 3:P30/1、P40/2、P30/2、T40/2、T40/1、TA/2
18根传感器的分析时间设置为200 s,取最高点的数值进行分析。实验条件如表3所示,每个样品重复4次。
表3 FOX4000 电子鼻分析条件
Table 3 Conditions of FOX4000 electronic nose analysis
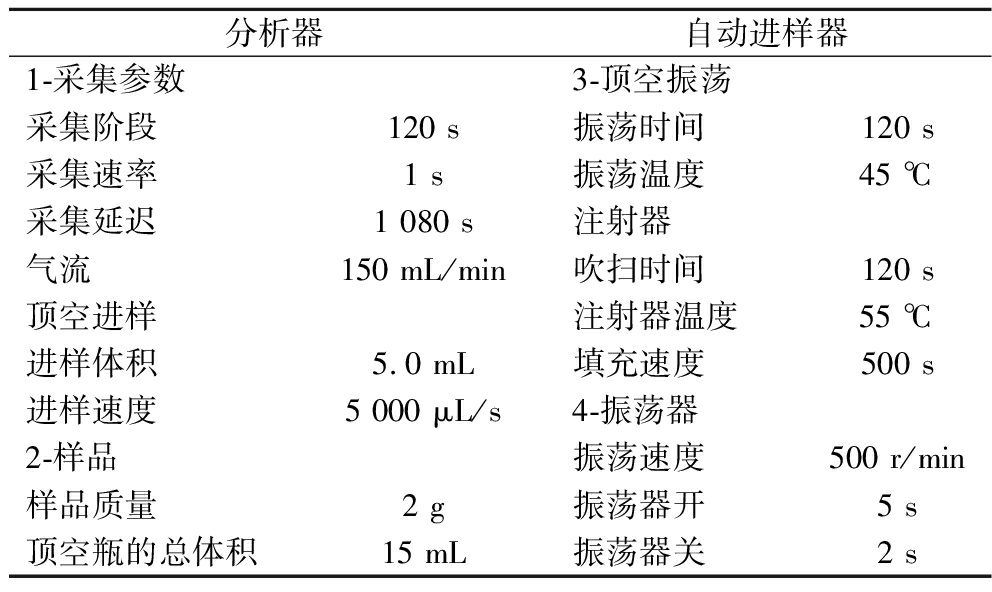
分析器自动进样器1-采集参数3-顶空振荡采集阶段120 s振荡时间120 s采集速率1 s振荡温度45 ℃采集延迟1 080 s注射器气流150 mL/min吹扫时间120 s顶空进样注射器温度55 ℃进样体积5.0 mL填充速度500 s进样速度5 000 μL/s4-振荡器2-样品振荡速度500 r/min样品质量2 g振荡器开5 s顶空瓶的总体积15 mL振荡器关2 s
1.3.6.2 电子舌参数设置
取发酵红糖液30 mL置于塑料杯中,使用电子舌分析样品的酸、甜、苦、咸、鲜、涩味觉值,各传感器可评价味道对照如表4所示,具体操作方法如下:
表4 电子舌传感器性能表
Table 4 Performance of electronic tongue sensor
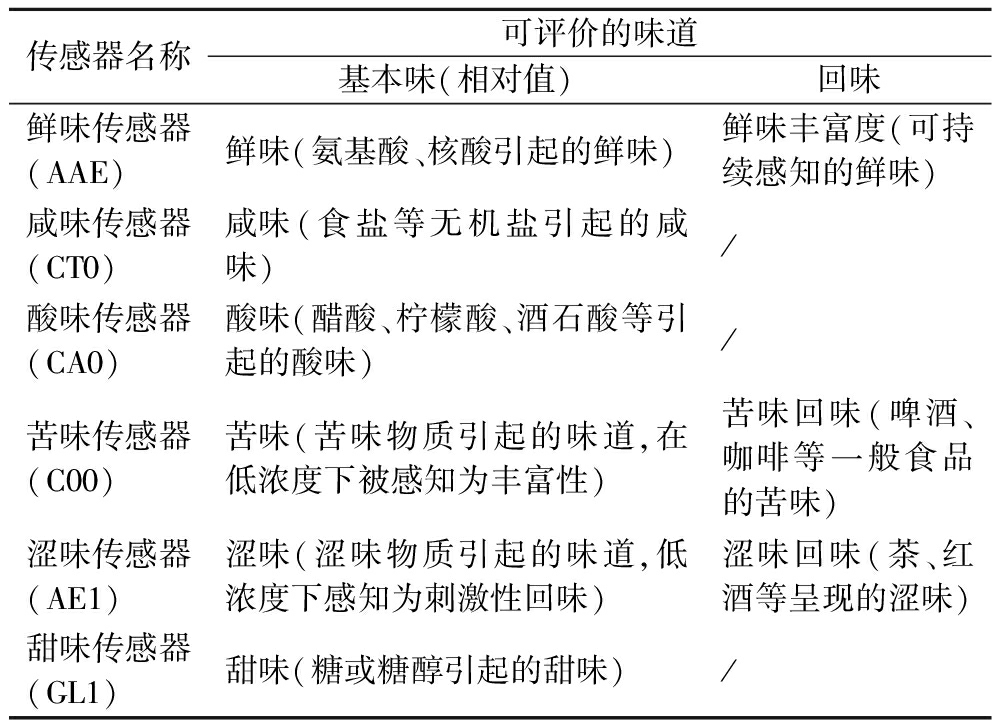
传感器名称可评价的味道基本味(相对值)回味鲜味传感器(AAE)鲜味(氨基酸、核酸引起的鲜味)鲜味丰富度(可持续感知的鲜味)咸味传感器(CT0)咸味(食盐等无机盐引起的咸味)/酸味传感器(CA0)酸味(醋酸、柠檬酸、酒石酸等引起的酸味)/苦味传感器(C00)苦味(苦味物质引起的味道,在低浓度下被感知为丰富性)苦味回味(啤酒、咖啡等一般食品的苦味)涩味传感器(AE1)涩味(涩味物质引起的味道,低浓度下感知为刺激性回味)涩味回味(茶、红酒等呈现的涩味)甜味传感器(GL1)甜味(糖或糖醇引起的甜味)/
取待测样品,分装于2个样品杯中。在室温(25 ℃)条件下测定。测定方法为电极清洗→缓冲液1清洗→缓冲液2清洗→稳定化→测试样品→缓冲液1清洗→缓冲液2清洗→回味测定,每个样品循环4次。
1.3.7 发酵红糖液人员感官评价
在1.3.1节所述工艺基础上,优化发酵工艺条件并制备发酵红糖液,同时增加稀释处理,对所得不同浓度的优化发酵红糖液进行电子鼻和电子舌评价。
依据GB/T 29605—2013《感官分析 食品感官质量控制导则》中所述的方法,对不同稀释度的发酵红糖液和未发酵红糖原液建立感官评价的评价集,从色泽、口味、香气、质感4个方面进行感官品评打分。评价集如表5所示,总分为100分,其中色泽20分、口味30分、香气30分、质感20分。选取21名评价员,评价员经挑选、培训后,具有一定感官分析能力且有一定的感官分析经验。最终各样品得分为21位评价员打分的平均值。
表5 人体感官评价标准赋分表
Table 5 Human sensory evaluation scoring sheet
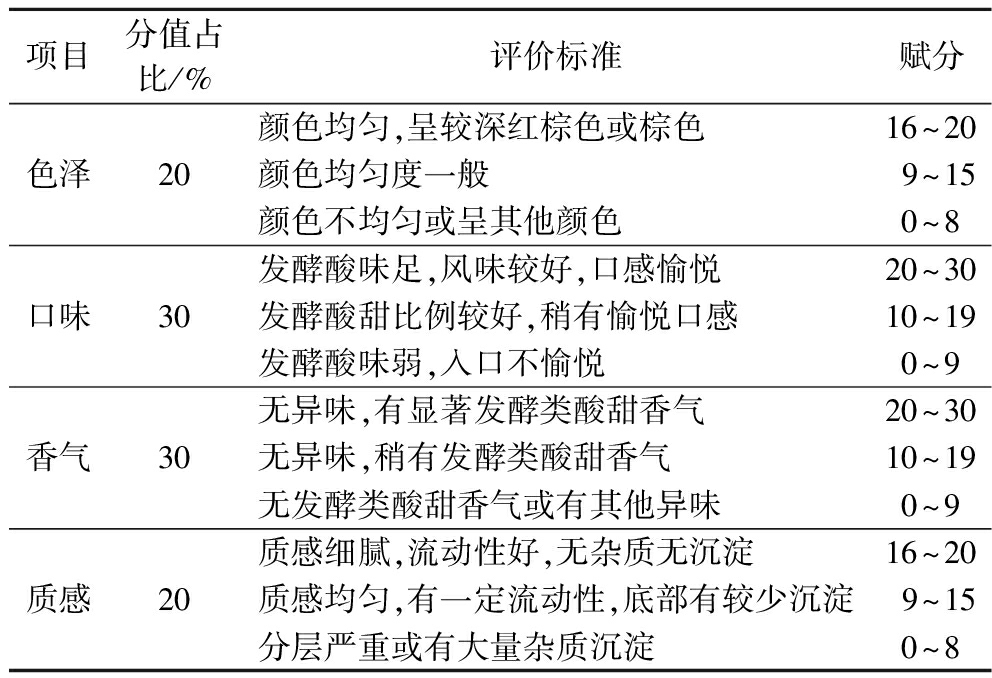
项目分值占比/%评价标准赋分色泽20颜色均匀,呈较深红棕色或棕色16~20颜色均匀度一般9~15颜色不均匀或呈其他颜色0~8口味30发酵酸味足,风味较好,口感愉悦20~30发酵酸甜比例较好,稍有愉悦口感10~19发酵酸味弱,入口不愉悦0~9香气30无异味,有显著发酵类酸甜香气20~30无异味,稍有发酵类酸甜香气10~19无发酵类酸甜香气或有其他异味0~9质感20质感细腻,流动性好,无杂质无沉淀16~20质感均匀,有一定流动性,底部有较少沉淀9~15分层严重或有大量杂质沉淀0~8
1.4 数据分析
实验中所有数据以“平均值±标准差”表示,所有指标均重复测定3次。使用Design-Expert 8.0.6 Trial 进行响应面试验设计。利用SPSS 26进行单因素方差分析,采用Origin 2022进行数据分析、图表处理。
2 结果与分析
2.1 发酵工艺参数优化的单因素试验
2.1.1 发酵时间对发酵红糖液pH及DPPH自由基清除率的影响
pH值的变化反映了微生物在发酵过程中新陈代谢活动,是评价发酵程度的重要指标[12]。如图1-a所示,随着发酵时间的延长,乳酸菌不断生长,有机酸持续积累,pH值下降。发酵红糖液在发酵时间为36 h时,DPPH自由基清除率最高达到78.21%,是发酵前红糖原液DPPH自由基清除率的2.27倍。国内外研究结果表明,采用乳酸菌进行发酵,可增加植物基产物的抗氧化活性[13-14],与本研究结果一致。基于此,选择发酵时间36 h进行后续实验。
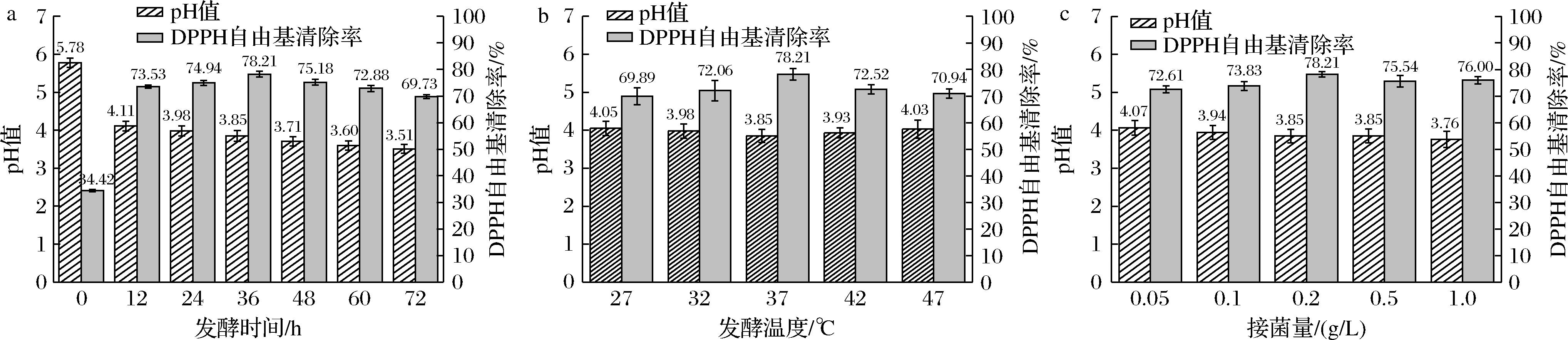
a-发酵时间;b-发酵温度;c-接菌量
图1 发酵工艺参数对发酵红糖液pH及DPPH自由基清除率的影响
Fig.1 Effect of fermentation process parameters on the pH and DPPH free radical scavenging rate of fermented brown sugar solution
2.1.2 发酵温度对发酵红糖液pH及DPPH自由基清除率的影响
发酵温度可以影响各阶段发酵体系的理化指标及活性物质的转化与合成,进而影响发酵过程中的动力学特性、发酵效率以及发酵结束的终端产品质量[15],因此筛选适宜的发酵温度至关重要。由图1-b可知,随着发酵温度的升高,红糖液的pH呈现先下降后上升的趋势,DPPH自由基清除率呈现先上升后下降的趋势,发酵温度为37 ℃时,pH最低、DPPH自由基清除率最高,出现这种现象的原因可能是发酵温度过低或过高,抑制了乳酸菌细胞内的生物酶等活性物质,减缓其生长代谢[16-17]。因此选择37 ℃为菌种发酵温度进行下一步实验。
2.1.3 接菌量对发酵红糖液pH及DPPH自由基清除率的影响
接菌量是制备发酵产品的关键参数,影响发酵速度、发酵质量等诸多方面。适宜的接菌量不仅可以减少发酵时间,而且还能提高发酵产物中营养物质的积累,改善发酵产物的感官品质[18]。由图1-c可知,随着接菌量的增加,pH逐步下降,但DPPH自由基清除率呈现先上升后下降的趋势,接菌量为0.2 g/L时,清除率最高。这可能是由于接菌量超过一定范围后,反应体系中微生物过多,竞争加剧,降低了代谢速度,从而对发酵产生不利影响[19]。
2.2 发酵红糖液制备最佳工艺条件的确定
依据单因素试验结果,选取发酵时间、发酵温度、接菌量3个变量作为响应因素,以DPPH自由基清除率作为响应值,建立Box-Behnken试验设计模型,开展3因素3水平响应面分析,优化红糖发酵工艺。设计方法及结果见表6。
表6 响应面试验结果
Table 6 Results of response surface experiment
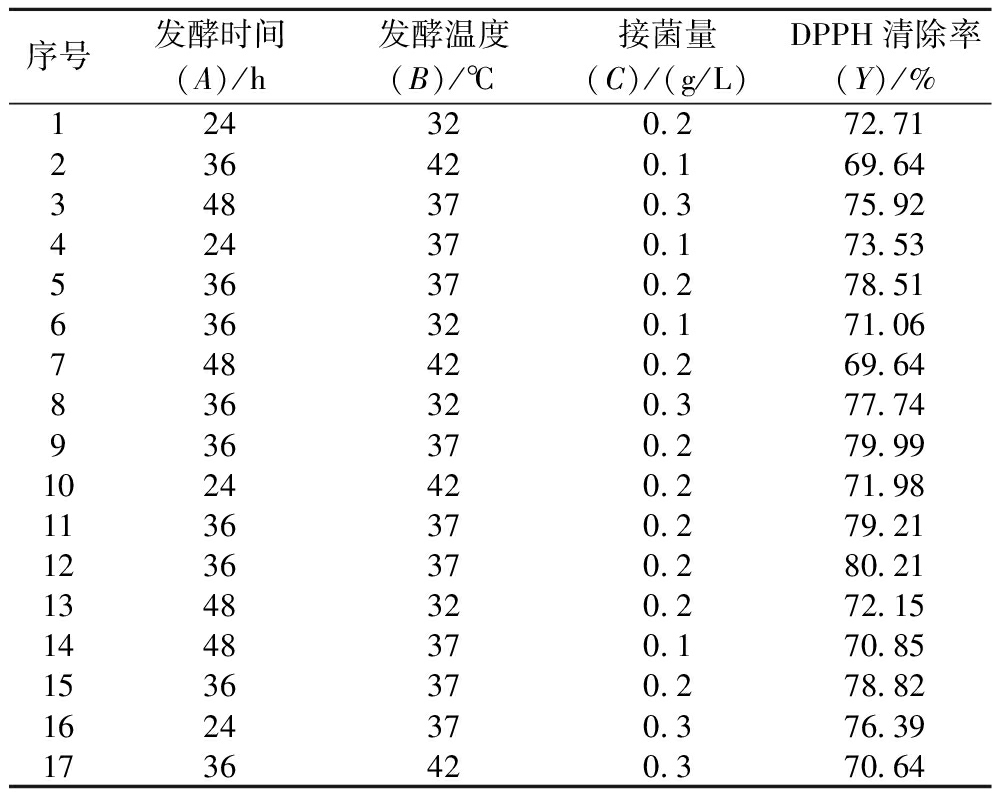
序号发酵时间(A)/h发酵温度(B)/℃接菌量(C)/(g/L)DPPH清除率(Y)/%124320.272.71236420.169.64348370.375.92424370.173.53536370.278.51636320.171.06748420.269.64836320.377.74936370.279.991024420.271.981136370.279.211236370.280.211348320.272.151448370.170.851536370.278.821624370.376.391736420.370.64
采用Box-Behnken响应面对表6试验数据进行多元回归拟合,得到DPPH自由基清除率的二元多项回归方程:Y=79.348-0.756 25A-1.47B+1.951 25C-0.445AB+0.552 5AC-1.42BC-2.912 75A2-4.815 25B2-2.262 75C2。
各变量间交互作用响应面三维图如图2所示,回归模型的方差分析结果见表7。进一步分析结果,红糖液发酵工艺条件优化的回归模型为极显著(P<0.000 1),失拟项P值为0.234 8>0.05,无显著性影响,决定系数R2=0.976 3,调整决定系数![]() 说明该模型能够较好地模拟红糖液体发酵工艺。由P值可以看出,一次项A、B、C,交互项AB、AC、BC,二次项A2、B2、C2对结果的影响中,一次项A、交互项BC达到显著水平(P<0.05),一次项B、C与二次项A2、B2、C2均达到了极显著水平(P<0.01),交互项AB、AC对结果影响不显著(P>0.05);由F值可以看出,各因素对DPPH自由基清除率的影响大小顺序为C>B>A。
说明该模型能够较好地模拟红糖液体发酵工艺。由P值可以看出,一次项A、B、C,交互项AB、AC、BC,二次项A2、B2、C2对结果的影响中,一次项A、交互项BC达到显著水平(P<0.05),一次项B、C与二次项A2、B2、C2均达到了极显著水平(P<0.01),交互项AB、AC对结果影响不显著(P>0.05);由F值可以看出,各因素对DPPH自由基清除率的影响大小顺序为C>B>A。
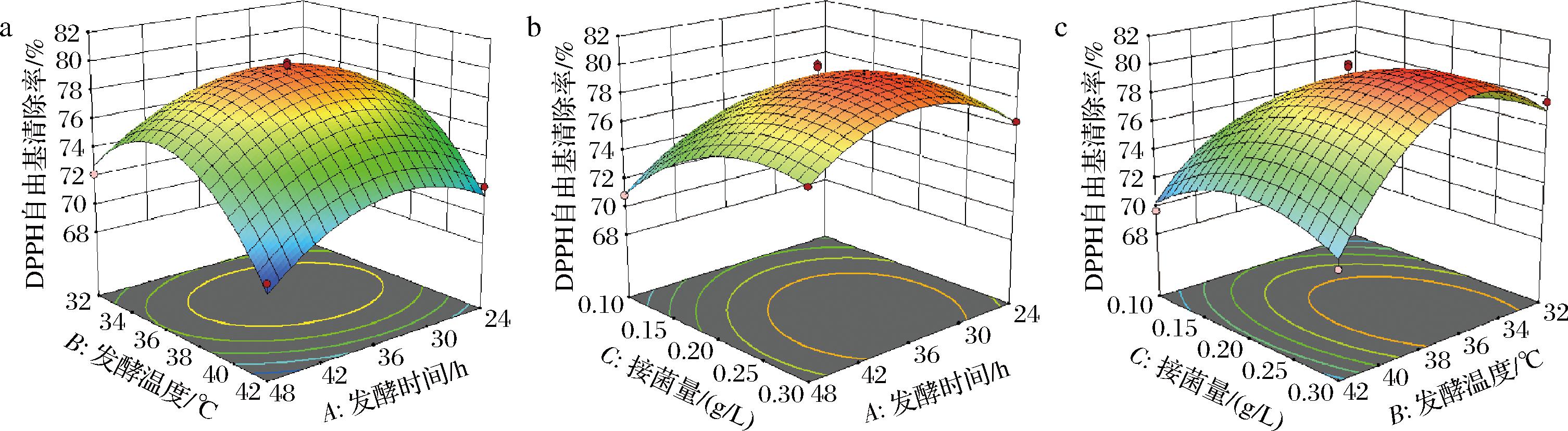
a-发酵时间与发酵温度;b-发酵时间与接菌量;c-发酵温度与接菌量
图2 各变量交互作用对发酵红糖液DPPH自由基清除率的影响响应面图和等高线图
Fig.2 Response surface plot and contour plot of interaction of variables on DPPH free radical scavenging rate in fermented brown sugar solution
表7 方差分析结果
Table 7 Results of analysis of variance
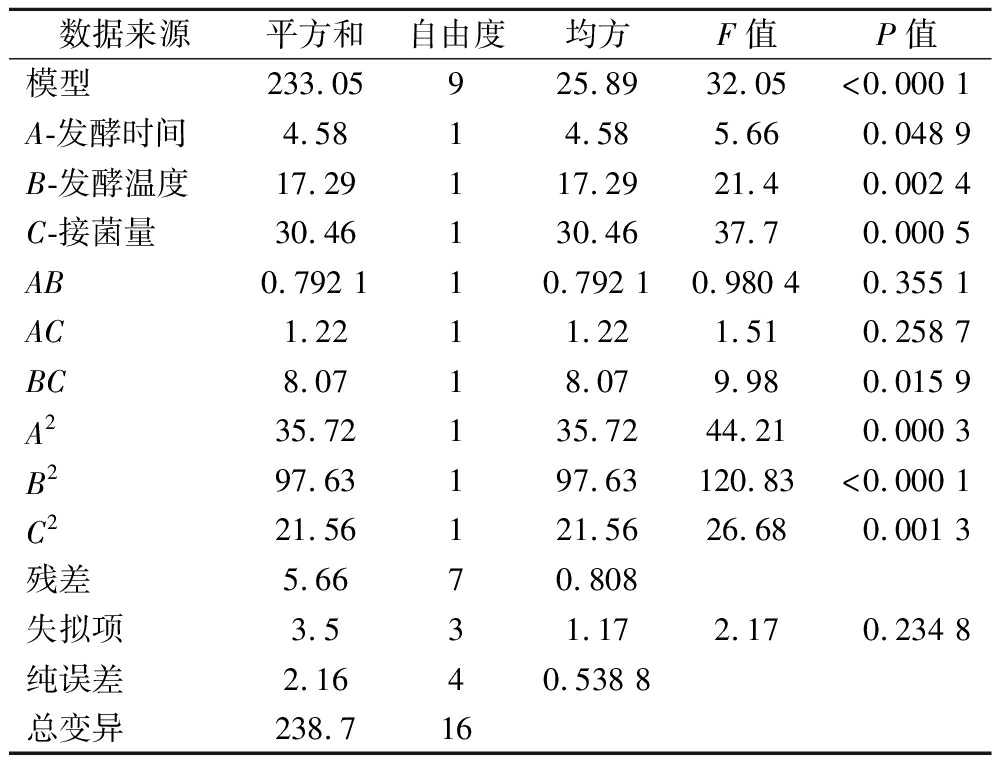
数据来源平方和自由度均方F值P值模型233.05925.8932.05<0.000 1A-发酵时间4.5814.585.660.048 9B-发酵温度17.29117.2921.40.002 4C-接菌量30.46130.4637.70.000 5AB0.792 110.792 10.980 40.355 1AC1.2211.221.510.258 7BC8.0718.079.980.015 9A235.72135.7244.210.000 3B297.63197.63120.83<0.000 1C221.56121.5626.680.001 3残差5.6670.808失拟项3.531.172.170.234 8纯误差2.1640.538 8总变异238.716
通过响应面分析法预测得到的最佳工艺为:发酵时间35.201 727 01 h、发酵温度35.887 093 41 ℃、接菌量0.239 343 1 g/L,预测所得发酵红糖液的DPPH自由基清除率为80.21%。考虑实际生产操作中各环节容易调控等因素,将3个发酵参数条件修正为:发酵时间35 h、发酵温度36 ℃、接菌量0.2 g/L。在此条件下制备的发酵红糖液DPPH自由基清除率实测值为80.19%,与预测值接近,可知利用响应面分析优化发酵红糖的制备工艺参数具有真实可靠性。
2.3 不同稀释度发酵红糖液的电子感官评价
2.3.1 电子鼻测试结果
从图3-a香气雷达图的整体轮廓来看,传感器PA/2、T30/1、P10/1、P10/2、P30/2、P40/2、TA/2、T40/1、T40/2、P40/1、T70/2、P30/1的响应信号较大。不同稀释度的发酵红糖液电子鼻响应信号存在差异。同时,相同稀释度的发酵红糖液与未发酵红糖原液电子鼻响应信号也存在差异。加之,随着浓度的增加,发酵红糖与未发酵红糖样品之间的差异越明显。这说明不同稀释度发酵红糖液风味不同,而且微生物发酵对红糖液风味产生了影响。
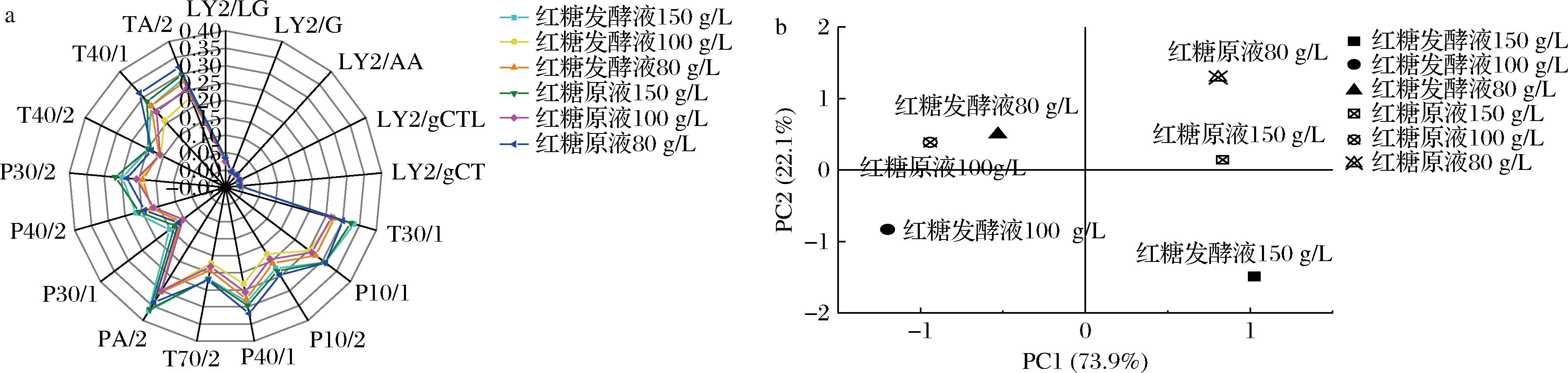
a-雷达图;b-主成分分析图
图3 不同稀释度发酵红糖液与未发酵红糖原液电子鼻检测结果
Fig.3 Electronic nose detection results of different diluted fermented and unfermented brown sugar solution
不同稀释度发酵红糖液与未发酵红糖原液电子鼻主成分分析结果见图3-b,第1主成分贡献率为73.9%,第2主成分贡献率为22.1%,2个主成分累计贡献率96.0%,超过85%,可以反映多指标信息。在第1主成分上,80、100 g/L的发酵红糖液与150 g/L的发酵红糖液可以很好区分,说明150 g/L的发酵红糖液与前两者风味区别明显。在第2主成分上,80 g/L的发酵红糖液与100 g/L的发酵红糖液存在差异,说明这2个稀释度的发酵红糖液之间风味也有明显区别,与上述雷达图结果一致。此外,80、100、150 g/L这3个稀释度的发酵红糖液与未发酵原液分别在第1主成分、第2主成分、第2主成分上区别明显,再次说明了微生物发酵对红糖液风味产生了影响。
2.3.2 电子舌测试结果
由图4-a可见,不同稀释度的发酵红糖液与未发酵红糖原液在酸味、甜味、涩味维度上的区分度较大。采用图4-b的三维气泡图对酸味、甜味、涩味进一步分析可知,红糖发酵液的酸味和涩味显著强于红糖原液。同时,随着浓度增加,红糖原液涩味逐渐加强,而红糖发酵液涩味基本保持不变。出现这种现象的原因可能是在发酵过程中微生物生长代谢产生酸类物质,极大程度改变了红糖原始味型,富集的酸涩味道超出电子舌区分范围,导致不同浓度的红糖发酵液涩味值相近。此外,分别以主成分1和主成分2为横纵坐标轴,结果如图4-c所示,区分贡献率分别为83.3%和16.2%,包含了主成分分析转换中的绝大部分的贡献率,能够较好反映多指标信息。不同浓度的红糖发酵液和红糖原液滋味可以被较好区分。
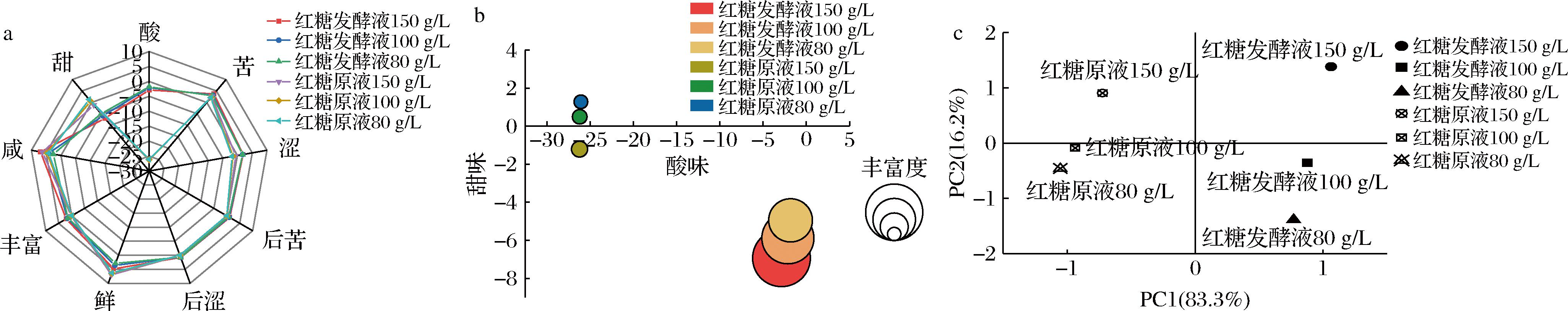
a-雷达图;b-三维气泡图;c-主成分分析图
图4 不同稀释度发酵红糖液与未发酵红糖原液电子舌检测结果
Fig.4 Electronic tongue test results of fermented brown sugar solution and unfermented brown sugar solution with different dilution
2.4 不同稀释度发酵红糖液的人体感官评价
如图5所示,发酵红糖液得分均高于未发酵红糖原液,说明乳酸菌发酵有利于改善红糖感官特性。此外,80 g/L的未发酵红糖原液在色泽、滋味、质感3个方面得分最低,150 g/L的未发酵红糖原液在香气方面得分最低。150 g/L的发酵红糖液在色泽、香气、滋味、质感4个维度上得分均为最高,因此红糖发酵液的最佳稀释度为150 g/L。
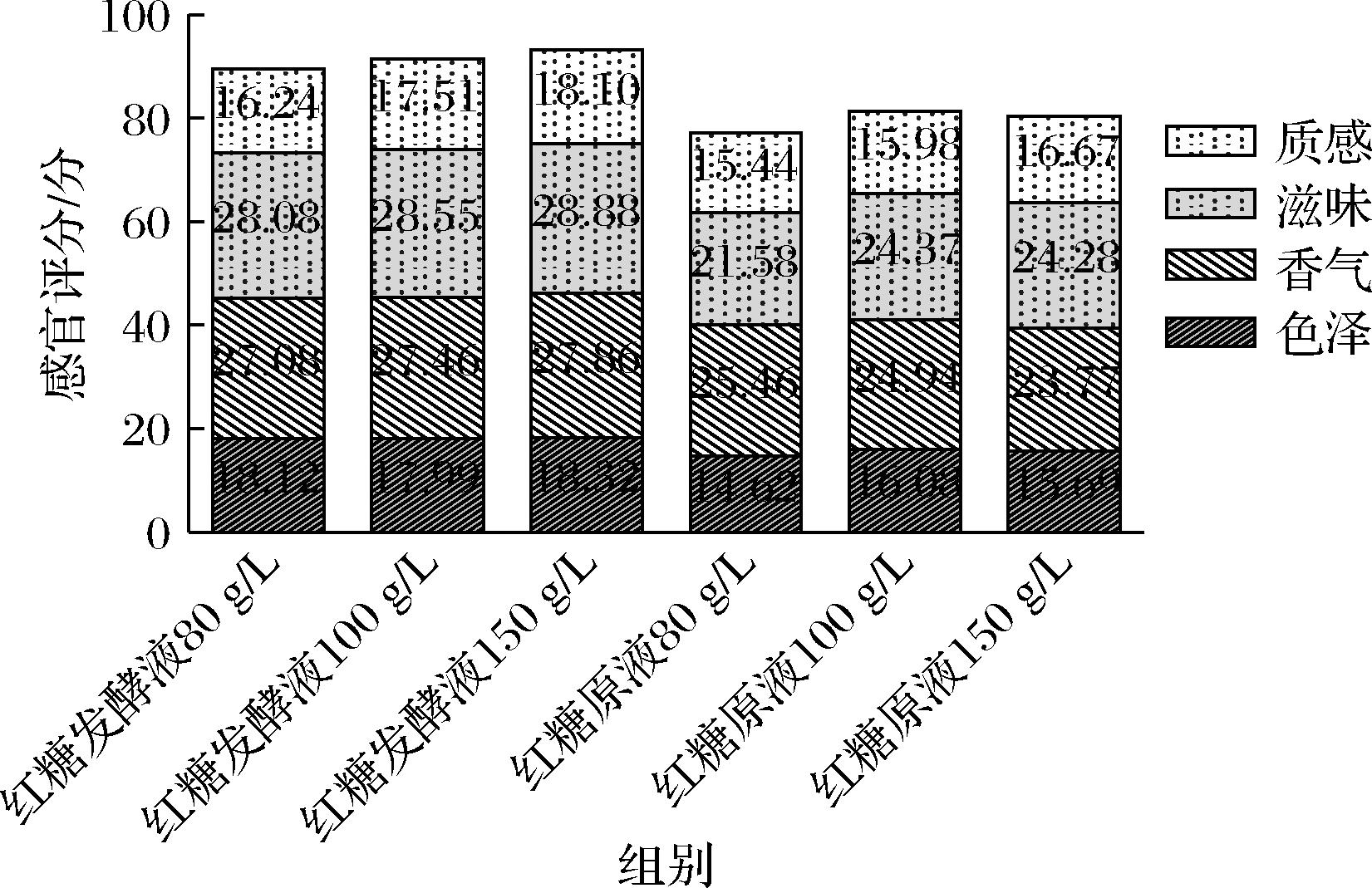
图5 不同稀释度发酵红糖液与未发酵红糖原液人体感官评价结果
Fig.5 Human sensory evaluation results of fermented brown sugar solution and unfermented brown sugar solution with different dilution
3 结论
为赋予红糖明确的功能特性和更好的感官特性,进而提升红糖的经济附加值,本研究采用乳酸菌液态发酵工艺制备发酵红糖液,并以抗氧化能力——DPPH自由基清除率为指标优化发酵工艺,制备发酵红糖液样品。在此基础上,采用电子鼻、电子舌对比不同稀释度发酵红糖液与未发酵红糖原液的风味与滋味,结果表明不同稀释度发酵红糖液、相同稀释度发酵红糖液与未发酵红糖原液在风味、滋味上都存在差异。人体感官评价结果进一步表明,稀释度150 g/L的发酵红糖液风味、滋味更佳,为后续开发一系列功能性红糖饮品提供了必要的依据。
[1] JAFFÉ W R.Health effects of non-centrifugal sugar (NCS):A review[J].Sugar Tech, 2012, 14(2):87-94.
[2] 徐灵均, 袁义明, 冯爱国, 等.传统红糖与精制赤砂糖理化性质比较[J].食品科学, 2018, 39(7):125-129.
XU L J, YUAN Y M, FENG A G, et al.Comparative studies on physical and chemical properties of traditional brown sugar and refined brown granulated sugar[J].Food Science, 2018, 39(7):125-129.
[3] TAKARA K, KINJYO A, MATSUI D, et al.Antioxidative phenolic compounds from non-sugar fraction in Kokuto, non-centrifugal cane sugar[J].Journal of the Agricultural Chemical Society of Japan, 2000, 74(8):885-890.
[4] CALABIA B P, TOKIWA Y.Production of D-lactic acid from sugarcane molasses, sugarcane juice and sugar beet juice by Lactobacillus delbrueckii[J].Biotechnology Letters, 2007, 29(9):1329-1332.
[5] MOKOENA M P.Lactic acid bacteria and their bacteriocins:Classification, biosynthesis and applications against uropathogens:A mini-review[J].Molecules, 2017, 22(8):1255.
[6] SENGUN I Y, KILIC G, CHAROENYINGCHAROEN P, et al.Investigation of the microbiota associated with traditionally produced fruit vinegars with focus on acetic acid bacteria and lactic acid bacteria[J].Food Bioscience, 2022, 47:101636.
[7] YEBOAH P J, WIJEMANNA N D, EDDIN A S, et al.Lactic acid bacteria:Review on the potential delivery system as an effective probiotic[J].Current Issues and Advances in the Dairy Industry.London:IntechOpen, 2023
[8] 王超, 刘青飞, 黄红艳.乳酸菌发酵香蕉、石斛复合汁的工艺条件优化及挥发性风味物质分析[J].饮料工业, 2024, 27(6):5-10.
WANG C, LIU Q F, HUANG H Y.Optimization of fermentation process of banana-Dendrobium officinale juice by lactic acid bacteria and analysis of volatile flavor substances[J].Beverage Industry, 2024, 27(6):5-10.
[9] 马晓娟, 谢有发, 倪彩新, 等.植物乳杆菌P9发酵对枸杞浆品质的影响[J].食品与发酵工业, 2023, 49(12):229-234.
MA X J, XIE Y F, NI C X, et al.Effect of Lactobacillus plantarum P9 fermentation on the quality of Lycium barbarum pulp[J].Food and Fermentation Industries, 2023, 49(12):229-234.
[10] 潘胜国, 王群, 刘制杰, 等.乳酸菌发酵对枇杷汁体外降血糖、降血脂活性的影响[J].食品工业科技, 2025, 46(7):161-168.
PAN S G, WANG Q, LIU Z J, et al.Effect of lactic acid bacteria fermentation on the hypoglycemic and hypolipidemic activities of loquat juice in vitro[J].Science and Technology of Food Industry, 2025, 46(7):161-168.
[11] 冯丹丹, 胡萍, 许浩翔, 等.乳酸菌发酵刺梨汁体外降血糖、降血脂活性研究[J].食品与发酵工业, 2022, 48(8):212-219.
FENG D D, HU P, XU H X, et al.Hypoglycemic and hypolipidemic activities of Rosa roxburghii juice fermented by lactic acid bacteria in vitro[J].Food and Fermentation Industries, 2022, 48(8):212-219.
[12] 高小朋, 何猛超, 许可, 等.工业微生物发酵过程中pH调控研究进展[J].中国生物工程杂志, 2020, 40(6):93-99.
GAO X P, HE M C, XU K, et al.Research progress on pH regulation in the process of industrial microbial fermentation[J].China Biotechnology, 2020, 40(6):93-99.
[13] 王储炎, 张继刚, 杨柳青, 等.3种乳酸菌发酵对蓝莓多酚、原花青素含量及抗氧化活性的影响[J].食品科学, 2020, 41(24):87-94.
WANG C Y, ZHANG J G, YANG L Q, et al.Comparative effects of fermentation with three species of lactic acid bacteria on polyphenol and proanthocyanidin contents and antioxidant activity of blueberry fruit[J].Food Science, 2020, 41(24):87-94.
[14] PARK J B, LIM S H, SIM H S, et al.Changes in antioxidant activities and volatile compounds of mixed berry juice through fermentation by lactic acid bacteria[J].Food Science and Biotechnology, 2017, 26(2):441-446.
[15] VALERO-CASES E, CERD -BERNAD D, PASTOR J J, et al.Non-dairy fermented beverages as potential carriers to ensure probiotics, prebiotics, and bioactive compounds arrival to the gut and their health benefits[J].Nutrients, 2020, 12(6):1666.
-BERNAD D, PASTOR J J, et al.Non-dairy fermented beverages as potential carriers to ensure probiotics, prebiotics, and bioactive compounds arrival to the gut and their health benefits[J].Nutrients, 2020, 12(6):1666.
[16] 张郁松. 纯种发酵红皮萝卜泡菜工艺[J].食品工业, 2023, 44(2):38-40.
ZHANG Y S.Pickling technology of pure breed fermented radish with red skin[J].The Food Industry, 2023, 44(2):38-40.
[17] 周灿, 齐成媚, 杨芳, 等.生姜酵素发酵工艺优化及抗氧化活性研究[J].中国酿造, 2024, 43(10):82-87.
ZHOU C, QI C M, YANG F, et al.Optimization of fermentation process and antioxidant activity of ginger Jiaosu[J].China Brewing, 2024, 43(10):82-87.
[18] 王佳, 黑果酵素的制备及抗氧化活性研究[D].青岛:青岛农业大学,2019.
WANG J.Preparation and antioxidant activity of black chokeberry enzyme[D].Qingdao:Qingdao Agricultural University,2019.
[19] 陈林林, 王玲, 郑凤鸣, 等.发酵紫苏粕制备抗氧化肽的工艺优化及抗氧化性[J].食品研究与开发, 2023, 44(18):116-124.
CHEN L L, WANG L, ZHENG F M, et al.Process optimization and activity of antioxidant peptides prepared from fermented perilla meal[J].Food Research and Development, 2023, 44(18):116-124.