益生菌被联合国粮食及农业组织定义为“活的微生物,当其摄入足够量时,能为宿主带来健康益处[1]”,其对人体健康的潜在作用被广泛证实,被应用于食品发酵、酸奶制作、奶粉配方、膳食补充剂等多个方面[2]。乳酸片球菌(Pediococcus acidilactici)是益生菌家族成员之一,隶属于厚壁菌门芽孢杆菌纲乳杆菌目乳杆菌科片球菌属[3],能够产生片球菌素,具有促进营养吸收、提高免疫力、减轻乳糖不耐症、调节肠道微生物菌群的重要作用[4],是健康人肠道菌群重要的组成部分。然而,大多数益生菌培养物需要冷藏储运,在此过程中益生菌活性难以维持、所需成本高昂且不方便使用,通常将益生菌干燥制备成菌粉,菌粉的稳定性较好,储运成本较低且便于使用[5]。
目前的制备方法中真空冷冻干燥技术以适用范围广、菌株存活率高、菌粉保藏时间长、菌种稳定性高的特点,成为工业上制备高活性高稳定性菌粉较为理想的方法[6]。但冻干过程可能会使益生菌细胞膜结构和功能受损,敏感蛋白和关键酶失活[7]。因此通常在菌株冻干前加入保护剂[8],减少菌体在冷冻干燥过程中受到的各种损伤,并最大限度地保留菌体原有的各种生理生化特性和生物活性[9]。如今被发掘出来的益生菌冻干保护剂有很多,按照保护剂的性质可分为糖类、蛋白质类、抗氧化剂类、多元醇类和肽类[10]。其中糖类、蛋白类、多元醇类作为传统保护剂,使用较为广泛。陈胜杰等[11]在植物乳植杆菌、凝结蘶茨曼氏菌、酵母酿酒菌的最优冻干保护剂配方探究中均使用到脱脂乳;李兵兵等[12]对银耳多糖在冷冻干燥过程中对植物乳植杆菌细胞膜以及关键酶活性的保护作用进行深入探讨;LI等[13]发现滑子菇多糖在干酪乳酪杆菌菌粉贮藏过程中明显提高其活力。肽类作为新型保护剂[14],是一种介于大分子蛋白质和小分子氨基酸之间的活性物质,其具体的作用与肽本身的生物活性相关。如KWON等[15]发现丝素蛋白具有β-折叠结构,其中的氢键可在冻干过程中提供疏水相互作用,稳定蛋白质结构,减少菌体细胞的冷冻损伤。王昊乾等[16]从乳清蛋白水解物中提取了一种抗氧化肽HP3-2,在动物双歧杆菌乳亚种冻干过程中能保护细胞膜结构和胞内蛋白酶活力,降低细胞的氧化损伤,维持胞内环境的稳定。植物源肽的研究较少,DING等[17]的研究发现将核桃寡肽添加到植物乳植杆菌Z7的培养基后,能增强细菌群体感应系统调控的生物膜分泌,从而提高了细菌抵抗不良环境的能力。
冻干保护剂的保护机制主要有3种:一是充当稳定剂,与蛋白质和膜磷脂的极性头基形成氢键,并在解吸未冷冻水的过程中充当水的替代物;二是增加溶液的玻璃化转变温度;三是限制冷冻干燥菌粉的氧化反应。但当保护剂转运到胞内后,能否发挥好的保护效果以及其具体的作用机制如何,需通过进一步研究其代谢活动来阐明。代谢组学能够对生物体内代谢物进行全面定性定量分析,并通过系统性检测生物样本中代谢物的组成与丰度,能够追踪基因表达和蛋白质功能的细微变化在代谢层面的放大效应。其中,非靶向代谢组学可无偏向性地解析样本中所有可检测代谢物,通过对比不同实验组的代谢谱差异,表征分子表型并鉴定关键代谢标志物。
在筛选得到最优的保护剂后,本研究旨在利用非靶向代谢组学技术,通过分析空白组和最优组乳酸片球菌制剂的代谢物变化,筛选关键差异代谢物,并解析相关代谢途径的调控作用,从表观遗传角度提出新的见解,探究保护剂对乳酸片球菌具体的冻干保护机制。以期为开发新型、高效的冻干保护剂提供新的思路和方法。
1 材料与方法
1.1 主要材料与试剂
乳酸片球菌(Pediococcus acidilactici)N8分离自奶酪,-80 ℃甘油保藏;姬松茸多糖(纯度为85%),陕西荣林生物科技有限公司;沙棘肽(纯度为80%),陕西云奇生物科技有限公司;L-谷氨酸钠(纯度为98%),山东齐鲁生物科技样品店;麦芽糖醇(纯度为98%),上海麦克林生化科技有限公司;乙腈、甲酸、甲醇,均为色谱级,美国Fisher科技公司;牛肉膏(分析纯),国药集团化学试剂有限公司;酵母粉(分析纯)、蛋白胨(分析纯),英国Oxoid公司;葡萄糖、硫酸锰、七水硫酸镁、吐温-80,广州化学试剂厂(以上均为分析纯);柠檬酸氢二铵(分析纯),天津市福晨化学有限公司;K2HPO4(分析纯),上海麦克林生化科技有限公司。
1.2 主要仪器与设备
SW-CJ-1F超净工作台,江苏苏州安泰空气技术有限公司;YXQ5高压蒸汽灭菌锅,江阴滨江医疗设备有限公司;LRH-70生化培养箱,上海一恒科学仪器有限公司;5804R高速冷冻离心机,德国Eppendorf公司;FD-1A-50真空冷冻干燥机,上海欧蒙实业有限公司;PHS-3C精密pH计,上海精密科学仪器有限公司制造;U410超低温冰箱,德国Eppendorf公司;ACQUITY UPLC I-Class plus/Thermo QE超高效液相串联高分辨质谱仪、色谱柱HSS T3,美国Waters公司;Agilent 7890B-5977A气质联用仪,美国安捷伦科技公司。
1.3 试验方法
1.3.1 菌株的冻干流程
从-80 ℃冰箱取出菌种,活化三代后将菌液4 ℃、6 000 r/min离心10 min,弃上清液,菌泥用无菌生理盐水洗涤2次得到菌泥。将菌泥与保护剂按1∶5的质量比混匀,得到菌悬液,将菌悬液中装入冻干瓶后放入-80 ℃冰箱预冻,2 h后取出,立即放入真空冷冻干燥机中,设置冷阱温度为-65 ℃,真空度为0.05 Pa,持续冻干24 h后取出,用生理盐水对冻干后的菌粉进行复水,涡旋混匀后稀释涂板计算其存活率及活菌数。
1.3.2 冻干保护剂的筛选
从4类不同保护剂中共选取20种,每类保护剂配制相同浓度的保护剂水溶液与菌泥按1.3.1节进行冻干,具体信息见表1。以活菌数为指标筛选出每类中保护效果最好的保护剂。
表1 保护剂筛选
Table 1 Protectant screening

类型保护剂名称质量浓度/(g/L)植物源肽葛根肽、苦瓜肽、沙棘肽、黑枸杞肽、核桃肽50真菌多糖杏鲍菇多糖、姬松茸多糖、银耳多糖、猴头菇多糖、蛹虫草多糖50抗氧化剂谷胱甘肽、维生素C钠、L-谷氨酸钠、L-半胱氨酸、胡萝卜粉20多元醇白藜芦醇、木糖醇、甘露醇、麦芽糖醇、山梨醇50
1.3.3 冻干保护剂的单因素试验
根据1.3.2节的结果筛选出乳酸片球菌最优保护剂并以10、30、50、70、90 g/L的质量浓度确定其最佳添加范围。
1.3.4 菌粉活菌数的测定
采用GB 4789.35—2023《食品安全国家标准 食品微生物学检测 乳酸菌检测》进行检测。
1.3.5 菌粉存活率的测定
(1)
式中:C,冻干菌粉的存活率,%;N,冻干菌粉复溶后的活菌数,CFU/mL;N1,冻干前菌悬液的活菌数,CFU/mL。
1.3.6 非靶向代谢组学分析
收集菌泥并分别加入生理盐水及沙棘肽,并将2组乳酸片球菌菌悬液预冻2 h后冷冻干燥24 h,此时得到完全干燥后的菌粉,将2组菌粉送至上海欧易生物医学科技有限公司进行非靶向代谢组学分析,具体操作如下。
1.3.6.1 样品前处理
准确称取30 mg样本置于1.5 mL离心管中,添加2颗小钢珠和600 μL V(甲醇)∶V(水)=4∶1(含混合内标,4 μg/mL);将混合溶液放入-40 ℃冰箱中预冷2 min并使用研磨机45 Hz研磨2 min;随后将样品放入冰水浴中超声波提取30 min,并放入-40 ℃冰箱静置过夜;将提取液4 ℃、12 000 r/min离心20 min,得到上清液,取150 μL转移到液相进样小瓶,-80 ℃下保存,直到进行LC-MS分析;取150 μL装入玻璃衍生小瓶中,用离心浓缩干燥器挥干样本后加入80 μL的甲氧胺盐酸盐吡啶溶液(15 mg/mL),于37 ℃振荡培养箱中进行1 h时肟化反应;反应结束后取出样本加入50 μL的双(三甲基硅烷基)三氟乙酰胺衍生化试剂和20 μL的正己烷,以及10种内标(C8/C9/C10/C12/C14/C16/C18/C20/C22/C24,均为氯仿配制)10 μL,于70 ℃反应1 h;取出样本,室温放置30 min,进行GC-MS代谢组学分析。质控样本(quality control,QC)由所有样本的提取液等体积混合制备而成。
1.3.6.2 液相色谱-质谱条件
液相:色谱柱为ACQUITY UPLC HSS T3(100 mm×2.1 mm,1.8 μm);柱温45 ℃;流动相:A-水(含体积分数为0.1%甲酸),B-乙腈;流速0.35 mL/min;进样体积5 μL。质谱条件如表2所示。
表2 液相质谱条件
Table 2 LC-MS conditions
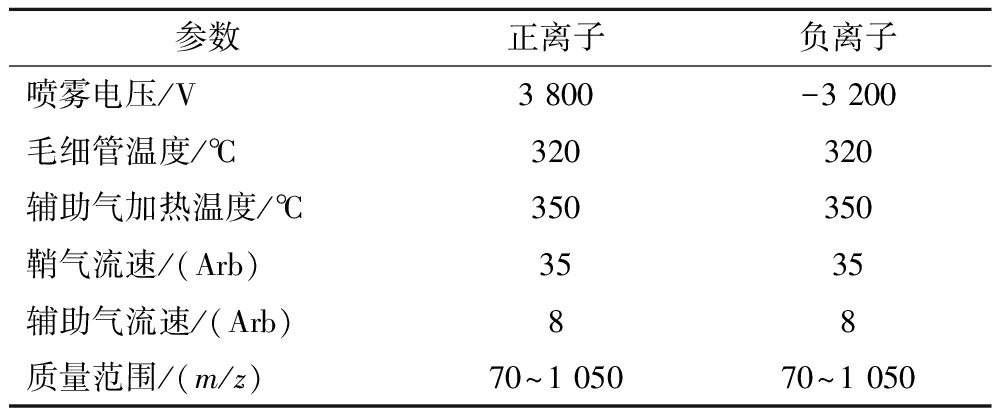
参数正离子负离子喷雾电压/V3 800-3 200毛细管温度/℃320320辅助气加热温度/℃350350鞘气流速/(Arb)3535辅助气流速/(Arb)88质量范围/(m/z)70~1 05070~1 050
1.3.6.3 气相色谱-质谱条件
气相色谱:DB-5MS毛细管柱(30 m×0.25 mm,0.25 μm),载气为高纯He(纯度不小于99.999%),流速1.0 mL/min,进样口的温度为260 ℃。进样量1 μL,不分流进样,溶剂延迟5.5 min。质谱:电子轰击离子源(electron impact ionization,EI),离子源温度230 ℃,四极杆温度150 ℃,电子能量70 eV。扫描方式为全扫描模式,质量扫描范围:m/z 50~500。
1.3.7 傅里叶红外光谱分析
将空白组与沙棘肽组冻干样品复溶,离心弃上清液,PBS洗涤2次,无菌纯化水重悬。取30 μL重悬液均匀平铺在ZnSs窗口片,45 ℃干燥1 h,再加入质量50~100倍KBr进行研磨压片,红外灯烘烤2 min。以KBr片为对照,进行傅里叶红外光谱仪测试,扫描范围4 000~400 cm-1,扫描次数64次,分辨率4 cm-l。由OMINIC 8.0 软件进行数据处理,对光谱曲线归一化处理并进行二阶求导,分析各基团特征峰变化,判断细胞结构变化。
1.4 数据处理
所有试验数据均重复3次,结果以“平均值±标准偏差”表示。数据采用SPSS软件进行数据分析,不同小写字母表示具有统计学差异(P<0.05)。
原始数据经代谢组学处理软件XCMS v4.5.1软件进行数据预处理,并使用MS-DIAL v4.24软件进行峰检测、峰识别、峰对齐等一系列处理,得到原始数据矩阵。使用The Human Metabolome Database(HMDB)、NIST数据库Lipidmaps(v2.3)和METLIN数据库以及LuMet-Plant3.0本地数据库进行鉴定分析,得到代谢物定性定量的结果。根据结果对代谢物进行主成分分析(principal component analysis,PCA)和正交偏最小二乘法判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)。基于OPLS-DA,根据变量投影重要度(variable importance in project,VIP)≥1,P<0.05和|log2FC|>2(FC为差异倍数,fold change)进行差异代谢物筛选,将差异代谢物通过代谢通路数据库KEGG Pathways(KEGG,www.genome.jp/kegg)进行注释解析。
2 结果与分析
2.1 保护剂筛选结果
由表3得出20种不同的保护剂中有18种保护剂的活菌数高于空白组且具有显著性差异(P<0.05),具有优良的保护效果。其中植物源肽类保护剂冻干菌粉活菌数均达到1×1012 CFU/g,说明植物源肽是一类优良的保护剂,其中沙棘肽的保护剂效果最佳,冻干后菌粉活菌数为1.43×1012 CFU/g。沙棘是一种抗冻耐寒的植物,有研究表明,从沙棘叶及沙棘浆果中提取出的沙棘蛋白均具有抗冻活性[18]。而沙棘肽是蛋白的水解产物,作为小分子肽具有生物活性,能减少细胞在冻干过程中的损伤。
表3 保护剂筛选结果
Table 3 Protectant screening results
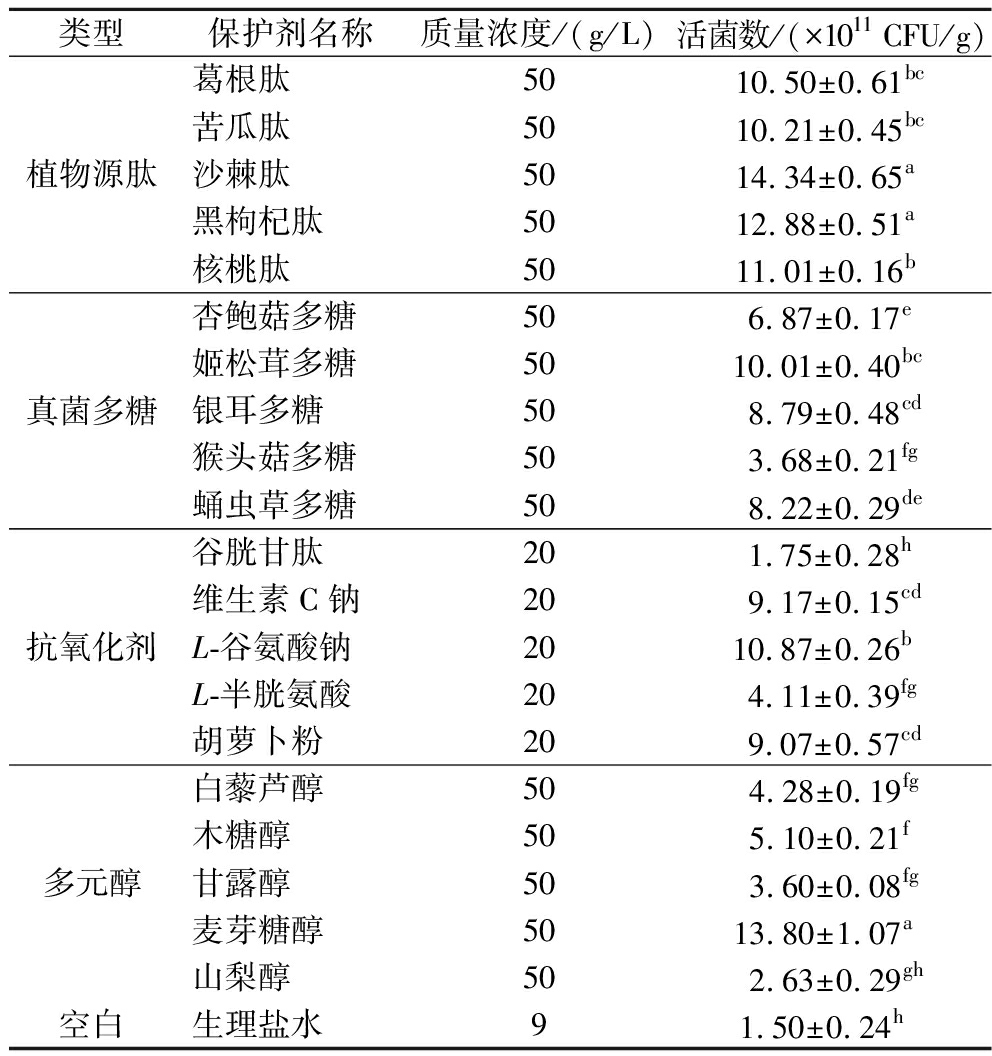
类型保护剂名称质量浓度/(g/L)活菌数/(×1011 CFU/g)植物源肽葛根肽5010.50±0.61bc苦瓜肽5010.21±0.45bc沙棘肽5014.34±0.65a黑枸杞肽5012.88±0.51a核桃肽5011.01±0.16b真菌多糖杏鲍菇多糖506.87±0.17e姬松茸多糖5010.01±0.40bc银耳多糖508.79±0.48cd猴头菇多糖503.68±0.21fg蛹虫草多糖508.22±0.29de抗氧化剂谷胱甘肽201.75±0.28h维生素C钠209.17±0.15cdL-谷氨酸钠2010.87±0.26bL-半胱氨酸204.11±0.39fg胡萝卜粉209.07±0.57cd多元醇白藜芦醇504.28±0.19fg木糖醇505.10±0.21f甘露醇503.60±0.08fg麦芽糖醇5013.80±1.07a山梨醇502.63±0.29gh空白生理盐水91.50±0.24h
注:同组数据不同字母表示差异显著(P<0.05);相同字母表示差异不显著(P>0.05)。
2.2 沙棘肽单因素试验结果
由图1可知,随着沙棘肽添加量的增加,菌粉活菌数呈现出先上升后下降的趋势,当质量浓度为30 g/L时,菌粉的活菌数最高,为2.34×1012 CFU/g,存活率为90.86%,具有良好的保护效果。当保护剂的添加量变大,菌粉的活菌数也随之降低,虽然存活率在缓步提升,但由于固形物含量的增加,菌粉的活菌数已经下降到1×1012 CFU/g以下。所以选取30 g/L沙棘肽制备的乳酸片球菌菌粉与空白组(生理盐水)进行代谢物的测定。
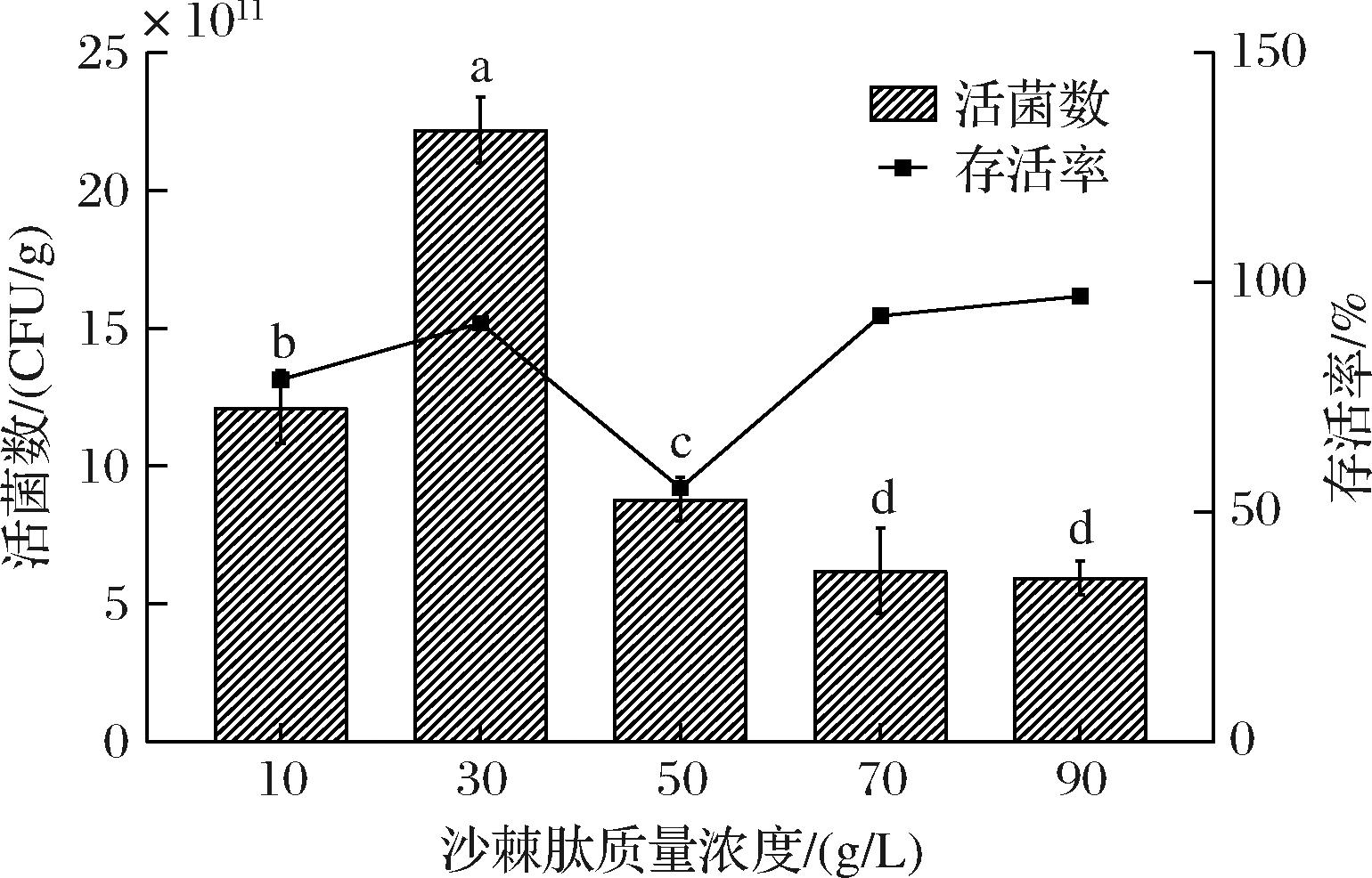
图1 沙棘肽对冻干菌粉活菌数及存活率的影响
Fig.1 Effect of seabuckthorn peptide on the number of viable bacteria and survival rate of lyophilized fungus powder
注:图中不同字母表示差异显著(P<0.05);相同字母
表示差异不显著(P>0.05)。
2.3 正交偏最小二乘法判别分析
为了区分各组间代谢轮廓的总体差异,找到2组间的主要差异代谢物信息,本研究利用多元变量统计分析方法对空白及沙棘肽菌粉的代谢组进行了有监督的OPLS-DA,结果如图2-a所示,横坐标展示样本的组间差异,纵坐标表示样本的组内差异,2组的样本点在OPLS-DA得分图上组间分离趋势明显,无任何交点,乳酸片球菌空白和沙棘肽2组间代谢物差异显著。OPLS-DA模型的具体参数为:![]() 其中
其中![]() 表示该模型对Y矩阵的解释率,Q2表示该模型的预测能力,
表示该模型对Y矩阵的解释率,Q2表示该模型的预测能力,![]() 和Q2≥0.999,该模型稳定可靠,可以区分2组样本并用于后续的差异代谢物分析。
和Q2≥0.999,该模型稳定可靠,可以区分2组样本并用于后续的差异代谢物分析。
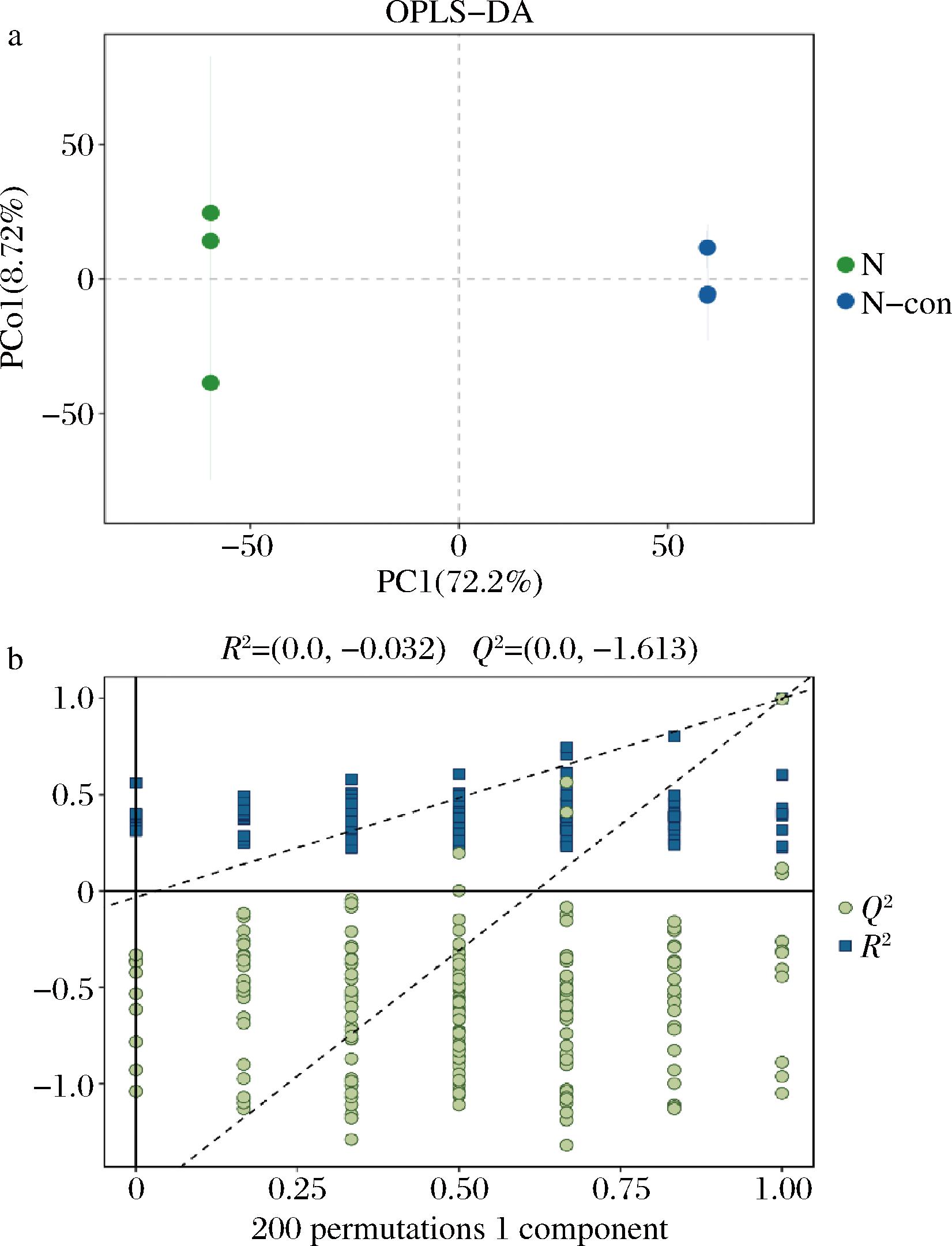
a-OPLS-DA得分图;b-置换检验图
图2 OPLS-DA得分图和置换检验图
Fig.2 OPLS-DA score plot and permutation test plot
对OPLS-DA模型进行200次响应排序检验,得到的回归直线与y轴的截距值分别为R2和Q2,用来衡量模型是否过拟合。通常![]() 和
和![]() 直线的斜率越接近水平直线,模型越有可能过拟合。如图2-b,置换检验模型中左边的所有绿色Q2值都低于右边的原始点且Q2点的绿色回归线与纵轴(左侧)相交于或低于零,这表明模型没有过拟合,数据可靠,结果可信度高。
直线的斜率越接近水平直线,模型越有可能过拟合。如图2-b,置换检验模型中左边的所有绿色Q2值都低于右边的原始点且Q2点的绿色回归线与纵轴(左侧)相交于或低于零,这表明模型没有过拟合,数据可靠,结果可信度高。
2.4 差异代谢物的筛选
根据OPLS-DA模型(生物学重复为3)得到的VIP初步筛选出2组菌粉之间的差异代谢物进行差异分析,以VIP≥1、P<0.05、FC≥4或FC≤0.25的标准绘制T检验火山图进行数据可视化,有利于筛选差异代谢物。图3中展示了2组间差异代谢物的数目及变化类型,其中红色圆点代表在实验组中上调的代谢物,蓝色圆点代表下调的代谢物,灰色点代表不显著的代谢物。如图3所示,共筛选出720种显著差异代谢物,显著上调差异代谢物508种,显著下调差异代谢物212种,上调代谢物多于下调的代谢物,上调的代谢物多为脂类和类脂类分子、有机酸及其衍生物以及有机杂环化合物。其中上调的部分差异代谢物如表4所示。
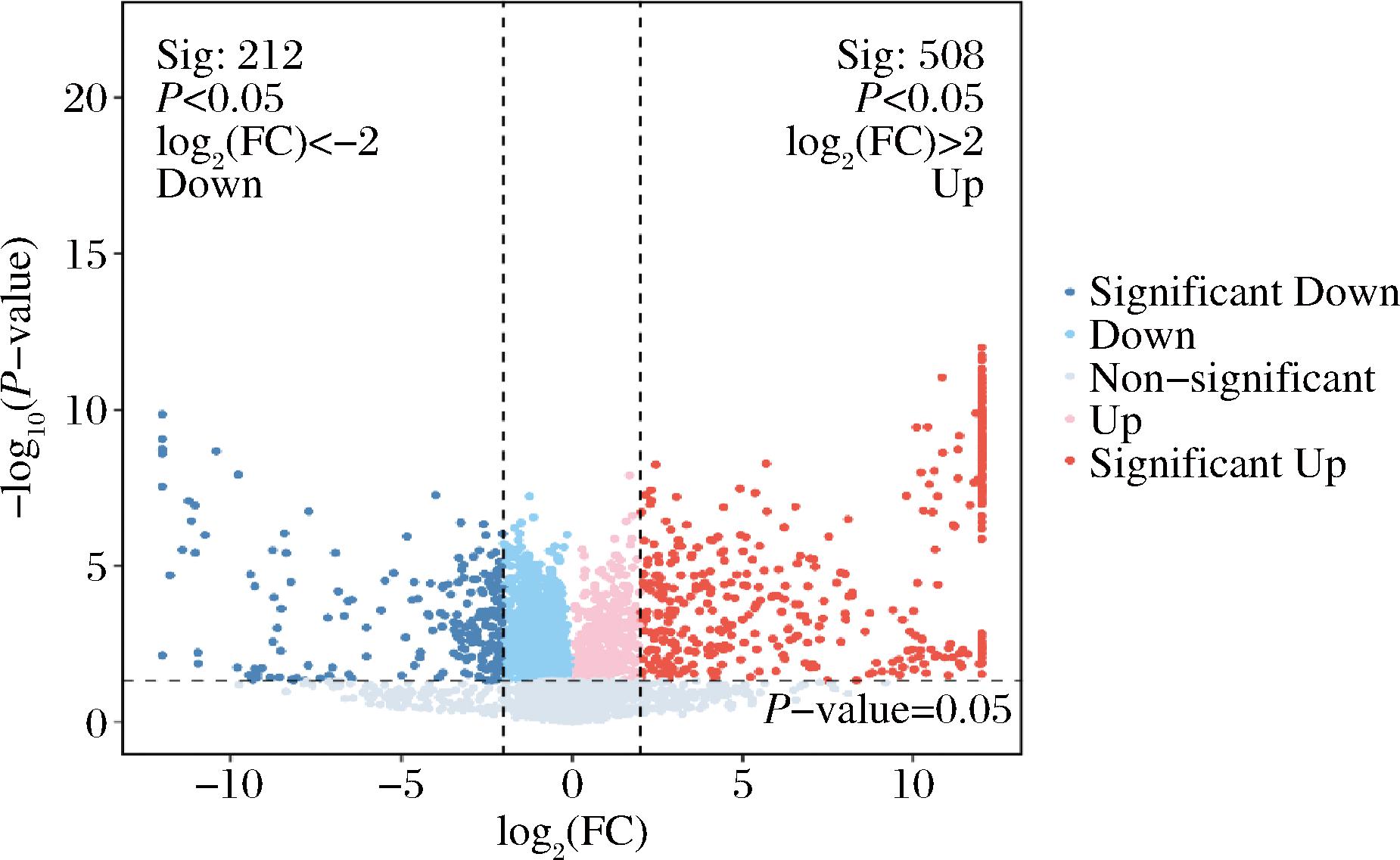
图3 差异代谢物的火山图
Fig.3 Volcano diagram of differential metabolites
表4 部分主要差异代谢物
Table 4 Some of the major differential metabolites
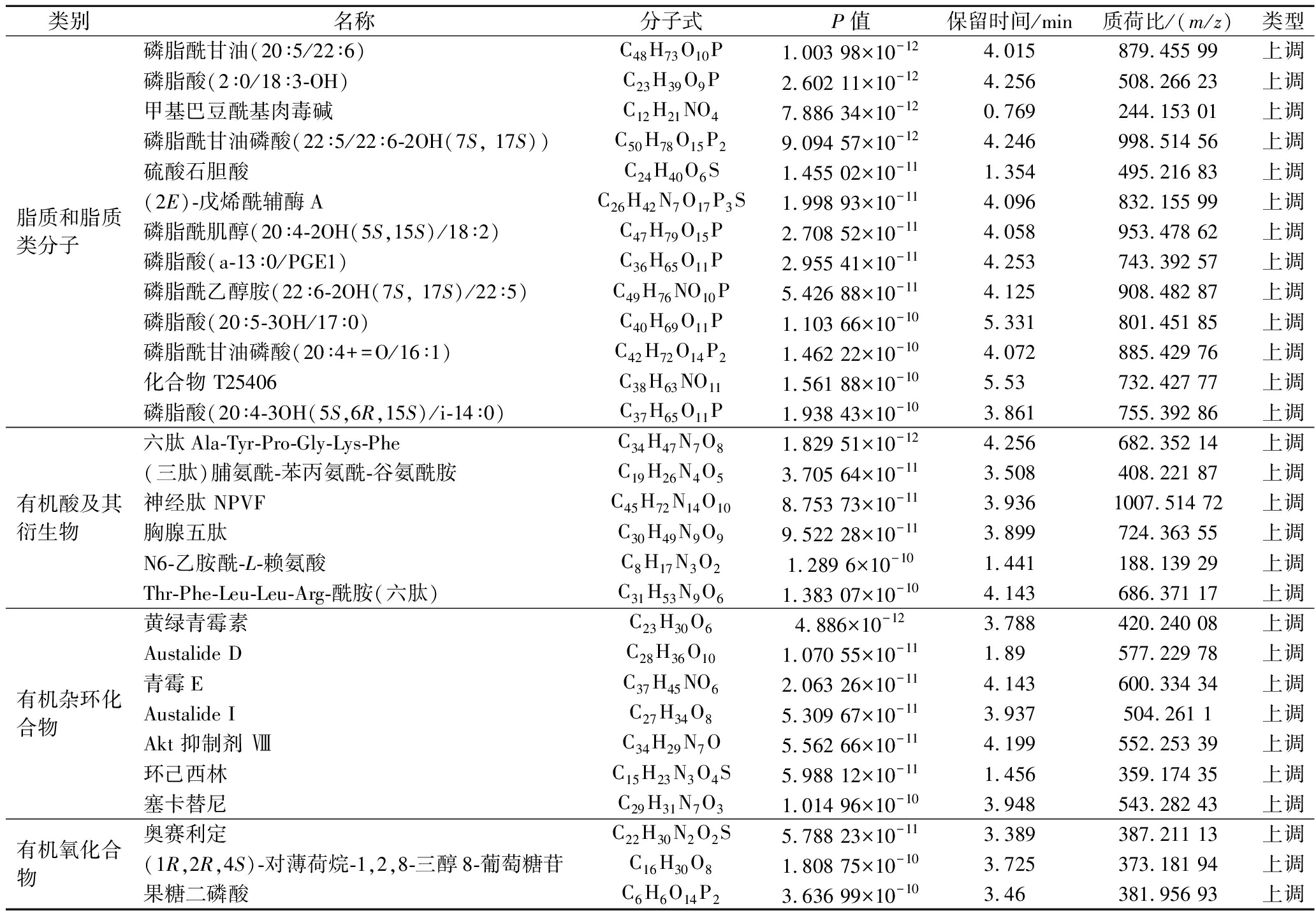
类别名称分子式P值保留时间/min质荷比/(m/z)类型脂质和脂质类分子磷脂酰甘油(20∶5/22∶6)C48H73O10P1.003 98×10-124.015879.455 99上调磷脂酸(2∶0/18∶3-OH)C23H39O9P2.602 11×10-124.256508.266 23上调甲基巴豆酰基肉毒碱C12H21NO47.886 34×10-120.769244.153 01上调磷脂酰甘油磷酸(22∶5/22∶6-2OH(7S, 17S))C50H78O15P29.094 57×10-124.246998.514 56上调硫酸石胆酸C24H40O6S1.455 02×10-111.354495.216 83上调(2E)-戊烯酰辅酶AC26H42N7O17P3S1.998 93×10-114.096832.155 99上调磷脂酰肌醇(20∶4-2OH(5S,15S)/18∶2)C47H79O15P2.708 52×10-114.058953.478 62上调磷脂酸(a-13∶0/PGE1)C36H65O11P2.955 41×10-114.253743.392 57上调磷脂酰乙醇胺(22∶6-2OH(7S, 17S)/22∶5)C49H76NO10P5.426 88×10-114.125908.482 87上调磷脂酸(20∶5-3OH/17∶0)C40H69O11P1.103 66×10-105.331801.451 85上调磷脂酰甘油磷酸(20∶4+=O/16∶1)C42H72O14P21.462 22×10-104.072885.429 76上调化合物 T25406C38H63NO111.561 88×10-105.53732.427 77上调磷脂酸(20∶4-3OH(5S,6R,15S)/i-14∶0)C37H65O11P1.938 43×10-103.861755.392 86上调有机酸及其衍生物六肽Ala-Tyr-Pro-Gly-Lys-PheC34H47N7O81.829 51×10-124.256682.352 14上调(三肽)脯氨酰-苯丙氨酰-谷氨酰胺C19H26N4O53.705 64×10-113.508408.221 87上调神经肽 NPVFC45H72N14O108.753 73×10-113.9361007.514 72上调胸腺五肽C30H49N9O99.522 28×10-113.899724.363 55上调N6-乙胺酰-L-赖氨酸C8H17N3O21.289 6×10-101.441188.139 29上调Thr-Phe-Leu-Leu-Arg-酰胺(六肽)C31H53N9O61.383 07×10-104.143686.371 17上调有机杂环化合物黄绿青霉素C23H30O64.886×10-123.788420.240 08上调Austalide DC28H36O101.070 55×10-111.89577.229 78上调青霉EC37H45NO62.063 26×10-114.143600.334 34上调Austalide IC27H34O85.309 67×10-113.937504.261 1上调Akt 抑制剂 ⅧC34H29N7O5.562 66×10-114.199552.253 39上调环己西林C15H23N3O4S5.988 12×10-111.456359.174 35上调塞卡替尼C29H31N7O31.014 96×10-103.948543.282 43上调有机氧化合物奥赛利定C22H30N2O2S5.788 23×10-113.389387.211 13上调(1R,2R,4S)-对薄荷烷-1,2,8-三醇8-葡萄糖苷C16H30O81.808 75×10-103.725373.181 94上调果糖二磷酸C6H6O14P23.636 99×10-103.46381.956 93上调
脂质涉及细胞膜结构、能量储存、信号传导和代谢调节等多个方面。空白组与沙棘肽组菌粉的代谢物相比,主要脂类和类脂类分子差异代谢物有170种,且145种均呈上调趋势,说明沙棘肽组的菌粉在冻干过程中生成了大量脂类和类脂类分子,如磷脂酰甘油、磷脂酸、磷脂酰乙醇胺、(2E)-戊烯酰辅酶A等,这些物质能维持菌体细胞膜的结构和功能,并且可以通过改变膜脂肪酸组成和含量调节细胞膜的通透性和流动性,以此来应对不良环境[19]。有机酸及其衍生物,即氨基酸、肽以及其类似物。氨基酸对蛋白质的构建至关重要,可以支持乳酸菌的多种生命活动[20]。沙棘肽是沙棘蛋白的水解产物,具有生物活性,含多种氨基酸残基和活性肽段。同时氨基酸和肽的累积也有助于稳定菌体的蛋白质结构和功能,增强菌体抵抗不良环境的能力。有机杂环化合物,其环结构包含至少一个非碳原子(杂原子,如氮、氧、硫等)。合成有机杂环化合物的底物通常来源于细胞的糖代谢、脂肪酸代谢、氨基酸代谢等过程。产生的部分有机杂环化合物可通过抑制细菌细胞壁合成、蛋白质合成或核酸合成,对乳酸片球菌等革兰氏阳性菌有抑制作用。
2.5 差异代谢物的代谢通路分析
对差异代谢物的通路富集分析,有助于了解相关的差异代谢物代谢途径的变化。基于KEGG数据库以及应用超几何检验,找出与整个背景相比,在显著差异表达代谢物中显著富集的通路条目。以P-value≤0.05为阈值,满足此条件则为在差异代谢物中显著富集的通路。P-value越小则差异性越显著。得到的结果如图4所示,图中横坐标为富集分值,纵坐标为前20的通路信息。气泡越大的通路包含的差异代谢物越多,气泡颜色由蓝-红变化,红色表示P-value小,显著程度大。
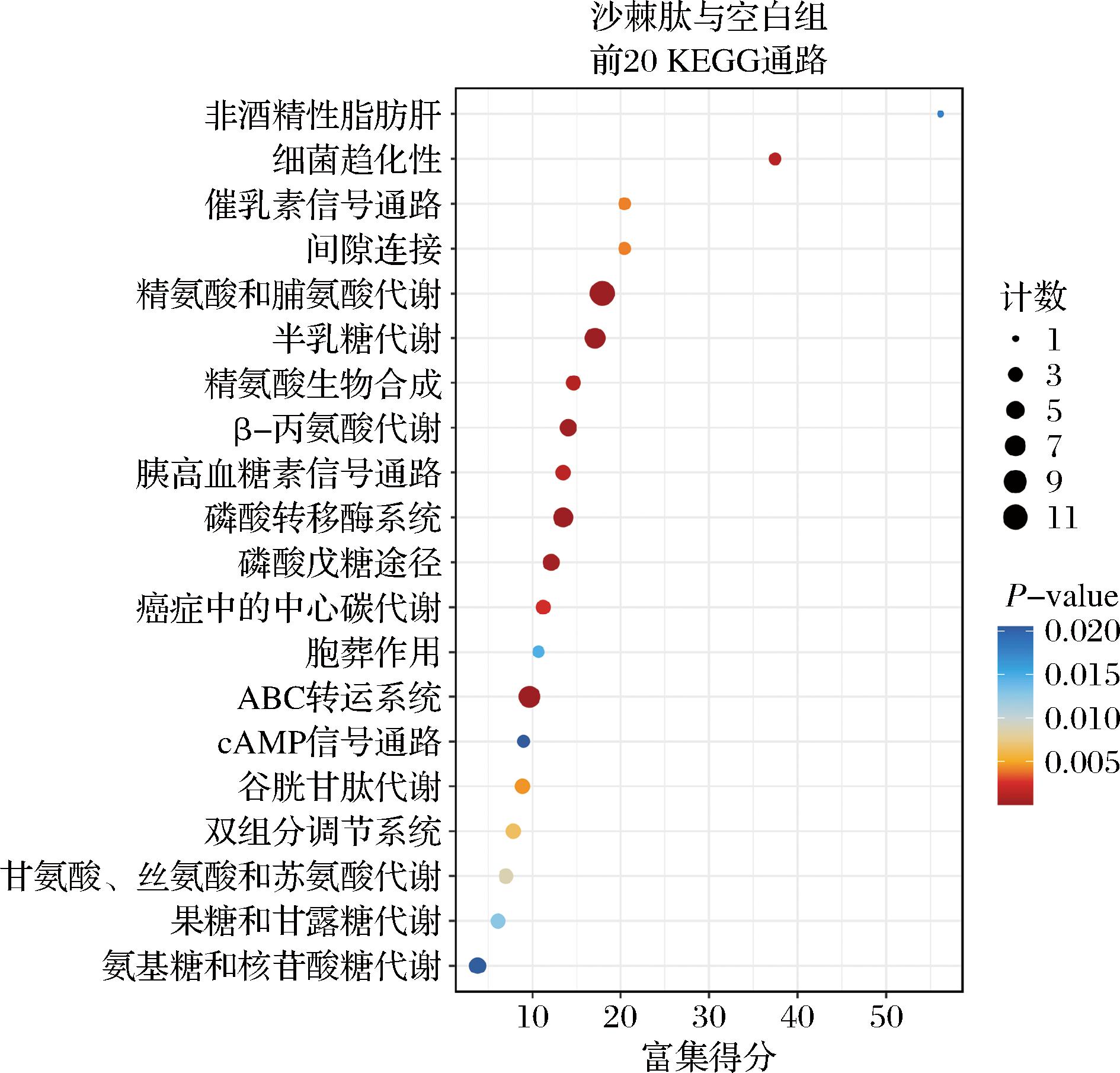
图4 差异代谢物的KEGG富集气泡图
Fig.4 KEGG-enrichment bubble plot of differential metabolites
在筛选出的720种差异代谢物中,只有56种参与了代谢调控,根据代谢物数量以及通路显著程度,可得到主要的代谢通路,如表5所示,可以看到差异代谢物富集的许多通路都涉及氨基酸代谢,可以推测沙棘肽的加入主要使乳酸片球菌通过调节氨基酸代谢来适应不良环境以维持细胞存活。除此之外,还有部分差异物富集于碳水化合物代谢以及膜运输通路中。其中参与某个通路的代谢物越多,说明该生物学通路越活跃。差异代谢物富集前三的代谢通路分别为精氨酸和脯氨酸代谢、半乳糖代谢、ABC转运蛋白。精氨酸和脯氨酸代谢是最为富集的通路,参与的差异代谢物有:腐胺、亚精胺、精胺等11种,这些代谢物共同构成精氨酸-脯氨酸代谢网络,协调氮源利用、能量供应及胁迫响应,减少不良环境给细胞造成的损伤[21]。半乳糖代谢通路参与的差异代谢物有:UDP-D-半乳糖、D-半乳糖等7种,主要作用是快速生成ATP支持冻干后菌体复苏的能量需求,同时通过UDP-半乳糖驱动脂多糖和荚膜多糖的合成,增强细胞壁机械强度以抵御冻干损伤。ABC转运蛋白可以通过摄入亲水性保护剂进入细胞体内发挥作用,并利用ATP的结合和水解为各种底物跨膜转运提供动力[22]。
表5 富集的主要代谢通路信息
Table 5 Enrichment of information on major metabolic pathways

通路名称代谢物总数匹配代谢物数量代谢物名称精氨酸和脯氨酸代谢5611尿素、腐胺、亚精胺、胍基乙酸、精胺、三亚甲基二胺、磷酸肌酸、N-甲基乙内酰脲、L-谷氨酰 5-磷酸、2-氧代-5-胍基戊酸酯(2-氧代精氨酸)、N(omega)-羟基精氨酸半乳糖代谢567葡萄糖、UDP-D-半乳糖、D-半乳糖、D-山梨糖醇、D-塔加糖、D-6-磷酸半乳糖、乳糖6-磷酸ABC 转运蛋白568葡萄糖、硫酸盐、尿素、D-核糖、四亚甲基二胺(腐胺)、亚精胺、D-山梨糖醇、壳聚糖磷酸转移酶系统566葡萄糖、D-半乳糖、D-甘露醇、D-山梨糖醇、D-6-磷酸半乳糖、乳糖6-磷酸盐β-丙氨酸代谢564亚精胺、精胺、三亚甲基二胺、β-丙氨酰辅酶A磷酸戊糖途径564葡萄糖、D-核糖、葡萄糖酸、2-磷酸-D-甘油酸精氨酸生物合成563尿素、富马酸、N-乙酰-L-谷氨酸
3 讨论
基于差异代谢物以及主要代谢途径的分析,预测沙棘肽进入菌体后,通过代谢调控对乳酸片球菌的冻干保护机制,如图5所示。沙棘肽作为生物活性肽,包含多种氨基酸以及小分子肽段,通过转运蛋白或被动运输途径均可进入菌体细胞内。由图5可知,差异代谢物L-谷氨酸5-磷酸、胍基乙酸、富马酸、尿素的上调说明多种氨基酸都参与了代谢调节。但在筛选差异代谢物时,氨基酸并没有上下调的波动,反而各种多肽出现显著上调及下调,可以推测氨基酸在菌体内通过肽键连接形成了多肽,如检测出的缬氨酰-酪氨酰-亮氨酰-精氨酸、脯氨酰-苯丙氨酰-谷氨酰胺、胸腺五肽、天冬酰胺酰-天冬酰胺酰-异亮氨酸等70多种肽类显著上调。其中部分多肽的氨基可与羧基形成氢键,形成α-螺旋和β-折叠等二级结构,防止蛋白质在低温下解旋或变形,或通过疏水相互作用力等形成三级结构,稳定蛋白质的天然构象,防止蛋白质在冷冻干燥过程中变性和聚集。如天冬氨酰-缬氨酰-异亮氨酸、甘氨酰-苯丙氨酰-谷氨酸、天冬氨酰-脯氨酰-苯丙氨酸等显著下调的50多种肽类。其中通过傅里叶红外光谱,对菌体细胞结构进行定性定量分析,也能验证菌体蛋白质结构的变化。如图6所示,光谱中与蛋白质相关的峰区域在1 700~1 500 cm-1,包括酰胺Ⅰ带(约1 700~1 600 cm-1)和酰胺Ⅱ带(1 600~1 500 cm-1),可反映蛋白质的二级结构[23]。其中酰胺Ⅰ带主要来源于C![]() O伸缩振动和C—N的拉伸振动,对二级结构的变化十分敏感。在酰胺Ⅰ带中,沙棘肽组吸收峰强于空白组,吸收峰的强度能反映含量的变化,说明沙棘肽能减少菌体蛋白质结构的损伤。空白组菌粉酰胺Ⅰ带峰值为1 657.70 cm-1,多为α-螺旋(1 650~1 658 cm-1附近),沙棘肽组酰胺Ⅰ带峰值为1 683.67 cm-1,多为β-折叠(1 680~1 700 cm-1附近)。酰胺Ⅱ带来源于N—H弯曲振动以及C—N伸缩振动,空白菌粉酰胺Ⅱ带对应的峰值为1 539.64 cm-1,与其相比,沙棘肽组菌粉的峰值发生了偏移,为1 529.98 cm-1,往低波数偏移主要是因为分子间氢键作用加强,氢键作用通常会导致分子内的化学键变弱,从而降低分子之间的振动频率,导致红外吸收峰向低波数方向移动,氢键作用的增强可使蛋白质结构更加稳定。
O伸缩振动和C—N的拉伸振动,对二级结构的变化十分敏感。在酰胺Ⅰ带中,沙棘肽组吸收峰强于空白组,吸收峰的强度能反映含量的变化,说明沙棘肽能减少菌体蛋白质结构的损伤。空白组菌粉酰胺Ⅰ带峰值为1 657.70 cm-1,多为α-螺旋(1 650~1 658 cm-1附近),沙棘肽组酰胺Ⅰ带峰值为1 683.67 cm-1,多为β-折叠(1 680~1 700 cm-1附近)。酰胺Ⅱ带来源于N—H弯曲振动以及C—N伸缩振动,空白菌粉酰胺Ⅱ带对应的峰值为1 539.64 cm-1,与其相比,沙棘肽组菌粉的峰值发生了偏移,为1 529.98 cm-1,往低波数偏移主要是因为分子间氢键作用加强,氢键作用通常会导致分子内的化学键变弱,从而降低分子之间的振动频率,导致红外吸收峰向低波数方向移动,氢键作用的增强可使蛋白质结构更加稳定。
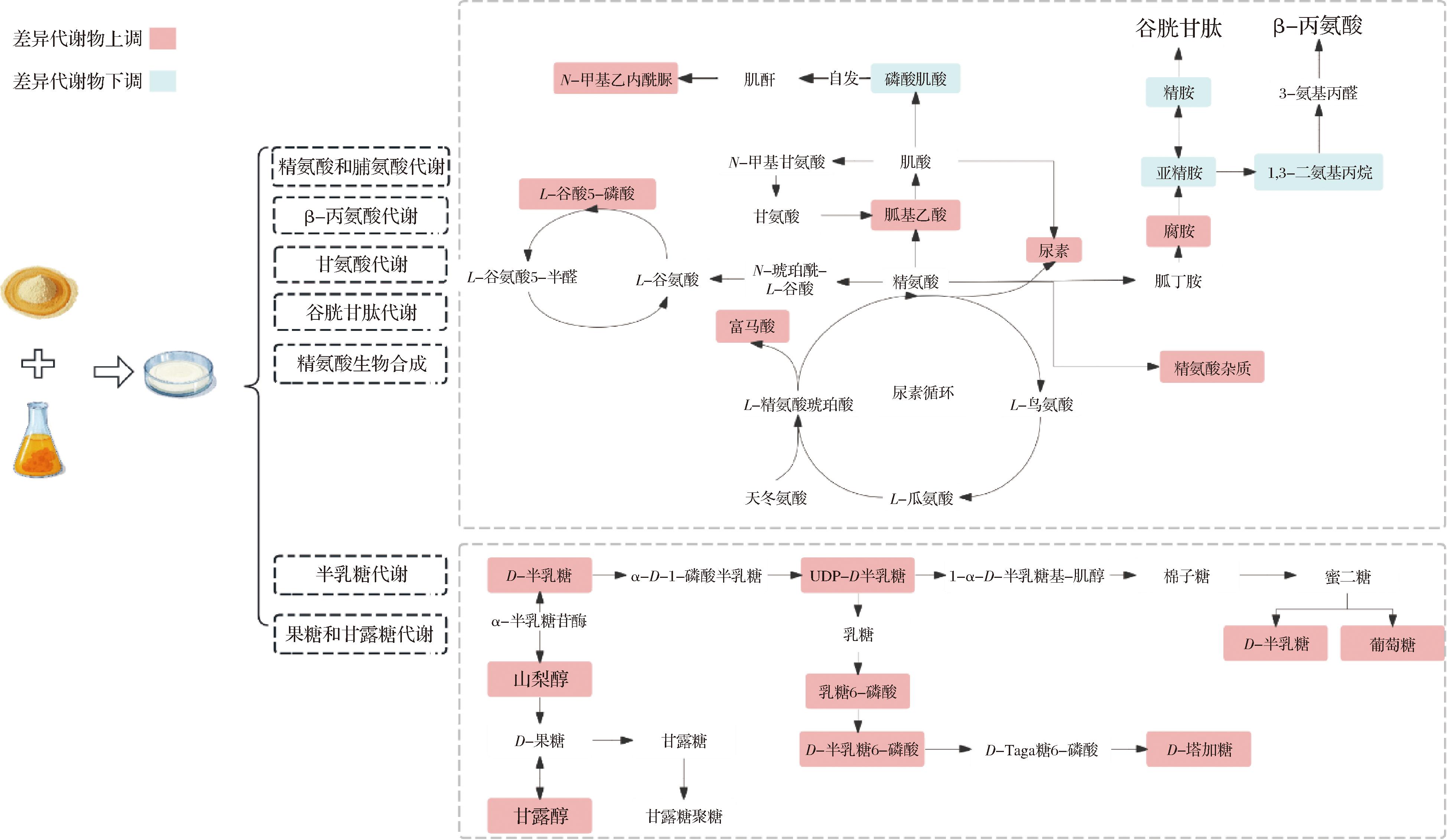
图5 沙棘肽通过代谢调控对乳酸片球菌的冻干保护机制
Fig.5 Lyophilization protective mechanism of seabuckthorn peptide against P.acidilactici through metabolic regulation
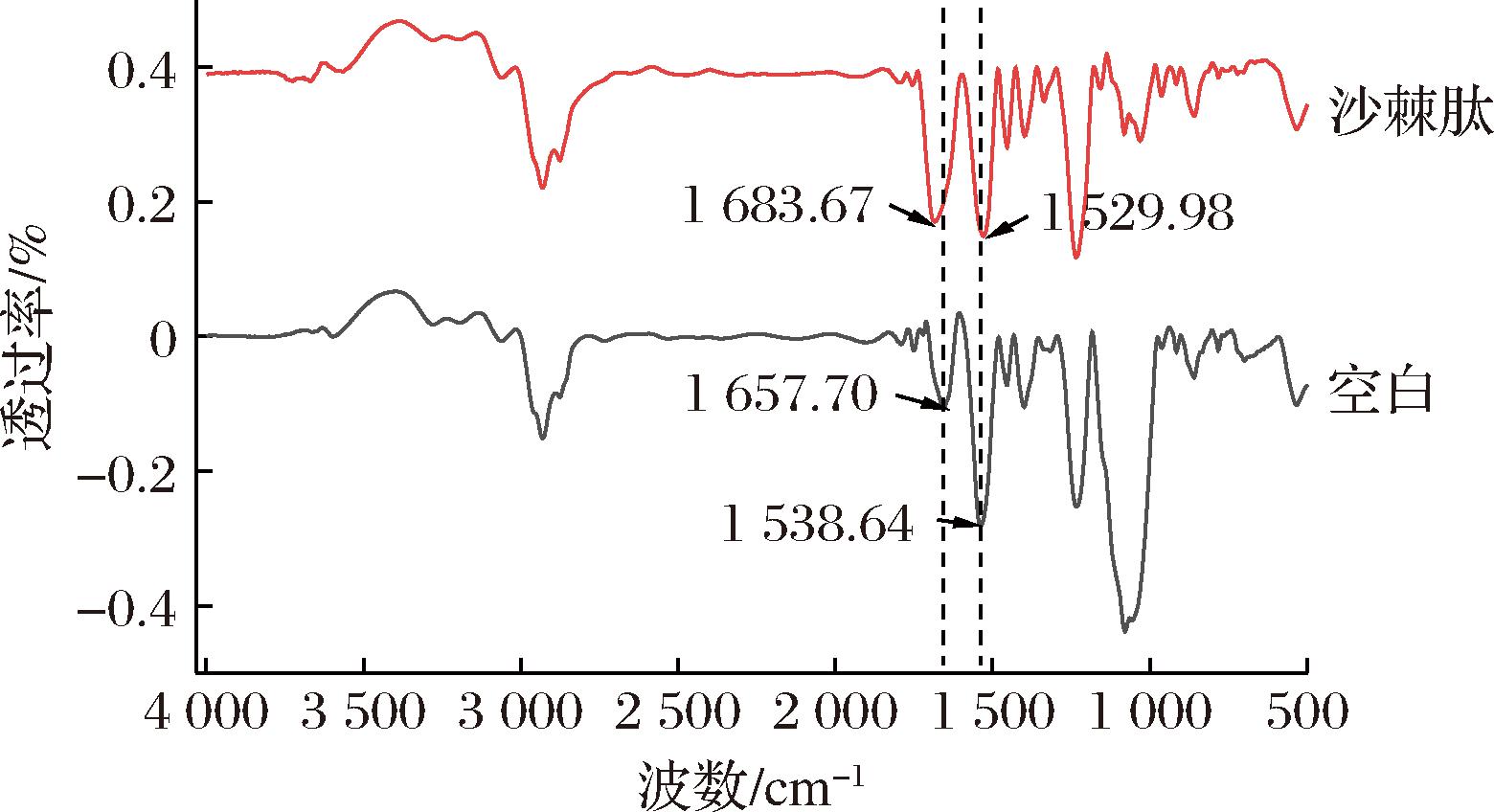
图6 空白与沙棘肽组菌粉的傅里叶红外光谱
Fig.6 Fourier transform infrared spectra of blank and seabuckthorn peptidactyl powder
在差异代谢物的富集中发现,在沙棘肽加入后,精氨酸和脯氨酸代谢、精氨酸生物合成、β-丙氨酸代谢、甘氨酸代谢、谷胱甘肽代谢等通路显著活跃。通过多条代谢通路网络图分析,可以推断沙棘肽在进入细胞体内后,先是通过精氨酸和脯氨酸途径生成腐胺,腐胺再生成精胺,精胺分别进入谷胱甘肽、β-丙氨酸代谢途径生成谷胱甘肽以及β-丙氨酸。其中谷胱甘肽是一种含γ-酰胺键和巯基的三肽,由谷氨酸、半胱氨酸及甘氨酸组成,具有抗氧化、清除自由基等生理功能,是冻干中常用的抗氧化类保护剂。有研究表明,在生物体内,谷胱甘肽通过保护蛋白质的巯基从而使生物体内的蛋白质维持在正常的活性水平;抑制脂质的过氧化,从而保护细胞膜,恢复细胞功能:抑制自由基的生成,对DNA的合成及修复发挥保护作用[24]。但在本研究中,谷胱甘肽合成的前体物质精胺含量显著下调,可能影响谷胱甘肽的合成,减少菌体对自由基的清除。而β-丙氨酸是天然存在的β型氨基酸[25],最重要的L-天冬氨酸衍生氨基酸之一,是泛酸和辅酶A生物合成的前体物质,在此代谢通路上检测到β-腺苷辅酶A上调。此外精氨酸还在其生物合成途径通过尿素循环,生成L-鸟氨酸以及L-瓜氨酸等氨基酸,还产生了富马酸,富马酸参与三羧酸循环,为细胞供能。
除了氨基酸代谢途径,半乳糖代谢途径也富集了近10种差异代谢物,其中半乳糖可通过α-半乳糖苷酶生成山梨醇,山梨醇又可通过果糖和甘露糖代谢途径生成甘露醇。代谢调控是山梨醇胞内合成的一个重要途径,有研究指出,部分乳酸菌可以通过甘露醇脱氢酶直接将果糖还原为甘露醇[26],并通过山梨醇磷酸转移酶系统控制山梨醇的转运及磷酸化,这与本研究结果相符。VIANA等[27]在缺乏乳酸脱氢酶的菌株中检测到甘露醇的合成,说明乳酸片球菌在冻干过程中乳酸脱氢酶的活性受到破坏。山梨醇和甘露醇都是常用的多元醇类保护剂,可通过氢键吸附水分、维持细胞内胶态,减少脱水引起的膜塌陷,其羟基与益生菌膜蛋白的极性基团或膜磷脂的磷酸基团结合,在冻干过程中稳定了菌体内蛋白质的结构,并保护细胞膜的完整性。从表3保护剂筛选中也可以看出山梨醇和甘露醇作为冻干保护剂时,活菌数与空白组具有显著差异(P<0.05),对乳酸片球菌具有保护效果。此外,在乳酸片球菌中,由磷酸转移酶系统转运的乳糖被水解为6-磷酸半乳糖,通过D-Taga糖6-磷酸途径转化,然后以磷酸丙糖形式进入糖酵解,为菌体生命活动供能。
在代谢物主要富集的通路中,没有出现与脂质代谢相关的通路。但在筛选差异代谢物的过程中,检测出145种上调的脂质和类脂质分子,结合上面β-丙氨酸代谢途径,可以推测β-丙氨酸在乳酸片球菌内合成辅酶A,如(2E)-戊烯酰辅酶A、β-丙氨酰辅酶A、4-乙酰氨基丁酰辅酶A、(2E)-谷氨酰肉碱-CoA等辅酶因子。这些辅酶因子能与酶结合,帮助催化脂肪酸的合成和降解,参与脂肪酸β-氧化过程,从而产生脂质和类脂质分子。
4 结论
本研究对乳酸片球菌的冻干保护剂进行了筛选,得到沙棘肽为最优保护剂,通过单因素试验对保护剂的浓度进行探究,发现30 g/L的沙棘肽作为保护剂时,乳酸片球菌制剂的活菌数最高,为2.34×1012 CFU/g。利用超高效液相色谱-质谱以及气相色谱-质谱双平台非靶向代谢组学分析方法,选取空白组与沙棘肽组,比较2组菌粉的差异代谢产物,根据P<0.05、变量投影重要性≥1和变化倍数≥4共筛选出720种显著差异代谢物,主要包括脂质和类脂质分子、有机酸及其衍生物。通过差异代谢物共富集到精氨酸和脯氨酸代谢、半乳糖代谢、ABC转运蛋白等多条代谢通路。结合差异代谢物及代谢通路,推测沙棘肽对乳酸片球菌的冻干保护机制通过半乳糖代谢途径生成山梨醇、甘露醇等常用保护剂,结合前期保护剂筛选已经发现其对乳酸片球菌的保护效果,但与沙棘肽比还有较大差距,说明除了生成甘露醇和山梨醇,更多的保护效果来源于氨基酸代谢,尤其是差异代谢物富集的精氨酸和脯氨酸代谢途径十分重要,沙棘肽的加入使菌体氨基酸代谢途径活跃,并利用氨基酸和肽进行连接或折叠,保护冻干过程中蛋白质的结构和功能,维持细胞正常生命活动。本研究结果从表观遗传角度上揭示沙棘肽对乳酸片球菌的冻干保护机制,为植物源肽对乳酸菌的冻干保护机制提供了理论支持,为植物源肽成为新型冻干保护剂提供了新思路。
[1] DIANAWATI D, MISHRA V, SHAH N P.Survival of microencapsulated probiotic bacteria after processing and during storage:A review[J].Critical Reviews in Food Science and Nutrition, 2016, 56(10):1685-1716.
[2] 寇佳祥. 益生菌复合冷冻及冻干保护剂的开发与应用[D].天津:天津大学, 2022.
KOU J X.Development and application of probiotic compound freezing and lyophilized protective agent[D].Tianjin:Tianjin University, 2022.
[3] 王轶男, 胡诗悦, 于龙政.乳酸片球菌在动物生产中的研究进展[J].中国兽医杂志, 2021, 57(4):54-57.
WANG Y N, HU S Y, YU L Z.Research progress of Pediococcus acidilactici in animal production[J].Chinese Journal of Veterinary Medicine, 2021, 57(4):54-57.
[4] 张馨钰, 钟明, 崔莲花, 等.植物淀粉对乳酸片球菌微胶囊冻干保护及储存性能的影响[J].中国畜牧兽医, 2024, 51(10):4596-4605.
ZHANG X Y, ZHONG M, CUI L H, et al.Effect of plant starch on freeze-drying protection and storage performance of Pediococcus acidilactici microcapsules[J].China Animal Husbandry &Veterinary Medicine, 2024, 51(10):4596-4605.
[5] 潘子怡, 陈则华, 毛丙永, 等.青春双歧杆菌冻干保护剂筛选及高密度冻干工艺优化[J].食品与生物技术学报, 2024, 43(2):23-29.
PAN Z Y, CHEN Z H, MAO B Y, et al.Screening of lyoprotectants and optimization of high-density freeze-drying process for Bifidobacterium adolescentis[J].Journal of Food Science and Biotechnology, 2024, 43(2):23-29.
[6] 朱蒙蒙, 李国莹, 顾秋亚, 等.响应面法优化青春双歧杆菌增殖培养基[J].食品与生物技术学报, 2019, 38(4):111-117.
ZHU M M, LI G Y, GU Q Y, et al.Optimization of enrichment medium for Bifidobacterium adolescentis by response surface methodology[J].Journal of Food Science and Biotechnology, 2019, 38(4):111-117.
[7] 吴家琳, 李滢, 刘振杰, 等.益生菌冷冻干燥高活性保护机制研究进展[J].微生物学报, 2024, 64(5):1402-1416.
WU J L, LI Y, LIU Z J, et al.Research progress in the mechanism of freeze-drying in protecting the high vitality of probiotics[J].Acta Microbiologica Sinica, 2024, 64(5):1402-1416.
[8] CAPELA P, HAY T K C, SHAH N P.Effect of cryoprotectants, prebiotics and microencapsulation on survival of probiotic organisms in yoghurt and freeze-dried yoghurt[J].Food Research International, 2006, 39(2):203-211.
[9] 刘开文, 马雯, 金刚.真空冷冻干燥提高乳酸菌存活率及延长贮藏期的研究进展[J].食品科学, 2024, 45(2):325-333.
LIU K W, MA W, JIN G.Research progress on improving the survival rate and extending the storage period of lactic acid bacteria through vacuum freeze-drying[J].Food Science, 2024, 45(2):325-333.
[10] 张晓月, 王涛, 左志晗, 等.复合益生菌发酵培养基与冻干保护剂的筛选[J].天津师范大学学报(自然科学版), 2023, 43(6):32-38.
ZHANG X Y, WANG T, ZUO Z H, et al.Screening of compound probiotic fermentation medium and freeze-drying protective agents[J].Journal of Tianjin Normal University (Natural Science Edition), 2023, 43(6):32-38.
[11] 陈胜杰, 高翔, 袁戎宇.真空冷冻干燥法制备益生菌粉的冻干保护剂配方优化[J].食品工业科技, 2021, 42(1):182-187;196.
CHEN S J, GAO X, YUAN R Y.Formulation optimization of freeze-drying protectant for probiotics powder by vacuum freeze-drying[J].Science and Technology of Food Industry, 2021, 42(1):182-187;196.
[12] 李兵兵, 龙慧, 伍恩慧, 等.银耳多糖对冻干植物乳杆菌细胞膜及糖代谢酶的保护作用[J].现代食品科技, 2021, 37(11):85-95.
LI B B, LONG H, WU E H, et al.Protective effects of polysaccharides extracted from Tremella on cell membrane and sugar metabolism enzymes of freeze-dried Lactobacillus plantarum[J].Modern Food Science and Technology, 2021, 37(11):85-95.
[13] LI H P, ZHAO P, ZHANG S H, et al.Protective effect of polysaccharides from Pholiota nameko on Lactobacillus casei ATCC 334 subjected to freeze-drying[J].LWT, 2019, 115:108463.
[14] MIKAJIRI S, SOGABE T, CAO R D, et al.Glass transition behavior of carnosine and its impact as a protectant on freeze-dried lactic acid bacteria[J].Food Biophysics, 2022, 17(1):1-9.
[15] KWON G, HEO B, KWON M J, et al.Effect of silk fibroin biomaterial coating on cell viability and intestinal adhesion of probiotic bacteria[J].Journal of Microbiology and Biotechnology, 2021, 31(4):592-600.
[16] 王昊乾. 抗氧化肽HP3-2在真空冷冻干燥过程中对乳双歧杆菌Probio-M8细胞保护机制的研究[D].呼和浩特:内蒙古农业大学, 2022.
WANG H Q.Study on the protective mechanism of antioxidant peptide HP3-2 on Bifidobacterium lactis Probio-M8 cells during vacuum freeze-drying[D].Hohhot:Inner Mongolia Agricultural University, 2022.
[17] DING T, LI Y.Beneficial effect and mechanism of walnut oligopeptide on Lactobacillus plantarum Z7[J].Food Science &Nutrition, 2021, 9(2):672-681.
[18] 王迪, 李文霞, 姚瑜, 等.沙棘蛋白和多肽的提取及功能活性研究进展[J].食品工业科技, 2022, 43(3):447-455.
WANG D, LI W X, YAO Y, et al.Research progress on extraction and functional activity of sea buckthorn protein and polypeptides[J].Science and Technology of Food Industry, 2022, 43(3):447-455.
[19] WU C D, ZHANG J, WANG M, et al.Lactobacillus casei combats acid stress by maintaining cell membrane functionality[J].Journal of Industrial Microbiology &Biotechnology, 2012, 39(7):1031-1039.
[20] MIYAJIMA M.Amino acids:Key sources for immunometabolites and immunotransmitters[J].International Immunology, 2020, 32(7):435-446.
[21] WANG W W, HE J Y, PAN D D, et al.Metabolomics analysis of Lactobacillus plantarum ATCC 14917 adhesion activity under initial acid and alkali stress[J].PLoS One, 2018, 13(5):e0196231.
[22] 王会莹, 薄晓宇, 袁保壹, 等.基于代谢组学分析Lentilactobacillus kefiri IMAU10804酸胁迫前后的代谢物差异[J].食品与发酵工业, 2024, 50(22):197-203;213.
WANG H Y, BO X Y, YUAN B Y, et al.Metabolomics-based analysis of Lentilactobacillus kefiri IMAU10804 metabolite differences before and after acid stress[J].Food and Fermentation Industries, 2024, 50(22):197-203;213.
[23] HU G, ZHANG J M, WANG Q, et al.Succinylation modified ovalbumin:Structural, interfacial, and functional properties[J].Foods, 2022, 11(18):2724.
[24] 高薇, 韩雪, 张兰威.乳酸菌渗透胁迫相关相容性溶质及其转运机制研究进展[J].微生物学通报, 2013, 40(11):2097-2106.
GAO W, HAN X, ZHANG L W.Research advances of the osmotic stress-related compatible solutes of lactic acid bacteria and it’s transport mechanism[J].Microbiology China, 2013, 40(11):2097-2106.
[25] 赵嫚, 刘薇, 成浩, 等.β-丙氨酸合成方法的研究进展[J].食品与发酵工业, 2022, 48(10):306-313.
ZHAO M, LIU W, CHENG H, et al.Research progress in synthesis method of β-alanine[J].Food and Fermentation Industries, 2022, 48(10):306-313.
[26] NISSEN L, PÉREZ-MART NEZ G, YEBRA M J.Sorbitol synthesis by an engineered Lactobacillus casei strain expressing a sorbitol-6-phosphate dehydrogenase gene within the lactose operon[J].FEMS Microbiology Letters, 2005, 249(1):177-183.
NEZ G, YEBRA M J.Sorbitol synthesis by an engineered Lactobacillus casei strain expressing a sorbitol-6-phosphate dehydrogenase gene within the lactose operon[J].FEMS Microbiology Letters, 2005, 249(1):177-183.
[27] VIANA R, YEBRA M J, GAL N J L, et al.Pleiotropic effects of lactate dehydrogenase inactivation in Lactobacillus casei[J].Research in Microbiology, 2005, 156(5-6):641-649.
N J L, et al.Pleiotropic effects of lactate dehydrogenase inactivation in Lactobacillus casei[J].Research in Microbiology, 2005, 156(5-6):641-649.