荔枝(Litchi chinensis Sonn.)是热带及亚热带区域种植的重要经济作物之一,富含酚类、抗氧化性物质等活性组分,是消费者喜爱的上乘果品[1]。荔枝常被加工成罐头、荔枝干等食品,但约为全果14.11%~22.88%的壳则作为废物被丢弃,且污染环境。荔枝壳富含酚类、黄烷醇衍生物、儿茶素、原花青素等活性成分,具有抗氧化、免疫调节、抗癌等作用[2]。这些成分在食品、化妆品和保健品等领域具有广泛的应用前景。
荔枝壳中的酚类有游离态和结合态2种形式,后者与其纤维素、半纤维素、木质素、果胶等以共价结合方式存在,水提取的效率非常低[3]。在曾报道的酸、碱、酶解等7种常用的提取方法中,用丙酮、乙醇等有机溶剂提取不仅成本高,且其残液等废弃物会污染环境,所以主要用于测定其活性成分[4]。果胶酶、β-葡萄糖苷酶、单宁酶等组成的复合酶辅助提取,提高了酚类的提取量,能将部分酚类转化为更高活性的苷元,但提取成分的一致性和效率难以保证。以菌群发酵液辅助提取的方式是一种更新颖的提取技术,复杂的酶系能够将部分底物水解,也可将前体物质转化为活性成分。如黑曲霉发酵荔枝壳将酚类等成分转化为游离态,且诱导了抗氧化成分合成[5],此外,也有用荔枝壳生产木聚糖酶[6]。以荔枝壳作底物,反复定向驯化菌群能有效地使群落及分泌的酶更适合其组织结构崩解、转化前体,具有改善提取活性成分的潜力,但鲜见相关报道。
本文描述了以荔枝壳为唯一碳源,以不同来源的微生物群落为对象,采用持续定向驯化策略,提高其菌群发酵液对荔枝壳活性成分的提取效果。同时优化溶剂提取过程参数,研究了有机溶剂与发酵液提取物中成分组成特点,且探究了发酵液间的群落结构及代谢途径的差异。本研究旨在揭示高效提取活性成分的群落与代谢网络互作机制,为开发菌群发酵液提取技术奠定理论基础。
1 材料与方法
1.1 材料与试剂
荔枝壳粉(妃子笑的荔枝壳),四川省泸州市农贸市场。
植物水解酶:纤维素酶(400 U/mg)、木聚糖酶(100 U/mg)、果胶酶(50 000 U/mg)、β-葡萄糖苷酶(30 000 U/mg)和单宁酶(200 U/mg),上海源叶生物科技有限公司;色谱级试剂:乙腈、甲酸,上海西格玛奥德里奇贸易有限公司;Fast DNA SPIN试剂盒,美国安诺论公司;分析纯试剂:酵母膏、蛋白胨,北京奥博星生物技术有限公司,乙酸乙酯、无水乙醇、福林酚、培养基试剂,成都科隆化学品有限公司;丙酮、羧甲基纤维素钠,天津福晨化学试剂有限公司。
无机培养基(g/L):荔枝壳粉20,KH2PO4 2.0,(NH4)2SO4 1.4,尿素0.3,FeSO4·7H2O 0.3,CaCl2·2H2O 0.4,FeSO4·7H2O 5.0 mg,MnSO4·H2O 1.6 mg,ZnSO4 1.7 mg,121 ℃灭菌20 min。
复合培养基(g/L):蛋白胨3.0;硫酸铵2.0;K2HPO4 4.0;MgSO4·7H2O 0.3;NaCl 0.3;酵母膏0.5;羧甲基纤维素钠10.0,121 ℃灭菌20 min。
1.2 仪器与设备
GL-20G-Ⅱ立式高速冷冻离心机,上海安亭科学仪器有限公司;DHG-9070A电热鼓风干燥箱,上海一恒科学仪器有限公司;1290 Infinity Ⅱ型超高效液相色谱-四极杆飞行质谱系统,美国安捷伦公司;RE-5298旋转蒸发器,上海生化仪器厂。
1.3 实验方法
1.3.1 溶剂法提取荔枝壳多酚物质条件优化
分别采用丙酮(体积分数为60%)、乙酸乙酯、无水乙醇和水,取经50 ℃烘箱干燥 12 h、60 目筛分的荔枝壳粉,按料液比1∶100(g∶mL), 30 ℃提取6 h,以提取物的总酚含量(total phenolic,TP),筛选最适溶剂。
最适溶剂(乙醇)提取参数的优化:提取温度和时间设置为30 ℃和6 h,测定乙醇体积分数分别为25%、45%、65%、85%、100%提取TP的含量,随后将乙醇体积分数和提取时间设置为85%和6 h,测定30、40、50、55、60 ℃提取的TP含量。然后将乙醇体积分数和温度设置为85%和50 ℃,测定6、12、18、24、30 h提取的TP含量。
1.3.2 定向驯化功能菌群
参考WRIGHT等[7]的方法,从中国四川省泸州市桂妃园的土壤(T组)和荔枝树下的自然腐败降解的果壳(K组)中定向驯化获得功能菌群。取5 g样品与50 mL无菌水均质,取10 mL均质液加入100 mL无机培养基,在30 ℃、150 r/min的条件下培养,每代培养结束后,测定活菌数,离心(4 ℃,12 000 r/min,10 min)收集菌团,无菌生理盐水洗涤沉淀物3次后,重新悬浮在相同体积无机培养基中,同条件培养。重复上述驯化过程,直至活菌数在代间趋于稳定(K组在第13和14代,T组在12代和13代时)。收集的菌团置于-80 ℃下保存,菌团分别标注为KA、KB、TA和TB。
1.3.3 不同方式提取TP含量的比较
乙醇提取(CE组):以1.3.1节获得的体积分数为85%的乙醇,加入质量分数为1%的荔枝壳粉,50 ℃下回流提取24 h。
酶法提取(E1~E5组):质量分数为1%的纤维素酶、木聚糖酶、果胶酶、β-葡萄糖苷酶和单宁酶,分别溶于磷酸盐缓冲液(pH 5.0,0.1 mol/L)中,以同样的底物(质量分数为1%),50 ℃下提取3 h。
功能菌群发酵液提取(MA组):4种不同类型菌团,分别接种到复合培养基培养72 h(30 ℃,150 r/min),离心(4 ℃,5 000 r/min,10 min)收集含有菌-酶复合物的发酵上清液。功能菌群发酵液KA、KB、TA和TB中加入质量分数为1%的荔枝壳粉,在50 ℃下提取3 h[7]。
水提取(B组):蒸馏水中加入质量分数为1%的荔枝壳粉,50 ℃下提取3 h。
TP测定:参照ZHANG等[8]的方法进行,以没食子酸当量(gallic acid equivalent, GAE)计算标准曲线(y=0.053 3x+0.023),TP含量以mg GAE/g计。
1.4 非靶向代谢组学分析活性组分
样品预处理:分别取50 mL的CE组、菌群发酵液组和B组的提取液,离心(4 ℃,10 000 r/min,10 min)取上清液,40 ℃真空旋转蒸发除去溶剂,提取物重溶于含2-氯-L-苯丙氨酸内标(质量浓度为102 mg/L)的甲醇溶液(体积分数为80%),使最终内标质量浓度为1.02 μg/mL,经0.22 μm尼龙滤膜过滤后备用。
活性成分的检测:参考LI等[9]的方法。采用配备Zorbax Eclipse Plus C18柱(2.1 mm×50 mm,1.9 μm)和电喷雾离子源的超高效液相色谱-四极杆飞行时间质谱(the ultra-high performance liquid chromatography-quadrupole time-of-flight mass spectrometry,UHPLC-Q/TOF-MS)进行活性成分的检测与鉴定。流动相:质量分数为0.1%的甲酸水溶液(A)和乙腈(B);流速为0.3 mL/min,进样量2 μL。梯度洗脱操作条件:0~3 min,5%~8% B;3~5 min,8%~15% B;5~6 min,15%~18% B;6~9 min,18%~20% B;9~10 min,20%~25% B;10~12 min,25%~60% B;12~14 min,60%~80% B;14~17 min,80%~90% B;17~19 min,90%~100% B;19~21 min,100% B;21~21.5 min,100%~30% B。柱温40 ℃,扫描范围和速率分别为100~1 700 m/z和3 spectra/s。MS条件和原始数据处理:参考MU等[10]叙述的过程与条件完成。根据内标含量与其峰面积的比值对各待测物质进行半定量分析。
1.5 微生物群落结构分析
用Fast DNA SPIN试剂盒提取菌团的总DNA。分别用分光光度计和凝胶电泳检测DNA的浓度和纯度,操作概述如下:配制质量浓度为0.8%的凝胶,将样品与DNA buffer混合后点样,电泳(175 V,20 min)后在凝胶色谱仪上成像。参考ZHANG等[11]所述的扩增程序,根据表1所述引物信息,进行细菌的16S rRNA V3~V4区域和真菌的ITS1区域的PCR扩增。扩增产物分离、纯化、定量后,委托上海派森诺生物科技有限公司使用Illumina NovaSeq平台(2×300 bp)测序。原始序列数据已存入国家基因组数据中心的基因组序列档案馆。序列读取档案编号为CRA016102,可在https://ngdc.cncb.ac.cn/gsa公开获取。
表1 引物信息
Table 1 Primer information
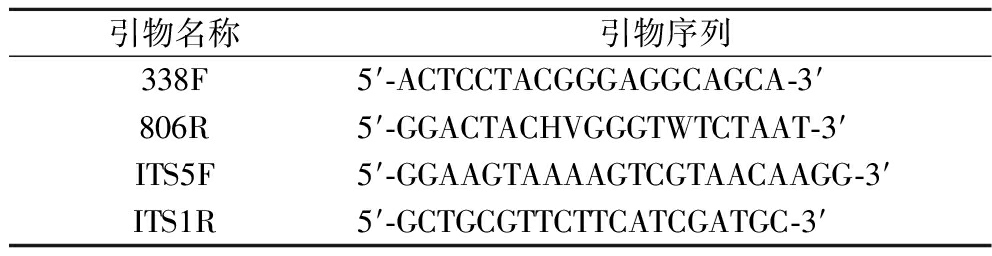
引物名称引物序列338F5′-ACTCCTACGGGAGGCAGCA-3′806R5′-GGACTACHVGGGTWTCTAAT-3′ITS5F5′-GGAAGTAAAAGTCGTAACAAGG-3′ITS1R5′-GCTGCGTTCTTCATCGATGC-3′
1.6 数据处理
所有实验均重复3次,数据以“平均值±标准差”表示,使用SPSS 25.0进行显著性差异分析(P<0.05)。β-多样性采用基于Bray-Curtis距离的主坐标分析(principal coordinates analysis,PCoA)。群落多样性图与Circos图在Genescloud(https://www.genescloud.cn/)平台上绘制。UHPLC-Q/TOF-MS原始二级质谱数据预处理后,与在线数据库(METLIN accurate mass compound,https://www.agilent.com/)比对,后对一级质谱进行物质定性。利用PICRUSt2(phylogenetic investigation of communities by reconstruction of unobserved states)预测微生物群落在KEGG功能数据库中编码酶的丰度。通过Spearman等级相关系数关联分析优势属与活性成分之间单调关系的强度和方向。绘图使用Origin 2021软件完成。
2 结果与分析
2.1 溶剂提取TP的条件优化
图1-a显示了不同溶剂对荔枝壳TP含量的影响。结果表明,体积分数为60%的丙酮提取效率最高,TP含量为31.68 mg GAE/g,无水乙醇次之,TP含量为27.24 mg GAE/g,乙酸乙酯提取TP含量为18.70 mg GAE/g。三者提取效率都显著高于水提取法(4.48 mg GAE/g)。无水乙醇的提取效率达丙酮的85.98%,但前者成本较低且毒性小,故确定乙醇为最佳溶剂。乙醇体积分数显著影响提取效果,见图1-b,体积分数为85%的乙醇溶液提取的TP最多,可能与某些酚类化合物的强极性有关。考察温度和时间对TP含量的结果表明,最佳的温度和时间是50 ℃,24 h,其含量为50.78 mg GAE/g(图1-c和图1-d),表明该条件下能够有效促进酚类物质的溶出,减少热敏感物质的分解。
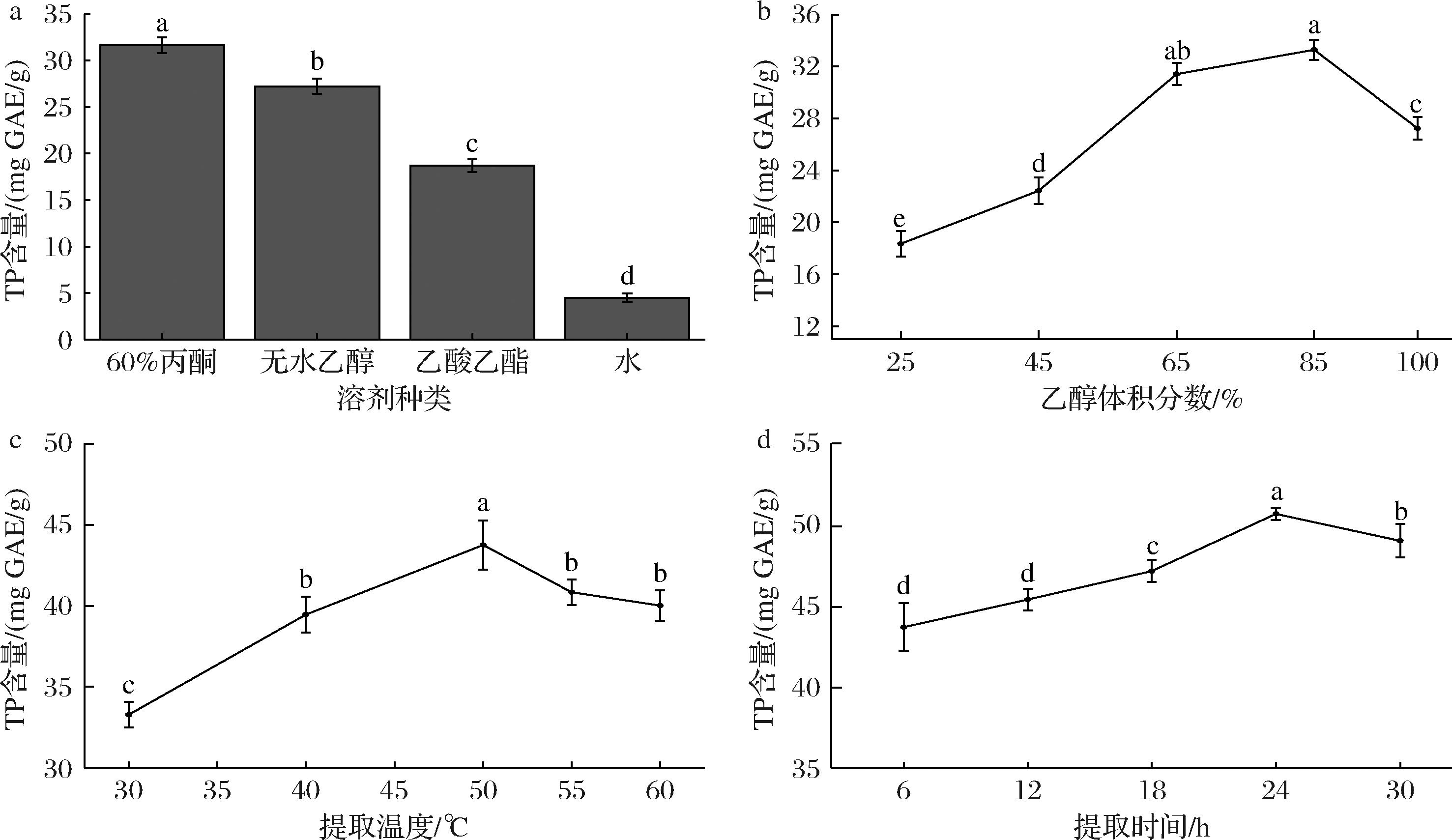
a-溶剂类型;b-乙醇体积分数;c-提取温度;d-提取时间
图1 溶剂提取荔枝壳TP的条件优化
Fig.1 Optimization of conditions for solvent extraction of active components from litchi pericarp
注:不同字母代表差异显著(P<0.05)。
2.2 不同方法提取荔枝壳TP的差异分析
不同提取物的TP含量差异显著。CE组是50.78 mg GAE/g,为最高,K组和T组次之,分别是11.36 mg GAE/g和9.60 mg GAE/g。酶法提取的TP含量与酶作用的特点有关,但差异不显著,在4.79~6.02 mg GAE/g间。虽然曾报道白腊品种荔枝壳的水提物中TP含量为16.06 mg GAE/g[12],但妃子笑品种中则仅为4.48 mg GAE/g,可能与品种间基因的表达水平和代谢物积累、栽培技术和种植区域有关[4,13]。由于降解纤维素和单宁等酶释放荔枝壳中TP的特点,所以酶法提取效果较水提取略增。菌群发酵液提取方式的TP含量较酶法有显著提升,可能与复合酶-功能菌群协同,高效酶解其组织结构有关。
2.3 UHPLC-Q/TOF-MS分析荔枝壳活性组分的差异
经处理的二级质谱数据共鉴定到19 062个特征峰,其中负离子2 296个和正离子16 766个。CE组共注释到30种活性成分:6种酚酸、4种有机酸、2种维生素、6种黄酮类、7种其他类、2种脂肪酸、1种糖类、2种氨基酸等8类活性成分(见表2),总含量为11.14 mg/g;MA组共注释到33种活性成分:3种酚酸、1种有机酸、1种维生素、17种黄酮类、5种其他类、4种脂肪酸、2种糖类、1种氨基酸等8类活性成分(见表3),KA、KB、TA和TB提取物的总含量分别是9.01、9.48、5.63、6.01 mg/g;B组鉴定到26种活性组分,含量仅有2.40 mg/g。
表2 CE提取物种类与含量 单位:μg/g
Table 2 Types and content of CE extracts
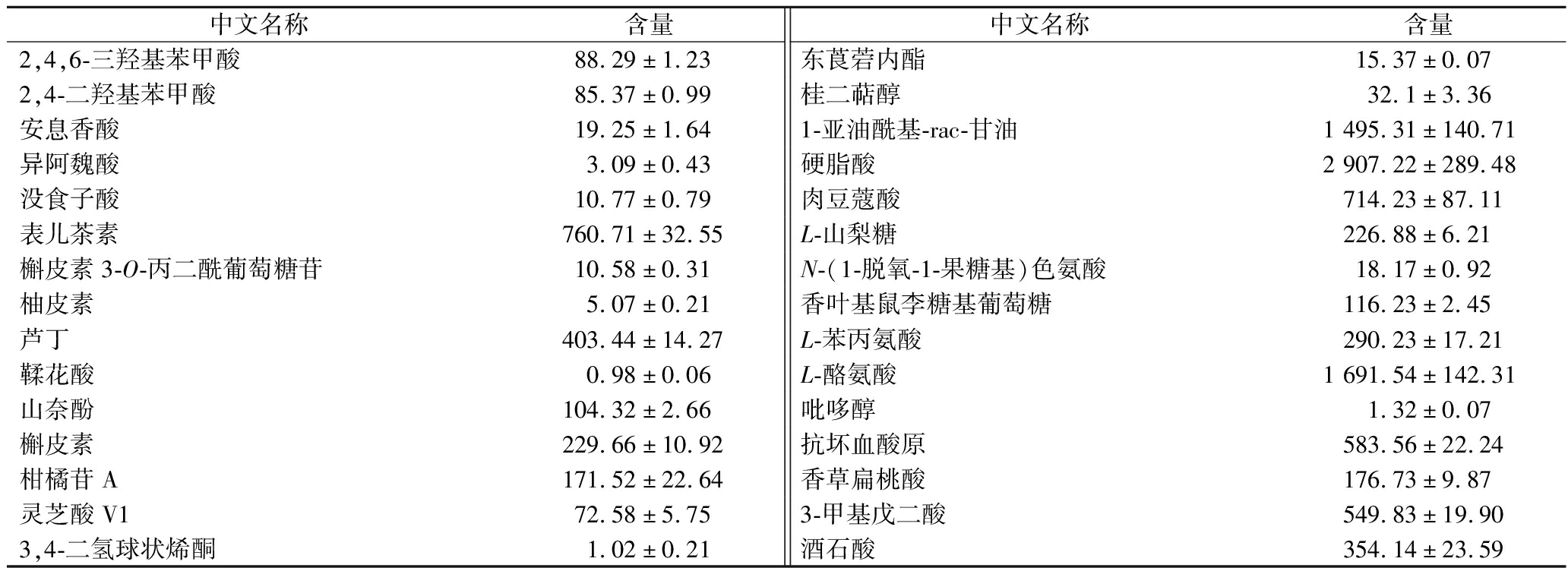
中文名称含量中文名称含量2,4,6-三羟基苯甲酸88.29±1.23东莨菪内酯15.37±0.072,4-二羟基苯甲酸85.37±0.99桂二萜醇32.1±3.36安息香酸19.25±1.641-亚油酰基-rac-甘油1 495.31±140.71异阿魏酸3.09±0.43硬脂酸2 907.22±289.48没食子酸10.77±0.79肉豆蔻酸714.23±87.11表儿茶素760.71±32.55L-山梨糖226.88±6.21槲皮素3-O-丙二酰葡萄糖苷10.58±0.31N-(1-脱氧-1-果糖基)色氨酸18.17±0.92柚皮素5.07±0.21香叶基鼠李糖基葡萄糖116.23±2.45芦丁403.44±14.27L-苯丙氨酸290.23±17.21鞣花酸0.98±0.06L-酪氨酸1 691.54±142.31山奈酚104.32±2.66吡哆醇1.32±0.07槲皮素229.66±10.92抗坏血酸原583.56±22.24柑橘苷A171.52±22.64香草扁桃酸176.73±9.87灵芝酸V172.58±5.753-甲基戊二酸549.83±19.903,4-二氢球状烯酮1.02±0.21酒石酸354.14±23.59
表3 生物活性物质种类与含量 单位:μg/g
Table 3 Types and content of bioactive components
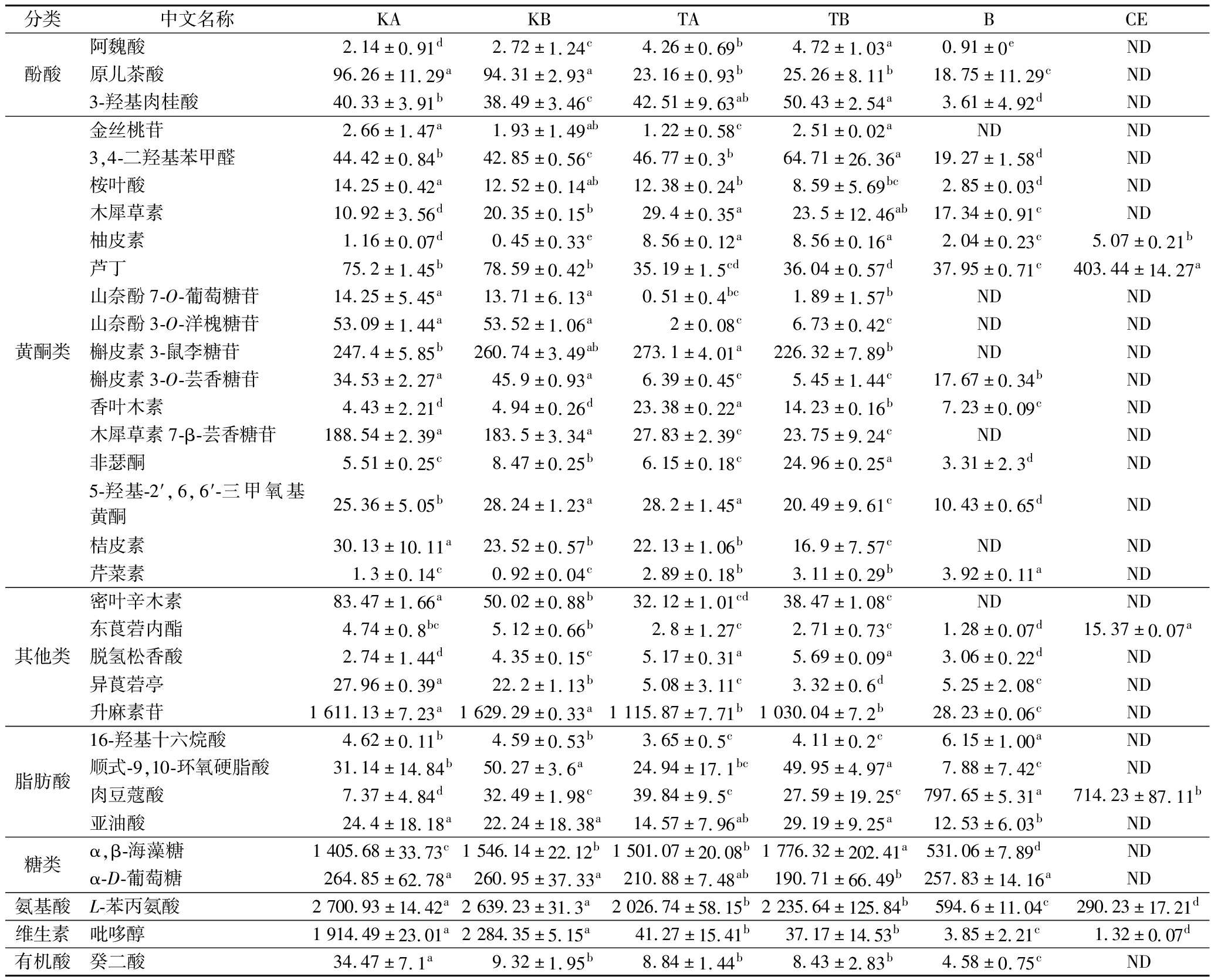
分类中文名称KAKBTATBBCE酚酸阿魏酸2.14±0.91d2.72±1.24c4.26±0.69b4.72±1.03a0.91±0eND原儿茶酸96.26±11.29a94.31±2.93a23.16±0.93b25.26±8.11b18.75±11.29cND3-羟基肉桂酸40.33±3.91b38.49±3.46c42.51±9.63ab50.43±2.54a3.61±4.92dND黄酮类金丝桃苷2.66±1.47a1.93±1.49ab1.22±0.58c2.51±0.02aNDND3,4-二羟基苯甲醛44.42±0.84b42.85±0.56c46.77±0.3b64.71±26.36a19.27±1.58dND桉叶酸14.25±0.42a12.52±0.14ab12.38±0.24b8.59±5.69bc2.85±0.03dND木犀草素10.92±3.56d20.35±0.15b29.4±0.35a23.5±12.46ab17.34±0.91cND柚皮素1.16±0.07d0.45±0.33e8.56±0.12a8.56±0.16a2.04±0.23c5.07±0.21b芦丁75.2±1.45b78.59±0.42b35.19±1.5cd36.04±0.57d37.95±0.71c403.44±14.27a山奈酚7-O-葡萄糖苷14.25±5.45a13.71±6.13a0.51±0.4bc1.89±1.57bNDND山奈酚3-O-洋槐糖苷53.09±1.44a53.52±1.06a2±0.08c6.73±0.42cNDND槲皮素3-鼠李糖苷247.4±5.85b260.74±3.49ab273.1±4.01a226.32±7.89bNDND槲皮素3-O-芸香糖苷34.53±2.27a45.9±0.93a6.39±0.45c5.45±1.44c17.67±0.34bND香叶木素4.43±2.21d4.94±0.26d23.38±0.22a14.23±0.16b7.23±0.09cND木犀草素7-β-芸香糖苷188.54±2.39a183.5±3.34a27.83±2.39c23.75±9.24cNDND非瑟酮5.51±0.25c8.47±0.25b6.15±0.18c24.96±0.25a3.31±2.3dND5-羟基-2′,6,6′-三甲氧基黄酮25.36±5.05b28.24±1.23a28.2±1.45a20.49±9.61c10.43±0.65dND桔皮素30.13±10.11a23.52±0.57b22.13±1.06b16.9±7.57cNDND芹菜素1.3±0.14c0.92±0.04c2.89±0.18b3.11±0.29b3.92±0.11aND其他类密叶辛木素83.47±1.66a50.02±0.88b32.12±1.01cd38.47±1.08cNDND东莨菪内酯4.74±0.8bc5.12±0.66b2.8±1.27c2.71±0.73c1.28±0.07d15.37±0.07a脱氢松香酸2.74±1.44d4.35±0.15c5.17±0.31a5.69±0.09a3.06±0.22dND异莨菪亭27.96±0.39a22.2±1.13b5.08±3.11c3.32±0.6d5.25±2.08cND升麻素苷1 611.13±7.23a1 629.29±0.33a1 115.87±7.71b1 030.04±7.2b28.23±0.06cND脂肪酸16-羟基十六烷酸4.62±0.11b4.59±0.53b3.65±0.5c4.11±0.2c6.15±1.00aND顺式-9,10-环氧硬脂酸31.14±14.84b50.27±3.6a24.94±17.1bc49.95±4.97a7.88±7.42cND肉豆蔻酸7.37±4.84d32.49±1.98c39.84±9.5c27.59±19.25c797.65±5.31a714.23±87.11b亚油酸24.4±18.18a22.24±18.38a14.57±7.96ab29.19±9.25a12.53±6.03bND糖类α,β-海藻糖1 405.68±33.73c1 546.14±22.12b1 501.07±20.08b1 776.32±202.41a531.06±7.89dNDα-D-葡萄糖264.85±62.78a260.95±37.33a210.88±7.48ab190.71±66.49b257.83±14.16aND氨基酸L-苯丙氨酸2 700.93±14.42a2 639.23±31.3a2 026.74±58.15b2 235.64±125.84b594.6±11.04c290.23±17.21d维生素吡哆醇1 914.49±23.01a2 284.35±5.15a41.27±15.41b37.17±14.53b3.85±2.21c1.32±0.07d有机酸癸二酸34.47±7.1a9.32±1.95b8.84±1.44b8.43±2.83b4.58±0.75cND
注:不同字母代表差异显著(P<0.05);“ND”表示该物质未检出。
表2列举了CE组提取物的组成,发现其富含多种酚类化合物、氨基酸、有机酸和脂肪酸,特别是表儿茶素(760.71 μg/g)、芦丁(403.44 μg/g)、槲皮素(229.66 μg/g)和山奈酚(104.32 μg/g)等,这些酚类前体物质已被证实存在于荔枝壳中[2]。值得注意的是,提取物中氨基酸和有机酸含量突出,表明乙醇对荔枝壳内源性活性成分的有效富集。
表3反映了在不同提取物中都检出的芦丁、柚皮素等6种成分中,MA中L-苯丙氨酸和吡哆醇的含量高于CE,东莨菪内酯、芦丁、柚皮素和肉豆蔻酸的含量低于CE。前者检出的20种酚类中,包括了木犀草素7-β-芸香糖苷、槲皮素3-O-芸香糖苷、山奈酚7-O-葡萄糖苷等5种糖苷类黄酮化合物,而CE法提取物仅有芦丁和柚皮素等2种共有成分,表明生物转化作用的发生。功能菌群发酵液可能在菌-酶的协同作用下部分降解荔枝壳的木质素,进而生成阿魏酸和对香豆酸[14],前者则可转化为酚酸等,且木质素降解有助于活性成分释放,所以显著提高MA中香叶木素、非瑟酮、柚皮素和槲皮素-3-鼠李糖苷等的含量。相反地,与B组相比,K组和T组中的芹菜素的含量降低,也包括K组中的香叶木素和柚皮素以及T组的槲皮素3-O-芸香苷、木犀草素7-β-芸香糖苷、山奈酚3-O-洋槐糖苷等多种活性成分的含量降低,表明菌群结构的多样性致使活性成分含量的不同变化。
MA和CE的活性组分含量差异如图2所示,CE组在提取酚酸、有机酸、脂肪酸等组分上占优势,而MA的特点是通过生物修饰作用,促进了前体化合物的利用,合成或转化出更丰富的黄酮类糖苷化合物、氨基酸、维生素、其他类等组分,这些新增的活性成分通常具有更好的抗炎、抗癌和抗菌等活性[1]。
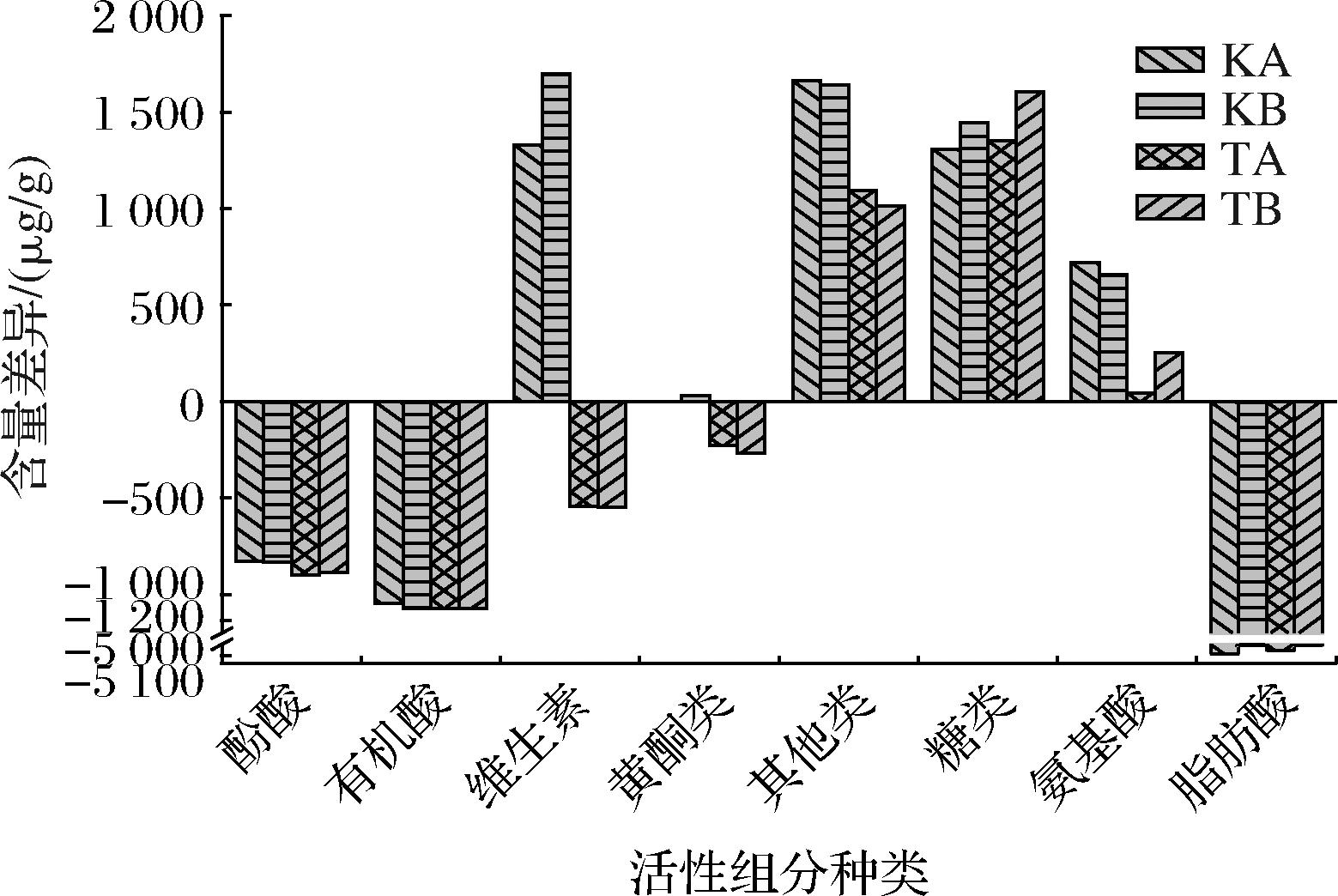
图2 菌群发酵液提取物中各类活性成分的含量差异
Fig.2 Content difference of components in microbiota extracts
注:K组和T组的测量值分别减去CE组的测量值。
2.4 富集微生物群落的差异分析
2.4.1 微生物多样性指数的差异
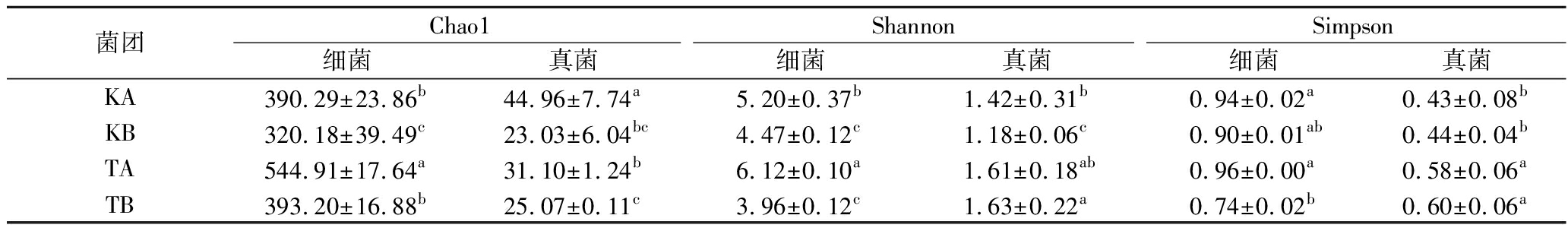
表4揭示了驯化代数增加,KB和TB细菌群落的Chao1、Shannon和Simpson指数降低,菌群内部的丰富度和多样性减少,但稀有物种的多样性增高。真菌群落的变化亦如此,可能与荔枝壳碳源的定向筛选作用有关。
表4 不同功能菌群的α多样性指数
Table 4 α-Diversity indices of different functional microbiota
菌团Chao1ShannonSimpson细菌真菌细菌真菌细菌真菌KA390.29±23.86b44.96±7.74a5.20±0.37b1.42±0.31b0.94±0.02a0.43±0.08bKB320.18±39.49c23.03±6.04bc4.47±0.12c1.18±0.06c0.90±0.01ab0.44±0.04bTA544.91±17.64a31.10±1.24b6.12±0.10a1.61±0.18ab0.96±0.00a0.58±0.06aTB393.20±16.88b25.07±0.11c3.96±0.12c1.63±0.22a0.74±0.02b0.60±0.06a
如图3-a所示,基于Bray-Curtis距离矩阵的PCoA结果表明,群落之间的细菌群落结构差异显著(P=0.001)。PCo1和PCo2分别解释了总变异的60.4%和23%,表明组间差异大于组内差异,菌群来源显著影响细菌群落组成。随着驯化代数增多,KA和KB的聚类紧密,而TA和TB较为分散,表明长期驯化驱动细菌群落形成稳定的核心菌群。相比之下,图3-b的真菌群落PCoA(P=0.17)则未呈现显著差异,表明其多样性随着驯化代数增加而降低。
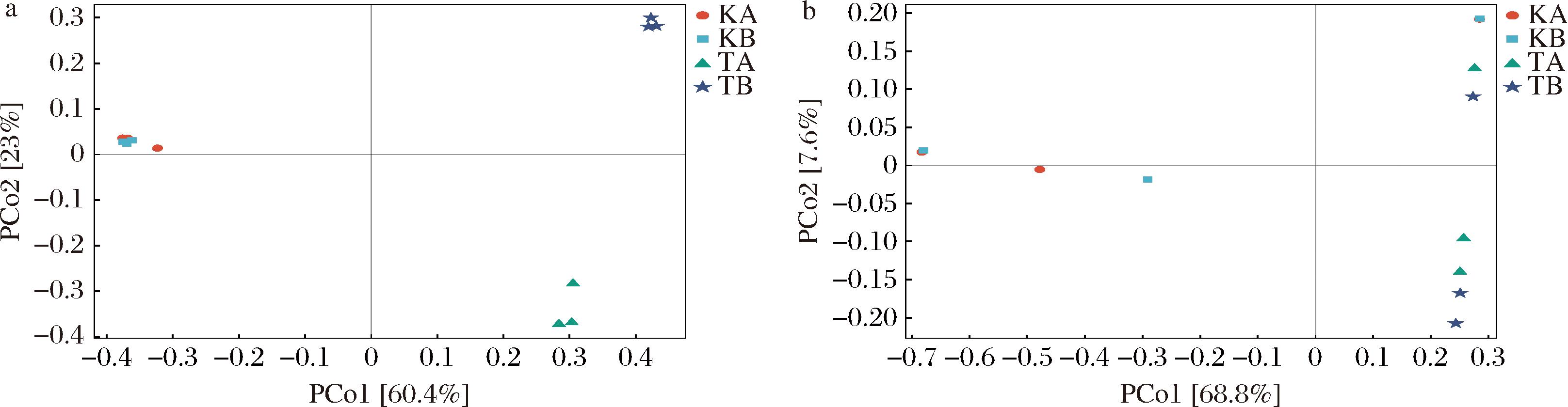
a-细菌;b-真菌
图3 功能菌群的细菌与真菌β多样性分析
Fig.3 Bacterial and fungi β diversity analysis of functional microbiota.
2.4.2 微生物群落结构的差异
如图4-a所示,K组和T组中优势细菌相对丰度(relative abundance,RA)≥1%的共有黄单胞菌目(Xanthomonadales)、黄杆菌目(Flavobacteriales)、几丁质降解菌目(Chitinophagales)等8个不同目。这些目水平细菌的RA在K组中为72.00%~82.10%,T组则是34.30%~57.19%。K组中优势细菌目芽单胞菌目(Gemmatimonadales),在KA和KB中的RA分别是6.94%和8.83%。而在T组中,Xanthomonadales占主导地位,在TA和TB中的RA分别是8.47%和50.43%。
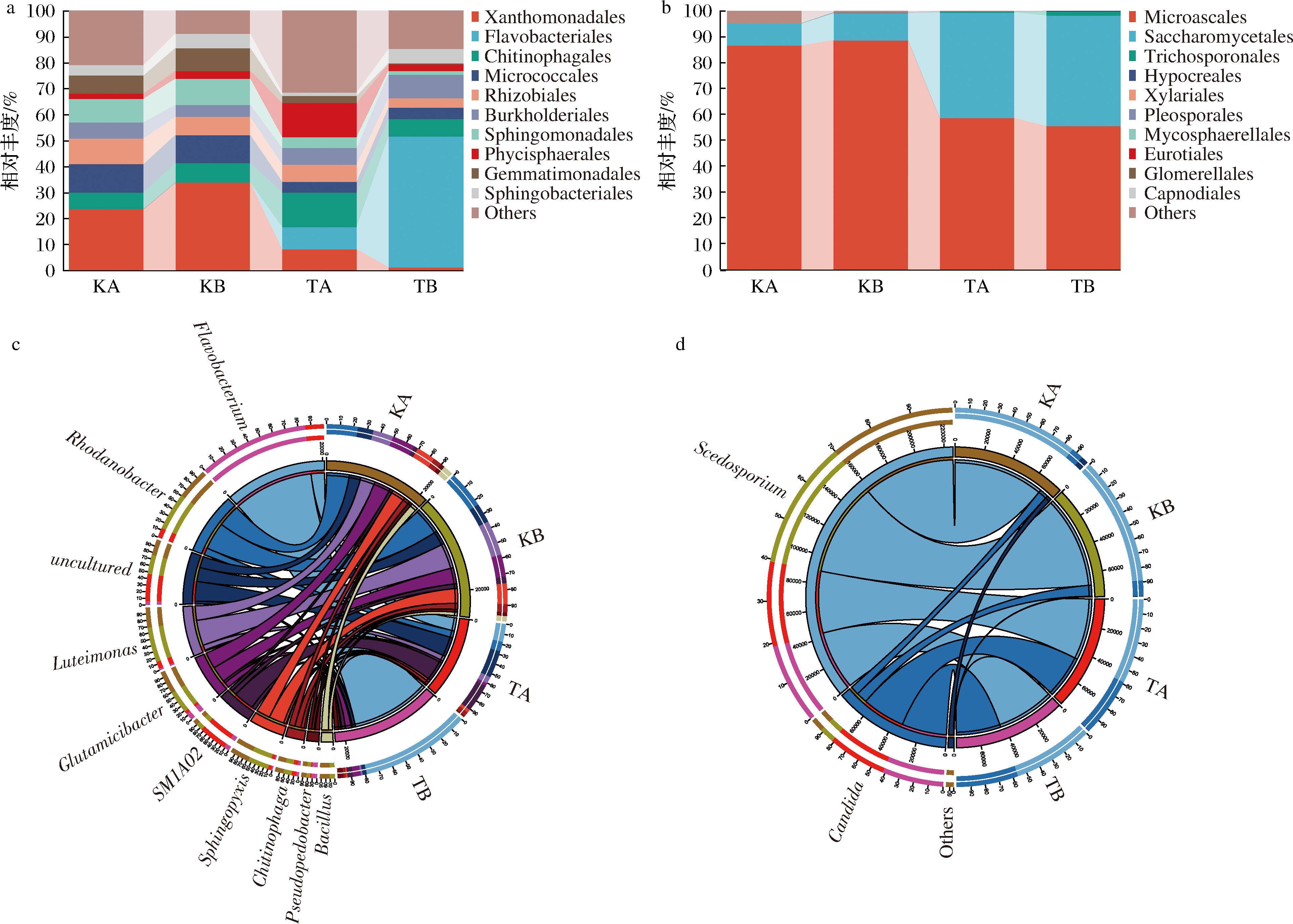
a、c-细菌;b、d-真菌
图4 功能菌群目水平堆叠图和属水平物种关系Circos图(前十)
Fig.4 Stacked bar charts of functional microbiota at the order level, and Circos charts of species relationship at the genus level (Top 10)
K组和T组中的优势菌属是谷氨酸杆菌属(Glutamicibacter)和噬几丁质菌属(Chitinophaga),其中在KA和KB中,优势属还包括鞘氨醇单胞菌属(Sphingopyxis)、红杆菌属(Rhodanobacter)、黄单胞菌属(Luteimonas)、假类杆菌属(Pseudopedobacter)和芽孢杆菌属(Bacillus)。但T组的A和B代中,黄杆菌属(Flavobacteriu)和潘多拉氏菌属(Pandoraea)都是优势细菌属。此外,TA中Rhodanobacter、Luteimonas和Sphingopyxis是优势细菌属,而在TB中Pseudopedobacter也是优势细菌(图4-c和图4-d)。这些细菌是土壤中的常见的,在有机物降解和碳氮循环中发挥关键作用[15]。Rhodanobacter、Pseudopedobacter和Sphingopyxis等产β-半乳糖苷酶、纤维素酶和木质素酶的能力强,在生物降解过程具有重要作用[16-17]。
K组和T组内的真菌群落中共鉴定到5个目,小囊菌目(Microascales)占绝对优势(图4-b)。赛多孢子菌属(Scedosporium)和念珠菌属(Candida)在2组中都是优势属(图4-b)。在TB组中的优势真菌目还有毛孢子菌目(Trichosporonales)。Scedosporium的RA在KA和KB中分别是86.58%和88.22%。真菌群落可能参与了各种生物降解过程,例如Scedosporium sp.能够裂解木质素的中的β-醚键[18]。
2.5 主要微生物属与活性组分之间的差异相关性分析
优势属与活性成分之间的Spearman分析结果如图5所示。在K组和TA组中,红杆菌属(Rhodanobacter)、谷氨酸杆菌属(Glutamicibacter)、黄单胞菌属(Luteimonas)和鞘氨醇单胞菌属(Sphingopyxis)是共有细菌属,其与多种活性成分(酚酸、维生素、大多数黄酮类、其他类和氨基酸)显示出显著的正相关。在K组中,芽孢杆菌属(Bacillus)与多种活性呈正相关。在T组中,黄杆菌属(Flavobacteriu)仅与香叶木素、脱氢松香酸和3,4-二羟基苯甲醛等特定活性成分呈正相关,而潘多拉氏菌属(Pandoraea)却与L-苯丙氨酸等6种成分呈负相关。这些相关性揭示其微生物降解荔枝壳的能力。例如,Rhodanobacter sp.具有降解纤维素和芳香族化合物的能力[19],Flavobacterium sp.利用果胶作为碳源,增强其碳代谢[20],Bacillus产酶能力强,与各种活性成分显著正相关,强调了增强活性组分提取效果的重要作用[21]。然而,Rhodanobacter等能降解有机污染物(如苯酚),多酚结构与苯酚类似。这些微生物可能参与了酚类物质的降解,所以部分微生物属与活性组分间呈负相关性。
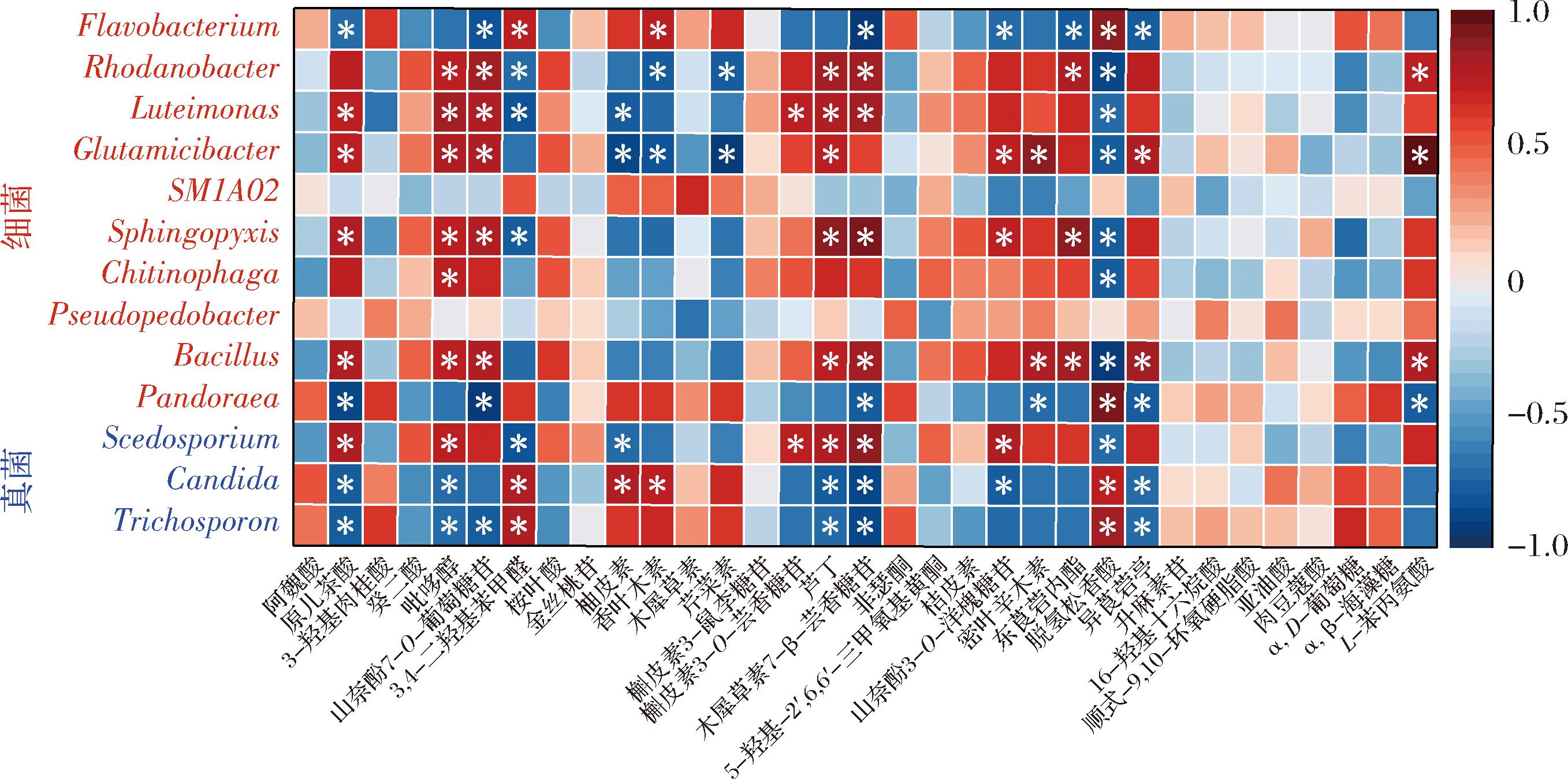
图5 功能菌群与活性成分间的相关性分析
Fig.5 Correlation analysis between functional microbiota and active components
注:“*”表示显著相关性(|ρ|>0.7,P<0.01)。
真菌方面,赛多孢子菌属(Scedosporium)能降解纤维素,与多种活性成分呈正相关[22]。念珠菌属(Candida)和毛孢子菌目(Trichosporonales)虽能降解纤维素和木质素,因多酚类会抑制部分真菌生长与代谢,所以K组中Candida的RA较低,且与活性成分呈负相关[23]。
2.6 综合分析活性组分的代谢途径
利用KEGG(代谢通路)和PlantCyc(植物代谢物途径)注释了33种活性成分,结果显示这些成分主要富集于苯丙氨酸代谢、糖酵解(embden-meyerhof-parnass, EMP)途径、碳水化合物代谢和黄酮类生物合成等关键途径。使用PICRUSt2预测微生物群落编码的酶丰度,结果如图6所示[24]。
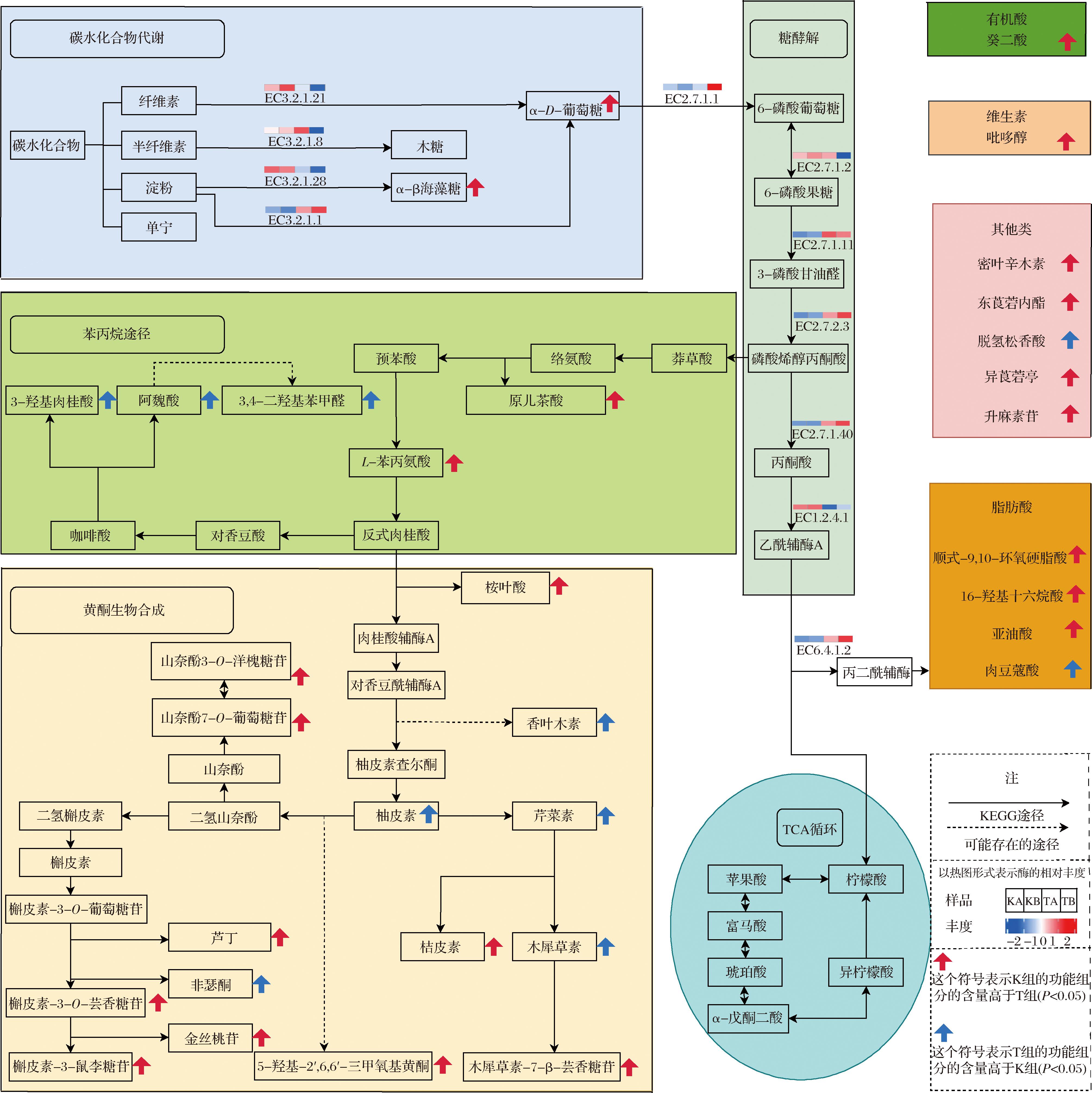
图6 不同功能菌群的酶丰度与活性成分的代谢途径注释相关图
Fig.6 Different functional microbiota’ enzyme abundance correlated with annotated metabolic pathways of active components
在K组和T组之间,碳水化合物代谢途径存在显著差异。K组中参与碳水化合物降解的多数酶的RA较高,表明其具有较好的碳水化合物降解能力。相反,T组中参与EMP途径的酶的RA较高,暗示其功能菌群可能更有效利用葡萄糖。在EMP途径中,葡萄糖先转化为磷酸烯醇丙酮酸,然后转化为莽草酸。后者是合成苯丙氨酸的前体。苯丙氨酸随后可转化为阿魏酸和对香豆酸等。苯丙氨酸的代谢产物也是黄酮类化合物的关键组成部分。PICRUSt2预测到仅K组中含有吡哆醇代谢酶,使吡哆醇的提取量最高达到2.28 mg/g,显著提高了L-苯丙氨酸的合成速率,含量提高到2.70 mg/g。
不同提取物间的差异也可能是因功能菌群增强各种生物修饰过程,如氧化、糖基化、甲基化、羟基化、酰化和聚合作用。这些过程不仅增加组分的多样性,还增强了其稳定性和生物活性[25]。例如,柚皮素的氧化产生木犀草素,随后可能通过葡萄糖基转移酶和鼠李糖基修饰酶形成木犀草素7-β-芸香糖苷,使K组中的该物质含量达到188.54 μg/g,显著高于后者的27.83 μg/g。芦丁也易受到β-葡萄糖苷酶的作用水解为槲皮素和芦丁苷,所以其芦丁含量均低于CE组。此外,槲皮素和山奈酚可能通过甲基转移酶和糖基转移酶转化为槲皮素3-O-半乳糖苷,山奈酚7-O-葡萄糖苷等化合物,而在CE组中未检出这些成分,佐证了生物转化的有效性。
3 结论
本文从TP含量、活性组分种类与含量、群落结构和代谢途径等多方面揭示了持续定向驯化的功能菌群发酵液提取荔枝壳活性组分的特点,主要是对黄酮类糖苷化合物的生物转化作用。与乙醇溶剂提取法相比,微生物发酵液提取法显著提高了黄酮类活性组分的多样性。Rhodanobacter等产β-半乳糖苷酶、纤维素酶和木质素酶的优势细菌属的作用突出。PICRUSt2对甲基转移酶、糖基转移酶等生物修饰酶的功能预测结果佐证了其推测。而乙醇提取则对荔枝壳TP具有较好的富集效果。研究结果为荔枝壳活性组分的开发利用提供了科学依据,后续可对菌群发酵液提取物中活性组分的生物功能以及荔枝壳的微观形态特征进行深入探讨。
[1] ZHAO L, WANG K, WANG K, et al.Nutrient components, health benefits, and safety of litchi (Litchi chinensis Sonn.):A review[J].Comprehensive Reviews in Food Science and Food Safety, 2020, 19(4):2139-2163.
[2] 蒋侬辉, 朱慧莉, 刘伟, 等.基于广泛代谢组学的荔枝果肉营养代谢物综合解析[J].食品科学, 2022, 43(16):269-278.
JIANG N H, ZHU H L, LIU W, et al.Widely targeted metabolomics analysis of the nutritional profile of litchi pulp[J].Food Science, 2022, 43(16):269-278.
[3] ACOSTA-ESTRADA B A, GUTIÉRREZ-URIBE J A, SERNA-SALD VAR S O.Bound phenolics in foods, a review[J].Food Chemistry, 2014, 152:46-55.
VAR S O.Bound phenolics in foods, a review[J].Food Chemistry, 2014, 152:46-55.
[4] 董科, 冷云, 何方婷, 等.植物多酚及其提取方法的研究进展[J].食品工业科技, 2019, 40(2):326-330.
DONG K, LENG Y, HE F T, et al.Research progress of polyphenol and extraction methods in plants[J].Science and Technology of Food Industry, 2019, 40(2):326-330.
[5] LIN S, HE J R, JIANG Y M, et al.Production of nigragillin and dihydrophaseic acid by biotransformation of litchi pericarp with Aspergillus awamori and their antioxidant activities[J].Journal of Functional Foods, 2014, 7:278-286.
[6] VERMA N, KUMAR V, BANSAL M C.Utility of Luffa cylindrica and Litchi chinensis peel, an agricultural waste biomass in cellulase production by Trichoderma reesei under solid state cultivation[J].Biocatalysis and Agricultural Biotechnology, 2018, 16:483-492.
[7] WRIGHT R J, GIBSON M I, CHRISTIE-OLEZA J A.Understanding microbial community dynamics to improve optimal microbiome selection[J].Microbiome, 2019, 7(1):85.
[8] ZHANG Y Z, HUANG J, ZHOU R Q, et al.An integrative metabolomics and metagenomics analysis of functional microbiota examines the extraction of bioactive products using Longan pericarp[J].Biochemical Engineering Journal, 2024, 211:109464.
[9] LI C R, HOU X H, XU Y Y, et al.Manual annotation combined with untargeted metabolomics for chemical characterization and discrimination of two major Crataegus species based on liquid chromatography quadrupole time-of-flight mass spectrometry[J].Journal of Chromatography.A, 2020, 1612:460628.
[10] MU Y, HUANG J, ZHOU R Q, et al.Comprehensive analysis for the bioturbation effect of space mutation and biofortification on strong-flavor Daqu by high-throughput sequencing, volatile analysis and metabolomics[J].Food Chemistry, 2023, 403:134440.
[11] ZHANG L, ZHOU R, NIU M, et al.Difference of microbial community stressed in artificial pit muds for Luzhou-flavour liquor brewing revealed by multiphase culture-independent technology[J].Journal of Applied Microbiology, 2015, 119(5):1345-1356.
[12] PRASAD N K, YANG B, ZHAO M M, et al.Effects of high-pressure treatment on the extraction yield, phenolic content and antioxidant activity of litchi (Litchi chinensis Sonn.) fruit pericarp[J].International Journal of Food Science and Technology, 2009, 44(5):960-966.
[13] 朱永聪, 崔子霄, 徐晗, 等.优新荔枝品种果实品质风味特征比较[J].中国食品学报, 2023, 23(6):327-338.
ZHU Y C, CUI Z X, XU H, et al.Comparison on fruit quality and flavor of new and fine litchi cultivars[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(6):327-338.
[14] MASAI E J, KATAYAMA Y, FUKUDA M.Genetic and biochemical investigations on bacterial catabolic pathways for lignin-derived aromatic compounds[J].Bioscience, Biotechnology, and Biochemistry, 2007, 71(1):1-15.
[15] KUYPERS M M M, MARCHANT H K, KARTAL B.The microbial nitrogen-cycling network[J].Nature Reviews Microbiology, 2018, 16(5):263-276.
[16] FEDERICI E, PEPI M, ESPOSITO A, et al.Two-phase olive mill waste composting:Community dynamics and functional role of the resident microbiota[J].Bioresource Technology, 2011, 102(23):10965-10972.
[17] SHARMA K, ANTUNES I L, RAJULAPATI V, et al.Molecular characterization of a first endo-acting β-1, 4-xylanase of family 10 glycoside hydrolase (PsGH10A) from Pseudopedobacter saltans comb.nov[J].Process Biochemistry, 2018, 70:79-89.
[18] OATES N C, ABOOD A, SCHIRMACHER A M, et al.A multi-omics approach to lignocellulolytic enzyme discovery reveals a new ligninase activity from Parascedosporium putredinis NO1[J].Proceedings of the National Academy of Sciences of the United States of America, 2021, 118(18):e2008888118.
[19] LIN P, YAN Z F, LI C T.Luteimonas cellulosilyticus sp.nov., cellulose-degrading bacterium isolated from soil in Changguangxi national wetland park, China[J].Current Microbiology, 2020, 77(7):1341-1347.
[20] KRAUT-COHEN J, SHAPIRO O H, DROR B, et al.Pectin induced colony expansion of soil-derived Flavobacterium strains[J].Frontiers in Microbiology, 2021, 12:651891.
[21] DADWAL A, SHARMA S, SATYANARAYANA T.Thermostable cellulose saccharifying microbial enzymes:Characteristics, recent advances and biotechnological applications[J].International Journal of Biological Macromolecules, 2021, 188:226-244.
[22] HAN Y Q, HUANG X D, WANG Y, et al.Fungal community and biodeterioration analysis of hull wood and its storage environment of the Nanhai No.1 shipwreck[J].Frontiers in Microbiology, 2021, 11:609475.
[23] SITHEEQUE M M, PANAGODA G J, YAU J, et al.Antifungal activity of black tea polyphenols (catechins and theaflavins) against Candida species[J].Chemotherapy, 2009, 55(3):189-196.
[24] 杨晓. 甘氨酸促进叶用莴苣(Lactuca sativa L.)酚类化合物积累的代谢组学分析[D].上海:上海交通大学, 2019.
YANG X.Metabolomics analysis reveals exogenous glycine promoting phenolic compounds accumulation in lettuce (Lactuca sativa L.)[D].Shanghai:Shanghai Jiao Tong University, 2019.
[25] WANG C, TANG D, XU W, et al.Glycosylation of the polyphenols from Resina draconis by glycosyltransferase YjiC1[J].Natural Product Research, 2023, 37(19):3245-3252.