荧光假单胞菌是鱼类主要特征腐败菌之一,可以导致挥发性盐基氮(total volatile basic nitrogen,TVBN)、尸胺和腐胺等腐败产物的积累,以及肌肉蛋白质和氨基酸的降解[1]。为了延长生鲜鱼的保鲜期,通常采用化学防腐剂以及低温贮存等措施。由于化学防腐剂可能对人体健康造成多种危害[2],植物来源的天然防腐物质用于鱼类及其产品保鲜备受关注。研究表明,许多天然香辛料如牛至、百里香、罗勒、香薄荷及其精油对荧光假单胞菌有较强的抑制效果,而百里香酚(2-异丙基-5-甲基苯酚)是这些香辛料及其精油中主要的抑菌成分,具有良好的抗菌活性[3-4],被欧盟和美国食品药品监督管理局认定为安全食品添加剂,应用于牛肉、鸡肉以及肉类腌制品等的保鲜[5]。然而,百里香酚在水产保鲜方面的报道较少,OZOGUL等[6]在鳕鱼片的保鲜实验中使用了百里香酚,使鱼片的保质期从对照组的8 d延长到了15 d。
目前,诸多研究发现百里香酚对禾谷镰刀菌、大肠杆菌、蜡样芽孢杆菌和铜绿假单胞菌等细菌具有抑制作用,其抑菌机制主要有破坏细菌的细胞膜,导致电解质泄漏和能量代谢不平衡[7],增加细胞质膜的通透性和去极化[8],诱导活性氧(reactive oxygen species, ROS)的积累[9],对DNA造成不可逆的损伤[10]等方面。但百里香酚对鱼类的主要特征腐败菌如荧光假单胞菌的抑制活性及其机制尚未明确。
因此,本研究以水产品主要腐败菌荧光假单胞菌为对象,探讨百里香酚对其的抑菌活性及作用机制。通过测定最低抑菌浓度(minimum inhibitory comcentration,MIC)与生长曲线评价其抑菌效果;进一步从细胞膜与DNA两个层面探究其作用机理,包括膜电位与ROS水平、蛋白质与K+泄漏情况,以及DNA含量变化,并结合扫描电子显微镜观察细胞形态,系统分析百里香酚的抑菌机制。
1 材料与方法
1.1 材料与试剂
荧光假单胞菌(Pseudomonas fluorescens) GDMCC1.776,广州微生物菌种保藏中心。
百里香酚(分析纯),广州日化化工有限公司;LB肉汤、LB琼脂,广东省环凯微生物科技有限公司;考马斯亮蓝G250和R250、次甲基蓝等(分析纯),上海阿拉丁试剂有限公司;钾(K)测试盒,南京建成生物工程研究所;PBS(0.01 mol/L,pH=7.4),白鲨生物科技有限公司;3,3′-二丙基硫杂二羰花青、碘化物[DiSC3(5)],MCE公司(美国);2′,7′-二氯二氢荧光素二乙酸酯(2′,7′-dichlorofluorescin diacetate,DCFH2-DA)、SDS-PAGE制备试剂盒、彩虹245 plus广谱蛋白marker、4′,6-二脒基-2-苯基吲哚(4′,6-diamidino-2-phenylindole,DAPI)、碘化吡啶(propidium iodide,PI),北京索莱宝科技有限公司;SDS-PAGE蛋白上样缓冲液(5X),碧云天生物技术有限公司。
1.2 仪器与设备
LRH-150生化培养箱,上海一恒科学仪器有限公司;MGC200PRO全自动微生物生长曲线分析仪,宁波新芝生物科技股份有限公司;SuPerMax 3100多功能酶标仪,上海闪谱生物科技有限公司;Olympus IX71荧光倒置显微镜,Olympus公司(日本);MIRA4 LMH扫描电子显微镜,TESCAN公司(捷克);WD-9413B凝胶成像系统,北京六一生物技术有限公司。
1.3 实验方法
1.3.1 菌种活化
将100 μL P.fluorescens的甘油保存液加到100 mL LB肉汤中,28 ℃摇床振荡培养18 h。用接种环蘸取少量溶液在LB固体培养基上划线后,将培养基放置在28 ℃的恒温培养箱中培养24 h。
1.3.2 MIC和最低杀菌质量浓度(minimum bactericidal concentration,MBC)测定
通过二倍稀释法来测定MIC和MBC[11]。将百里香酚(溶于丙二醇)和菌液添加到LB肉汤中,百里香酚质量浓度为62.5~2 000 mg/L,使菌液中P.fluorescens的数量为107 CFU/mL(OD600nm值=0.15)。将菌悬液28 ℃摇匀24 h,以无菌种生长的最低药物质量浓度为MIC。
100 μL 1 MIC试验溶液取于澄清管中,置于培养皿中,倒入营养琼脂,摇匀,28 ℃培养24 h。平板上菌落总数≤30的最低药物质量浓度为MBC。
1.3.3 检测用菌悬液配制
按照1.3.2节的方法配制百里香酚质量浓度为0、125、250 mg/L的菌悬液(107 CFU/mL)。
1.3.4 生长曲线测定
根据FEI等[12]的方法绘制生长曲线,将100 μL菌悬液加入96孔板,在自动生长曲线分析仪中28 ℃培养24 h。每隔1 h记录菌液在600 nm处的吸光值。
1.3.5 膜电位测定
参考WENG等[9]的方法,200 μL不含百里香酚菌悬液加入黑色不透明96孔板,每孔加2 μL 100 mmol/L DiSC3(5)荧光探针,28 ℃培养30 min。加入百里香酚调节质量浓度分别为0、125、250 mg/L,28 ℃下培养30 min。使用酶标仪(28 ℃)测定激发波长622 nm和发射波长670 nm下荧光强度。
1.3.6 菌液K+离子泄漏的测定
采用1.3.3节配制的菌悬液,根据说明书使用钾试剂盒测定钾离子水平。
1.3.7 菌液蛋白质含量测定
采用考马斯亮蓝法[13]测定菌液蛋白质含量。1.3.3节配制的菌悬液,在15、30、60、90、120 min取1 mL菌液4 000 r/min离心5 min,加入G-250,反应2 min。测定595 nm处的吸光度,用牛血清白蛋白标准曲线计算蛋白质质量浓度。
1.3.8 胞内蛋白含量测定
参考CHANG等[14]的方法测定。1.3.3节配制的菌悬液28 ℃下培养1、2、3、6、9、12 h。以8 000 r/min离心10 min后,沉淀用PBS洗涤3次,无菌生理盐水重悬。10 μL的样品中加入4倍体积的上样缓冲液,95 ℃水浴10 min。取10 μL样品上样于5%(体积分数)堆积凝胶和15%(体积分数)分离凝胶,以110 V电泳30 min后,升至150 V电泳2 h。考马斯亮蓝R-250染色,用10%(体积分数)乙酸、20%(体积分数)甲醇的溶液脱色,用凝胶成像仪进行观察。
1.3.9 活性氧测定
参考WENG等[9]、MAJEED等[15]的方法,将DCFH2-DA与不含百里香酚的菌悬液按1∶1 000(体积比)混合,28 ℃下培养30 min,4 000 r/min离心取沉淀,用PBS洗涤2次并重悬。加入百里香酚溶液,培养8 min后,使用酶标仪(28 ℃)测定激发波长488 nm和发射波长525 nm下荧光强度。
1.3.10 DAPI和PI染色实验
参考CHANG等[14]的方法,1.3.3节配制的菌悬液在28 ℃下培养3 h,4 000 r/min离心10 min,沉淀用PBS洗涤2次并重悬。
DNA含量测定:1 mL菌悬液加入5 μg DAPI,28 ℃黑暗环境培养30 min。荧光倒置显微镜激发波长364 nm和发射波长454 nm下进行观察。
细胞膜完整性测试:1 mL菌悬液加入2 μg PI,28 ℃ 黑暗环境培养30 min。荧光倒置显微镜激发波长536 nm和发射波长617 nm下(536/617 nm)进行观察。
1.3.11 扫描电镜观察
参考ZHANG等[16]的方法,1.3.3节配制的菌悬液在28 ℃下培养3 h,4 000 r/min离心10 min,用PBS洗涤沉淀3次,用5%(体积分数)戊二醛在4 ℃固定12 h,4 000 r/min离心,PBS洗涤沉淀3次,依次使用30%、50%、70%、90%、100%(体积分数)乙醇梯度脱水15 min后,冷冻干燥,喷金,在扫描电镜下观察。
2 结果与分析
2.1 百里香酚对P.fluorescens的抑制作用
当百里香酚质量浓度低于125 mg/L时,经过24 h培养,培养液出现浑浊;当质量浓度高于125 mg/L时,培养液未出现浑浊;当质量浓度高于1 500 mg/L时,营养琼脂上的菌落数少于30个。由此确定百里香酚对P.fluorescens的MIC和MBC分别为125、1 500 mg/L。
2.2 百里香酚对生长曲线的影响
如图1所示,百里香酚处理抑制了P.fluorescens的生长,抗菌活性随着百里香酚质量浓度增加而增强。与对照组相比,当质量浓度为0.5 MIC时,可抑制P.fluorescens的生长,对数生长期消失。当百里香酚质量浓度超过1 MIC时,P.fluorescens的生长几乎完全停止。
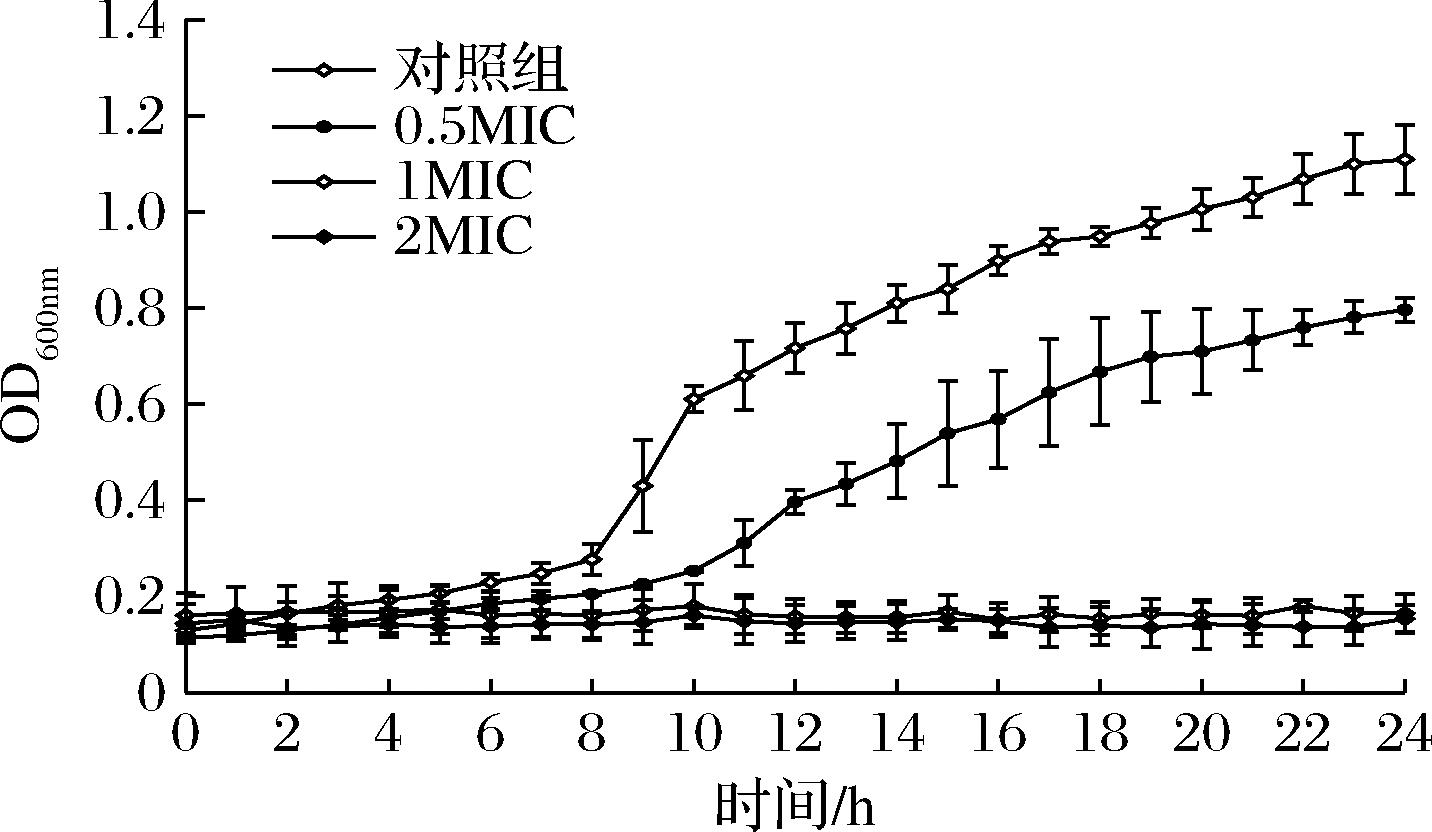
图1 不同百里香酚浓度下P.fluorescens的生长曲线
Fig.1 Growth curve of P.fluorescens treated with thymol
2.3 百里香酚对细胞膜电位的影响
对于正常细胞来说,膜电位的稳定维持是细胞膜结构完整性的关键指标[17]。百里香酚处理对P.fluorescens膜电位的影响如图2所示,对照组的荧光强度为9.845×102,1 MIC组和2 MIC组的荧光强度分别为5.904×102和1.927×102,均显著低于对照组(P<0.05),分别降低了40%和80%。结果表明,百里香酚能够有效破坏细胞膜的电位平衡,去极化现象随质量浓度的增高而更加明显。这一结果可能与百里香酚对细胞膜通透性的影响有关。膜电位的去极化通常意味着细胞膜表面电荷的紊乱,细胞膜的完整性和选择性通透性遭到破坏,从而导致内外离子的交换失控,细胞膜功能受损[14]。TIAN等[18]也观察到百里香酚对其他细菌细胞膜的去极化作用。因此,百里香酚对P.fluorescens膜电位的去极化效应,表明其可能通过改变膜的通透性,打破内外离子平衡,最终导致细胞膜功能的损害。
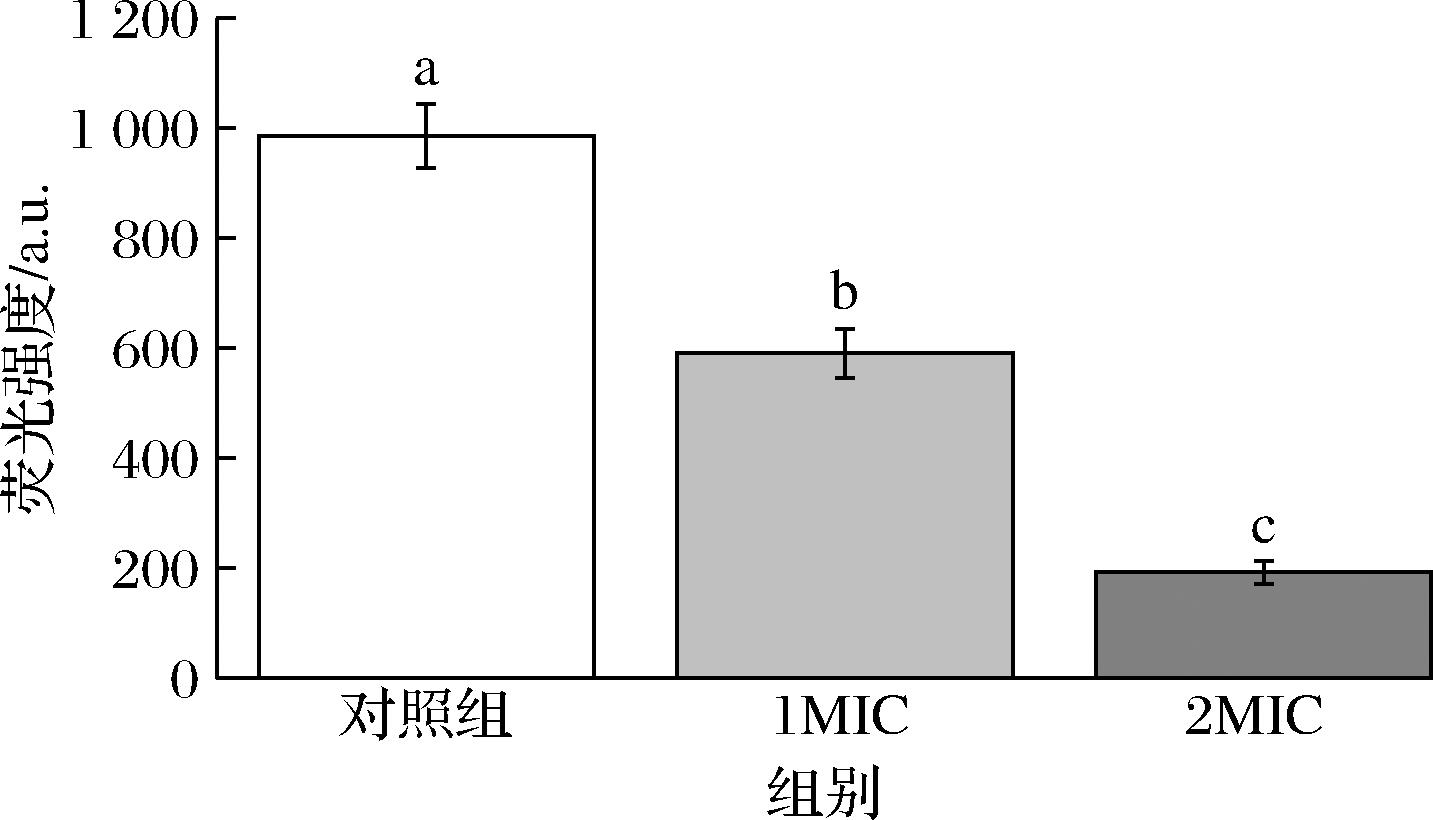
图2 百里香酚处理后P.fluorescens细胞膜电位变化
Fig.2 Changes in the membrane potential of P.fluorescens treated with thymol
注:图中不同字母表示差异显著(P<0.05)(下同)。
2.4 百里香酚对K+、可溶性蛋白泄漏量的影响
去极化导致细胞膜受损,通透性增加,细胞内离子泄漏,严重时,细胞内的大分子物质也会渗漏[18]。如图3所示,随着处理时间的延长,所有样品K+外泄量均有所增加。对照组的K+摩尔浓度在30 min后趋于平稳,在120 min达到0.014 5 mmol/L。相比之下,百里香酚处理组的K+摩尔浓度随百里香酚质量浓度增高而显著上升(P<0.05),1 MIC和2 MIC组在120 min时K+摩尔浓度分别为0.029 7、0.041 7 mmol/L,显著高于对照组(P<0.05)。YAMMINE等[19]的研究表明,百里香酚能破坏肠炎沙门氏菌的细胞膜,引起K+的大量泄漏。在125 mg/L百里香酚下,细胞外K+摩尔浓度随时间增加,在1 h后达到0.051 mmol/L。
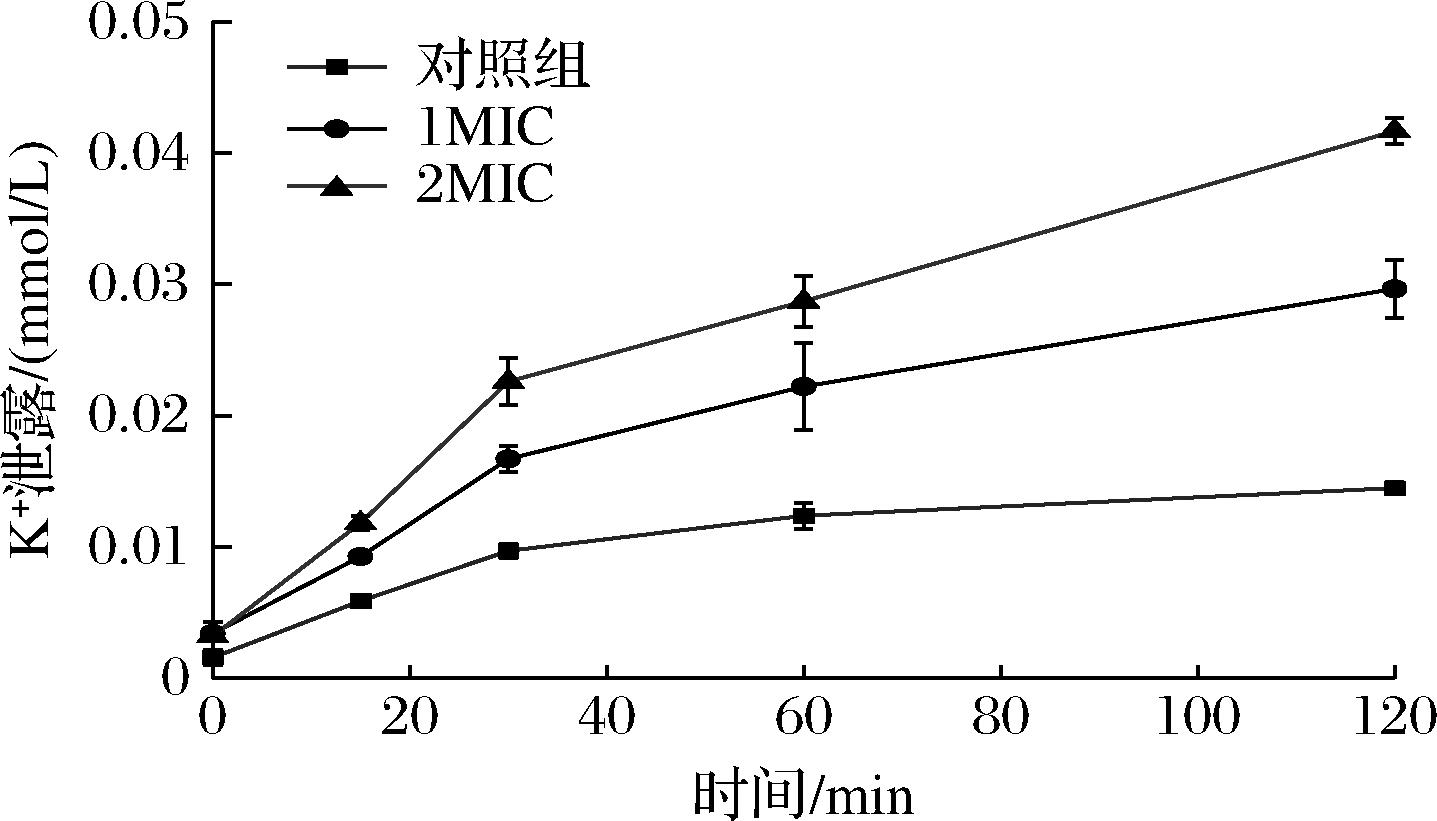
图3 百里香酚处理后P.fluorescens菌液K+浓度变化
Fig.3 Changes in the leakage of K+ of P.fluorescens treated with thymol in bacterial suspension
如图4所示,对照组的蛋白质质量浓度在实验过程中无显著变化(P>0.05),而样品组渗漏量随着百里香酚质量浓度和处理时间的增加而上升。1 MIC和2 MIC组在20 min内迅速增加,30 min后增幅趋缓,在120 min分别达到8.676、17.044 μg/mL,显著高于对照组(P<0.05)。结果表明,百里香酚通过破坏细胞膜的功能和结构,增加膜的通透性,促使细胞内K+和蛋白质的泄漏,最终导致细菌死亡。
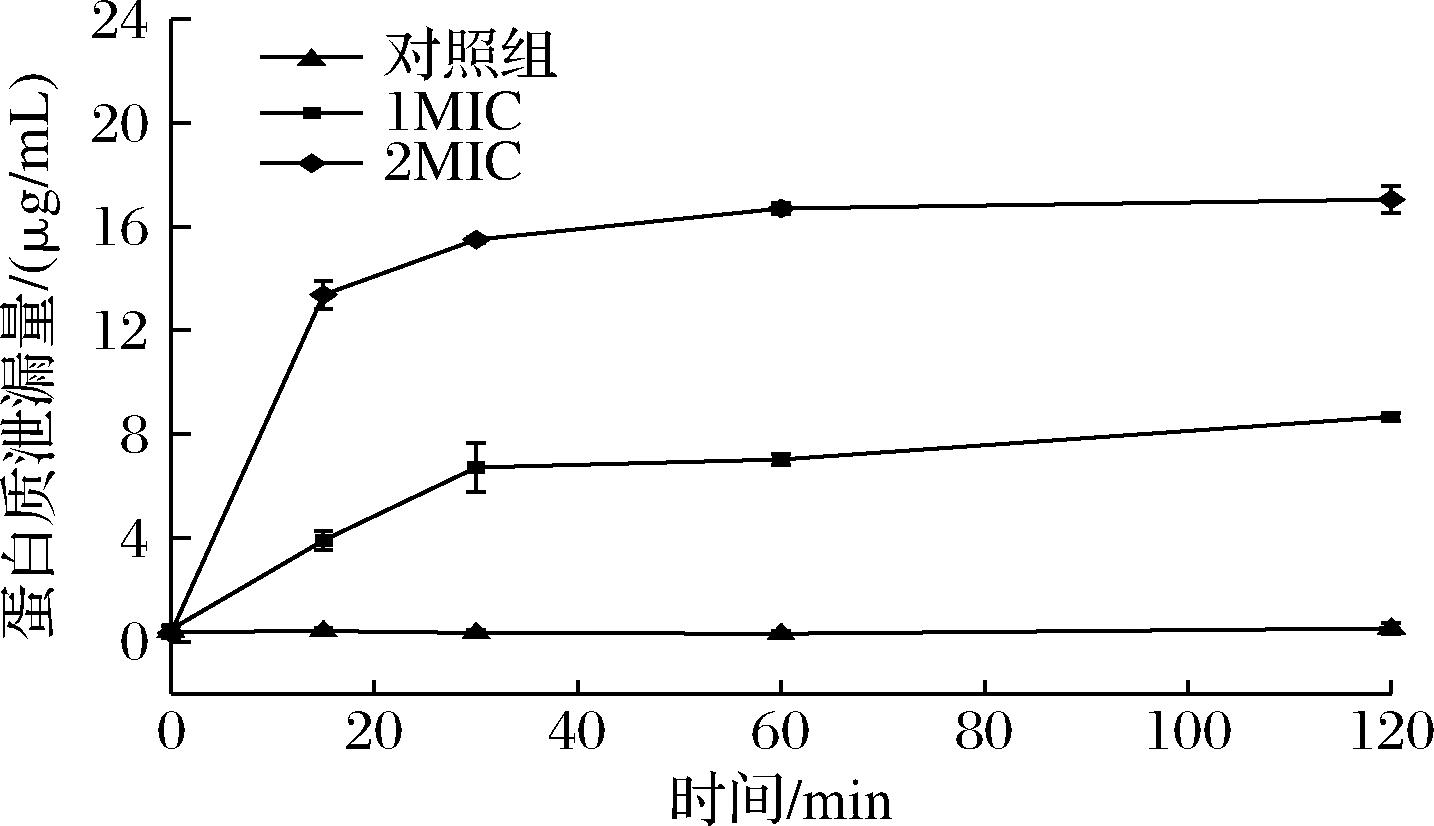
图4 百里香酚处理后P.fluorescens菌液可溶性蛋白质量浓度变化
Fig.4 Changes of soluble protein concentration of P.fluorescens treated with thymol in bacterial suspension
2.5 百里香酚对胞内蛋白含量的影响
蛋白质含量变化是揭示抗菌机制的重要途径之一,细菌胞内蛋白质的减少与膜通透性增加以及蛋白质合成的抑制有关[20]。如图5所示,泳道颜色深度与蛋白质含量呈正相关。随着百里香酚质量浓度和处理时间的增加,1 MIC和2 MIC组蛋白质含量均低于对照组。结合2.3节和2.4节的实验结果,推测百里香酚处理后细胞膜通透性增加导致胞内蛋白质泄漏至胞外,细胞内的蛋白质含量降低。同时,0.5 MIC组在处理3 h后63 000 Da以下的蛋白质含量高于对照组、1 MIC和2 MIC组,可能是由于百里香酚质量浓度低,虽然能够抑制P.fluorescens的生长,但其可以通过合成小分子蛋白质以抵抗百里香酚的作用。KANG等[21]在研究0.5 MIC柠檬醛对小肠结肠炎耶尔森菌的抑制时发现,35 000~60 000 Da的蛋白质水平升高,其原因是小肠结肠炎耶尔森菌产生应激蛋白质增强了对柠檬醛的抵抗力。
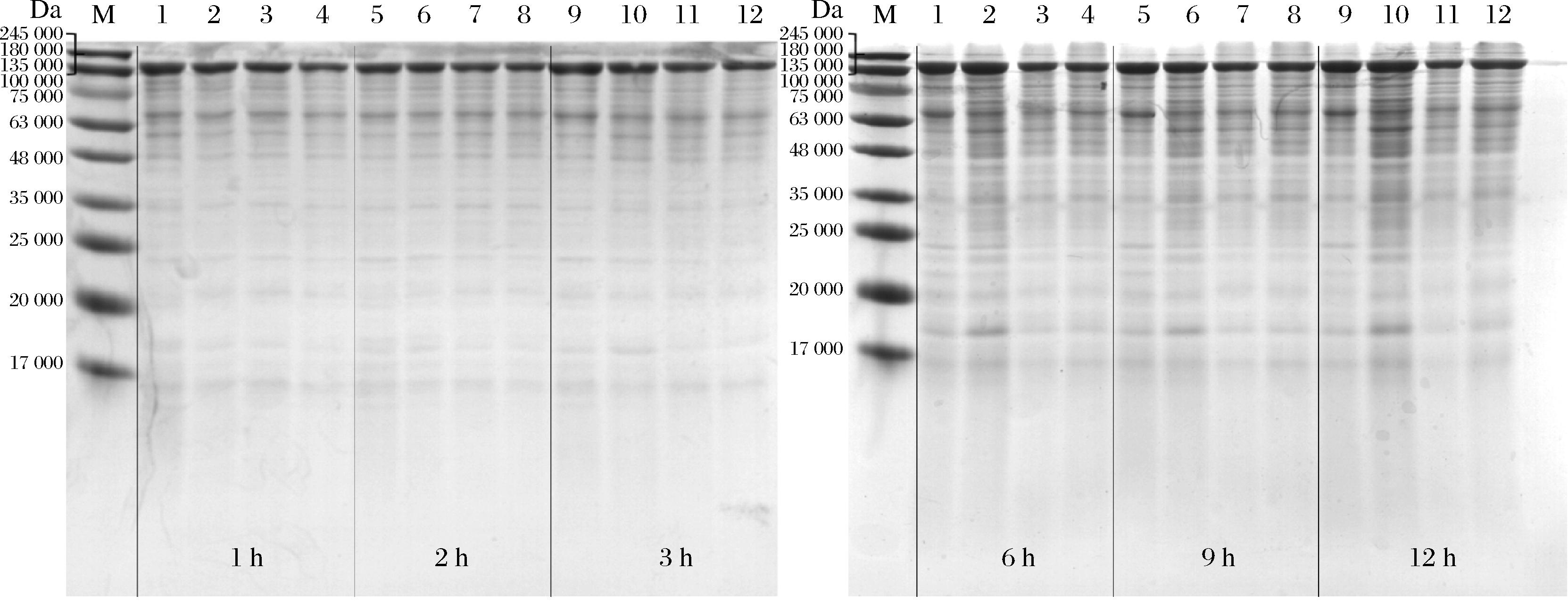
Marker:泳道M;对照组:泳道1、5、9;0.5 MIC:泳道2、6、10;1 MIC:泳道3、7、11;2MIC:泳道4、8和12。
图5 百里香酚处理的P.fluorescens中蛋白质的SDS-PAGE图像
Fig.5 SDS-PAGE images of P.fluorescens treated with thymol
2.6 百里香酚对细胞ROS含量的影响
ROS的积累是细胞凋亡的关键指标之一,能直接损伤大分子,破坏细胞膜及呼吸过程中的电子传递链,导致细胞死亡[17]。细胞ROS含量与DCFH-DA荧光强度成正比,如图6所示,1 MIC和2 MIC组的荧光强度相对于对照组的3.526×103分别显著上升至4.155×103和4.963×103(P<0.05),表明细胞内部ROS水平显著升高(P<0.05)。LIU等[10]的研究发现62.5、125 mg/L的百里香酚质量浓度处理铜绿假单胞菌时,ROS水平从对照组的3.8×104上升至4.8×104和5.4×104,也证明了百里香酚能够诱导ROS的积累,进一步对脂质和细胞膜造成氧化损伤,影响细胞膜的正常功能,最终导致细胞膜破裂[22]。
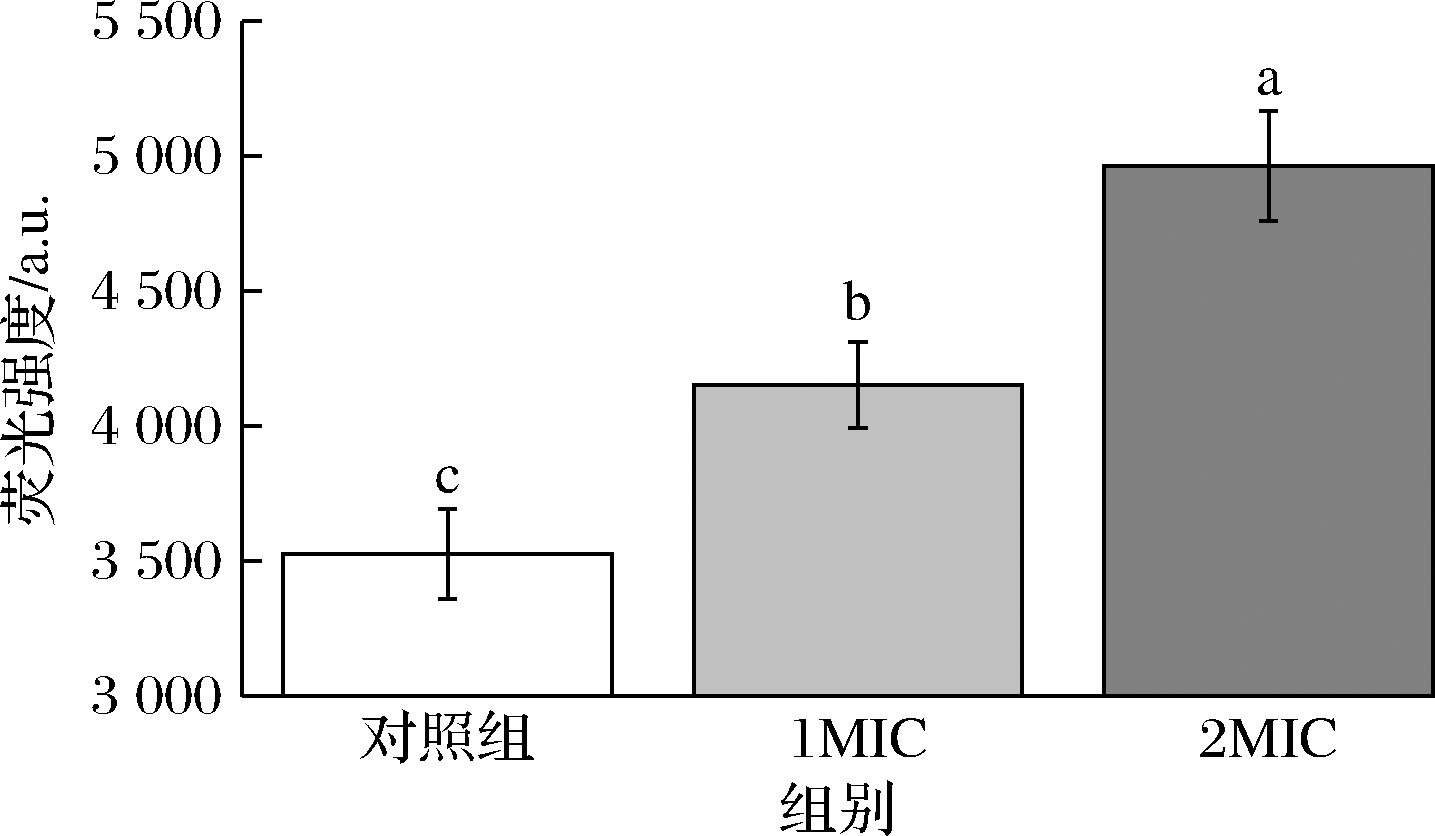
图6 百里香酚处理后P.fluorescens的活性氧水平变化
Fig.6 Changes in ROS levels in P.fluorescens after thymol treatment
2.7 百里香酚对DNA合成的影响
DNA是细菌正常生长和繁殖的基础,降低其水平可有效抑制细菌生长。DAPI染料能穿透活细胞和死细胞的完整细胞膜,与DNA结合,使其染成亮蓝色(图7-a~图7-c)。对照组DNA分布明显且均匀,而1 MIC和2 MIC处理组的荧光强度降低,表明百里香酚处理后,菌株内DNA含量减少。

a-对照组(DPAI);b-1 MIC(DPAI);c-2 MIC(DPAI);d-对照组(PI);e-1 MIC(PI);f-2 MIC(PI)
图7 百里香酚处理前后的P.fluorescens的荧光倒置显微镜图片
Fig.7 Fluorescence inverted microscope images of P.fluorescens treated with thymol
PI染料能与细胞核的DNA结合,当细胞膜受损时,PI能穿透细胞膜,发出红色荧光(图7-d~图7-f)。在对照组中,由于细胞膜完整,PI仅被少数自然死亡的细胞吸收,显示微弱的红色荧光。相比之下,1 MIC 和2 MIC百里香酚处理组呈现较亮的红色荧光,表明细胞膜完整性受到破坏。
GUO等[23]报道,酚类化合物可通过抑制DNA合成或促进DNA降解,增加细胞膜通透性,导致DNA泄漏。LIU等[10]则证明百里香酚能对铜绿假单胞菌的细胞膜和DNA造成不可逆的损伤,进一步支持了百里香酚对细菌细胞膜和DNA的破坏作用。
2.8 百里香酚处理前后细胞形态变化
如图8所示,与未处理的细胞相比,1 MIC百里香酚处理的细胞表面变得粗糙,有皱纹,轻微收缩,2 MIC百里香酚处理后的细胞出现明显的收缩和干瘪,部分细胞出现明显碎裂。因此,百里香酚能使P.fluorescens的形态发生变化,证实其膜结构受到严重破坏,导致细胞质渗漏。WANG等[24]在百里香酚灭活蜡样芽孢杆菌的研究中同样观察到细胞表面收缩和干瘪,细胞内物质泄漏。
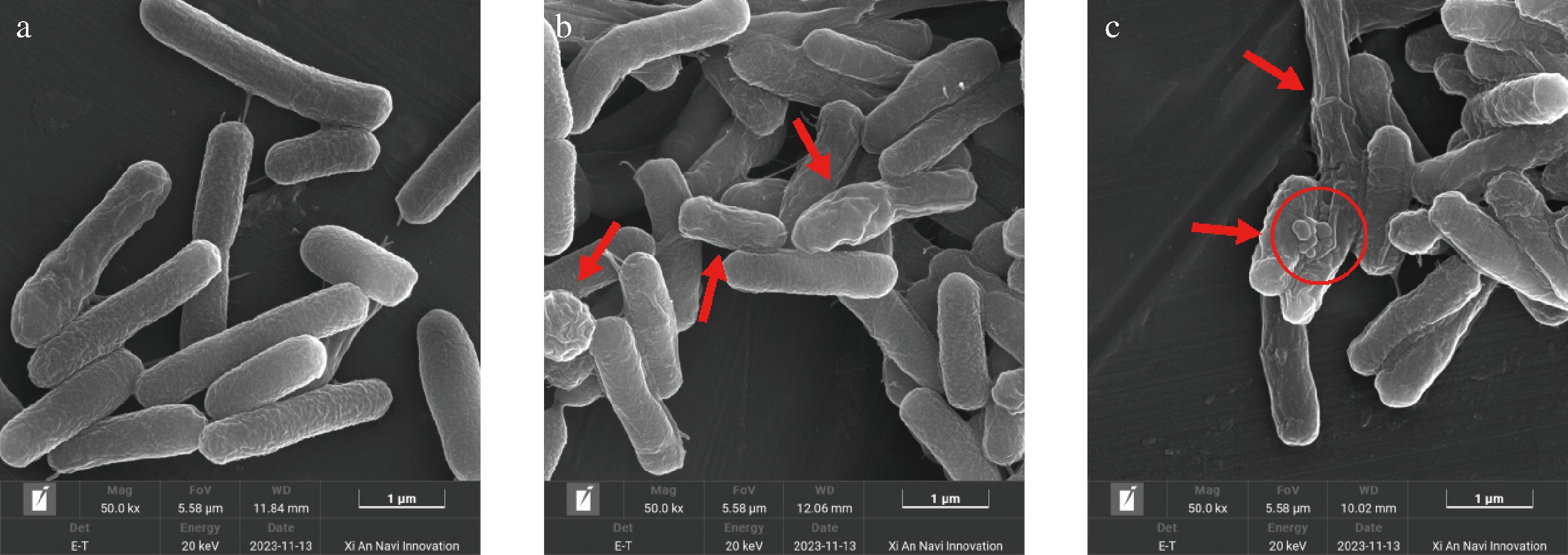
a-对照组;b-1 MIC;c-2 MIC
图8 百里香酚处理前后P.fluorescens的扫描电镜图片
Fig.8 Scanning electron microscope images of P.fluorescens cells treated with thymol
3 结论
本文研究表明,百里香酚对P.fluorescens具有显著的抗菌活性,能够使细胞膜发生去极化,引起细胞膜通透性的改变,细胞膜功能的异常使得百里香酚足以深入细胞内部抑制DNA的合成,影响细胞代谢的正常表达。ROS的累积对细胞膜和脂质的氧化损伤,进一步破坏细胞膜的完整性,造成大分子物质泄漏,进一步加速细菌死亡。研究结果阐明了百里香酚对鱼类特定腐败菌P.fluorescens的抑制机理,为百里香酚在鱼类保鲜方面作为天然抑菌剂的开发与应用提供了实验依据。
[1] XIE J, ZHANG Z, YANG S P, et al.Study on the spoilage potential of Pseudomonas fluorescens on salmon stored at different temperatures[J].Journal of Food Science and Technology, 2018, 55(1):217-225.
[2] PRESENZA L, FERRAZ TEIXEIRA B, ANTUNES GALV O J, et al.Technological strategies for the use of plant-derived compounds in the preservation of fish products[J].Food Chemistry, 2023, 419:136069.
O J, et al.Technological strategies for the use of plant-derived compounds in the preservation of fish products[J].Food Chemistry, 2023, 419:136069.
[3] OUATTARA B, SIMARD R E, HOLLEY R A, et al.Antibacterial activity of selected fatty acids and essential oils against six meat spoilage organisms[J].International Journal of Food Microbiology, 1997, 37(2-3):155-162.
[4] OUSSALAH M, CAILLET S, SAUCIER L, et al.Antimicrobial effects of selected plant essential oils on the growth of a Pseudomonas putida strain isolated from meat[J].Meat Science, 2006, 73(2):236-244.
[5] POSGAY M, GREFF B, KAPCS NDI V, et al.Effect of Thymus vulgaris L.essential oil and thymol on the microbiological properties of meat and meat products:A review[J].Heliyon, 2022, 8(10):e10812.
NDI V, et al.Effect of Thymus vulgaris L.essential oil and thymol on the microbiological properties of meat and meat products:A review[J].Heliyon, 2022, 8(10):e10812.
[6] OZOGUL F, ÇETINKAYA A, EL ABED N, et al.The effect of carvacrol, thymol, eugenol and α-terpineol in combination with vacuum packaging on quality indicators of anchovy fillets[J].Food Bioscience, 2024, 59:104008.
[7] 崔醒, 朱秋劲, 侯瑞, 等.丁香酚、香芹酚和百里香酚对禾谷镰刀菌的抑菌活性及机制[J].食品科学, 2022, 43(23):10-18.
CUI X, ZHU Q J, HOU R, et al.Antibacterial activity and mechanism of eugenol, carvacrol and thymol against Fusarium graminearum[J].Food Science, 2022, 43(23):10-18.
[8] XU J, ZHOU F, JI B P, et al.The antibacterial mechanism of carvacrol and thymol against Escherichia coli[J].Letters in Applied Microbiology, 2008, 47(3):174-179.
[9] WENG Z B, ZENG F, WANG M X, et al.Antimicrobial activities of lavandulylated flavonoids in Sophora flavences against methicillin-resistant Staphylococcus aureus via membrane disruption[J].Journal of Advanced Research, 2024, 57:197-212.
[10] LIU T, KANG J M, LIU L.Thymol as a critical component of Thymus vulgaris L.essential oil combats Pseudomonas aeruginosa by intercalating DNA and inactivating biofilm[J].LWT, 2021, 136:110354.
[11] BURT S.Essential oils:Their antibacterial properties and potential applications in foods:A review[J].International Journal of Food Microbiology, 2004, 94(3):223-253.
[12] FEI P, FENG H X, WANG Y Y, et al.Amaranthus tricolor crude extract inhibits Cronobacter sakazakii isolated from powdered infant formula[J].Journal of Dairy Science, 2020, 103(11):9969-9979.
[13] BRADFORD M M.A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J].Analytical Biochemistry, 1976, 72(1-2):248-254.
[14] CHANG Y H, XIA S W, FEI P, et al.Houttuynia cordata Thunb.crude extract inactivates Cronobacter sakazakii:Antibacterial components, antibacterial mechanism, and application as a natural disinfectant[J].Food Control, 2023, 145:109467.
[15] MAJEED S, DANISH M, ZAKARIYA N A, et al.Tailored silver nanoparticles capped with gallic acid and its potential toxicity via ROS mediated pathway against osteosarcoma cells[J].Materials Today Communications, 2022, 32:103844.
[16] ZHANG H Y, YANG Z, WANG Z, et al.Freezing enhances the killing of S.aureus by thymol via a unique bactericidal mechanism in cold chain food[J].Food Control, 2023, 153:109936.
[17] LIN Y Q, HUANG L, ZHANG X Y, et al.Multi-omics analysis reveals anti-Staphylococcus aureus activity of actinomycin D originating from Streptomyces parvulus[J].International Journal of Molecular Sciences, 2021, 22(22):12231.
[18] TIAN L, WANG X Y, LIU R J, et al.Antibacterial mechanism of thymol against Enterobacter sakazakii[J].Food Control, 2021, 123:107716.
[19] YAMMINE J, GHARSALLAOUI A, FADEL A, et al.Enhanced antimicrobial, antibiofilm and ecotoxic activities of nanoencapsulated carvacrol and thymol as compared to their free counterparts[J].Food Control, 2023, 143:109317.
[20] CHEN M S, ZHAO Z G, MENG H C, et al.The antibiotic activity and mechanisms of sugar beet (Beta vulgaris) molasses polyphenols against selected food-borne pathogens[J].LWT - Food Science and Technology, 2017, 82:354-360.
[21] KANG S M, LI X J, XING Z Y, et al.Antibacterial effect of citral on Yersinia enterocolitica and its mechanism[J].Food Control, 2022, 135:108775.
[22] WANG B Q, WANG Y, ZHANG J, et al.ROS-induced lipid peroxidation modulates cell death outcome:Mechanisms behind apoptosis, autophagy, and ferroptosis[J].Archives of Toxicology, 2023, 97(6):1439-1451.
[23] GUO L, SUN Q, GONG S Y, et al.Antimicrobial activity and action approach of the olive oil polyphenol extract against Listeria monocytogenes[J].Frontiers in Microbiology, 2019, 10:1586.
[24] WANG X Y, TIAN L, FU J P, et al.Evaluation of the membrane damage mechanism of thymol against Bacillus cereus and its application in the preservation of skim milk[J].Food Control, 2022, 131:108435.