亚麻又称胡麻,是传统的油料作物之一,富含ω-3多不饱和脂肪酸、木酚素、环肽、多糖、蛋白质等多种活性营养物质。亚麻粕作为亚麻籽榨油后的主要副产物,其蛋白质含量达32%~36%(干基占比),主要成分为球蛋白(26%~58%)和清蛋白(20%~42%)[1]。亚麻粕蛋白含有18种氨基酸,包括必需氨基酸(如赖氨酸、蛋氨酸),且谷氨酸和天冬氨酸含量较高,具备良好的营养均衡性和生理活性,是优质的植物蛋白资源[2],其酶解产物可调节胆固醇[3]、血糖[4],蛋白及衍生肽具有ACE抑制、抗菌、抗氧化等活性[5],并能有效清除·O2-、OH-、ABTS阳离子、DPPH等自由基[6]。目前亚麻粕主要应用于动物饲料领域和低附加值领域,高值化利用程度低,造成植物蛋白资源浪费[7]。常规碱溶酸沉法提取亚麻蛋白溶解性和起泡性较差,需通过改性提升功能特性以拓展其食品应用。
超声波处理作为一种高效物理改性技术,可通过空化效应调控蛋白构象,显著改善蛋白的溶解度、乳化性等功能特性[8]。研究表明,超声波处理能优化亚麻籽蛋白乳液均匀性[9],减小芝麻蛋白粒径并调控其二级与三级结构,碱性条件下可改善蛋白的溶解性和乳化性,提升其吸水率和吸油量[10],还可增强大豆蛋白表面疏水性、乳化性及发泡性[11]及豇豆蛋白的持水能力[12]。此外,超微粉碎和糖基化改性亦可改善亚麻蛋白的功能特性[13-14]。
本研究系统探究了超声波处理时间对亚麻粕蛋白结构及功能特性的影响,并研究了其消化产物抗氧化活性,同时分析了蛋白结构和功能特性之间的相关性。目前超声波已广泛应用于植物蛋白功能特性的改性处理,但关于超声波处理对亚麻蛋白结构和功能特性影响的研究未见报道。本研究旨在为亚麻粕高值化利用、亚麻蛋白的深度开发提供理论依据和技术支撑,进而推动亚麻资源的可持续利用。
1 材料与方法
1.1 材料与试剂
亚麻粕、金龙鱼色拉油,市售;NaOH、盐酸、K2HPO4、KH2PO4等均为国产分析纯。
1.2 仪器与设备
RF-5301PC荧光分光光度计,日本日立公司;LGJ-10冷冻干燥机,松源华兴科技发展公司;TU-1901紫外-可见分光光度计,北京普析通用仪器有限责任公司;HH-8数显恒温水浴锅,金坛区水北科普仪器实验厂;Vortex-Genie2涡旋混合器,北京海天友诚科技有限公司;LA204 电子天平,梅特勒-托利多科技有限公司;RHP-100高速粉碎机,永康市荣浩工贸有限公司;H1850湘仪离心机,湖南湘仪实验室仪器开发有限公司;85-2磁力搅拌器,常州金坛宏华仪器厂;STA 449 F5同步热分析仪,德国耐驰仪器;BeNano 180纳米粒度仪,丹东百特仪器有限公司。
1.3 实验方法
1.3.1 亚麻粕预处理
新鲜亚麻粕粉碎,过80目筛,将粉末于石油醚(沸程30~60 ℃)中回流脱脂8 h,置于40 ℃烘箱中干燥12 h,得到亚麻粕脱脂粉,4 ℃保存备用。
1.3.2 亚麻粕蛋白的提取
参考李一举[15]的方法,称取10.00 g亚麻粕脱脂粉,按料液比1∶30 (g∶mL)加入去离子水,调pH至9.5~10,80 ℃水浴提取1 h。离心(3 400 r/min,15 min)后,上清液用1 mol/L盐酸调至等电点(pH 4.4),再次离心(3 400 r/min,20 min)收集沉淀,冷冻干燥获得亚麻粕蛋白。
1.3.3 不同时间超声波处理亚麻粕蛋白
亚麻粕蛋白溶于去离子水(pH 7.0,20 mg/mL)。取5份30 mL溶液于探头超声仪(20 kHz、40%振幅,25 ℃水浴)下分别处理2、4、6、8、10 min,经冷冻干燥后得到样品,未处理组作对照。
1.3.4 亚麻粕蛋白结构特征
1.3.4.1 SDS-PAGE分析
参考郑杰等[16]的方法,取超声波处理后的亚麻粕蛋白样品,溶于去离子水(pH 7.00),40 ℃搅拌30 min(2 mg/mL)。与上样缓冲液按体积比2∶1混合后沸水浴4 min,4 000 r/min离心4 min后取7 μL上清液点样。130 V电泳45 min(至溴酚蓝达底部)。
1.3.4.2 红外光谱测定
将亚麻粕蛋白粉末置于衰减全反射元件,分辨率为4 cm-1,在透射模式下采用傅里叶变换红外光谱仪扫描500~4 000 cm-1的红外光谱。
1.3.4.3 粒径及zeta-电位测定
采用动态光散射仪测定亚麻粕蛋白溶液(2 mg/mL)粒径及zeta电位(折射率:样品1.35,介质1.33),重复3次。
1.3.4.4 荧光光谱测定
配制2 mg/mL的亚麻粕蛋白溶液,荧光分光光度计激发波长设置为300 nm,发射光谱采集范围为280~350 nm,激发波长与发射波长狭缝均为5 nm。
1.3.5 亚麻粕蛋白理化及功能性质的测定
1.3.5.1 溶解性测定
参考曾秋兵等[17]的方法,亚麻粕蛋白溶液10 mg/mL,调pH 7.0,45 ℃搅拌2 h,离心(4 000 r/min,10 min)后烘干至恒重,称得干重m1,总蛋白质量m0。计算如公式(1)所示:
溶解性![]()
(1)
1.3.5.2 发泡性测定
参考ZHAO等[18]的方法,取蛋白溶液(30 mL,10 mg/mL)经均质处理(10 000 r/min,1 min),取10 mg/mL蛋白溶液30 mL均质(10 000 r/min,1 min),记录初始体积V0、均质后V1,静置30 min后测V2。发泡性和泡沫稳定性计算如公式(2)、公式(3)所示:
发泡性![]()
(2)
泡沫稳定性![]()
(3)
1.3.5.3 乳化性测定
参考牟全生等[19]的方法,亚麻粕蛋白溶液(2 mg/mL)24 mL与大豆油8 mL均质(10 000 r/min,1 min)制备乳液。于乳化后0、10、30 min分别取底部50 μL乳液加5 mL十二烷基硫酸钠(sodium dodecyl sulfate,SDS)溶液(1 g/L)混匀,测500 nm吸光度(A0、A10、A30)。乳化活性指数(emulsifying activity index,EAI)和乳化稳定性指数(emulsifying stability index,ESI)计算如公式(4)、公式(5)所示:
(4)
(5)
式中:D,稀释倍数,100;ρ,乳化液形成前溶液蛋白质的质量浓度,g/L;θ,乳状液中油相体积分数,0.25;φ,比色皿直径,0.01 m。
1.3.6 亚麻粕蛋白的体外模拟胃肠消化性测定
采用改良YANG等[20]体外消化模型。模拟胃液(simulated gastric fluid,SGF):称取NaCl(2.00 g)与胃蛋白酶32.00 g溶于1 L去离子水,盐酸调至pH 1.20;模拟肠液(simulated intestinal fluid,SIF):KH2PO4 6.80 g与胰蛋白酶10.00 g溶于同体积去离子水,NaOH溶液调至pH 7.50后超声(40 kHz,15 min)。取pH 1.2的超声波处理亚麻粕蛋白液(25 mg/mL)8 mL与SGF 2 mL混合,37 ℃、130 r/min振荡消化,于0、30、60、90、120 min取样,沸水灭活10 min,调pH至7.0后溶解。肠液消化条件同前持续12 h,按2、4、6、8、10、12 h取样,灭活后调pH至7.0备用。
1.3.7 亚麻粕蛋白消化液的SDS-PAGE分析
将消化液稀释至2 mg/mL,按照1.3.4.1节方法进行分析。
1.3.8 亚麻粕蛋白消化液的抗氧化性分析
1.3.8.1 还原力测定
参考WANG等[21] 的方法,取蛋白试液(2 mg/mL,2.5 mL)依次加入等体积磷酸盐缓冲液(0.2 mol/L,pH 6.6)及10 g/L铁氰化钾,50 ℃水浴20 min。冷却后加入100 g/L三氯乙酸2.5 mL终止反应,4 ℃离心(4 000 r/min,10 min),取上清液2.5 mL与去离子水、1 g/L FeCl3避光反应10 min,测定700 nm吸光度。
1.3.8.2 Fe2+螯合力测定
参考曾秋兵等[17]的方法,将样品溶液(2 mg/mL,0.2 mL)与去离子水(3.65 mL)、FeCl2(2 mmol/L,0.05 mL)混合,室温平衡后加入菲洛嗪(5 mmol/L,0.1 mL)避光反应10 min。离心(4 000 r/min,5 min)后测定562 nm吸光度(A),空白组以超纯水替代样品同法测定A0。螯合力计算如公式(6)所示:
螯合力![]()
(6)
1.3.8.3 脂质过氧化抑制率测定
参考王海霞等[22]的方法,取1 mL卵磷脂悬浮液(10 mg/mL,pH 7.4 PBS)、400 μmol/L FeCl3、400 μmol/L抗坏血酸及2 mg/mL蛋白试液混合,37 ℃避光反应60 min。加入2 mL显色剂(分别将15 g三氯乙酸,0.37 g硫代巴比妥酸和2 mL浓盐酸加入去离子水中,用去离子水定容至100 mL),90 ℃加热15 min后冰浴。4 000 r/min离心10 min,测定上清液532 nm吸光度(A)。空白组以超纯水代替样品测得A0。计算如公式(7)所示:
抑制百分率![]()
(7)
1.3.8.4 DPPH自由基清除率测定
参考郑杰等[16]的方法,将0.5 mL蛋白试液(2 mg/mL)与1.5 mL DPPH溶液(0.1 mmol/L)混合,25 ℃避光反应20 min,离心后测517 nm吸光度A1,对照组测A2、A0。计算如公式(8)所示:
清除率![]()
(8)
1.3.8.5 ABTS阳离子自由基清除率测定
参考郑杰等[16]的方法,ABTS工作液(pH 7.4,A0=0.70)与蛋白试液(2 mg/mL)按体积比4∶1混合,25 ℃避光反应6 min后测定734 nm吸光度(A)。计算如公式(9)所示:
清除率![]()
(9)
1.3.8.6 羟自由基清除率测定
参考SHI等[23]的方法,混合2 mmol/L FeSO4、2 mmol/L水杨酸-乙醇溶液各2 mL与蛋白试液1 mL,加12 mmol/L H2O2 2 mL启动反应,25 ℃避光温育30 min后测定510 nm吸光度(A1)。对照组以水替代水杨酸测A2,空白组以水替代样品测A0。计算如公式(10)所示:
清除率![]()
(10)
1.3.8.7 超氧阴离子自由基清除率测定
参考CHEN等[24]的方法,样品溶液(2 mg/mL,0.3 mL)与Tris-HCl缓冲液(0.05 mol/L,pH 8.2,4.5 mL)混合,25 ℃水浴10 min,加入邻苯三酚(30 mmol/L,0.1 mL)4 min后以盐酸(0.5 mL)终止,测定325 nm吸光度A1;对照组以水替代邻苯三酚A2,空白组以水替代样品A0。计算如公式(11)所示:
清除率![]()
(11)
1.4 数据统计分析
所有实验设3次重复,数据表示为“平均值±标准差”,使用Origin 2018绘图,SPSS 24.0进行单因素方差分析(ANOVA),Duncan法检验组间差异(P<0.05)。
2 结果与分析
2.1 亚麻粕蛋白结构分析
2.1.1 分子质量分布
不同时间超声波处理亚麻粕蛋白的电泳条带如图1所示,亚麻粕蛋白主要条带分子质量约为11、17、25 kDa。经超声处理后,其条带分子质量无明显变化,表明超声处理未引起蛋白质分子质量级改变。此现象与O’SULLIVAN等[25] 关于超声波处理对蛋白构效关系影响的研究结论一致。超声波的能量阈值不足以断裂肽键,因此可维持蛋白质一级结构完整性,这与傅里叶变换红外光谱检测结果相印证[26]。
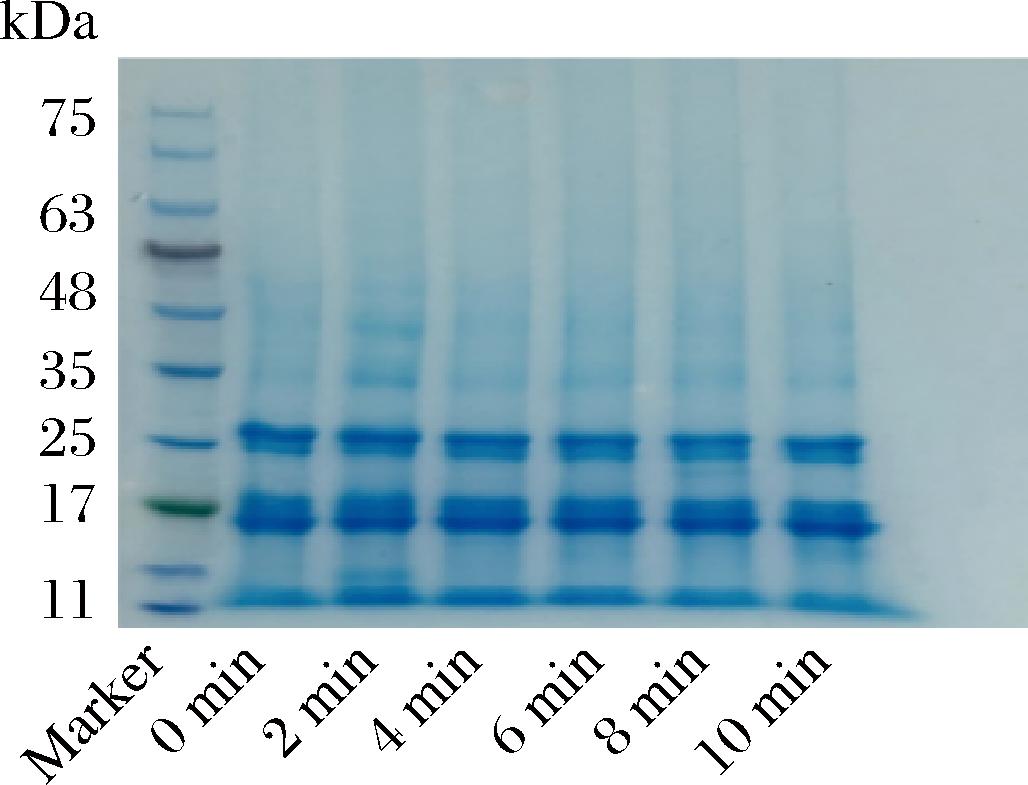
图1 不同时间超声波处理亚麻粕蛋白的SDS-PAGE图
Fig.1 SDS-PAGE image of ultrasound-treated Flaxseed meal protein with different durations
2.1.2 不同时间超声波处理亚麻粕蛋白的粒径及zeta-电位
超声波处理显著改变亚麻粕蛋白结构特性(图2)。随着处理时间延长(0~10 min),空化效应使蛋白粒径持续降低,8 min时达最小值(234.20±2.71)nm,10 min时多分散指数(polydispersity index,PDI)增至0.40 (图2-a)。分子动力学模拟表明,空化泡溃灭产生的剪切应力破坏了非共价键,驱动聚集体解离重组形成稳定的小粒径体系[27](17.69~651.73 nm)(图2-b)。
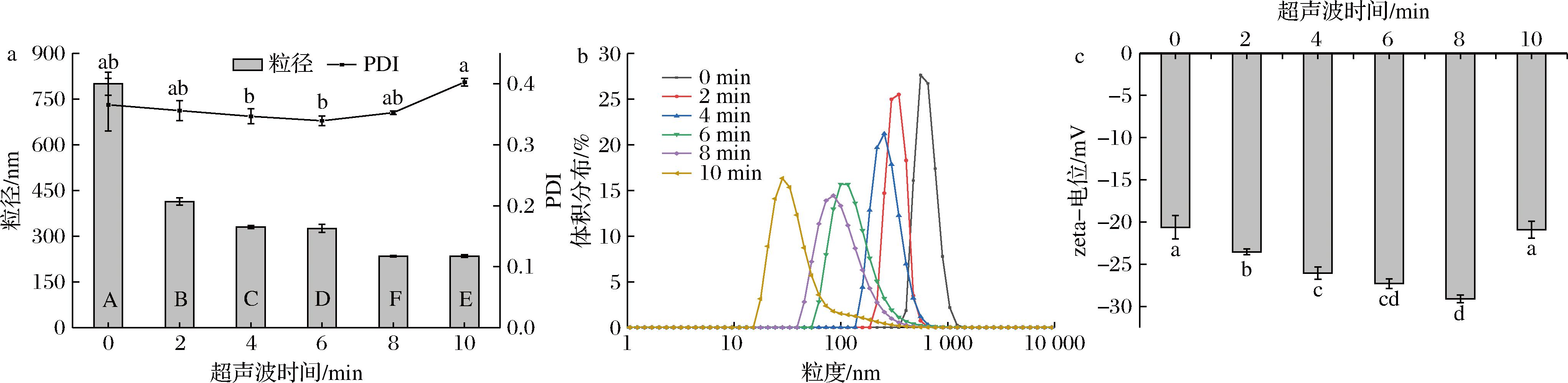
a-粒径、PDI;b-粒度分布;c-zeta-电位
图2 不同时间超声波处理亚麻粕蛋白的粒径、PDI、粒度分布和zeta-电位
Fig.2 Particle size, PDI, particle size distribution, and zeta potential of ultrasound-treated flaxseed meal protein with different durations
注:同一指标不同小写或大写字母表示组间差异显著(P<0.05)(下同)。
zeta-电位分析显示,未处理组电位为(-20.63±1.40) mV,超声波8 min处理组升至(-29.1±0.46) mV,归因于粒径减小提升电荷密度及静电斥力[28]。超声波10 min后电位回调至(-20.92±1.01) mV,提示过度处理引发蛋白降解或团聚[29]。该电荷-粒径协同效应证实超声波通过调控表面电荷与粒度分布改善溶解性[30]。
2.1.3 红外和荧光光谱
不同时间超声波处理亚麻粕蛋白的红外光谱如图3-a所示。各条曲线的大致形状相似,但在某些波长处的透过率存在差异。超声波处理过程中,亚麻粕蛋白的红外透过率均随波数的增大而呈先降低后增加,之后趋于平稳。红外光谱显示,超声波处理对亚麻粕蛋白质结构没有明显影响,表明其二级结构未被超声波处理破坏[31]。
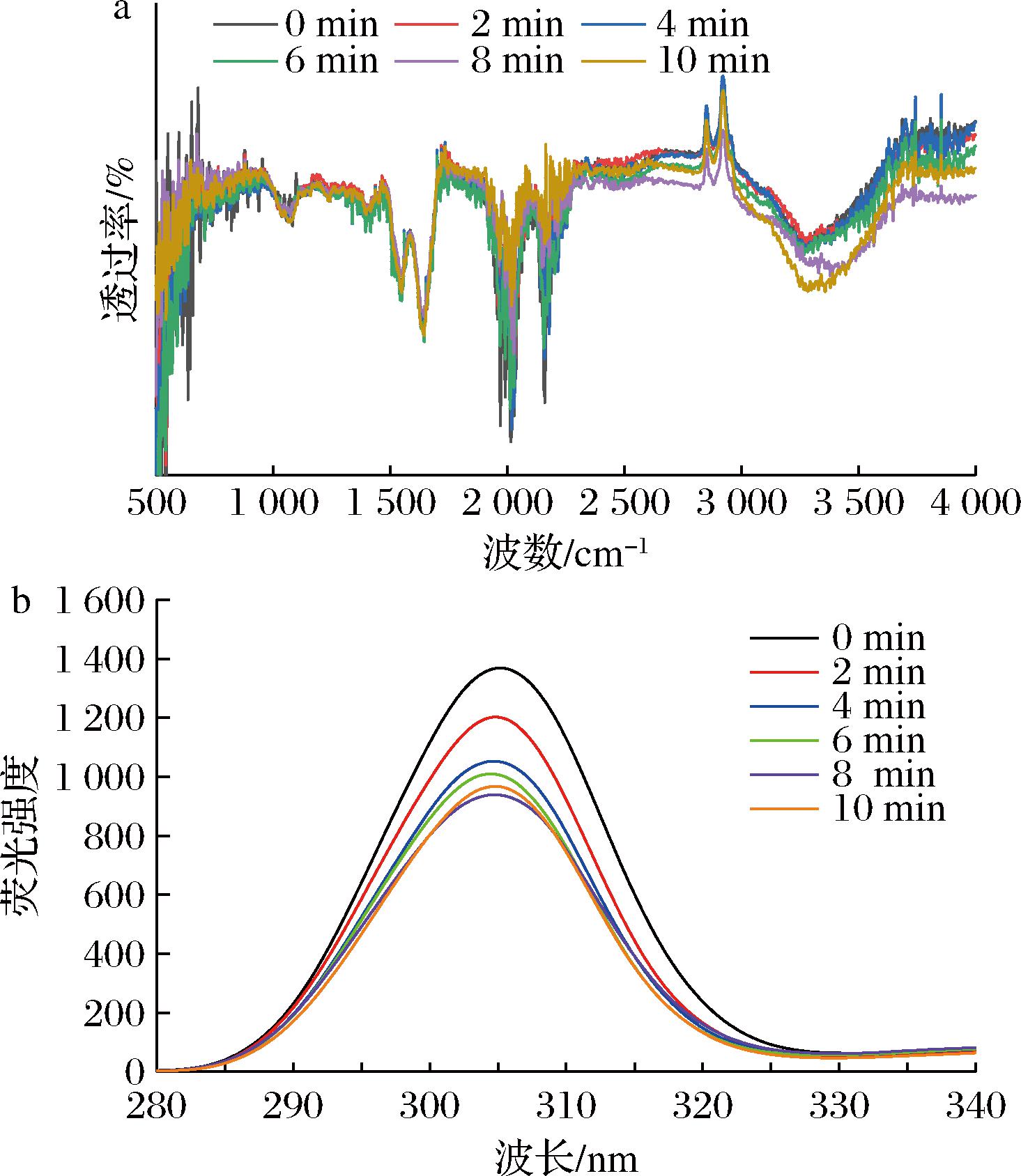
a-红外-可见吸收光谱;b-荧光光谱
图3 不同时间超声波处理亚麻粕蛋白的红外-可见吸收光谱和荧光光谱
Fig.3 UV-Vis absorption and fluorescence spectra of ultrasound-treated flaxseed meal protein with different durations
不同时间超声波处理亚麻粕蛋白的荧光光谱如图3-b所示。与对照组相比,经超声处理后的亚麻粕蛋白,最大荧光强度均在305 nm处,且荧光强度随超声波时间的延长而降低。这可能归因于超声波作用破坏了蛋白质分子的内部疏水相互作用,诱导了分子的解离,致使更多的疏水基团和区域暴露在分子表面[32]。蛋白质中的色氨酸残基等发色基团于溶剂中产生荧光猝灭作用,蛋白质间相互作用的荧光强度降低,导致三级结构发生改变[33]。
2.2 亚麻粕蛋白功能性质分析
2.2.1 溶解性
不同时间超声波处理亚麻粕蛋白的溶解性见图4。溶解度能够反映蛋白质与水分子间的水合能力。超声波改善了亚麻粕蛋白的溶解性,与粒径变化趋势一致。随着超声波时间的延长,所有样品溶解性均呈现先升高后降低的趋势,在8 min时达到最大值,为80.92%。当超声波处理时间为10 min时,亚麻粕蛋白的溶解性迅速下降,这一现象可能是因为超声波时间过长,蛋白质分子结构进一步改变,出现轻度聚集。可见,8 min超声波处理有助于促进亚麻粕蛋白的溶解。这是由于超声波处理产生的空化效应引发一系列物理反应,此过程导致了亚麻粕蛋白中的亲水基团显露并使得可溶性的蛋白质集结在一起,蛋白质分子之间的非共价键被破坏,聚集体被削弱,结构变得疏松[7]。类似文献指出,适当的超声波处理可以有效提高燕麦可溶性蛋白质含量,改善燕麦蛋白质功能特性[34]。
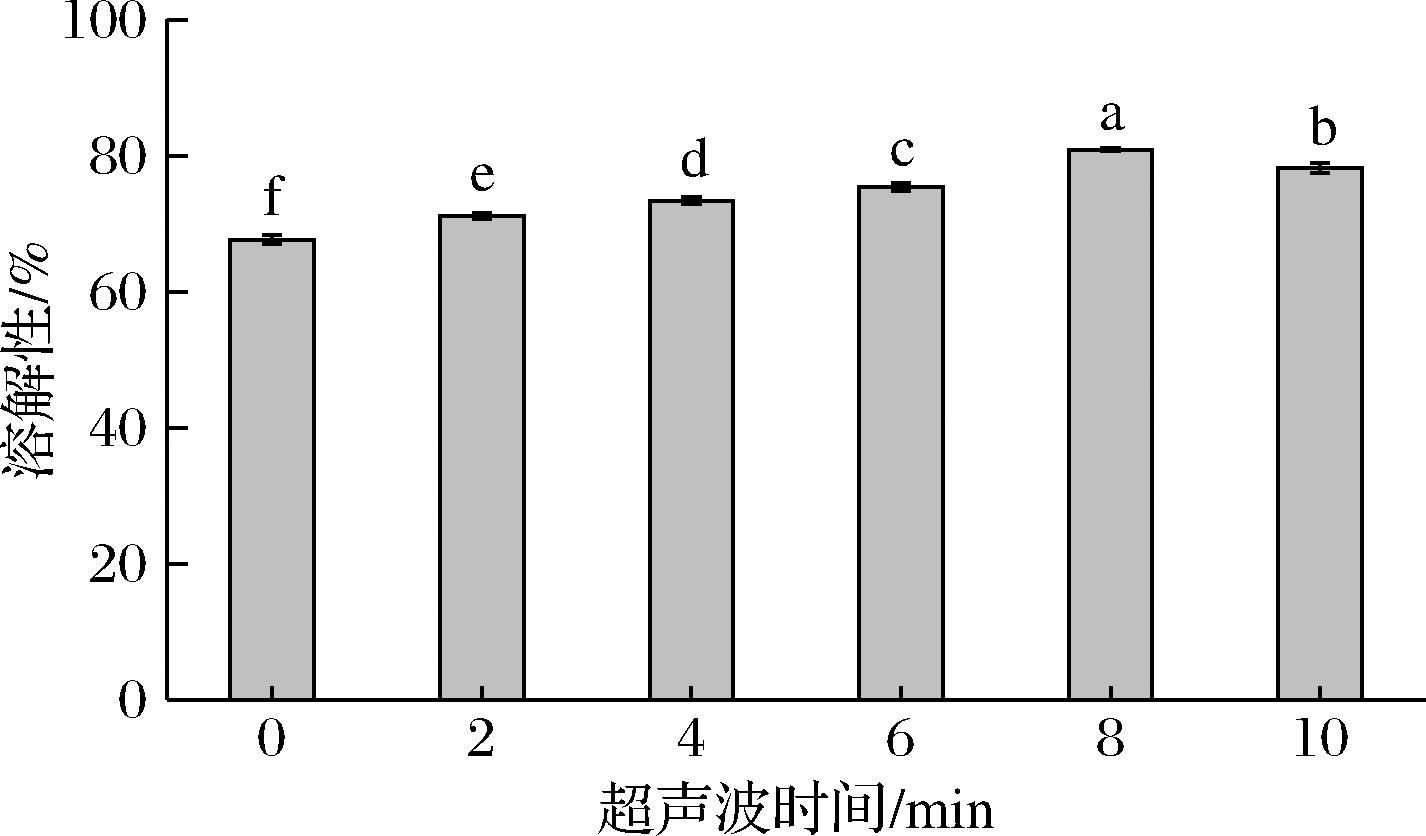
图4 不同时间超声波处理亚麻粕蛋白的溶解性
Fig.4 Solubility of ultrasound-treated flaxseed meal protein with different durations
2.2.2 发泡性
不同时间超声波处理亚麻粕蛋白的发泡性和泡沫稳定性变化如图5所示。随着超声波处理时间的延长,亚麻粕蛋白发泡性呈先升后降的趋势,在8 min时达到最大值,为55%;泡沫稳定性的变化趋势与之相反,0~6 min内逐渐降低,在6 min时最低,为33.59%,而后又逐渐增大(图5-a)。短时间超声波处理使蛋白质分子解聚,粒径减小,溶解度提升,表面疏水性提高,有利于蛋白质在气-液界面的吸附,发泡性能改善。与未经超声波处理的亚麻粕蛋白相比,短时超声波处理的亚麻粕蛋白质的发泡性显著提高,这是由于超声波促使其粒径减小、溶解性增大,从而提高了其结构柔韧性,更容易形成气-水界面膜[35]。
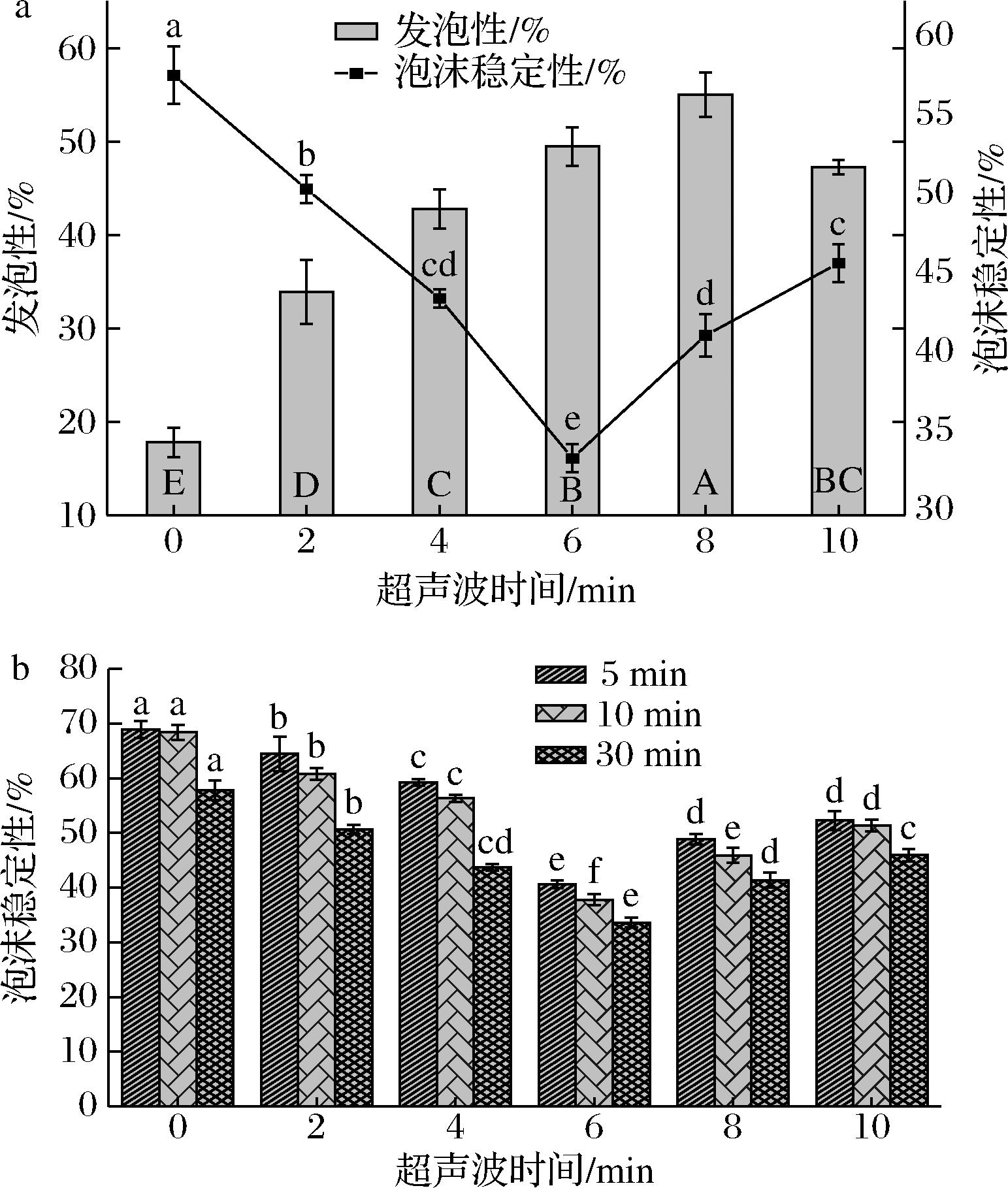
a-发泡性与泡沫稳定性;b-不同超声波处理时间的泡沫稳定性
图5 不同时间超声波处理亚麻粕蛋白的发泡性及泡沫稳定性
Fig.5 Foaming capacity and foam stability of ultrasound-treated flaxseed meal protein with different durations
由图5-b可知,与未经超声波处理的亚麻粕蛋白泡沫稳定性(5、10、30 min)相比,经超声波处理后的蛋白质泡沫稳定性显著降低,且时间越长泡沫稳定性越低。由此可知,超声波处理降低了亚麻粕蛋白的泡沫稳定性,阻止了蛋白质分子的展开,不利于界面蛋白质的吸附,从而降低界面处蛋白质的稳定性[36]。因此,超声波处理促使亚麻粕蛋白结构伸展,不利于其泡沫稳定。
2.2.3 乳化性
乳化性能表示蛋白质单位质量稳定的界面面积,表征蛋白质对油水界面的吸附能力。蛋白质的乳化性和乳化稳定性与分子的柔韧性有关。不同时间超声波处理对亚麻粕蛋白的乳化性和乳化稳定性影响如图6所示。随超声波处理时间的延长,亚麻粕蛋白的乳化性和乳化稳定度都表现为先增后降的变化规律。当处理时间为8 min时,亚麻粕蛋白乳化性最大,为(16.30±0.13) m2/g;30 min时蛋白质的乳化稳定性较10 min时显著下降。在 0~8 min内,乳化性和乳化稳定性随着超声波时间的延长而迅速增加,是由于亚麻粕蛋白溶解性的增大,表面疏水性增强,使其具有更灵活的构象,从而提高了其乳化性和乳化稳定性[37]。
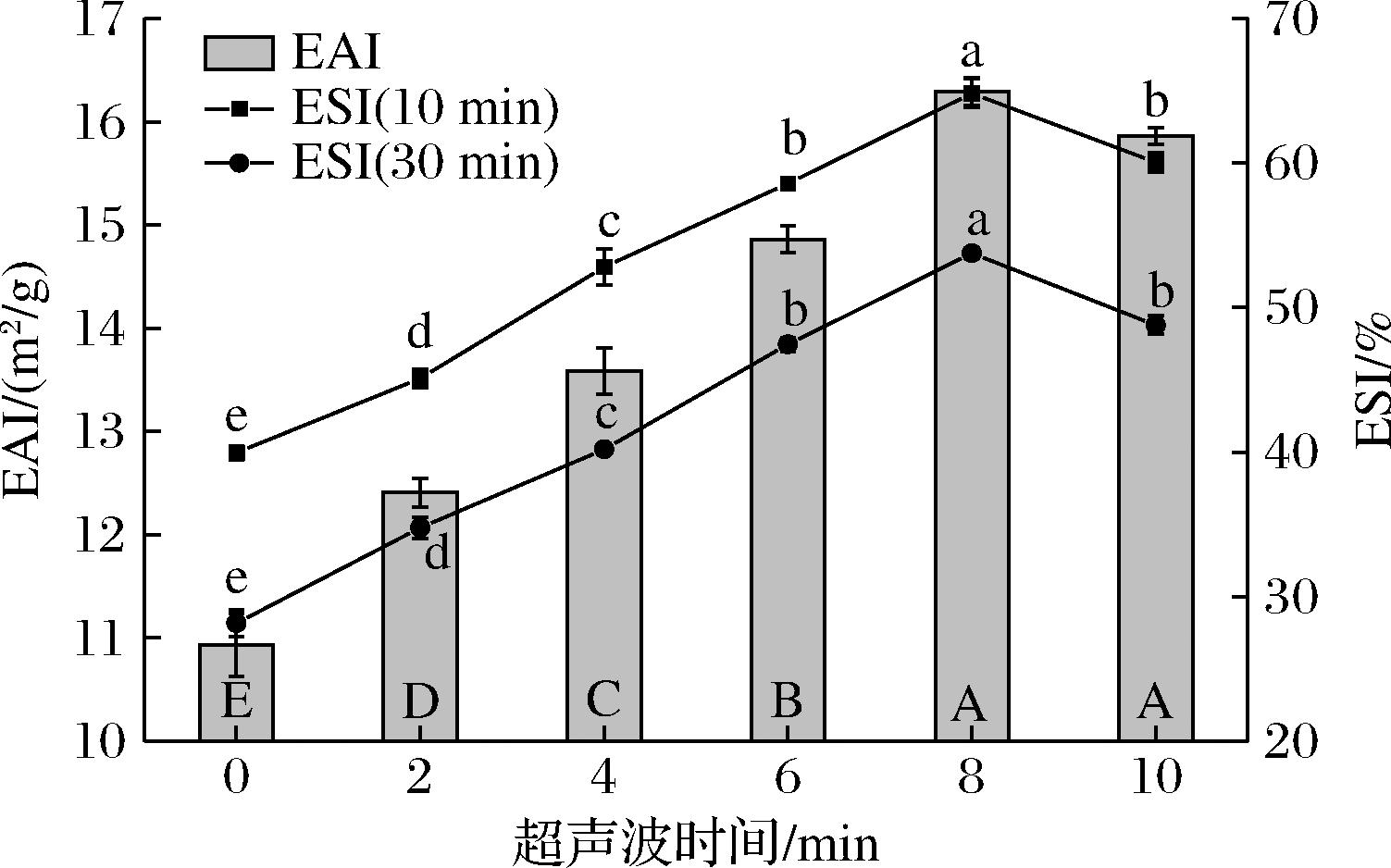
图6 不同时间超声波处理亚麻粕蛋白的乳化性及乳化稳定性
Fig.6 Emulsifying activity and emulsion stability of ultrasound-treated flaxseed meal protein with different durations
与未经超声波处理的样品相比,超声波处理后的亚麻粕蛋白乳化性及乳化稳定性显著改善,是由于超声波处理减小了亚麻粕蛋白的粒径,增加了蛋白质在油水界面的吸附倾向,从而改善了乳化性和乳化稳定性。此外,蛋白质溶解性的增大会加速其在油-水界面的扩散速度,蛋白质粒子间的静电斥力阻碍了液滴间的聚合,使亚麻粕蛋白的乳化性得到改善,静电排斥力会使蛋白质疏水性增大,蛋白质聚集并吸附于界面上形成高强度界面膜,减小界面张力,使乳液更加稳定的同时提高了蛋白质乳化稳定性[38]。卢秋玲等[28]通过超声波处理冠果种粕蛋白,研究表明随着超声波时间的延长,冠果种粕蛋白的乳化性和乳化稳定性呈现先升后降的趋势,与本文研究结果类似。
2.3 亚麻粕蛋白消化性分析
2.3.1 亚麻粕蛋白消化产物的SDS-PAGE分析
选择最佳超声波时间(8 min)处理后的亚麻粕蛋白进行消化性分析,其模拟胃肠消化产物的SDS-PAGE图见图7,分别为模拟胃消化0、1、2 h和肠道消化0、0.5、1、2、3、6 h的消化产物SDS-PAGE条带。从图中可以看出,亚麻粕蛋白在胃液中条带较少,是因为胃液强酸性条件下蛋白质沉淀,且消化程度较低[39]。
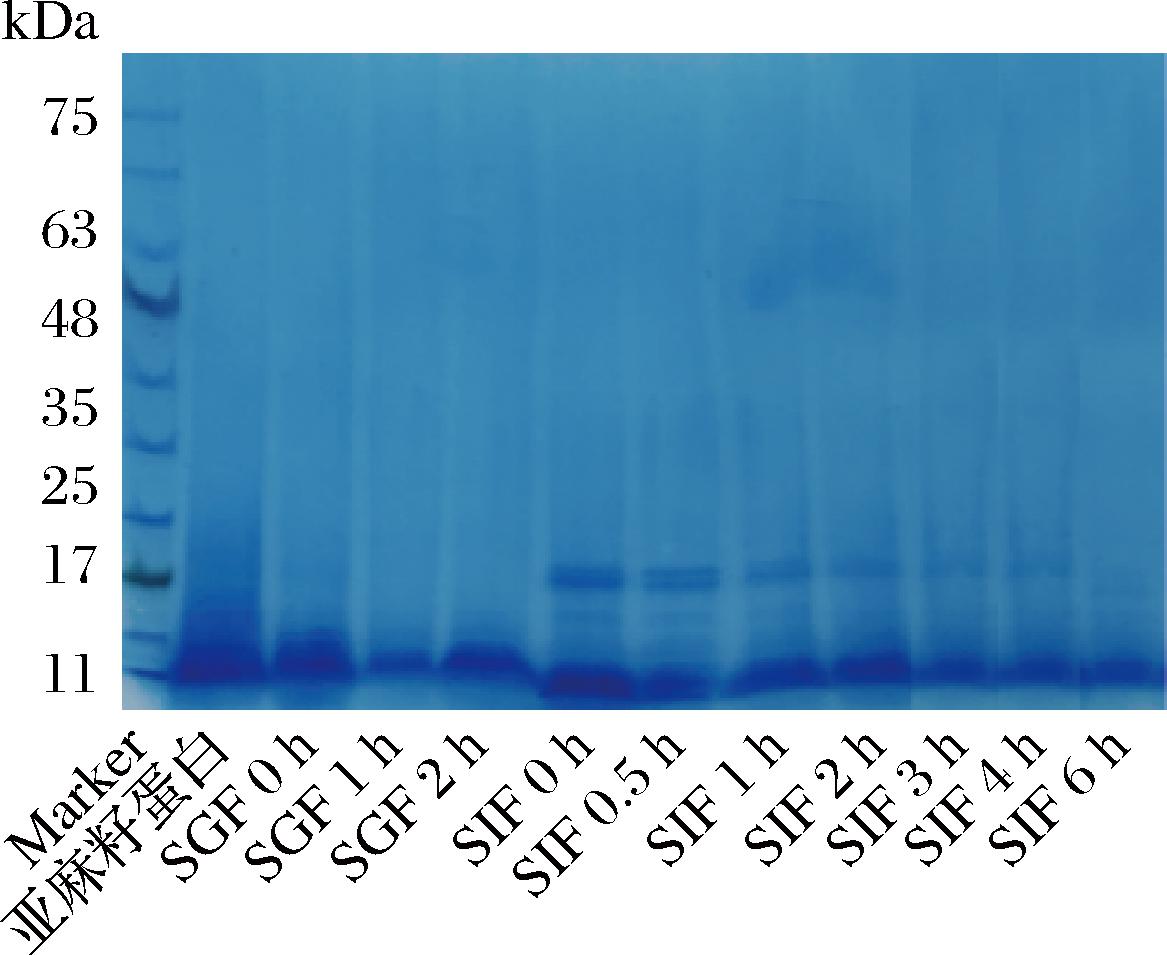
图7 不同消化时间亚麻粕蛋白的SDS-PAGE图
Fig.7 SDS-PAGE image of flaxseed meal protein at different digestion times
在模拟肠消化过程中,随着消化的进行,条带的分布和强度也发生了变化。0 h时,在11、17 kDa处出现条带,随着消化时间延长,11、17 kDa处的条带逐渐变淡,可能是肠液中的胰蛋白酶和羧肽酶等多种酶共同作用,将亚麻粕蛋白进一步水解为较小的肽段和氨基酸[39]。可见,亚麻粕蛋白具有良好的消化特性。
2.3.2 亚麻粕蛋白消化产物的抗氧化活性分析
超声波处理8 min后,不同消化时间下亚麻粕蛋白模拟肠道消化产物的抗氧化活性如图8所示。各抗氧化指标均呈现显著的消化时程依赖性,具体表现为:ABTS阳离子和DPPH自由基清除率在消化10 h时达到峰值(分别为69.01%和71.59%)(图8-a)。这表明超声波处理能够有效提升亚麻粕蛋白对ABTS阳离子和DPPH自由基的清除效率,这与已有研究结论相吻合[40]。超声波处理有利于酶对蛋白的水解作用。因此在消化液中,具有抗氧化活性的肽类物质含量有所增加[41]。当消化时间超过10 h后,消化产物的分子质量呈现下降趋势,伴随其抗氧化性能逐渐减弱,这一现象可归因于过度水解导致的活性肽降解,肽被进一步分解为游离氨基酸,导致消化产物对ABTS阳离子和DPPH自由基清除能力有所下降。
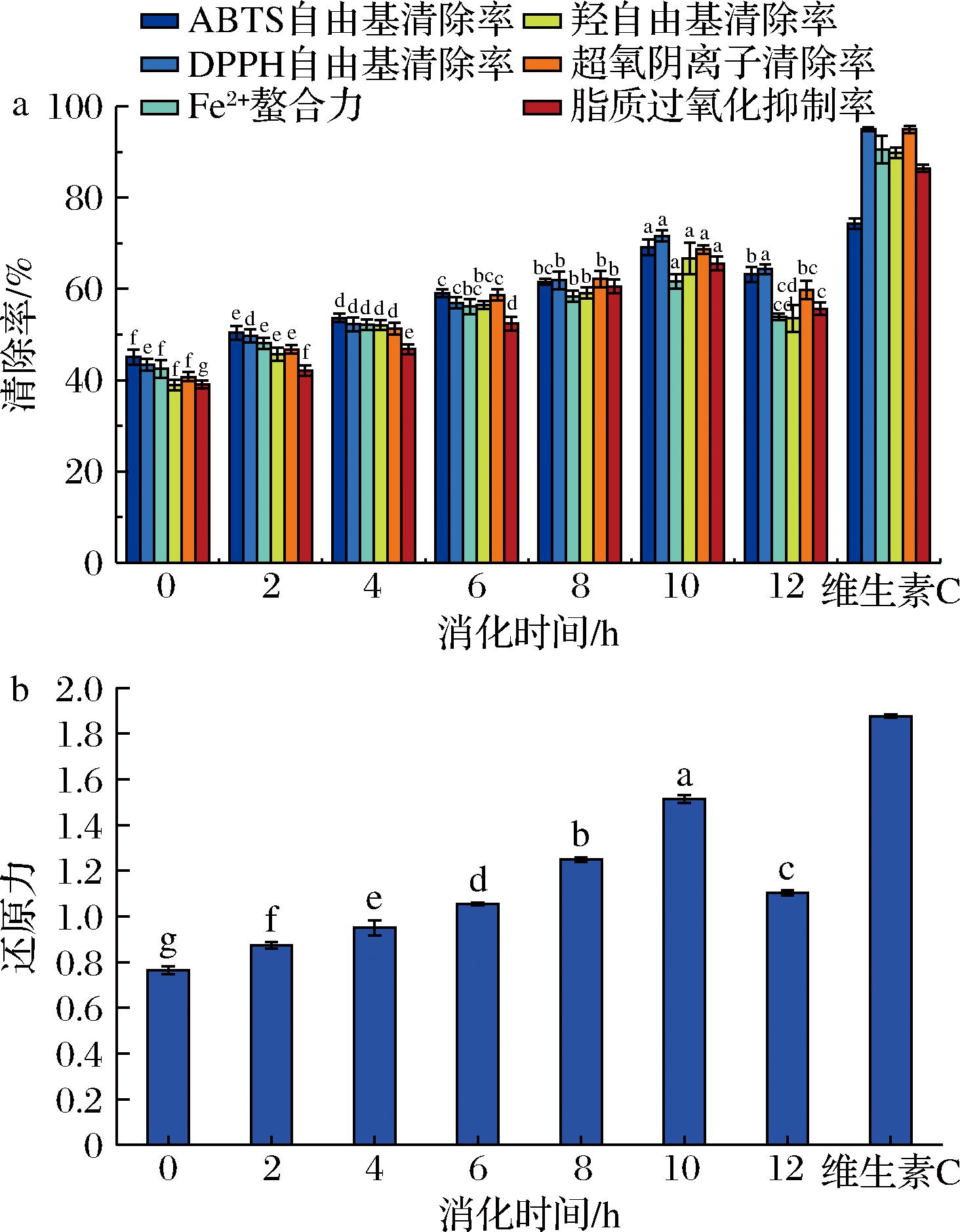
a-ABTS阳离子自由基清除率、DPPH自由基清除率、Fe2+螯合力、羟自由基清除率、超氧阴离子自由基清除率和脂质过氧化抑制率;b-还原力
图8 超声波处理亚麻粕蛋白模拟肠消化产物抗氧化特性
Fig.8 Antioxidant properties of simulated intestinal digestion products from ultrasound-treated flaxseed meal protein
如图8所示,亚麻粕蛋白的还原力、Fe2+螯合力、羟自由基清除率、超氧阴离子自由基清除率和脂质过氧化抑制率也随消化时间延长呈现出先增后降的变化趋势,且均在消化10 h时达到峰值,分别为1.51、61.60%、66.64%、68.61%和65.54%。有研究指出,模拟胃-肠消化后,鸡蛋蛋清蛋白消化产物具有较强的DPPH自由基、羟自由基、超氧阴离子自由基清除能力和还原能力[42],与本研究结果一致。
2.4 亚麻粕蛋白结构和功能特性之间相关性分析
通过Pearson相关分析揭示了亚麻粕蛋白结构-功能特性间的关系(图9)。蛋白质溶解性与发泡性、EAI及ESI呈极显著正相关(r=0.94**、0.99**、0.98**),证明其作为关键结构参数的主导作用。乳化特性间存在高度协同效应,EAI与ESI呈极显著相关(r=0.99**),且均与发泡性极显著正相关(r=0.95**、0.97**),表明蛋白质表面性质对发泡和乳化过程具有共性调控机制。

图9 不同超声波处理时间亚麻粕蛋白结构和功能性之间的相关性热图
Fig.9 Correlation heatmap between structural and functional properties of ultrasound-treated flaxseed meal proteins with different durations
注:*P≤0.05;**P≤0.01。
粒径参数呈现显著负向调控作用,与溶解性、发泡性、乳化性均呈强负相关(r=-0.88*~-0.95**),表明粒径增大显著降低功能特性。zeta电位与功能特性(溶解性、发泡性、乳化性)负相关(r=-0.53~-0.71),但与粒径(r=0.56)和泡沫稳定性正相关(r=0.76),电位绝对值的降低能够降低界面处静电屏障,促进蛋白在气水界面处的吸附,从而改善泡沫稳定性[43]。功能特性间存在显著负相关:泡沫稳定性与溶解性(r=-0.68)、发泡性(r=-0.87*)及乳化性(r=-0.75~-0.80)均呈负相关,表明蛋白质在实现不同功能特性时可能存在构象选择的竞争机制[44]。该关联网络阐释了亚麻粕蛋白结构特性对其功能特性表现的协同与拮抗作用。
3 结论
本研究以亚麻粕为原料,提取亚麻粕蛋白,并深入分析了不同时间超声波处理下其结构及功能特性的变化规律。研究发现,超声波处理后亚麻粕蛋白分子质量几乎不变,表明其一级结构未发生改变。随超声波处理时间延长,亚麻粕蛋白粒径逐渐减小,PDI增大,负电基团暴露程度增加,zeta电位的绝对值逐渐增大,体系稳定性增强。超声波处理8 min时,亚麻粕蛋白的负电荷达最大值,zeta电位为(-29.1±0.46) mV,负电量的增加有利于增强水分子与亚麻粕蛋白之间的相互作用。红外光谱结果进一步表明,超声波处理未引起亚麻粕蛋白质主要官能团变化,但其亲水性有所改善。Pearson 相关性分析结果进一步印证了亚麻粕蛋白结构和功能特性之间的关系。
超声波处理8 min后,亚麻粕蛋白表现出良好的消化性,其10 h模拟肠道消化产物的ABTS阳离子、DPPH、羟自由基和超氧阴离子自由基清除率最佳,分别为69.01%、71.59%、66.64%和 68.61%。同时,还原力、Fe2+螯合力和脂质过氧化抑制率均达到最佳,分别为1.51、61.60%和65.54%。由此可见,超声波处理可显著改善亚麻粕蛋白的功能特性。
综上所述,亚麻粕蛋白是一种优良的植物蛋白来源,其消化产物具有一定的抗氧化功效,本研究为亚麻粕蛋白的功能改性提供了数据参考。不足之处在于仅选择了超声波时间对亚麻粕蛋白结构和功能特性的影响,对于超声波功率、温度等其他参数条件的控制未做研究,下一步应优化超声波条件。此外研究仅对亚麻粕蛋白模拟肠道消化产物的抗氧化活性进行了初步探究,后期可进一步进行动物实验验证。
[1] 孔慧广.亚麻籽饼粕中蛋白的提取及其理化性质研究[D].郑州:河南工业大学,2018.
KONG H G.Extraction of protein from flaxseed meal and its physicochemical properties [D].Zhengzhou:Henan University of Technology, 2018.
[2] 邹仙果,关晓倩,郑淼,等.亚麻籽主要功能成分及其生物活性研究进展[J].食品与发酵工业,2024,50(3):366-373.
ZOU X G, GUAN X Q, ZHENG M, et al.Research progress on main functional components and biological activity of Linum usitatissimum L[J].Food and Fermentation Industries, 2024, 50(3):366-373.
[3] 侯一峰,李雪馨,包小兰.亚麻籽蛋白酶解肽的降胆固醇作用研究[J].中国油脂, 2024, 49(9):28-35.
HOU Y F, LI X X, BAO X L.Study on cholesterol-lowering effect of flaxseed protein hydrolysate peptide[J].China Oils and Fats, 2024,49 (9):28-35.
[4] 王惠敏.亚麻籽抗氧化肽制备、活性鉴定及降血糖研究[D].福州:福州大学,2018.
WANG H M.Preparation, activity identification and hypoglycemic study of flaxseed antioxidant peptides [D].Fuzhou:Fuzhou University, 2018.
[5] WU S F, WANG X C, QI W, et al.Bioactive protein/peptides of flaxseed:A review[J].Trends in Food Science &Technology, 2019, 92:184-193.
[6] ZHANG X Q, DONG W B, ZHANG M.Optimization of enzymatic preparation anti-oxidation peptides from pigskin gelatin[J].Advanced Materials Research, 2013, 641-642:984-987.
[7] CHEN X, DAI Y J, HUANG Z, et al.Effect of ultrasound on the glycosylation reaction of pea protein isolate-arabinose:Structure and emulsifying properties[J].Ultrasonics Sonochemistry, 2022, 89:106157.
[8] ZHI Z J, YAN L, LI H, et al.A combined approach for modifying pea protein isolate to greatly improve its solubility and emulsifying stability[J].Food Chemistry, 2022, 380:131832.
[9] 徐珍霞,邓乾春,董绪燕,等.超声对亚麻籽蛋白稳定的水包油乳液理化性质的影响[J].中国食物与营养,2019,25(11):35-40.
XU Z X, DENG Q C, DONG X Y, et al.Effect of ultrasound on physicochemical properties of oil-in-water emulsions stabilized by flaxseed protein[J].Food and Nutrition in China, 2019, 25(11):35-40.
[10] KIM D R, JUNG Y, RHO S J, et al.Sonication of sesame meal protein isolates modified its microstructural and functional properties[J].LWT, 2023, 186:115242.
[11] WIJATNIKO B D, MURDIATI A, ELIZA C R, et al.Optimizatoin of anti-nuntritional removal, protein extraction and modification of functional properties of cowpea (Vigna unguiculata L.) protein with sonication[J].Indonesian Food and Nutrition Progress, 2023, 19(1):14.
[12] WIJATNIKO BAMBANG-DWI, MURDIATI AGNES, ELIZA CHELSEA-RIE, et al.Optimizatoin of anti-nuntritional removal. protein extraction and modification of functional properties of cowpea (Vigna unguiculata L.) protein with sonication[J].Indonesian Food and Nutrition Progress, 2023, 19:14.
[13] 梁亚丽,高荣华,秦那日苏,等.超微粉碎对亚麻籽蛋白结构和功能特性的影响[J].食品工业科技,2025,46(16):1-10.
LIANG Y L, GAO R H, QIN N R S, et al.Effect of superfine grinding on the structure and functional properties of flaxseed protein[J].Food Industry Science and Technology, 2025,46(16):1-10.
[14] 任娟蕊,金丽娜,赵习爱,等.糖基化改性对亚麻籽蛋白理化性质的研究[J].中国粮油学报,2024,39(10):118-127.
REN J R, JIN L N, ZHAO X A, et al.Physicochemical properties of flaxseed protein by glycosylation modification [J].Journal of the Chinese Cereals and Oils Association, 2024, 39(10):118-127.
[15] 李一举.藜麦蛋白的超声辅助提取及其水解物对肥胖的改善作用研究[D].杨凌:西北农林科技大学,2024.
LI Y J.Study on ultrasonic-assisted extraction of quinoa protein and the improvement effect of its hydrolysate on obesity[D].Yangling:Northwest University of Agriculture and Forestry, 2024.
[16] 郑杰,杨敏,甄晨波,等.酪蛋白胶束与多元活性分子的相互作用及其复合物特性[J].食品科学,2023,44(14):8-19.
ZHENG J, YANG M, ZHEN C B, et al.Interactions between casein micelles and various active molecules and properties of their complexes[J].Food Science, 2023, 44(14):8-19.
[17] 曾秋兵,杨敏,王裕成,等.喷雾干燥工艺对胶束态酪蛋白结构及抗氧化性的影响[J].食品与发酵工业,2020,46(6):140-147.
ZENG Q B, YANG M, WANG Y C, et al.Effect of spray-drying conditions on the structure and antioxidant activities of micellar casein[J].Food and Fermentation Industries, 2020, 46(6):140-147.
[18] ZHAO Y J,WEN C T,FENG Y Q, et al.Effects of ultrasound-assisted extraction on the structural, functional and antioxidant properties of Dolichos lablab L.Protein[J].Process Biochemistry, 2021, 101:274-284.
[19] 牟全生,杨敏,王裕成,等.脱脂牛乳体系中乳蛋白-葡萄糖美拉德反应程度及产物功能性质研究[J].食品工业科技,2019,40(12):1-6.
MOU Q S, YANG M, WANG Y C, et al.Study on the degree of milk protein-glucose Maillard reaction and functional properties of products in skim milk system [J].Food Industry Science and Technology, 2019,40 (12):1-6.
[20] YANG M, WEI Y M, ASHOKKUMAR M, et al.Effect of ultrasound on binding interaction between emodin and micellar casein and its microencapsulation at various temperatures[J].Ultrasonics Sonochemistry, 2020, 62:104861.
[21] WANG H X,YANG J T,YANG M, et al.Antioxidant activity of Maillard reaction products from a yak casein-glucose model system[J].International Dairy Journal, 2019, 91:55-63.
[22] 王海霞.牦牛乳酪蛋白—葡萄糖美拉德反应产物结构和性质研究[D].兰州:甘肃农业大学,2018.
WANG H X.Study on the structure and properties of Maillard reaction products of yak casein-glucose [D].Lanzhou:Gansu Agricultural University, 2018.
[23] SHI M J, WEI X Y, XU J, et al.Carboxymethylated degraded polysaccharides from Enteromorpha prolifera:Preparation and in vitro antioxidant activity[J].Food Chemistry, 2017, 215:76-83.
[24] CHEN L, HUANG G L.Antioxidant activities of sulfated pumpkin polysaccharides[J].International Journal of Biological Macromolecules, 2019, 126:743-746.
[25] O’SULLIVAN J, MURRAY B, FLYNN C, et al.The effect of ultrasound treatment on the structural, physical and emulsifying properties of animal and vegetable proteins[J].Food Hydrocolloids, 2016, 53:141-154.
[26] O’SULLIVAN J, ARELLANO M, PICHOT R, et al.The effect of ultrasound treatment on the structural, physical and emulsifying properties of dairy proteins[J].Food Hydrocolloids, 2014, 42:386-396.
[27] OKUMURA H, ITOH S G.Amyloid fibril disruption by ultrasonic cavitation:Nonequilibrium molecular dynamics simulations[J].Journal of the American Chemical Society, 2014, 136(30):10549-10552.
[28] 卢秋玲, 李琅, 杨敏, 等.超声处理对文冠果种粕蛋白结构及性质的影响[J].食品与发酵工业, 2024, 50(20):79-87.
LU Q L, LI L, YANG M, et al.Effect of ultrasound treatment on structural and functional properties of Xanthoceras sorbifolium Bunge seeds meal protein[J].Food and Fermentation Industries, 2024, 50(20):79-87.
[29] 王子凌,熊可心,蒋景淳,等.高强度超声处理时间对克氏原螯虾肌原纤维蛋白理化性质的影响[J].食品科学,2023,44(23):13-20.
WANG Z L, XIONG K X, JIANG J C, et al.Effect of high-intensity ultrasonic treatment time on physicochemical properties of myofibrillar protein from Procambarus clarkii[J].Food Science, 2023, 44(23):13-20.
[30] HUANG J W, WU Y H, LIU X L, et al.Heat treatment induced structural change and aggregation behavior of Moringa oleifera seed salt-soluble protein[J].Journal of Food Measurement and Characterization, 2024, 18(2):1121-1132.
[31] JAFARZADEH S, ALIAS A K, ARIFFIN F, et al.Physico-mechanical and microstructural properties of Semolina flour films as influenced by different sorbitol/glycerol concentrations[J].International Journal of Food Properties, 2018, 21(1):983-995.
[32] XIONG T, XIONG W F, GE M T, et al.Effect of high intensity ultrasound on structure and foaming properties of pea protein isolate[J].Food Research International, 2018, 109:260-267.
[33] JIN J, MA H L, WANG K, et al.Effects of multi-frequency power ultrasound on the enzymolysis and structural characteristics of corn gluten meal[J].Ultrasonics Sonochemistry, 2015, 24:55-64.
[34] 徐长韦, 周海龙, 马利华, 等.超声波处理对燕麦蛋白质含量及功能特性的影响[J].保鲜与加工, 2022, 22(9):51-55.
XU C W, ZHOU H L, MA L H, et al.Effects of high power ultrasonic treatments on functional properties of oat protein[J].Storage and Process, 2022, 22(9):51-55.
[35] ZOU H N,ZHAO N,SUN S, et al.High-intensity ultrasonication treatment improved physicochemical and functional properties of mussel sarcoplasmic proteins and enhanced the stability of oil-in-water emulsion[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2020, 589:124463.
[36] 杨陈旭,徐拥军,肖荣辉,等.超声对冷榨花生饼蛋白功能与结构特性的影响[J].食品与发酵工业,2025,51(2):142-150.
YANG C X, XU Y J, XIAO R H, et al.Effect of ultrasound on the functional and structural properties of cold-pressed peanut cake protein [J].Food and Fermentation Industries, 2025,51 (2):142-150.
[37] YANG X Y, SHI L S, GONG T, et al.Structural modification induced by heat treatments improves the emulsifying attributes of lacquer seed protein isolate[J].International Journal of Biological Macromolecules, 2022, 222:1700-1708.
[38] RAQUEL Reis L,MARIA EDUARDA M V,NATHALIA DA S C, et al.Synergism interactions of plant-based proteins:Their effect on emulsifying properties in oil/water-type model emulsions[J].Applied Sciences, 2024, 14:8086.
[39] LI X, QI B K, ZHANG S, et al.Effects of ultrasonic treatment on the structural and functional properties of cactus (Opuntia ficus-indica) seed protein[J].Ultrasonics Sonochemistry, 2023, 97:106465.
[40] 胡锦瑞, 曹荣安, 陈洪生, 等.超声辅助酶解对绿豆肽结构和抗氧化性的影响[J].中国食品学报, 2025, 25(1):239-251.
HU J R, CAO R A, CHEN H S, et al.Impact of ultrasound-assisted enzymatic digestion on the structure and antioxidant properties of mung bean peptides[J].Journal of Chinese Institute of Food Science and Technology, 2025, 25(1):239-251.
[41] 冯晓文, 赵晓涵, 潘骁琦, 等.体外模拟消化对海洋鱼骨胶原低聚肽结构和抗氧化活性的影响[J].食品与发酵工业, 2022, 48(5):173-179.
FENG X W, ZHAO X H, PAN X Q, et al.The effect of simulated digestion in vitro on structure and antioxidant activity of marine fish bone collagen oligopeptides[J].Food and Fermentation Industries, 2022, 48(5):173-179.
[42] 王雪芬.不同热处理条件对鸡蛋蛋清蛋白质体外消化的影响研究[D].武汉:华中农业大学,2018.
Wang Xuefen.Effect of different heat treatment conditions on in vitro digestion of egg white protein [D].Wuhan:Huazhong Agricultural University, 2018.
[43] DING L X, XIA M Q, ZENG Q, et al.Foaming properties and aggregation mechanism of egg white protein with different physical treatments[J].LWT, 2022, 153:112505.
[44] 张思雨,程建军,孙玉雪,等.热处理对乳清蛋白原料起泡性、理化特性的影响及关系研究[J].食品与发酵工业,2023,49(22):117-124.
ZHANG S Y, CHENG J J, SUN Y X, et al.Effect of heat treatment on foaming properties of whey protein ingredients and its relationship with physicochemical and structural[J].Food and Fermentation Industries, 2023, 49(22):117-124.