凉粉,是淀粉类原料与水糊化后适度回生制成的传统特色食品,具有晶莹剔透、清爽滑溜的特点,深受消费者的喜爱。豌豆淀粉(pea starch,PeS)作为豌豆蛋白提取的主要副产物,是制作豌豆凉粉的核心原材料,与小麦、玉米、马铃薯淀粉相比,其价格更低[1]。然而,PeS中的直链淀粉含量较高,约占30%~60%,远高于小麦淀粉(20.78%)、玉米淀粉(24.33%)和马铃薯淀粉(19.67%),这使得豌豆凉粉存在一些固有的不良特性。例如,经加工后的豌豆凉粉消化速度较快,可能会导致血糖快速上升,这对血糖管理人群的膳食选择构成限制;同时,在贮藏过程中容易出现回生现象,质地变得僵硬,失去原有的爽滑口感,进而影响相关产品的营养价值和食用体验[2]。目前,豌豆凉粉在生产和贮藏过程中存在的问题并未得到有效地控制和解决,进而限制其货架期及工业化生产。
非淀粉多糖是一种除淀粉以外的复合多糖,主要包括β-葡聚糖、纤维素、果胶等。大量研究发现,非淀粉多糖与不同淀粉复配,可对复合体系糊化特性、回生特性及消化特性产生显著的影响[3]。如武娜等[4]探究了可溶性大豆多糖对大米淀粉物化特性的影响,结果表明可溶性大豆多糖可降低大米淀粉回生值,提高其热稳定性。LI等[5]研究发现,添加魔芋葡甘露聚糖可以抑制甘薯淀粉糊化,增加抗性淀粉含量;LIU等[6]向马铃薯淀粉中添加无花果多糖,结果发现该多糖可提高马铃薯淀粉凝胶硬度;YURIS等[7]研究发现凉粉草多糖显著降低了小麦淀粉消化率,还具有降低血糖指数的潜力。青稞β-葡聚糖(highland barley β-glucan,HBBG)是一种来源于青稞的天然非淀粉多糖,其基本结构单位是β-吡喃葡萄糖[8],属于高分子黏性多糖,也是优质的水溶性膳食纤维,对水分子具有亲和力,近年来备受关注。现有研究表明,HBBG具有延缓血糖升高、降低胆固醇和改善肠道功能等[9]的生理功能,同时HBBG还能引起淀粉的黏度、流变和质构等性质发生变化,这使得HBBG在改善食品品质以及开发健康食品方面展示出巨大的潜力。
目前,关于PeS自身性质及HBBG功能的研究已取得一定成果,但将HBBG添加到以PeS为主要原料的豌豆凉粉中,探究其对豌豆凉粉营养价值以及产品品质影响的研究鲜少见报道。在本研究中,将探究不同添加量的HBBG对PeS糊化、回生及消化特性的影响。通过深入了解HBBG与PeS结合后,PeS在糊化、回生及消化特性上的变化,以及其对豌豆凉粉品质产生的影响,以期为以PeS为主要原料的食品工业提供创新思路,开发出兼具良好品质与健康功效的豌豆凉粉等新产品。
1 材料与方法
1.1 材料与试剂
豌豆淀粉(批号JS240549,含直链淀粉43.23%),上海源叶生物科技有限公司;青稞β-葡聚糖(批号WTLS230309),兰州沃特莱斯生物科技有限公司;研究中使用的所有试剂均为分析纯。
1.2 仪器与设备
FA2104S电子天平,广州玉治仪器有限公司;HH-4数显恒温水浴锅,上海辰邦仪器科技有限公司;LGJ-25 JY冷冻干燥机,八方中大科技发展有限公司;RVA-TecMaster快速黏度分析仪,瑞典波通科技仪器(北京)有限公司;DZ-DSC300差示扫描量热仪,南京大展检测仪器有限公司;Anton Paar MCR92流变仪,无锡迈莱博生物科技有限公司;NMI20-015V-I型核磁共振成像分析仪,苏州纽迈分析仪器股份有限公司;SU8020扫描电子显微镜,日本日立公司;Nicolet iS 50 衰减全反射-傅里叶变换红外光谱,赛默飞世尔科技公司;X’Pert3 MRD高分辨薄膜X射线衍射仪,英国马尔文帕纳分析公司;TA-XT.Plus质构仪,上海保圣实业发展有限公司。
1.3 实验方法
1.3.1 样品制备
将0.12、0.24、0.48、0.6、0.72 g的HBBG分别加入到PeS中,总重为3 g,用25 mL超纯水进行溶解,充分搅拌使其混合均匀,从而获得PeS-4%HBBG、PeS-8%HBBG、PeS-12%HBBG、PeS-16%HBBG和PeS-20%HBBG复合体系溶液,将PeS溶液作为空白对照。在95 ℃下水浴糊化30 min制备的淀粉糊样品,4 ℃下贮藏24 h和7 d形成复合体系样品,于冷冻干燥机中制备冻干样品用于淀粉回生特性测定及体外消化性能检测。
1.3.2 糊化特性测定
参照LI等[10]方法,将复合体系在30 ℃时以960 r/min的转速搅拌60 s,在3.7 min内加热至87 ℃,然后在87 ℃的温度下以160 r/min的转速保持2.5 min,然后在3.7 min内冷却至50 ℃,并在该温度下继续搅拌2 min。
1.3.3 热特性测定
参考LI等[11]方法并做修改。将PeS样品称重0.5 g并分散在1 mL蒸馏水或不同浓度HBBG溶液中。随后,将混合物涡旋并定量转移到DSC坩埚中,立即密封。在实验之前,样品在4 ℃下平衡12 h。在测试过程中,使用空坩埚作为对照,温度以10 ℃/min的速度从30 ℃升至100 ℃。
1.3.4 流变特性测定
参照LI等[11]方法进行测试。取1 mL质量分数为6%的淀粉糊趁热立即转移到25 ℃的流变仪板(直径50 mm,间隙1 mm)并使用流变仪测定流变特性。
1.3.4.1 静态流变测定
在剪切速率0.1~100 s-1内进行静态流变实验。记录剪切应力与剪切速率的关系,并通过幂律方程进行拟合,计算如公式(1)所示:
τ=K·γn
(1)
式中:τ,剪切应力,Pa;K,稠度系数,Pa·Sn;γ,剪切速率,s-1;n,流体指数。
1.3.4.2 动态流变测定
通过动态流变测试确定PeS-HBBG复合体系的储能模量(G′)和损耗模量(G″)。采用动态频率扫描程序,应变设置为1%,频率扫描:0.1~10 Hz。
1.3.5 水分迁移特性测定
将糊化得到的热糊样品置于试管中,在4 ℃分别贮藏24 h和7 d后记录质子弛豫信号。水分分布测定采用NMI20-015V-I型核磁共振成像分析仪完成,通过自由感应衰减进行校准。自旋-自旋弛豫时间(T2)采用Carr-Purcell-Meiboom-Gill(CPMG)脉冲序列测定,使用的参数如下:采样次数4;等待时间8 000 ms;回波次数18 000;回波时间根据样品特性在0.3~1.3 ms内调整。
1.3.6 微观结构观察
将1.3.1节制备的冻干样品固定在铜台上的导电胶中,并放入喷金机中真空喷金处理,使用扫描电镜在加速电压为2.0 kV条件下观察放大为500倍的样品。
1.3.7 短程有序结构分析
通过基线在1 200~800 cm-1中校正光谱,随后进行去卷积。ATR-FTIR参数:4 000~400 cm-1波长,扫描32次,分辨率4 cm-1,得到红外光谱图。测量在1 047、1 022、995 cm-1的吸光度,并计算1 047 cm-1/1 022 cm-1与1 022 cm-1/995 cm-1处吸光度比值,即R1047/1022和R1022/995。
1.3.8 结晶结构分析
参照赵娅杰等[12]的方法进行测试。X-射线衍射仪角范围2θ为5°~35°,扫描速率5 °/min。样品的相对结晶度采用Jade 9.0软件计算,计算如公式(2)所示:
(2)
式中:Ac,结晶区面积;Aa,无定形区面积。
1.3.9 凝胶质构特性测定
采用P/0.5型探头,TPA测试模式,样品尺寸为直径×高度3.2 cm×1.5 cm。测试参数:测前速度、测中速度和测后速度均设定为1 mm/s,测试距离10.0 mm,触发力设定2.5 g,触发类型为自动,每个样品重复测试3次。
1.3.10 体外模拟消化
参照ENGLYST等[13]的方法并稍做修改。称取冻干样品200 mg。随后,加入15 mL 0.02 mol/L醋酸钠缓冲液(pH 5.5)。将样品在沸水浴中加热30 min,冷却至室温后平衡10 min,并向样品中加入5 mL含有α-淀粉酶(290 U/mL)和糖化酶(180 U/mL)的混合酶溶液,于水浴摇床消化,分别在0、10、20、30、60、90、120 min时取0.5 mL酶解液。随后沸水煮沸10 min使酶失活。在4 500 r/min下离心5 min,并使用DNS方法测量上清液中的葡萄糖含量。淀粉水解速率、快速消化淀粉(ready digestible starch,RDS)、慢消化淀粉(slow digestible starch,SDS)及抗性淀粉(resistant starch,RS)计算如公式(3)~公式(6)所示:
淀粉水解率![]()
(3)
(4)
(5)
RS=1-RDS-SDS
(6)
式中:TS,总淀粉含量,mg;G0,水解0 min释放的葡萄糖含量,mg;G20,水解20 min释放的葡萄糖含量,mg;G120,水解120 min释放的葡萄糖含量,mg。
淀粉的体外消化曲线可拟合为一级动力学方程,计算如公式(7)所示:
Ct=C∞×(1-e-kt)
(7)
式中:t,消化时间,min;k,淀粉消化动力学常数,min-1;Ct,t min时淀粉的消化率;C∞,无限消化时间的淀粉消化率。
1.4 数据处理
所有实验均进行3次重复,Origin 2024、SPSS 27软件进行数据分析及绘制曲线,通过单因素方差分析(ANOVA)和邓肯多重比较法进行显著性分析,显著性水平设为P<0.05。利用Origin2024软件绘图。
2 结果与分析
2.1 青稞β-葡聚糖对豌豆淀粉糊化特性的影响
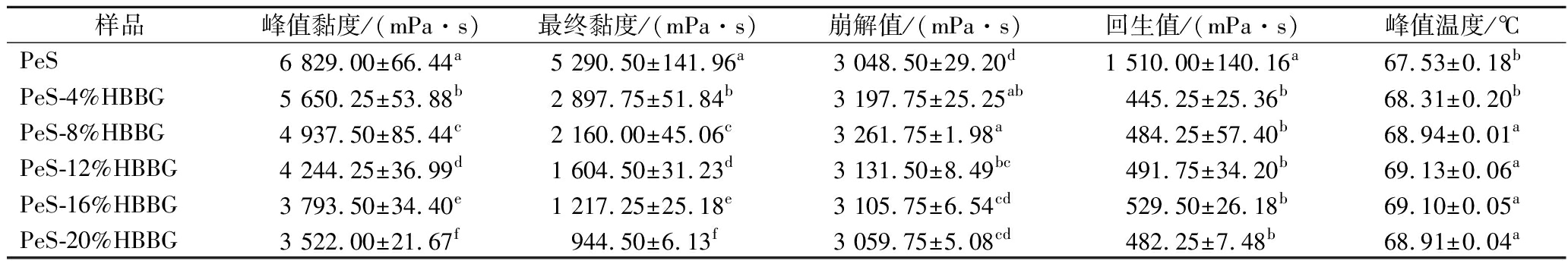
淀粉糊化的本质是淀粉颗粒中无序以及有序结构发生水合作用的过程,颗粒溶胀崩解,组分溶出并分散在水中形成胶体溶液。如图1所示,PeS的糊化模式与其他淀粉不同,在糊化过程中其糊化曲线表现出连续的增长趋势,即豌豆淀粉颗粒在连续加热过程中不易崩解[14]。由表1可知,随着HBBG添加量的增加,PeS-HBBG复合体系的峰值黏度逐渐降低,这是由于HBBG与淀粉颗粒竞争水分,导致淀粉糊化受阻,与周婧琦等[15]的研究结果相似。最终黏度是衡量淀粉糊冷却静置后黏度的重要指标,反映淀粉凝沉与重结晶特性。实验显示,HBBG添加量增加时,最终黏度从5 290.50 mPa·s骤降至944.50 mPa·s。这是因为HBBG通过竞争水分,形成空间位阻和氢键,抑制淀粉颗粒膨胀与直链淀粉溶出,降低淀粉糊黏度。此抑制作用可延缓凉粉回生变硬,利于保持品质。
表1 PeS和PeS-HBBG复合体系的糊化特性参数
Table 1 Pasting properties of PeS and PeS-HBBG composite systems
样品峰值黏度/(mPa·s)最终黏度/(mPa·s)崩解值/(mPa·s)回生值/(mPa·s)峰值温度/℃PeS6 829.00±66.44a5 290.50±141.96a3 048.50±29.20d1 510.00±140.16a67.53±0.18bPeS-4%HBBG5 650.25±53.88b2 897.75±51.84b3 197.75±25.25ab445.25±25.36b68.31±0.20bPeS-8%HBBG4 937.50±85.44c2 160.00±45.06c3 261.75±1.98a484.25±57.40b68.94±0.01aPeS-12%HBBG4 244.25±36.99d1 604.50±31.23d3 131.50±8.49bc491.75±34.20b69.13±0.06aPeS-16%HBBG3 793.50±34.40e1 217.25±25.18e3 105.75±6.54cd529.50±26.18b69.10±0.05aPeS-20%HBBG3 522.00±21.67f944.50±6.13f3 059.75±5.08cd482.25±7.48b68.91±0.04a
注:同一列中具有相同上标字母的值在P>0.05时没有显著差异(下同)。
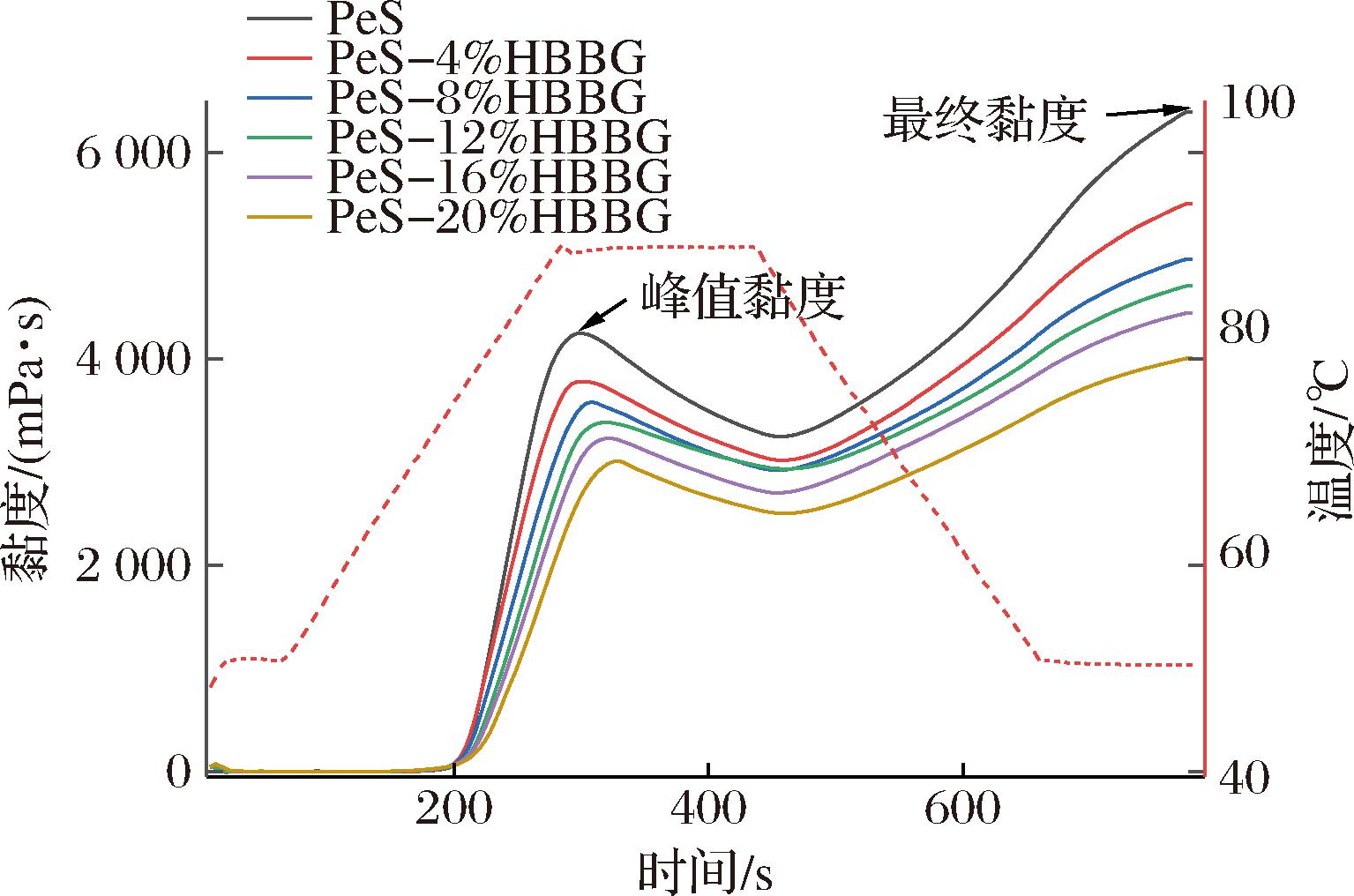
图1 PeS和PeS-HBBG复合体系的糊化特性曲线
Fig.1 Pasting properties curves of PeS and PeS-HBBG composite systems
崩解值反映淀粉在加热过程中的稳定性。崩解值越高,淀粉膨胀能力越高,其抗剪切能力越强。与纯PeS相比,复合体系的崩解值显著降低(P<0.05),并随着HBBG的添加量增加,崩解值不断下降。这表明,HBBG能够使PeS的热稳定性增加,但会降低PeS的抗剪切能力。回生值表征了糊化后的淀粉颗粒重新缔合程度以及短期回生程度[16]。由表1可知,随着HBBG添加量的增加,复合体系的回生值从1 510.00 mPa·s下降到482.25 mPa·s。这归因于HBBG与渗透出来的直链淀粉通过氢键结合,阻碍了淀粉网络结构的形成,从而延缓了豌豆淀粉的短期回生。在PeS-HBBG复合体系中,峰值温度随着HBBG添加量的增加而升高。向PeS中添加HBBG后,HBBG会优先和水分子结合,导致淀粉颗粒可吸收的自由水减少,吸收膨胀过程受到阻碍,从而需更高温度才能达到糊化条件,这与李妍等[17]报道的玉米耳多糖的添加对玉米淀粉糊化性质的影响相类似。
2.2 青稞β-葡聚糖对豌豆淀粉热特性的影响
表2为采用DSC测定的PeS-HBBG复合体系热特性参数。其中,糊化焓可表征破坏双螺旋结构所需的能量[18]。与纯PeS相比,添加HBBG后,复合体系的糊化焓呈现出轻微上升、随后随添加量增加而下降的趋势,从9.59 J/g降至7.69 J/g。这归因于β-葡聚糖存在时,可能会与淀粉颗粒表面发生相互作用,从而减缓淀粉颗粒吸水膨胀的速度。为了克服这种阻碍,淀粉糊化就需要更多的能量,进而导致糊化焓出现轻微上升。然而,随着青稞β-葡聚糖添加量的进一步增加,β-葡聚糖可能会干扰淀粉分子间的有序排列,破坏部分淀粉颗粒内部的结晶结构,因此糊化焓下降。由表2中数据可知,复合体系的起始温度、结束温度均随HBBG添加量的增加而升高。当HBBG添加量达到20%时,复合体系的峰值温度从63.52 ℃升至66.32 ℃。这可能是由于HBBG与淀粉竞争可利用的水分,从而限制水分吸附到淀粉的无定形区域,使得复合体系的峰值温度逐渐趋向于更高的温度。这与快速黏度分析仪观察到的结果一致。
表2 PeS和PeS-HBBG复合体系的热特性参数
Table 2 Thermal properties of PeS and PeS-HBBG composite systems
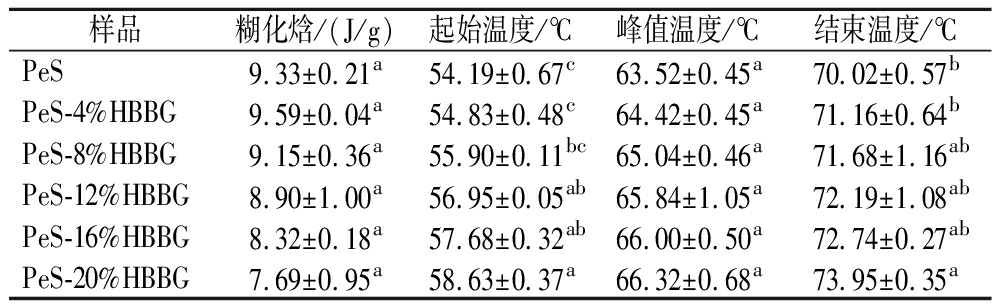
样品糊化焓/(J/g)起始温度/℃峰值温度/℃结束温度/℃PeS9.33±0.21a54.19±0.67c63.52±0.45a70.02±0.57bPeS-4%HBBG9.59±0.04a54.83±0.48c64.42±0.45a71.16±0.64bPeS-8%HBBG9.15±0.36a55.90±0.11bc65.04±0.46a71.68±1.16abPeS-12%HBBG8.90±1.00a56.95±0.05ab65.84±1.05a72.19±1.08abPeS-16%HBBG8.32±0.18a57.68±0.32ab66.00±0.50a72.74±0.27abPeS-20%HBBG7.69±0.95a58.63±0.37a66.32±0.68a73.95±0.35a
2.3 青稞β-葡聚糖对豌豆淀粉流变特性的影响
2.3.1 静态流变学分析
如图2所示,随着剪切速率的增加,样品表观黏度的降低,而样品的剪切应力略微上升,表现出典型的剪切稀化行为[19]。与纯PeS相比,HBBG的添加会使得复合体系的表观黏度呈降低的趋势,这与RVA观察到的结果一致。图2-b为HBBG及PeS-HBBG复合体系的剪切应力随剪切速率的变化曲线,实验数据通过幂律方程模型拟合后得到参数,如表3所示。拟合参数分析表明,所有样品的R2值均高于0.9,证明该模型能较好地描述样品的静态流变特性。稠度系数(K)可体现表观黏度变化,K值越高表明体系黏性越强。随着HBBG在样品中的质量分数从0%增至20%,K值持续降低,HBBG添加量较高(16%~20%)时降幅更显著。这一结果与XIE等[20]关于罗望子籽多糖对高压均质玉米淀粉影响的研究结论相似。这是因为HBBG与PeS通过氢键相互作用,抑制淀粉溶胀,进而降低了复合体系剪切流动阻力。流体指数(n)反映样品的流动特性,当n=1时为牛顿流体,n<1则表现为假塑性流体。所有样品的n值均小于1,说明添加HBBG前后的PeS复合体系均为假塑性流体。
表3 PeS和PeS-HBBG复合体系剪切应力随剪切速率的变化幂律方程参数
Table 3 Power-law equation parameters for shear stress versus shear rate in PeS and PeS-HBBG composite systems
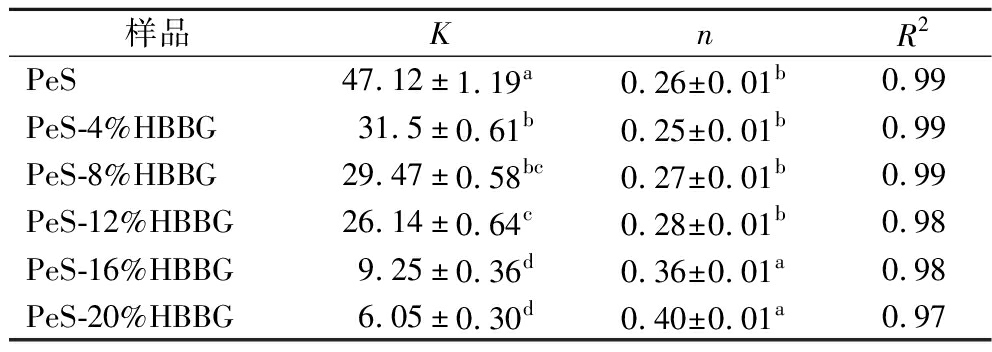
样品KnR2PeS47.12±1.19a0.26±0.01b0.99PeS-4%HBBG31.5±0.61b0.25±0.01b0.99PeS-8%HBBG29.47±0.58bc0.27±0.01b0.99PeS-12%HBBG26.14±0.64c0.28±0.01b0.98PeS-16%HBBG9.25±0.36d0.36±0.01a0.98PeS-20%HBBG6.05±0.30d0.40±0.01a0.97
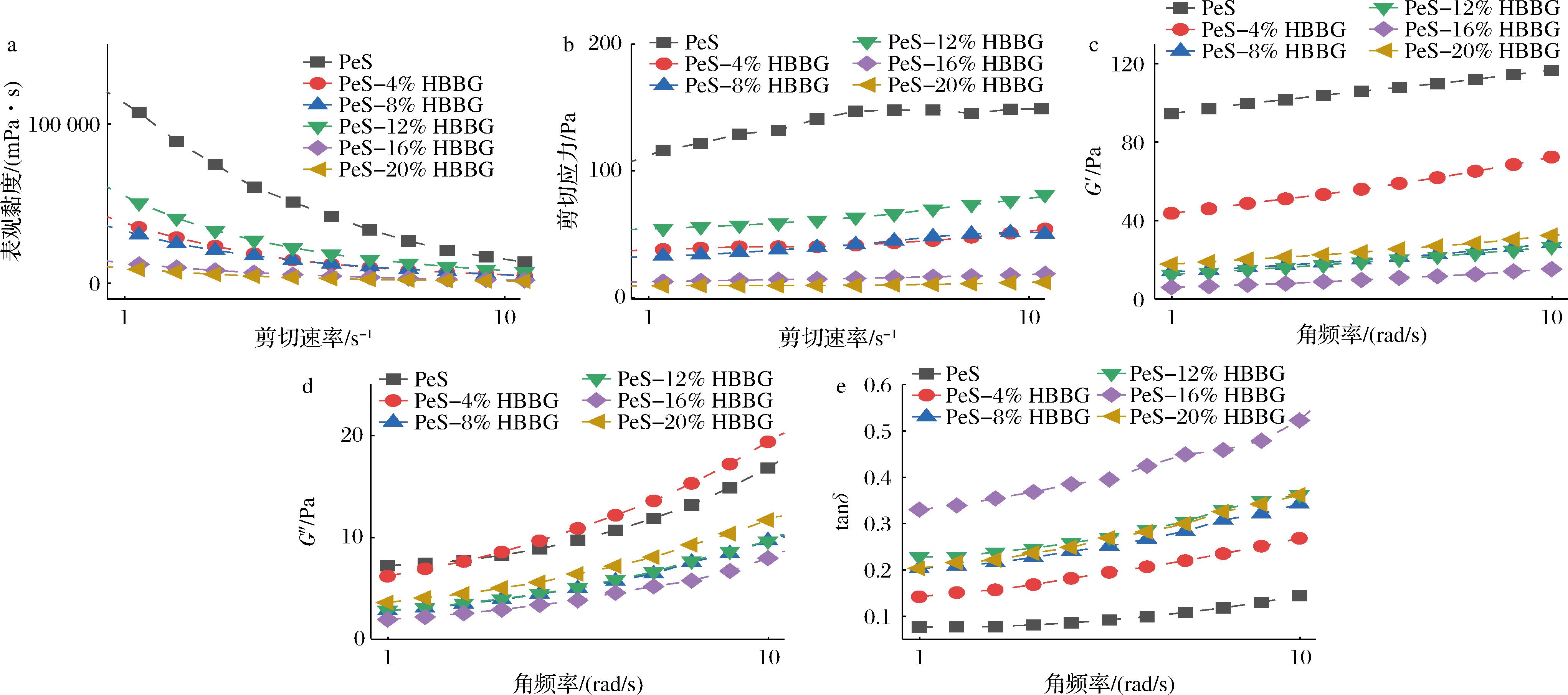
a-表观黏度;b-剪切应力;c-储能模量;d-损耗模量;e-损耗角正切值
图2 PeS和PeS-HBBG复合体系的流变学特性曲线
Fig.2 Rheological characteristic curves of PeS and PeS-HBBG composite systems
2.3.2 动态流变学分析
动态流变学特性可以用于表征不同流体是以弹性为主还是以黏性为主[21]。G′是由卷曲链构象熵的变化引起,表征发生弹性形变而储存能量的大小,属于可逆形变;G″则表示链段和分子链相对移动造成的黏性形变,由于发生黏性形变而损耗的能量大小,属于不可逆形变;损耗角正切值(tanδ)为G″与G′的比值。如图2所示,随着角频率的增大,G′和G″逐渐增大。同时,所有样品的G′>G″,tanδ<1,表明PeS-HBBG复合体系具有弱凝胶行为。与对照组相比,添加HBBG后,PeS凝胶的G′和G″值降低。HBBG与浸出的直链淀粉之间相互作用并干扰了淀粉之间的相互作用,进而使得复合体系的黏弹性能下降,与刘素臣等[14]的研究结果相似。
2.4 青稞β-葡聚糖对豌豆淀粉水分迁移的影响
淀粉回生是指糊化后的淀粉分子氢键相互作用和重排而使淀粉分子重结晶的过程,在这个过程中会伴随着水分子的迁移[22]。T21可归为较为紧密的结合水,T22是存在于凝胶结构空隙中的大量的弱结合水,T23被判定为自由水。弛豫峰积分面积与水分子相对含量成正比,其中A21、A22、A23分别对应各组峰面积。由图3可知,添加HBBG后T2峰整体左移,这表明HBBG可以稳定弱结合水、限制流动性。相同贮藏时间下,与纯PeS相比,A21峰面积显著减小(P<0.05),A22峰面积增大,这表明HBBG的添加使得淀粉和结合水之间的相互作用被破坏,部分转变为结合程度相对较弱的水。同时,由于HBBG在体系中可以形成一定的网络结构,这些网络结构能够截留更多的水分,使大部分水固定在凝胶结构空隙中,进而A22的面积增大。随着贮藏时间的延长,复合体系峰面积A21和A22都减小,而峰面积A23增大。长期贮藏过程中,淀粉回生会使体系结构致密化,让结合水变自由水,反而可能加速水分流失。
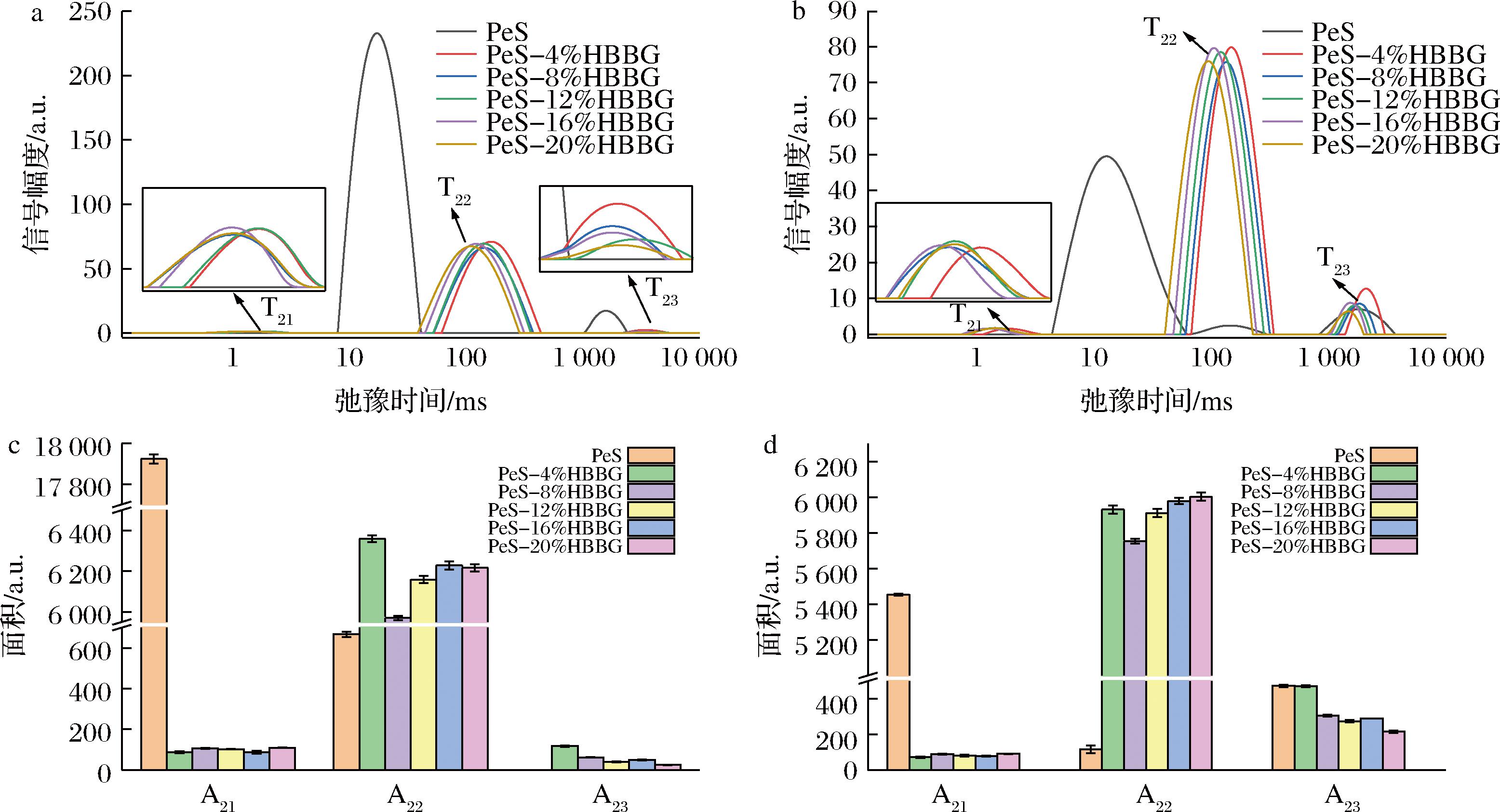
a-24 h复合体系横向弛豫时间;b-7 d复合体系横向弛豫时间;c-24 h复合体系弛豫峰面积;d-7 d复合体系弛豫峰面积
图3 PeS和PeS-HBBG复合体系的横向弛豫时间(T2)和弛豫峰面积
Fig.3 Transverse relaxation time (T2) and relaxation peak area of PeS and PeS-HBBG composite systems
2.5 青稞β-葡聚糖对豌豆淀粉微观结构的影响
如图4~图5所示,贮藏24 h的纯PeS,凝胶微观结构中存在较大且不规则的孔洞,部分区域结构松散。随着HBBG添加量的增加,复合体系中小尺寸孔隙有所增加,结构连续性增强,致密性提升。这种现象可归因于HBBG与PeS形成氢键,增强了分子间作用力。贮藏7 d的样品整体变化趋势和24 h一致。比较添加相同量HBBG,不同贮藏时间的复合体系发现,贮藏24 h的样品整体孔洞相对规整,但贮藏7 d的样品结构更加致密,这与低场核磁测定结果相似。

a-PeS;b-PeS-4%HBBG;c-PeS-8%HBBG;d-PeS-12%HBBG;e-PeS-16%HBBG;f-PeS-20%HBBG
图4 在4 ℃贮藏24 h PeS和PeS-HBBG复合体系的扫描电镜图
Fig.4 Scanning electron micrographs of the PeS and PeS-HBBG composite systems stored at 4 ℃ for 24 h

a-PeS;b-PeS-4%HBBG;c-PeS-8%HBBG;d-PeS-12%HBBG;e-PeS-16%HBBG;f-PeS-20%HBBG
图5 在4 ℃贮藏7 d PeS和PeS-HBBG复合体系的扫描电镜图
Fig.5 Scanning electron micrographs of PeS and PeS-HBBG composite systems stored at 4 ℃ for 7 d
2.6 青稞β-葡聚糖对豌豆淀粉短程有序结构的影响
图6是PeS-HBBG复合体系的傅里叶红外光谱图,不同波数特征峰与分子结构相关。HBBG的添加并未使复合体系中出现或消失任何特征吸收峰,这表明HBBG与PeS之间没有形成新的共价键,而是通过非共价键相互作用。3 320 cm-1附近峰对应—OH伸缩振动,反映体系中氢键及羟基相互作用。此处的吸收峰相对较宽,由于HBBG中存在—OH基团,在复合体系中分子间形成更强的氢键,使羟基伸缩振动所需能量降低。2 910 cm-1附近峰源于C—H伸缩振动,反映碳水化合物中甲基、亚甲基等烷基链的结构特征。
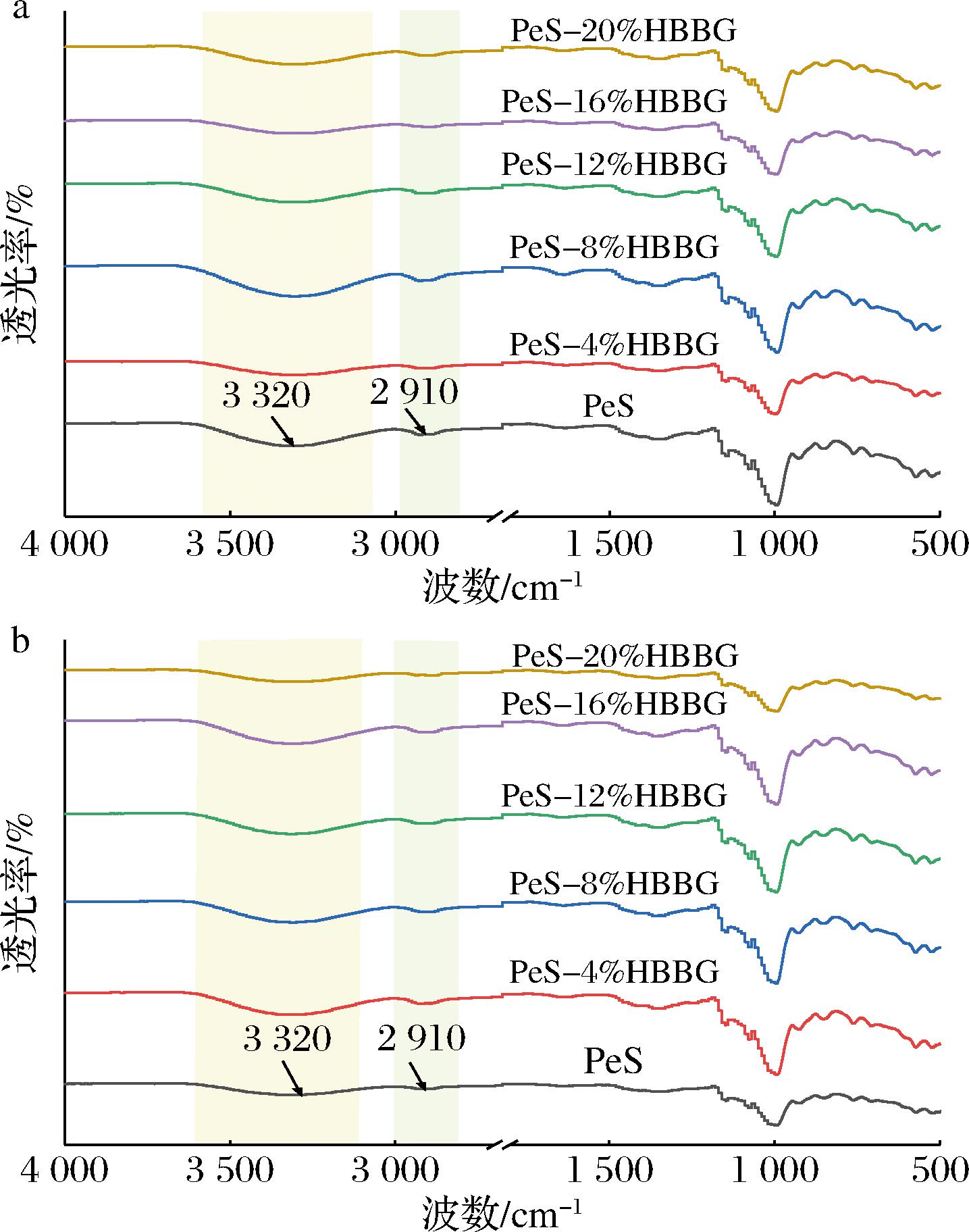
a-24 h复合体系冻干样品;b-7 d复合体系冻干样品
图6 在4 ℃贮藏24 h和7 d后PeS和PeS-HBBG复合体系的红外光谱图
Fig.6 Infrared spectra of PeS and PeS-HBBG composite systems after storage at 4 ℃ for 24 h and 7 d
1 200~800 cm-1的光谱区域与淀粉的构象和结晶状态高度相关,对光谱区域进行处理和拟合,得到1 047 cm-1/1 022 cm-1和1 022 cm-1/995 cm-1的比值,分别表示内部的有序度和双螺旋变化[23]。如表4所示,当贮藏时间为24 h,添加4%HBBG使得复合体系R1047/1022比值显著上升,这可能是由于HBBG与淀粉分子形成适度氢键,促进短程有序结构稳定。而7 d贮藏复合体系的R1047/1022比值显著降低。淀粉凝胶长时间贮藏时,淀粉分子会发生重结晶、回生,进而纯淀粉因分子有序排列,比值较高。HBBG可能通过分子空间位阻抑制淀粉重结晶,破坏短程有序结构,使比值降低。HBBG的添加,使得复合体系的R1022/995比值呈上升趋势,这可能是由于HBBG填充淀粉无定形区,增强分子间相互作用,这表明HBBG的添加会增强体系的双螺旋结构。
表4 在4 ℃贮藏24 h和7 d后PeS和PeS-HBBG复合体系的短程有序性
Table 4 Short-range order in PeS and PeS-HBBG composite systems after storage at 4 ℃ for 24 h and 7 d
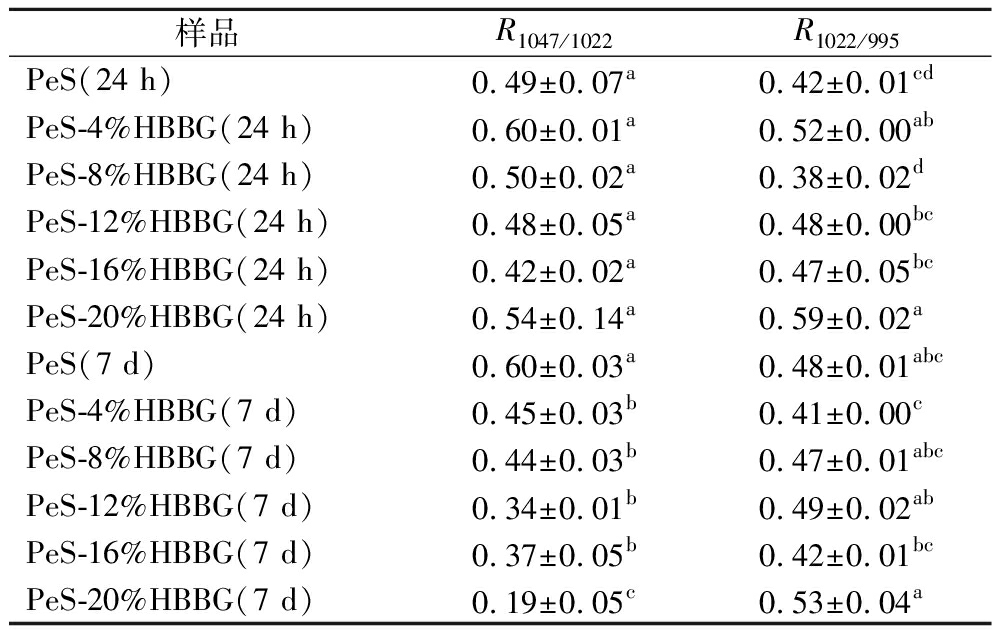
样品R1047/1022R1022/995PeS(24 h)0.49±0.07a0.42±0.01cdPeS-4%HBBG(24 h)0.60±0.01a0.52±0.00abPeS-8%HBBG(24 h)0.50±0.02a0.38±0.02dPeS-12%HBBG(24 h)0.48±0.05a0.48±0.00bcPeS-16%HBBG(24 h)0.42±0.02a0.47±0.05bcPeS-20%HBBG(24 h)0.54±0.14a0.59±0.02aPeS(7 d)0.60±0.03a0.48±0.01abcPeS-4%HBBG(7 d)0.45±0.03b0.41±0.00cPeS-8%HBBG(7 d)0.44±0.03b0.47±0.01abcPeS-12%HBBG(7 d)0.34±0.01b0.49±0.02abPeS-16%HBBG(7 d)0.37±0.05b0.42±0.01bcPeS-20%HBBG(7 d)0.19±0.05c0.53±0.04a
2.7 青稞β-葡聚糖对豌豆淀粉结晶结构的影响
天然PeS具有典型的C型晶体结构,衍射峰分布在5.61 °、15.25 °、17.32 °和23.16 °。淀粉糊化后,失去了其原有的晶体结构,仅在17 °附近处具有较为明显的衍射峰。加入HBBG后,豌豆淀粉的晶体结构并没有明显改变。PeS与HBBG复合体系的相对结晶度(relative crystallinity,RC)如图7所示,RC值表征样品中结晶物所占比重。与纯PeS相比,添加HBBG后,贮藏时间为24 h的复合体系的RC呈短暂上升后下降的趋势,这表明HBBG对淀粉的重结晶有抑制作用。贮藏时间为7 d的复合体系RC均小于纯PeS。归因于HBBG与PeS之间的氢键作用阻碍了直链淀粉分子的缔合和有序堆积,从而有效抑制了PeS的长期回生[24]。
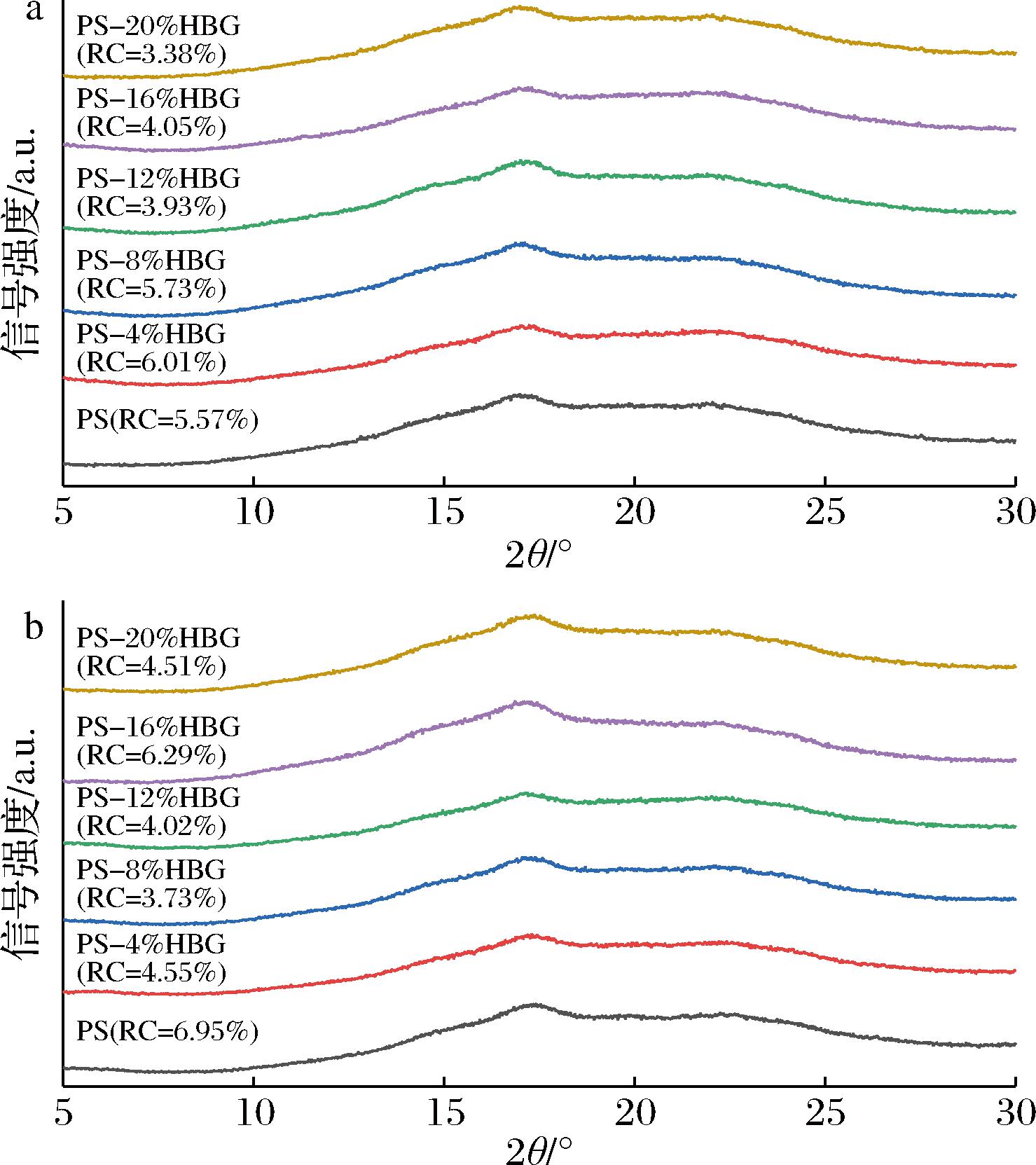
a-24 h复合体系冻干样品;b-7 d复合体系冻干样品
图7 在4 ℃贮藏24 h和7 d后PeS和PeS-HBBG复合体系的X-射线衍射图谱
Fig.7 X-ray diffraction patterns of PeS and PeS-HBBG composite systems after storage at 4 ℃ for 24 h and 7 d
2.8 青稞β-葡聚糖对豌豆淀粉凝胶质构特性的影响
弹性与回复性是反映淀粉凝胶抵抗变形并保持其形态能力的重要指标。如表5所示,在相同贮藏期内,随着HBBG添加量的增加,复合体系的弹性呈现显著下降趋势(P<0.05)。当HBBG添加量增加时,其分子中的极性基团可能与PeS分子链上的羟基发生竞争性氢键结合,削弱了淀粉分子间原有的相互作用,导致凝胶网络的刚性降低;同时,HBBG的引入可能增加了凝胶网络中的缺陷位点,使得网络结构在受力后难以完全恢复到初始状态。此外,24 h复配体系的回复性下降17%,7 d则下降23%。硬度表征臼齿间压缩样品所需的力,其大小主要与凝胶回生过程中的脱水收缩现象及支链淀粉的结晶行为相关。与对照组相比,HBBG的添加使体系硬度呈现先升高后降低的变化趋势,这一结果表明,HBBG添加量较低时可增强PeS凝胶的硬度,而HBBG添加量较高则会导致PeS凝胶硬度下降。胶着性反映凉粉的黏附性及抗断裂能力,内聚性则体现体系内部的结合力。当贮藏时间为24 h,复合体系的胶着性呈现先增加后降低的趋势,内聚性则逐渐降低。这一现象表明,HBBG的添加可使豌豆凉粉的抗断裂性增强,同时提升其食用时的顺滑感。咀嚼性由弹性、硬度及内聚性共同决定。由表5可知,咀嚼性随HBBG添加量的增加呈现先上升后下降的趋势。这一结果说明,适量添加HBBG可使豌豆凉粉的口感更为扎实。
表5 在4 ℃贮藏24 h和7 d后PeS和PeS-HBBG复合体系的凝胶特性参数
Table 5 Gel characteristic parameters of the PeS and PeS-HBBG composite systems after storage at 4 ℃ for 24 h and 7 d
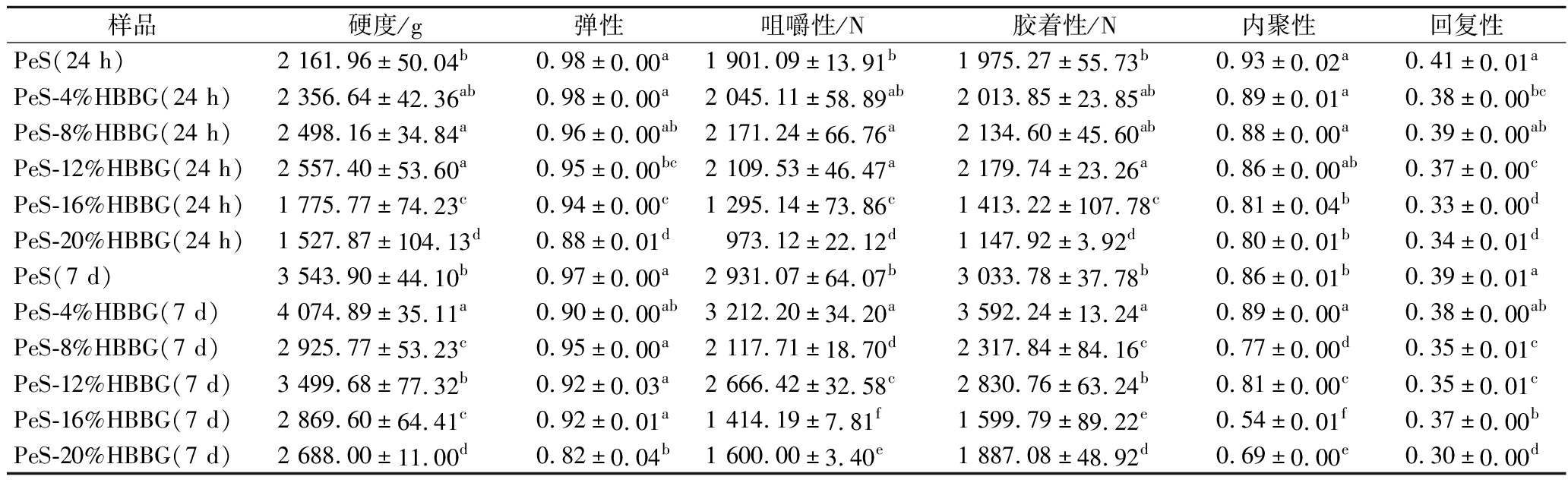
样品硬度/g弹性咀嚼性/N胶着性/N内聚性回复性PeS(24 h)2 161.96±50.04b0.98±0.00a1 901.09±13.91b1 975.27±55.73b0.93±0.02a0.41±0.01aPeS-4%HBBG(24 h)2 356.64±42.36ab0.98±0.00a2 045.11±58.89ab2 013.85±23.85ab0.89±0.01a0.38±0.00bcPeS-8%HBBG(24 h)2 498.16±34.84a0.96±0.00ab2 171.24±66.76a2 134.60±45.60ab0.88±0.00a0.39±0.00abPeS-12%HBBG(24 h)2 557.40±53.60a0.95±0.00bc2 109.53±46.47a2 179.74±23.26a0.86±0.00ab0.37±0.00cPeS-16%HBBG(24 h)1 775.77±74.23c0.94±0.00c1 295.14±73.86c1 413.22±107.78c0.81±0.04b0.33±0.00dPeS-20%HBBG(24 h)1 527.87±104.13d0.88±0.01d973.12±22.12d1 147.92±3.92d0.80±0.01b0.34±0.01dPeS(7 d)3 543.90±44.10b0.97±0.00a2 931.07±64.07b3 033.78±37.78b0.86±0.01b0.39±0.01aPeS-4%HBBG(7 d)4 074.89±35.11a0.90±0.00ab3 212.20±34.20a3 592.24±13.24a0.89±0.00a0.38±0.00abPeS-8%HBBG(7 d)2 925.77±53.23c0.95±0.00a2 117.71±18.70d2 317.84±84.16c0.77±0.00d0.35±0.01cPeS-12%HBBG(7 d)3 499.68±77.32b0.92±0.03a2 666.42±32.58c2 830.76±63.24b0.81±0.00c0.35±0.01cPeS-16%HBBG(7 d)2 869.60±64.41c0.92±0.01a1 414.19±7.81f1 599.79±89.22e0.54±0.01f0.37±0.00bPeS-20%HBBG(7 d)2 688.00±11.00d0.82±0.04b1 600.00±3.40e1 887.08±48.92d0.69±0.00e0.30±0.00d
2.9 青稞β-葡聚糖对豌豆淀粉消化性的影响
淀粉的消化率与餐后血糖和胰岛素水平的变化密切相关,对人体健康具有重要作用。图8-a展示了添加不同添加量的HBBG对PeS-HBBG复合体系体外消化特性的影响。与纯PeS相比,添加HBBG后,SDS组分从30%显著降低到17%,20%HBBG使复合体系中RS组分增加了17%,而RDS组分降低了4%,这表明HBBG的存在能够延缓淀粉的消化吸收速度,对血糖的波动具有一定的缓冲作用。HBBG是一种具有较高黏度的多糖,与PeS复合时,会在淀粉颗粒周围形成一种物理屏障,阻碍了淀粉酶与淀粉分子的接触。
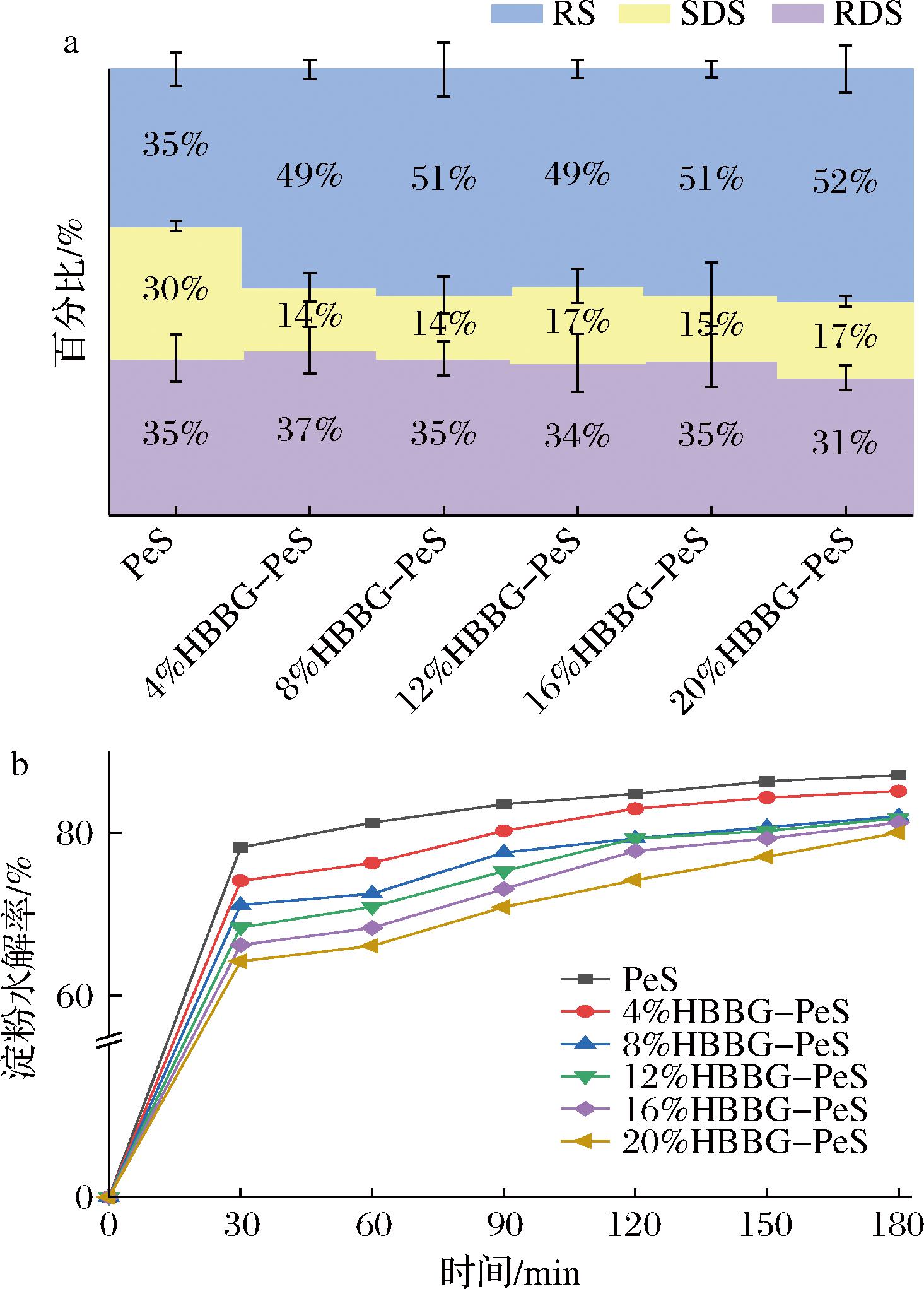
a-淀粉组分;b-淀粉消化拟合曲线
图8 PeS和PeS-HBBG复合体系的淀粉组分和淀粉消化拟合曲线
Fig.8 Starch content of PeS and PeS-HBBG composite systems and starch digestion fitting curves
为进一步探究HBBG对复合体系消化性的影响,对体外消化曲线进行一级动力学拟合,计算样品的C∞和k值。所有样品的R2值均大于0.9,表明淀粉消化曲线拟合良好。由表6可知,HBBG的添加对PS-HBBG复合体系的体外消化性影响显著(P<0.05)。C∞表征样品被消化酶完全水解为可吸收小分子糖类的最大比例。HBBG的添加使得复合体系的C∞降低,并随着HBBG含量从0%增加到20%,复合体系的C∞呈下降趋势,表明C∞与HBBG添加量呈负相关。淀粉糊化程度与淀粉消化性成正比,HBBG的存在抑制了淀粉的糊化,未完全糊化的淀粉颗粒较难被消化酶水解。k值表征淀粉被酶水解的速率的快慢。与纯PeS相比,PeS-HBBG复合体系k值从0.09下降到0.06,这可能是由于在糊化过程中,HBBG与浸出的直链淀粉相互作用,形成更复杂的分子结构,进一步减缓了酶的水解作用[25]。同时,如图8-b所示,添加HBBG的复合体系消化曲线上升更为平缓,在相同时间内淀粉水解率低于纯PeS,直观体现出HBBG对淀粉酶解速率的抑制效果,与k值的变化一致。
表6 PeS和PeS-HBBG复合体系消化模型参数
Table 6 Digestion model parameters for PeS and PeS-HBBG composite system
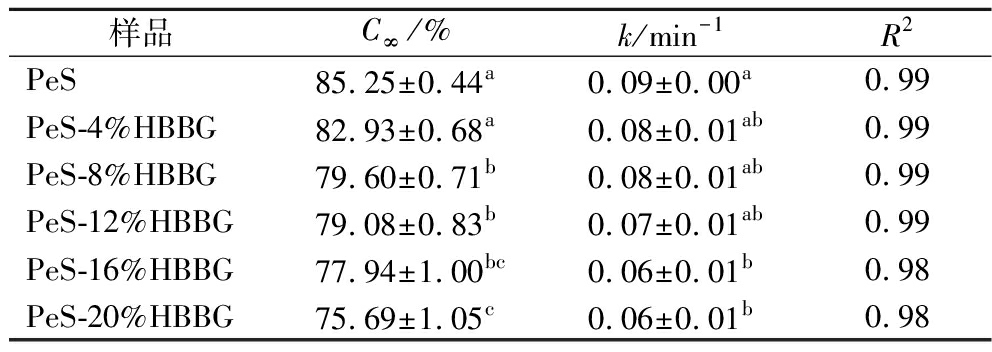
样品C∞/%k/min-1R2PeS85.25±0.44a0.09±0.00a0.99PeS-4%HBBG82.93±0.68a0.08±0.01ab0.99PeS-8%HBBG79.60±0.71b0.08±0.01ab0.99PeS-12%HBBG79.08±0.83b0.07±0.01ab0.99PeS-16%HBBG77.94±1.00bc0.06±0.01b0.98PeS-20%HBBG75.69±1.05c0.06±0.01b0.98
4 结论
本研究证实了HBBG的存在显著影响PeS的多种特性。与纯PeS相比,HBBG的存在显著降低了豌豆淀粉的糊化黏度、崩解值、回生值,提高了豌豆淀粉的糊化温度以及热稳定性。同时,与纯PeS相比,PeS-HBBG复合体系均为假塑性流体,G′和G″降低;HBBG通过氢键与直链淀粉相互作用,干扰了直链淀粉的重排,从而导致淀粉有序度降低,延缓了淀粉的回生。此外,适量的HBBG还能增加淀粉凝胶的硬度,使豌豆凉粉口感更扎实、顺滑。随着HBBG添加量的增加,HBBG与直链淀粉相互作用形成的致密微观结构及稳定水分分布可提供一个屏障,并且HBBG还能抑制淀粉颗粒完全糊化,从而抑制淀粉水解。综上,HBBG不仅为改善PeS加工特性提供关键技术支撑,也为豌豆凉粉的功能化开发及工业化生产提供重要理论依据与实践指导。同时,该研究将为慢消化食品的研发提供新思路,为血糖管理人群提供更适配的膳食选择,对提升淀粉基食品的健康价值具有重要意义。
[1] JI X L, YIN M S, HAO L R, et al.Effect of inulin on pasting, thermal, rheological properties and in vitro digestibility of pea starch gel[J].International Journal of Biological Macromolecules, 2021, 193:1669-1675.
[2] CUI Y M, HAN X D, HUANG X, et al.Effects of different sources of β-glucan on pasting, gelation, and digestive properties of pea starch[J].Food Hydrocolloids, 2023, 135:108172.
[3] 冀晓龙, 尹明松, 赵阳, 等.菊粉-小麦淀粉复配体系理化特性及相互作用[J].食品与发酵工业, 2022, 48(3):135-140.
JI X L, YIN M S, ZHAO Y, et al.Study on physicochemical properties of inulin-wheat starch blended systems and the interactions between the components[J].Food and Fermentation Industries, 2022, 48(3):135-140.
[4] 武娜, 杨杨, 边鑫, 等.可溶性大豆多糖对大米淀粉物化特性的影响[J].食品安全质量检测学报, 2022, 13(19):6140-6146.
WU N, YANG Y, BIAN X, et al.Effects of soluble soybean polysaccharides on the physical and chemical properties of rice starch[J].Journal of Food Safety &Quality, 2022, 13(19):6140-6146.
[5] LI T, ZHANG Y J, YU X W, et al.Konjac glucomannan molecular weight:A critical factor in shaping the physicochemical and digestive properties of sweet potato starch matrices[J].International Journal of Biological Macromolecules, 2025, 305:140953.
[6] LIU C M, ZHANG H B, CHEN R Y, et al.Effects of creeping fig seed polysaccharide on pasting, rheological, textural properties and in vitro digestibility of potato starch[J].Food Hydrocolloids, 2021, 118:106810.
[7] YURIS A, GOH K K T, HARDACRE A K, et al.The effect of gel structure on the in vitro digestibility of wheat starch-Mesona chinensis polysaccharide gels[J].Food &Function, 2019, 10(1):250-258.
[8] 王昕慧, 刘娟, 李俏, 等.大麦/青稞β-葡聚糖研究进展[J].应用与环境生物学报, 2024, 30(6):1176-1188.
WANG X H, LIU J, LI Q, et al.Study on barley β-glucan:A review[J].Chinese Journal of Applied and Environmental Biology, 2024, 30(6):1176-1188.
[9] ZHAO Y, ZHOU H M, HUANG Z H, et al.Different aggregation states of barley β-glucan molecules affects their solution behavior:A comparative analysis[J].Food Hydrocolloids, 2020, 101:105543.
[10] LI L, PAN F, TIAN X Z, et al.Assessing the influences of β-glucan on highland barley starch:Insights into gelatinization and molecular interactions[J].Food Chemistry, 2024, 460:140767.
[11] LI L, ZHAO Y J, MOU A Q, et al.Influence of highland barley β-glucan on textural, structural, and rheological characteristics of corn starch[J].International Journal of Biological Macromolecules, 2025, 307:141971.
[12] 赵娅杰, 牟安琼, 沈鑫, 等.青稞β-葡聚糖对玉米淀粉结构、流变性和回生特性的影响[C].中国食品科学技术学会第二十一届年会论文集.2024:430-431.
ZHAO Y J, MOU A Q, SHEN X, et al.Effects of barley β-glucan on the structure, rheological properties, and regeneration characteristics of corn starch[C]. 21 st Annual Meeting of the Chinese Society of Food Science and Technology Chongqing, China, 2024.
[13] ENGLYST H N, KINGMAN S M, CUMMINGS J H.Classification and measurement of nutritionally important starch fractions[J].European Journal of Clinical Nutrition, 1992, 46(Suppl 2):S33-S50.
[14] 刘素臣. 基于凉粉草多糖-不同类型淀粉相互作用形成的凝胶特性及新型黑凉粉制品研发[D].南昌:南昌大学, 2019.
LIU S C.Gel characteristics formed by the interaction between Polygonum cuspidatum polysaccharides and different types of starch, and the development of new black jelly products [D].Nanchang:Nanchang University, 2019.
[15] 周婧琦, 黄琴, 秦令祥, 等.山药淀粉与燕麦β-葡聚糖共混体系理化及消化性能研究[J].食品工业科技, 2022, 43(18):114-121.
ZHOU J Q, HUANG Q, QIN L X, et al.Physicochemical and digestive properties of yam starch/oat β-glucan blends[J].Science and Technology of Food Industry, 2022, 43(18):114-121.
[16] PUNIA BANGAR S, ASHOGBON A O, SINGH A, et al.Enzymatic modification of starch:A green approach for starch applications[J].Carbohydrate Polymers, 2022, 287:119265.
[17] 李妍, 崔维建, 赵城彬, 等.玉米淀粉-玉木耳多糖复配体系理化及结构性质[J].食品科学, 2021, 42(4):58-64.
LI Y, CUI W J, ZHAO C B, et al.Physicochemical and structural properties of corn starch-Auricularia cornea ehrenb.polysaccharide blends[J].Food Science, 2021, 42(4):58-64.
[18] ZHANG S S, YUE M H, WANG S H, et al.Insights into the modification of physicochemical properties and digestibility of pea starch gels with barley β-glucan[J].Journal of Food Science, 2023, 88(7):2833-2844.
[19] WU X L, ZHANG Q, ZHANG J W, et al.Effect of Cyperus esculentus polysaccharide on Cyperus esculentus starch:Pasting, rheology and in vitro digestibility[J].Food Chemistry:X, 2024, 22:101511.
[20] XIE F, ZHANG H, WU Y, et al.Effects of tamarind seed polysaccharide on physicochemical properties of corn starch treated by high pressure homogenization[J].LWT, 2021, 150:112010.
[21] 章乐乐, 崔鑫儒, 赵创谦, 等.青稞多糖对玉米淀粉糊化和流变特性的影响[J].食品与生物技术学报, 2020, 39(10):73-81.
ZHANG L L, CUI X R, ZHAO C Q, et al.Effects of polysaccharides from highland barley on gelatinization and rheological properties of corn starch[J].Journal of Food Science and Biotechnology, 2020, 39(10):73-81.
[22] LIU Y F, CHEN J, WU J Y, et al.Modification of retrogradation property of rice starch by improved extrusion cooking technology[J].Carbohydrate Polymers, 2019, 213:192-198.
[23] ZHOU D T, MA Z, YIN X X, et al.Structural characteristics and physicochemical properties of field pea starch modified by physical, enzymatic, and acid treatments[J].Food Hydrocolloids, 2019, 93:386-394.
[24] WANG J Y, YU Z W, ZHANG X, et al.Effect of feruloylated Arabinoxylan on the retrogradation and digestibility properties of pea starch during short-term refrigeration:Dependence of polysaccharide structure and bound ferulic acid content[J].International Journal of Biological Macromolecules, 2024, 257:128524.
[25] SHI X D, YU M L, YIN H M, et al.Multiscale structures, physicochemical properties, and in vitro digestibility of oat starch complexes co-gelatinized with jicama non-starch polysaccharides[J].Food Hydrocolloids, 2023, 144:108983.