酱油作为中国传统发酵调味品的典型代表,其酿造历史可追溯至三千年前的周代,是人们日常生活中必不可少的调味品[1-2]。色泽是消费者对酱油进行感官评估的首要指标,严重影响消费者的购买选择[3-4]。这一现象在中国北方饮食文化中尤为显著,酱油特有的红褐色泽与卤制、红烧等传统烹饪技法形成视觉与风味的双重协同效应[5-6],直接主导着消费者的产品选择倾向。
酱油色泽的形成与酱油生产过程中一系列复杂的生化反应密切相关[7]。研究发现,非酶促褐变反应(尤其是美拉德反应)生成的类黑精是决定酱油色泽的关键物质。类黑精作为美拉德反应的最终产物,其由还原糖与氨基酸经一系列缩合和聚合反应生成,属于一种天然的高分子聚合物,广泛存在于热加工食品(咖啡、可可)及发酵食品(酱油、啤酒)中[8-9]。近年来,大量研究聚焦于分析食品及模型食品体系中类黑精的组成、风味特征及其潜在的生物活性,为食品质量控制提供了理论依据[9-14]。YANG等[10]研究表明类黑精成分复杂、结构各异,具有多种生理活性,如抗氧化、抗高血压、抗炎、抗菌及调节肠道菌群等,是食品中的重要功能成分。此外,类黑精通过形成特征性色泽前体物质,直接影响食品的感官品质[11]。李丹等[3]研究证明类黑精在酱油独特红褐色泽的形成过程中扮演着关键作用。然而,目前对类黑精在酱油发酵过程中对色泽的具体影响尚不明确,特别是不同分子质量类黑精组分在酱油色泽形成中的定量贡献仍缺乏系统性的研究与报道。
本研究旨在定量分析不同分子质量类黑精组分对酱油色泽的贡献,并结合扫描电镜、粒径及zeta电位分析、差示扫描量热(differential scanning calorimetry, DSC)等多种表征方法,全面分析不同分子质量类黑精的微观形貌、粒径分布及热稳定性。同时,利用色度分析技术定量评估各分子质量组分对酱油色泽的具体贡献,可为酱油生产过程中色泽的精准调控提供科学依据。
1 材料与方法
1.1 材料与试剂
D101、AB-8、DA201-E型大孔吸附树脂,郑州和成新材料科技有限公司;不同分子质量组分(1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa和>50 kDa)酱油类黑精,实验室保藏(超滤制备);高盐稀态酱油(发酵6个月,盐水的质量浓度为180 g/L),实验室制作。
NaOH、盐酸、乙醇等试剂(均为分析纯),国药集团有限公司。
1.2 仪器与设备
DHG-9070烘箱,上海一恒科学仪器有限公司;ColorQuest XE分光测色仪,美国Hunterlab公司;R-100旋转蒸发仪,瑞士BUCHI公司;DSC 3差示扫描量热仪,梅特勒托利多科技(中国)有限公司;JSM-7001F扫描电子显微镜,日本电子JEOL公司;LitesizerTM 500激光粒度仪,安东帕(上海)商贸有限公司;Zetasizer Nano ZS Zeta电位分析仪,英国Malvern Panalytical公司;SCIENTZ-10 N冷冻干燥机,宁波新芝冻干设备有限公司。
1.3 实验方法
1.3.1 树脂的筛选
1.3.1.1 大孔树脂的预处理
参照ZHUANG等[15]方法,选取D101、AB-8及DA201-E 3种型号树脂,分别装填于交换柱,采用95%(体积分数,下同)乙醇静态浸渍12 h使树脂充分溶胀平衡,以蒸馏水动态冲洗至流出液无乙醇残留。随后进行酸碱活化处理,注入1.3 mol/L盐酸溶液进行静态改性(4 h),再以3~4 BV同浓度盐酸溶液动态过柱(1.5 mL/min),用蒸馏水洗涤至接近中性(pH 6.5~7.5)。同法采用1 mol/L NaOH溶液进行碱处理,最终经蒸馏水淋洗至流出液pH=7.0±0.2,真空干燥后密封保存于干燥器中待用。
1.3.1.2 大孔树脂的静态吸附
将5 g预处理后的3种树脂分别置于250 mL锥形瓶中,加入30 mL 30 mg/mL的酱油样液,置于摇床25 ℃、180 r/min恒温振荡进行静态吸附。分别于5、10、30、60、90、120、180、240、360 min时取样,每次取5 mL上清液,参照秦礼康等[16]的方法测定类黑精含量,并绘制吸附平衡时间曲线。吸附率的计算如公式(1)所示:
吸附率![]()
(1)
式中:ρ1,酱油样中类黑精质量浓度,mg/mL;ρ2,上清液中类黑精质量浓度,mg/mL。
1.3.1.3 大孔树脂的静态解吸
将5 g经预处理后的3种树脂分别置于250 mL锥形瓶中,加入30 mL配制好的30 mg/mL酱油样液,置于摇床180 r/min、25 ℃恒温振荡3 h。待静态吸附完成后,过滤树脂并转移至250 mL锥形瓶中,加入20 mL不同体积分数乙醇解吸剂(0%、20%、40%、60%、80%、100%),于25 ℃、180 r/min下恒温振荡1 h。每1 h取5 mL解吸液,测定类黑精含量[16],解吸率的计算如公式(2)所示:
解吸率![]()
(2)
式中:ρ0,解吸液中类黑精质量浓度,mg/mL;ρ1,酱油样中类黑精质量浓度,mg/mL;ρ2,表示上清液中类黑精质量浓度,mg/mL。
1.3.2 酱油类黑精的提取
参考YANG等[17]的方法,采用大孔树脂吸附提取类黑精。首先,将200 g(干重)大孔树脂浸泡于分析乙醇中24 h,随后用蒸馏水洗涤以去除杂质。将酱油稀释10倍后,转移至含有预处理树脂(内径2.5 cm×40 cm)填料的柱中,设定流速为1.5 mL/min。达到吸附平衡后,使用40%(体积分数)乙醇溶液以1.5 mL/min流速洗脱树脂。最后,采用旋转蒸发仪在55 ℃下蒸发洗脱液中的乙醇,得到棕色洗脱液。对棕色洗脱液进一步进行超滤分离,分离后的酱油类黑精依据分子质量大小,主要分为1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa和>50 kDa 5个组分。经定量测定,各组分在酱油中的含量依次为:(0.31±0.07)、(0.42±0.09)、(0.20±0.05)、(0.61±0.10)、(0.90±0.13) g/100 mL酱油。将分离纯化所得各组分类黑精冻干保存(低温),以备后续实验使用。
1.3.3 不同分子质量类黑精的物理特性
1.3.3.1 微观结构
使用扫描电镜揭示生物大分子表面形貌的微观结构[18]。将冻干的类黑精样品均匀分散于导电胶上,经喷金处理后,在15 kV的加速电压下观察类黑精微观结构形态。
1.3.3.2 粒径测定
使用激光粒度分析仪测定类黑精的粒径分布[19]。配制1 mg/mL的类黑精溶液,使用激光粒度分析仪测定粒径分布,平均粒径(Davg)及多分散指数(polydispersity index, PDI)的计算如公式(3)和公式(4)所示:
(3)
(4)
式中:Di,第i个粒径区间中值,Ni,对应颗粒数。
1.3.3.3 Zeta电位测定
Zeta电位检测用于评估类黑精的结构稳定性[20]。类黑精溶液(1 mg/mL)经超声波均质后,使用zeta电位分析仪于25 ℃下测定zeta电位,按公式(5)计算:
zeta电位![]()
(5)
式中:f(λ),电泳迁移率,μm2/Vs;ε,溶剂的介电常数,F/m;λ,Debye长度,nm。
1.3.3.4 热稳定性分析
使用DSC检测类黑精的热稳定性[21]。称取2.0 mg的类黑精冻干样品置于铝坩埚中,以10 ℃/min速率升温(30~480 ℃),记录热流曲线并分析变性温度(Tonset、Tpeak)及热焓值(ΔH)。
1.3.4 不同分子质量类黑精的色泽测定
采用分光测色仪测定不同分子质量类黑精组分(1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa、>50 kDa)溶液(1 mg/mL)的色度参数(L*、a*、b*),总色差(ΔE)的计算如公式(6)所示:
(6)
1.3.5 不同分子质量类黑精对酱油色泽的贡献
1.3.5.1 类黑精溶液的制备
根据酱油中不同分子质量类黑精组分(1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa和50 kDa以上)的实际含量(见1.3.2节),将冻干的类黑精样品溶解于180 g/L盐水中,定容至100 mL,制得类黑精溶液。
1.3.5.2 类黑精对酱油色泽的定量贡献
按1.3.4节方法测定类黑精溶液及酱油的色度参数(ΔE),各分子质量组分的色泽贡献率(Wi)的计算如公式(7)所示:
(7)
式中:Mi,类黑精组分(i=1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa、>50 kDa)的ΔE值;N1,酱油原液的ΔE值。
1.4 数据处理
所有实验重复3次,数据以“平均值±标准差”表示。用Origin 2021作图,采用SPSS 27.0进行单因素方差分析(ANOVA),以P<0.05为显著性差异。
2 结果与讨论
2.1 大孔树脂纯化类黑精
类黑精的高效分离纯化是研究其物理性质及功能特性的关键。本研究对比了非极性(D101)、弱极性(AB-8)以及极性(DA201-E)大孔树脂对酱油类黑精的吸附和解吸特性。如图1-a所示,3种树脂的吸附率随时间的增加均呈现先快速吸附后平衡的趋势。其中,在前30 min内,DA201-E型树脂(极性)吸附速率较高,其吸附率为85%,在120 min时趋于稳定,其平衡吸附率为92.24%,显著高于AB-8(81.36%)和D101(73.52%)(P<0.05)。这一结果表明,酱油类黑精中富含极性基团(如羧基、氨基等),与极性树脂表面官能团之间可能存在较强的氢键或静电相互作用[17]。乙醇浓度对解吸效率的影响进一步验证了类黑精的极性特性(图1-b)。在40%乙醇中,DA201-E树脂的解吸率78.10%,而AB-8和D101则需要更高浓度的乙醇(60%)才能达到最佳解吸率,分别为69.31%、66.32%。这是因为高极性类黑精在低浓度乙醇中,可通过调节溶剂极性来削弱树脂的吸附作用;而当乙醇体积分数>60%时,类黑精溶解度降低,致使解吸效率下降。该结果与酱油及黑酒类黑精纯化的研究结果一致[15,22]。上述结果表明,采用DA201-E极性大孔吸附树脂纯化酱油中类黑精效果最佳。
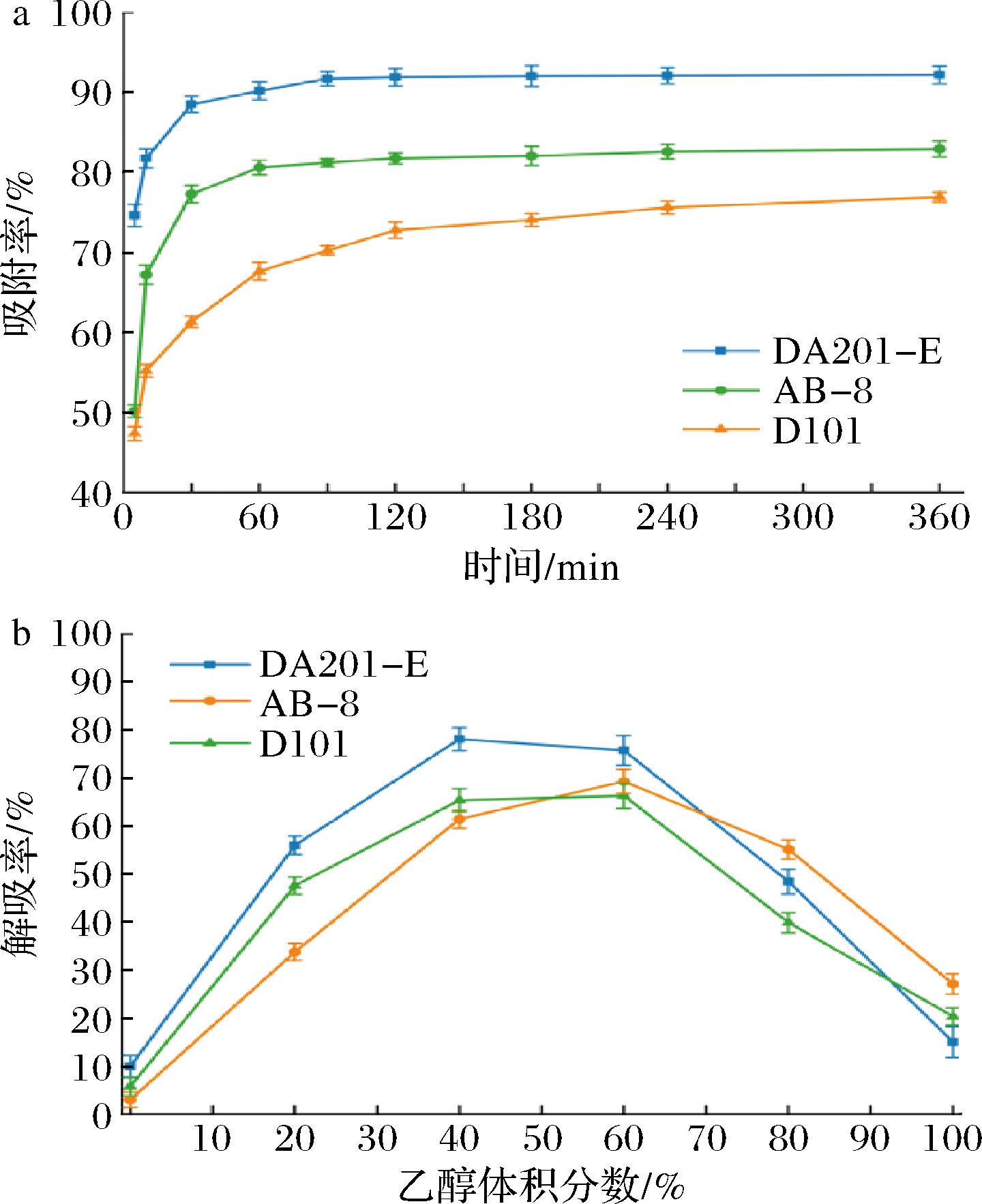
a-静态吸附;b-静态解吸
图1 不同类型树脂对酱油类黑精的静态吸附和解吸曲线
Fig.1 Static absorption curve and desorption curves of different types of resins for soy sauce melanoidins
2.2 微观结构分析
如图2所示,5种酱油类黑精组分微观结构均呈现出丰富的多样性,形态包括球形、层状以及不规则形状,其表面显著的多孔特征为美拉德反应的发生提供了良好的条件[22]。具体而言,1~3 kDa组分呈现出较小且不规则的碎片状结构,这是因为其分子质量较低,分子间交联作用较弱。相比之下,10~30 kDa组分类黑精分散较为均匀,颗粒细密且相对独立。这种结构特性有利于光线在酱油中均匀散射,从而对酱油色泽的均匀性以及光学特性的形成起到积极的促进作用。然而,30~50 kDa和>50 kDa组分的类黑精则展现出较高的分子聚合程度,形成了明显的团聚体结构,这与WANG等[7]对啤酒类黑精的研究结果相符。随着分子质量的增大,分子间的空间位阻效应致使光线发生强烈的漫反射与非均匀散射,这会致使类黑精颜色过深且偏暗,严重干扰酱油中类黑精色泽均匀性的呈现以及理想色调的达成。综上所述,类黑精的分子质量与微观结构特征紧密相关,进而影响其在酱油中的溶解性与分散性,最终对产品的色泽均匀性和质量产生重要作用。

A,a-1~3 kDa组分;B,b-3~10 kDa组分;C,c-10~30 kDa组分;D,d-30~50 kDa组分;E,e->50 kDa组分
图2 不同分子质量类黑精的扫描电镜图
Fig.2 Scanning electric microscope image of melanoidins with different molecular weight
2.3 粒径分析
如表1可知,类黑精的分子质量与平均粒径之间存在显著的正相关关系(P<0.05)。其中,中低分子质量组分(1~30 kDa)的平均粒径范围为650.37~981.89 nm,明显低于高分子质量组分的1 283.87~1 338.33 nm。这种粒径差异主要归因于分子质量不同所引发的结构变化。高分子质量组分借助范德华力和氢键,构建起紧密的交联网络,极大地增强了分子间的聚合程度。DING等[18]对莲花根茎类黑精的研究也发现,中低分子质量组分由于分子链较短,分子间相互作用较弱,所以在溶液中展现出更优异的分散性能。尤其是10~30 kDa组分的PDI值最低,仅为19.22%,且粒径适中(981.89 nm),能够形成高度均一的分散相(2.2节)。相较而言,高分子质量组分(>50 kDa)由于分子内交联程度较高,形成了较大的粒径,且PDI值高达40.98%。在酱油体系中,较大的粒径和高PDI值使得分子间极易发生空间位阻效应[23]。这种效应阻碍了分子的自由运动,促使颗粒相互靠近并发生团聚(2.2节)。颗粒发生团聚现象后,光线传播路径受到阻碍,酱油的透光率显著降低,进而呈现出浑浊状态。与此同时,团聚区域内类黑精浓度急剧升高,引发局部色泽深度增加[4],可能破坏酱油整体色泽的均一性。
表1 不同分子质量类黑精的粒径分布
Table 1 Particle size distribution of melanoidins with different molecular weight
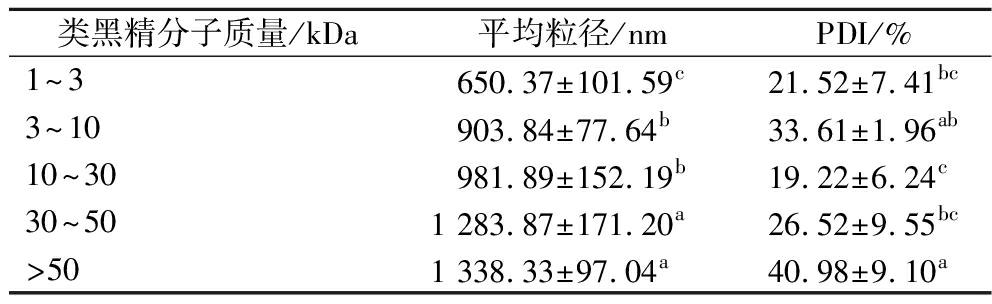
类黑精分子质量/kDa平均粒径/nmPDI/%1~3650.37±101.59c21.52±7.41bc3~10 903.84±77.64b33.61±1.96ab10~30981.89±152.19b19.22±6.24c30~501 283.87±171.20a26.52±9.55bc>501 338.33±97.04a40.98±9.10a
注:同列不同小写字母表示差异显著(P<0.05)(下同)。
2.4 Zeta电位分析
如图3所示,酱油类黑精的zeta电位绝对值随分子质量增加呈显著递增趋势(P<0.05)。1~3 kDa低分子质量组分的zeta电位绝对值为17.82 mV,显著低于10~30 kDa(20.52 mV)、30~50 kDa(21.02 mV)以及>50 kDa(23.00 mV)组分,这种差异与类黑精的复杂分子结构紧密相关。由于低分子质量类黑精较为简单的支链结构和表面带电基团(如羧基、氨基)暴露不足,导致电荷密度较低,进而削弱了静电稳定效应[23]。相反,中高分子质量组分(>10 kDa)在美拉德反应后期,通过缩合与交联作用,形成了复杂的三维结构。值得注意的是,所有组分的zeta电位绝对值均比醋中类黑精(11.13~16.17 mV)高[19],这一结果表明酱油类黑精具有更为优异的分散稳定性。此外,在美拉德反应过程中,低分子物质或中间产物的重排、异构化、缩合及聚合反应可能促使高分子质量组分的形成[10]。这些反应使得分子结构更加复杂,增加了分子间的相互作用和空间位阻,进而提升了体系的稳定性。当分子质量>10 kDa时,zeta电位绝对值均大于20 mV,且随着分子质量的增加,类黑精表面的负电荷逐渐增多,静电排斥作用随之增强,从而提高了分散体系的稳定性。这一结果与其他黑精体系(如白酒和结晶麦芽中的类黑精)中的发现相似[23-24]。
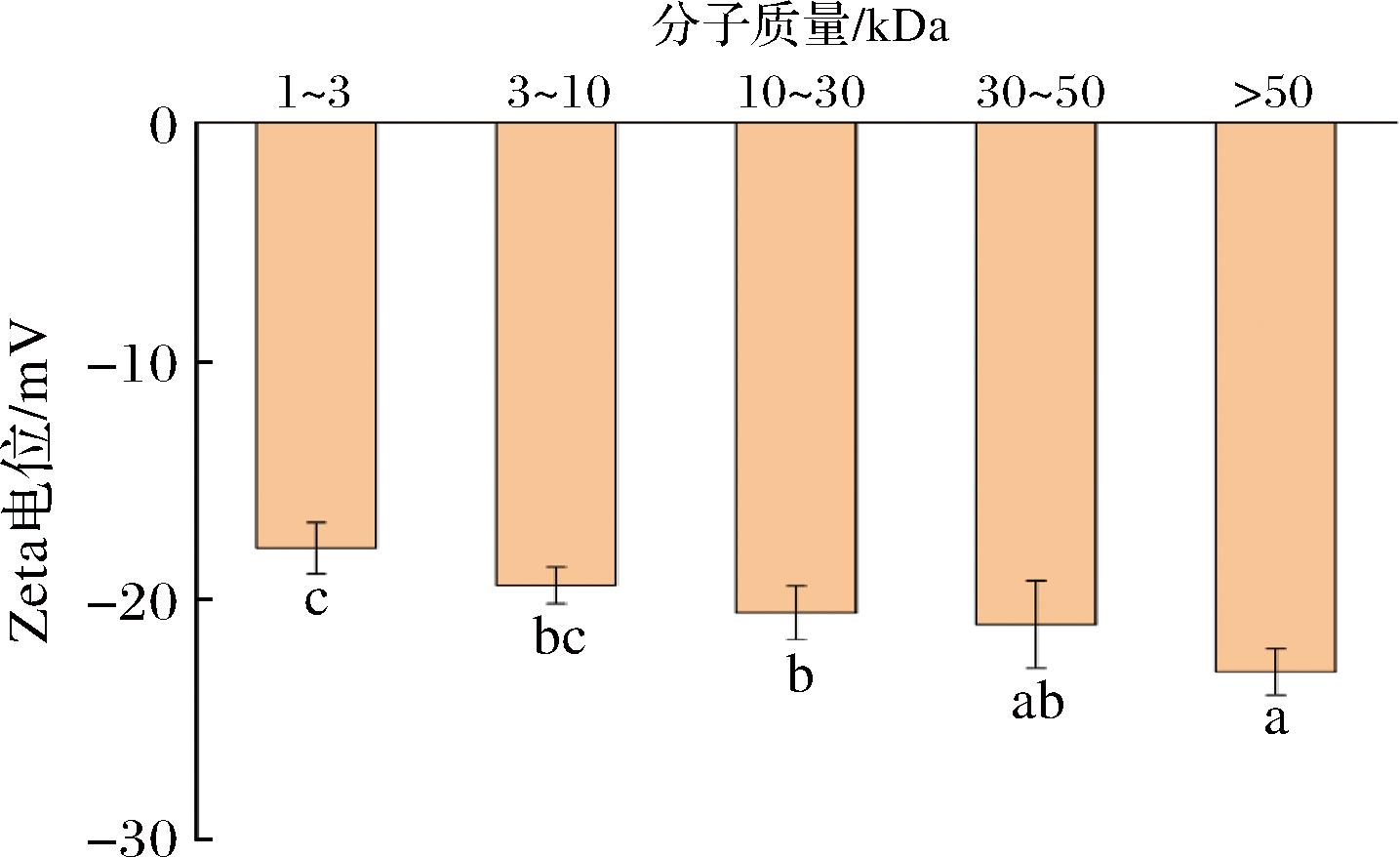
图3 不同分子质量类黑精的zeta电位
Fig.3 Zeta-potential of melanoidins with different molecular weight
注:不同小写字母表示差异显著(P<0.05)。
2.5 DSC分析
DSC分析揭示了类黑精的热稳定性及热解特性(图4)。在30~300 ℃的温度范围内,所有类黑精组分均表现出较宽的吸热峰,这可能是由于类黑精侧链的脱水及其结构的丧失[22]。各组分热分解起始温度(onset)与峰值温度(peak)随分子质量增大递增,表明高分子质量类黑精热稳定性更优,这主要归因于其复杂的结构、分子间交联致密及作用力增强。对于10~30 kDa组分,热解温度表现较为特殊,具有2个热解峰,分别为357.41 ℃和453.09 ℃,均高于30~50 kDa组分(356.80 ℃和449.66 ℃)以及>50 kDa组分(355.80 ℃和451.10 ℃)。这表明10~30 kDa组分的类黑精分子内部结构更加有序和稳定,受热时需要吸收更多的能量来打破分子内部的化学键,从而引发热解,导致热解温度升高[25]。10~30 kDa组分热解特性呈现出相对稳定且均匀的特征,使其能均匀地分散在酱油体系中,有助于光线与分子的有效相互作用,这与2.2节微观结构分析和2.3节粒径分析结果相呼应。相反,高分子质量组分(>30 kDa)虽然具有较高的起始温度和峰值温度,但由于分子间聚合程度过高、相互作用复杂强烈,受热时容易形成局部应力集中点,从而导致分子在相对较低温度下发生不规则的解聚和分解,这在啤酒类黑精中也有类似发现[4]。
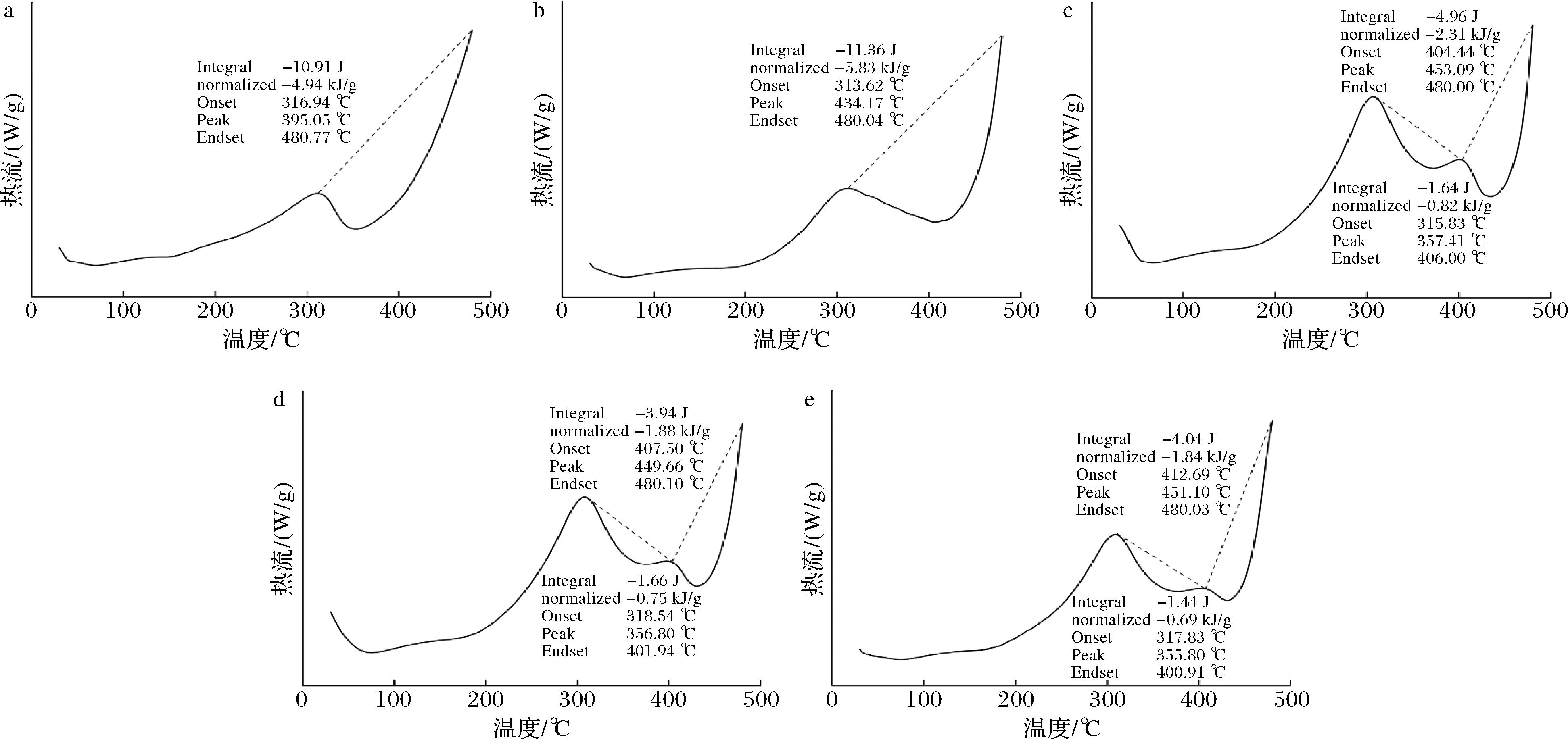
a-1~3 kDa组分;b-3~10 kDa组分;c-10~30 kDa组分;d-30~50 kDa组分;e->50 kDa组分
图4 不同分子质量类黑精的DSC分析曲线
Fig.4 DSC curve of melanoidins with different molecular weight
热解焓用于衡量物质发生变性时所需的热量,反映其分子展开的难易程度[21]。3~10 kDa类黑精的积分热解焓(integral)为-11.36 J,归一化热解焓(normalized)为-5.83 kJ/g,其热焓绝对值相对较大,这可能是因为其热转变过程相对单一,需要较多能量破坏分子内相互作用,致使能量变化显著。而>10 kDa类黑精组分的归一化热焓值相对较小,这可能与双峰的存在有关,热反应较为复杂,且可能受到杂质的影响,不同阶段的热焓相互作用使得归一化热焓值较小,这与黑蒜类黑精及饼干类黑精的DSC研究结果一致[25-26],表明不同食物来源的类黑精在热力学性质上具有一定的相似性。然而,目前关于真实食品体系中类黑精热力学性质的研究文献较为有限,未来还需进一步研究不同来源的类黑精,以深入了解类黑精的热力学性质。
2.6 类黑精的色度分析
本研究通过测定不同分子质量类黑精组分的色度参数,定量分析了其色泽表现。为了确保分析结果的可比性,所有类黑精组分均在相同浓度下配制。不同分子质量(1~3 kDa、3~10 kDa、10~30 kDa、30~50 kDa、>50 kDa)的酱油类黑精溶液(1 mg/mL)如图5所示。

图5 不同分子质量的酱油类黑精溶液
Fig.5 Soy sauce melanoidins solutions of different molecular weights
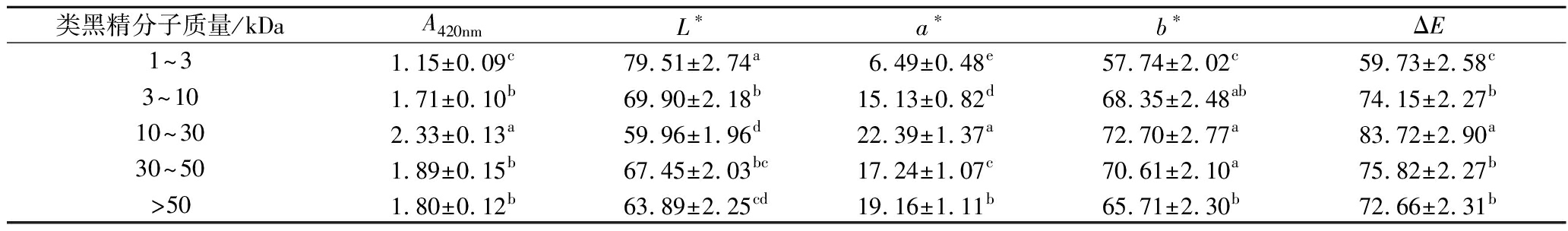
美拉德反应终产物(类黑精)在A420nm处有强烈的吸收,通常用于表示类黑精中发色团的含量[2]。表2数据显示,A420nm的吸光度值随着分子质量的变化呈现先上升后下降的趋势。具体而言,10~30 kDa组分的A420nm值最高(2.33),显著高于其他组分(P<0.05)。这可能是因为该组分分子聚合程度适度,形成了较多能有效吸收特定波长光的共轭体系,进而具有较高的A420nm吸光度值[3,27]。相比之下,30~50 kDa组分和>50 kDa组分由于较大的分子质量,可能发生过度聚合和交联,导致共轭体系的结构扭曲或破坏,进而降低了其光吸收能力。此外,较大的分子质量(>30 kDa)可能促使团聚体的形成,进一步减少了有效共轭结构的暴露,导致吸光度的下降[7]。1~3 kDa组分的A420nm值最低(1.15),由于其分子质量较小,美拉德反应未完全进行,因此表现出较浅的颜色,这与莲花根茎类黑精的研究结果一致[18]。
表2 不同分子质量类黑精的色泽
Table 2 Color of melanoidins with different molecular weight
类黑精分子质量/kDaA420nmL∗a∗b∗ΔE1~31.15±0.09c79.51±2.74a6.49±0.48e57.74±2.02c59.73±2.58c3~101.71±0.10b69.90±2.18b15.13±0.82d68.35±2.48ab74.15±2.27b10~302.33±0.13a59.96±1.96d22.39±1.37a72.70±2.77a83.72±2.90a30~501.89±0.15b67.45±2.03bc17.24±1.07c70.61±2.10a75.82±2.27b>501.80±0.12b63.89±2.25cd19.16±1.11b65.71±2.30b72.66±2.31b
在酱油发酵过程中,高温和较长的发酵时间促进了类黑精内部结构的交联与延伸,进而促进构建更复杂的结构,并促进了有色物质的生成[2]。类黑精的颜色可通过色度参数(L*、a*、b*)及色差指数(ΔE)进行定量评估[27]。随着分子质量的增加,类黑精的色泽逐渐从黄色转变为红黄色调。1~3 kDa组分的L*值最高(79.51),呈现明亮的黄色,而10~30 kDa组分的L*值最低(59.96),表现为较深的颜色。1~3 kDa组分的a*值较低,表明红色成分较少,b*值较高,呈现较强的黄色调,这与SATOH等[5]的研究结果一致。相比之下,10~30 kDa组分的a*值较高(22.39),表现出较强的红色调,同时b*值也较高(72.70),形成了明显的红黄色混合色调。这是这可能是由于10~30 kDa组分的分子结构相对稳定,使其能够在酱油体系中较为均匀地分散,进而使光线能够更有效地与分子作用,这与DSC分析结果相符。结合2.3节的分析,30~50 kDa组分和>50 kDa组分的PDI值较高,容易在酱油中形成大小不一的团聚体,导致光线散射不均匀,部分光线被团聚体遮挡,进而降低了亮度L*值,同时影响了a*和b*值,使得整体色度参数低于10~30 kDa组分[4]。色差指数(ΔE)进一步验证了不同组分间色泽的差异。1~3 kDa组分的ΔE值最低(59.73),呈现较为清亮的颜色;而10~30 kDa组分的ΔE值最高(83.72),表明其色泽差异显著且较为浓烈,是酱油类黑精单位色泽的主要贡献者。综上,低分子质量类黑精组分(<10 kDa)主要呈现的色泽以黄色为主,而高分子质量组分(>10 kDa)则呈现红黄混合色[3]。10~30 kDa组分凭借较高的A420nm值和ΔE值,成为酱油类黑精色泽的关键贡献者。
2.7 类黑精对酱油色泽的贡献
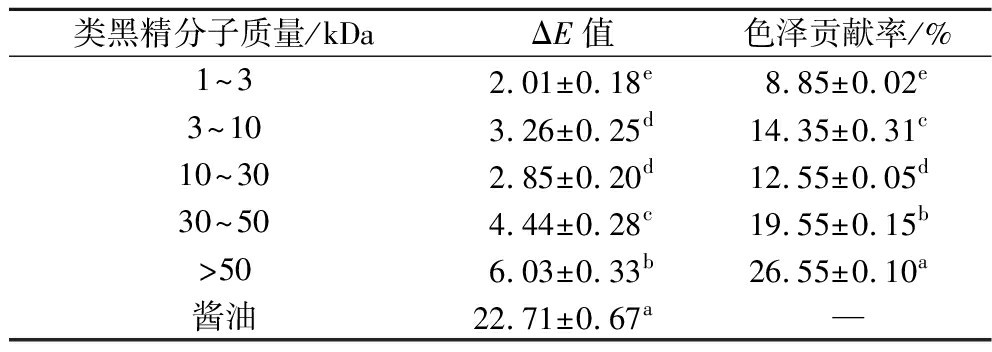
酱油的独特色泽是其感官品质的重要指标,类黑精是决定酱油色泽的关键物质[10]。本研究结果表明,类黑精的分子质量分布及其在酱油中的实际含量共同决定了其对色泽贡献的权重(表3)。
表3 不同分子质量类黑精对酱油色泽的贡献
Table 3 Contribution of melanoidins with different molecular weight to the color of soy sauce
类黑精分子质量/kDaΔE值色泽贡献率/%1~32.01±0.18e8.85±0.02e3~103.26±0.25d14.35±0.31c10~302.85±0.20d12.55±0.05d30~504.44±0.28c19.55±0.15b>506.03±0.33b26.55±0.10a酱油22.71±0.67a—
如表3所示,不同分子质量的类黑精对酱油色泽的贡献存在显著差异(P<0.05)。结果表明(2.6节),在相同浓度下,10~30 kDa组分具有最高的A420nm吸光度值(2.33)和ΔE值(83.72),但由于其在酱油中的实际含量较低,其对整体色泽的贡献仅为12.55%。相比之下,>50 kDa组分的ΔE值(6.03)低于10~30 kDa组分,然而由于其在酱油中的实际含量最高,对色泽的贡献占比达到26.55%,成为酱油色泽的主要贡献者。这主要归因于在酱油发酵进程中,长时间的高温条件极大地促进了高分子质量类黑精的积累[28]。此外,30~50 kDa组分的贡献(19.55%)仅次于>50 kDa组分,表明中高分子质量类黑精组分(>30 kDa)的协同作用对酱油红黄色的呈现至关重要。值得注意的是,低分子质量类黑精(1~10 kDa)尽管色度表现较浅(ΔE值2.01~3.26),其贡献总和(23.20%)不可忽视,尤其在提供基础黄色(高b*值)起到了补充作用。然而,高分子质量组分(>30 kDa)的过度聚合可能引发团聚效应,进而导致光散射增强、L*值降低,从而影响色泽的均匀性[18]。这一结论与粒径分析及色度分析的结果相一致。此外,所有分子质量组分的ΔE值总和(18.59)低于酱油的ΔE值(22.71)。这表明,除类黑精外,酱油色泽的形成可能还涉及多酚氧化产物、焦糖色素等非类黑精物质的协同作用,或者分子间的相互作用对色泽的增强效应[10]。
综上所述,酱油色泽的形成是不同分子质量类黑精组分协同作用的结果。尽管中分子质量类黑精(10~30 kDa)具有最强的单位呈色能力,但由于高分子质量组分(>30 kDa)在酱油中的实际含量较高,其成为色泽贡献的主体。
3 结论
本研究系统分析了不同分子质量类黑精组分对酱油色泽的贡献,揭示了类黑精分子质量与其微观结构、粒径、zeta电位、热稳定性及色度等性质之间的内在关联。10~30 kDa的类黑精单位呈色能力上最强。然而,由于>50 kDa的类黑精在酱油中的实际含量高,是酱油色泽的主要贡献者,30~50 kDa的类黑精贡献次之。尽管低分子质量类黑精(1~10 kDa)呈色能力弱,但对酱油色泽的贡献也达到23.20%,对酱油黄色的形成发挥了补充作用。该研究为酱油色泽调控提供了重要的理论依据,通过精确控制发酵时间和温度,优化类黑精的分子质量分布,可以实现酱油色泽品质的定向提升,为酱油行业的高质量发展提供坚实支持。
[1] GAO X L, CUI C, REN J Y, et al.Changes in the chemical composition of traditional Chinese-type soy sauce at different stages of manufacture and its relation to taste[J].International Journal of Food Science &Technology, 2011, 46(2):243-249.
[2] GAO X L, LIU E M, ZHANG J K, et al.Effects of sonication during moromi fermentation on antioxidant activities of compounds in raw soy sauce[J].LWT, 2019, 116:108605.
[3] 李丹, 崔春, 赵谋明.高盐稀态酱油酿造过程中的色泽变化[J].食品与发酵工业, 2010, 36(4):75-79.
LI D, CUI C, ZHAO M M.Study on the changes of color during the fermentation of high-salt diluted soy sauce[J].Food and Fermentation Industries, 2010, 36(4):75-79.
[4] ZHAO Y M, DING Y F, WANG D F, et al.Effect of high hydrostatic pressure conditions on the composition, morphology, rheology, thermal behavior, color, and stability of black garlic melanoidins[J].Food Chemistry, 2021, 337:127790.
[5] SATOH M, NOMI Y, YAMADA S, et al.Identification of 2, 4-dihydroxy-2, 5-dimethyl-3(2H)-thiophenone as a low-molecular-weight yellow pigment in soy sauce[J].Bioscience, Biotechnology, and Biochemistry, 2011, 75(7):1240-1244.
[6] GAO X L, ZHAO X, HU F, et al.The latest advances on soy sauce research in the past decade:Emphasis on the advances in China[J].Food Research International, 2023, 173:113407.
[7] WANG H Y, QIAN H, YAO W R.Melanoidins produced by the Maillard reaction:Structure and biological activity[J].Food Chemistry, 2011, 128(3):573-584.
[8] MES AS M, DELGADO-ANDRADE C.Melanoidins as a potential functional food ingredient[J].Current Opinion in Food Science, 2017, 14:37-42.
AS M, DELGADO-ANDRADE C.Melanoidins as a potential functional food ingredient[J].Current Opinion in Food Science, 2017, 14:37-42.
[9] ORACZ J, LEWANDOWSKA U, OWCZAREK K, et al.Isolation, structural characterization and biological activity evaluation of melanoidins from thermally processed cocoa beans, carob kibbles and acorns as potential cytotoxic agents[J].Food Chemistry, 2024, 442:138423.
[10] YANG S Q, FAN W L, XU Y.Melanoidins present in traditional fermented foods and beverages[J].Comprehensive Reviews in Food Science and Food Safety, 2022, 21(5):4164-4188.
[11] LANGNER E, RZESKI W.Biological properties of melanoidins:A review[J].International Journal of Food Properties, 2014, 17(2):344-353.
[12] WANG K T, LI Y W, BIAN X J, et al.In vitro simulated digestive properties of Monascus vinegar melanoidins, and cytoprotective functions on Caco-2 cells[J].Food Research International, 2025, 202:115720.
[13] HU J X, BI J F, WANG W Y, et al.Comparison of characterization and composition of melanoidins from three different dried apple slices[J].Food Chemistry, 2024, 455:139890.
[14] XIA T, DUAN W H, ZHANG Z J, et al.Polyphenol-rich vinegar extract regulates intestinal microbiota and immunity and prevents alcohol-induced inflammation in mice[J].Food Research International, 2021, 140:110064.
[15] ZHUANG M Z, ZHAO M M, LIN L Z, et al.Macroporous resin purification of peptides with umami taste from soy sauce[J].Food Chemistry, 2016, 190:338-344.
[16] 秦礼康, 丁霄霖.陈窖豆豉粑类黑精提取及骨架肽段氨基酸组成分析[J].食品科学, 2006, 27(1):125-129.
QIN L K, DING X L.Extractions of melanoidins in the long- ripenned douchiba(DCB) and analyses of amino acid compositions in its peptide skeltons[J].Food Science, 2006, 27(1):125-129.
[17] YANG H R, ZONG X Y, CUI C, et al.Wheat gluten hydrolysates separated by macroporous resins enhance the stress tolerance in brewer’s yeast[J].Food Chemistry, 2018, 268:162-170.
[18] DING X F, ZHANG Y B, LI J, et al.Structure, spectral properties and antioxidant activity of melanoidins extracted from high temperature sterilized lotus rhizome juice[J].International Journal of Biological Macromolecules, 2024, 270:132171.
[19] WANG K T, TANG N, BIAN X J, et al.Structural characteristics, chemical compositions and antioxidant activity of melanoidins during the traditional brewing of Monascus vinegar[J].LWT, 2024, 209:116760.
[20] WANG Z S, ZHANG Z J, LI S P, et al.Formation mechanisms and characterisation of the typical polymers in melanoidins from vinegar, coffee and model experiments[J].Food Chemistry, 2021, 355:129444.
[21] ZHANG C, LI X Y, LI J J, et al.The dynamic changes in physicochemical properties, functionalities, and gel properties of the starch-konjac gum mixture during the melting process:Based on three typical melting temperatures of DSC[J].Food Hydrocolloids, 2025, 158:110495.
[22] ZHANG Q H, CHEN M T, EMILIA COLDEA T, et al.Structure, chemical stability and antioxidant activity of melanoidins extracted from dark beer by acetone precipitation and macroporous resin adsorption[J].Food Research International, 2023, 164:112045.
[23] YANG S Q, FAN W L, NIE Y, et al.The formation and structural characteristics of melanoidins from fermenting and distilled grains of Chinese liquor (Baijiu)[J].Food Chemistry, 2023, 410:135372.
[24] 李存. 结晶麦芽美拉德反应产物的初步研究[D].无锡:江南大学, 2022.
LI C.Preliminary study on Maillard reaction products of crystalline malt[D].Wuxi:Jiangnan University, 2022.
[25] 吴剑夫. 黑蒜类黑精结构鉴定及生物活性研究[D].天津:天津科技大学, 2021.
WU J F.Structure identification and bioactivity of black garlic melanoidin[D].Tianjin:Tianjin University of Science and Technology, 2021.
[26] PATRIGNANI M, DEL SOL GONZ LEZ-FORTE L, RUFI
LEZ-FORTE L, RUFI N-HENARES J
N-HENARES J  , et al.Elucidating the structure of melanoidins derived from biscuits:A preliminary study[J].Food Chemistry, 2023, 419:136082.
, et al.Elucidating the structure of melanoidins derived from biscuits:A preliminary study[J].Food Chemistry, 2023, 419:136082.
[27] YANG H R, ZHANG Q H, ZENG Y J, et al.Differences in structure, stability and antioxidant activity of melanoidins from lager and ale beers[J].LWT, 2024, 205:116517.
[28] GAO X L, LIU E M, ZHANG J K, et al.Accelerating aroma formation of raw soy sauce using low intensity sonication[J].Food Chemistry, 2020, 329:127118.