食品中挥发性气味成分在风味构建、品质感知和消费体验中发挥着至关重要的作用[1]。这些气味物质种类繁多,化学结构多样,广泛来源于原料成分的热反应、酶促降解、微生物代谢及氧化过程,是食品加工、贮藏和发酵等环节中形成风味特征的重要基础[2-3]。不同结构的挥发性分子对应不同的感官特性与气味描述,但其结构特征如何影响与人体感官系统之间的相互作用,仍有待深入研究[4-5]。
目前,人类嗅觉系统通过嗅觉受体(olfactory receptors, ORs)识别挥发性气味分子,完成气味的初级感知[6]。ORs隶属于G蛋白偶联受体(G protein-coupled receptors, GPCRs)家族[7],是膜蛋白中结构多样性最高的一类[8],已知人类具有约400种功能性OR受体,可识别成千上万种结构各异的气味分子[9]。然而,由于OR蛋白的实验解析难度较大,气味分子与OR蛋白之间的结合机制在分子层面尚未完全阐明[10]。因此,如何深入了解不同气味分子与嗅觉受体的相互作用,尤其是结构特征对识别模式的影响,仍是一个亟待解决的问题[11]。近年来,随着蛋白结构预测技术和分子模拟方法的发展,分子对接与分子动力学模拟逐渐成为研究气味分子-OR蛋白相互作用的有效手段[12-13]。通过构建配体-受体复合物并模拟其在时间维度上的动态行为,可以深入揭示气味分子在结合位点的构象适配性、相互作用类型及稳定性特征,为理解嗅觉识别过程提供可靠的理论支持[14-15]。将该方法应用于食品科学领域,可从分子层面探索风味成分的识别规律,并为人工嗅觉系统与风味预测模型提供结构基础。
研究前期通过机器学习方法,结合分子描述符与感官评测数据,成功建立了食品挥发性气味分子的分类预测模型。该模型将食品中常见的气味分子分为3类:清新果香类(以醛类为代表)、复杂浓郁类(以酚类为代表)和刺激不良性气味类(以含硫醇/醇/硫醚类化合物为代表)。这些分类结果为深入探讨气味分子与嗅觉受体之间的相互作用提供了重要基础。然而,目前的模型仅揭示了气味的宏观分类特征,尚未深入探讨不同类别气味分子在分子层面与嗅觉受体的结合机制。
因此,本研究基于前期分类模型的预测结果,选择了食品中典型的挥发性气味功能团,进一步筛选出每类中的代表性分子。通过分子对接与分子动力学模拟,研究其与人类嗅觉受体(OR2W1、OR10K1、OR10S1)的结合模式与识别机制。本研究旨在从分子结构的角度,揭示不同气味功能团在嗅觉受体识别中的差异性,为食品气味的感知机制提供理论基础,并为人工嗅觉系统的设计与风味调控提供指导。
1 材料与方法
1.1 嗅觉受体蛋白与配体的选择与预处理
本研究从前期构建的气味分类模型中筛选出得分靠前的代表性化合物,采用的气味分类模型是一种基于机器学习算法构建的预测模型,以分子结构特征为输入、气味感官描述为输出,通过随机森林与梯度提升决策树等算法建立结构-感官关系的分类预测模型。模型评价采用准确率、精确率、召回率和F1分数等多项指标进行综合评分。得分靠前的分子意味着模型能准确且稳定地识别其结构特征与感官描述的关系,因此具有典型代表性。本研究即基于此原则选择了模型中评分较高的化合物,用于进一步的分子对接和分子动力学模拟,以确保研究对象的典型性和代表性。这一操作的目的是探索模型的分类偏好,通过分子对接与分子动力学模拟探索模型分类的气味分子在嗅觉受体上的表现差异。由于不同气味分子能够结合的嗅觉受体蛋白不同,所以选择较为常见且有实验验证过的嗅觉受体OR2W1[16]、OR10K1[17]、OR10S1[18]作为化合物的受体蛋白。从AlphaFold数据库获取嗅觉受体蛋白结构(UniProt ID:OR2W1-Q9Y3N9;OR10K1-Q8NGX5;OR10S1-Q8NGN2),并使用AMBER软件(Version-20, University of California, USA)对受体进行预处理,包括去除水分子、添加氢原子、修复缺失的残基以及能量最小化。配体分子的三维结构从PubChem数据库根据其SMILES(simplified molecular input line entry system)字符串生成。
1.2 分子对接
使用AutoDock 4.2.6(The Scripps Research Institute, USA)对配体分子进行预处理,包括添加电荷、识别可旋转键以及分配非极性氢原子。通过加氢和加水对OR及配体小分子进行预处理,并导出为Pdbqt格式文件。利用AutoGrid程序在受体蛋白周围创建涵盖整个蛋白的网格盒子,所有其他参数均使用默认值。分子对接计算采用拉马克遗传算法(lamarckian genetic algorithm, LGA),运行次数设定为250 000次,并根据预测的停靠口袋坐标选择最合理的构象。随后,将对接获得的OR和配体构象文件联合导入PyMol 3.0.5(Schrödinger, USA)进行可视化,并导出Pdbqt文件。结合LigPlot+2.2(European bioinformatics institute, UK)分析结合机制,并生成2D交互图,以直观展示蛋白质与配体的相互作用[19-20]。
1.3 分子动力学模拟
使用GROMACS(Version-linux 2022)进行模拟,力场选择CHARMM36,蛋白质拓扑文件通过GROMACS的pdb2 gmx工具生成,配体拓扑和参数文件使用CGenFF工具处理获得。使用简单点电荷水分子模型构建整个系统,并将复合物放置在三斜晶系盒中,设置分子与盒边界的最小距离为1.0 nm。为确保系统的电中性,同时加入了0.15 mol/L的NaCl以模拟生理环境。首先通过最陡峭下降法进行了5 000步的能量最小化,以消除初始结构中的不合理接触。随后,系统在300 K的恒温条件下进行了NVT(number of particles-volume-temperature)系综模拟(100 ps),通过Berendsen温度耦合器逐渐升温,同时维持恒体积。接着在NPT(number of particles-pressure-temperature)(100 ps)阶段,通过Parrinello-Rahman压力耦合器将系统压强调整到1 bar,并允许盒子体积自由变化,以实现等压平衡。随后运行100 ns的生产性分子动力学模拟,生成了大约100 000帧的轨迹文件,用于后续分析。轨迹分析包括系统的均方根偏差(root mean square deviation, RMSD)、均方根波动(root mean square fluctuation, RMSF)、回转半径(radius of gyration, Rg)、氢键数量的动态变化及主成分分析(principal components analysis, PCA)等[21-24]。
2 结果与分析
2.1 分子对接结果分析
根据理论计算,3种醛类气味分子(清新果香类)[反式-2-壬烯醛,反式,反式-2,4-壬二烯醛,(2E,4E)-癸-2,4-二烯醛]的结合能依次为-4.9、-4.8、-5.0 kcal/mol,结合能的差异体现了配体官能团的结构和极性特征对于受体识别效率的直接影响。对接结果如图1所示,结合模式受结合口袋的几何构型与电荷分布共同影响。反式-2-壬烯醛结合于较开阔的口袋,通过与Ser217形成氢键(2.87 Å),并与Tyr120、Leu213等形成疏水作用,体现出极性与疏水协同结合特征。(2E,4E)-癸-2,4-二烯醛结合位点更紧凑,形成稳定氢键(3.07 Å)并嵌入疏水核心区域,嵌合度最高,结合能最低,显示出与受体良好的结构匹配性。反式,反式-2,4-壬二烯醛则嵌入以疏水性为主的腔体中,主要通过与Tyr120、Phe123等残基的疏水作用实现结合,缺乏稳定的氢键支持,整体结合以疏水驱动为主。
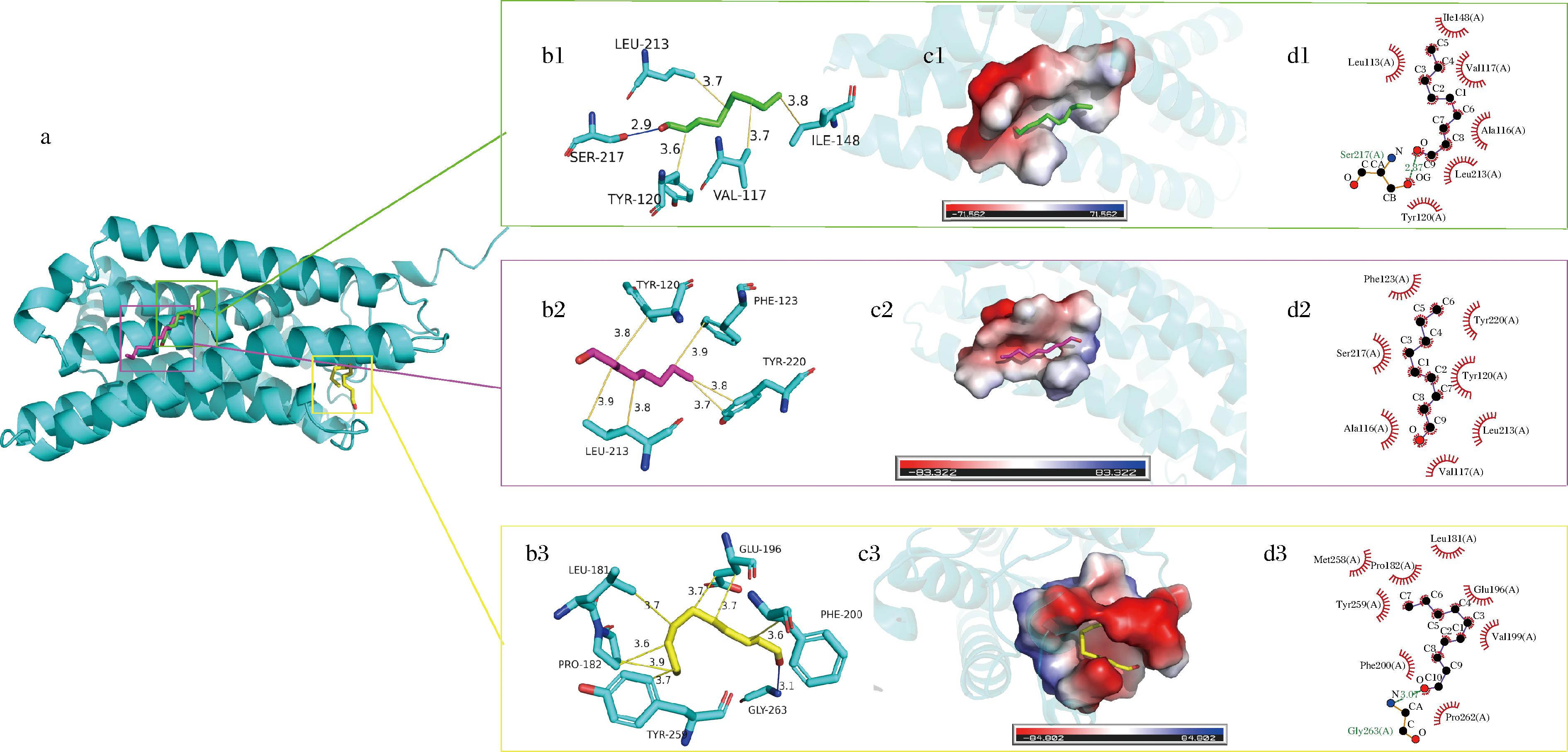
a-3种配体(反式-2-壬烯醛,绿色;反式,反式-2,4-壬二烯醛,紫色;(2E,4E)-癸-2,4-二烯醛,黄色)在结合口袋中的构象;b-与4.00 Å范围内残基的三维相互作用(蓝色为氢键,橙色为疏水作用);c-结合口袋电荷表面分布(红为负,蓝为正);d-配体与残基的二维相互作用图(绿色虚线为氢键)
图1 OR2 W1嗅觉受体蛋白与3种醛类气味分子的结合模式
Fig.1 Binding modes of OR2 W1 with three aldehyde ligands
图2展示了3种酚类气味分子(复杂浓郁类)——2-甲氧基-4-甲基苯酚、2-甲氧基-4-丙基苯酚和异丁香酚的结合模式,其结合能依次为-6.4、-5.9、-5.5 kcal/mol。该类分子含芳香环和醚/羟基取代,极性较强,兼具氢键形成能力与疏水相互作用。2-甲氧基-4-甲基苯酚结合于OR10K1的开阔口袋中,与Tyr278形成氢键(2.89 Å),并与Pro283、Glu70、Phe170等残基形成疏水网络,同时与Tyr73发生π-π堆积,结合最为稳定。2-甲氧基-4-丙基苯酚与OR2W1结合,主要通过Asn155(3.28 Å)形成氢键,并与Tyr259、Tyr104、Ile206等产生疏水作用,结合力略弱。异丁香酚结合于OR10K1的紧凑口袋中,与Leu144形成氢键(3.08 Å),并与Phe133、Leu213等多点疏水结合,芳香环嵌合性良好,尽管氢键较少,但整体结构稳定。酚类分子通常含有羟基等极性官能团,能够与嗅觉受体形成稳定的氢键网络,从而锁定配体-受体复合物结构,使其RMSD波动较小,这也解释了酚类具有较高亲和力和稳定性的原因。
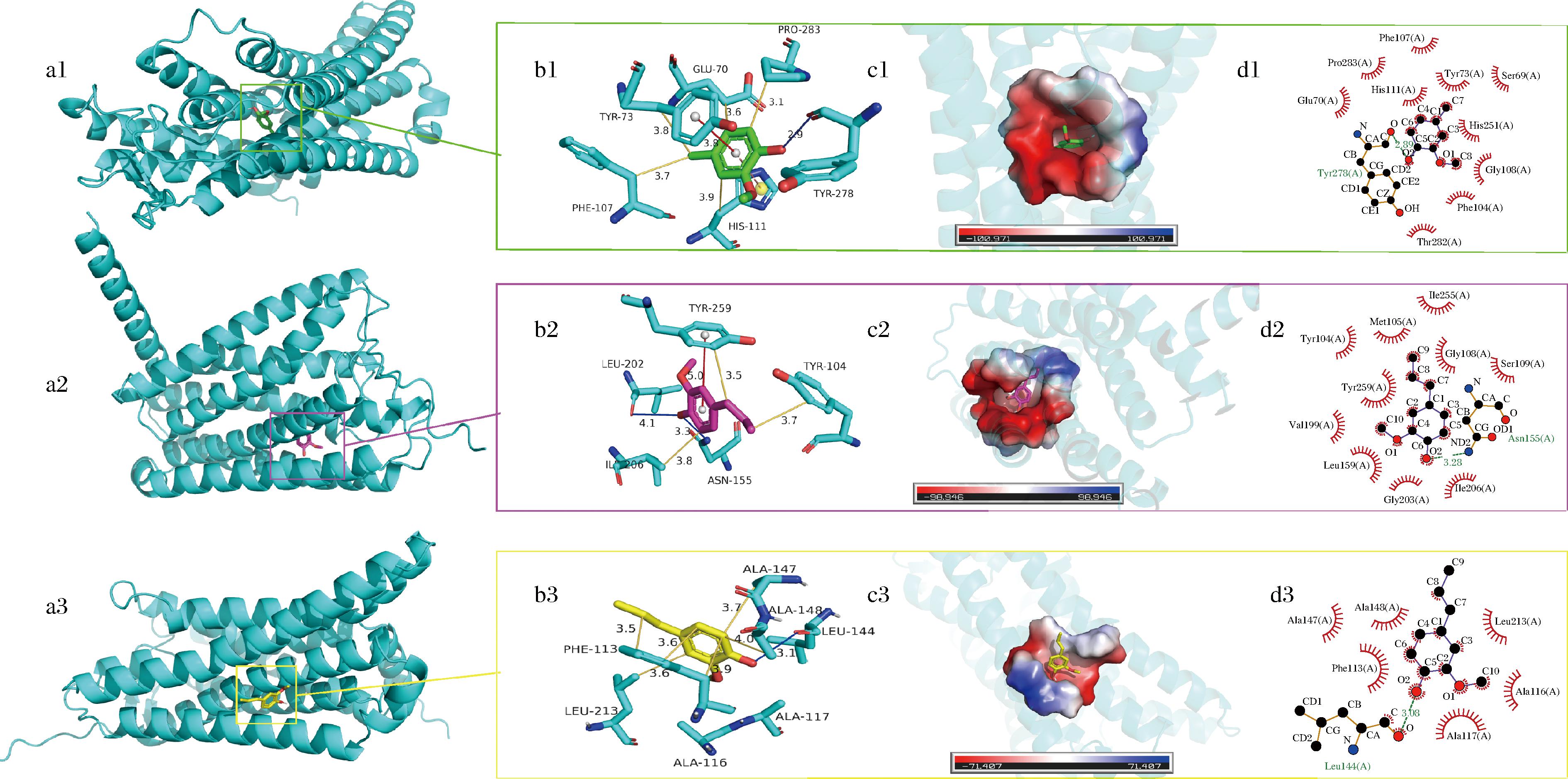
a-3种配体(2-甲氧基-4-甲基苯酚,绿色;2-甲氧基-4-丙基苯酚,紫色;异丁香酚,黄色)在结合口袋中的构象;b-与 4.00 Å范围内残基的三维相互作用(蓝色为氢键,橙色为疏水作用);c-结合口袋电荷表面分布(红为负,蓝为正);d-配体与残基的二维相互作用图(绿色虚线为氢键)
图2 OR10K1/OR2W1嗅觉受体蛋白与酚类配体的结合模式
Fig.2 Binding modes of OR10K1/OR2W1 with three phenolic ligands
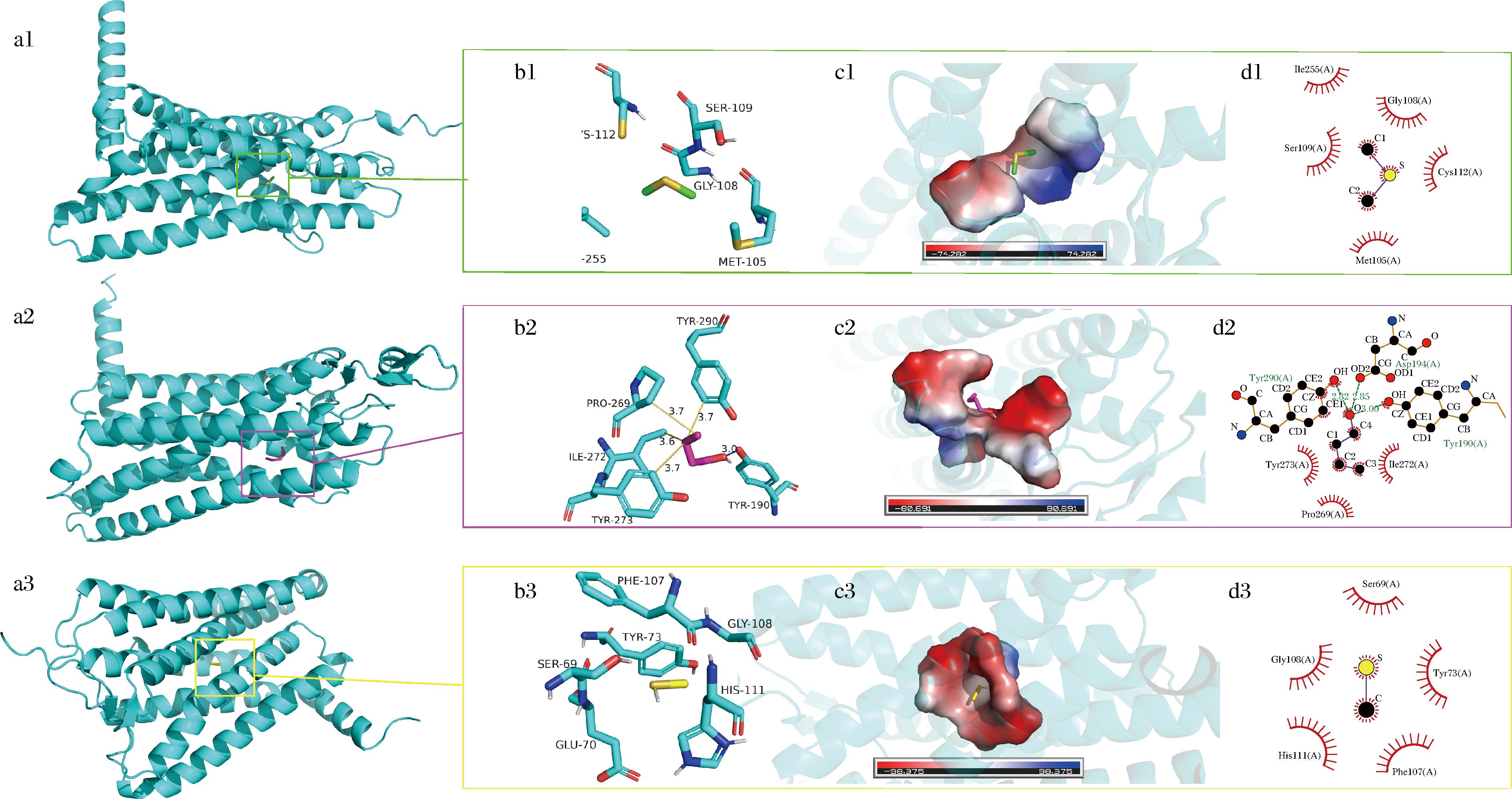
a-3种配体(二甲硫醚,绿色;1-丁醇,紫色;甲硫醇,黄色)在结合口袋中的构象;b-与4.00 Å范围内残基的三维相互作用(蓝色为氢键,橙色为疏水作用);c-结合口袋电荷表面分布(红为负,蓝为正);d-配体与残基的二维相互作用图(绿色虚线为氢键)
图3 OR2W1/OR10S1/OR10K1嗅觉受体蛋白与硫醇类配体的结合模式
Fig.3 Binding modes of OR2W1/OR10S1/OR10K1 with three sulfur- and alcohol-type ligands
图3展示了二甲硫醚、1-丁醇和甲硫醇3种气味分子(不良刺激类)与OR2W1、OR10S1、OR10K1三种嗅觉受体的结合构象及相互作用模式。该类分子结构简单、极性弱、分子量低,整体以疏水作用为主,结合特征明显不同于醛类和酚类。二甲硫醚结合于OR2W1的疏水口袋中,未形成氢键,仅有松散的疏水接触,结合能较低(-1.9 kcal/mol),稳定性较差。甲硫醇与OR10K1结合模式相似,未观察到有效氢键,结合能最低(-1.6 kcal/mol),嵌合性差。相比之下,1-丁醇的羟基与OR10S1中的多个极性残基形成氢键(如Tyr290、Asp194),同时烷基链与疏水残基相互作用,结合能为-3.2 kcal/mol,稳定性显著优于其余两者,表明其极性官能团对受体结合起关键作用。这类气味分子结合普遍较松散,这种现象的发生可能在于含硫化合物缺乏可与受体形成强相互作用的极性基团,只能通过范德华力或疏水作用力暂时停留在结合位点,因此复合物容易发生构象变化。
总体而言,由分子对接结果可以看出,气味分子官能团的极性越强,其与OR结合时形成特定氢键等强相互作用的能力越强,复合物的预测结合稳定性(亲和力)也越高,这一点与已有文献报道的规律一致。例如,某项针对香兰素的研究表明[25],配体分子能够通过氢键显著提高其在嗅觉受体中的结合稳定性。上述分析进一步支持了本研究关于气味分子官能团在识别机制中关键作用的推论。
2.2 动态氢键分析
动态氢键数量的稳定与持续,表明配体在模拟过程中能与受体保持持续有效的接触,从而提高复合物整体构象稳定性。氢键分析显示,酚类配体(图4-d~图4-f)在模拟过程中氢键可生成数量为1~5个,实际生成数量为1个或2个,保持了较为稳定的氢键数量,黑色线条(氢键数量)较平稳,红色区域(0.35 nm以内的配体-蛋白接触)较为密集,表明这些配体与蛋白形成了较稳定的相互作用。醛类配体氢键(图4-a~图4-c)可生成数量均约1个,实际生成数量为1个或0个,氢键数量相对较少,并且在模拟过程中存在一定波动,表明其结合模式存在一定的构象调整。含硫类配体(图4-g和图4-i)在模拟过程中既无可生成氢键,也未形成实际氢键;1-丁醇体系中可生成氢键的数量波动较大,实际形成的氢键数量为0~1个,整体数量偏少。这些体系中配体与蛋白间的接触频率较低且不连续(红色区域稀疏),表明其主要依靠较弱的疏水作用或范德华力与蛋白相互作用,结合模式较为松散,更容易发生构象解离。
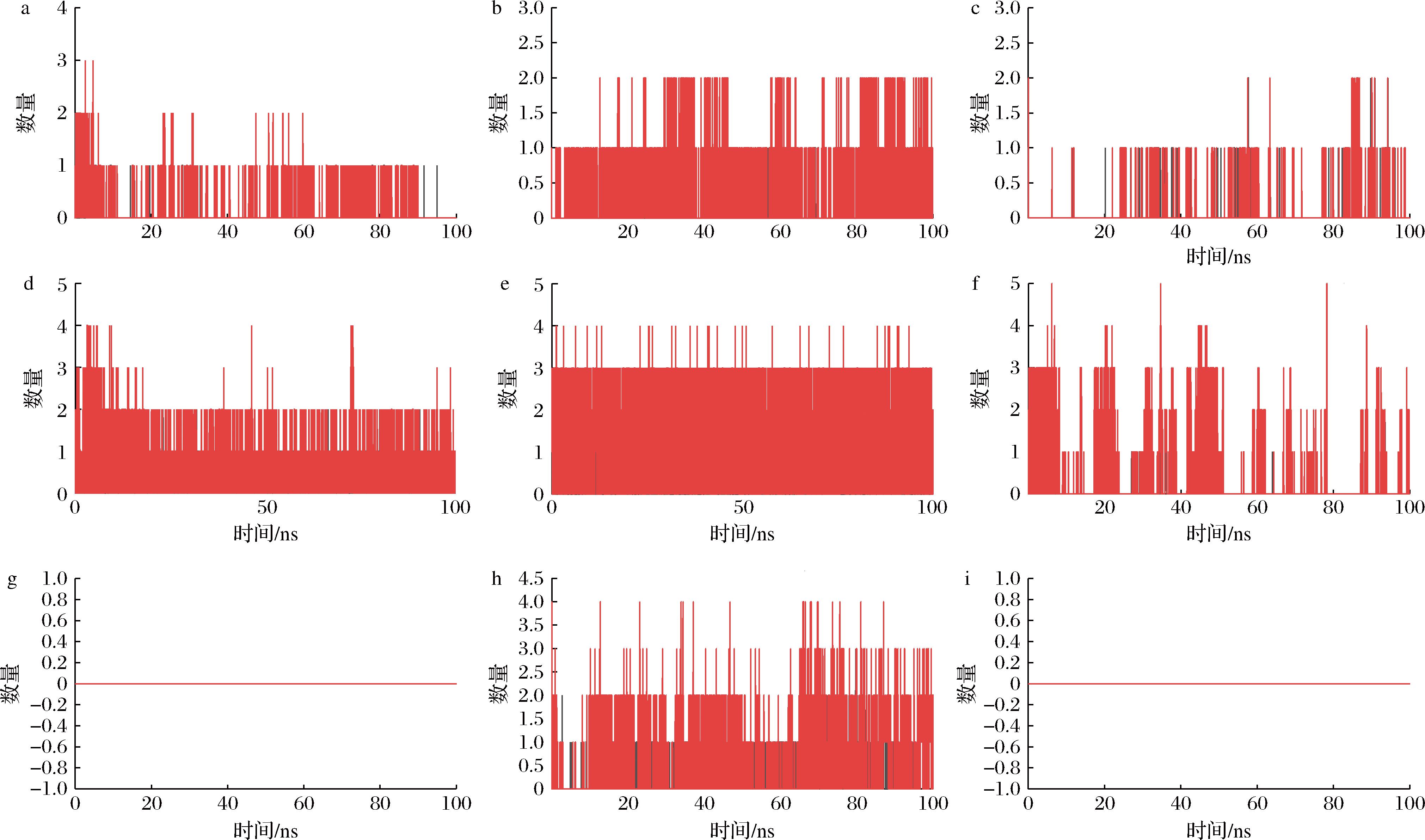
a-反式-2-壬烯醛;b-反式,反式-2,4-壬二烯醛;c-(2E,4E)-癸-2,4-二烯醛;d-2-甲氧基-4-甲基苯酚;e-2-甲氧基-4-丙基苯酚;f-异丁香酚;g-二甲硫醚;h-1-丁醇;i-甲硫醇
图4 不同类别气味分子与嗅觉受体蛋白在模拟过程中的氢键动态变化
Fig.4 Dynamic changes in hydrogen bonding between different odorant molecules and olfactory receptor proteins during simulation
注:黑色线条表示实际生成氢键数量,红色区域表示配体与蛋白间距离小于0.35 nm的接触频率(即可生成氢键的数量)。
2.3 RMSD
RMSD用于评估复合物体系在模拟过程中的结构变化程度,是衡量结合稳定性的关键指标。RMSD值低且变化趋稳通常表明蛋白-配体复合物构象稳定,结合可靠;而RMSD值持续上升或波动幅度较大则可能预示体系结构不稳定,配体与受体之间的相互作用较弱或存在脱离风险[26]。如图5所示,酚类配体的RMSD波动较小(0.15~0.45 nm),60 ns后逐渐趋于稳定,最终保持在约0.4 nm,说明其与受体的构象适配性较高,结合后体系结构稳定,蛋白骨架波动较小。醛类配体的RMSD值略高(0.2~0.8 nm),约在40 ns后趋于平稳,反映出在初期存在一定的构象调整过程,表明配体与受体之间的结合在适应初始构象后可维持相对稳定状态。二甲硫醚在模拟后期(约80 ns)出现明显上升,说明其可能发生了较大的构象重排甚至结合位点偏移,结合过程不稳定。甲硫醇和1-丁醇的RMSD波动相对较小但仍高于酚类,说明尽管存在一定的结合,但结构扰动较明显。模拟结果进一步说明,不同类型的气味小分子在结合后对蛋白构象波动影响存在显著差异,这与配体的结构特性及其与蛋白形成的非共价作用模式密切相关,类似观察也曾在其他蛋白-配体体系中通过分子模拟得到验证[27]。
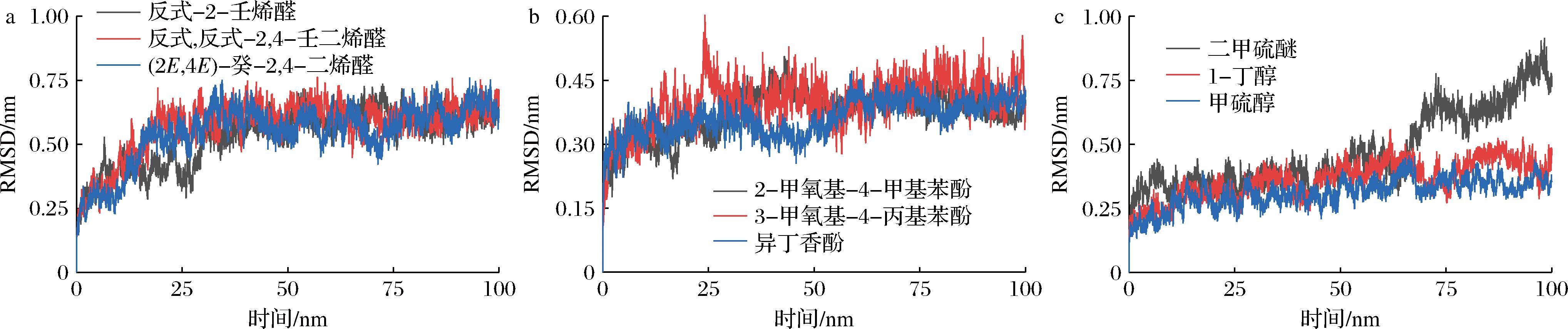
a-醛类气味分子与OR2W1蛋白的RMSD变化;b-酚类气味分子分别与OR10K1、OR2W1和OR10K1蛋白的RMSD变化;c-硫醇类气味分子分别与OR2W1、OR10S1和OR10K1蛋白的RMSD变化
图5 不同类别气味分子与嗅觉受体蛋白复合物的主链RMSD图
Fig.5 RMSD plots of protein backbones in complexes of different categories of odorant molecules and olfactory receptor proteins
2.4 RMSF
氨基酸残基RMSF波动用于衡量蛋白质在分子动力学过程中各残基的柔性变化,数值越高表示该区域构象波动越大。RMSD反映整体稳定性趋势,而RMSF则提供了蛋白局部波动的信息,两者结合能够全面描述体系的动态行为。如图6所示,醛类配体复合物整体RMSF较低,仅在C端(280号残基以后)存在一定程度的波动,其中反式-2-壬烯醛和反式,反式-2,4-壬二烯醛的RMSF略高,说明其在结合后对蛋白某些区域产生了一定扰动。酚类配体体系的RMSF值分布最为集中,范围为0.1~0.4 nm,C端波动最小,表明该类配体结合后蛋白骨架更加稳定,结合位点周围构象变动较小。该类配体通过芳香环、羟基等极性基团与蛋白形成稳定的氢键与疏水网络,进一步增强了结构稳定性,与已有研究中酚类分子倾向于通过多重相互作用稳定蛋白构象的发现一致[28]。相比之下,第三类复合物的RMSF波动最为剧烈,尤其是二甲硫醚在200~280号残基区域的变化幅度明显高于其他体系,提示其对蛋白局部区域的扰动显著,可能导致结合口袋结构松动,降低结合稳定性。这一趋势与RMSD分析结果一致,进一步验证了酚类分子结合稳定性强、而第三类分子稳定性差的判断。
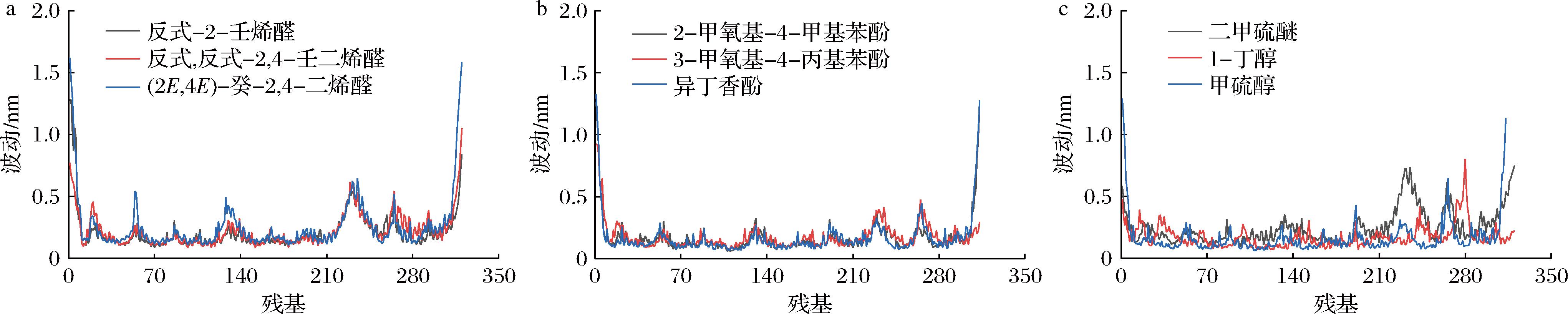
a-醛类气味分子与OR2W1蛋白的;b-酚类气味分子分别与OR10K1、OR2W1和OR10K1蛋白;c-硫醇类气味分子分别与OR2W1、OR10S1和OR10K1蛋白
图6 不同类别气味分子与嗅觉受体蛋白模拟的主链RMSF图
Fig.6 Main-chain RMSF plots of different categories of odor molecules with olfactory receptor proteins during the simulation
2.5 Rg
Rg用于衡量蛋白质整体构象的紧凑程度,是评估其在配体作用下是否保持原有折叠状态的重要参数,结构紧凑意味着蛋白维持其功能态所需的正确折叠构象能够维持配体结合位点的稳定性,从而促进有效的受体识别与信号传导过程。Rg值越小且波动越小,通常表明蛋白维持在较稳定、折叠良好的构象,有助于结合口袋的结构完整性及结合功能的维持[29]。如图7所示,酚类复合物的Rg变化最小(2.2~2.35 nm),在整个模拟过程中几乎未出现显著波动,表明其结合并未引起蛋白结构的松动或膨胀,体现出高度的构象适配性与结合稳定性,这一结果与已有研究一致[28]。醛类复合物的Rg值略高且在40~80 ns期间波动略大(2.2~2.45 nm),提示蛋白可能经历轻度结构调整,以适应配体的空间结构,整体稳定性次于酚类。含硫/醇/醚类复合物的Rg波动最为明显,尤其是二甲硫醚和1-丁醇在模拟后期Rg值升高,提示蛋白受到较强扰动,可能导致结合口袋局部解构,降低结合强度与稳定性。总体而言,Rg与RMSD、RMSF结果高度一致,体现出酚类配体诱导的复合物结构最稳定,醛类适中,硫/醇/醚类最弱。
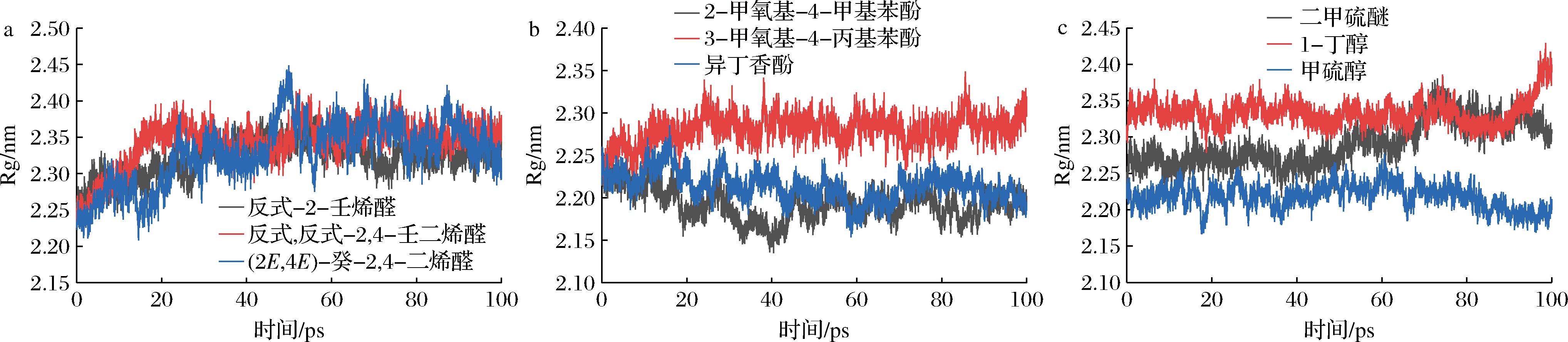
a-醛类气味分子与OR2W1蛋白;b-酚类气味分子分别与OR10K1、OR2W1和OR10K1蛋白;c-硫醇类气味分子分别与OR2W1、OR10S1和OR10K1蛋白
图7 不同类别气味分子与嗅觉受体蛋白模拟的主链Rg图
Fig.7 Main-chain Rg plots of different categories of odor molecules with olfactory receptor proteins during the simulation
2.6 PCA
PCA用于提取分子动力学模拟中的主要运动模式,以揭示蛋白复合物的构象变化特征。根据前述RMSD和RMSF分析,所有体系在60 ns后趋于稳定,故选取60~100 ns的数据进行PCA,绘制PC1与PC2的投影图,并计算前5个PC的贡献率(见表1)。一般而言,PC1和PC2的累计贡献率越高,表明体系构象变化可被较少的主成分更有效地表达。然而本研究发现,多数体系的前2个PC贡献率普遍较低,意味着PCA无法完全概括复杂蛋白-配体体系的整体运动模式。这主要是由于蛋白与气味分子间的构象相互作用涉及多个区域同时发生的细微而协同的变化,单纯的线性降维方法难以有效捕捉这些复杂的动态特征[27]。
表1 不同气味分子-受体复合物平衡轨迹前5个主成分贡献率的PCA 单位:%
Table 1 PCA contribution rates of the top 5 principal components for the conformational change of the odorant-olfactory receptor complex
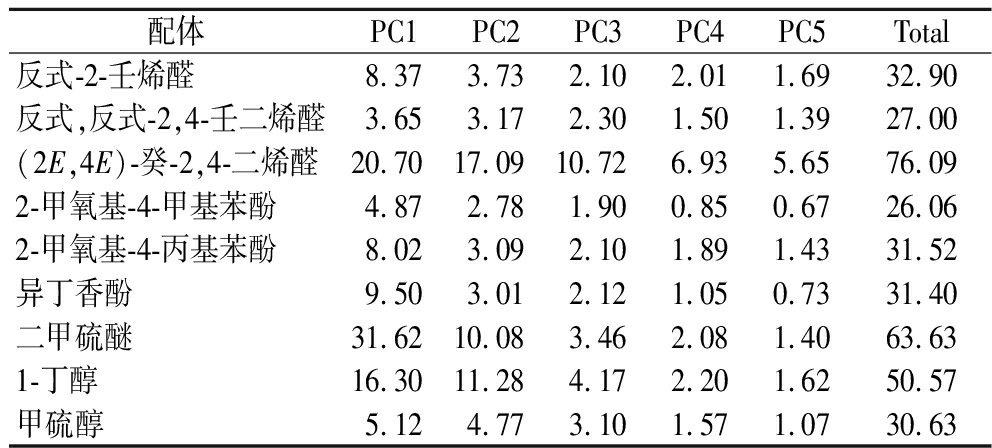
配体PC1PC2PC3PC4PC5Total反式-2-壬烯醛8.373.732.102.011.6932.90反式,反式-2,4-壬二烯醛3.653.172.301.501.3927.00(2E,4E)-癸-2,4-二烯醛20.7017.0910.726.935.6576.092-甲氧基-4-甲基苯酚4.872.781.900.850.6726.062-甲氧基-4-丙基苯酚8.023.092.101.891.4331.52异丁香酚9.503.012.121.050.7331.40二甲硫醚31.6210.083.462.081.4063.631-丁醇16.3011.284.172.201.6250.57甲硫醇5.124.773.101.571.0730.63
具体来看,酚类复合物体系(图8-d~图8-f)的PC1与PC2累计贡献率相对较高(26.06%~31.52%),且投影分布较为分散。这表明虽然酚类配体整体结合较为稳定,但仍伴随一定程度的局部构象波动。考虑到酚类分子结构中的芳香环和亲疏水取代基,这种波动可能与芳香环的旋转、侧链摆动或氢键网络的动态重构等结构调整有关。相比之下,其他几类体系的主成分贡献率更低,且PC1与PC2的投影更为集中,说明这些体系的构象变化受限于较简单的结合模式,更倾向于个体结构的局部调整,而非复杂的整体构象重排。这进一步佐证了酚类配体在结合过程中表现出更丰富的构象调节行为,而醛类与硫/醇/醚类配体的构象活动模式相对单一。
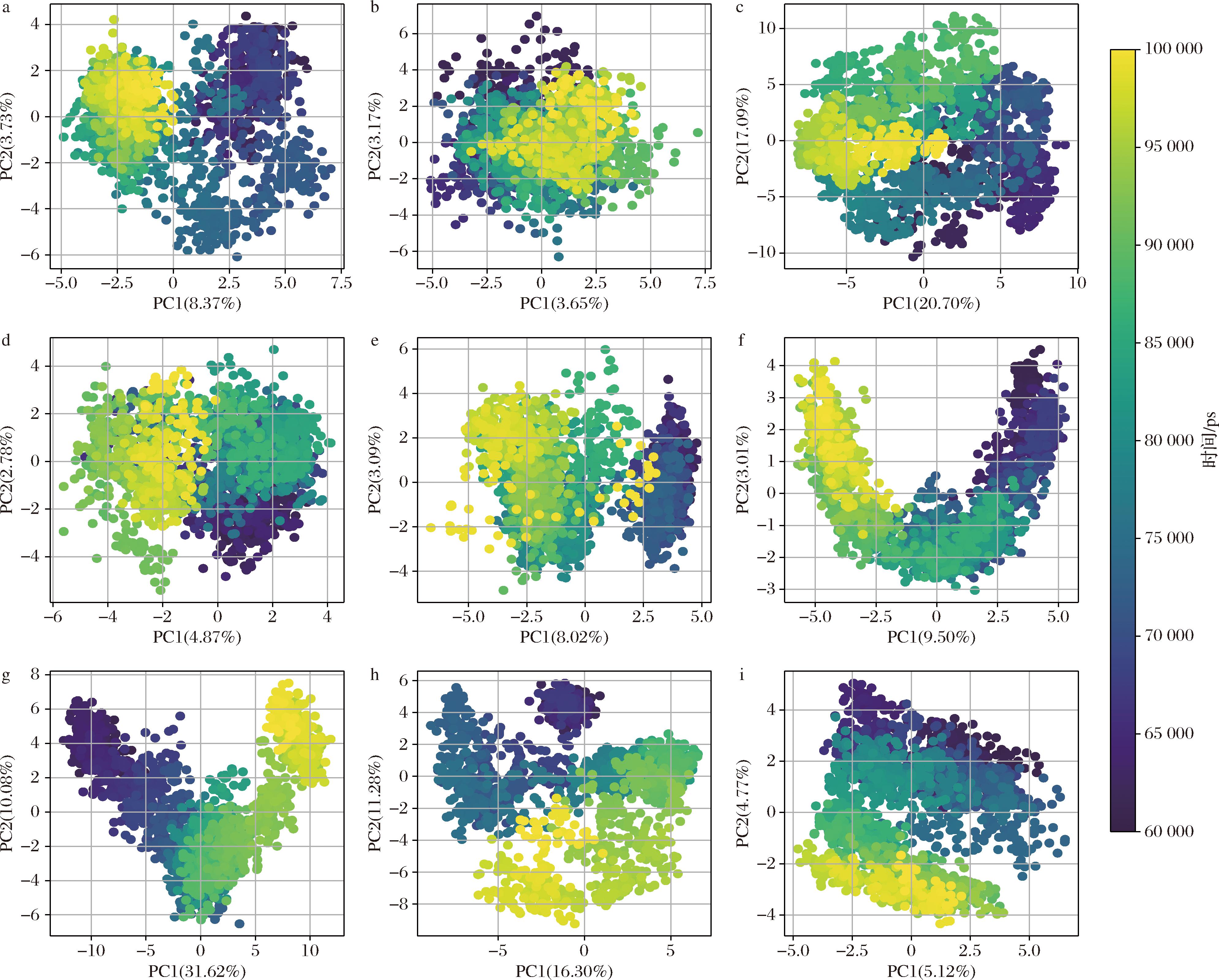
a-反式-2-壬烯醛;b-反式,反式-2,4-壬二烯醛 ;c-(2E,4E)-癸-2,4-二烯醛;d-2-甲氧基-4-甲基苯酚;e-2-甲氧基-4-丙基苯酚;f-异丁香酚;g-二甲硫醚;h-1-丁醇;i-甲硫醇
图8 不同类别复合物体系分子动力学模拟轨迹的第1、2主成分
Fig.8 First and second principal components of the molecular dynamics simulation trajectories of different category complex systems
3 结论
本研究以食品中常见挥发性气味功能团(醛类、酚类、硫醚类、醇类、硫醇类)为对象,结合分子对接和分子动力学模拟,系统探讨了9种代表性气味分子与人类嗅觉受体(OR2W1、OR10K1、OR10S1)的结合模式与构象稳定性。研究发现:
1)酚类气味分子形成稳定且多样化的氢键和疏水作用网络、表现出最高的结合亲和力和最强的构象稳定性,配体-受体体系结构紧凑、动态波动小;醛类分子结合模式适中,疏水作用主导,氢键次之,体系具有一定波动但整体稳定性较高;硫醇类分子主要通过范德华力弱结合,缺乏稳定氢键网络,构象波动剧烈,稳定性最低。
2)RMSD、RMSF、Rg分析结果一致,表明酚类配体最为稳定,能有效维持蛋白的整体紧密构象;醛类次之,硫/醇/醚类配体的结构扰动最大,影响蛋白构象稳定性。
3)PCA未能提取出明显主导构象运动模式,但揭示了酚类分子结合过程中涉及更多的局部构象调整,如芳香环旋转和氢键网络重构,而醛类和硫/醇/醚类体系的构象变化相对单一,更依赖于个体结构特性。
本研究从分子结构视角明确了气味功能团类型与人类嗅觉受体识别机制间的关系,为深入理解食品风味感官机制提供了重要理论依据,同时对风味分子的人工感知系统设计、风味调控技术和食品品质评价具有潜在应用价值。
[1] ZHANG J Y, CHEN Z M, WANG Z, et al.Interactions of fish proteins and volatile flavor compounds:Mechanisms, affecting factors and analytical methods[J].Mini-Reviews in Organic Chemistry, 2021, 18(2):259-269.
[2] MALNIC B, HIRONO J, SATO T, et al.Combinatorial receptor codes for odors[J].Cell, 1999, 96(5):713-723.
[3] YANG H, YANG W, ZHANG Y, et al. Analysis of key aroma compound changes in grass carp fillets during cold storage using two-dimensional gas chromatography-olfactometry-mass spectrometry and odor activity value[J]. Journal of Agricultural and Food Chemistry, 2025, 73(14): 8503-8514.
[4] KATRITCH V, FENALTI G, ABOLA E E, et al.Allosteric sodium in class A GPCR signaling[J].Trends in Biochemical Sciences, 2014, 39(5):233-244.
[5] KJØLBYE L R, SØRENSEN L, YAN J, et al.Lipid modulation of a class B GPCR:Elucidating the modulatory role of PI(4, 5)P2 lipids[J].Journal of Chemical Information and Modeling, 2022, 62(24):6788-6802.
[6] NIIMURA Y, NEI M.Evolutionary dynamics of olfactory receptor genes in fishes and tetrapods[J].Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(17):6039-6044.
[7] FREITAG J, LUDWIG G, ANDREINI I, et al.Olfactory receptors in aquatic and terrestrial vertebrates[J].Journal of Comparative Physiology A, 1998, 183(5):635-650.
[8] MALINSKA M, KIM S K, GODDARD W, et al.Structural Variation and Odorant Binding for Olfactory Receptors Selected from the Six Major Subclasses of the OR Phylogenetic Tree[M].Computational Materials, Chemistry, and Biochemistry:From Bold Initiatives to the Last Mile:In Honor of William A.Goddard’s Contributions to Science and Engineering, 2021, 284:855-925.
[9] SHIM T, PACALON J, KIM W C, et al.The third extracellular loop of mammalian odorant receptors is involved in ligand binding[J].International Journal of Molecular Sciences, 2022, 23(20):12501.
[10] BUSHDID C, DE MARCH C A, TOPIN J, et al.Mammalian class I odorant receptors exhibit a conserved vestibular-binding pocket[J].Cellular and Molecular Life Sciences, 2019, 76(5):995-1004.
[11] KALRA S, MITTAL A, GUPTA K, et al.Analysis of single-cell transcriptomes links enrichment of olfactory receptors with cancer cell differentiation status and prognosis[J].Communications Biology, 2020, 3:506.
[12] BILLESBØLLE C B, DE MARCH C A, VAN DER VELDEN W J C, et al.Structural basis of odorant recognition by a human odorant receptor[J].Nature, 2023, 615(7953):742-749.
[13] CHOI C, BAE J, KIM S, et al.Understanding the molecular mechanisms of odorant binding and activation of the human OR52 family[J].Nature Communications, 2023, 14:8105.
[14] CRASTO C J.Computational biology of olfactory receptors[J].Current Bioinformatics, 2009, 4(1):8-15.
[15] 杨春婷, 弘子姗, 张丽, 等.基于虚拟筛选和分子动力学模拟发现新型核桃源α-葡萄糖苷酶抑制肽[J].食品与发酵工业, 2025, 51(16):236-244.
YANG C T, HONG Z S, ZHANG L, et al.Discovery of novel walnut-derived α-glucosidase inhibitory peptides based on virtual screening and molecular dynamics simulations[J].Food and Fermentation Industries, 2025, 51(16):236-244.
[16] HAAG F, DI PIZIO A, KRAUTWURST D.The key food odorant receptive range of broadly tuned receptor OR2W1[J].Food Chemistry, 2022, 375:131680.
[17] MAINLAND J D, LI Y R, ZHOU T, et al.Human olfactory receptor responses to odorants[J].Scientific Data, 2015, 2:150002.
[18] YASI E A, EISEN S L, WANG H F, et al.Rapid deorphanization of human olfactory receptors in yeast[J].Biochemistry, 2019, 58(16):2160-2166.
[19] KRAUTWURST D, YAU K W, REED R R.Identification of ligands for olfactory receptors by functional expression of a receptor library[J].Cell, 1998, 95(7):917-926.
[20] ALFONSO-PRIETO M, CAPELLI R.Machine learning-based modeling of olfactory receptors in their inactive state:Human OR51E2 as a case study[J].Journal of Chemical Information and Modeling, 2023, 63(10):2911-2917.
[21] 曾祥权, 曹瑞, 余美宏, 等.基于分子模拟技术的不同聚合度多酚与氧化三甲胺脱甲基酶的相互作用机制研究[J].食品与发酵工业, 2024, 50(11):85-97.
ZENG X Q, CAO R, YU M H, et al.Interaction mechanism between polyphenols with different degree of polymerization and trimethylamine-N-oxide demethylase based on molecular simulation study[J].Food and Fermentation Industries, 2024, 50(11):85-97.
[22] FRIEDRICH R W, KORSCHING S I.Combinatorial and chemotopic odorant coding in the zebrafish olfactory bulb visualized by optical imaging[J].Neuron, 1997, 18(5):737-752.
[23] HAMANA H, HIRONO J, KIZUMI M, et al.Sensitivity-dependent hierarchical receptor codes for odors[J].Chemical Senses, 2003, 28(2):87-104.
[24] SATO T, MATSUKAWA M, IIJIMA T, et al.Hierarchical elemental odor coding for fine discrimination between enantiomer odors or cancer-characteristic odors[J].Frontiers in Behavioral Neuroscience, 2022, 16:849864.
[25] ZENG S T, ZHANG L L, LI P, et al.Molecular mechanisms of caramel-like odorant-olfactory receptor interactions based on a computational chemistry approach[J].Food Research International, 2023, 171:113063.
[26] HOLLINGSWORTH S A, DROR R O.Molecular dynamics simulation for all[J].Neuron, 2018, 99(6):1129-1143.
[27] LIU K, WATANABE E, KOKUBO H.Exploring the stability of ligand binding modes to proteins by molecular dynamics simulations[J].Journal of Computer-Aided Molecular Design, 2017, 31(2):201-211.
[28] SHAHIDI F, DISSANAYAKA C S.Phenolic-protein interactions:Insight from in-silico analyses-A review[J].Food Production, Processing and Nutrition, 2023, 5(1):2.
[29] DE VIVO M, MASETTI M, BOTTEGONI G, et al.Role of molecular dynamics and related methods in drug discovery[J].Journal of Medicinal Chemistry, 2016, 59(9):4035-4061.