桑葚又名桑果、桑子、桑枣等,是一种常见的水果,属于桑科,主要分布在我国四川、云南、广东、贵州及江浙一带[1]。桑葚富含花色苷、多糖、多酚、黄酮等活性物质,具有延缓衰老、降血糖、降血脂、抗癌等药理作用,是国家卫生健康委员会批准的第一批“药食同源”物质[2]。桑葚季节性强,皮薄多汁,不易运输和贮藏,除应季鲜销外,通常加工成桑葚果酒、果干、果汁、酵素等产品,既提高桑葚的附加值,也避免了因其不耐贮藏而造成的资源浪费[3]。随着桑葚酒、桑葚汁等加工业的发展,加工过程会产生高达30%的果渣副产物[4]。桑葚渣中仍含有大量花色苷、多酚和黄酮等活性成分[5],目前已大量用于花青素的提取。然而,榨汁后桑葚渣初始含水率>70%,易发生腐败变质。干燥可降低其水分活度,抑制微生物繁殖,延长桑葚渣贮藏时间,还可以减轻桑葚渣重量,便于运输,为桑葚渣的周年利用提供原料保障。
不同干燥方式和温度会显著影响果渣干燥后品质[6]。ZHANG等[7]采用6种不同的干燥工艺制备猕猴桃果渣,发现真空冷冻干燥(vacuum freeze-drying,VFD)(冷阱温度-60 ℃、60 Pa)能较好地保持猕猴桃果渣的物理特性、色泽、营养成分、抗氧化活性和微观结构,但能耗较高,干燥时间较长,不合适工业生产,而真空微波干燥(60 ℃,0.087 mPa)猕猴桃果渣抗氧化能力仅次于VFD,且干燥时间显著缩短。XIONG等[8]研究热泵干燥(heat pump drying,HPD)和热风干燥(hot air drying,HAD)(60 ℃)对荔枝果肉渣结合酚含量及其组成、形态、微观结构的影响,结果表明HPD组荔枝果肉渣粉中结合酚物质含量保留率较HAD组提升44.8%。苟小菊等[9]探究HAD(40~80 ℃)对红肉苹果粉理化性质、感官品质、营养成分及抗氧化的影响,发现HAD 50 ℃制备的红肉苹果粉在色泽、溶解性、多酚含量及抗氧化性上表现最佳。目前,关于桑葚果渣干燥加工的研究报道较少,范铭等[10]虽研究了HAD和VFD制备的桑葚渣在不同乙醇体积分数下提取液中总酚、总黄酮、总花色苷的含量以及其对α-淀粉酶的抑制率的影响,但并未对桑葚渣粉制备过程和干燥后粉体品质进行综合评价。
本研究以VFD为对照,探究了HAD和HPD两种不同干燥方式下不同干燥温度(50~70 ℃)对桑葚渣干燥特性、粉体理化性质、营养成分、抗氧化能力及风味的影响,以期为高品质桑葚渣粉体的制备提供理论依据和技术参考。
1 材料与方法
1.1 材料与试剂
桑葚渣,攀枝花四喜农业发展有限责任公司,采用GB 5009.3—2016《食品安全国家标准 食品中水分的测定》测得其水分含量为71.60%,贮藏于-20 ℃冷库中备用。
福林酚、DPPH(HPLC≥98%)、6-羟基-2,5,7,8-四甲基苯并二氢吡喃-2-甲酸(Trolox, HPLC≥98%)、ABTS(HPLC≥98%),上海源叶生物科技有限公司;无水乙醇,天津市富宁精细化工有限公司;NaCO3、NaNO2、NaOH,福晨(天津)化学试剂有限公司;芦丁、没食子酸、NaCl、醋酸钠,天津市大茂化学试剂厂;AlNO3,西陇化工股份有限公司;乙腈(HPLC≥99.9%),天津市彪仕奇科技发展有限公司;H3PO4(HPLC级),天津市科密欧化学试剂有限公司;矢车菊素-3-O-芸香糖苷(C-3-R,HPLC≥98%),乐天美医药;矢车菊素-3-O-葡萄糖苷(C-3-G,HPLC≥98%),成都钠钶锂生物科技有限公司。
1.2 仪器与设备
XMT-8电热鼓风干燥箱,上海科恒实业发展有限公司;WRH-100TB1S热泵干燥箱,广东威而信实业有限公司;DRC-1100型真空冷冻干燥机,东京理化器械有限公司;M2000PRO酶标仪,瑞士帝肯公司;DSC214差示扫描量热仪,德国耐驰公司;Bettersize 2600激光粒度分析仪,丹东百特仪器有限公司;S-3400 N电子显微镜,日本日立公司;Air sense-pen 3.5电子鼻,德国艾森公司;LC-20AT高效液相色谱仪,日本岛津公司;Ultra Scan VIS型全自动色差仪,美国Hunter Lab公司。
1.3 实验方法
1.3.1 不同干燥方法
每份样品称取200 g,分别进行干燥。VFD组样品需先在-80 ℃冰箱预冻8 h,经预实验确定冷冻干燥机冷阱温度-80 ℃, 干燥仓真空度81.3 Pa,干燥时间36 h,最终得到VFD样品;HAD组设置50、60、70 ℃ 3个温度梯度进行干燥,对应得到HAD50、HAD60及HAD70这3组样品;HPD组设置50、60、70 ℃ 3个温度梯度进行干燥,设置恒温恒湿模式,干燥仓内相对湿度设置为15%,得到HPD50、HPD60及HPD70P这3组样品。每组实验均平行3次,并且所有干燥终点均以物料水分含量<8%为判定标准,干燥后样品经高速粉碎机(30 000 r/min)粉碎60 s,过40目筛后密封避湿保存于干燥器中备用。
1.3.2 水分含量相关指标的测定
1.3.2.1 水分含量测定
参考GB 5009.3—2016《食品安全国家标准 食品中水分的测定》。
1.3.2.2 干燥过程水分比的计算
水分比的计算如公式(1)所示:
水分比![]()
(1)
式中:pt,t时刻干基含水量,g/g;p0,初始干基含水量,g/g。
1.3.2.3 干燥速率的计算
干燥速率的计算如公式(2)所示:
干燥速率![]()
(2)
式中:Pt,t时刻的干基含水量,g/g;Pt+Δt,桑葚渣Pt+Δt时刻的干基含水量,g/g;Δt,干燥间隔时间,h。
1.3.3 色泽测定
采用色差仪测定桑葚渣果粉的色泽L*(亮度)、a*(红/绿)、b*(黄/蓝),测定前分别用白色反射板和黑色反射板对色差仪进行校正。总色差ΔE、色泽饱和度C和色调角h°的计算如公式(3)~公式(5)所示:
(3)
(4)
(5)
1.3.4 微观结构观察
采用扫描电子显微镜(scanning electron microscope,SEM)对桑葚渣粉进行表观形貌观察,先将桑葚渣粉粘到样品台上,喷金处理后,放大1 000倍进行扫描观察、采集图片。
1.3.5 粒径特性测定
采用激光粒度分析仪,湿法测定桑葚渣粉的粒径,以D10、D50、D90、离散度和比表面积评价桑葚渣粉体粒径特性,离散度按公式(6)计算:
(6)
式中:Span,样品离散度;D10、D50和D90分别为粒度体积分布10%、50%、90%所对应的直径。
1.3.6 持水性与持油性测定
参考DONG等[11]的方法,称取1 g桑葚渣粉置于50 mL离心管中,加入10 mL蒸馏水/大豆油,涡旋混匀5 min后在室温下静置2 h,再用10 000 r/min离心10 min,使其分离沉淀,持水性/持油性的计算如公式(7)所示:
(7)
式中:W,桑葚渣粉的持水性/持油性,g/g;m1,样品和离心管的质量,g;m2,样品吸水后和离心管的质量,g;m3,桑葚渣粉的质量,g。
1.3.7 溶解度测定
参考DONG等[11]的方法,称取1 g桑葚渣粉,置于50 mL的离心管中,40 ℃水浴恒温振荡器中摇匀30 min后,10 000 r/min离心10 min,取上清液置于干燥皿中,105 ℃烘箱中烘干至恒重,溶解性的计算如公式(8)所示:
(8)
式中:W,桑葚渣粉的溶解度,%;m1,干燥皿的质量,g;m2,溶解物质和干燥皿的质量,g;m3,桑葚渣粉的质量,g。
1.3.8 堆积密度与休止角
将桑葚渣粉自然落入10 mL量筒中,使粉体积到10 mL的刻度线处,记录容器内桑葚渣粉的质量为m,堆积密度的计算如公式(9)所示:
(9)
式中:B,堆积密度,g/cm3;m,桑葚渣粉质量,g;V,粉末到达量筒的体积,cm3。
将漏斗固定在试管架上并距离桌面8 cm,漏斗下端平放一张白纸,使8 g桑葚渣粉沿漏斗落到白纸上,粉末完全落下后,量取粉末形成圆锥高度为H,底部直径为2R,休止角的计算如公式(10)所示:
(10)
式中:A′,休止角,°;H,桑葚渣粉散落圆锥高度,cm;R,桑葚渣粉散落后底部半径,cm。
1.3.9 可溶性糖与还原糖测定
参考方晓彤等[12]的方法,可溶性糖采用苯酚-硫酸法,在485 nm波长处测定,以蔗糖为标准品制作标准曲线;还原糖采用3,5-二硝基水杨酸法,在540 nm波长处测定,以葡萄糖为标准品制作标准曲线。可溶性糖、还原糖的计算如公式(11)、公式(12)所示:
(11)
式中:S1,可溶性糖含量,mg/g;g,从标准曲线查得的蔗糖质量,μg;V,样品提取液总体积,mL;N,样品提取液稀释倍数;Vs,测定时间所取样品提取液体积,mL;m,样品质量,g。
(12)
式中:S2,还原糖含量,mg/g;g,从标准曲线查得的葡萄糖质量,mg;V,样品提取液总体积,mL;N,样品提取液稀释倍数;Vs,测定时间所取样品提取液体积,mL;m,样品质量,g。
1.3.10 酚类物质测定
1.3.10.1 桑葚渣粉提取液制备
参考卢靖辉等[13]的方法,称取1 g桑葚渣粉,加入10 mL的60%(体积分数)乙醇,在45 ℃、550 W下超声波浸提30 min后,离心(10 000 r/min,10 min),收集上清液,滤渣按上述方式重复浸提2次,将2次收集的上清液合并得到20 mL桑葚渣粉提取液,保存在-20 ℃的环境下备用。
1.3.10.2 总酚
采用Folin-Ciocalteau法,以没食子酸为标准品制作标准曲线,总酚含量以单位质量干燥样品中所含没食子酸的当量表示(mg/g)。
1.3.10.3 总黄酮
取0.5 mL提取液,加入0.1 mL 5%(质量分数)NaNO2,混匀静置5 min后,加入0.1 mL 10%(质量分数)Al(NO3)3,混匀静置6 min,再加入400 μL 1 mol/L NaOH,混匀静置15 min后,使用酶标仪在510 nm处测定吸光值,以芦丁为标准品制作标准曲线,总黄酮含量以单位质量干燥样品中所含芦丁毫克表示(mg/g)。
1.3.11 总花色苷及花色苷单体测定
参考邹颖等[14]的方法,称取1 g桑葚渣粉,加入10 mL的0.5%(体积分数)的酸化乙醇,在45 ℃、550 W条件下超声波浸提10 min后,离心(10 000 r/min,10 min),收集上清液,滤渣按上述方式重复浸提2次,合并上清液,采用pH示差法测量。分别添加pH为1.0的缓冲溶液和pH为4.5的缓冲溶液后,避光静置10 min,在510 nm和700 nm波长处测定。总花色苷计算如公式(13)所示:
(13)
式中:A,花色苷含量,mg/mL;ΔA=(A510nm-A700nm)pH 1.0-(A510nm-A700nm)pH 4.5;MW,C-3-G的相对分子质量,449.2;DF,稀释倍数,160;ε,C-3-G的摩尔消光系数,26 900;1,比色皿光程。
采用高效液相色谱法测定花色苷单体。色谱柱:Phenomenex C18柱(150 mm×4.6 mm,2.6 μm);流动相B为体积分数1.2%的H3PO4溶液,流动相D为乙腈。梯度洗脱程序如下:0~10 min,8% D;10~25 min,8%~10% D;25~55 min,10%~16% D;55~55.01 min,16%~60% D;55.01~57.00 min,60%~60% D;57.00~57.01,60%~8% D;进样量10 μL,流速0.4 mL/min,检测波长520 nm,柱温35 ℃。
1.3.12 抗氧化活性测定
1.3.12.1 DPPH
参考HOU等[15]的方法,取0.5 mL 1.3.10.1节制备的提取液,加入1.5 mL 0.2 mmol/L DPPH,摇匀避光反应30 min,在517 nm波长处测定。以Trolox为标准品制作标准曲线,DPPH含量以单位质量干燥样品中所含的Trolox当量表示(mg/g)。
1.3.12.2 ABTS
参考HOU等[15]的方法,将50 mL 7 mmol/L ABTS溶液和0.88 mL 140 mmol/L的过硫酸钾溶液混合,在室温避光条件下静置24 h,形成ABTS储备液。使用前吸取一定量储备液用无水乙醇进行稀释,将其稀释至在734 nm处吸光值为0.7±0.2。取0.3 mL 1.3.10.1节制备的提取液,加入0.9 mL ABTS,摇匀避光反应6 min,在734 nm波长处测定。以Trolox为标准品制作标准曲线,ABTS含量以单位质量干燥样品中所含的Trolox当量表示(mg/g)。
1.3.12.3 FRAP
参考沈袁媛等[16]的方法,取1 mL 1.3.10.1节制备的提取液,加入0.2 mL 0.2 mol/L pH为6.6的PBS和1.5 mL 0.1%(质量分数)铁氰化钾混合均匀,放入50 ℃水浴锅中孵育20 min后迅速冷却后,加入1 mL 10%(体积分数)三氯乙酸混合均匀后,离心3 000 r/min 10 min,取2 mL上清液,加入0.5 mL 0.1%(质量分数)FeCl3混合均匀,再加入3 mL蒸馏水混合均匀后,在700 nm处测定吸光值,以Trolox为标准品制作标准曲线,铁离子还原能力以单位质量干燥样品中所含Trolox当量表示(mg/g)。
1.3.13 电子鼻检测
参考李丽霞等[17]的方法,称取1 g桑葚渣粉置于50 mL的离心管中,用保鲜膜密封,在室温下(23±2) ℃平衡30 min后,将电子鼻进样器针头戳破保鲜膜进入离心管内进行测定,并注意针头不能碰到样品。测定间隔时间1 s,分析采集时间120 s,传感器和样品流速400 mL/min,清洗时间120 s,归零时间10 s,准备进样时间10 s。电子鼻各传感器的响应特性如表1所示。
表1 电子鼻各传感器的响应特性
Table 1 Response characteristics of each sensor of electronic nose
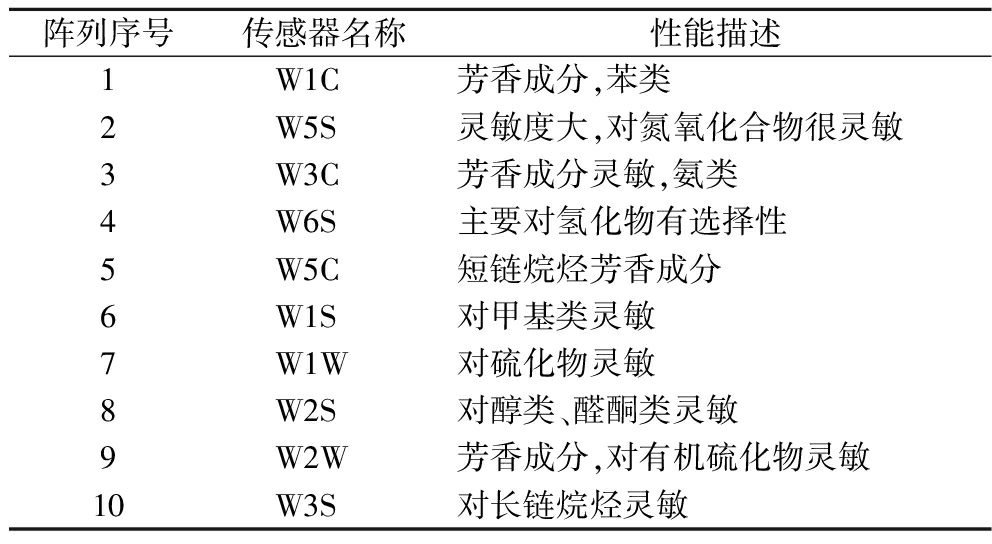
阵列序号传感器名称性能描述1W1C芳香成分,苯类2W5S灵敏度大,对氮氧化合物很灵敏3W3C芳香成分灵敏,氨类4W6S主要对氢化物有选择性5W5C短链烷烃芳香成分6W1S对甲基类灵敏7W1W对硫化物灵敏8W2S对醇类、醛酮类灵敏9W2W芳香成分,对有机硫化物灵敏10W3S对长链烷烃灵敏
1.4 数据处理
上述实验均重复测定3次,采用SPSS 27.0软件对数据进行统计学分析,结果以“平均值±标准差”表示,P<0.05表示差异显著,并使用Origin 2021进行绘图。
2 结果与分析
2.1 不同干燥方式及温度对桑葚干燥特性的影响
随着干燥时间的延长,不同干燥条件下桑葚渣水分比在0~2 h显著下降,2 h后呈逐渐变缓的趋势(图1-a和图1-b),这是因为前期内部水分扩散阻力小,桑葚渣内部温度低于表面,形成温度梯度差,且内部水分含量高于外部,形成水分梯度,使得水分快速向外迁移。随着干燥过程地进行,桑葚渣内部水分自由度逐渐降低,不易流动水占主导,导致内部迁移速度低于表面水分蒸发速度,桑葚渣表面结块硬化,水分的扩散受到内外阻力,导致干燥速率逐渐降低[18]。随着干燥温度的升高,HAD和HPD两种干燥方式干燥时间均显著缩短,HAD组在50、60、70 ℃条件下达到目标含水量所需时间分别为12.0、5.0、4.5 h;HPD组在相同温度下耗时仅为10.0、3.5、2.5 h。进一步分析发现,HAD组由50 ℃升至60 ℃时,干燥时间缩短58.3%,由60 ℃升至70 ℃时,干燥时间缩短10%,类似地,HPD组由50 ℃升至60 ℃时干燥时间缩短65.0%,由60 ℃升至70 ℃时,干燥时间缩短28.6%。上述结果表明,在干燥后期,部分水与桑葚渣结合较为紧密,在较低干燥温度(50 ℃)下难以脱除,需进一步提升干燥温度,才能有效提高干燥效率。
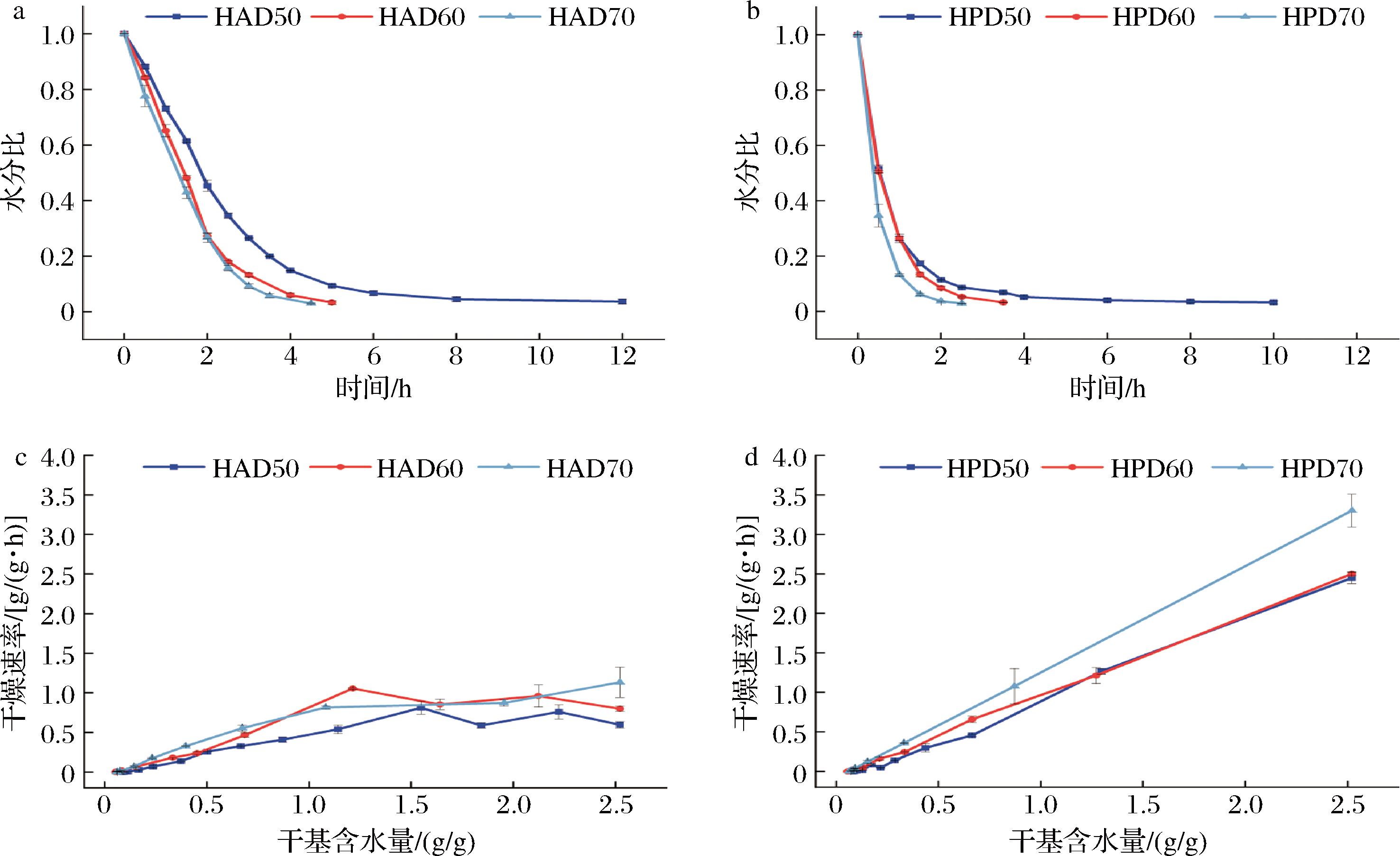
a-HAD水分比曲线图;b-HPD水分比曲线图;c-HAD干燥速率曲线图;d-HPD干燥速率曲线图
图1 不同干燥方式及温度的桑葚渣干燥特性曲线
Fig.1 Drying characteristics of mulberry pomace under different drying methods and temperatures
在相同干燥温度下,HPD组的干燥速率显著高于HAD组(图1-c和图1-d),在50~70 ℃的温度区间,HPD组的干燥速率较HAD组提升了16.7%~44.4%,这主要是因为HAD主要通过热空气逐渐蒸发物料表面的水分,而HPD可调节干燥仓内相对湿度,使桑葚渣内部水分形成更大的湿度差,从而增强了干燥过程中水分迁移动力,驱使水分更快向表面迁移,提升干燥速率[19]。
2.2 干燥方式及温度对桑葚渣粉体色泽的影响
如表2和图2所示,经干燥并粉碎的桑葚渣L*、a*和C值均显著高于未脱水的桑葚渣(P<0.05),表明干燥提高了桑葚渣的亮度、红值,改善了桑葚渣整体色泽饱和度;b*和h°值显著低于未脱水的桑葚渣(P<0.05),b*为负值,表明干燥后蓝色调增强,h°均在270°~360°,干燥后h°降低,色调向红紫色区间偏移。干燥过程a*值升高,b*值下降是因为花色苷发生降解,并且长时间与空气接触,导致其发生氧化褐变;而L*值的升高,可能是因为干燥后的桑葚渣经过粉碎,使粉体粒径变小,导致粉体的颜色变亮;此外,粉碎过程中机械摩擦产热,色素类物质发生分解转化,也会导致粉体颜色发生变化[20]。对于干燥桑葚渣粉体而言,VFD组的L*值显著高于HAD和HPD组(P<0.05),这是因为VFD组样品预冷冻形成了稳定的细胞结构,并且样品疏松多孔,从而提高了亮度[19];HAD组与HPD组的ΔE值无显著性差异(P>0.05),说明在所选50~70 ℃条件下,HAD和HPD方式和温度的变化不会对桑葚渣粉体色泽造成显著影响。

图2 不同干燥方式与温度条件下桑葚渣及对应粉体的外观图
Fig.2 Appearance diagrams of mulberry pomace and corresponding powders under different drying methods and temperatures
表2 不同干燥方式及温度对桑葚渣粉体色泽的影响
Table 2 Effect of different drying methods and temperatures on the color of mulberry pomace powder

样品L∗a∗b∗ΔECh°湿桑葚渣28.05±0.64c1.62±0.18c-0.12±0.05a-1.53±0.10d355.75±1.57aVFD41.22±0.19a2.12±0.10b-0.87±0.07bc13.21±0.19a2.29±0.07bc337.65±2.41bHAD5040.39±0.16b2.32±0.25ab-1.18±0.05d12.42±0.18b2.60±0.24ab332.84±1.72cHAD6040.40±0.36b2.19±0.24b-0.87±0.06bc12.35±0.49b2.23±0.10c337.19±0.73bHAD7040.33±0.19b2.30±0.38ab-1.00±0.06c12.32±0.17b2.67±0.33a314.57±1.56d
续表2
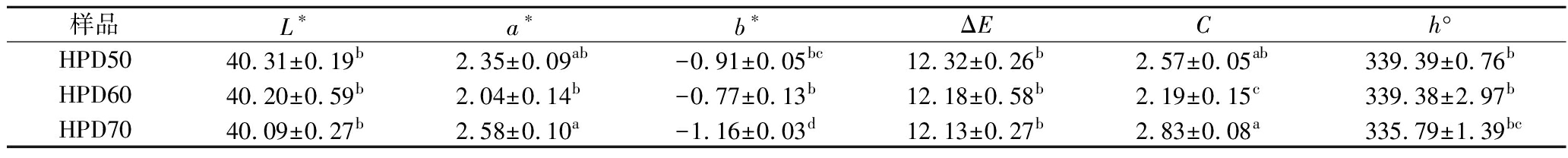
样品L∗a∗b∗ΔECh°HPD5040.31±0.19b2.35±0.09ab-0.91±0.05bc12.32±0.26b2.57±0.05ab339.39±0.76bHPD6040.20±0.59b2.04±0.14b-0.77±0.13b12.18±0.58b2.19±0.15c339.38±2.97bHPD7040.09±0.27b2.58±0.10a-1.16±0.03d12.13±0.27b2.83±0.08a335.79±1.39bc
注:表中小写字母表示不同样品间存在显著性差异(P<0.05)(下同)。
2.3 干燥方式及温度对桑葚渣粉体微观结构的影响
如图3所示,VFD组的桑葚渣粉表面相对光滑,呈不规则片状、颗粒大小和分布不均,这主要是因为VFD组是直接升华除去桑葚渣中的水分,并且范德华力在低温下较稳定[21],使样品保持了原有组织结构。相比之下,HAD组、HPD组的桑葚渣粉体表面均出现不同程度的褶皱,呈不规则球形颗粒状,大小不一、分布不均,这是由于干燥过程中物料受湿度、温度和热风的影响形成较大的表面张力,样品外部表面先达到干燥终点,内部水分不断向外部迁移,出现收缩变形、结块,使得颗粒表面粗糙。粉体微观结构特性的差异,会造成粉体物理特性的变化。

图3 不同干燥方式和干燥温度条件下桑葚渣粉体的SEM图
Fig.3 SEM images of mulberry pomace powder after drying under different methods and temperatures
2.4 干燥方式及温度对桑葚渣粉体粒径、离散度、比表面积的影响
粒径、离散度和比表面积是描述粉体颗粒大小和均匀度的重要指标,离散度越小,粉体分布越均匀;比表面积越大,则粉体粒径越小[22]。如表3所示,VFD组的粒径、离散度和比表面积与HAD组、HPD组之间均存在显著性差异(P<0.05),不同干燥温度HAD与HPD组间也存在一定的差异。
表3 不同干燥方式及温度对桑葚渣粉体粒径、离散度、比表面积的影响
Table 3 Effect of different drying methods and temperatures on particle size, dispersion, and specific surface area of mulberry pomace powder
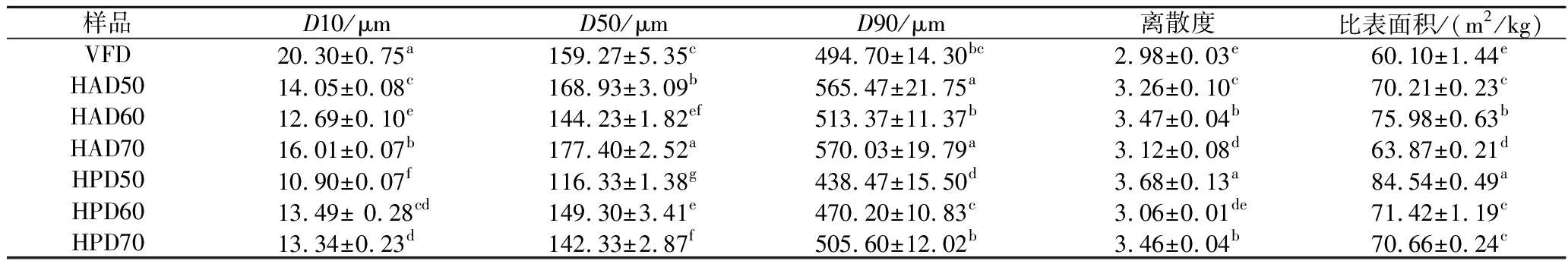
样品D10/μmD50/μmD90/μm离散度比表面积/(m2/kg)VFD20.30±0.75a159.27±5.35c494.70±14.30bc2.98±0.03e60.10±1.44eHAD5014.05±0.08c168.93±3.09b565.47±21.75a3.26±0.10c70.21±0.23cHAD6012.69±0.10e144.23±1.82ef513.37±11.37b3.47±0.04b75.98±0.63bHAD7016.01±0.07b177.40±2.52a570.03±19.79a3.12±0.08d63.87±0.21dHPD5010.90±0.07f116.33±1.38g438.47±15.50d3.68±0.13a84.54±0.49aHPD6013.49± 0.28cd149.30±3.41e470.20±10.83c3.06±0.01de71.42±1.19cHPD7013.34±0.23d142.33±2.87f505.60±12.02b3.46±0.04b70.66±0.24c
VFD组离散度、比表面积比HAD组、HPD组样品小,表明VFD组颗粒大小均匀,但粉体粒径较大;HPD50组离散度、比表面积最大,表明颗粒大小均匀度最差,但粉体粒径小,其D10、D50和D90分别为10.90、116.33、438.47 μm,均小于其他干燥处理组。桑葚渣粉体颗粒大小的均匀性差异是由于不同干燥方法的水分脱除方式造成的,VFD组物料中的大部分水分在升华阶段缓慢去除,干燥后的桑葚渣硬度不足,不易粉碎成小颗粒;相比之下,HAD组、HPD组初期水分含量迅速下降,导致物料内部温度和湿度分布不均,干燥过程物料出现皱缩、团聚等现象[23],导致果渣粉碎成不同颗粒大小,粉体颗粒均匀性差。
2.5 干燥方式及温度对桑葚渣粉体持水性、持油性、溶解性、堆积密度、休止角的影响
如表4所示,不同干燥方式和温度制备的桑葚渣粉持水性无显著差异(P>0.05),VFD组持油性(4.87 g/g)、溶解性(32.36%)显著高于HAD和HPD组(P<0.05),不同干燥温度HAD和HPD组持油性无显著差异(P>0.05),溶解性随干燥温度的升高呈上升趋势。果蔬粉的持油性和溶解性与其粉体结构有关,VFD组桑葚渣粉结构疏松,有利于增大其接触面积,使亲油基团、亲水基团暴露在油、水相中[24],提升了样品持油性和溶解性。
表4 不同干燥方式及温度对桑葚渣粉体持水性、持油性、溶解性、堆积密度、休止角的影响
Table 4 Effects of different drying methods and temperatures on water retention, oil retention, solubility, packing density, and resting angle of mulberry pomace powder

样品持水性/(g/g)持油性/(g/g)溶解性/%堆积密度/(g/cm3)休止角/°VFD4.08±0.18a4.87±0.10a32.36±0.29a0.26±0.03b48.52±1.81aHAD503.66±0.71a3.19±0.18b24.11±1.55c0.44±0.01a40.87±1.04bHAD603.57±0.48a3.30±0.42b26.36±0.70b0.44±0.01a43.29±0.83bHAD703.18±0.31a3.45±0.22b28.01±1.17b0.45±0.01a39.74±0.58bHPD504.01±0.51a3.38±0.47b26.15±0.48bc0.45±0.01a40.68±0.86bHPD603.50±0.86a3.16±0.37b25.77±1.52bc0.45±0.01a43.10±1.31bHPD703.54±0.06a3.25±0.17b27.77±1.03b0.44±0.01a42.83±4.62b
堆积密度与粉体粒径大小、颗粒结构密切相关,堆积密度越小,则粉体越疏松;休止角反映粉体流动性,休止角越大则流动性越差。如表4所示,不同干燥温度HAD和HPD组粉体间堆积密度和休止角无显著性差异(P>0.05),而VFD组桑葚渣粉体堆积密度显著小于HAD和HPD组,休止角显著大于HAD和HPD组,表明冷冻干燥制备的桑葚渣粉较HAD和HPD的堆积起来更疏松更稳定,不易流动。这与VFD组呈不规则片状微观结构有关(图3),不规则的片状会导致颗粒间的摩擦力和表面聚合力增加,而HAD和HPD组制备的粉体由于干燥过程体积收缩,粉碎后更倾向于球形颗粒状,使颗粒间接触面减小,摩擦力减少,提升了粉体颗粒的流动性。
2.6 干燥方式及温度对可溶性糖和还原糖的影响
如图4所示,HAD和HPD组可溶性糖含量显著高于VFD组(P<0.05),HAD50组最高为309.4 mg/g,这是因为桑葚渣中残留的纤维素酶、果胶酶等在热干燥过程中水解了部分纤维和果胶大分子物质,导致样品可溶性糖含量显著高于VFD组,HAD50组干燥温度较低、时间最长,因此水解产生的可溶性糖含量最高。HPD50、HPD60、HPD70组的可溶性糖含量无显著差异(P>0.05),是因为干燥速率快,导致水解的可溶性糖含量差异不大。
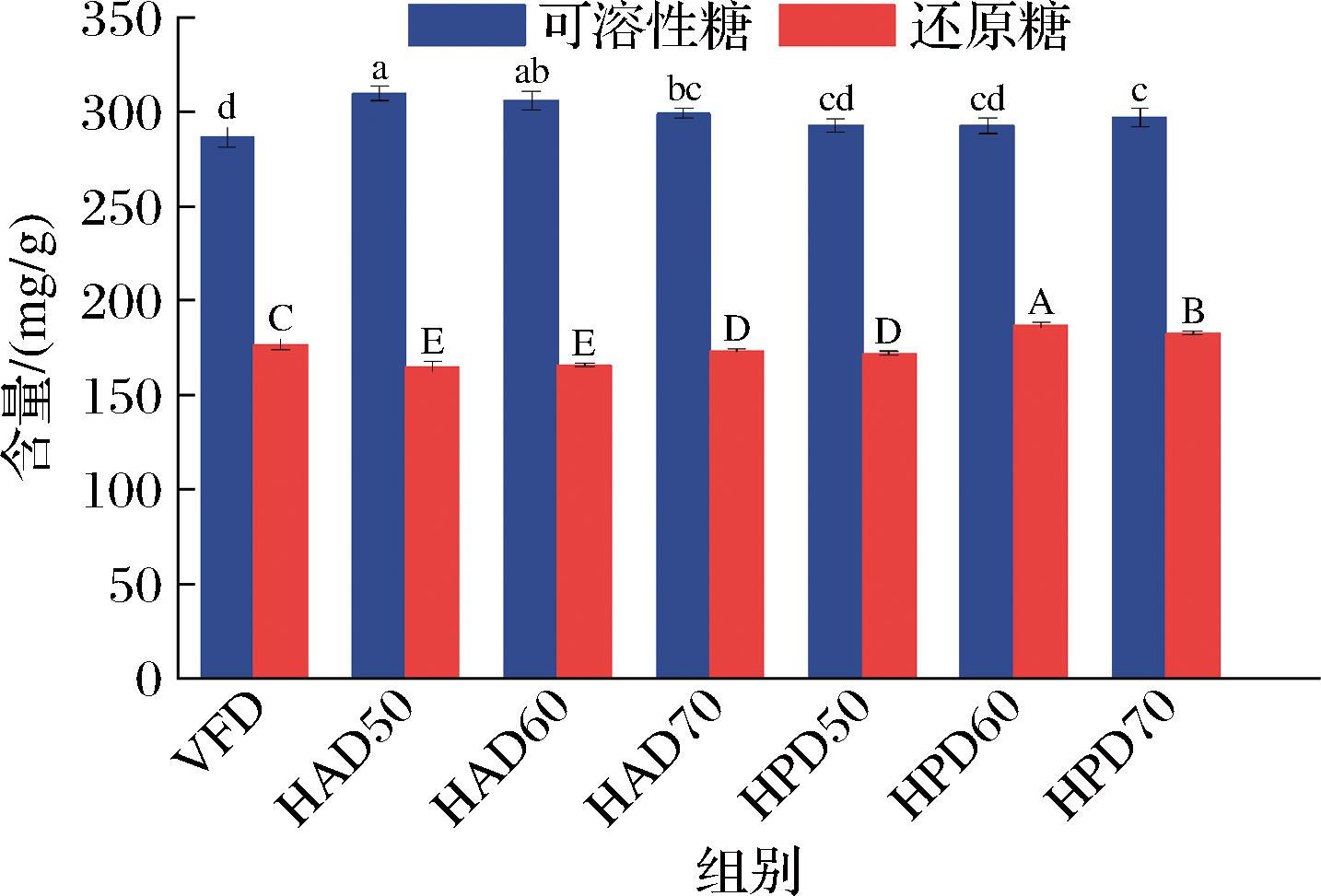
图4 不同干燥方式及温度对可溶性糖和还原糖的影响
Fig.4 Effect of different drying methods and temperatures on soluble and insoluble sugars of mulberry pomace powder
注:不同字母表示组间存在显著差异(P<0.05)(下同)。
在热干燥过程中桑葚渣还原糖含量是动态变化的,一方面糖类物质的热分解会生成还原糖,另一方面干燥过程因温度和时间的影响会发生不同程度的氧化反应,使还原糖可能被氧化为其他产物,从而降低还原糖含量[25]。如图4所示,HPD60、HPD70组还原糖含量显著高于VFD组(P<0.05),HAD50~HAD70组及HPD50组显著低于VFD组(P<0.05)。这是因为VFD组是在真空和低氧环境下进行干燥,减少了氧化反应带来的还原糖量消耗,同时糖类物质也未受热分解产生还原糖,最终维持基础还原糖水平;HPD60、HPD70组干燥时间较短,减少了氧化反应的时间,因此HPD60、HPD70组还原糖含量较VFD组高,而较高温度(HPD70组)虽加速糖类热解,但同时也会加剧氧化反应,导致HPD70组还原糖含量低于HPD60组。同样地,HAD50~HAD70组及HPD50组因干燥时间长,增加了氧化反应的时间,使其还原糖含量低于VFD组。
2.7 干燥方式及温度对酚类物质和花色苷的影响
如图5-a所示,VFD组总酚(56.3 mg/g)和总黄酮(59.6 mg/g)的含量最高,显著高于HAD与HPD组(P<0.05),这是由于多酚氧化酶(polyphenol oxidase, PPO)和过氧化物酶(peroxidase, POD)在VFD的低温和真空环境受到抑制[26],有效控制了多酚类物质降解。HAD和HPD组,随着温度的升高,总酚和总黄酮含量均呈现出先上升再下降的趋势,这是由于PPO和POD活性在40~50 ℃时较高,会导致酚类物质降解,60 ℃时PPO活性随着干燥时间的延长逐渐降低;70 ℃时虽PPO和POD活性显著降低,但高温同样会导致酚类物质受热降解[27-28]。总黄酮同样受PPO和POD的影响[29],因此与总酚呈现一致趋势。在同温度下,HAD50组干燥时间长,PPO和POD活性较活跃,使酚类化合物含量较HPD50组低;不同的是,HAD60、HAD70组酚类物质含量分别高于HPD60、HPD70组,这可能是因为HPD60、HPD70组干燥速率较HAD60、HAD70组更快,同时诱导了酚类物质的快速降解,但具体原因仍需进一步探究。整体而言,无论采用HAD还是HPD,均在温度为60 ℃时,桑葚渣中总酚、黄酮含量最高。
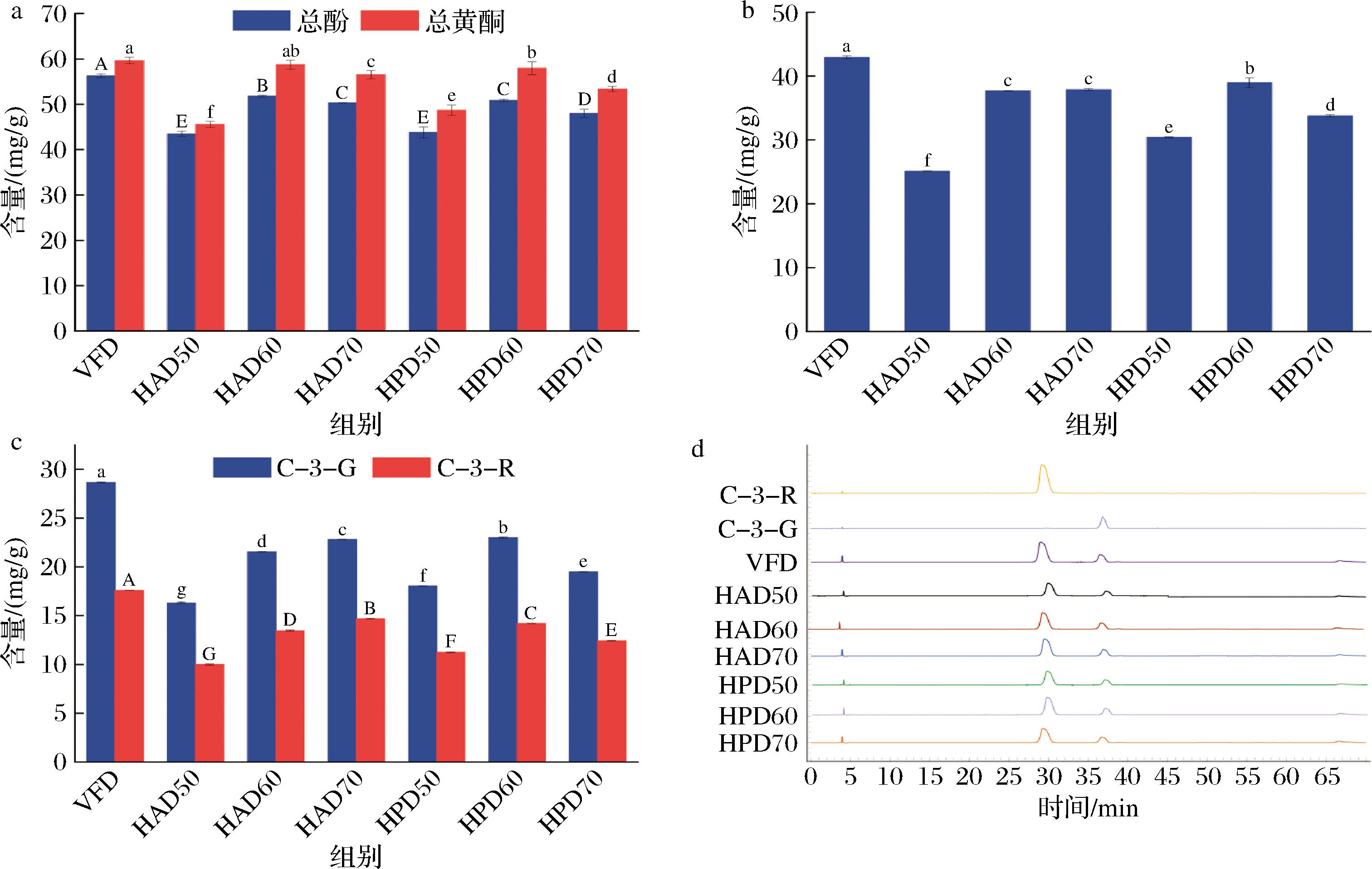
a-桑葚渣粉总酚、总黄酮含量;b-桑葚渣粉总花色苷含量;c-桑葚渣粉C-3-G、C-3-R含量;d-桑葚渣粉C-3-G、C-3-R液相谱图
图5 不同干燥方式及温度对桑葚渣酚类物质和花色苷的影响
Fig.5 Effect of different drying methods and temperatures on phenolic substances and anthocyanins of mulberry pomace powder
不同干燥方式及温度桑葚渣中总花色苷如图5-b所示,C-3-G和C-3-R含量和液相图谱如图5-c和图5-d所示。VFD组总花色苷(42.9 mg/g)、C-3-G(28.6 mg/g)和C-3-R(17.6 mg/g)含量均显著高于HAD与HPD组(P<0.05),这是因为花色苷为多酚类化合物,同样受PPO和POD影响,真空和低温减少花色苷降解。值得注意的是,HPD组总花色苷及其单体物质也呈现出随温度升高呈先上升再下降的趋势,HPD60组总花色苷和C-3-G含量较接近VFD组,说明60 ℃能较好保留酚类物质。
2.8 干燥方式及温度对桑葚渣粉抗氧化活性的影响
DPPH、ABTS和FRAP分别针对不同的抗氧化机制,DPPH法主要检测自由基清除能力,ABTS法检测的是电子转移能力,FRAP法则检测铁离子还原能力,能够从不同角度评估样品抗氧化活性[30]。因此,同一样品不同评估方法测定的抗氧化活性存在差异(图6)。VFD组DPPH(88.0 mg/g)、ABTS(151.6 mg/g)、FRAP(142.7 mg/g)的抗氧化活性均显著高于HAD与HPD组,这是因为HAD与HPD组在干燥过程中会激活PPO等氧化酶且热敏性抗氧化物质会因温度发生降解[31]。此外,HAD和HPD两种干燥方式下,60 ℃干燥制备样品抗氧化活性均高于其他温度,且HAD60组的抗氧化活性显著高于HPD60组。进一步分析发现,HAD与HPD组随着温度的升高,其抗氧化性呈现与总酚、总黄酮含量同步的“先上升再下降”变化趋势,这是因为酚类和黄酮类化合物中酚羟基结构里的邻位酚羟基很容易被氧化成醌类结构,导致其对活性氧等自由基具有很强的捕捉能力[32],这也让植物源多酚和黄酮成为抗氧化作用的重要功能成分及主要贡献因子[31,33],因而样品抗氧化性与总酚、总黄酮含量的趋势一致。
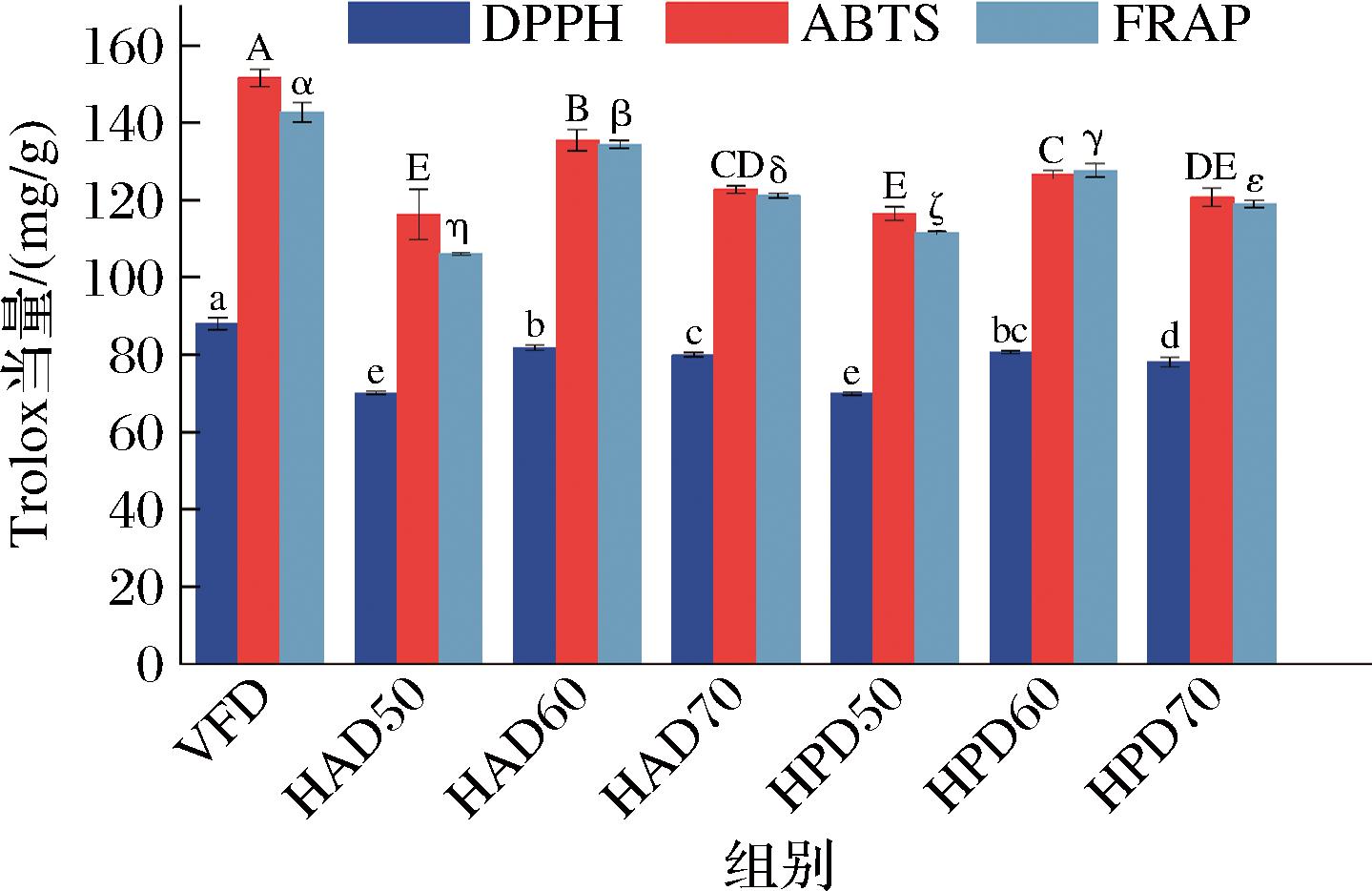
图6 不同干燥方式及温度对桑葚渣抗氧化活性的影响
Fig.6 Effect of different drying methods and temperatures on antioxidant activity of mulberry pomace powder
2.9 干燥方式及温度对桑葚渣粉风味的影响
如图7-a所示,桑葚渣粉的挥发性香气成分主要被W1W、W2W和W5S 3个传感器识别,如表1所示,3个传感器分别对应硫化物、有机硫化物、氮氧化合物。7组不同干燥条件下桑葚渣粉的风味轮廓大致相同,但响应程度有所差异,VFD组的W1W、W2W、W5S响应值均大于其他6组,表明冷冻干燥可以有效保留桑葚渣的风味,这是由于VFD较低的温度和真空环境,减少了因温度引起的氧化、降解和酶促反应,能更好地保留风味[34]。对比不同HAD和HDP组发现,在硫化物、有机硫化物的保留上HAD70组最接近VFD组,可能因为HAD70组干燥时间相对较短,且干燥过程中无HPD的强制循环排湿,风味成分逸散减少。
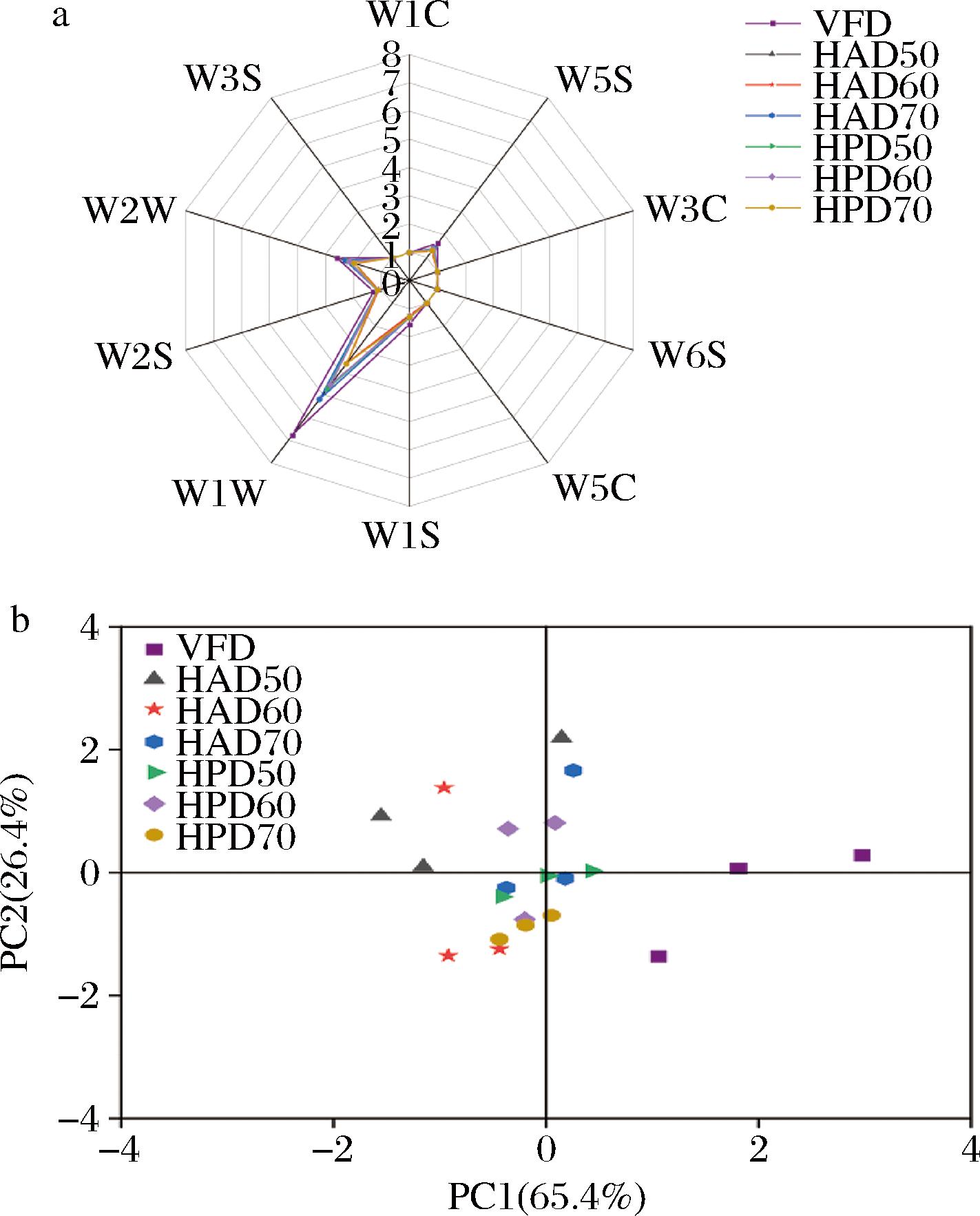
a-电子鼻响应值;b-电子鼻PCA图
图7 不同干燥方式及温度下电子鼻响应值雷达图与电子鼻PCA图
Fig.7 Radar diagram and PCA diagram of electronic nose response of mulberry pomace powder dried with different drying methods and temperatures
为进一步评价不同干燥条件下桑葚渣风味的差异,基于电子鼻传感器的响应值进行了主成分分析(principal component analysis,PCA),结果如图7-b。PC1和PC2的贡献率分别为65.4%和26.4%,累积贡献率为91.8%(>85%),表明经该模型分析出来的2种主成分包括了桑葚渣主要挥发性气味化合物信息,结果具有可靠性[35]。在结果分析中,风味相似度较高的组分会重叠在一起或距离相近[36],VFD组、HAD和HPD组样品之间挥发性香气区域数据点整体较为集中,VFD组在PC1轴上与其他样品有明显区分,而其他样品在PC1和PC2轴上均有部分重叠,表明VFD组与HAD组、HPD组风味存在一定差异,而HAD和HPD组样品间风味差异并不明显。
3 结论
本实验采用VFD、HAD(50、60、70 ℃)、HPD(50、60、70 ℃)制备桑葚渣粉。VFD虽能较好地保持桑葚渣粉的物理特性、营养成分、抗氧化活性和风味,但其微观结构呈不规则片状,流动性差,且干燥时间长,耗能高,不适合桑葚渣的工业化生产。相较而言,采用HPD和HAD制备的桑葚渣粉体在色泽、微观结构、持水性、持油性、堆积密度和休止角等指标上并无显著差异。但在风味和活性成分保留方面,HAD70组的风味响应值、C-3-R含量,HPD60组的总花色苷、C-3-G与VFD组较接近;HAD60组不仅可溶性糖含量显著高于VFD组,其总酚、总黄酮、DPPH、ABTS、FRAP等指标也与VFD组最为接近,同时干燥耗时显著缩短了83.3%。综上所述,HAD60和HPD60组的综合干燥品质最接近VFD,因此HAD/HPD 60 ℃是桑葚渣工业化干燥的适宜工艺参数,在有效保留桑葚渣粉营养物质含量和功能特性的同时,实现节能干燥,本研究可以为桑葚渣干燥及其进一步加工利用提供一定的理论依据。
[1] 诸梦洁. 桑葚渣粗提物降糖活性成分稳定性研究及微胶囊制备[D].南京:南京农业大学, 2019.
ZHU M J.Study on the stability and microcapsulation of active components in mulberry residue crude extract[D].Nanjing:Nanjing Agricultural University, 2019.
[2] 张文娜, 魏萌, 韩爱云, 等.桑葚果实、桑葚干酒和桑葚利口酒中酚类化合物的高效液相色谱串联电喷雾二级质谱分析及其抗氧化活性比较[J].食品与发酵工业, 2024,50(14):246-252.
ZHANG W N, WEI M, HAN A Y, et al.High performance liquid chromatography-electron spray ionization-mass spectrometry/mass spectrometry analysis of phenolic compounds in berry, dry wine, liqueur of mulberry and comparison of the antioxidant activities[J].Food and Fermentation Industries, 2024,50(14):246-252.
[3] KHALIFA I, ZHU W, LI K K, et al.Polyphenols of mulberry fruits as multifaceted compounds:Compositions, metabolism, health benefits, and stability:A structural review[J].Journal of Functional Foods, 2018, 40:28-43.
[4] 栾琳琳. 桑葚果渣花青素的提取及稳定性研究[D].贵阳:贵州大学, 2020.
LUAN L L.Study on the extraction and stability of anthocyanins from mulberry pomace[D].Guiyang:Guizhou University, 2020.
[5] 盛金凤, 何雪梅, 唐雅园, 等.桑葚全果粉与果渣粉对曲奇饼干品质和抗氧化特性的影响[J].食品工业科技, 2021, 42(10):1-7.
SHENG J F, HE X M, TANG Y Y, et al.Effects of mulberry powder and mulberry pomace powder on the quality and antioxidant properties of cookies[J].Science and Technology of Food Industry, 2021, 42(10):1-7.
[6] 赵金梅, 孙蕊, 巩丽莉, 等.干燥方式对沙枣花品质和挥发性风味成分的影响[J].食品科学, 2020, 41(22):265-270.
ZHAO J M, SUN R, GONG L L, et al.Effects of different drying methods on nutritional and volatile aroma components in flowers of elaegnus angustifolia[J].Food Science, 2020, 41(22):265-270.
[7] ZHANG M M, WU C Y, ZHANG H X, et al.Comparison of different drying technologies for kiwifruit pomace:Changes in physical characteristics, nutritional properties and antioxidant capacities[J].Food Chemistry, 2024, 451:139497.
[8] XIONG X, CAO X J, ZENG Q Z, et al.Effects of heat pump drying and superfine grinding on the composition of bound phenolics, morphology and microstructure of lychee juice by-products[J].LWT, 2021, 144:111206.
[9] 苟小菊, 刘冬, 杨曦, 等.热风干燥温度对新疆红肉苹果粉品质的影响[J].食品科学, 2018, 39(21):87-93.
GOU X J, LIU D, YANG X, et al.Effect of drying temperature on the quality of apple powder made from red-fleshed apples grown in Xinjiang[J].Food Science, 2018, 39(21):87-93.
[10] 范铭, 刘哲, 曹艳, 等.不同干燥方式对桑葚渣提取物主要活性成分及α-淀粉酶抑制活性的影响[J].浙江农业科学, 2018, 59(10):1911-1914;1916.
FAN M, LIU Z, CAO Y, et al.Effects of different drying methods on main active components and α-amylase inhibitory activity of mulberry pomace extract[J].Journal of Zhejiang Agricultural Sciences, 2018, 59(10):1911-1914;1916.
[11] DONG R H, LIAO W, XIE J H, et al.Enrichment of yogurt with carrot soluble dietary fiber prepared by three physical modified treatments:Microstructure, rheology and storage stability[J].Innovative Food Science &Emerging Technologies, 2022, 75:102901.
[12] 方晓彤, 王前菊, 穆波, 等.超声波辅助酶法处理对百香果出汁率及品质的影响[J].食品安全质量检测学报, 2024, 15(10):234-242.
FANG X T, WANG Q J, MU B, et al.Effects of ultrasonic assisted enzymatic treatment on juice yield and quality of passion fruit[J].Journal of Food Safety &Quality, 2024, 15(10):234-242.
[13] 卢靖辉, 温靖, 赖慧宁, 等.不同浓缩方式对枸杞汁品质特性的影响[J].食品工业科技, 2025, 46(3):31-40.
LU J H, WEN J, LAI H N, et al.Effect of different concentration methods on quality characteristics of Lycium chinense juice[J].Science and Technology of Food Industry, 2025, 46(3):31-40.
[14] 邹颖, 余元善, 邹波, 等.桑葚渣多酚提取物冻干粉的制备及稳定性分析[J].食品科学, 2021, 42(1):73-78.
ZOU Y, YU Y S, ZOU B, et al.Preparation and stability of freeze-dried polyphenol extracted from mulberry juice processing residues[J].Food Science, 2021, 42(1):73-78.
[15] HOU S B, ZHAO Q S, CHANG S L, et al.Effect of superfine grinding on the physico-chemical and antioxidant properties of Cistanche deserticola powders[J].Journal of Food Process Engineering, 2023, 46(5):e14319.
[16] 沈袁媛, 郑太极, 王保忠, 等.梅花茶窨制工艺创新及抗氧化能力研究[J].食品科技, 2024, 49(4):92-99.
SHEN Y Y, ZHENG T J, WANG B Z, et al.Research on scenting process innovation and antioxidant capacity of plum blossom tea[J].Food Science and Technology, 2024, 49(4):92-99.
[17] 李丽霞, 张浩, 林宇浩, 等.电子鼻结合GC-MS鉴别不同部位的三七粉[J].食品科学, 2023, 44(20):321-329.
LI L X, ZHANG H, LIN Y H, et al.Identification of Panax notoginseng powders from different root parts using electronic nose and gas chromatography-mass spectrometry[J].Food Science, 2023, 44(20):321-329.
[18] BI Y X, ZIELINSKA S, NI J B, et al.Effects of hot-air drying temperature on drying characteristics and color deterioration of rape bee pollen[J].Food Chemistry:X, 2022, 16:100464.
[19] MA Q C, BI J F, YI J Y, et al.Stability of phenolic compounds and drying characteristics of apple peel as affected by three drying treatments[J].Food Science and Human Wellness, 2021, 10(2):174-182.
[20] MA L K, CHEN K, TIAN X F, et al.Effect of particle size on the physicochemical property of the peel powder from Aloe barbadensis[J].IOP Conference Series:Earth and Environmental Science, 2020, 612(1):012005.
[21] TIAN J, YU Y, WANG Y, et al.Tannic acid-induced surface-catalyzed secondary nucleation during the amyloid fibrillation of hen egg-white lysozyme[J].International Journal of Molecular Sciences, 2018, 19(12):4009.
[22] 李明娟, 王颖, 张雅媛, 等.5种干燥方式对木薯酸淀粉性能的影响[J].食品工业科技, 2024, 45(8):134-142.
LI M J, WANG Y, ZHANG Y Y, et al.Effects of five drying methods on the properties of sour cassava starch[J].Science and Technology of Food Industry, 2024, 45(8):134-142.
[23] 巨浩羽, 赵海燕, 张卫鹏, 等.相对湿度对胡萝卜热风干燥过程中热质传递特性的影响[J].农业工程学报, 2021, 37(5):295-302.
JU H Y, ZHAO H Y, ZHANG W P, et al.Effects of relative humidity on heat and mass transfer characteristics of carrot during hot air drying[J].Transactions of the Chinese Society of Agricultural Engineering, 2021, 37(5):295-302.
[24] JIANG Z M, ZHANG M H, HUANG Y X, et al.Comparison and characterization of the structure and physicochemical properties of three citrus fibers:Effect of ball milling treatment[J].Foods, 2022, 11(17):2665.
[25] LIN Q N, HAN L P, LIU G Q, et al.A preliminary study on the formation pathways of glycated phosphatidylethanolamine of food rich in phospholipid during the heat-processing[J].RSC Advances, 2018, 8(21):11280-11288.
[26] 陈红惠, 张鲁梅.不同干燥方式对山药品质的影响[J].食品工业, 2020, 41(11):195-199.
CHEN H H, ZHANG L M.Effects of different drying methods on quality of Chinese yam[J].The Food Industry, 2020, 41(11):195-199.
[27] CIOU J Y, LIN H H, CHIANG P Y, et al.The role of polyphenol oxidase and peroxidase in the browning of water caltrop pericarp during heat treatment[J].Food Chemistry, 2011, 127(2):523-527.
[28] 刘钊含, 杨同香, 许韩山, 等.干燥方式对百香果皮理化、功能及抗氧化特性的影响[J].食品与机械, 2023, 39(10):166-174.
LIU Z H, YANG T X, XU H S, et al.The influence of drying methods on the physicochemical, functional, and antioxidant properties of passion fruit peel[J].Food &Machinery, 2023, 39(10):166-174.
[29] 杨婉如, 余洋洋, 陈树鹏, 等.不同热泵干燥温度对柑橘果皮品质的比较分析[J].现代食品科技, 2021, 37(6):237-243.
YANG W R, YU Y Y, CHEN S P, et al.Quality of Citrus peels dried at different temperatures using heat pump[J].Modern Food Science and Technology, 2021, 37(6):237-243.
[30] HUANG D J, OU B X, PRIOR R L.The chemistry behind antioxidant capacity assays[J].Journal of Agricultural and Food Chemistry, 2005, 53(6):1841-1856.
[31] KUMAR D, LADANIYA M S, GURJAR M, et al.Impact of drying methods on natural antioxidants, phenols and flavanones of immature dropped Citrus sinensis L.Osbeck fruits[J].Scientific Reports, 2022, 12:6684.
[32] 邵佩兰, 徐明, 郭晓丹, 等.红枣色素中活性成分含量与抗氧化活性的相关性[J].食品工业科技, 2016, 37(17):171-174.
SHAO P L, XU M, GUO X D, et al.Correlation between active component contents and antioxidant activity of jujube pigment[J].Science and Technology of Food Industry, 2016, 37(17):171-174.
[33] ZHENG Y, ZHAO L, YI J J.Phytochemical characterization and antioxidant and enzyme inhibitory activities of different parts of Prinsepia utilis royle[J].Journal of Food Quality, 2022, 2022(1):9739851.
[34] HOU S T, ZHANG D F, YU D M, et al.Effect of different drying methods on the quality of Oudemansiella raphanipes[J].Foods, 2024, 13(7):1087.
[35] 盛梦龙, 林松毅, 马婷婷, 等.不同干燥方式对香菇粉物化特性、抗氧化活性和风味的影响[J].食品科学, 2024, 45(19):192-200.
SHENG M L, LIN S Y, MA T T, et al.Effects of different drying methods on physicochemical properties, antioxidant activity and flavor profile of Lentinus edodes powder[J].Food Science, 2024, 45(19):192-200.
[36] 薛晶晶, 李山, 许志杰, 等.干燥方式对糯米香叶干燥动力学及挥发性成分的影响[J].食品与发酵工业, 2025, 51(11):342-350.
XUE J J, LI S, XU Z J, et al.Effect of drying methods on drying kinetics and volatile components of Strobilanthes tonkinensis leaves[J].Food and Fermentation Industries, 2025, 51(11):342-350.