油桃(Prunus persica var.nectarina)果面鲜红,香味浓郁,富含多酚及维生素C、氨基酸等多种生物活性物质[1]。油桃采后呼吸旺盛,贮、运、销过程中软化、腐烂等现象较为普遍。低温保鲜是延长油桃贮藏期、保持油桃商品品质的有效方法。然而,油桃果实对低温非常敏感,0~7 ℃贮藏会诱发油桃冷害,主要表现为桃果表面凹陷、果肉浸水、褐变等,严重影响了果实的商品价值[2]。因此,减少油桃贮期冷害的发生,是油桃低温贮藏亟待解决的关键问题。
细胞膜损伤是引起桃果冷害发生的重要因素,细胞膜作为细胞的屏障,同时为一系列生化反应提供稳定的细胞内环境,完整的细胞膜是油桃采后进行正常生理代谢的前提。然而,当果实受到低温胁迫时,会使膜脂代谢发生紊乱,导致细胞膜组分和结构受到破坏,影响采后果品的保鲜效果[3]。磷脂是细胞膜脂质的重要组成部分,主要包括磷酸肌醇(phosphatidylinositol,PI)、磷脂酰胆碱(phosphatidylcholine,PC)、磷脂酸(phosphatidic acid,PA)。膜脂代谢相关酶磷脂酶D(phospholipase D,PLD)、脂氧合酶(lipoxygenase,LOX)、脂肪酶、磷脂酶A(phospholipase A,PLA)、磷脂酶 C(phospholipase C,PLC)和甘油二酯激酶(diacylglycerol kinase,DGK)通过调节膜脂组分及不饱和脂肪酸的含量,进而影响细胞膜完整性。其中PLD和PLC可以将PI和PC水解为PA和二酰基甘油,这2种水解产物可以被PLA和脂肪酶进一步降解为游离脂肪酸,或通过DGK将二酰基甘油磷酸化为PA[4-5]。此外,低温条件下PLC和PLA催化甘油磷脂降解,从而导致细胞膜发生不可逆的损伤[6]。另外,膜脂过氧化是细胞膜损伤的重要因素。LOX可将不饱和脂肪酸(亚油酸和亚麻酸)的碳碳双键氧化,使细胞膜的流动性降低,而细胞有氧代谢过程中生成的活性氧会将磷脂和不饱和脂肪酸氧化,最终产生丙二醛(malondialdehyde,MDA),不饱和脂肪酸含量下降以及MDA含量增加均会对细胞膜造成损伤[7-8]。因此,探究油桃冷害与膜脂代谢的作用机制具有重要意义。
乙烯抑制剂1-甲基环丙烯(1-methylcyclopropene,1-MCP)广泛应用于水果采后保鲜,其作用效果长久、化学性质稳定。研究表明1-MCP处理可有效降低李果[9]、枇杷果[10]、桃果[11]的冷害程度。课题组前期发现1 μL/L 1-MCP 熏蒸油桃可提升桃果的抗冷害能力,但1-MCP处理对油桃贮藏期间冷害及果皮膜脂代谢的影响尚不清楚,本研究旨在探讨1-MCP处理对油桃果实冷害和膜脂组分及相关酶活性的影响,为提高油桃采后贮藏保鲜水平,提供理论依据。
1 材料与方法
1.1 材料与试剂
‘早红宝石’油桃,2024年6月采摘于运城市临猗县角杯乡油桃种植园,采收结束后立即送至山西农业大学龙城校区,挑选大小均匀、颜色一致、无病虫害、无机械性损伤且成熟度为八成熟的果实作为试验材料。
正己烷、异丙醇、甲醇、乙酸、丙酮、氯仿、苯、石油醚,天津方大同正化工有限公司;1-MCP,安徽添福生物科技有限公司。以上试剂均为分析纯。
1.2 主要仪器与设备
HS-2900P液相色谱仪,美国Agilent公司;F920型O2/CO2气体分析仪,Felix公司;GC-14C气相色谱仪,日本岛津公司;UX620H电子天平,深圳市三利化学品有限公司;Ultrospec 2100 pro紫外线/可见光光谱分析仪,北京盛科信德科技有限公司;PLC、PLA、DGK酶检测试剂盒,上海酶联生物科技有限公司。
1.3 油桃处理方法
将油桃分为2个处理,每个处理设置3个重复,每个重复10 kg油桃。对照组(CK):油桃果实置于98 cm×98 cm×120 m密闭大帐中室温静置12 h,随后将果实放入内衬有0.02 mm保鲜袋[聚乙烯(polyethylene,PE)]的周转框中(10 kg/框)。1-MCP处理组:使用1 μL/L 1-MCP在98 cm×98 cm×120 m密闭大帐室温熏蒸12 h,熏蒸完成后将果实通风晾干2 h,最后转入内衬有0.02 mm PE保鲜袋的周转框中(10 kg/框)。以上处理好的果实均于(5±0.5) ℃、相对湿度70%~80%的保鲜库中贮藏35 d,在第0、7、14、21、28、35天对油桃果实指标进行测定。
1.4 指标测定
1.4.1 乙烯释放率、冷害指数的测定
参照XIE等[3]的方法,计算油桃冷害指数。乙烯释放率参照张新宪等[12]的方法,每个处理取油桃果实3个,置于密闭保鲜盒4 h,注射器抽取1 mL气体测定。
1.4.2 电导率及MDA含量测定
参照张新宪等[12]的方法,测定电导率、MDA含量。
1.4.3 膜脂代谢相关酶活力测定
参照WANG等[13]的方法测定,粗酶液制备:10 g油桃果皮组织加入5 mL缓冲液(pH 7.8),并研磨成浆。离心取上清液进行酶活性测定。
PLD活性测定:取500 μL酶液,随后加入1.5 mL 0.4 mg/mL 1,3-磷脂酰胆碱溶液,反应1 h。将生成的沉积物溶解于丙酮溶液,测定520 nm处吸光值。酶活力单位为U/g。
LOX活性测定:取500 μL酶液,随后加入2 mL 0.1 mg/mL亚油酸,反应10 min后,测定234 nm处吸光值。
脂肪酶活性测定:依次加入1 mL磷酸盐缓冲液(pH 7.8)、0.5 mL 0.2 mmol α-萘乙酸溶液和0.5 mL酶液。测定520 nm处吸光值。
PLC、PLA、DGK活性按照试剂盒说明书的方法进行。
1.4.4 果皮中膜磷脂的测定
参照CHEN等[14]的方法,略作修改。选取5 g果皮组织并在液氮中进行研磨,将果皮粉末与20 mL氯仿/甲醇溶剂混合液(2∶1,体积比,下同)充分混匀,于4 ℃超声波提取2 h。随后将混合液以4 ℃、10 000 r/min离心20 min。收集上清液并将其与1 mL丙酮溶液涡旋混合5 min,重复上述步骤3次。使用N2将提取物干燥,最后用5 mL氯仿/甲醇混合液溶解。取1 mL提取液用液相色谱分析,在254 nm处测定,流动相由V(N-己烷)∶V(异丙醇)∶V(甲醇)∶V(1%乙酸,体积分数)=4∶9∶5∶2组成。
1.4.5 果皮中脂肪酸含量的测定
参照CHEN等[14]的方法进行脂肪酸的提取。取液氮研磨好的果皮粉末1 g,用V(氯仿)∶V(甲醇)=2∶1溶剂抽提2次。将提取液在105 ℃下干燥得到脂肪酸的粉末。随后将上述粉末溶解在氯仿中,与V(苯)∶V(石油醚)=1∶1溶剂混合进行脂肪酸甲基化,随后将混合液与甲醇混合进行萃取,收集上清液用于进一步分析,取上清液1 mL用于气相色谱分析。色谱条件:柱温、进样口温度、检测器温度分别为195、220、240 ℃,H2、空气、N2流速分别为50、500、50 mL/min。
1.5 数据处理
采用Origin 2022绘图,实验数据均重复3次并进行显著性分析,P<0.05表示差异显著。
2 结果与分析
2.1 1-MCP处理对乙烯释放率及冷害指数的影响
油桃果皮表面水渍化是判断油桃冷害程度最直观的现象,如图1-a所示,14 d时CK组桃果出现轻微冷害症状,35 d时水渍化程度较高,桃果已经失去商品价值,而1-MCP处理后的桃果35 d时仅有轻微水渍化症状,说明1-MCP处理延缓了油桃冷害的发生。如图1-b所示,CK组油桃的乙烯释放率在0~21 d呈上升趋势,21 d时达到最大值6.82 μL/(kg·h),21~35 d逐渐降低,1-MCP处理后,油桃的乙烯释放率大幅下降,乙烯释放率高峰推迟到28 d,此时乙烯释放率为5.39 μL/(kg·h)。如图1-c所示,CK组与1-MCP组在0~7 d冷害指数均为0,14 d时CK组冷害指数为3.1%,同时期1-MCP组冷害指数仍0,至35 d时,CK组冷害指数为10.26%,为1-MCP组的5.1倍。以上结果表明,1-MCP处理可以降低油桃贮藏期间乙烯释放率的快速增加,在一定程度上降低了油桃冷害程度。
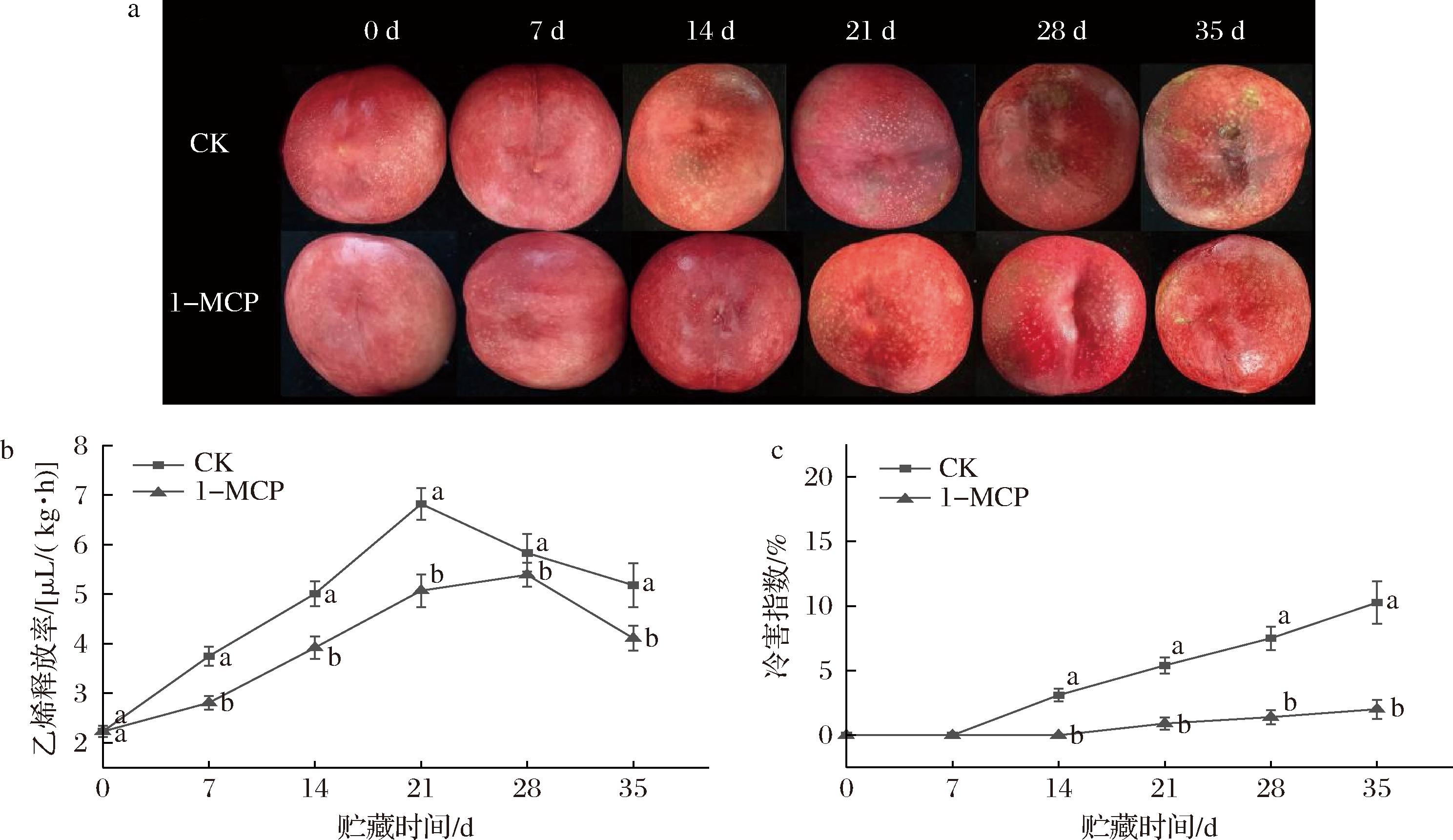
a-油桃外观品质;b-乙烯释放率;c-冷害指数
图1 1-MCP处理对油桃乙烯释放率及冷害指数的影响
Fig.1 Effect of 1-MCP treatment on appearance, ethylene release rate and cold damage index in nectarines
注:不同字母表示同一时间不同处理有显著性差异(P<0.05)(下同)。
2.2 1-MCP处理对MDA含量及相对电导率的影响
如图2-a所示,CK组油桃果实MDA积累量逐渐上升,且上升幅度较大。与CK组相比,1-MCP 处理组MDA积累量上升幅度明显受到抑制,35 d时仅为CK组的74.6%。相对电导率的变化与MDA的变化趋势较为相似,CK组油桃果实的相对电导率逐渐增大,尤其是21~28 d时,相对电导率急剧上升;而1-MCP处理组相对电导率增幅相对较小,35 d时仅为CK组的62.27%。以上结果表明,1-MCP处理可有效抑制细胞膜脂质的过氧化,有利于维持细胞膜的通透性。
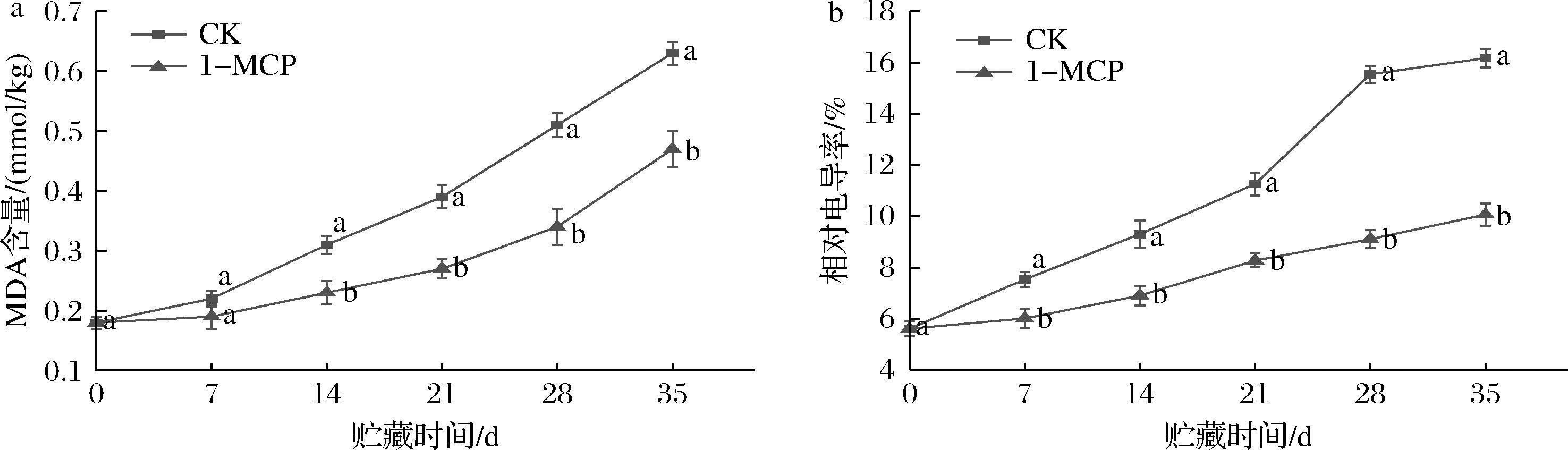
a-MDA含量;b-相对电导率
图2 1-MCP处理对油桃MDA及相对电导率的影响
Fig.2 Effect of 1-MCP treatment on MDA and relative conductivity in nectarines
2.3 1-MCP处理对膜脂代谢相关酶活性的影响
如图3-a、图3-b所示,LOX、PLD活力在贮藏前期呈上升趋势,CK组显著高于1-MCP组(P<0.05),LOX活力于21 d时达到峰值,此时CK组酶活力为1-MCP组的1.37倍,PLD活力于21 d时达到最大值,此时1-MCP组活力为CK组的77.41%。如图3-c~图3-f所示,脂肪酶、PLA,PLC和DGK活力整体呈上升趋势,1-MCP处理组脂肪酶活力在0~14 d变化并不明显,7 d时略有降低,而CK组脂肪酶活力显著增加(P<0.05),随后2个处理的脂肪酶活力逐渐增大,35 d时为1-MCP组酶活力为0.55 U/g,CK组为0.69 U/g;CK组PLA活力在35 d时为12.47 U/g,显著高于1-MCP组。CK组与1-MCP组PLC活力在0~21 d时虽然均有升高,但两者差异并不显著,21 d后CK组PLC酶活力上升幅度较大;CK组与1-MCP组DGK活力在0~7 d时变化不明显,随后CK组DGK活力大幅上升,至35 d时已达0.89 U/g,此时1-MCP组仅为0.51 U/g。以上结果表明,1-MCP处理可以抑制LOX、PLD、脂肪酶、PLA、PLC和DGK活力的升高。
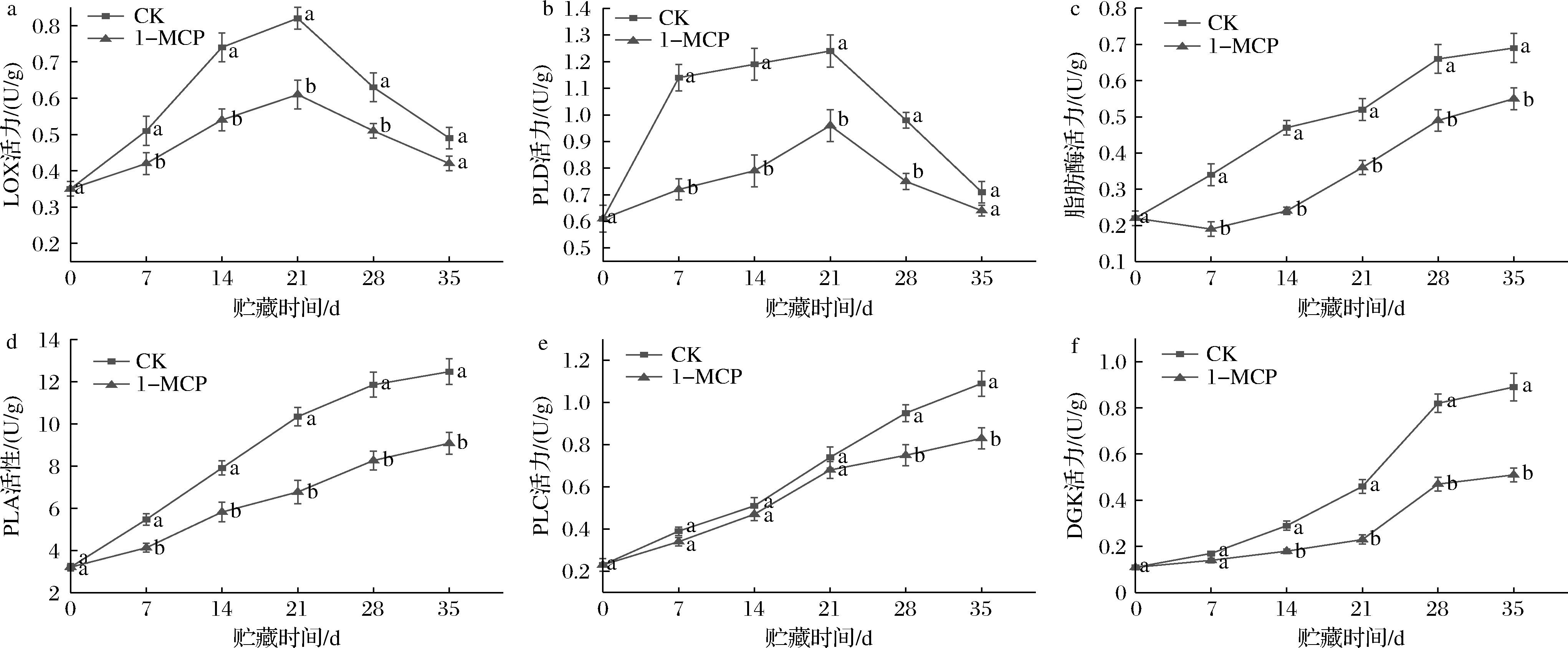
a-LOX活力;b-PLD活力;c-脂肪酶活力;d-PLA活力;e-PLC活力;f-DGK活力
图3 1-MCP处理对膜脂代谢相关酶的影响
Fig.3 Effect of 1-MCP treatment on membrane lipid metabolism related enzymes
2.4 1-MCP处理对膜磷脂成分的影响
如图4-a所示,贮藏期间油桃果实的PC含量下降较为明显,1-MCP处理可以减缓PC含量的大幅下降,35 d时较CK组提高了11.86%;如图4-b所示,PI含量变化与PC含量变化趋势较为相似,但PI含量在0~14 d与28~35 d时下降幅度较小,而14~28 d时急剧减少,28 d时CK组、1-MCP组PI含量较贮藏初始时分别减少了27.78%、19.69%。如图4-c所示,虽然不同处理的桃果实PA含量逐渐增加,但0~35 d期间1-MCP处理组桃果实PA含量均显著低于CK组(P<0.05)。以上研究结果表明,1-MCP处理明显抑制了PA的生物合成,迟滞了细胞膜的降解。
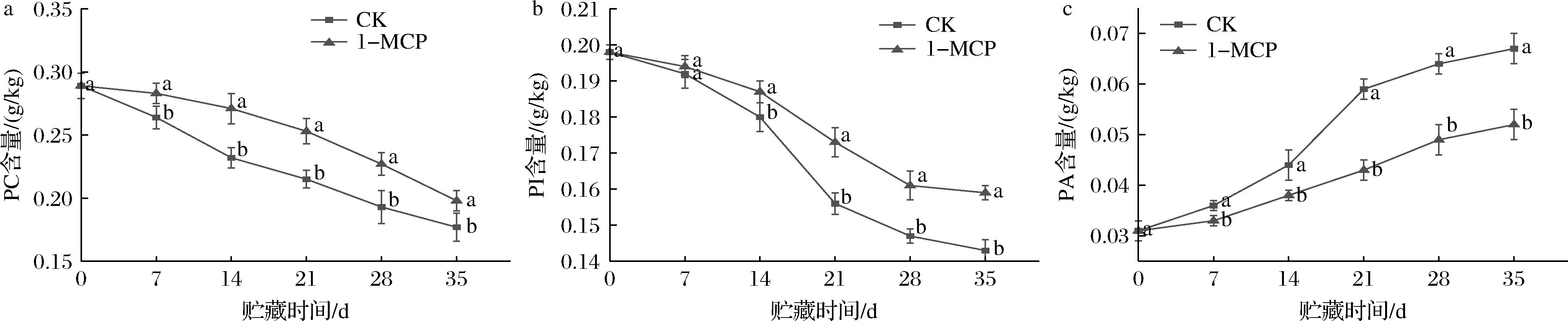
a-PC含量;b-PI含量;c-PA含量
图4 1-MCP处理对膜磷脂成分的影响
Fig.4 Effect of 1-MCP treatment on membrane phospholipid composition
2.5 1-MCP处理对膜脂肪酸组分的影响
如图5-a、图5-b所示,各处理组棕榈酸和硬脂酸的含量均逐渐升高;但CK组这2种饱和脂肪酸的上升幅度明显大于1-MCP组,35 d时CK组棕榈酸和硬脂酸的含量分别较1-MCP组提高了35.38%、45.74%,差异显著(P<0.05)。虽然2种不饱和脂肪酸的含量整体呈下降趋势,但亚麻酸的含量在0~14 d时逐渐增大,14 d时达到峰值,此时1-MCP组亚麻酸含量为CK组的1.28倍,14 d后2组处理的亚麻酸的含量大幅下降(图5-c),而亚油酸在整个贮藏期间均呈下降趋势(图5-d)。此外,如图5-e所示,0~14 d时,1-MCP组不饱和脂肪酸与饱和脂肪酸的比值逐渐增大,而CK组变化较为平缓,14 d后虽然2组处理不饱和脂肪酸与饱和脂肪酸的比值降幅较大,但CK组降幅显著高于1-MCP组(P<0.05)。以上结果表明,1-MCP处理可以维持细胞膜较高的不饱和酸比,缓解了膜脂过氧化。
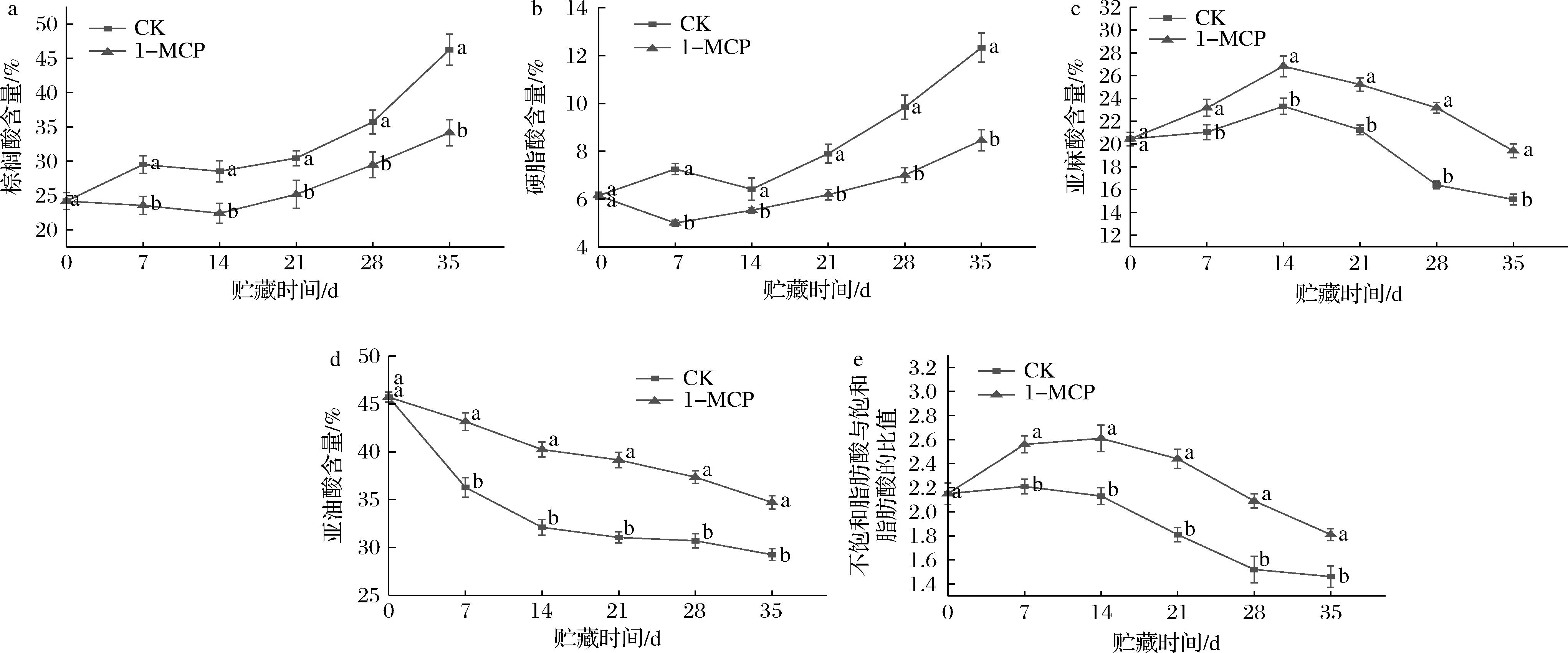
a-棕榈酸含量;b-硬脂酸含量;c-亚油酸含量;d-亚麻酸含量;e-不饱和脂肪酸与饱和脂肪酸的比值
图5 1-MCP处理对膜脂肪酸组分的影响
Fig.5 Effect of 1-MCP treatment on membrane fatty acid composition
2.6 1-MCP处理对油桃贮藏期间各指标的相关性分析
如图6所示,冷害指数与MDA含量、相对电导率、膜脂代谢酶(脂肪酶、PLA、PLC、DGK)活力、膜脂成分(棕榈酸、硬脂酸、PA)呈显著正相关关系,而与膜脂成分(PC、PI、亚油酸)呈显著负相关关系。LOX、PLD与冷害指数、膜脂组分等指标的相关性较低,可能是受油桃贮藏后期各处理LOX、PLD活性差异不显著所影响。以上结果表明,1-MCP处理可抑制油桃相对电导率、MDA含量、膜脂代谢酶活力、膜脂成分(棕榈酸、硬脂酸、PA)的大幅升高,减缓冷害进程。
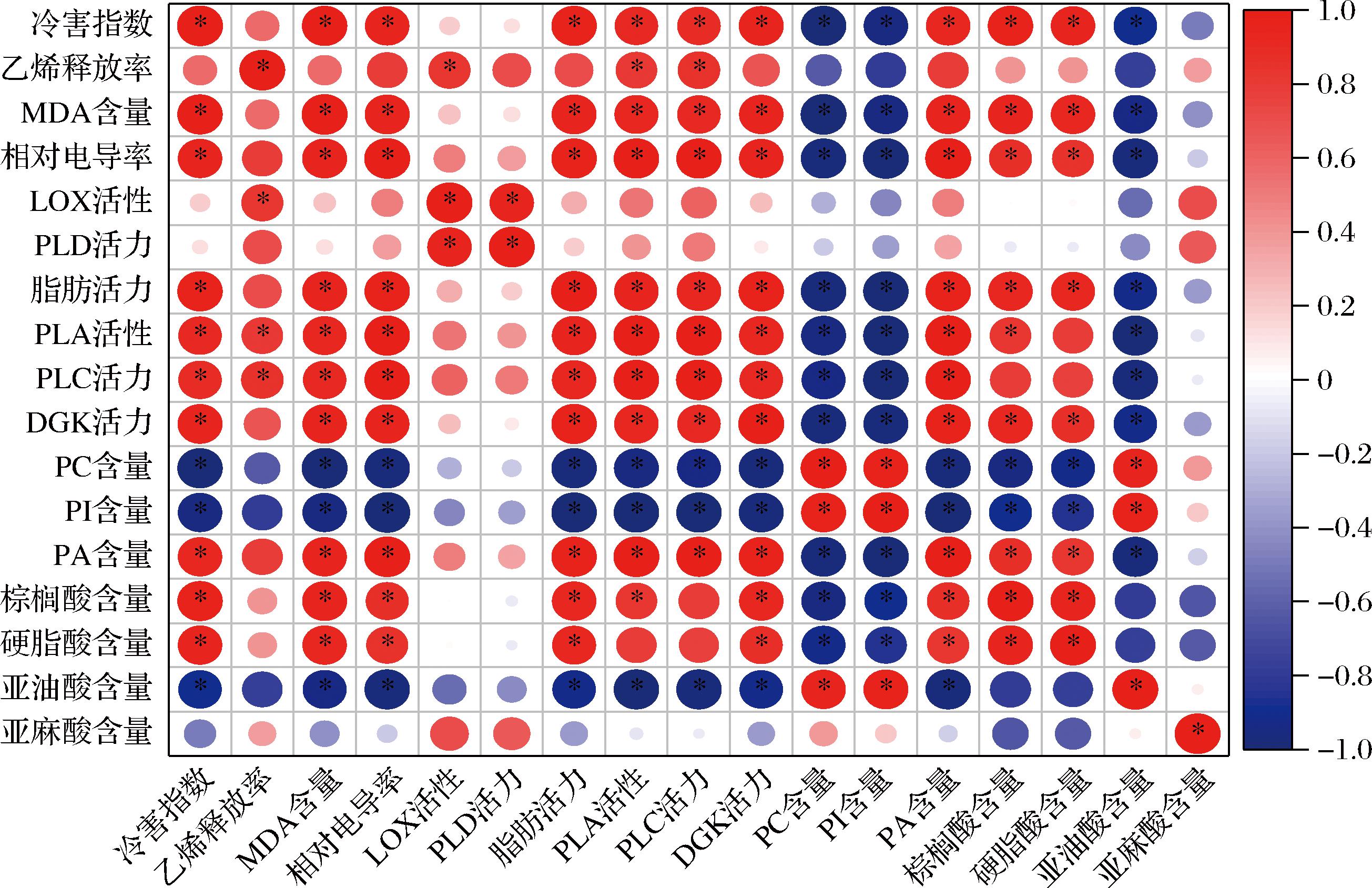
图6 1-MCP处理对油桃贮藏期间各指标的相关性分析
Fig.6 Correlation analysis of various indicators during storage of peaches treated with 1-MCP
注:*P<0.05。
3 讨论
冷敏型水果在低温贮存期间会发生严重的冷害,这是由于低温胁迫破坏了细胞膜的完整性,进而导致果品冷害[15]。本研究发现,尽管5 ℃贮藏时油桃果实MDA含量和果皮细胞膜透性随时间的延长不断升高,但1-MCP处理显著降低了果实MDA的积累与细胞膜透性的升高,这表明1-MCP处理提高了细胞膜磷脂的抗氧化能力[11,16],同时1-MCP处理降低了乙烯释放率,乙烯是果蔬体内重要的植物激素之一,对调节果蔬衰老、提高逆境抗性及维持贮期品质有重要意义。有研究表明适当的乙烯积累可以延缓果品冷害程度[17],这与本研究中1-MCP处理抑制乙烯释放量的大幅增加,提升油桃保鲜效果的结论并不冲突,由于低温胁迫会使桃果乙烯代谢发生紊乱,使乙烯释放量大幅升高,导致乙烯积累量急剧上升,加速桃果品质劣变进程;而1-MCP处理显著降低了低温胁迫对桃果乙烯代谢的干扰,抑制了乙烯释放率的大幅上升,延缓了乙烯的积累,乙烯这种缓慢积累对提升油桃的抗冷害能力非常重要。这与董欣瑞等[18]采用1-MCP结合乙烯吸收剂处理可显著抑制黄桃冷害褐变指数上升的结论相似,同时JIANG等[19]采用转录组学与代谢组学联合分析1-MCP处理对油桃贮期品质影响的研究中同样发现降低油桃贮期乙烯释放率,可有效提升油桃贮藏品质。以上结果表明,1-MCP处理在提高油桃贮期品质方面效果较好。
细胞膜损伤与膜脂质组成、含量及膜脂质代谢相关酶活性密切相关,低温胁迫下果蔬PLD、LOX等酶活性的升高,不仅加速了PI、PC等膜脂的降解,促进了PA的生成,而且提高了细胞膜的氧化程度,使细胞膜流动性减弱,逐渐从液晶态转变为固晶态[20]。SHI等[21]在南果梨中研究发现,当LOX、PLD和脂肪酶等膜脂代谢酶活力升高时,梨果细胞膜通透性升高、膜脂中主要脂肪酸含量下降,导致梨果冷害程度加重。RUI等[7]在枇杷的研究中发现,抑制PLD和LOX活性的升高,可延缓棕榈酸,硬脂酸等饱和脂肪酸含量的上降,提高了枇杷的抗冷害能力。此外,JANNATIZADEH等[22]在对番茄的保鲜研究中从分子层面证实了抑制PLD和LOX等基因的表达,有利于提高番茄不饱和/饱和脂肪酸比值,进而增强番茄抗冷害能力。本研究同样发现,1-MCP处理桃果后减轻了果实冷害程度,延缓了细胞膜PI和PC的降解,抑制了PA含量的升高(图4);同时1-MCP处理组的油桃不饱脂肪酸和/饱和的脂肪酸比值35 d时较CK组提高了23.97%,这可能是由于脂质代谢相关的酶(PLD、PLA、DGK、LOX、PLC和脂肪酶)活性受到抑制(图3)减轻了细胞膜损伤,这与CHENG等[23]研究发现1-MCP熏蒸可提高南果梨不饱和脂肪酸/饱和的脂肪酸比值,较好地维持细胞膜的完整性,进而减轻冷害对梨果的影响这一结论一致。相关分析也表明,冷害指数与膜脂代谢酶活性及饱和脂肪酸含量呈显著正相关关系。这表明1-MCP处理通过抑制膜脂代谢酶活性,维持细胞膜组分,延缓膜脂氧化程度进而增强桃果抗冷害能力。这与PURWANTO等[24]发现抑制芒果脂肪酶、PLD等膜脂代谢酶活性的升高,可减轻果实冷害程度,以及GAO等[25]有关桃果LOX活性受到抑制时会减轻膜脂过氧化氧化程度,提高桃果抗冷害能力的结论一致。
4 结论
综上所述,采用1-MCP处理油桃可以显著抑制贮藏期间LOX、PLD、脂肪酶、PLA,PLC和DGK等果皮膜脂代谢酶活力的大幅上升,同时降低了乙烯释放率及MDA的积累,使PI、PC等膜磷脂与亚麻酸、亚油酸等不饱和脂肪酸维持在较高水平,较好地维持了油桃果皮细胞膜的完整性,提高了果品品质。
[1] 孙亚静, 王燕, 郝雅婧, 等.不同LED处理对油桃果实采后类胡萝卜素及可溶性糖代谢的影响[J].核农学报, 2023, 37(8):1634-1642.
SUN Y J, WANG Y, HAO Y J, et al.Effects of different LED treatments on carotenoids and soluble sugar metabolism in postharvest nectarines[J].Journal of Nuclear Agricultural Sciences, 2023, 37(8):1634-1642.
[2] ZHAO Y Y, TANG J X, SONG C C, et al.Nitric oxide alleviates chilling injury by regulating the metabolism of lipid and cell wall in cold-storage peach fruit[J].Plant Physiology and Biochemistry, 2021, 169:63-69.
[3] XIE P D, YANG Y Y, GONG D, et al.Spraying L-phenylalanine during fruit development alleviates chilling injury in harvested muskmelons by regulating membrane lipid metabolism[J].Postharvest Biology and Technology, 2024, 211:112858.
[4] CHEN Y Z, YU J, LIN H T, et al.Membrane lipids metabolism participates in the pulp breakdown of fresh Longan caused by Phomopsis longanae Chi[J].Postharvest Biology and Technology, 2022, 193:112049.
[5] 周成, 方怡, 周锦杨, 等.低温诱导的桃果实采后膜脂代谢变化与冷害的关系[J].园艺学报, 2023, 50(6):1305-1317.
ZHOU C, FANG Y, ZHOU J Y, et al.The relationship between membrane lipid metabolism and chilling injury of postharvest peach fruit induced by low temperature[J].Acta Horticulturae Sinica, 2023, 50(6):1305-1317.
[6] KONG X M, GE W Y, WEI B D, et al.Melatonin ameliorates chilling injury in green bell peppers during storage by regulating membrane lipid metabolism and antioxidant capacity[J].Postharvest Biology and Technology, 2020, 170:111315.
[7] RUI H J, CAO S F, SHANG H T, et al.Effects of heat treatment on internal browning and membrane fatty acid in loquat fruit in response to chilling stress[J].Journal of the Science of Food and Agriculture, 2010, 90(9):1557-1561.
[8] LIU L, WEI Y N, SHI F, et al.Intermittent warming improves postharvest quality of bell peppers and reduces chilling injury[J].Postharvest Biology and Technology, 2015, 101:18-25.
[9] 魏宝东, 周爽, 郝义.逐步降温结合1-MCP处理对李果冷害及品质影响[J].食品工业科技, 2017, 38(6):319-323.
WEI B D, ZHOU S, HAO Y.Effects of gradually cooling binding 1-MCP treatment on chilling injury and storage quality of Angeleno plums[J].Science and Technology of Food Industry, 2017, 38(6):319-323.
[10] 孙正烜, 陈惠云, 杨虎清, 等.纳米乳涂膜和1-甲基环丙烯处理对枇杷果实保鲜效果的影响[J].食品科学, 2018, 39(23):257-262.
SUN Z X, CHEN H Y, YANG H Q, et al.Effects of nanoemulsion coating and 1-methylcyclopropene on quality maintenance of loquat fruits[J].Food Science, 2018, 39(23):257-262.
[11] 刘晨, 张轶斌, 贾晓昱, 等.臭氧结合1-MCP处理对油桃贮藏色泽和品质的影响[J].食品工业科技, 2025, 46(4):342-349.
LIU C, ZHANG Y B, JIA X Y, et al.Effect of ozone combined with 1-MCP on the color and quality of nectarines during postharvest storage[J].Science and Technology of Food Industry, 2025, 46(4):342-349.
[12] 张新宪, 焦旋, 冯志宏, 等.压差预冷结合高分子隔热保温膜处理对甜樱桃货架品质的影响[J].食品与发酵工业, 2025, 51(18):109-117.
ZHANG X X, JIAO X, FENG Z H, et al.Effect of forced-air precooling combined with high-molecular thermal insulation film treatment on quality of cherry during shelf-life period[J].Food and Fermentation Industries, 2025, 51(18):109-117.
[13] WANG H, CHEN G, SHI L L, et al.Influences of 1-methylcyclopropene-containing papers on the metabolisms of membrane lipids in Anxi persimmons during storage[J].Food Quality and Safety, 2020, 4(3):143-150.
[14] CHEN Y Z, LIN H T, ZHANG H L, et al.Dicyclohexylcarbodiimide and disodium succinate regulate the browning development in fresh Longan pericarp by modulating the antioxidant system and the metabolisms of membrane lipids and phenolics[J].Postharvest Biology and Technology, 2023, 203:112388.
[15] KUANG X Y, CHEN Y Z, LIN H T, et al.Comprehensive analyses of membrane lipids and phenolics metabolisms reveal the developments of chilling injury and browning in Chinese olives during cold storage[J].Food Chemistry, 2023, 416:135754.
[16] ZHANG Y T, LING J, ZHOU H S, et al.1-Methylcyclopropene counteracts ethylene inhibition of anthocyanin accumulation in peach skin after harvest[J].Postharvest Biology and Technology, 2022, 183:111737.
[17] ZHOU H W, DONG L I, BEN-ARIE R, et al.The role of ethylene in the prevention of chilling injury in nectarines[J].Journal of Plant Physiology, 2001, 158(1):55-61.
[18] 董欣瑞, 张珮, 袁楚珊, 等.1-MCP联合乙烯吸附剂处理对黄桃果实冷害与糖代谢的影响[J].中国食品学报, 2022, 22(9):208-216.
DONG X R, ZHANG P, YUAN C S, et al.Effects of 1-MCP combined with ethylene adsorbent on chilling injury and sugar metabolism of peach fruit[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(9):208-216.
[19] JIANG Y Q, LI W H, WANG H F, et al.1-MCP delays ripening and maintains postharvest quality of nectarines by regulating transcriptional and metabolic responses[J].Scientia Horticulturae, 2024, 330:113083.
[20] SAITA E, ALBANESI D, DE MENDOZA D.Sensing membrane thickness:Lessons learned from cold stress[J].Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids, 2016, 1861(8):837-846.
[21] SHI F, ZHOU X, ZHOU Q, et al.Membrane lipid metabolism changes and aroma ester loss in low-temperature stored Nanguo pears[J].Food Chemistry, 2018, 245:446-453.
[22] JANNATIZADEH A, AGHDAM M S, LUO Z S, et al.Impact of exogenous melatonin application on chilling injury in tomato fruits during cold storage[J].Food and Bioprocess Technology, 2019, 12(5):741-750.
[23] CHENG S C, WEI B D, ZHOU Q, et al.1-Methylcyclopropene alleviates chilling injury by regulating energy metabolism and fatty acid content in ‘Nanguo’ pears[J].Postharvest Biology and Technology, 2015, 109:130-136.
[24] PURWANTO Y A, OKVITASARI H, MARDJAN S, et al.Chilling injury in green mature ‘gedong gincu’ mango fruits based on the changes in ion leakage[J].Acta Horticulturae, 2013(1011):219-226.
[25] GAO H, LU Z M, YANG Y, et al.Melatonin treatment reduces chilling injury in peach fruit through its regulation of membrane fatty acid contents and phenolic metabolism[J].Food Chemistry, 2018, 245:659-666.