丁酸乙酯作为一种具有浓郁果香的短链脂肪酸乙酯,不仅是白酒中提升酒体层次和香气的重要风味物质,在食品、饮料和香精香料领域也有着广泛应用[1-2]。尽管传统化学合成法具有反应迅速、转化率高的优点,但其生产过程往往伴随着高能耗、环境污染以及食品安全隐患等问题,使得生物合成法成为更绿色环保和可持续的选择[3-4]。利用微生物催化合成脂肪酸乙酯(包括丁酸乙酯)主要依赖于4类关键酶:酯酶、醇酰基转移酶(alcohol acyltransferase, AATs)、Baeyer-Villiger单加氧酶以及半醛脱氢酶[5-6]。尽管已有部分微生物被证实具有合成丁酸乙酯的能力,如细菌、霉菌和酵母等[5],但天然菌株的代谢通量受限,难以满足工业化生产需求[7]。因此,代谢工程改造微生物合成丁酸乙酯成为关键研究方向。
酿酒酵母作为一种理想的模式真核生物,已被广泛应用于各种工业产品的合成与生产。然而,野生型酿酒酵母丁酸乙酯的合成能力较低,其关键制约因素在于脂肪酸合成酶生成丁酰辅酶A底物水平不足,导致经醇酰基转移酶介导的酯化反应(乙醇与丁酰辅酶A)生成丁酸乙酯受限。尽管有研究通过改变脂肪酸合酶的碳链延伸机制,提高前体酰基辅酶A的供应[8],以及过表达外源酯酶WS2进一步提升酯的合成[9],但脂肪酸合成途径依赖丙二酰辅酶A作为底物,丙二酰辅酶A合成过程需要消耗ATP,限制了其工业应用潜力。近年来,逆β-氧化途径因其较低的能耗需求,被认为是更经济的丁酸乙酯合成策略。本课题组前期已在酿酒酵母AY12α中引入逆β-氧化途径,构建了重组菌株E01[10],使得丁酸乙酯产量达(48.95±3.38) mg/L。然而,逆β-氧化途径的连续脱氢反应需消耗还原型辅因子(NADH、NADPH),导致胞内辅因子的动态平衡失调,使得丁酸乙酯合成受限。因此,探究胞内氧化还原平衡调控策略对丁酸乙酯产量的提升至关重要。
本研究首先尝试敲除ADH1基因减少碳流和NADH竞争;其次,结合NADH调节基因(cPOS5、mPOS5、udhA、noxE)优化胞内氧化还原平衡;最后,利用乙酰辅酶A合成酶(ACS1、SeACSL641P)缓解乙酸抑制的同时强化胞浆乙酰辅酶A的供应。通过上述策略,旨在突破现有合成瓶颈,为丁酸乙酯的高效生物制造提供新思路。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
本实验所用菌株如表1所示。
表1 菌株
Table 1 Strains

菌株特征来源AY12αSaccharomyces cerevisiaeAY12的单倍体,MATα本实验室E01AY12α, YCR011C::TDH3p-CsHbd-TDH1t,YBR128C::CCW12p-CsCrt-SSA1t,YHR142W::PGK1p-SAAT-ENO2t,308a::TEF1p-TdTer-ADH1t本实验室[10]AYcAY12α, YPR028W::TDH3p-cPOS5-HISt本研究AYmAY12α, YPR028W::TDH3p-mPOS5-HISt本研究AYuAY12α, YPR028W::TDH3p-udhA-HISt本研究AYnAY12α, YPR028W::TDH3p-noxE-HISt本研究EcE01, YPR028W::TDH3p-cPOS5-HISt本研究EmE01, YPR028W::TDH3p-mPOS5-HISt本研究EuE01, YPR028W::TDH3p-udhA-HISt本研究EnE01, YPR028W::TDH3p-noxE-HISt本研究AYcDAYcΔADH1本研究AYmDAYmΔADH1本研究AYuDAYuΔADH1本研究AYnDAYnΔADH1本研究AYDAY12αΔADH1本研究EcDEcΔADH1本研究EmDEmΔADH1本研究EuDEuΔADH1本研究EnDEnΔADH1本研究EDE01ΔADH1本研究EcDAEcD, GAL80::TDH3p-ACS1-HISt-NRS本研究EmDAEmD, GAL80::TDH3p-ACS1-HISt-NRS本研究EuDAEuD, GAL80::TDH3p-ACS1-HISt-NRS本研究EnDAEnD, GAL80::TDH3p-ACS1-HISt-NRS本研究EDAED, GAL80::TDH3p-ACS1-HISt-NRS本研究EcDSEcD, GAL80::TDH3p-SeACSL641P-HISt-NRS本研究EmDSEmD, GAL80::TDH3p-SeACSL641P-HISt-NRS本研究EuDSEuD, GAL80::TDH3p-SeACSL641P-HISt-NRS本研究EnDSEnD, GAL80::TDH3p-SeACSL641P-HISt-NRS本研究EDSED, GAL80::TDH3p-SeACSL641P-HISt-NRS本研究SePG-AAY12α, GAL80::TEF1p-SeACSL641P-PGK1t-PGK1p-ALD6-GIC1t-PGK1p-ATF1-PGK1t-loxP-KanMX-loxP本实验室
1.1.2 主要试剂
供实验所用的酶制剂,宝生物工程(大连)有限公司;供实验所用试剂盒,南京诺唯赞生物科技股份有限公司;抗生素,索莱宝(北京)科技有限公司;PCR引物,苏州金唯智生物科技有限公司;酸酯标准品,阿拉丁(上海)生化科技股份有限公司,α-淀粉酶、糖化酶、酸性蛋白酶,诺维信(中国)生物医药公司;其他试剂,永大(天津)化学试剂开发中心及奥博星(北京)生物科技有限公司等。
1.1.3 培养基
LB培养基(g/L):蛋白胨10,酵母浸粉5,NaCl 10,水。121 ℃灭菌20 min。YPD培养基(g/L):蛋白胨20,酵母粉10,葡萄糖20,水。115 ℃灭菌20 min。
高粱水解液:在1 kg高粱粉中加入3 L蒸馏水,料液比1∶3(g∶mL),60 ℃糊化30 min,加入1 mL的α-淀粉酶90 ℃液化30 min。煮沸20 min后迅速冷却至60 ℃,加入2 mL糖化酶60 ℃恒温水浴4 h。降温至40 ℃后加入1 mL酸性蛋白酶,40 ℃保温2 h。用4层纱布过滤得澄清溶液,使用糖度计测量糖度。获得初始高粱水解液。取适量初始高粱水解液,调节糖度至8°为一级种子培养基,调节糖度至12°为二级种子培养基,调节糖度至16°为发酵培养基。一、二级培养基均需加入0.5%(质量分数)酵母浸粉,115 ℃灭菌20 min。发酵接种时每瓶加入1 mL营养盐[11]。
1.2 仪器和设备
LRH-250A 生化培养箱,上海博讯实业有限公司;7230G紫外-可见分光光度计,上海菁华技术公司;WH-3A水浴锅,杭州佑宁仪器公司;1100高效液相色谱仪、7890A气相色谱仪、HP-INNOWAX色谱柱,北京安捷伦科技有限公司。
1.3 方法
1.3.1 菌株的构建
本研究所有PCR引物和Sanger测序由苏州金唯智生物科技有限公司完成。
基因敲除:以酿酒酵母E01基因组为模板,通过PCR扩增获得ADH1基因的上下游同源臂。以本课题组先前构建的质粒pUC19-Kan-loxp为模板,扩增出带loxp位点的Kan抗性标签(Kan-loxp片段)[12],通过Overlap-PCR融合成基因敲除片段DADH1-Kan,转入AY12α和E01酵母菌株,经过PCR和测序验证,分别获得重组菌株AYD和ED。重组菌株AYcD、AYmD、AYuD、AYnD、EcD、EmD、EuD和EnD同样采取相同的方法构建获得。
基因整合:4个NADH消耗基因分别以AY12α基因组为模板扩增cPOS5和mPOS5基因片段,以大肠杆菌基因组为模板扩增udhA,通过合成手段获得noxE基因。选用TDH3p启动子和HISt终止子作为NADH消耗基因表达的调控元件。利用双质粒CRISPR-Cas9系统将4个表达盒分别整合至底盘细胞基因组YPR028W位点[10]。经过PCR和测序验证,获得菌株AYc、AYm、AYu、AYn和Ec、Em、Eu、En。重组菌株EDA、EcDA、EmDA、EuDA、EnDA、EDS、EcDS、EmDS、EuDS和EnDS同样采取相同的启动子和终止子,诺尔斯菌素为抗性标签,并将其整合在酿酒酵母高表达位点GAL80下游非编码区域获得。
1.3.2 培养方法
种子培养:从平板上挑取适量菌体接种至含有5 mL YPD培养基的试管中,30 ℃静置培养24 h形成一级种子液;将一级培养基接种至含有45 mL YPD培养基的150 mL三角瓶中,30 ℃静置培养18 h形成二级种子液。
静置发酵:接种适量二级种子液进入发酵培养基三角瓶中,控制初始OD600约为0.25,并加入1 mL营养盐,30 ℃静置培养。每12 h称重一次并记录,发酵至恒重即视为发酵完成。发酵结束后,取100 mL发酵液和100 mL蒸馏水,加入少量消泡剂,充分密封蒸馏装置后收集100 mL酒样,进行后续风味物质测定。
生长曲线测定:将二级种子液接种至含有135 mL YPD培养基的250 mL三角瓶,调节初始OD600为0.25左右,初始体积为150 mL。记接入时间为0 h,30 ℃静置培养。每次取样间隔2 h,测定0~36 h时间段内培养基实时OD600值并记录。
1.3.3 分析方法
生物量测定:本研究使用紫外分光光度计测定OD600处的吸光度以测定细胞密度。
高效液相色谱仪:本研究使用高效液相色谱示差折光检测器测定酒样中葡萄糖和酒样乙醇的含量[13],检测条件为Agilent GH0830078H色谱柱(300 mm×7.8 mm×8 μm),紫外检测器,柱温50 ℃,流动相为5 mmol/L稀硫酸缓冲液,流速0.6 mL/min,波长210 nm,进样量20 μL。
气相色谱仪:本研究使用气相色谱仪测定酒样挥发性酸、醇、酯等风味物质的含量[14],检测条件为HP-INNOWAX色谱柱(30 m×0.320 mm×0.25 μm石英毛细管柱),200 ℃进样温度,载气为高纯氮气,分流比10∶1,流速为8 mL/min;起始柱温为35 ℃,保持1 min,以3 ℃/min升温至60 ℃,保持2 min,再以2 ℃/min升温至85 ℃,保持1 min,然后8 ℃/min升温至230 ℃,保持5 min。
1.4 数据处理
实验数据利用Excel 2019软件处理,用“平均值±标准差”表示。利用SPSS 26.0软件进行显著差异分析。利用GraphPad Prism绘制相关图。
2 结果与分析
2.1 减少乙醇合成碳通量
在重组菌株E01中,丁酸乙酯的合成通路和乙醇的代谢通路存在碳流竞争(图1),由葡萄糖代谢而来的乙醛一方面可以后续形成乙酰辅酶A进入逆β-氧化途径完成丁酸乙酯的合成;另一方面,乙醛在乙醇脱氢酶(ADH1为主)的催化下合成乙醇[15]。
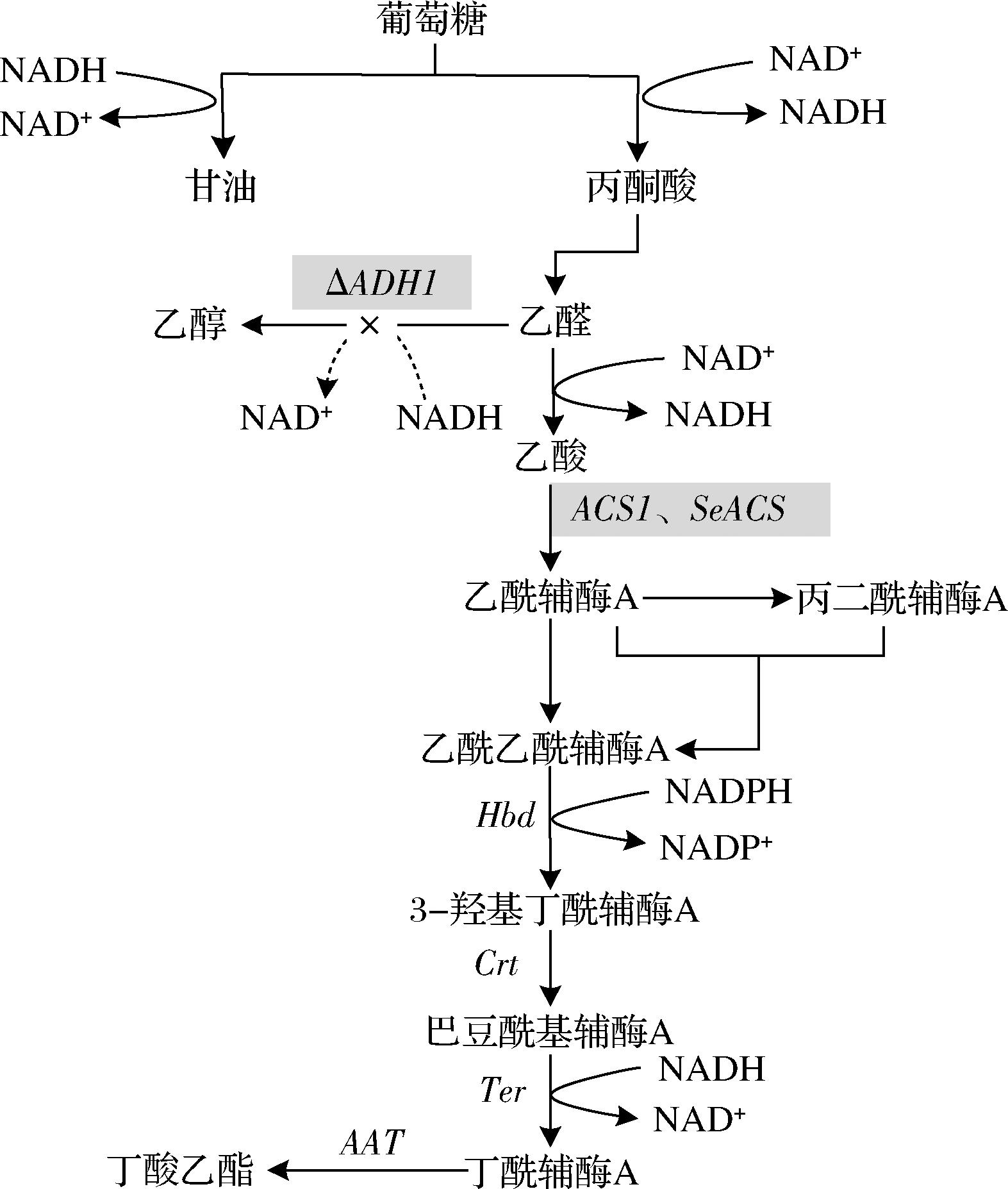
图1 逆β-氧化途径合成丁酸乙酯代谢通路
Fig.1 Metabolic pathway of ethyl butyrate synthesis through the reverse β-oxidation pathway
注:图中“ΔADH1”表示ADH1基因被敲除,叉号“×”表示该代谢路径被阻断,阴影表示本研究改造步骤。
为减少乙醇合成碳流并探索氧化还原稳态维持机制,本研究以酿酒酵母AY12α(对照组)和产丁酸乙酯重组菌株E01(实验组)为底盘,分别敲除ADH1基因构建重组菌株AYD和ED,旨在阻断乙醛向乙醇转化,引导碳流至丁酸乙酯合成途径。E01中引入的逆β-氧化途径含Ter(NADH依赖型烯酰辅酶A还原酶)和Hbd(NADPH依赖型3-羟基丁酰辅酶A脱氢酶),通过消耗NADH再生NAD+,并通过转氢酶间接调节NAD+/NADH平衡[16],理论上可补偿ADH1缺失引发的氧化还原失衡。
如图2所示,通过测定重组菌株在YPD培养基中的生长曲线,AYD和ED的终生物量较出发菌分别下降57.45%和48.56%。在高粱水解液静置发酵中,重组菌株CO2排放量显著降低,初始还原糖质量浓度约为150 g/L,重组菌株的还原糖也未完全利用,乙醇产量分别降至对照菌株的34.33%和18.31%。使用气相色谱仪对发酵后酒样中的风味物质进行测定后发现,ADH1缺失导致乙醛积累,其氧化产物乙酸在AYD和ED中分别增加2.3倍和3.1倍,ED菌株丁酸乙酯产量仅为出发菌的8.97%。
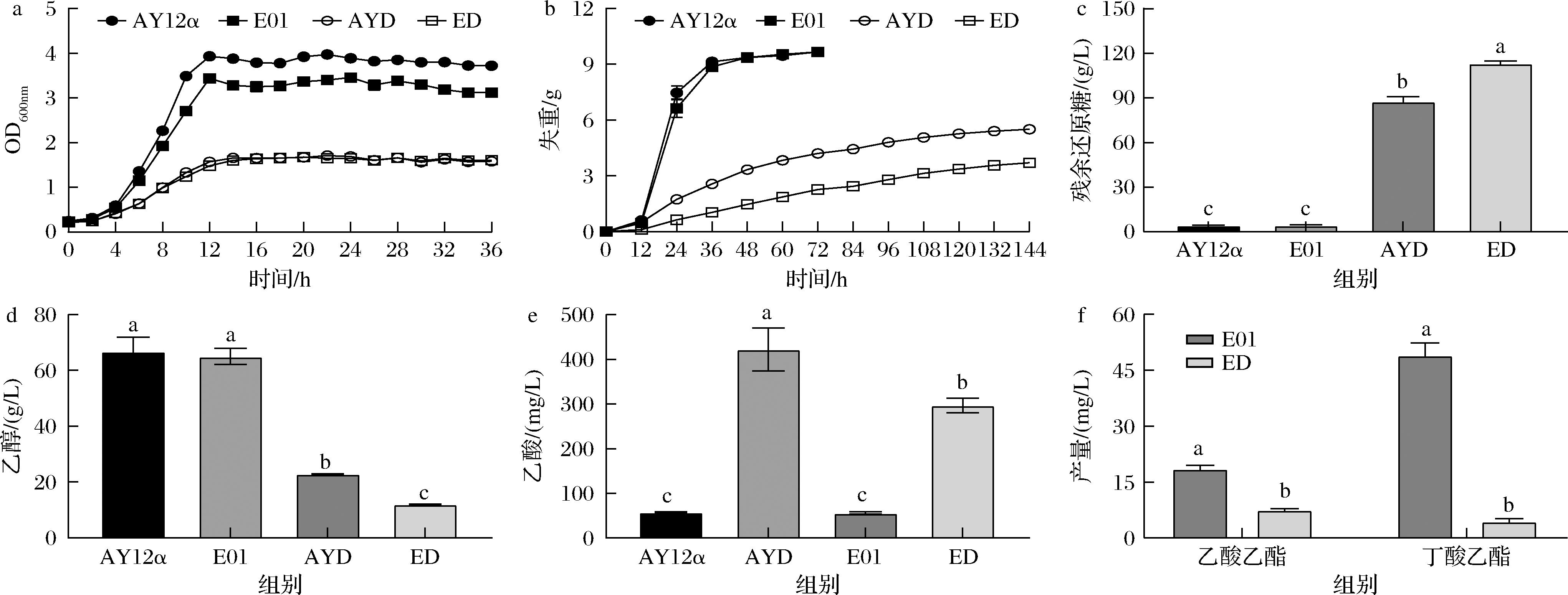
a-生长曲线;b-CO2排放量;c-残余还原糖;d-乙醇产量;e-乙酸产量;f-乙酸乙酯、丁酸乙酯产量
图2 出发菌株和敲除ADH1菌株的生长与发酵情况
Fig.2 Growth and fermentation characteristics of the starting strain and ADH1 knockout strains
注:图中不同字母表示在P<0.05水平上差异显著(下同)。
逆β-氧化途径的Ter步骤虽可通过消耗NADH再生NAD+,但因丁酸乙酯合成通量不足效率有限。同时,Hbd步骤持续消耗NADPH,导致NADPH/NADP+失衡,并通过转氢酶作用加剧NADH积累[17],进而抑制糖酵解关键酶活性,最终表现为残余还原糖堆积、生物量显著下降及丁酸乙酯合成受限。逆β-氧化途径通过Ter和Hbd的氧化还原平衡调节,使ED的生物量降幅较AYD低8.89%,表明其部分缓解了NADH压力,但碳通量不足仍无法完全恢复氧化还原稳态。上述结果表明,ADH1敲除通过中断NAD+再生途径导致碳代谢流受阻。表明单一阻断策略难以平衡复杂代谢网络,需结合辅因子动态调控优化碳流分配。
2.2 氧化还原平衡的调节
为了恢复胞内因为敲除ADH1而导致的氧化还原失衡,尝试引入多种与NADH消耗相关的酶,以解决NADH积累带来的生长抑制问题。考虑到直接在缺失菌株中进行复杂的代谢调控可能导致结果难以解析,本研究首先在未敲除ADH1的菌株AY12α和E01中分别过表达cPOS5、mPOS5、udhA和noxE,构建重组菌株AYc、AYm、AYu、AYn、Ec、Em、Eu和En。4种酶的催化反应见表2。
表2 NADH消耗相关基因
Table 2 NADH-related depletion genes
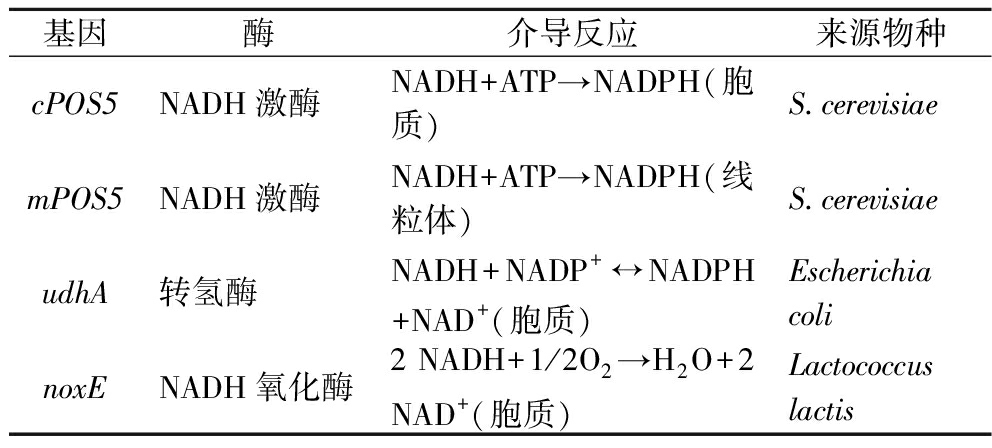
基因酶介导反应来源物种cPOS5NADH激酶NADH+ATP→NADPH(胞质)S.cerevisiaemPOS5NADH激酶NADH+ATP→NADPH(线粒体)S.cerevisiaeudhA转氢酶NADH+NADP+↔NADPH+NAD+(胞质)Escherichia colinoxENADH氧化酶2 NADH+1/2O2→H2O+2 NAD+(胞质)Lactococcus lactis
在YPD静置发酵实验中,NADH调节基因的引入显著提升了乙醇产量:AYc和Eu菌株较出发菌分别提高19.60%和22.77%,CO2释放量增加,表明碳代谢活性增强。然而,通过测定重组菌株的生长曲线发现,noxE过表达菌株AYn和En的生物量分别下降至出发菌的79.2%和87.3%,这可能与其需氧依赖性有关,其他菌株的最终生物量也略低于出发菌(图3-a~图3-f)。推测因NADH被优先用于乙醇生成,减少甘油生成途径的NAD+再生,增强了糖酵解速率,但也限制了生长代谢碳流供给[18-19],导致生物量下降。
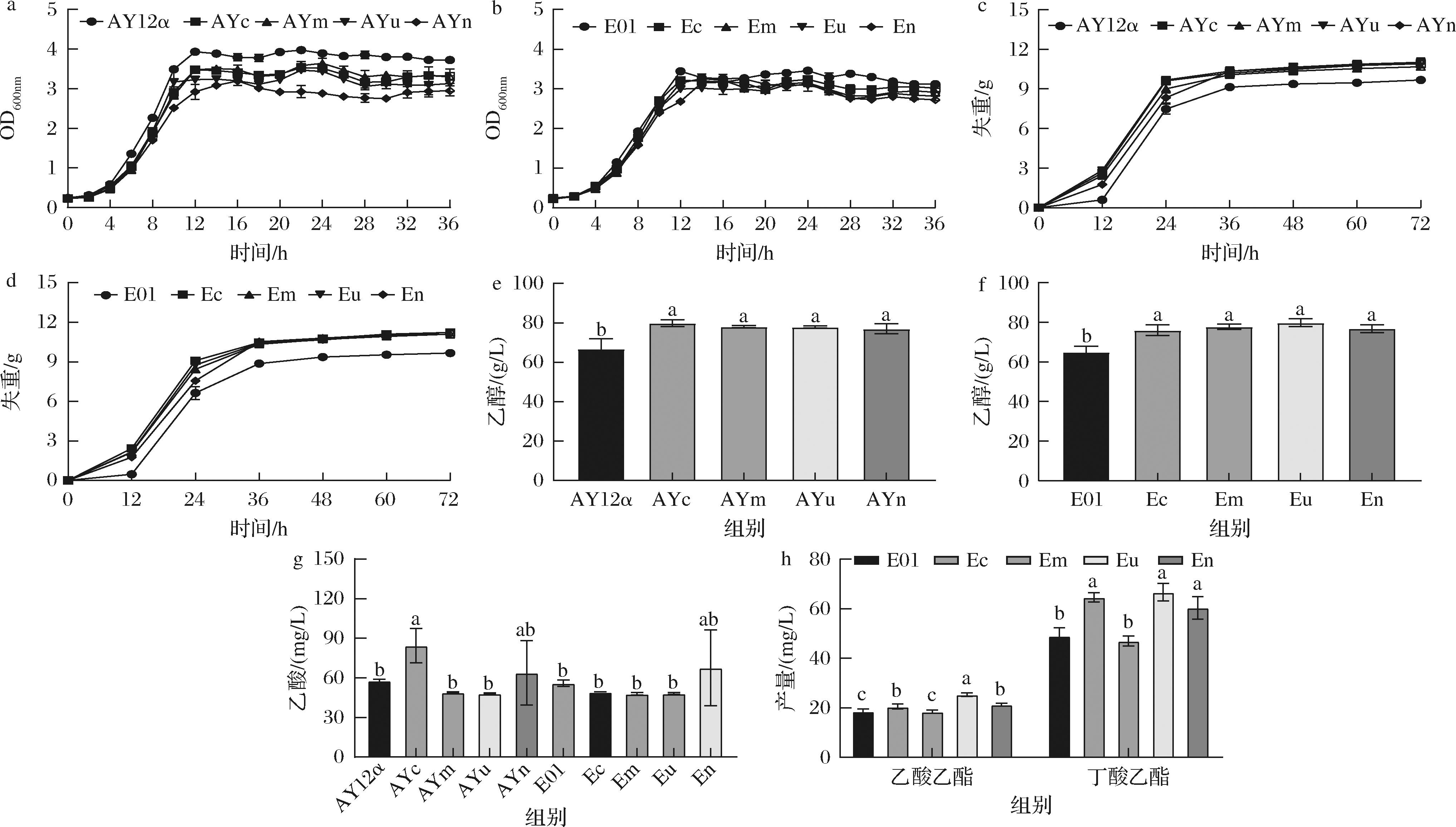
a-AY12α和引入与NADH消耗相关基因后重组菌株的生长曲线;b-E01和重组菌株的生长曲线;c-AY12α和重组菌株CO2排放量;d-E01和重组菌株CO2排放量;e-AY12α和重组菌株的乙醇产量;f-E01和重组菌株的乙醇产量;g-出发菌和重组菌株的乙酸产量;h-E01和重组菌株的乙酸乙酯、丁酸乙酯产量
图3 出发菌株和氧化还原平衡调节菌株的生长与发酵情况
Fig.3 Growth and fermentation characteristics of the starting strain and redox balance regulation strains
对酒样中风味物质检测显示,仅AYc菌株乙酸积累显著提高了46.29%(图3-g)。以E01为底盘的udhA过表达菌株Eu效果最佳,乙酸乙酯、丁酸乙酯产量较E01分别提升36.24%、35.02%(图3-h)。可能是由于udhA作为转氢酶,通过双向反应将NADH转化为NADPH,促进NAD+的再生,确保糖酵解和乙醇发酵过程持续进行,同时为Hbd步骤提供NADPH还原力[20],推动乙酰辅酶A向丁酸乙酯等产物转化。
相反,mPOS5过表达菌株Em因线粒体NADH/NADPH调控伴随ATP消耗,可能促使线粒体增强TCA循环以补偿能量缺口,导致乙酰辅酶A被进一步氧化而非用于酯类合成。此外,ATP消耗的增加也可能影响整体能量平衡,从而对细胞生长及产物合成产生不利影响[21]。由于胞质NAD+/NADH比例变化有限,mPOS5过表达未能显著促进乙酯合成,但其对线粒体代谢调控为后续ADH1敲除菌株优化提供潜在方向。
2.3 调节氧化还原平衡后的碳通量优化
为探究协同策略对丁酸乙酯合成的提升潜力,本研究在引入NADH调节基因的基础上进一步敲除ADH1,构建重组菌株AYcD、AYmD、AYuD、AYnD、EcD、EmD、EuD和EnD。
实验结果显示,无论单独敲除ADH1或在引入NADH调节基因后敲除ADH1,重组菌株在YPD培养基中的生长均显著受抑制(图4)。其中,AYcD和AYmD相比于仅敲除ADH1的AYD,生长性能表现略优,推测因cPOS5(胞质NADH激酶)和mPOS5(线粒体NADH激酶)通过催化NADH向NADPH的转化,缓解了各自区室内的氧化还原失衡。EcD在发酵后期的生长性能略优于ED,可能是因为调控NADH平衡使细胞代谢活力部分恢复。相比之下,noxE过表达菌株AYnD和EnD生长严重受抑,可能是由于noxE介导的NADH快速氧化破坏了糖酵解与NAD+再生平衡,且厌氧条件下ADH1敲除又阻断了乙醇途径的NAD+再生,导致能量供应不足和氧化还原失调[22]。
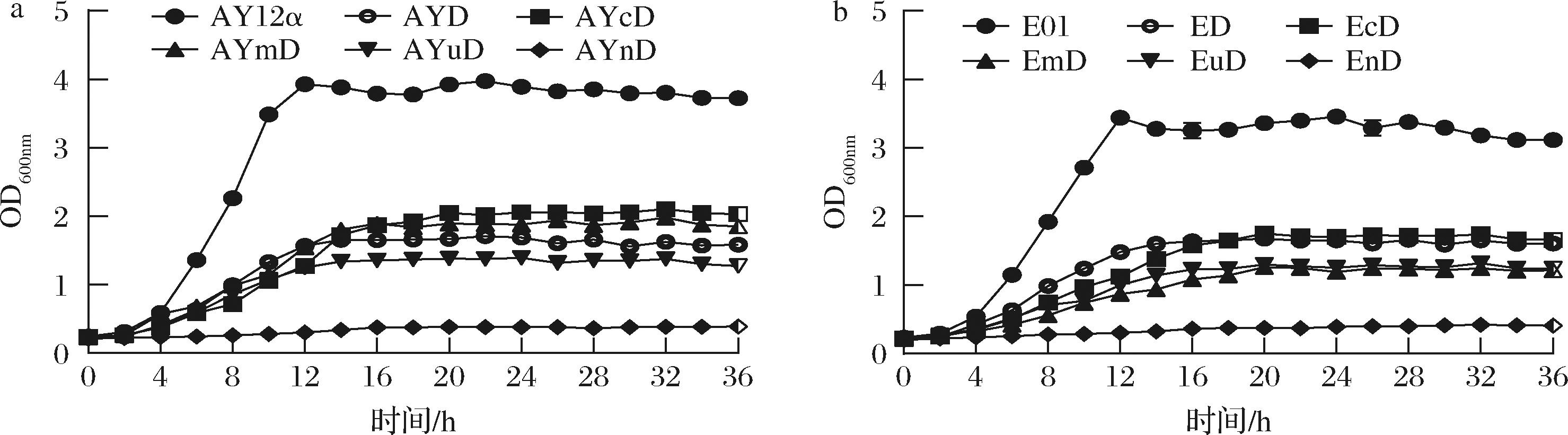
a-AY12α及敲除ADH1后重组菌株的生长曲线;b-E01及敲除ADH1后重组菌株的生长曲线
图4 出发菌株和调控氧化还原平衡后碳通量优化的重组菌株生长情况
Fig.4 Growth characteristics of the starting and recombinant strains with optimized carbon flux after redox balance regulation
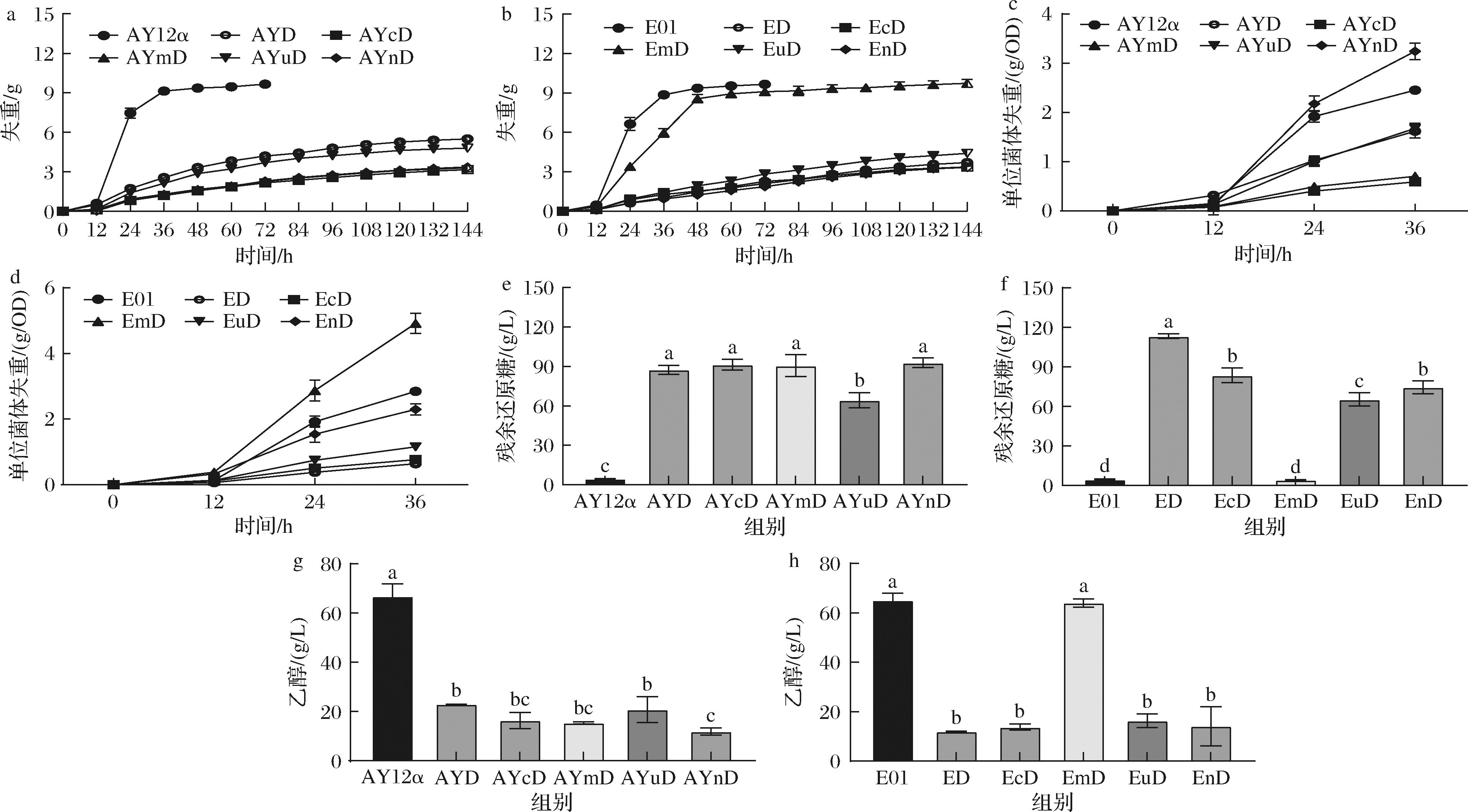
a-AY12α及敲除ADH1后重组菌株的CO2排放量;b-E01及敲除ADH1后重组菌株的CO2排放量;c-AY12α及敲除ADH1后重组菌株的单位菌体失重;d-E01及敲除ADH1后重组菌株的单位菌体失重;e-AY12α及敲除ADH1后重组菌株的残余还原糖;f-E01及敲除ADH1后重组菌株的残余还原糖;g-AY12α及敲除ADH1后重组菌株的乙醇产量;h-E01及敲除ADH1后重组菌株的乙醇产量
图5 出发菌株和调控氧化还原平衡后的碳通量优化的重组菌株的发酵情况
Fig.5 Fermentation characteristics of the starting strain and recombinant strains with optimized carbon flux after redox balance regulation
在高粱水解液静置发酵过程中,重组菌株的CO2释放量降低,其中引入cPOS5和noxE的菌株降幅最大,而EuD虽然具备udhA调节NAD+/NADH比例的能力,但仍难以维持平衡。然而,由于部分菌株(如AYnD)几乎不生长,CO2释放的降低更多反映的是生长受抑制,而非单位菌体代谢活性下降(图5-a~图5-d)。
值得注意的是,EmD表现出较强的发酵能力,其发酵液中残余还原糖较低,乙醇产量与出发菌E01无显著差异,表明mPOS5可以缓解NADH积累压力,并促进TCA循环活性,使部分乙酰辅酶A重新进入乙醇合成途径,但AYmD未出现类似效应(图5-e~图5-h),可能由于AY12α缺乏逆β-氧化途径,电子传递活性较低,削弱了NADH/NADPH调控效果。尽管ADH1已敲除,EmD仍能维持乙醇合成,推测是由于胞质中其他醇脱氢酶(如ADH2和ADH3)的补偿作用[23],但其具体机制尚不明确,需进一步研究。
代谢分析表明,ADH1敲除导致乙酸积累量显著增加,而单独引入NADH调节基因并未显著改变乙酸积累,说明NADH平衡调节本身不直接影响乙酸合成。在ADH1敲除基础上,引入mPOS5的EmD菌株乙酸含量显著降至(152.8±22.7) mg/L,推测mPOS5通过促进线粒体NADH/NADPH转化增强TCA循环活性,加速乙酸代谢。而其他菌株可能因NADH过度消耗导致乙酸代谢受阻,积累量仍较高,表明菌株背景对调控策略的敏感性(图6-a~图6-b)。
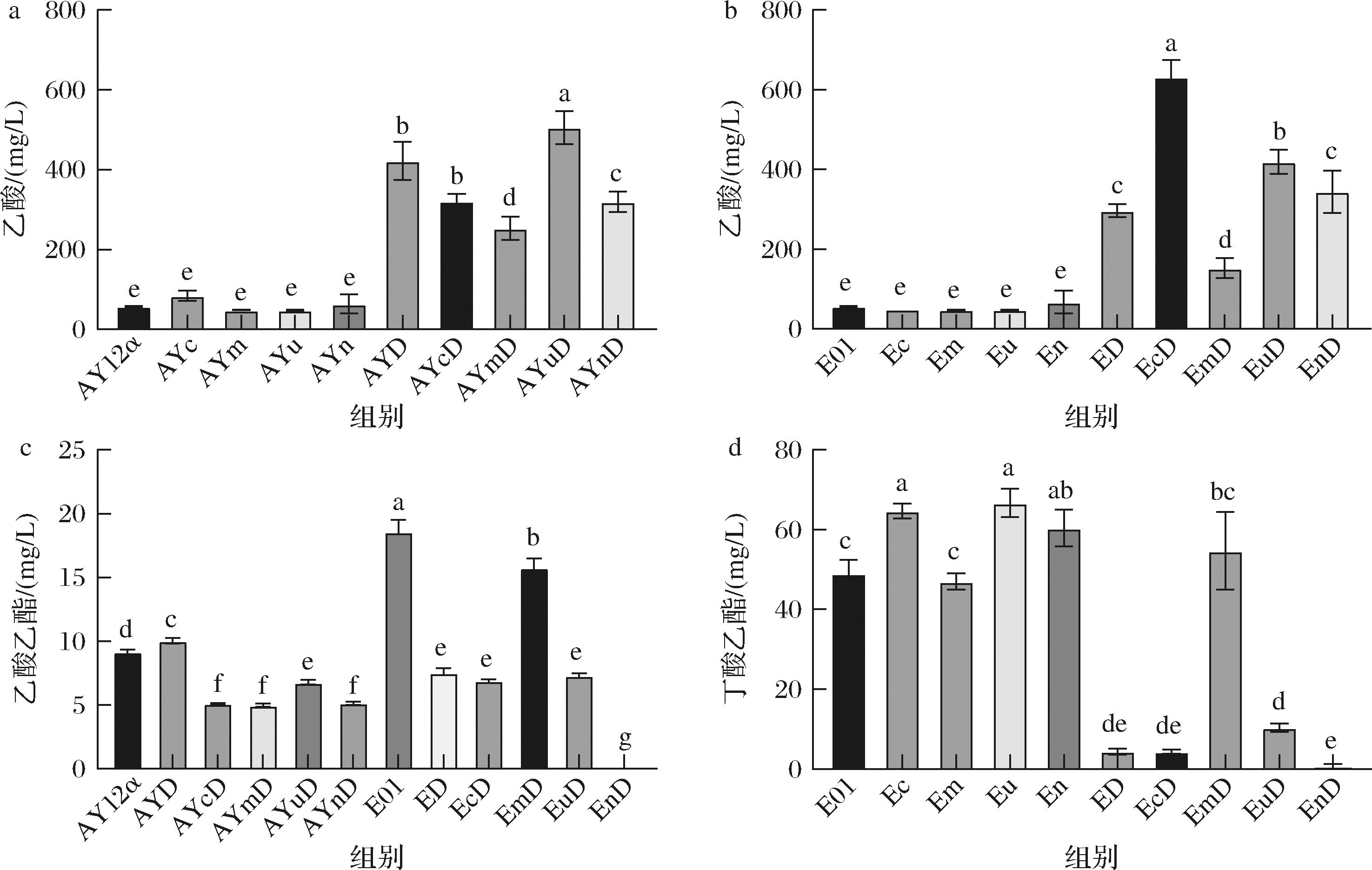
a-AY12α及其改造菌株乙酸产量;b-E01及其改造菌株乙酸产量;c-出发菌株及其改造菌株乙酸乙酯产量;d-E01及其改造菌株丁酸乙酯产量
图6 出发菌株和调控氧化还原平衡后的碳通量优化的重组菌株的乙酸、乙酸乙酯和丁酸乙酯产量
Fig.6 Production of acetate, ethyl acetate, and butyl acetate by the parental and redox-regulated carbon flux-optimized recombinant strains
酯类合成方面,ADH1敲除菌株ED因乙醇受限,导致乙酸乙酯产量降至(7.51±0.39) mg/L,而引入mPOS5的EmD菌株乙酸乙酯产量回升至(15.75±0.74) mg/L,丁酸乙酯产量也显著提高至(54.66±6.73) mg/L(出发菌的112%),而EcD、EuD丁酸乙酯产量仅为出发菌的8.8%和21.1%(图6-c~图6-d),该差异可能源于mPOS5的双重调控:一是增强β-氧化逆反应提供丁酰辅酶A前体,降低乙酸积累;二是可能激活了ADH2或ADH3补偿乙醇合成,提高了单位耗糖生成乙醇的效率,并促使碳流向酯类分流。
进一步分析EmD发现,其乙醇生成与E01相似,但菌体量明显下降,丁酸乙酯产量恢复至E01的112%,这可能与β-氧化逆反应有关:mPOS5可能通过促进NADH向NADPH转化,补充了Hbd反应所需的NADPH,Ter反应还缓解了NADH消耗压力,间接优化了NAD+的再生效率。这种双向调节使能量代谢偏向NADH消耗(如TCA循环),而非用于菌体生长,从而在抑制生物量的同时维持了碳流向其他物质的分配。此外,菌株背景对NADH调控策略具有决定性影响,相对于AY12α,E01系列菌株更适合通过mPOS5实现碳代谢流的重新分配。
总体而言,ADH1敲除扰乱了NADH平衡,导致乙酸积累抑制菌体生长,引入NADH调节基因虽能部分恢复代谢,但仍需进一步降低乙酸积累以改善整体代谢状态。
2.4 乙酰辅酶A生成途径的优化
为进一步缓解乙酸积累对菌株的抑制作用,本研究尝试强化乙酰辅酶A合成途径,以促进乙酸向乙酰辅酶A的代谢转化。本研究在以E01为出发菌构建的系列重组菌株中引入其内源ACS1基因及沙门氏菌来源的突变型乙酰辅酶A合成酶SeACSL641P(该突变体在第641位点亮氨酸被替换为脯氨酸,能够保留催化乙酸生成乙酰辅酶A的功能,同时避免乙酰化导致的失活),构建重组菌株EDA、EcDA、EmDA、EuDA、EnDA、EDS、EcDS、EmDS、EuDS和EnDS。
在YPD静置发酵中,SeACSL641P的引入可显著改善菌株生长,其中EmDS的最终生物量较EmD和EuD提高59.84%,而ACS1过表达菌株EcDA、EmDA生物量也分别提升35.54%和38.52%,但仍然没有改善EnD的生长(图7),因此推测乙酰辅酶A强化策略可以减弱ADH1敲除对菌株生长带来的不利影响,且对特定菌株背景有效。
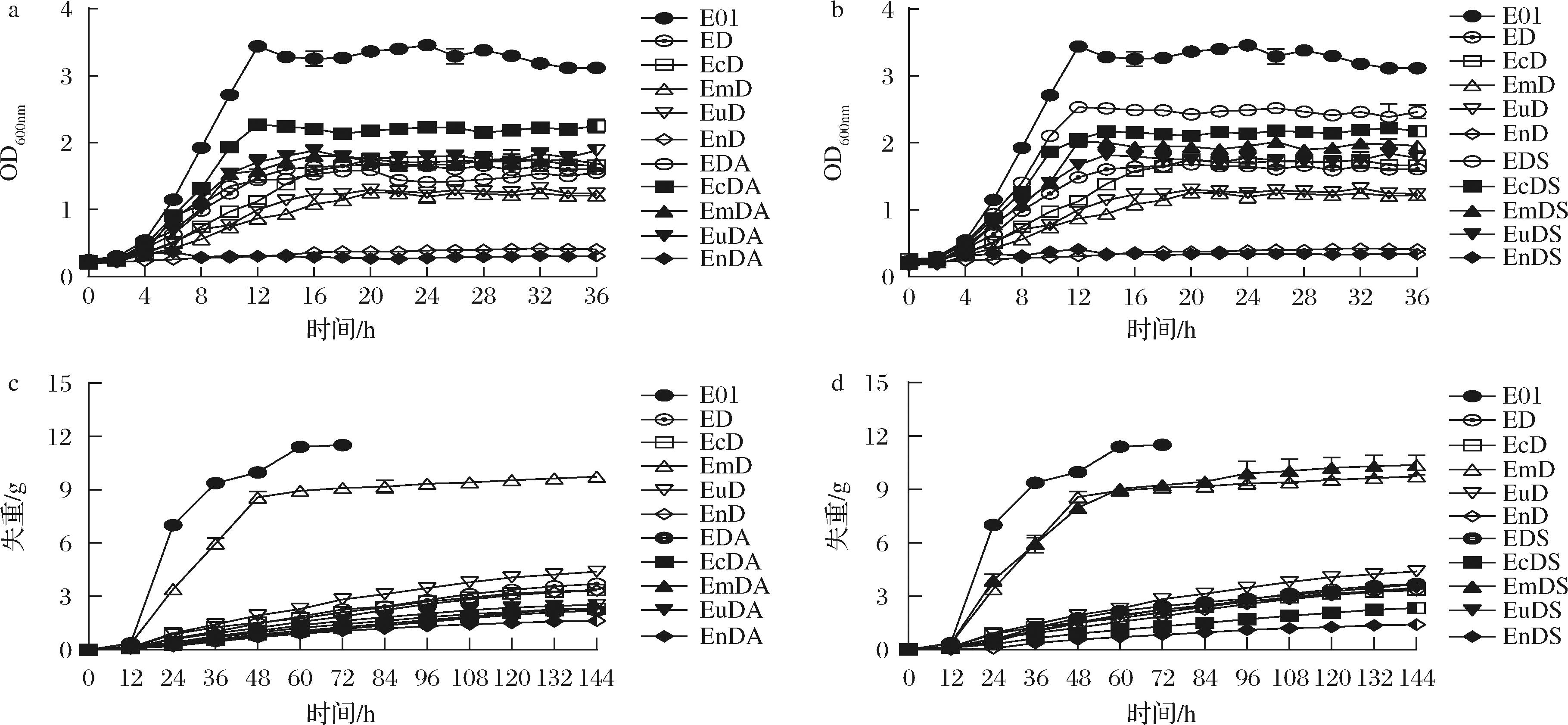
a-过表达ACS1前后重组菌株的生长曲线;b-引入SeACSL641P前后重组菌株的生长曲线;c-过表达ACS1前后重组菌株的CO2排放量;d-引入SeACSL641P前后重组菌株的CO2排放量
图7 出发菌株和乙酰辅酶A生成途径优化重组菌株生长和发酵失重情况
Fig.7 Growth and fermentation weight loss of the parental strain and recombinant strains with optimized acetyl-CoA biosynthetic pathways
高粱水解液发酵结果显示,SeACSL641P改造菌株(如EmDS)CO2释放量与出发菌株E01持平(图7),残余还原糖维持低水平,乙醇产量未显著下降,证明其通过高效催化乙酸转化维持了碳代谢平衡。相比之下,ACS1过表达重组菌株CO2排放量降低,残余还原糖也显著提高,乙醇积累量下降(表3),说明碳流在糖酵解和TCA循环受阻,可能与ACS1过表达引发ATP过度消耗有关[24]。
表3 E01及乙酰辅酶A合成强化重组菌株残余还原糖和乙醇生成量 单位:g/L
Table 3 Residual reducing sugar and ethanol contents of E01 and recombinant strains with enhanced acetyl-CoA synthesis
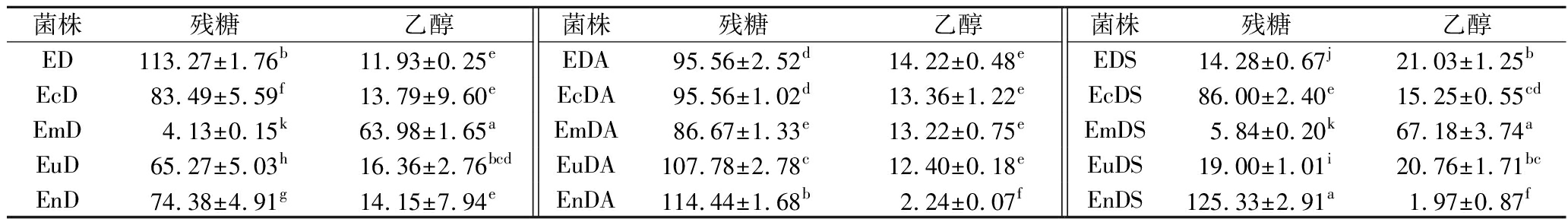
菌株残糖乙醇菌株残糖乙醇菌株残糖乙醇ED113.27±1.76b11.93±0.25eEDA95.56±2.52d14.22±0.48eEDS14.28±0.67j21.03±1.25bEcD83.49±5.59f13.79±9.60eEcDA95.56±1.02d13.36±1.22eEcDS86.00±2.40e15.25±0.55cdEmD4.13±0.15k63.98±1.65aEmDA86.67±1.33e13.22±0.75eEmDS5.84±0.20k67.18±3.74aEuD65.27±5.03h16.36±2.76bcdEuDA107.78±2.78c12.40±0.18eEuDS19.00±1.01i20.76±1.71bcEnD74.38±4.91g14.15±7.94eEnDA114.44±1.68b2.24±0.07fEnDS125.33±2.91a1.97±0.87f
注:不同小写字母表示差异显著(P<0.05)。
基于以上碳代谢流分析,SeACSL641P可能通过突变体抗乙酰化失活和低ATP依赖性的催化模式,将释放的碳流导向菌体生长或其他产物合成,使其在平衡乙酸代谢与菌体生长方面显著优于ACS1,为构建高产低耗的工业菌株提供了关键靶点。
对酒样中风味物质进行测定,ACS1过表达菌株EmDA乙酸含量反常上升至EmD的124.13%,推测是因为乙酰辅酶A过量积累的反馈抑制及ATP过度消耗,导致乙酸代谢受阻。相比之下,SeACSL641P由于其突变特性,能够避免乙酰化失活,显著提升乙酸转化效率,使多数重组菌株的乙酸水平下降。
酯类合成中,SeACSL641P对风味物质合成的促进效果优于ACS1。乙酸乙酯方面,SeACSL641P改造菌株EmDS产量达(22.71±1.72) mg/L,较出发菌E01提升17.55%,而ACS1过表达菌株并无显著增长。丁酸乙酯合成中,SeACSL641P改造菌株EcDS、EmDS和EuDS,丁酸乙酯产量分别提高3.18、1.13和2.42倍,其中EmDS菌株含量达(61.82±1.05) mg/L,较出发菌E01显著提高了19.56%,但其合成效率仍略低于单一引入NADH调节基因的Ec和Eu(图8),揭示辅因子调控对丁酸乙酯合成的特殊贡献,尽管如此,SeACSL641P在优化乙酸向乙酰辅酶A的转化方面仍然展现了明显优势。
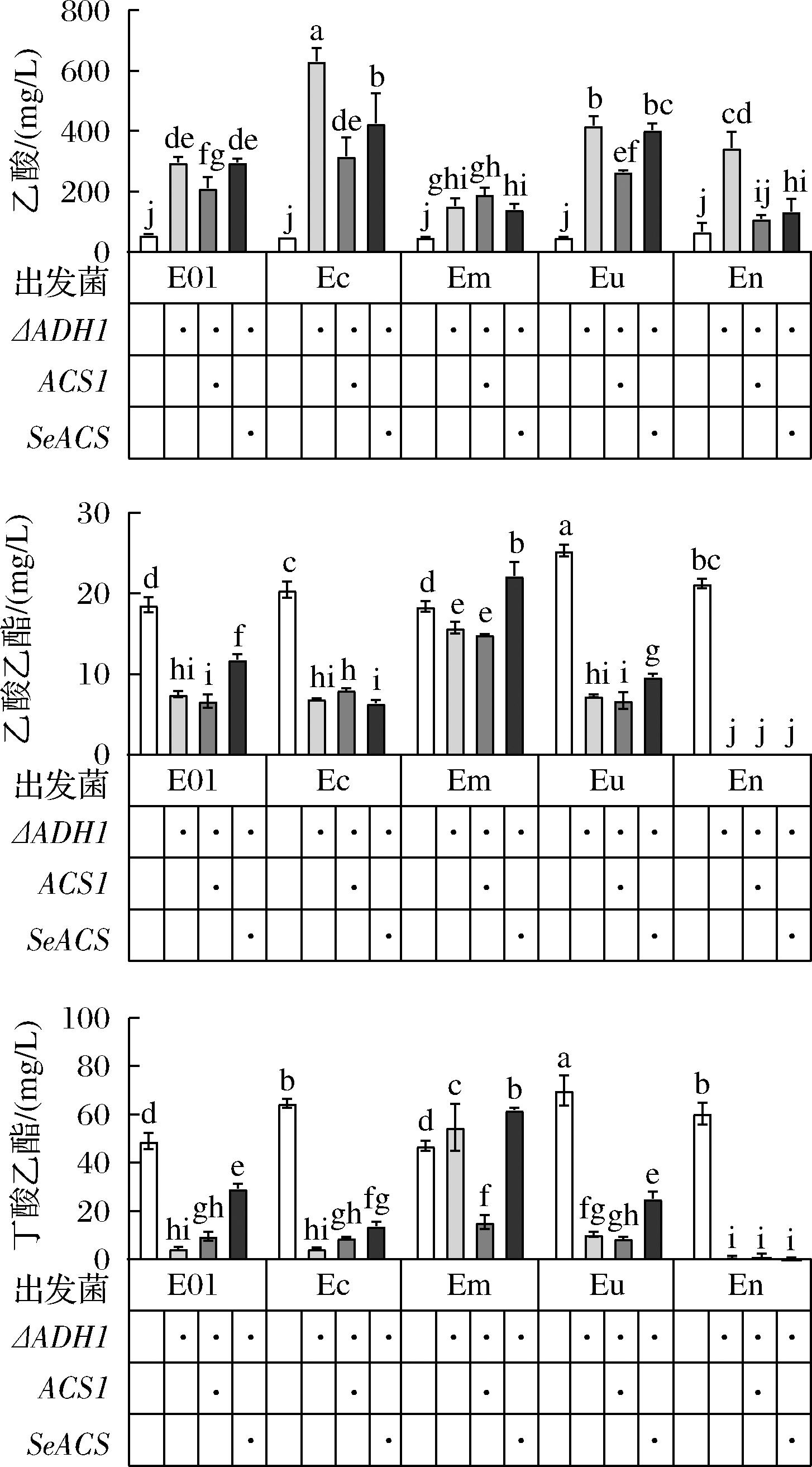
图8 以E01为出发菌的各改造重组菌株的乙酸、乙酸乙酯与丁酸乙酯产量
Fig.8 Production of acetate, ethyl acetate, and butyl butyrate by E01-derived recombinant strains
注:“·”表示在出发菌上进行的相应基因改造。
综上,SeACSL641P通过稳定酶活性和低能耗催化模式,显著优化了乙酸代谢与碳代谢流分配,尽管EnDA等菌株改造未达预期,研究证实了代谢工程在调控碳流和优化代谢产物合成方面的潜力,未来可结合代谢通量分析或联合多基因调控策略,解析突变体对代谢网络的重构机制,进一步优化菌株以提高目标产物的合成。
3 结论
本研究通过多重代谢工程手段优化酿酒酵母的代谢途径,旨在提高丁酸乙酯的生物合成效率。首先,通过敲除乙醇合成途径中的关键基因ADH1,期望实现更多的碳代谢流向丁酸乙酯的合成,但ADH1的敲除仍会造成胞内NADH积累,引发氧化还原失调、乙酸积累等问题,进而抑制细胞的生长。本研究分别引入4种不同来源的NADH调节基因(cPOS5、mPOS5、udhA和noxE),再进行乙醇合成通路的阻断,但细胞生长未见明显恢复,且发酵液中乙酸大量积累,进一步限制了菌株的代谢能力。为减少乙酸的负面影响,提高乙酰辅酶A的供应量,本研究进一步引入乙酰辅酶A合成酶,包括酿酒酵母内源的ACS1和突变体SeACSL641P。结果表明,SeACSL641P的引入使部分菌株显著提升了丁酸乙酯产量,推测其突变特性能避免乙酰化失活,保持较高的催化活性。然而,EmD背景下的代谢调控机制仍不清晰,EmDS在丁酸乙酯产量提升的同时,其碳代谢分配模式仍需进一步研究。
本研究基于代谢工程的多层次调控策略,综合碳流分配优化、氧化还原平衡调节及乙酸代谢重构,成功提升了酿酒酵母的丁酸乙酯合成能力,并验证了SeACSL641P在优化酯类合成中的潜力。研究结果不仅拓展了酿酒酵母在脂肪酸乙酯类化合物生物合成中的应用,也为未来通过代谢流分析和多基因协同调控进一步优化菌株提供了理论依据。
[1] 丁力杰, 唐云, 赵亚雄, 等.白酒中的重要酯类物质及主要来源研究现状[J].酿酒科技, 2024(3):91-100;107.
DING L J, TANG Y, ZHAO Y X, et al.Research status of important esters in Baijiu and their sources[J].Liquor-Making Science &Technology, 2024(3):91-100;107.
[2] ZAAK H, FERNANDEZ-LOPEZ L, OTERO C, et al.Improved stability of immobilized lipases via modification with polyethylenimine and glutaraldehyde[J].Enzyme and Microbial Technology, 2017, 106:67-74.
[3] 张舍熹. 丁酸发酵液萃取-酯化偶联合成丁酸乙酯的研究[D].广州:华南理工大学, 2015.
ZHANG S X.Study on synthesis of ethyl butyrate by butyric acid fermentation broth extraction coupling with esterification[D].Guangzhou:South China University of Technology, 2015.
[4] KRUIS A J, BOHNENKAMP A C, PATINIOS C, et al.Microbial production of short and medium chain esters:Enzymes, pathways, and applications[J].Biotechnology Advances, 2019, 37(7):107407.
[5] 赵静溶, 徐友强, 朱华, 等.浓香型白酒风味乙酯微生物合成机制研究进展[J].食品与生物技术学报, 2022, 41(10):1-16.
ZHAO J R, XU Y Q, ZHU H, et al.Research progress on microbial synthetic mechanism of flavor ethyl esters in strong-flavor Baijiu[J].Journal of Food Science and Biotechnology, 2022, 41(10):1-16.
[6] 王晓程, 徐友强, 李秀婷, 等.中国传统发酵食品来源典型小分子脂肪酸酯合成微生物及酶的研究进展[J].中国食品学报, 2021, 21(4):345-355.
WANG X C, XU Y Q, LI X T, et al.Research progress in microorganisms and enzymes for synthesis of typical small molecule fatty acid esters from traditional Chinese fermented foods[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(4):345-355.
[7] 沈咏梅, 谢晓娜, 荀二娜, 等.脂肪酶催化制备丁酸乙酯的研究[J].成都大学学报(自然科学版), 2012, 31(1):4-7.
SHEN Y M, XIE X N, XUN E N, et al.Research on preparation of ethyl butyrate catalyzed by lipase[J].Journal of Chengdu University (Natural Science Edition), 2012, 31(1):4-7.
[8] GAJEWSKI J, PAVLOVIC R, FISCHER M, et al.Engineering fungal Tailored designing of a diploid S.cerevisiae natural isolate for increased production of fatty acid ethyl ester[J].Nature Communications, 2017, 8:14650.
[9] KUMARI P, SHARMA J, SINGH A K, et al.Tailored designing of a diploid S.cerevisiae natural isolate for increased production of fatty acid ethyl ester[J].Chemical Engineering Journal, 2023, 453:139852.
[10] 张果. 高产己酸乙酯酿酒酵母菌株的选育[D].天津:天津科技大学, 2022.
ZHANG G.Construction of Saccharomyces cerevisiae strain with higher production of ethyl hexanoate[D].Tianjin:Tianjin University of Science and Technology, 2022.
[11] 任津莹. 同时高产乳酸乙酯和乙酸乙酯酿酒酵母菌株的构建[D].天津:天津科技大学, 2020.
REN J Y.Construction of Saccharomyces cerevisiae strains with simultaneous high yield of ethyl lactate and ethyl acetate[D].Tianjin:Tianjin University of Science and Technology, 2020.
[12] 石文琪. 高产风味酯酿酒酵母菌株的选育[D].天津:天津科技大学, 2021.
SHI W Q.Breeding of flavor esters high-producing Saccharomyces cerevisiae strains[D].Tianjin:Tianjin University of Science and Technology, 2021.
[13] 郑楠. 低产高级醇酿酒酵母菌株的构建及应用研究[D].天津:天津科技大学, 2018.
ZHENG N.Research on the construction and application of Saccharomyces cerevisiae strains for low-production of higher alcohols[D].Tianjin:Tianjin University of Science and Technology, 2018.
[14] 张卜升, 袁丛丛, 高杏, 等.不同产地酱香型白酒化学风味和感官特征差异分析[J].食品科学, 2023, 44(12):235-243.
ZHANG B S, YUAN C C, GAO X, et al.Differences in chemical flavor and sensory characteristics of sauce-flavor Baijiu from different regions[J].Food Science, 2023, 44(12):235-243.
[15] RAJ S B, RAMASWAMY S, PLAPP B V.Yeast alcohol dehydrogenase structure and catalysis[J].Biochemistry, 2014, 53(36):5791-5803.
[16] COURTNEY D K, SU Y, JACOBSON T, et al.Relative activities of the β-ketoacyl-CoA and acyl-CoA reductases influence product profile and flux in a reversed β-oxidation pathway[J].ACS Catalysis, 2023, 13(9):5914-5925.
[17] XIAO W S, LOSCALZO J.Metabolic responses to reductive stress[J].Antioxidants &Redox Signaling, 2020, 32(18):1330-1347.
[18] ZHAI X W, YANG R H, CHU Q Y, et al.AMPK-regulated glycerol excretion maintains metabolic crosstalk between reductive and energetic stress[J].Nature Cell Biology, 2025, 27(1):141-153.
[19] 秦义, 董志姚, 刘立明, 等.工业微生物中NADH的代谢调控[J].生物工程学报, 2009, 25(2):161-169.
QIN Y, DONG Z Y, LIU L M, et al.Manipulation of NADH metabolism in industrial strains[J].Chinese Journal of Biotechnology, 2009, 25(2):161-169.
[20] ZHAO H J, ZHOU F, XING Q, et al.The soluble transhydrogenase UdhA affecting the glutamate-dependent acid resistance system of Escherichia coli under acetate stress[J].Biology Open, 2018, 7(9):bio031856.
[21] 孙明娣. 酿酒酵母NADH激酶Pos5p在细胞抵抗氧化胁迫中的作用[D].无锡:江南大学, 2010.
SUN M D.The role of Saccharomyces cerevisiae NADH kinase Pos5p on the defense of oxidative stress [D].Wuxi:Jiangnan University, 2010.
[22] BAKKER B M, OVERKAMP K M, VAN MARIS A J A, et al.Stoichiometry and compartmentation of NADH metabolism in Saccharomyces cerevisiae[J].FEMS Microbiology Reviews, 2001, 25(1):15-37.
[23] GATTER M, OTTLIK S, KÖVESI Z, et al.Three alcohol dehydrogenase genes and one acetyl-CoA synthetase gene are responsible for ethanol utilization in Yarrowia lipolytica[J].Fungal Genetics and Biology, 2016, 95:30-38.
[24] LIU W S, ZHANG B, JIANG R R.Improving acetyl-CoA biosynthesis in Saccharomyces cerevisiae via the overexpression of pantothenate kinase and PDH bypass[J].Biotechnology for Biofuels, 2017, 10:41.