随着贝类养殖业和加工业不断发展,中国每年会产生大量废弃贝壳,其直接丢弃不仅造成了大量土地资源的浪费,还引发了周围环境的严重污染[1]。针对废弃贝壳的资源化利用,国内外学者将其制备成吸附剂、土壤改良剂、建筑材料、催化剂、医药填料和动物饲料等[2]各类新材料。
贝壳中主要成分是CaCO3,其经高温煅烧后转变成CaO。煅烧生成的CaO粉末溶于水后呈弱碱性,能有效分解酸性农药,释放的Ca2+还能抑制微生物的生长[3]。并且,其还具有多孔结构,因此具有良好的吸附性能,能有效去除多种果蔬表面的杂质和农药残留,是一种较好的果蔬洗涤剂原料。日本、韩国及中国都有多种以煅烧贝壳粉制备的果蔬清洗剂,其具有天然无毒、环保可降解、适合敏感人群等优点,深受消费者青睐[4]。然而,目前市场上的贝壳粉基清洗剂基本以CaO粉末形式存在,后者会与水反应生成Ca(OH)2,微溶于水,会快速沉淀析出,这就导致清洗剂与待洗物接触不充分,需要长时间清洗才能达到较好效果。
泡腾片是一种特殊剂型的片剂,广泛应用于医药和饮料领域,同时在清洁领域也展现出一定的应用潜力。其工作原理是利用有机酸和弱碱作为崩解剂,通过酸碱反应生成CO2气体,从而实现水中泡腾反应的效果,进而延长洗涤剂与待洗物之间的接触时间,提高洗涤效果。截至目前,已有研究人员将NaCl、NaClO2等作为清洗剂的主要原料,制备泡腾片清洗剂,后者能高效去除果蔬表面的微生物[5-6]。然而,目前尚无关于将煅烧贝壳粉制备成泡腾片剂型的研究报道。基于此,本研究以不同温度煅烧的贻贝壳粉为原料,以泡腾片的崩解时限和发泡量为主要指标,优化了泡腾片清洗剂的制备工艺,并研究了该清洗剂对圣女果微生物的清除效果、感官品质及营养成分的保留情况。本研究成果为贝壳的高值化利用提供了新的方案,所研发的贝壳泡腾片清洗剂也展现出广阔的市场前景。
1 材料与方法
1.1 材料与试剂
贻贝,德清秋山市场;NaHCO3、三氯乙酸(trichloroacetic acid,TCA)、H3PO4、果胶、福林-酚、没食子酸、芦丁,杭州吉工生物科技有限公司;无水柠檬酸,上海泰坦科技股份有限公司;NaOH、HCl、无水乙醇、聚乙二醇(polyethylene glycol,PEG)6000、聚乙烯吡咯烷酮(polyvinylpyrrolidone,PVP)K30、抗坏血酸、NaCl、邻苯二甲酸氢钾、酚酞、Na2CO3、NaNO2、Al(NO3)3,国药集团化学试剂有限公司;红菲咯啉,杭州邦易化工有限公司;FeCl3、甲基纤维素,杭州双木化工有限公司。
1.2 仪器与设备
Q-500B2高速多功能粉碎机,上海冰都电器有限公司;KSL-1100X马弗炉,合肥科晶材料技术有限公司;YXQM-2L油封行星球磨机,长沙米淇仪器设备公司;纳米粒度电位分析仪,英国Malvern Panalytical公司;Sigma300扫描电子显微镜(scanning electron microscope,SEM),德国Zeiss股份公司;IMJ-54A高温灭菌锅,施都凯仪器设备有限公司;HX-4拍打式均质机,上海沪析实业有限公司;LRH-250F培养箱,上海一恒科学仪器有限公司;Spark 20M酶标仪,Tecan集团;himac CR系列高速冷冻离心机,天美仪拓实验室设备有限公司;TA XT PlusC质构仪,厦门超技仪器设备有限公司;Color Quest色差仪,美国HunterLab公司。
1.3 实验方法
1.3.1 贝壳粉的制备
将贻贝煮沸至开口,去除贝肉并将外表面刷洗干净得到贻贝壳,将贻贝壳放入65 ℃干燥箱中烘干3 h,将烘干后贻贝壳破碎成小块。称取破碎的贻贝壳250 g,向其中加入2 500 mL 4 mol/L的NaOH溶液浸泡处理36 h。在浸泡处理的第1小时和最后1小时分别进行超声波协同处理,超声波频率40 kHz,功率300 W。处理后的贻贝壳用清水冲洗干净并置入65 ℃干燥箱烘干3 h。称取NaOH溶液处理且干燥后的贻贝壳250 g,向其中加入2 500 mL 1 mol/L的盐酸浸泡处理4 h。处理后的贻贝壳用清水冲洗并置于65 ℃干燥箱中烘干3 h。将经过碱酸处理的贻贝壳倒入高速多功能粉碎机对其进行粉碎,粉碎时间5 min,取出后过150目的不锈钢标准筛,得到微米级贝壳粉。以微米级贝壳粉作为原料,分别在马弗炉中以750、850、950 ℃煅烧2 h,然后放入球磨机中进行球磨,球磨条件为:料球比1∶20(质量比)、球磨时间60 min、球磨转速600 r/min,得到纳米贝壳粉。
1.3.2 贝壳粉泡腾片清洗剂的制备
以球磨后的煅烧贻贝壳粉为原料,采用碱制粒后与酸颗粒混合压片的制粒技术制备泡腾片清洗剂。选用黏合剂(PVP无水乙醇溶液)质量分数为3%,润滑剂(PEG 6 000)质量分数为2%[7],同时为保证贝壳粉作为有效成分发挥作用,选用贝壳粉质量分数为35%,崩解剂质量分数为60%,以泡腾片单位质量崩解时限和单位质量发泡量为指标,通过单因素试验确定崩解剂的比例,具体实验操作如下:
选取崩解剂(NaHCO3∶柠檬酸)质量比为0.3∶1、0.4∶1、0.5∶1。取3份3.50 g的贝壳粉分别与1.38、1.71、2.00 g NaHCO3混合均匀,每份加入10 mL 30 mg/mL 的PVP无水乙醇溶液作为黏合剂制软材,软材要求“手握成团,轻压则散”;然后经过24目筛整粒,50 ℃干燥3 h得到碱颗粒;再向每份中分别加入4.62、4.29、4.00 g柠檬酸和0.20 g润滑剂(PEG 6 000),充分混合均匀,用单冲压片机中压片。
1.3.3 贝壳粉泡腾片清洗性能测定
1.3.3.1 崩解时限检测[8]
取1片泡腾片于装有200 mL水的烧杯中,把泡腾片放入水中开始计时,等完全崩解时终止计时,即为崩解时限。
1.3.3.2 发泡量检测[9]
取干燥的250 mL量筒,向其中加入20 mL水,然后投入1片泡腾片,观察最大发泡量的体积,平均发泡体积不得少于6 mL。
1.3.3.3 明亮度测定
使用色差仪对贝壳粉和对应泡腾片的明亮度进行测定,每个样品记录6次读数并计算平均值。
1.3.4 贝壳粉泡腾片清洗剂对圣女果的清洗效果评价
挑选大小相近、表面完整无损伤的圣女果。为探究作用时间对圣女果的清洗效果:取8个装有100 mL水的烧杯,编号1~8,各放入10 g圣女果;其中1~4号为不加入泡腾片的清水处理组,按编号从小到大分别浸泡10、20、30、40 min后取出样品;5~8号为加入泡腾片的处理组,按编号从小到大分别浸泡10、20、30、40 min后取出样品,以未经任何处理的圣女果作为对照组。为探究作用浓度对圣女果的清洗效果:取5个装有100 mL水的烧杯,各放入10 g圣女果,然后每杯中分别加入0、1、2、3、4 g泡腾片,浸泡20 min后取出样品。通过菌落总数、颜色、硬度、可滴定酸、维生素C、总酚、总黄酮、果胶酶等指标评价圣女果的品质,测定方法如下:
1.3.4.1 菌落总数测定
参照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》并稍作修改,将10.0 g样品放入盛有90 mL无菌生理盐水的无菌均质袋中,用拍击式均质器拍打2 min,制成质量比为1∶10的样品匀液。用无菌生理盐水对样品匀液进行10倍系列梯度稀释,选取适合稀释度的样品匀液,取1 mL加入装有平板计数琼脂培养基的培养皿中,涂布均匀,平放于实验台上20 min,使菌液渗入培养基内。倒置于37 ℃培养箱中培养48 h,计平板菌落数,并计算菌落总数。
1.3.4.2 SEM分析
从圣女果上切下长×宽为2 mm×2 mm的果皮样品,置于2.5%(体积分数,下同)戊二醛溶液中,保证样品全部浸没在液体中,4 ℃下固定24 h;使用PBS(0.1 mol/L,pH=7.2)漂洗3次,每次10 min;随后按照如下顺序脱水,每步15 min:30%乙醇→50%乙醇→70%乙醇→80%乙醇→90%乙醇→95%乙醇→无水乙醇;最后冷冻干燥至完全脱水。将制备好的样品用导电胶黏在样品台上,喷金电流10 mA,喷金时间30 s,3.0 kV加速电压下进行观察。
1.3.4.3 色差测定
根据CIE LAB颜色参数,使用色差仪在每个圣女果的赤道区域测量其外部颜色。每个样品记录6次读数。色差通常使用ΔE表示,其计算如公式(1)所示:
(1)
式中:ΔE,色差;ΔL,明度差;Δa,红绿轴色度差;Δb,黄蓝轴色度差。
1.3.4.4 硬度测定
取大小相似、形状接近的样品,用TA-XT2质构仪进行压缩实验。采用直径40 mm的圆柱形探头,测试参数为:测试速度1 mm/s,间隔2 s,距离35 mm,压缩程度25%,触发力3 g,每组实验重复3次,取平均值。
1.3.4.5 果胶酶活性测定
采用3,5-二硝基水杨酸终止法。称取0.2 g果皮于预冷的研钵中,加入1 mL(0.04 mol/L,pH=4.5)醋酸钠溶液研磨,将研磨过后的匀浆倒入10 mL离心管,用醋酸钠缓冲液冲洗3遍,每次加1 mL,将样液置于4 ℃冰箱中保存1 h。4 ℃、5 000 r/min离心30 min,上清液即为粗酶液提取液。将提取液置于0 ℃碎冰中以保存其酶活性。吸取0.2 mL(0.04 mol/L,pH=4.5)醋酸钠缓冲液于玻璃试管中,加入10 mg/mL果胶溶液0.3 mL,吸取0.1 mL粗酶提取液于试管中,后加入0.4 mL蒸馏水,于37 ℃水浴保温1 h,立即加入1 mL DNS终止,置于沸水中显色5 min,待冷却后于540 nm下比色。根据葡萄糖标准曲线回归方程(y=0.149 5x+0.094 3,R2=0.996 2)查出相应的还原糖微克数。果胶酶的活性以每小时每克鲜重果蔬组织样品在37 ℃催化多聚半乳糖醛酸水解形成还原糖的质量(mg)表示,即mg/(h·g),计算如公式(2)所示:
果胶酶活性![]()
(2)
式中:V,样品提取液总体积,mL;C,标准曲线得到的葡萄糖质量,μg;Vs,测定时所用样品提取液体积,mL;t,酶促反应时间,h;m,样品质量,g。
1.3.4.6 维生素C含量的测定
参照曹建康等[10]的方法并稍作修改。取10.0 g圣女果置于研钵中,加入20 mL 50 mg/mL TCA溶液,在冰浴条件下研磨成浆状,转入到100 mL容量瓶中,并用50 mg/mL TCA溶液定容,混合、提取10 min后,8 000 r/min离心10 min,收集上清液。取1.0 mL上清液于试管中,加入1.0 mL 50 mg/mL TCA溶液,再加入1.0 mL无水乙醇,混合、摇匀后加入0.5 mL 4 mg/mL磷酸-乙醇溶液,1.0 mL 5 mg/mL红菲咯啉-乙醇溶液和0.5 mL 0.3 mg/mL FeCl3-乙醇溶液,30 ℃反应60 min,在波长534 nm处测定吸光值,重复3次。制作维生素C标准曲线(y=0.582 3x-0.494 2,R2=0.998 5)。根据吸光度值在标准曲线上查出相应的维生素质量,圣女果中维生素C含量的计算如公式(3)所示:
维生素C含量![]()
(3)
式中:V,样品提取液总体积,mL;C,标准曲线得到的维生素C质量,μg;Vs,测定时样品提取液体积,mL;m,样品质量,g。
1.3.4.7 可滴定酸含量测定
采用NaOH滴定法。配制0.1 mol/L的NaOH溶液,滴定前使用邻苯二甲酸氢钾标定NaOH溶液。称取圣女果10.0 g,研磨充分后,转移至100 mL容量瓶中,纯水定容至刻度,摇匀。5 000 r/min离心15 min。吸取20.0 mL上清液,加入2滴10 mg/mL酚酞指示剂,用已标定的NaOH溶液滴定至溶液为微红色,并在30 s内不褪色,记录滴定消耗NaOH溶液体积。可滴定酸含量的计算如公式(4)所示:
可滴定酸含量![]()
(4)
式中:V,样品提取液总体积,mL;C,NaOH滴定液浓度,mol/L;V1,滴定滤液消耗的NaOH的体积,mL;V0,滴定蒸馏水消耗的NaOH的体积,mL;f,折算系数,g/mmol;Vs,滴定时所取滤液体积,mL;m,样品质量,g。
1.3.4.8 可溶性固形物测定
使用手持折光仪测定。取圣女果肉研磨充分,5 000 r/min离心15 min。吸取2滴汁液滴到折射棱镜上进行读数。
1.3.4.9 总酚测定
采用福林-酚法。称取1.0 g样品,加入20 mL 60%乙醇溶液,超声波提取30 min,4 ℃、8 000 r/min离心10 min。取1 mL上清液,加入1 mL福林-酚试剂、3 mL 75 g/L的Na2CO3溶液和5 mL蒸馏水,避光显色2 h,测定反应液在760 nm波长下的吸光度。根据没食子酸标准曲线回归方程(y=0.000 6x+0.111 1,R2=0.995 4)计算总酚含量,计算如公式(5)所示:
总酚含量![]()
(5)
式中:V,样品提取液总体积,mL;C,标准曲线得到的质量浓度,μg/mL;m,样品质量,g。
1.3.4.10 总黄酮含量测定
采用硝酸铝显色法。样品提取步骤同1.3.4.9节。取1 mL样品上清液,加入1 mL 50 g/L NaNO2溶液,振荡摇匀后静置6 min,加入1 mL 100 g/L AgNO3溶液,再静置6 min,加入10 mL 40 g/L的NaOH溶液,反应15 min后测定在510 nm波长下的吸光度。根据芦丁标准曲线回归方程(y=0.004 6x+0.100 4,R2=0.999)计算总黄酮含量,计算如公式(6)所示:
总黄酮含量![]()
(6)
式中:V,样品提取液总体积,mL;C,标准曲线得到的质量浓度,μg/mL;m,样品质量,g。
1.4 数据统计及分析
每组实验平行进行3次,数据以“平均值±标准差”表示。采用Excel 2010对数据进行整理,采用SPSS 27分析数据,P值采用Duncan多主范围检验和独立样本T检验,P<0.05认为具有显著性差异。使用Origin 2024软件作图。
2 结果与分析
2.1 贝壳粉泡腾片清洗剂制备工艺研究
2.1.1 贝壳煅烧温度和崩解剂配比对贝壳粉泡腾片崩解时限和发泡量的影响
泡腾片是利用有机酸和弱碱作崩解剂,二者通过酸碱反应生成CO2气体,以此实现水中发生泡腾反应的效果(反应式1)。泡腾片中常用的有机酸有柠檬酸、酒石酸、富马酸等。其中,柠檬酸使用最为广泛,其酸性强,易溶于水,通过非水制粒技术(如PVP乙醇溶液制粒)可有效延缓吸湿,保证制剂稳定[11]。常用的碱源有Na2CO3、NaHCO3、K2CO3、KHCO3、CaCO3等,其中以NaHCO3最为常用[12]。NaHCO3与柠檬酸作为泡腾片的核心辅料,其比例会对泡腾片的崩解时限和发泡量有很大影响[13],而崩解时限和发泡量是评价泡腾片性质的重要指标。
泡腾片崩解的反应式为:
C6H8O7+3 NaHCO3![]() Na3C6H5O7+3H2O+3CO2↑
Na3C6H5O7+3H2O+3CO2↑
(1)
2C6H8O7+3CaCO3![]() Ca3(C6H5O7)2+3H2O+3CO2↑
Ca3(C6H5O7)2+3H2O+3CO2↑
(2)
2C6H8O7+3CaO![]() Ca3(C6H5O7)2+3H2O+CO2↑
Ca3(C6H5O7)2+3H2O+CO2↑
(3)
煅烧贝壳粉中含有CaCO3和CaO,自身可作为一部分碱源(反应式2、3),而煅烧温度对煅烧贝壳粉中CaCO3与CaO含量有重要影响。基于此,在本研究中,以不同温度(750、850、950 ℃)煅烧的贝壳粉为原料,考察崩解剂中碱与酸的比例(NaHCO3∶柠檬酸=0.3∶1、0.4∶1、0.5∶1)对贝壳粉泡腾片崩解时限和发泡量的影响(图1)。结果表明,煅烧温度和酸碱比都对贝壳粉泡腾片性能有显著影响。当以750 ℃煅烧贝壳粉为原料,NaHCO3∶柠檬酸比分别为0.3∶1、0.4∶1、0.5∶1的条件下,所研发的泡腾片的崩解时限分别为45.4、46.2、69.5 s/g,发泡量分别为29.7、25.2、28.7 mL/g。结果表明,随着NaHCO3∶柠檬酸配比的增加,崩解效率呈现降低的趋势。若采用850 ℃煅烧的贝壳粉制备泡腾片,在3种NaHCO3∶柠檬酸配比下的崩解时限分别为35.8、32.1、31.1 s/g,发泡量分别为48.2、58.0、54.5 mL/g。综合各项指标来看,在此条件下,NaHCO3∶柠檬酸=0.4∶1为最优配比。而对于950 ℃煅烧贝壳粉制备的泡腾片,虽然在0.4∶1和0.5∶1的配比下能够实现27.5~30.5 s/g的快速崩解,然而其发泡量却急剧下降至2.7~2.8 mL/g。
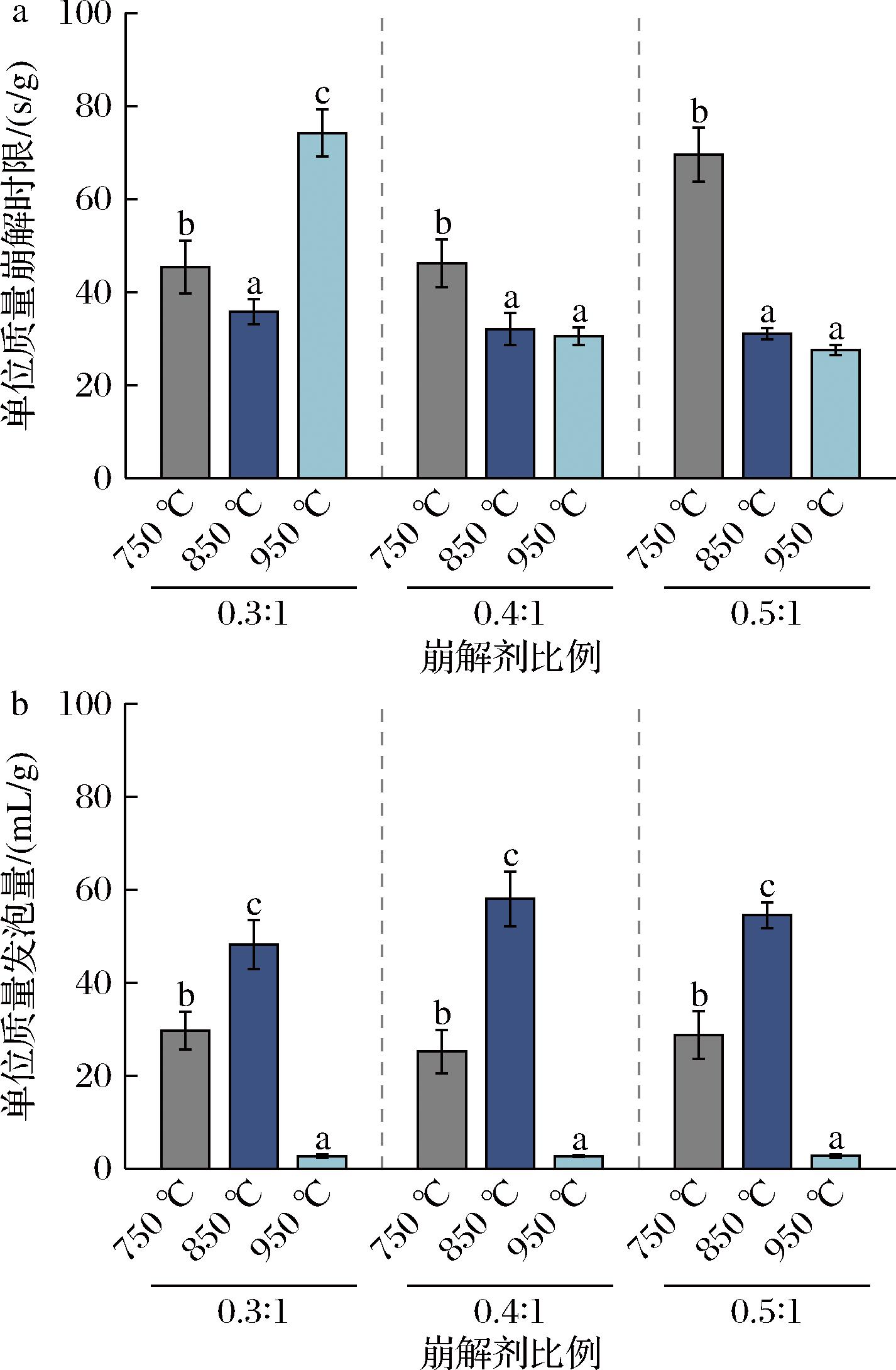
a-单位质量崩解时限;b-单位质量发泡量
图1 崩解剂比例(NaHCO3∶柠檬酸)对泡腾片性质的影响
Fig.1 Effect of disintegrant ratio (sodium bicarbonate∶citric acid) on the properties of effervescent tablets
注:不同小写字母表示同一崩解剂比例下的不同温度煅烧贝壳粉,具有统计学意义(P<0.05)(下同)。
由图2可知,NaHCO3∶柠檬酸=0.4∶1时,750 ℃煅烧的贝壳粉制备的泡腾片崩解速度较快,但发泡量不足,刚入水时泡腾片剂因重力下沉,随后产生气体使片剂漂浮,与水接触生成的气体均匀,整体崩解过程差异小;850 ℃煅烧的贝壳粉制备的泡腾片崩解速度快,发泡量大,刚入水时即产生大量气体,泡腾片剂悬浮在液面上,泡腾反应剧烈,有利于清洗过程中泡腾片有效成分与待洗物的充分、全面接触;950 ℃煅烧的贝壳粉制备的泡腾片崩解速度较慢,发泡量小,生成的气体不足以支撑片剂本身质量,整体崩解过程在溶液底部进行。综合上述结果可知,以850 ℃煅烧的贝壳粉为原料,NaHCO3∶柠檬酸=0.4∶1制备的泡腾片性能最佳。

a-750 ℃;b-850 ℃;c-950 ℃
图2 泡腾片崩解过程图(NaHCO3∶柠檬酸=0.4∶1)
Fig.2 Diagram of the disintegration process of effervescent tablets (sodium bicarbonate∶citric acid=0.4∶1)
2.1.2 贝壳煅烧温度和崩解剂配比对泡腾片明亮度和外观的影响
泡腾片的色泽和外观是影响其品质的重要指标,贝壳粉作为泡腾片的核心功能组分(占比35%),其明亮度(L*值)直接决定终产品的表观品质。如图3-a所示。随着煅烧温度从750 ℃升至850 ℃,贝壳粉L*值由91.03显著提升至96.57;当温度继续升高至950 ℃,贝壳粉L*值增加至99.27。该结果与邸玲[14]研究得出的煅烧温度对不同种类贝壳粉白度的影响规律相似,原因是800 ℃时,贝壳粉中的CaCO3发生热解生成CaO,CaO呈白色粉末状,造成白度急剧增大。采用相同煅烧温度的贝壳粉为原料时,不同崩解剂比例的泡腾片L*值均无显著性差异。
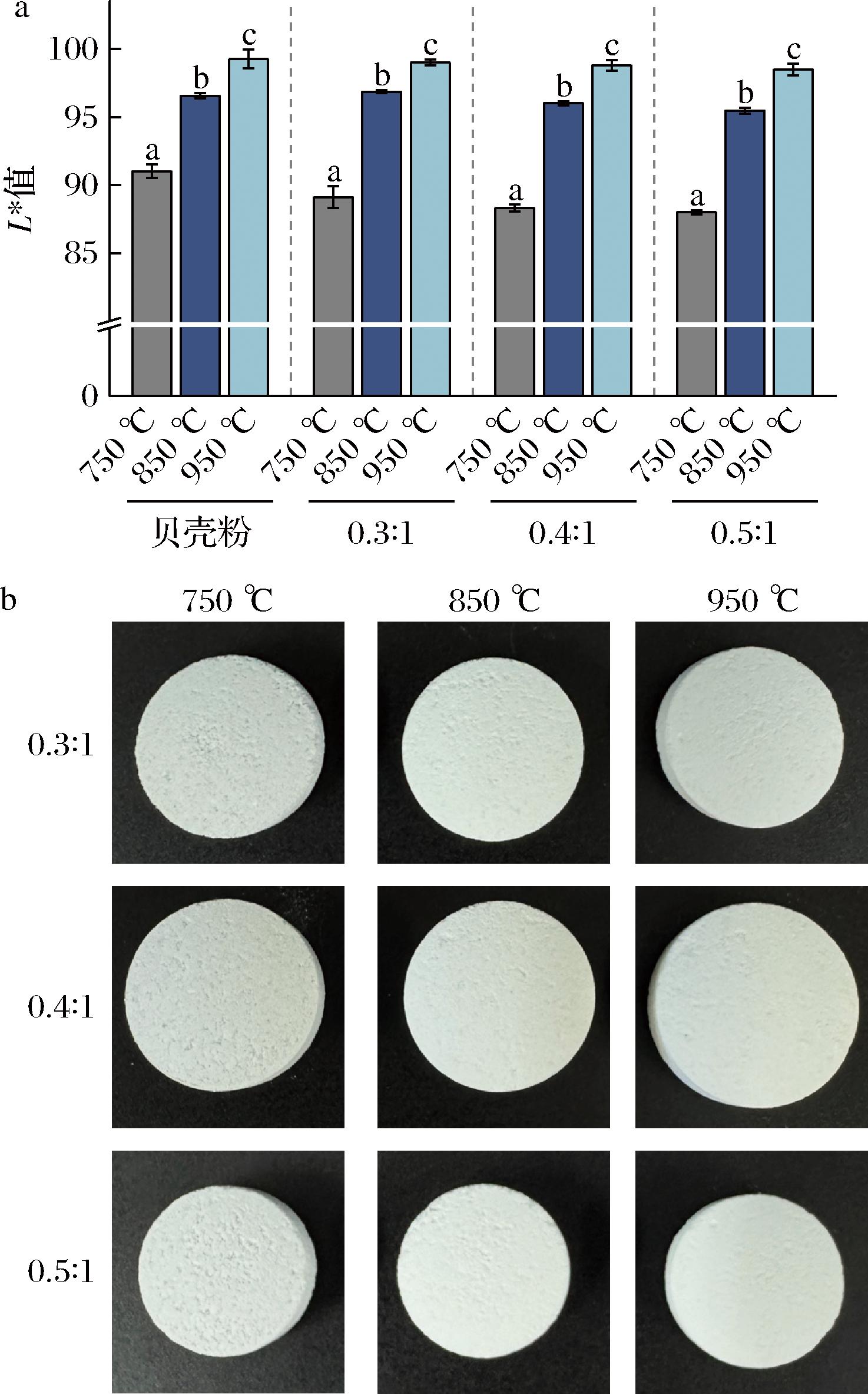
a-对明亮度的影响;b-对外观的影响
图3 对明亮度和外观的影响
Fig.3 Effect on brightness and appearance
如图3-b所示,当煅烧温度为750 ℃时,所得泡腾片外观偏灰色,颜色较暗,表面粗糙,有明显的不规则凹陷;温度提升至850 ℃时,样品色度显著改善,粗糙度降低,形成光滑表面;当温度达到950 ℃时,制得的泡腾片更加洁白光滑。这可能与高温下CaCO3发生热分解,生成CaO和CO2的同时内部形成孔隙结构[15],促使泡腾片各组分颗粒界面融合形成连续致密结构有关。
2.2 贝壳粉泡腾片清洗剂对圣女果的清洗作用评价
2.2.1 对微生物的清除效果
以圣女果为对象,评价850 ℃煅烧、NaHCO3∶柠檬酸=0.4∶1条件下制备的泡腾片对微生物去除效果,结果如图4所示,当泡腾片使用量为2 g/100 mL时,其去除微生物的效果随浸泡时间的延长而增加(图4-a)。处理10 min时,菌落总数减少(0.90±0.01) lg CFU/g,清除率为87.4%;若处理时间延长至20 min 和30 min,菌落总数分别减少了(1.36±0.04)、(2.32±0.20) lg CFU/g,清除率提升至91.3%和99.6%。当作用时间达到40 min时,微生物清除率达到100%。相比之下,清水组在同等时间梯度下的清除率仅分别为14.8%、21.7%、29.1%和34.3%。清洗剂浓度梯度实验表明(图4-b),固定作用时间为25 min时,当泡腾片质量浓度从0 g/100 mL(清水组)提升至1 g/100 mL时,菌落总数减少(0.71±0.01) lg CFU/g,对应清除率84.4%;质量浓度增加至2 g/100 mL时,菌落总数进一步减少(0.66±0.05) lg CFU/g,对应清除率96.5%;当质量浓度≥3 g/100 mL时,可实现完全灭菌。该结果显示,清洗剂在较低浓度下即表现出高效微生物清除能力。
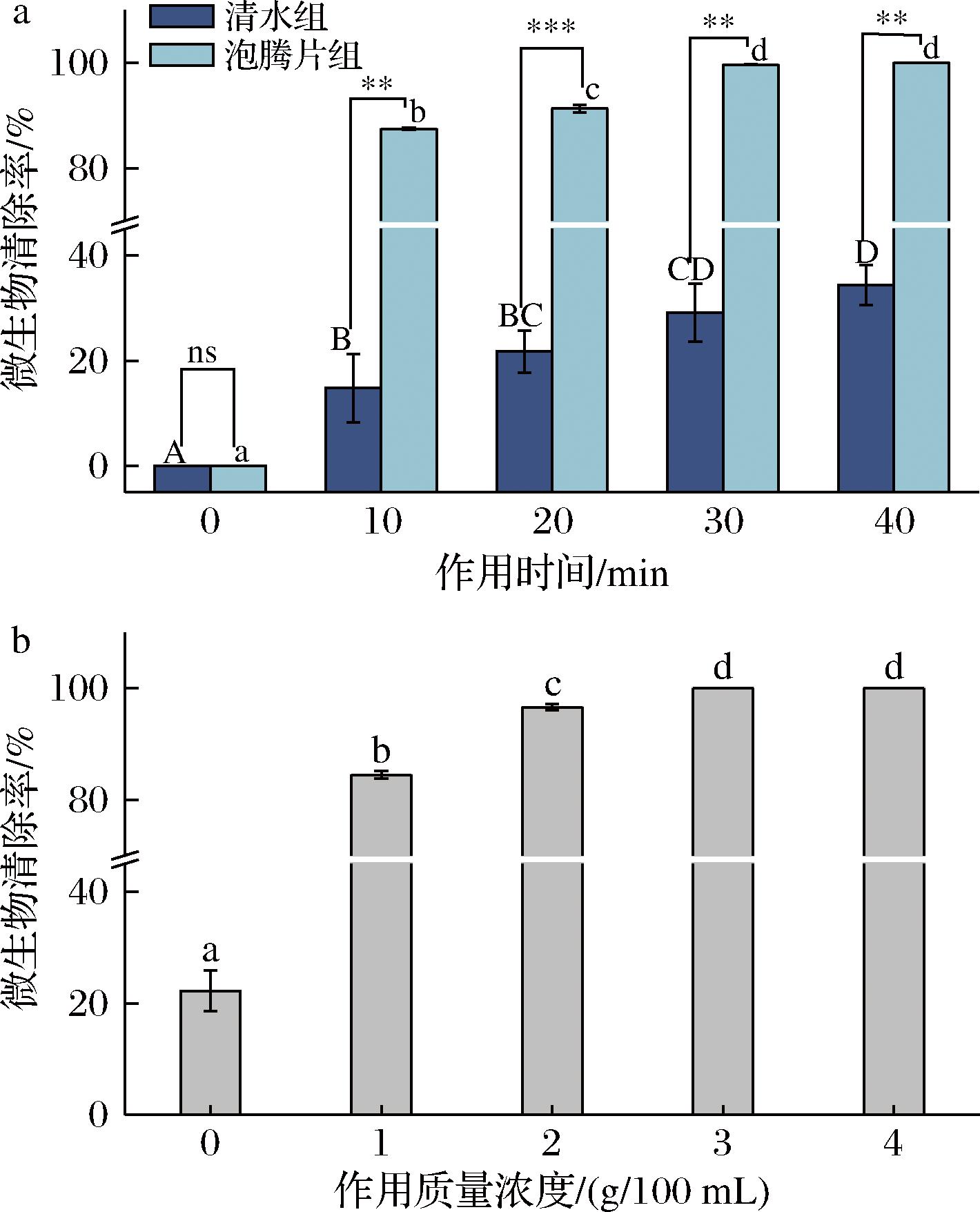
a-作用时间;b-作用质量浓度
图4 贝壳粉泡腾片对圣女果微生物的清除效果
Fig.4 Effect of nano-shell powder effervescent tablet on removal of microorganisms from cherry tomatoes
注:不同大写字母表示清水组内,不同小写字母表示泡腾片组内,*表示清水组和泡腾片组间,均具有统计学意义(P<0.05),**表示P<0.01,***表示P<0.001,ns表示无显著差异(下同)。空白对照 组菌落总数<10,无菌落长出,此次检验结果有效。
贝壳粉泡腾片清洗剂中发挥减菌作用的主要是CaO,其抗菌活性主要基于2个作用机制,一是CaO与水反应形成碱性的氢氧化物,后者阻碍了细菌呼吸的电子传递链[16];二是从CaO表面产生超氧化物和其他活性氧基团(reactive oxygen specie,ROS),破坏细菌细胞膜导致细菌死亡[17]。
2.2.2 对圣女果表观形态的影响
如图5所示,SEM分析表明,与对照组相比,清水处理10 min后圣女果皮上附着的污染物等杂质减少,但伴随表面粗糙度轻微增加;随着清水处理时间的延长,污染物去除效率增加,但不能完全清除,同时表皮的皱缩程度变大,说明清水处理对圣女果有一定的清洗效果。使用1 g/100 mL泡腾片浸泡10 min,圣女果表面污染物基本被清除;随着处理时间的进一步延长,污染物的去除效果更为显著,但果皮皱缩程度会变大;随着泡腾片作用浓度的增加,果皮上的污染物等杂质清洗得更彻底,但果皮皱缩程度进一步加剧。综合上述结果可知,当选用1~2 g/100 mL的泡腾片浸泡处理10~20 min,可实现对圣女果较好的清洗效果,且表皮结构完整性保持较好,残留风险较低。

a-圣女果实物图;b-放大30倍的SEM图像;c-放大100倍的SEM图像
图5 圣女果表观形态图
Fig.5 Apparent morphology diagram of cherry tomatoes
2.2.3 对圣女果色泽的影响
果蔬色泽作为采后品质的重要指标,其变化与机械损伤、色素流失等密切相关。泡腾片清洗剂在崩解过程中释放的CO2微泡可产生物理冲刷作用,在清除圣女果表面污染物的同时可能破坏表皮细胞结构,导致色泽发生变化。表1为泡腾片清洗剂对圣女果色泽的影响。时间效应分析表明,当作用时间从0 min增加到10 min时,清水组和泡腾片组的ΔE分别为2.79和3.04,这很大程度上是由于浸泡处理清除了圣女果上附着的部分灰尘、微生物等污染物,从而提升整体明亮度,导致色差的增大。清水组在作用时间增加到20、30、40 min时,ΔE分别为2.11、1.96、1.74;1 g/100 mL泡腾片组依次为2.87、2.78、1.53。根据ADEKUNTE等[18]的分类,当ΔE>3时,色差可归类为非常显著;当ΔE为1.5~3时,色差显著;当ΔE<1.5时,视为没有显著性,因此研究证明经清水和泡腾片处理对圣女果色差有显著影响,但仍在可接受范围内。浓度梯度实验结果表明,较清水处理组相比,1、2、3、4 g/100 mL泡腾片处理样品的ΔE分别为2.45、2.82、2.33、2.78,这很可能是由于泡腾片浓度的增加使得溶液pH上升,加剧了对细胞内水分和可溶性固形物等营养物质的影响,从而影响最终色泽[19]。
表1 各处理对圣女果色泽的影响
Table 1 Influence of different treatment on the color of cherry tomatoes
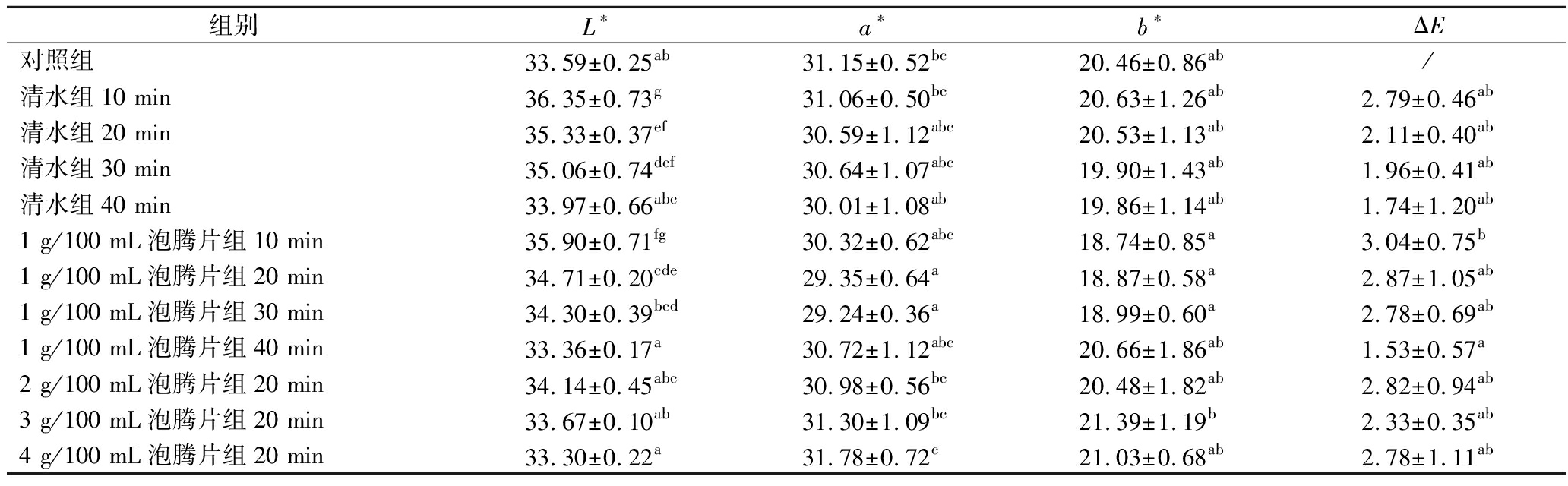
组别L∗a∗b∗ΔE对照组33.59±0.25ab31.15±0.52bc20.46±0.86ab/清水组10 min36.35±0.73g31.06±0.50bc20.63±1.26ab2.79±0.46ab清水组20 min35.33±0.37ef30.59±1.12abc20.53±1.13ab2.11±0.40ab清水组30 min35.06±0.74def30.64±1.07abc19.90±1.43ab1.96±0.41ab清水组40 min33.97±0.66abc30.01±1.08ab19.86±1.14ab1.74±1.20ab1 g/100 mL泡腾片组10 min35.90±0.71fg30.32±0.62abc18.74±0.85a3.04±0.75b1 g/100 mL泡腾片组20 min34.71±0.20cde29.35±0.64a18.87±0.58a2.87±1.05ab1 g/100 mL泡腾片组30 min34.30±0.39bcd29.24±0.36a18.99±0.60a2.78±0.69ab1 g/100 mL泡腾片组40 min33.36±0.17a30.72±1.12abc20.66±1.86ab1.53±0.57a2 g/100 mL泡腾片组20 min34.14±0.45abc30.98±0.56bc20.48±1.82ab2.82±0.94ab3 g/100 mL泡腾片组20 min33.67±0.10ab31.30±1.09bc21.39±1.19b2.33±0.35ab4 g/100 mL泡腾片组20 min33.30±0.22a31.78±0.72c21.03±0.68ab2.78±1.11ab
注:同列不同字母表示差异显著(P<0.05)。
2.2.4 对圣女果硬度的影响
果蔬硬度作为表征细胞壁结构完整性的关键参数,直接影响采后品质与商品价值,主要受细胞的黏着力、构成细胞壁物质的机械强度以及细胞的体积、形状和紧缩膨胀程度等的影响[20]。由图6可知,在处理10、20、30、40 min后,清水组硬度从28.14 N分别减小至27.22、25.63、24.30、23.18 N,这可能是由于水分渗入果实内部,改变细胞组织结构功能,发生软化所致。另外,其内营养成分,如可溶性固体等的含量变化也会影响圣女果的组织强度和结构密度[21]。1 g/100 mL泡腾片组硬度随时间延长分别减小至27.72、27.16、26.04、24.99 N,整体较清水组下降慢的原因可能是泡腾片中的Ca2+与果胶分子结合,延缓了硬度的下降。泡腾片使用量从0增至1 g/100 mL时,圣女果硬度从25.63 N增大至27.16 N,可能是因为当钙存在时,不同果胶分子中带负电荷的残基域会通过Ca2+离子键结合在一起,形成钙果胶凝胶,增强壁强度[22]。当浓度继续增大时,细胞硬度又略有下降,在2、3、4 g/100 mL时分别减小至25.87、25.20、24.60 N。这与邱雪[23]的研究结果相似,2 g/100 mL CaCl2处理组可以有效降低灵武长枣的软化速率,而4 g/100 mL CaCl2处理组的枣果硬度略低,这可能是由于过高的钙浓度处理导致了果实内部产生植物毒性,使果实内部结构瓦解所致。因此合理浓度的贝壳粉泡腾片处理,可以通过强化果胶酸钙网络结构,从而维持果胶的物理形态,延缓细胞壁中多糖的分解,增强细胞间的凝聚力,提高果实硬度。
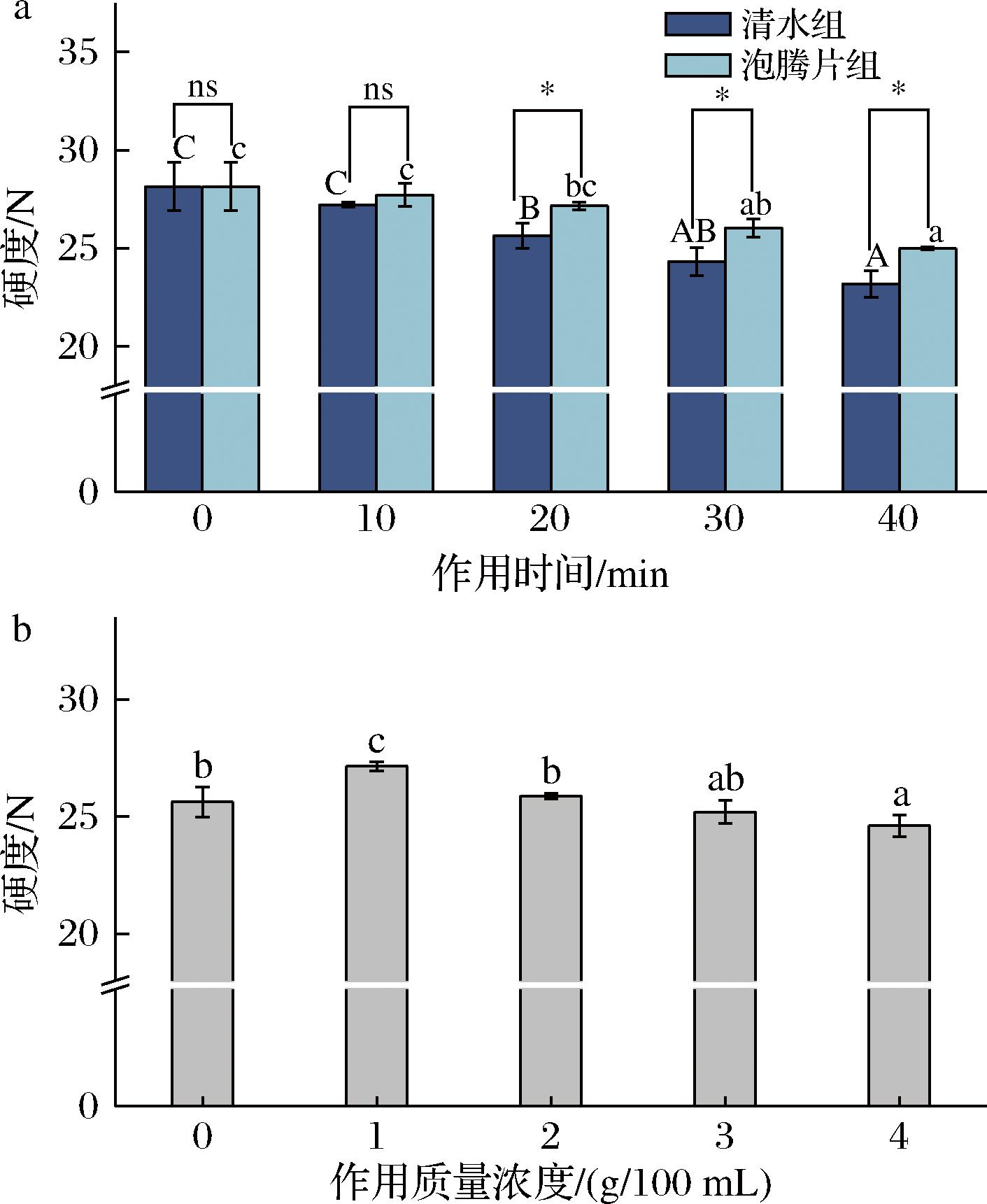
a-作用时间;b-作用质量浓度
图6 纳米贝壳粉泡腾片对圣女果硬度的影响
Fig.6 Effect of nano-shell powder effervescent tablets on the hardness of cherry tomatoes
2.2.5 对圣女果果胶酶活性的影响
果胶酶活性是评估采后处理对果蔬细胞壁代谢影响的关键生物标志物。如图7所示,初始果胶酶活性为1 275.29 mg/(h·g),当处理时间从0延长至40 min,清水组酶活性从1 473.30 mg/(h·g)递增至2 001.17 mg/(h·g),类似的现象也在蒸馏水浸泡处理巴梨果实的研究中报道[24]。经泡腾片处理后,果胶酶活性也有一定程度增加,但增加幅度较清水处理显著降低。例如,2 g/100 mL泡腾片处理40 min后,其果胶酶活性较清水组低16.2%(图7-a)。浓度梯度实验表明(图7-b),泡腾片浓度与酶活性呈负相关。4 g/100 mL时活性降低10.8%。推测可能是Ca2+竞争性占据酶活性中心,抑制其与果胶底物结合[22]。另外,果胶酶最适pH为4.0左右[25],碱性的环境也能抑制酶活性。本研究表明,泡腾片浸泡处理能够显著抑制圣女果细胞壁降解酶的活性,这可能也是减少果实硬度下降的关键原因。采用1~2 g/100 mL处理10~20 min的方案,可有效控制酶活性,阻止植物细胞壁主要成分的过度降解,从而维持果实的硬度。
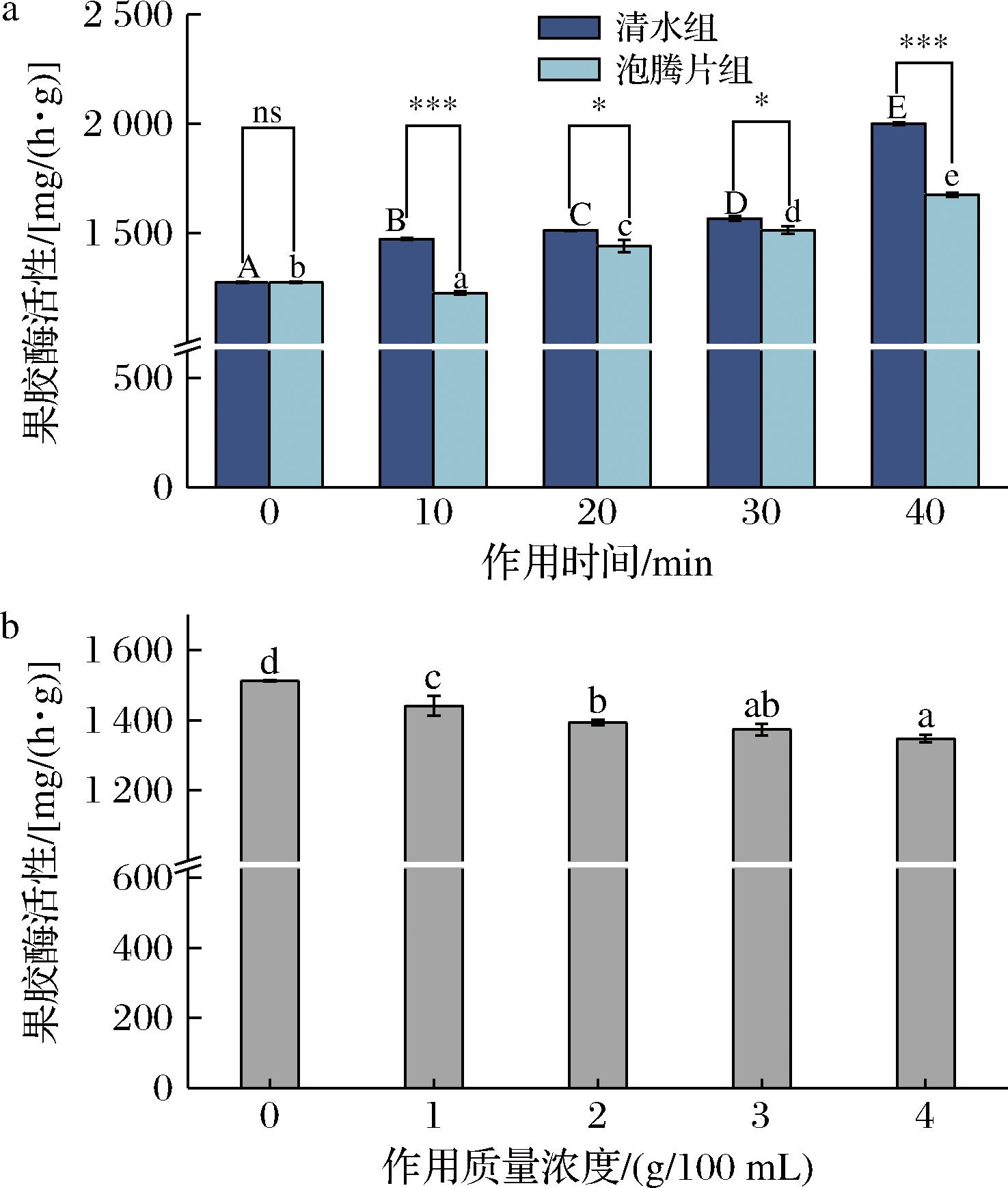
a-作用时间;b-作用质量浓度
图7 纳米贝壳粉泡腾片对果胶酶活性的影响
Fig.7 Effect of nano-shell powder effervescent tablets on the activity of pectinase
2.2.6 对圣女果维生素C含量的影响
维生素C是评价果蔬营养品质的重要指标。如图8所示,在初始处理阶段,泡腾片组的维生素C保留率较高。2 g/100 mL泡腾片处理10 min后,维生素C含量为18.6 mg/100 g,保留率为92.7%;处理20 min后,维生素C含量为18.0 mg/100 g,保留率为89.8%。然而,当处理时间超过30 min时,维生素C开始加速降解,30、40 min时的含量分别降至17.0 mg/100 g 和15.5 mg/100 g,对应的保留率为84.6%和77.1%。清水组显示出相似的趋势,但其整体维生素C在40 min时为82.8%,显著优于泡腾片处理组。这一现象与已有研究结论一致,同一处理方法中,随处理时间和pH的升高,果蔬维生素C含量显著下降。浓度梯度实验结果显示(图8-b),当清洗剂质量浓度≤2 g/100 mL时,维生素C的保留率超过88%;然而,当泡腾片浓度≥3 g/100 mL时,保留率显著下降:3 g/100 mL处理组的维生素C含量降至12.5 mg/100 g(保留率84.5%),而4 g/100 mL时进一步降至11.8 mg/100 g(保留率80.1%)。维生素C是一种己糖醛基酸,所以在酸性条件下稳定,而遇碱中和分解。当泡腾片浓度增加时,其溶液的碱性环境增强,从而加速了维生素C的流失。在10~20 min的常规清洗时间内,1~2 g/100 mL浓度泡腾片处理的维生素C保留率与清水对照组的差异小于5个百分点(P>0.05),显示其在实际应用中具有可行性。
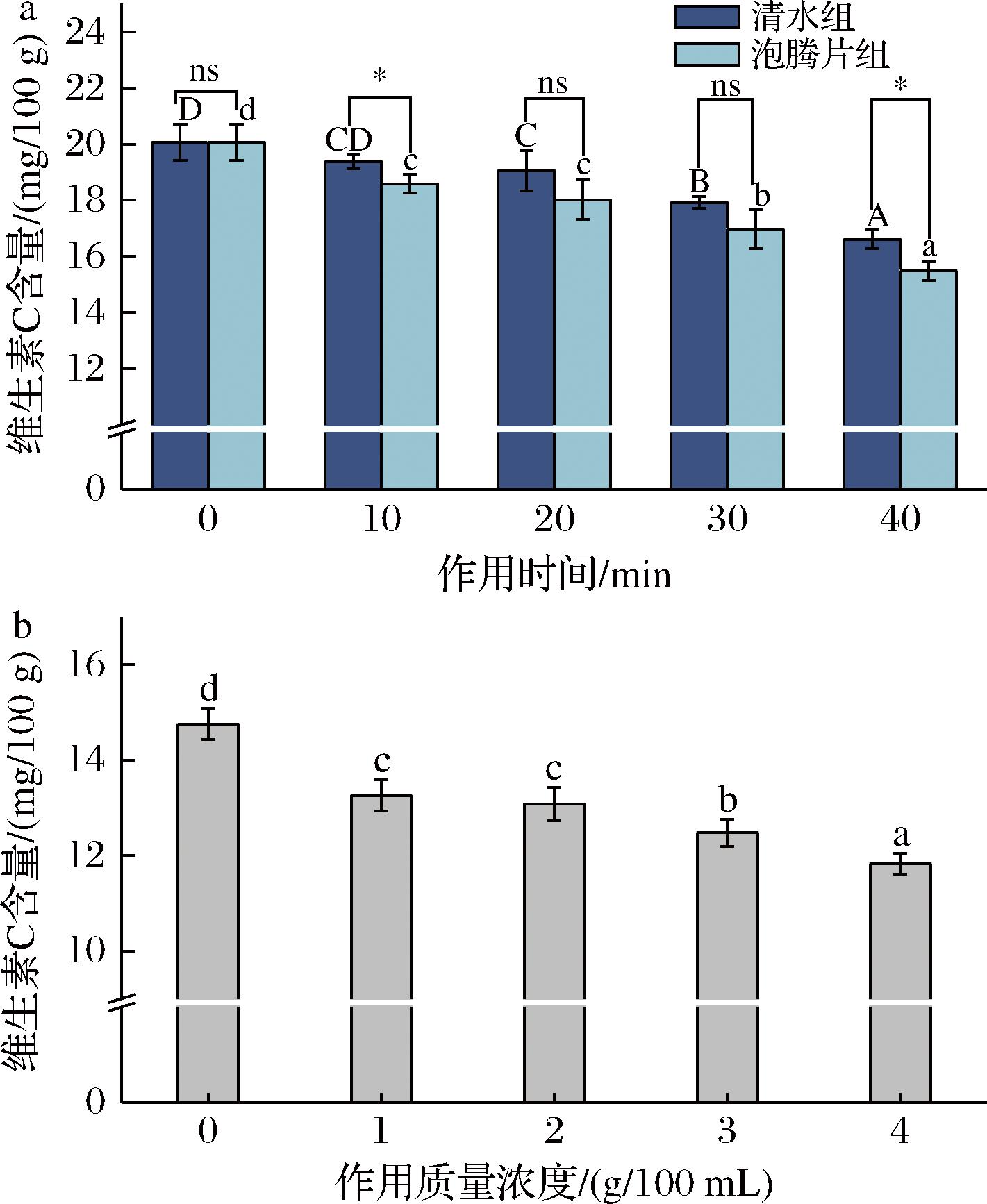
a-作用时间;b-作用质量浓度
图8 纳米贝壳粉泡腾片对维生素C含量的影响
Fig.8 Effect of nano-shell powder effervescent tablet on vitamin C content
2.2.7 对圣女果可滴定酸、可溶性固形物、总酚和总黄酮含量的影响
果蔬可滴定酸含量是表征果蔬有机酸代谢平衡的关键指标,直接影响其食用品质。可溶性固形物(total soluble solid,TSS)是表征果蔬细胞完整性与营养物质保留的关键指标。本研究所用圣女果初始可滴定酸含量为0.601%,TSS含量为8.67%。时间效应分析表明(图9-a~图9-b),在处理时间≤20 min时,清水组和2 g/100 mL泡腾片组的可滴定酸、TSS含量变化不明显。但处理时间≥30 min时,可滴定酸和TSS流失加剧。浓度实验表明(图9-c),泡腾片使用浓度与可滴定酸、TSS含量呈负相关。4 g/100 mL泡腾片分别会导致0.89%的可滴定酸和1.20% TSS损失。推测清水组含量下降与细胞吸水导致组织结构发生变化有关,泡腾片组更多与化学中和效应相关,碱性环境也会加剧营养物质的部分流失。果蔬中的总酚、总黄酮具有较强的抗氧化性[26],其含量变化可反映清洗处理对植物次级代谢产物的影响。圣女果初始总酚含量为476.56 mg/100 g,清水处理导致其含量持续下降,而泡腾片组下降趋势较缓;质量浓度超过3 g/100 mL时损失增大。初始总黄酮含量5.99 mg/100 g,清水组呈现波动下降趋势,泡腾片组整体递减,但均无显著性差异(图9-d~图9-e)。浓度梯度实验表明(图9-f),泡腾片质量浓度≤2 g/100 mL时总酚和总黄酮含量无显著差异,≥3%时总酚和总黄酮流失加剧,4 g/100 mL的泡腾片会导致36.33 mg/100 g和0.94 mg/100 g的总酚和总黄酮损失。在1 g/100 mL下处理20 min,可滴定酸、TSS、总酚和总黄酮的保留率分别超过99.0%、94.5%、99.3%和96.8%。
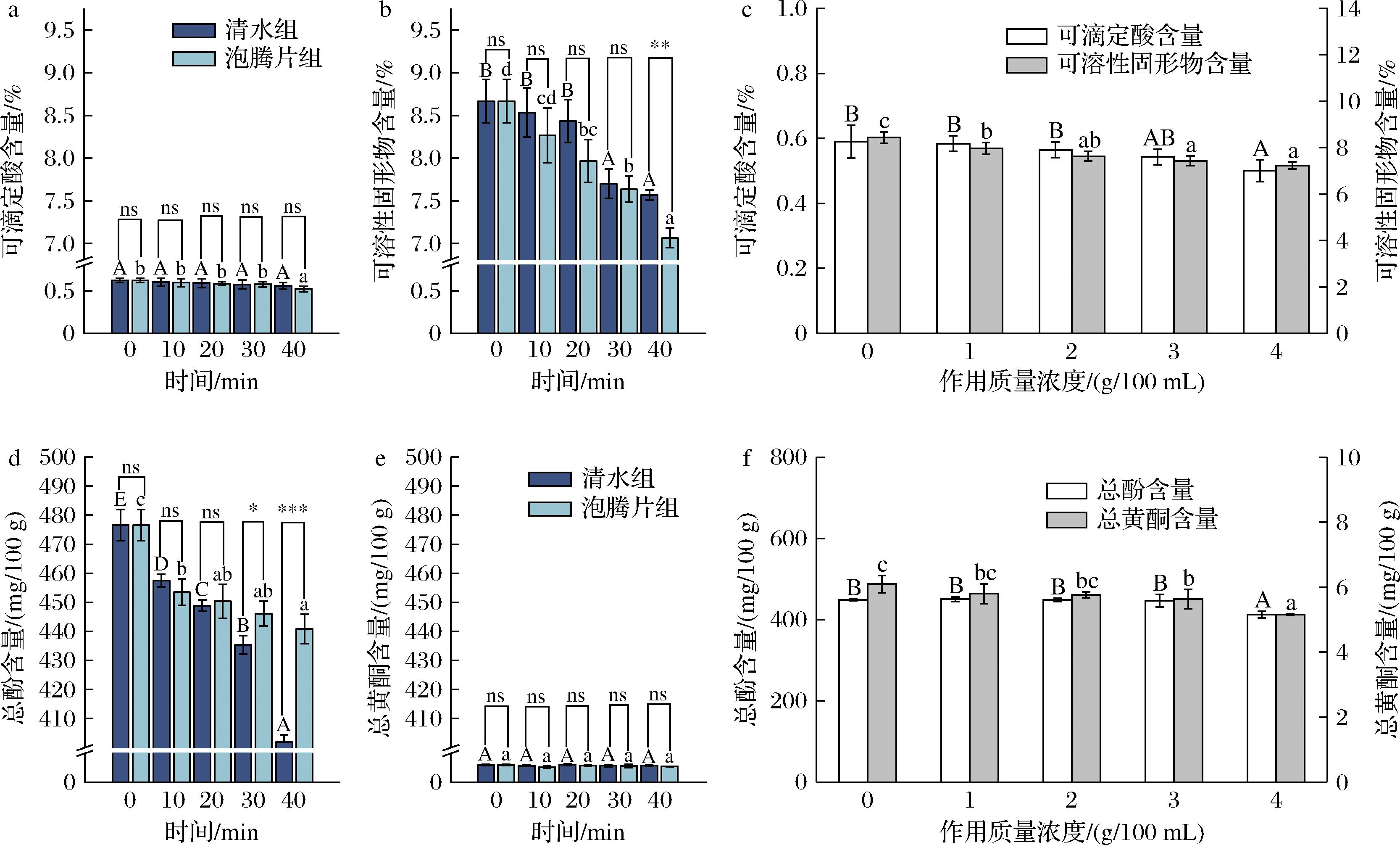
a-作用时间对可滴定酸的影响;b-作用时间对可溶性固形物的影响;c-作用浓度对可滴定酸和可溶性固形物的影响;d-作用时间对总酚的影响;e-作用时间对总黄酮的影响;f-作用浓度对总酚和总黄酮的影响
图9 贝壳粉泡腾片对可滴定酸、可溶性固形物、总酚和总黄酮的影响
Fig.9 Effect of nano-shell powder effervescent tablets on titrable acids, soluble solids, total phenols and total flavonoids
3 结论
本研究针对市场上煅烧贝壳粉清洗剂存在的接触时间短、清洗效果差等问题,成功研发了一种以贻贝壳为原料的纳米贝壳粉泡腾片清洗剂,为贝壳的高值化利用提供了新思路。通过优化泡腾片的制备工艺,确定最佳条件为:以850 ℃煅烧2 h的贝壳粉为原料,经微细化加工后,再按如下配方制备:贝壳粉质量分数35%、崩解剂质量分数60%(NaHCO3与柠檬酸比例为0.4∶1)、黏合剂质量分数3%、润滑剂质量分数2%。制备的泡腾片表面洁白光滑,发泡迅速,有效延长了清洗剂与待洗物的接触时间。对圣女果的清洗实验表明,在处理时间≤20 min,使用质量浓度≤2 g/100 mL下,该清洗剂能在有效控制微生物的同时,保持圣女果的颜色、硬度和多种营养物质含量,展现出优异的实际应用性能和环保性,具备良好的市场应用前景。
[1] 王洪波. 废弃贝壳资源化利用现状及研究进展[J].水产养殖, 2021, 42(5):15-19.
WANG H B.The current situation and research progress of resource utilization of waste mollusk shell[J].Journal of Aquaculture, 2021, 42(5):15-19.
[2] CHENG M Q, LIU M, CHANG L R, et al.Overview of structure, function and integrated utilization of marine shell[J].Science of the Total Environment, 2023, 870:161950.
[3] 王权. 基于紫贻贝壳的果蔬清洗剂制备及其吸附性能研究[D].舟山:浙江海洋大学, 2021.
WANG Q.Preparation and adsorption properties of fruit and vegetable detergent based on Mytilus edulis shell powder[D].Zhoushan:Zhejiang Ocean University, 2021.
[4] 王雅颖. 海洋微纳米果蔬清洗剂的制备及性能研究[D].舟山:浙江海洋学院, 2015.
WANG Y Y.Study on preparation and properties of micro-nano shell powder purifier for fruits and vegetables[D].Zhoushan:Zhejiang Ocean University, 2015.
[5] 杨丽梅, 刘烨.果蔬洗涤盐泡腾片的开发[J].中国井矿盐, 2017, 48(4):4-5;11.
YANG L M, LIU Y.The exploitation of garden stuff washing salt effervescent tablets[J].China Well and Rock Salt, 2017, 48(4):4-5;11.
[6] 孙燕达. 复合亚氯酸钠果蔬清洗泡腾片的制备与质量评价[D].石家庄:河北科技大学, 2019.
SUN Y D.Preparation and quality evaluation of composite sodium chlorite cleaning effervescent tablets for fruits and vegetables[D].Shijiazhuang:Hebei University of Science and Technology, 2019.
[7] SUN W H.Development of effervescent tablets containing elderberry vine tea compound and evaluation of their antioxidant activity[J].Journal of Food Processing and Preservation, 2023, 2023:4312278.
[8] 唐婧红, 范可帷, 张素, 等.黑曲霉泡腾片制备工艺优化[J].中国酿造, 2018, 37(10):186-189.
TANG J H, FAN K W, ZHANG S, et al.Preparation process optimization of Aspergillus niger effervescent tablets[J].China Brewing, 2018, 37(10):186-189.
[9] 国家药典委员会. 中华人民共和国药典[M].北京:中国医药科技出版社, 2020.
National Pharmacopoeia Commission.Pharmacopoeia of the People’s Republic of China[M].Beijing:China Medical Science and Technology Press, 2020.
[10] 曹建康, 姜微波, 赵玉梅.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社, 2007, 24-41.
CAO J K, JIANG W B, ZHAO Y M.Guidance of Postharvest Physiological and Biochemical Experiments of Fruits and Vegetables[M].Beijing:China Light Industry Press, 2007, 24-41.
[11] 刘心建, 李梦雪, 王泽云, 等.浅谈消毒泡腾片[J].日用化学品科学, 2020, 43(10):44-47.
LIU X J, LI M X, WANG Z Y, et al. Brief discussion on the disinfection effervescent tablets[J].Detergent &Cosmetics, 2020, 43(10):44-47.
[12] 王艳, 万庆家, 廖海慧, 等.芦荟泡腾片的制备[J].食品工业, 2022, 43(1):9-12.
WANG Y, WAN Q J, LIAO H H, et al.Preparation of Aloe vera effervescent tablets[J].The Food Industry, 2022, 43(1):9-12.
[13] 王媛媛, 郝璟嵘, 闫思颖, 等.沙棘冻干粉泡腾片的制备工艺优化及其品质分析[J].食品工业科技, 2023, 44(10):235-241.
WANG Y Y, HAO J R, YAN S Y, et al.Optimization of preparation process and quality analysis of seabuckthorn lyophilized powder effervescent tablets[J].Science and Technology of Food Industry, 2023, 44(10):235-241.
[14] 邸玲. 贝壳粉涂料的研究[D].长春:吉林建筑大学, 2018.
DI L.Research for shell powder coating[D].Changchun:Jilin Jianzhu University, 2018.
[15] XIAO J, HU R, CHEN G C.Micro-nano-engineered nitrogenous bone biochar developed with a ball-milling technique for high-efficiency removal of aquatic Cd(Ⅱ), Cu(Ⅱ) and Pb(Ⅱ)[J].Journal of Hazardous Materials, 2020, 387:121980.
[16] TAN J, LIU Z X, WANG D H, et al.A facile and universal strategy to endow implant materials with antibacterial ability via alkalinity disturbing bacterial respiration[J].Biomaterials Science, 2020, 8(7):1815-1829.
[17] GEDDA G, PANDEY S, LIN Y C, et al.Antibacterial effect of calcium oxide nano-plates fabricated from shrimp shells[J].Green Chemistry, 2015, 17(6):3276-3280.
[18] ADEKUNTE A O, TIWARI B K, CULLEN P J, et al.Effect of sonication on colour, ascorbic acid and yeast inactivation in tomato juice[J].Food Chemistry, 2010, 122(3):500-507.
[19] WANG J, WANG J, YE J H, et al.Influence of high-intensity ultrasound on bioactive compounds of strawberry juice:Profiles of ascorbic acid, phenolics, antioxidant activity and microstructure[J].Food Control, 2019, 96:128-136.
[20] 潘永贵, 谢江辉.现代果蔬采后生理[M].北京:化学工业出版社, 2009.
PAN Y G, XIE J H.Postharvest Physiology of Modern Fruits and Vegetables[M].Beijing:Chemical Industry Press, 2009.
[21] WANG J, MUJUMDAR A S, WANG H, et al.Effect of drying method and cultivar on sensory attributes, textural profiles, and volatile characteristics of grape raisins[J].Drying Technology, 2021, 39(4):495-506.
[22] TOIVONEN P M A, BRUMMELL D A.Biochemical bases of appearance and texture changes in fresh-cut fruit and vegetables[J].Postharvest Biology and Technology, 2008, 48(1):1-14.
[23] 邱雪. 钙处理对灵武长枣质地品质与细胞壁多糖纳米结构的影响研究[D].银川:宁夏大学, 2020.
QIU X.Effects of calcium treatment on the quality and cell wall polysaccharides nanostructure of Lingwu Long-Jujube[D].Yinchuan:Ningxia University, 2020.
[24] 经亚丽, 王梦真, 庄英钰, 等.薄荷提取液对巴梨采后品质的影响[J].核农学报, 2025, 39(5):983-990.
JING Y L, WANG M Z, ZHUANG Y Y, et al.Effect of peppermint extract on postharvest quality of bartlett[J].Journal of Nuclear Agricultural Sciences, 2025, 39(5):983-990.
[25] 苏玮. 利用初榨草莓汁探究pH对果胶酶活性的影响[J].中学生物学, 2016, 32(5):47-48.
SU W.The effect of pH on pectinase activity was explored using freshly squeezed strawberry juice[J].Middle School Biology, 2016, 32(5):47-48.
[26] 兰文忠, 冀利, 贺晓芳, 等.冬枣汁与金丝小枣汁总酚、总黄酮含量及抗氧化性能的比较研究[J].食品与发酵科技, 2021, 57(1):90-94.
LAN W Z, JI L, HE X F, et al.Comparative study on the contents of total phenols, flavonoids and antioxidant activity of winter jujube juice and golden-silk jujube juice[J].Food and Fermentation Sciences &Technology, 2021, 57(1):90-94.