肉类食品的掺假问题是全球范围内十分关注的食品安全热点问题之一,2013年2月欧洲曝出“马肉丑闻”事件[1-2],掺假牛肉席卷英国、法国、德国等16个国家,肉类掺假现象花样百出、层出不穷,人造牛肉、猪肉冒充牛肉、牛肉卷中掺杂鸭肉,利用鸡肉和鸭皮冒充猪肉馅等乱象,无一不暴露了肉制品市场的混乱和监管治理的窘境。随着肉类价格差异不断扩大,不法商家为了追求利益,借机用价格低廉的肉或植物蛋白进行掺假,这些无良商家的商业欺诈行为影响到民族饮食禁忌等问题,这些与价格、原料和宗教等有关的食品掺假事件,不仅侵害了消费者的权益和食品公平交易,还严重威胁到了人们的身体健康和宗教信仰[3-5],未标识的食品成分往往会成为潜在的安全隐患,如过敏原及有毒成分会影响消费者的健康,错误的标签也可能会违背特定群体的饮食习惯。
为了加强对市售肉制品的监管工作、维护消费者的合法权益及市场中公平有序的交易环境,建立精准、快速、高效的鉴别技术尤为重要,应用现代分析仪器与分子生物学方法对食品中肉类成分的鉴别技术不断发展,鉴别精度与检测灵敏度均极大提高,已逐步形成了分别以核酸检测和以蛋白质检测为基础的方法体系。以核酸检测为基础的食品中肉类种属的定性检测主要是以动物种属间遗传信息的差异作为物种鉴别的检测靶点,具有特异性高、方法便捷、不受组织类别限制等诸多优点,已逐渐成为食品中肉类成分鉴别的权威检测方法。但是食品中DNA成分复杂,加之PCR技术的灵敏度高,使得应用PCR扩增方法来鉴定物种具有因非特异性扩增而产生假阳性结果的缺点,因此这些方法用于深加工的肉类制品掺伪鉴别的检验过程中略有力不从心之态。以蛋白质检测为基础的肉类鉴别方法具有独特的优势,蛋白质的一级结构在高度加工条件下相对稳定、蛋白质具有更高的组织特异性,因而蛋白组学法更适宜用于肉类掺假检测。基于高分辨质谱的“鸟枪”蛋白组学法使用自下而上的方法定量测定复杂混合物中的蛋白质,其独特优势在于以最小限度分离蛋白质,可对多种蛋白质进行鉴定和定量,已成为鉴别肉类掺假及蛋白质种属来源的主要技术之一[6-9]。
本文基于超高效液相色谱串联四级杆飞行时间高分辨质谱技术定量测定牛肉丸样品中的大豆蛋白源特征肽,根据特征肽的测定结果鉴别大豆蛋白,以期建立一种高效、灵敏的定量检测牛肉丸制品中大豆蛋白的方法,为牛肉丸等制品的掺假鉴别提供技术支撑。
1 材料与方法
1.1 材料与试剂
牛肉、牛肉丸,购于当地市场;大豆蛋白粉,市售;猪胰蛋白酶(trypsin)(酶活力≥10 000 U/mg蛋白)、正己烷(色谱级),西格玛有限公司;甲酸、乙腈、甲醇等,均为质谱级,默克股份有限公司;二硫苏糖醇、碘代乙酰胺、NH4HCO3、尿素、CaCl2·2H2O、三羟甲基氨基甲烷(Tris)、硫脲等,生工生物工程(上海)股份有限公司;肽标准品(VFDGELQEGR、NLQGENEGEDK、NPFLFGSNR、LITLAIPVNKPGR、NILEASYDTK,纯度均>95%),南京杰肽生物科技有限公司;固相萃取柱HLB(100 mg/3 mL)、Prime HLB(100 mg/3 mL)、WCX(100 mg/3 mL)、WAX(100 mg/3 mL)、C18(100 mg/3 mL),沃特世科技(上海)有限公司;超纯水(电阻率≥18.2 MΩ·cm),实验室自制。
1.2 仪器与设备
H-Class Plus超高效液相色谱仪、Xevo G2 QTOF高分辨质谱仪,沃特世科技有限公司;CV200真空离心浓缩仪,北京吉艾姆科技有限公司;Milli Q超纯水系统,密理博有限公司;ZX4涡旋振荡器,意大利VELP公司;3K15冷冻离心机,西格玛有限公司;JY3002电子天平,梅特勒-托利多仪器有限公司。
1.3 实验方法
1.3.1 原料处理及样品制备
牛肉:将市场购买的新鲜牛肉(牛臀肉)剔除筋膜,搅碎后置于蓝盖瓶中,加热至中心温度72 ℃后,再煮20 min,冷却后真空冷冻干燥,研磨成粉,于-20 ℃冷冻保存备用。
大豆蛋白粉:取大豆蛋白粉按料液比1∶1(g∶mL)加入超纯水混匀,置于蓝盖瓶中,加热至中心温度72 ℃后,再煮20 min,冷却后真空冷冻干燥,研磨成粉,于-20 ℃冷冻保存备用。
牛肉丸样品:将购买的牛肉丸,切片搅碎,真空冷冻干燥,研磨成粉,于-20 ℃冷冻保存备用。
含大豆蛋白的牛肉样品:准确称取40 g大豆蛋白粉及60 g绞碎的牛肉,加入20 g水,混匀,置于蓝盖瓶中,加热至中心温度72 ℃后,再煮20 min,冷却后真空冷冻干燥,研磨成粉,于-20 ℃冷冻保存备用。
1.3.2 蛋白提取
准确称取0.2 g样品置于10 mL离心管中,加入4 mL提取液(6 mol/L尿素、2 mol/L硫脲、50 mmol/L Tris-HCl,pH 8.0),涡旋混合5 min,超声波处理3 min,在4 ℃于12 000 r/min下离心4 min,收集上清液,转移至15 mL离心管并用水定容至10 mL,涡旋1 min,所得溶液即为蛋白提取液。
1.3.3 蛋白酶解
取2 mL蛋白提取液于10 mL离心管中,加入1.5 mL NH4HCO3溶液(0.5 mol/L),涡旋30 s,加入100 μL二硫苏糖醇溶液(0.5 mol/L),混匀,75 ℃下水浴处理30 min后使溶液冷却至室温。添加碘代乙酰胺溶液(0.15 mol/L)使蛋白质烷基化,使终浓度为15 mmol/L,置于暗处反应30 min。迅速添加500 μL牛胰蛋白酶溶液(0.5 mg/mL)和100 μL CaCl2·2H2O溶液(0.1 mol/L)。立刻将溶液涡旋1 min,37 ℃下水浴酶解,酶解反应结束后向酶解液中加入200 μL甲酸终止反应,混匀后于室温中静置15 min,过0.22 μm滤膜,加水定容至10 mL。
1.3.4 脱盐
固相萃取柱用3 mL甲醇活化后,用3 mL甲酸水溶液(1%,体积分数)平衡。将1 mL酶解液定量转移到固相萃取柱中,用2 mL甲酸水溶液(1%,体积分数)冲洗固相萃取柱。分别用1 mL 90%乙腈水溶液(含0.1%甲酸,体积分数)洗脱2次,真空离心浓缩至近干。用0.50 mL 3%乙腈水溶液(含0.1%甲酸,体积分数),涡旋30 s,过0.22 μm滤膜,上机检测。
1.3.5 超高效液相色谱-高分辨质谱分析条件
采用Acquity BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),以0.1%甲酸水溶液(A相,体积分数)和0.1%甲酸乙腈溶液(B相,体积分数)梯度洗脱,洗脱条件:0~1 min 95% A相、3~8 min 90%~80% A、8~18 min 80%~70% A、18~20 min 70%~10% A、20~23 min 10% A、23~23.1 min 10%~95% A、23.1~25 min 95% A;流速0.2 mL/min,柱温40 ℃,进样量5 μL;质谱条件:电喷雾离子源、正离子模式、准多重反应监测(pseudo-multiple reaction monitoring,p-MRM)、毛细管电压3.0 kV、离子源温度130 ℃、脱溶剂气温度250 ℃、脱溶剂气流量800 L/h、锥孔气流量60 L/h、扫描时间0.2 s、质量扫描范围200~1 200。目标特征肽在p-MRM采集模式中进行目标增益分析,使用氩气作为碰撞气,设置碰撞能(collision energy,CE)为6.0~50 eV,并设置锥孔电压(cone voltage,CV)为20~200 eV,对各个特征肽做高能扫描优化。质谱数据在采集过程中使用外部锁定液进行对质荷比的实时锁定,外部锁定液由200 pg/μL的亮氨脑啡肽酸溶液组成、以10 μL/min的流速注入,在正离子模式下产生实时参考离子[M+H]+(m/z 556.2771),以确保准确的质谱分析[10]。
1.3.6 酶解时间的优化
选用含40%(质量分数)大豆蛋白的牛肉样品为研究对象,将按照1.3.2节提取后的肉蛋白提取液经1.3.3节酶解前的步骤处理后,于37 ℃下设定水浴酶解时间分别为0.3、0.5、1、2、4、6、10、12 h,经脱盐纯化,由质谱信号中得出的特征肽含量分析其酶解效率。
1.3.7 固相萃取柱的优化
将牛肉与大豆蛋白混合物提取的蛋白样品作为研究对象,按1.3.2节和1.3.3节处理制备酶解物,各固相萃取柱经活化平衡后,各取1 mL酶解液定量分别转移至HLB柱、Prime HLB柱、MAX柱、WAX柱、MCX柱、C18柱,洗脱后上机测定,通过对比特征肽的质谱信号强度,分析各固相萃取柱的净化效果。
1.3.8 加标回收率
为了客观评估该方法的准确性,以20、50、100 μg/L 3个浓度水平的大豆肽标准品溶液50 μL混合牛肉丸蛋白酶解液(按1.3.4节制备),过C18固相柱后上机测定,通过测定目标肽段的含量,按照公式(1)计算加标回收率:
回收率![]()
(1)
式中,Ci和C0,牛肉丸加标样液和非加标样液中特征肽的质量浓度,μg/L;Vi和V0,加标样液和非加标样液的体积,mL;m,特征肽的加标量,μg。
1.3.9 方法学验证
从线性范围、检出限(limit of determination,LOD)、定量限(limit of quantitation,LOQ)和基质效应(matrix effect,ME)等方面对该方法进行验证。分别按照信噪比S/N≥3和S/N≥10为依据计算LOD和LOQ。通过在相同浓度水平下进行日内和日间研究来评估精密度,并以相对标准偏差(relative standard deviation,RSD)表示。取一定量的特征肽标准溶液(20~800 μg/L)按质量比加入到按1.3.2节~1.3.3节处理的样品酶解中,配制成一定浓度梯度的混合工作液,过膜后测定,建立标准曲线,得到基质匹配的线性回归方程,将基质匹配的标准曲线与相同浓度水平下的标准曲线进行比较,按照公式(2)计算ME:
(2)
式中:KS,溶剂标准曲线斜率;KM,基质匹配标准曲线斜率。
1.4 数据处理
使用MassLynx V4.2软件(沃特世有限公司)进行仪器控制、数据采集和数据分析,各特征肽的母离子及碎片离子理论质核比通过Skyline软件(MacCoss实验室,美国华盛顿大学)获得。实验结果以至少重复3个平行样的“平均值±标准偏差”表示,用SPSS 19.0进行一维方差分析,差异显著性采用邓肯(Duncan)检验,检验水平P<0.05。
2 结果与分析
2.1 特征肽的筛选
基于“自下而上”的蛋白组学法鉴定蛋白质种属来源的关键是特征肽的选择,其挑选标准为:长度6~20个氨基酸,不含易氧化或修饰的残基(如M、C),具有良好的色谱保留特征;质谱信号响应强,低浓度下的信噪比强,无漏切位点,尽量减少加工引起的修饰,以确保在复杂基质(如加工肉制品)中仍能实现可靠溯源[10]。常规的方法是通过纳升级液相色谱分离蛋白酶解产物,使用高分辨质谱测定,根据母离子和碎片离子鉴别肽段。将鉴定到的肽段通过UniProt数据库(https://www.uniprot.org/)的基本局部比对搜索工具(basic local alignment search tool,BLAST)算法对比验证特异性。该方法灵敏度高、分离效率好、通量高,但是存在耗时长、筛选效率有限且严重依赖昂贵的纳升级液相色谱和高分辨质谱平台的问题。值得注意的是,在纳升级液相色谱串联高分辨质谱法中可检出的部分特征肽段,在超高效液相色谱串联三重四极杆质谱中无法测定[11]。
采用“鸟枪法”靶向蛋白组学鉴别蛋白质的种属来源中,除考虑肽段的特异性外,还需考虑目标蛋白的丰度、可提取性及酶解效率,大豆分离蛋白中的主要成分为大豆球蛋白和伴大豆球蛋白[12],其中大豆球蛋白glycin1和大豆伴球蛋白β-conglycinin α subunit 2经胰蛋白酶酶解形成的肽段数分别为18条和30条。在UniProt数据库中利用BLAST算法进行候选特征肽的筛选,分别有6条和7条肽段可作为潜在特征肽[13]。利用Skyline软件求得其参数,如表1所示,多肽的疏水值与其出峰时间存在正相关关系,选择相对分子质量适中(1 000~1 400 Da)、疏水值差异较大的5条肽作为特征肽,根据多肽疏水性的差异来实现有效的分离,以便于后续利用质谱仪检测这些特征肽在不同样品中的可检出性。
表1 大豆蛋白及其潜在特征肽的信息
Table 1 Information on soy protein and corresponded potential marker peptides
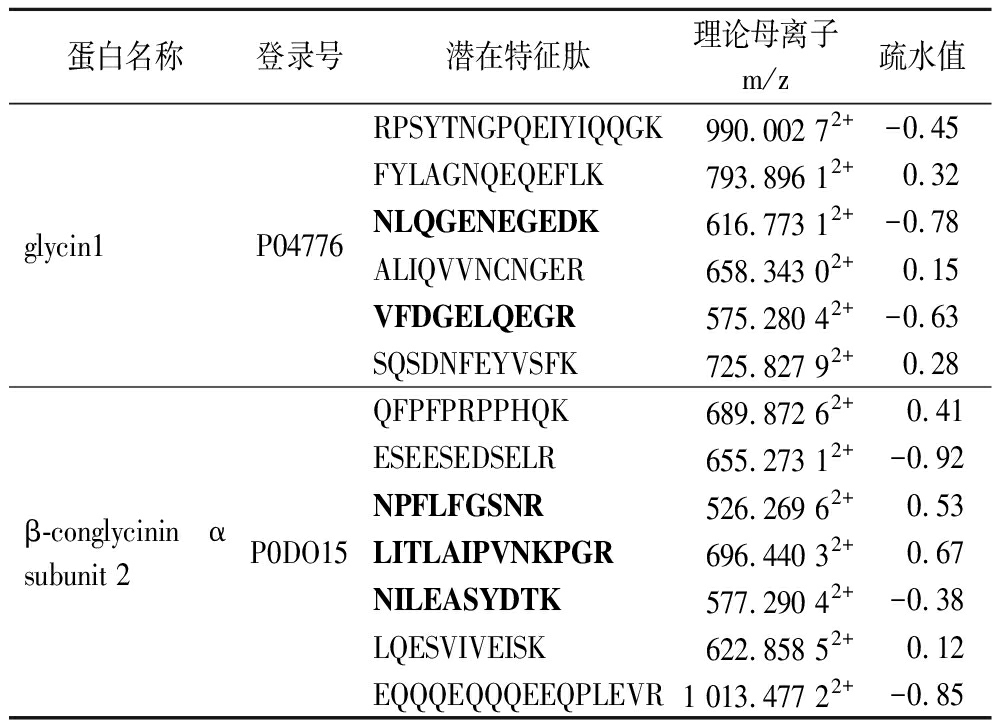
蛋白名称登录号潜在特征肽理论母离子m/z疏水值glycin1P04776RPSYTNGPQEIYIQQGK 990.002 72+-0.45FYLAGNQEQEFLK793.896 12+0.32NLQGENEGEDK616.773 12+-0.78ALIQVVNCNGER658.343 02+0.15VFDGELQEGR575.280 42+-0.63SQSDNFEYVSFK725.827 92+0.28β-conglycinin α subunit 2P0DO15QFPFPRPPHQK 689.872 62+ 0.41ESEESEDSELR655.273 12+-0.92NPFLFGSNR526.269 62+0.53LITLAIPVNKPGR696.440 32+0.67NILEASYDTK577.290 42+-0.38LQESVIVEISK622.858 52+0.12EQQQEQQQEEQPLEVR1 013.477 22+-0.85
注:加粗表示的肽段选为特征肽。
2.2 质谱参数的优化
CE值与CV值是质谱检测中的两个重要参数,CE值会影响碎片离子的产生及其丰度,不同化合物为产生特定碎片离子可能需通过设置不同CE值来实现;CV值的变化可用以控制母离子的碎裂程度,从而直接影响到样品测定的灵敏度。为确定出最优的CE值和CV值,用高分辨质谱在MS/MS采集模式下分析含有目标特征肽段的标准液,分别检测在不同的CV值(20~200 eV)和CE值(6~50 eV)下的各特征肽碎片离子的信号强度,其中CV值的大小对特征肽pep1信号强度的影响如图1所示。
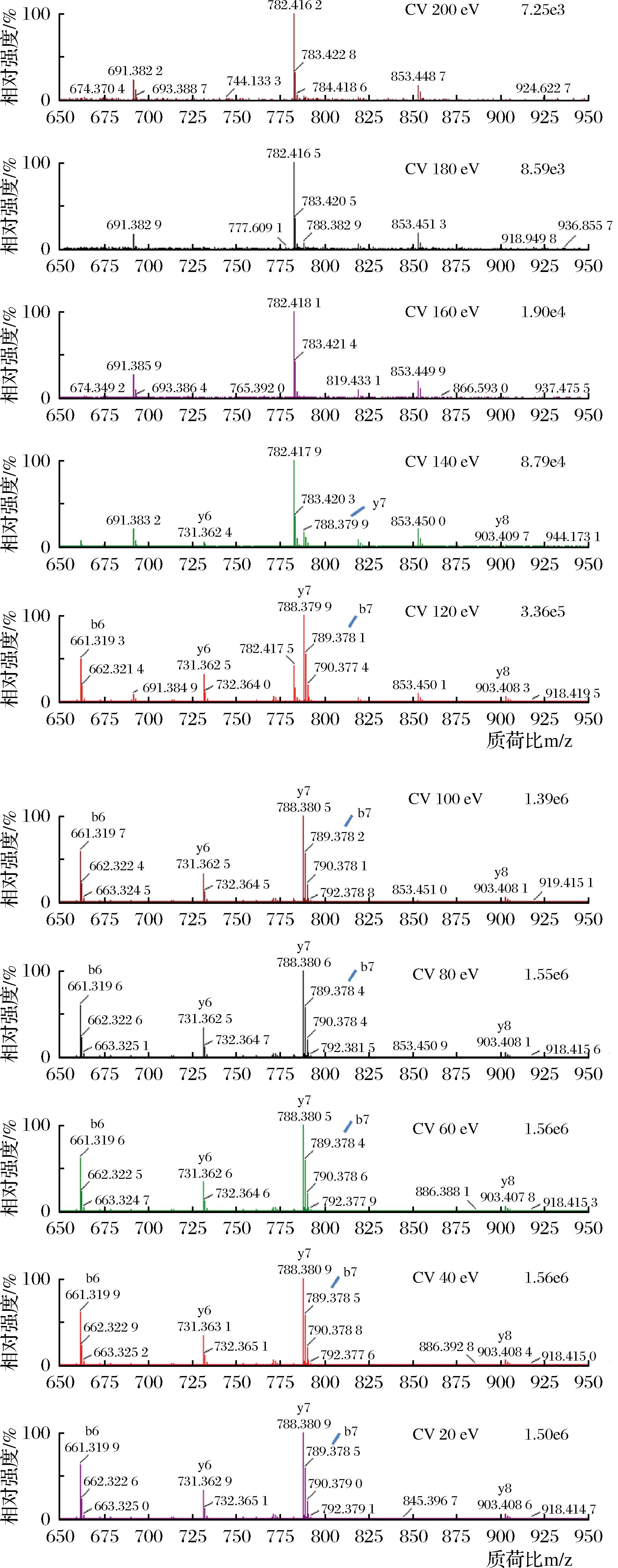
图1 不同CV值下特征肽pep1的二级质谱图
Fig.1 MS/MS spectrum of marker peptide pep1 obtained with different CV values
特征肽段pep1在MS/MS采集模式下测得有较高信号强度的碎片离子m/z分别为:903.408 6+(y8、偏差-8.97×10-6)、788.380 9+(y7、偏差-11.2×10-6)、731.362 9+(y6、偏差-7.25×10-6)、661.319 9+(b6、偏差1.06×10-6)、789.378 5+(b7、偏差1.01×10-6),而y7碎片离子的信号强度是相对最高的。在MS/MS采集模式下,随着CV值的增大,y7碎片离子的信号强度呈现先上升再下降的趋势,在CV值为40~80 eV时信号强度相对较高。来自液相的样品液经传输毛细管(或喷雾针)雾化后,在高压电场作用下发生去溶剂化和电离,形成气相离子。这些带电粒子在样品锥孔处受到锥孔电压的加速作用,从而提升离子传输效率并增强母离子信号强度。然而,过高的锥孔电压可能引发显著的源内裂解,这不仅会干扰母离子的准确选择,还会导致检测灵敏度下降[14-15]。源内裂解主要发生在传输毛细管出口与气相分离器之间的过渡区域,该区域处于质谱仪高真空系统的前级。在此区间,由于系统压力已显著降低,离子的平均自由程足够长,使其在电场加速下获得较高动能,进而与残余溶剂分子或干燥气体发生碰撞诱导解离形成碎片离子。离子加速程度直接取决于传输毛细管与分离器之间所施加的电压梯度,该电压越高,源内裂解的强度就越大。
质谱的MS/MS采集模式是通过选择特定的母离子(前体离子)施加碰撞能进行碎裂,分析产生的所有碎片离子,而p-MRM采集模式是通过筛选特定的母离子施加碰撞能进行碎裂产生二级碎片离子,再筛选并采集特定的二级碎片离子,与三重四级杆的多重反应监测质谱采集模式类似,但p-MRM模式是基于高分辨质谱可获得精确的质量数。特征肽pep1在p-MRM采集模式下获得的二级质谱图中碎片离子的分布会有一定变化,如表2所示,而y7碎片离子的强度仍是最高的,易作为特征肽pep1的定量离子。采用p-MRM采集模式优化CE值,随着CE值的增加,y7定量离子的信号强度也是呈现先上升后下降的趋势,在20 eV处达到最大值,与其理论CE值接近,其他肽段优化后的参数值见表2。
表2 优化后的特征肽测定用质谱参数
Table 2 Optimized mass spectrometry parameters for determination of marker peptides
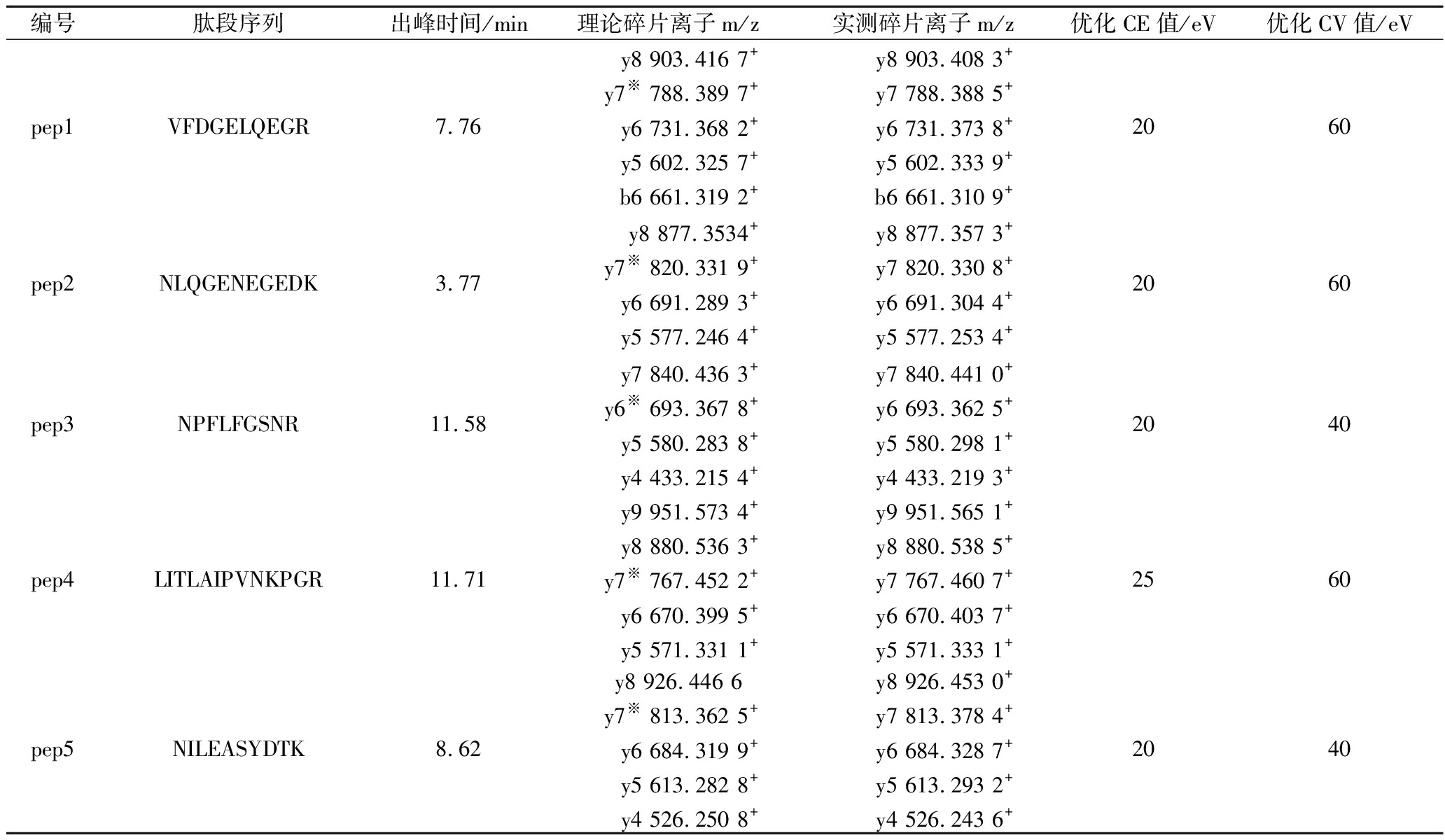
编号肽段序列出峰时间/min理论碎片离子m/z实测碎片离子m/z优化CE值/eV优化CV值/eVpep1VFDGELQEGR7.76y8 903.416 7+y7※ 788.389 7+y6 731.368 2+y5 602.325 7+b6 661.319 2+y8 903.408 3+y7 788.388 5+y6 731.373 8+y5 602.333 9+b6 661.310 9+2060pep2NLQGENEGEDK3.77y8 877.3534+y7※ 820.331 9+y6 691.289 3+y5 577.246 4+y8 877.357 3+y7 820.330 8+y6 691.304 4+y5 577.253 4+2060pep3NPFLFGSNR11.58y7 840.436 3+y6※ 693.367 8+y5 580.283 8+y4 433.215 4+y7 840.441 0+y6 693.362 5+y5 580.298 1+y4 433.219 3+2040pep4LITLAIPVNKPGR11.71y9 951.573 4+y8 880.536 3+y7※ 767.452 2+y6 670.399 5+y5 571.331 1+y9 951.565 1+y8 880.538 5+y7 767.460 7+y6 670.403 7+y5 571.333 1+2560pep5NILEASYDTK8.62y8 926.446 6 y7※ 813.362 5+y6 684.319 9+y5 613.282 8+y4 526.250 8+y8 926.453 0+y7 813.378 4+y6 684.328 7+y5 613.293 2+y4 526.243 6+2040
注:碎片离子右上角标注※表示定量离子。
2.3 固相萃取柱的选择
为了提高特征肽的离子化效率与可检出性,常用固相萃取法去除样品中的无机盐、基质干扰物等,净化和富集目标肽段。使用不同的固相萃取柱对特征肽进行分离纯化,质谱检测,将各目标肽段的峰面积平均并归一化,结果见表3。从表3可知,5条特征肽经不同固相萃取柱净化后测得的信号强度差异显著(P<0.05),采用C18固相萃取柱净化后,其峰值强度相对最高,经HLB、Prime HLB固相萃取柱净化后测出的峰值强度约为C18固相萃取柱净化后强度的一半,而经MCX、MAX等离子交换固相萃取柱净化后的信号强度较低。C18柱是在硅胶基质上直接键合十八烷基硅烷,通过具疏水性的键合硅胶与极性目标物相互作用,其可被有机溶剂洗脱,不易被水洗脱,故能有效去除盐分并富集目标物。HLB柱属于反相吸附剂的一种,其固定相含有具亲脂性的二乙烯基苯及亲水性的N-乙烯吡咯烷酮,使HLB柱既有优良的水可浸润性,又具有反相保留特性,其适用于酸性、中性、碱性化合物。Prime HLB柱是在HLB柱的基础上开发的反向固相萃取吸附剂,其优化了对磷脂等干扰物的净化效果,改善了HLB易堵塞的缺点。MAX为强阴离子交换柱、MCX为强阳离子交换柱,分别适用于酸性、碱性化合物的吸附与富集,在吸附特征肽方面效果较差。综合考虑,C18固相萃取柱较适合作为5条特征肽的富集除杂。
表3 不同固相萃取柱富集的特征肽信号相对强度
Table 3 Peak relative intensities of marker peptides enriched by different solid phase extraction columns
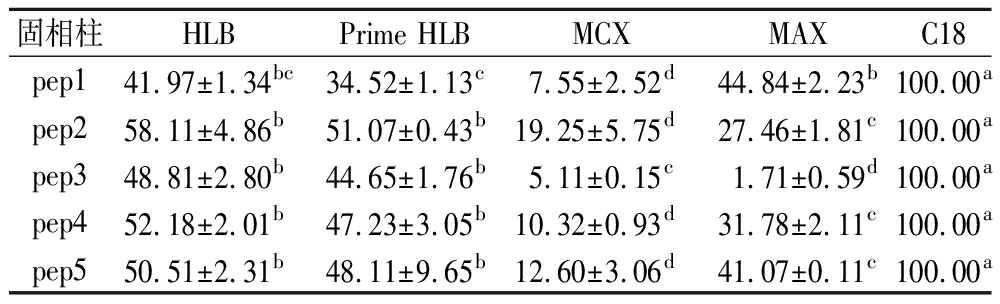
固相柱HLBPrime HLBMCXMAXC18pep141.97±1.34bc34.52±1.13c7.55±2.52d44.84±2.23b100.00apep258.11±4.86b51.07±0.43b19.25±5.75d27.46±1.81c100.00apep348.81±2.80b44.65±1.76b5.11±0.15c1.71±0.59d100.00apep452.18±2.01b47.23±3.05b10.32±0.93d31.78±2.11c100.00apep550.51±2.31b48.11±9.65b12.60±3.06d41.07±0.11c100.00a
注:同行不同小写字母表示差异显著(P<0.05)(下同)。
2.3 酶解时间的优化
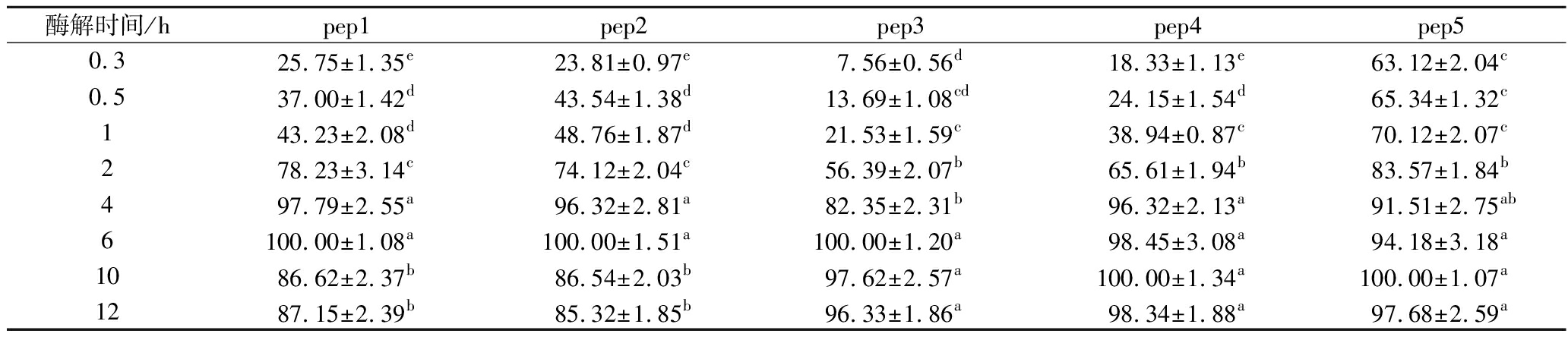
胰蛋白酶可特异性识别并切断赖氨酸或精氨酸C端肽键,将目标蛋白酶解为肽,赖氨酸和精氨酸侧链使得肽段带有正电荷,有利于质谱检测中肽段的离子化。为更好地对目标蛋白实现准确定量分析,需要用胰蛋白酶将目标蛋白完全酶解释放肽段,不同酶解时间对样品中大豆蛋白特征肽段形成的影响如表4所示,将目标肽峰面积平均并归一化。随着酶解时间的延长,特征肽段的信号强度随之增加,特征肽pep1、pep2、pep3的信号强度在6 h处达到最大值,而pep4和pep5的信号强度在10 h处达到最大值,但10 h后肽段pep1和pep2的信号强度已明显下降,这可能是由于部分肽段在较高浓度体系下发生聚集现象,而在离心分离过程中沉聚,或者是影响离子化而无法检出。过长的酶解时间无法提高肽段信号强度,反而降低部分目标肽段的可检出性,综合考虑酶解效果与效率等各种因素,酶解时间选择为6 h。
表4 酶解时间对特征肽信号相对强度的影响
Table 4 Effect of digestion time on peak relative intensities of marker peptides
酶解时间/hpep1pep2pep3pep4pep50.325.75±1.35e23.81±0.97e7.56±0.56d18.33±1.13e63.12±2.04c0.537.00±1.42d43.54±1.38d13.69±1.08cd24.15±1.54d65.34±1.32c143.23±2.08d48.76±1.87d21.53±1.59c38.94±0.87c70.12±2.07c278.23±3.14c74.12±2.04c56.39±2.07b65.61±1.94b83.57±1.84b497.79±2.55a96.32±2.81a82.35±2.31b96.32±2.13a91.51±2.75ab6100.00±1.08a100.00±1.51a100.00±1.20a98.45±3.08a94.18±3.18a1086.62±2.37b86.54±2.03b97.62±2.57a100.00±1.34a100.00±1.07a1287.15±2.39b85.32±1.85b96.33±1.86a98.34±1.88a97.68±2.59a
2.4 方法学考察
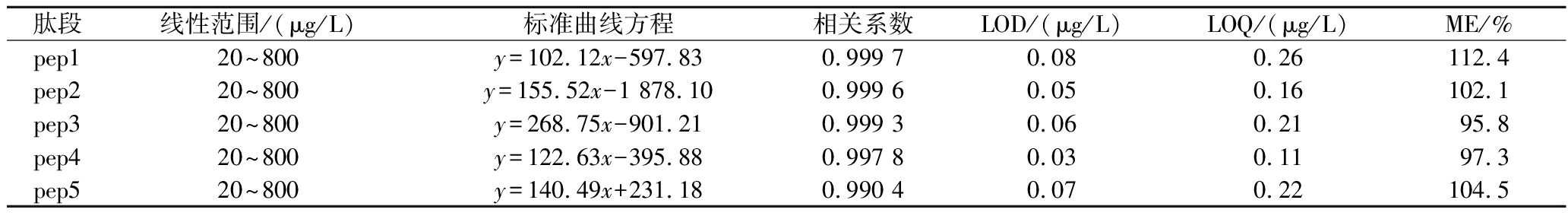
特征肽峰强度(y)与其浓度(x)呈线性关系,回归分析结果如表5,特征肽在20~800 μg/L范围内线性相关系数>0.99,线性关系非常好;确定5条特征肽的LOD为0.03~0.08 μg/L,LOQ为0.11~0.26 μg/L(相当于2.75~6.50 μg/kg),目标肽的灵敏度可以满足较低浓度肽定量测定的要求。超高效液相色谱串联四极杆飞行时间高分辨质谱的方法分析过程中会存在一定程度的ME,特征肽pep1、pep2、pep5存在一定程度的增强效应,而特征肽pep3和pep4存在一定程度的抑制效应,结果如表5所示,5条特征肽段的ME为95%~113%,无显著的抑制或增强效应,对实验结果不会产生显著影响。
表5 特征肽含量测定的标准曲线、LOQ、LOD与ME
Table 5 Standard curve, LOQ, LOD and ME of marker peptides
肽段线性范围/(μg/L)标准曲线方程相关系数LOD/(μg/L)LOQ/(μg/L)ME/%pep120~800y=102.12x-597.830.999 70.080.26112.4pep220~800y=155.52x-1 878.100.999 60.050.16102.1pep320~800y=268.75x-901.210.999 30.060.2195.8pep420~800y=122.63x-395.880.997 80.030.1197.3pep520~800y=140.49x+231.180.990 40.070.22104.5
2.5 加标回收率
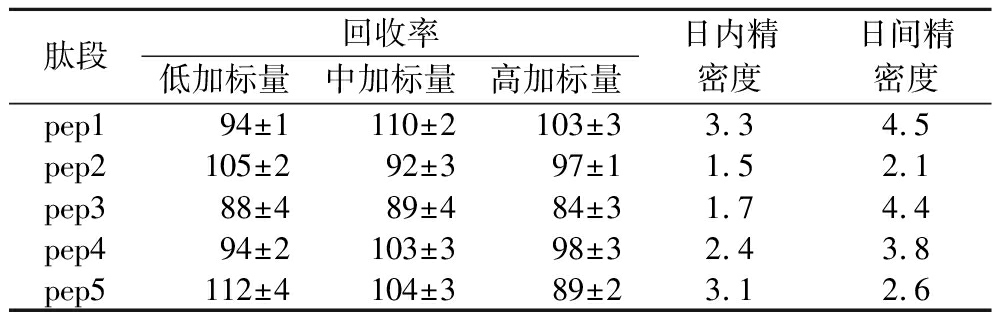
为了考查超高效液相色谱串联四极杆飞行时间高分辨质谱定量测定的可靠性,在牛肉丸酶解液中加入5条目标特征肽段混合标准溶液50 μL,分别选取20、50、100 μg/L的低、中、高3个质量浓度,相当于样品中特征肽的添加质量为0.5、1.25、5.0 mg/kg,进行分析试验,平行测定5次,分别计算其回收率,结果见表6。低、中、高加标量下的回收率分别为88%~112%、89%~110%、84%~103%,均介于80%~120%的范围内,处于可接受的范围。分别对5条特征肽加标样品进行日内和日间平行测定5次,以RSD值评定精密度,日内和日间的RSD范围分别为1.5%~3.3%、2.1%~4.5%,均小于10%,适用于牛肉丸样品中大豆特征肽的定量鉴别与测定。
表6 牛肉丸样品中不同特征肽的加标回收率
及测定精密度 单位:%
Table 6 The recoveries of different characteristic peptides in beef meatball samples
肽段回收率低加标量中加标量高加标量日内精密度日间精密度pep194±1110±2103±33.34.5pep2105±292±397±11.52.1pep388±489±484±31.74.4pep494±2103±398±32.43.8pep5112±4104±389±23.12.6
2.6 样品测定
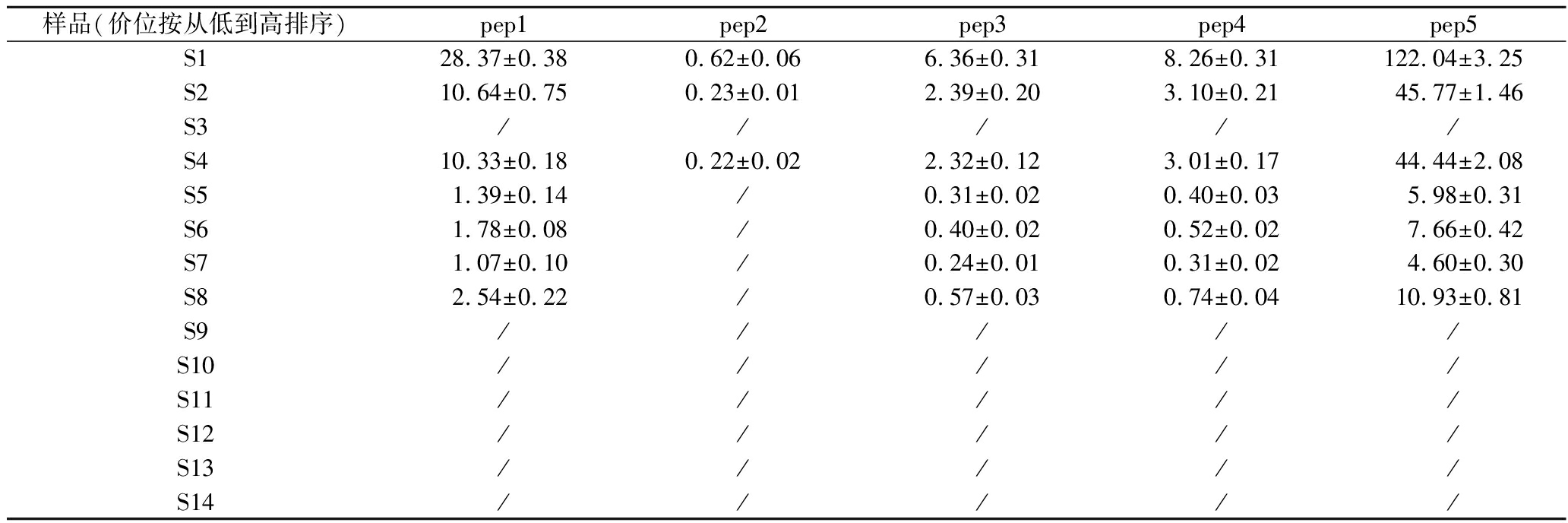
从市场购买的14种不同价位的牛肉丸样品处理后测定特征肽的含量,结果见表7。本次检测的目标肽段的种属来源为大豆,不同价位的牛肉丸样品中部分检测出含有目标特征肽段的存在,特别是在低价位的牛肉丸样品中含有较高量的目标肽段。S1样品中能测出特征肽段的含量最多,S2和S4样品中能测出的大豆特征肽的含量也较高。S3样品的价位较低,但未检测出大豆源特征肽段。从总体上看,随着牛肉丸样品价位的升高,在其中能测出的大豆源特征肽段的含量总体呈下降的趋势,特别是后6类样品中未测出大豆源特征肽。
表7 牛肉丸样品中特征肽段测试含量结果 单位:mg/kg
Table 7 Test results of characteristic peptides in beef meatball samples
样品(价位按从低到高排序)pep1pep2pep3pep4pep5S128.37±0.380.62±0.066.36±0.318.26±0.31122.04±3.25S210.64±0.750.23±0.012.39±0.203.10±0.2145.77±1.46S3/////S410.33±0.180.22±0.022.32±0.123.01±0.1744.44±2.08S51.39±0.14/0.31±0.020.40±0.035.98±0.31S61.78±0.08/0.40±0.020.52±0.027.66±0.42S71.07±0.10/0.24±0.010.31±0.024.60±0.30S82.54±0.22/0.57±0.030.74±0.0410.93±0.81S9/////S10/////S11/////S12/////S13/////S14/////
注:表中标注“/”代表未测出。
以样品S1为例,其pep3的对应通道中目标物的出峰时间与标准品中对应通道里目标物的出峰时间相差0.06 min,时间偏差<0.1 min,可视为出峰时间一致,如图2所示;在二级质谱图里样品与标准品中检测的碎片离子一致、且质荷比偏差均<20×10-6,这表明该样品中11.52 min处出峰物质为目标物pep3,该牛肉丸样品可判定为含有大豆蛋白的阳性样品,如图3所示。综上所述,根据样品中目标物的出峰时间及高分辨质谱中碎片离子的质荷比,与标准品中的目标物进行鉴别,可以有效排除假阳性结果以提高检测的准确度。
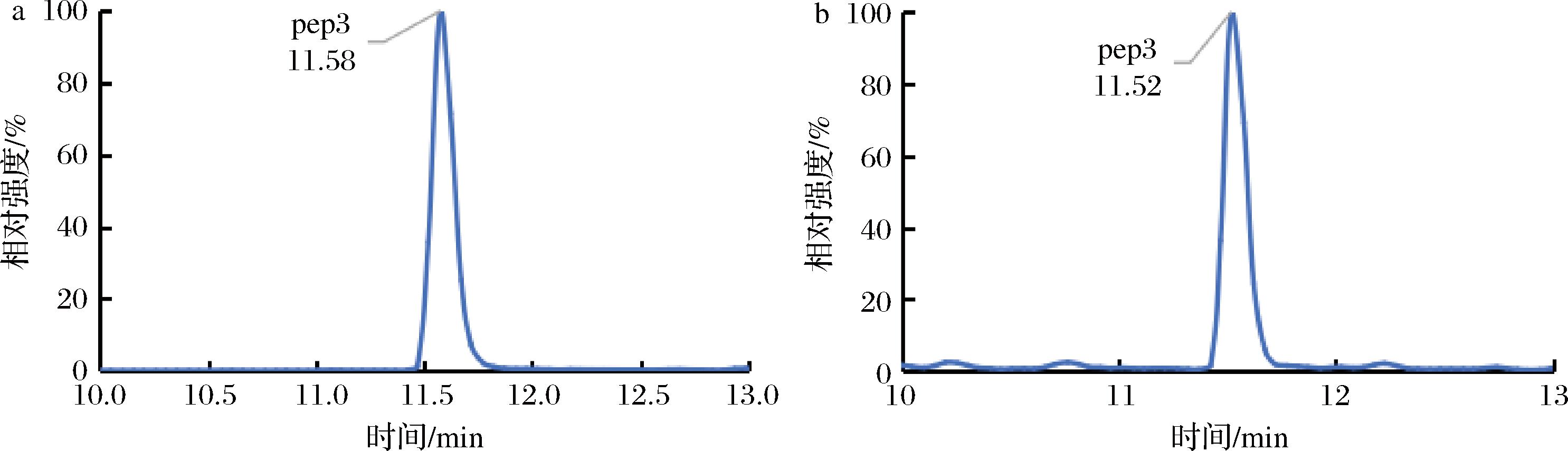
a-标准品;b-样品
图2 特征肽pep3在标准品和样品中的色谱图
Fig.2 Chromatograms of marker peptide pep3 in standard and sample
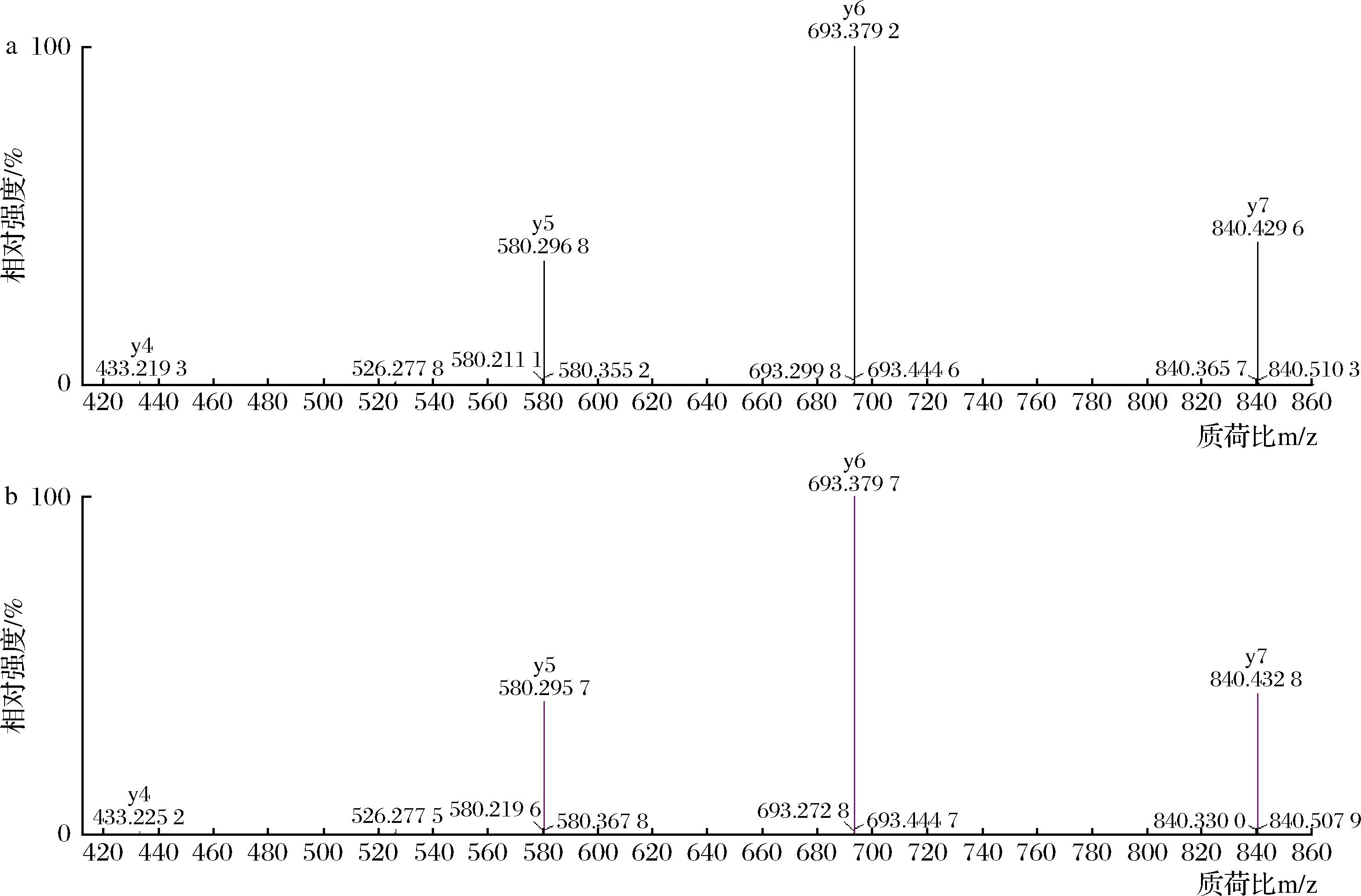
a-标准品;b-样品
图3 特征肽pep3在标准品和样品中的质谱图
Fig.3 Mass spectrum of marker peptide pep3 in standard and sample
3 结论
对牛肉丸样品前处理中的酶解时间与脱盐纯化的固相萃取参数进行优化,在超高效液相色谱串联四极杆飞行时间高分辨质谱的p-MRM采集模式下,再优化质谱检测条件中的CE值和CV值,采用外标法进行定量分析。特征肽的分离条件良好,具有非常好的重现性,提高了试验的准确度和灵敏度。在一定的线性范围下,检测得到的特征肽段相关系数>0.99。特征肽在低、中、高3个水平添加浓度的加标回收率在95.8%~112.4%,RSD值均<10%,可用于进一步地定量检测牛肉丸制品中大豆蛋白特征肽的含量。市售的14种价位的牛肉丸中有7种中可检测出大豆特征肽,成功检出含大豆目标肽的样品占不同价位的牛肉丸样品总数的50%。随着牛肉丸价位的升高,其混入该大豆特征肽的含量总体呈下降趋势。综上所述,该方法可为牛肉丸等制品中蛋白质种属鉴别提供一定的技术参考。
[1] PREMANANDH J.Horse meat scandal—A wake-up call for regulatory authorities[J].Food Control, 2013, 34(2):568-569.
[2] MEDINA S, PERESTRELO R, SILVA P, et al.Current trends and recent advances on food authenticity technologies and chemometric approaches[J].Trends in Food Science &Technology, 2019, 85:163-176.
[3] BÖHME K, CALO-MATA P, BARROS-VEL ZQUEZ J, et al.Recent applications of omics-based technologies to main topics in food authentication[J].TrAC Trends in Analytical Chemistry, 2019, 110:221-232.
ZQUEZ J, et al.Recent applications of omics-based technologies to main topics in food authentication[J].TrAC Trends in Analytical Chemistry, 2019, 110:221-232.
[4] GRUNDY H H, BROWN L C, ROMERO M R, et al.Review:Methods to determine offal adulteration in meat products to support enforcement and food security[J].Food Chemistry, 2023, 399:133818.
[5] BENESOVA E, VIDOVA V, SPACIL Z.A comparative study of synthetic winged peptides for absolute protein quantification[J].Scientific Reports, 2021, 11:10880.
[6] VON BARGEN C, DOJAHN J, WAIDELICH D, et al.New sensitive high-performance liquid chromatography-tandem mass spectrometry method for the detection of horse and pork in halal beef[J].Journal of Agricultural and Food Chemistry, 2013, 61(49):11986-11994.
[7] SARAH S A, FARADALILA W N, SALWANI M S, et al.LC-QTOF-MS identification of porcine-specific peptide in heat treated pork identifies candidate markers for meat species determination[J].Food Chemistry, 2016, 199:157-164.
[8] STOBERNACK T, HÖPER T, HERFURTH U M.How processing affects marker peptide quantification-A comprehensive estimation on bovine material relevant for food and feed control[J].Food Chemistry, 2024, 454:139768.
[9] STACHNIUK A, SUMARA A, MONTOWSKA M, et al.Peptide markers for distinguishing Guinea fowl meat from that of other species using liquid chromatography-mass spectrometry[J].Food Chemistry, 2021, 345:128810.
[10] 王忠合, 李晓婷, 胡文梅, 等.超高效液相色谱-高分辨质谱法测定肉类特征肽[J].食品与发酵工业, 2021, 47(18):258-266.
WANG Z H, LI X T, HU W M, et al.Determination of peptide markers of meat species by ultra-high pressure liquid chromatography coupled with high resolution mass spectrometry[J].Food and Fermentation Industries, 2021, 47(18):258-266.
[11] H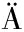 FNER L, KALKHOF S, JIRA W.Authentication of nine poultry species using high-performance liquid chromatography-tandem mass spectrometry[J].Food Control, 2021, 122:107803.
FNER L, KALKHOF S, JIRA W.Authentication of nine poultry species using high-performance liquid chromatography-tandem mass spectrometry[J].Food Control, 2021, 122:107803.
[12] LEITNER A, CASTRO-RUBIO F, MARINA M L, et al.Identification of marker proteins for the adulteration of meat products with soybean proteins by multidimensional liquid chromatography-tandem mass spectrometry[J].Journal of Proteome Research, 2006, 5(9):2424-2430.
[13] 王忠合, 胡文梅, 卢燎源, 等.非标记蛋白组学法鉴别牛肉丸中肉类掺假的方法研究[J].中国食品学报, 2022, 22(4):295-308.
WANG Z H, HU W M, LU L Y, et al.Methods for quantitative identification of meat adulteration in beef meatballs by label-free proteomics[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(4):295-308.
[14] HE Z Y, ZHAO L Q, LIU X W, et al.The application of in-source fragmentation in ultra-high performance liquid chromatography-electrospray ionization-tandem mass spectrometry for pesticide residue analysis[J].Journal of Chromatography A, 2020, 1633:461637.
[15] MUEHLWALD S, BUCHNER N, KROH L W.Investigating the causes of low detectability of pesticides in fruits and vegetables analysed by high-performance liquid chromatography-time-of-flight[J].Journal of Chromatography A, 2018, 1542:37-49.