青稞(Hordeum vulgare Linn.var.nudum Hook.f.)是我国青藏地区特色的主要粮食作物[1-2],富含多种生物活性成分,如β-葡聚糖、γ-氨基丁酸、多酚类和花青素等[3-4]。根据颜色不同青稞可分为蓝青稞、白青稞、黑青稞三大类,其中蓝青稞因独特的花青素积累呈现高抗氧化活性,但品种间活性成分差异对发酵代谢的影响尚未明晰。
青稞红曲是以蒸熟的青稞为基质由紫色红曲霉(Monascus purpureus Went)经固态发酵而成[5],具有消食健脾、活血祛瘀、降血脂、降血糖、降血压、缓解跌打损伤等药理作用[6-7]。在固态发酵过程红曲霉菌在固态多孔基质表面及内部生长,通过分泌酶分解底物,产生多种次级代谢产物,如洛伐他汀、麦角甾醇和色素等,其降血脂功效与洛伐他汀、麦角甾醇等代谢物密切相关[8-9]。
目前已有的报道多集中在发酵条件优化方面,缺乏对原料品种差异-终产物积累关联性的系统研究。本文基于多指标分析技术,以蓝、白、黑青稞及其发酵产物青稞红曲为研究对象,通过HPLC定量酸式、内酯式洛伐他汀及麦角甾醇,结合紫外-可见分光光度法测定β-葡聚糖,构建以“原料成分-终产物含量”为核心的多指标质量评价体系,旨在解析青稞品种差异对发酵产物青稞红曲活性成分的影响,为青稞红曲的原料优选提供科学依据。
1 材料与方法
1.1 材料与试剂
洛伐他汀,中国食品药品检定研究院;麦角甾醇、β-葡聚糖,成都普思生物科技有限公司;甲醇、乙腈(色谱纯),国药集团化学试剂有限公司;葡萄糖、蛋白胨,北京奥博星生物技术有限责任公司;NaOH、HCl、NaNO3、MgSO4、KH2PO4、乙醚、无水乙醇、NaH2PO4、Na2HPO4、H3PO4(分析纯),国药集团化学试剂有限公司;刚果红,上海源叶生物科技有限公司;自制超纯水。蓝青稞、白青稞、黑青稞均购于专卖店。
紫色红曲霉DCYY-001(经中国科学院微生物研究所鉴定,鉴定报告编号为微检字第2021JB298号),保藏于实验室-80 ℃冰箱。
液体种子培养基(g/L):葡萄糖 60,蛋白胨10,青稞粉2,NaNO3 2,MgSO4 2,KH2PO4 1,pH自然,121 ℃灭菌20 min,备用。
固态发酵培养基:青稞粉碎成40~50目,放入1 000 mL三角瓶中,每瓶160 g,加水48 mL,浸润30 min,121 ℃灭菌20 min,热打散,冷却,备用。
1.2 仪器与设备
LC-2030Cplus 型高效液相色谱仪、UV-1900i 型紫外可见分光光度计,日本Shimadzu公司;WB400US 型超声波清器,上海望标仪器有限公司;ME55 型分析天平,瑞士Mettler Toledo公司;H1750 型台式高速离心机,湖南湘仪实验室开发有限公司;Genie U 型超纯水机,上海乐枫生物科技有限公司。
1.3 实验方法
1.3.1 青稞红曲的制备
将紫色红曲霉菌接种于无菌的液体种子培养基中,30 ℃、150 r/min,避光培养72 h。然后将液体种子液按21 mL接种于灭菌的固态发酵培养基中并摇匀,置于30 ℃下培养4 d,后转入22 ℃,继续培养15 d,低温干燥备用。以蓝、白、黑青稞为基质发酵的青稞红曲分别命名为蓝青稞红曲、白青稞红曲、黑青稞红曲。
1.3.2 测定酸式和内酯式洛伐他汀的含量
色谱柱WondaSil C18 Superb(4.6 mm×250 mm, 5 μm),流动相A为乙腈,流动相B为0.1%(体积分数)磷酸水溶液,以A相与B相的体积比为60∶40为洗脱条件,检测波长238 nm,流速1.0 mL/min,柱温30 ℃,进样量10 μL[10-12]。对照品溶液的制备是精密称取内酯式洛伐他汀对照品,甲醇溶解,得内酯式洛伐他汀对照品溶液;于酸式洛伐他汀对照品溶液的制备是将内酯式洛伐他汀对照品溶解于甲醇,加入25 mL 0.2 mol/L NaOH溶液,超声波转化30 min,冷却后加入25 mL 0.2 mol/L HCl溶液中和,并用纯化水定容至刻度,得酸式洛伐他汀对照品溶液。供试品溶液的制备是取样品粉末0.5 g于容量瓶中,精密加入75%(体积分数)乙醇15 mL,超声波处理30 min,待其冷却至室温,摇匀后过0.45 μm有机滤膜,得到供试品溶液。
1.3.3 测定麦角甾醇的含量
以Cosmosil 5C18-MS-Ⅱ(4.6 mm×250 mm, 5 μm)为色谱柱,流动相为纯甲醇,检测波长284 nm,流速1.0 mL/min,柱温30 ℃,进样量20 μL[13-15]。对照品溶液制备是精密称取麦角甾醇对照品加入适量甲醇溶解,充分摇匀,制成0.4 mg/mL的麦角甾醇对照品溶液。供试品溶液的制备是称取50 g NaOH于80 mL超纯水中,用无水乙醇定容到200 mL,制成25%(体积分数)碱乙醇溶液。精密称取样品粉末1.0 g于容量瓶中,精密加入25%碱乙醇溶液20 mL,摇匀,放入85 ℃水浴锅中,皂化1 h,补加2 mL无水乙醇,继续皂化30 min,待其冷却至室温,加入15 mL乙醚,充分摇匀,静置提取30 min,用纯水缓缓将乙醚层冲洗至中性,将乙醚层转移至蒸发皿中,放入40 ℃的水浴锅上,将乙醚全部蒸干,向蒸发皿中加入无水乙醇,使其完全溶解,过0.45 μm有机滤膜[15-16],备用。
1.3.4 测定β-葡聚糖的含量
精密称取β-葡聚糖对照品加入4 mL的纯水,置60 ℃水浴中加热直至溶解,制成0.2 mg/mL的β-葡聚糖对照品溶液。取8.96 g Na2HPO4加入适量纯水,使其完全溶解后,定容至250 mL。取0.78 g NaH2PO4加入适量纯水,使其溶解完全后,定容至50 mL。用NaH2PO4溶液调整Na2HPO4溶液的pH值至8.0,即得0.1 mol/L的磷酸盐缓冲溶液。精密称取0.03 g刚果红,加入0.1 mol/L的磷酸盐缓冲溶液100 mL使其完全溶解,即得刚果红溶液。精密称取1.0 g样品于25 mL容量瓶中,加水定容至刻度,超声波处理10 min,放置70 ℃水浴中60 min后,取出放冷滤取1 mL续滤液,加入4 mL刚果红溶液,室温下放置30 min[17],即得供试品溶液。采用紫外-可见分光光度法在545 nm处测量吸光度[17-18]。
1.4 数据处理
采用SPSS 26进行数据整理及分析,结果以“平均值±标准差”表示(n=3)。采用GraphPad Prism 9.0绘制相关图。
2 结果与分析
2.1 酸式和内酯式洛伐他汀的含量
青稞红曲可代谢多种生物活性物质,其中洛伐他汀是一种具有降压和降脂作用的功能成分。由天然发酵青稞红曲产生的洛伐他汀主要包括2种结构形式:酸式和内酯式。其中,酸式洛伐他汀表现出更显著的生物活性[19]。目前,使用HPLC检测洛伐他汀的方法已经成熟。本研究分析了不同品种青稞及其发酵后的青稞红曲样品。建立了一种HPLC法来确定青稞红曲中的酸式和内酯式洛伐他汀的含量。酸式洛伐他汀的回归方程为Y=1 805.5X-10 761,相关系数r为0.999 2,线性范围为12.5~800 μg/mL。内酯式洛伐他汀的回归方程为Y=41 320X-4 196.5,相关系数r为0.999 6,线性范围为3.125~200 μg/mL。方法学验证表明,样品中酸式和内酯式洛伐他汀与对照品峰保留时间一致,酸式和内酯式洛伐他汀色谱峰分离度好且附近无杂峰(图1);精密度试验中酸式和内酯式洛伐他汀峰面积的相对标准偏差(relative standard deviation,RSD)分别为1.75%和0.13%,显示仪器具有良好精密度,重复性试验中酸式和内酯式洛伐他汀峰面积的RSD分别为1.01%和1.21%,在稳定性试验中,室温保存24 h的样品溶液的酸式和内酯式洛伐他汀峰面积RSD分别为1.49%和0.30%,表明方法具有良好的重复性和溶液稳定性。酸式洛伐他汀的加样回收率和RSD分别为99.54%和0.73%,内酯式洛伐他汀的加样回收率和RSD分别为99.13%和1.27%。
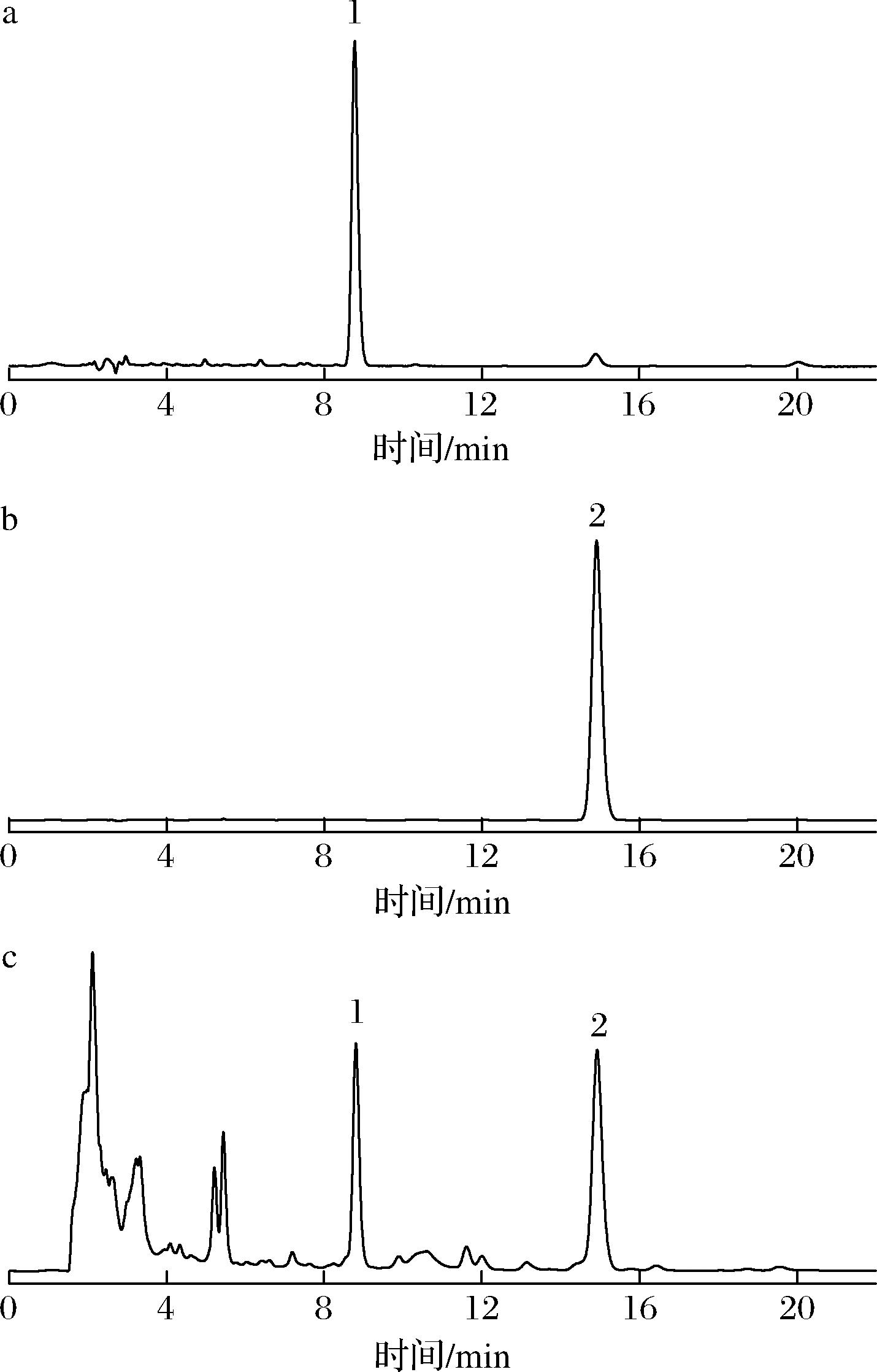
a-酸式洛伐他汀对照品;b-内酯式洛伐他汀对照品;c-样品
图1 酸式和内酯式洛伐他汀的专属性试验色谱图
Fig.1 Chromatograms for specificity test of acidic and lactone lovastatin
注:1-酸式洛伐他汀;2-内酯式洛伐他汀。
该方法分析了不同品种青稞与其发酵青稞红曲样品。不同品种的青稞均不含酸式和内酯式洛伐他汀,而发酵后的青稞红曲均产生了酸式和内酯式洛伐他汀,蓝青稞红曲中酸式和内酯式洛伐他汀的含量分别为14.64~15.97 mg/g和0.39~0.45 mg/g,白青稞红曲中酸式和内酯式洛伐他汀的含量分别为8.37~10.02 mg/g和0.15~0.22 mg/g,黑青稞红曲中酸式和内酯式洛伐他汀的含量分别为11.64~13.81 mg/g和0.24~0.31 mg/g,以发酵后的青稞红曲中酸式和内酯式洛伐他汀含量平均值对比(图2),蓝青稞红曲中酸式洛伐他汀含量[(15.21±0.68) mg/g]和内酯式洛伐他汀含量[(0.43±0.032) mg/g]显著高于白青稞红曲[(9.40±0.90)、(0.19±0.035) mg/g]、黑青稞红曲[(12.56±1.12)、(0.28±0.038) mg/g](P<0.05),蓝青稞红曲中酸式和内酯式洛伐他汀含量约为白、黑青稞红曲的1.6倍、1.2倍和2.3倍、1.5倍,黑青稞红曲中酸式和内酯式洛伐他汀含量与白青稞红曲相比有显著性差异(P<0.05)。
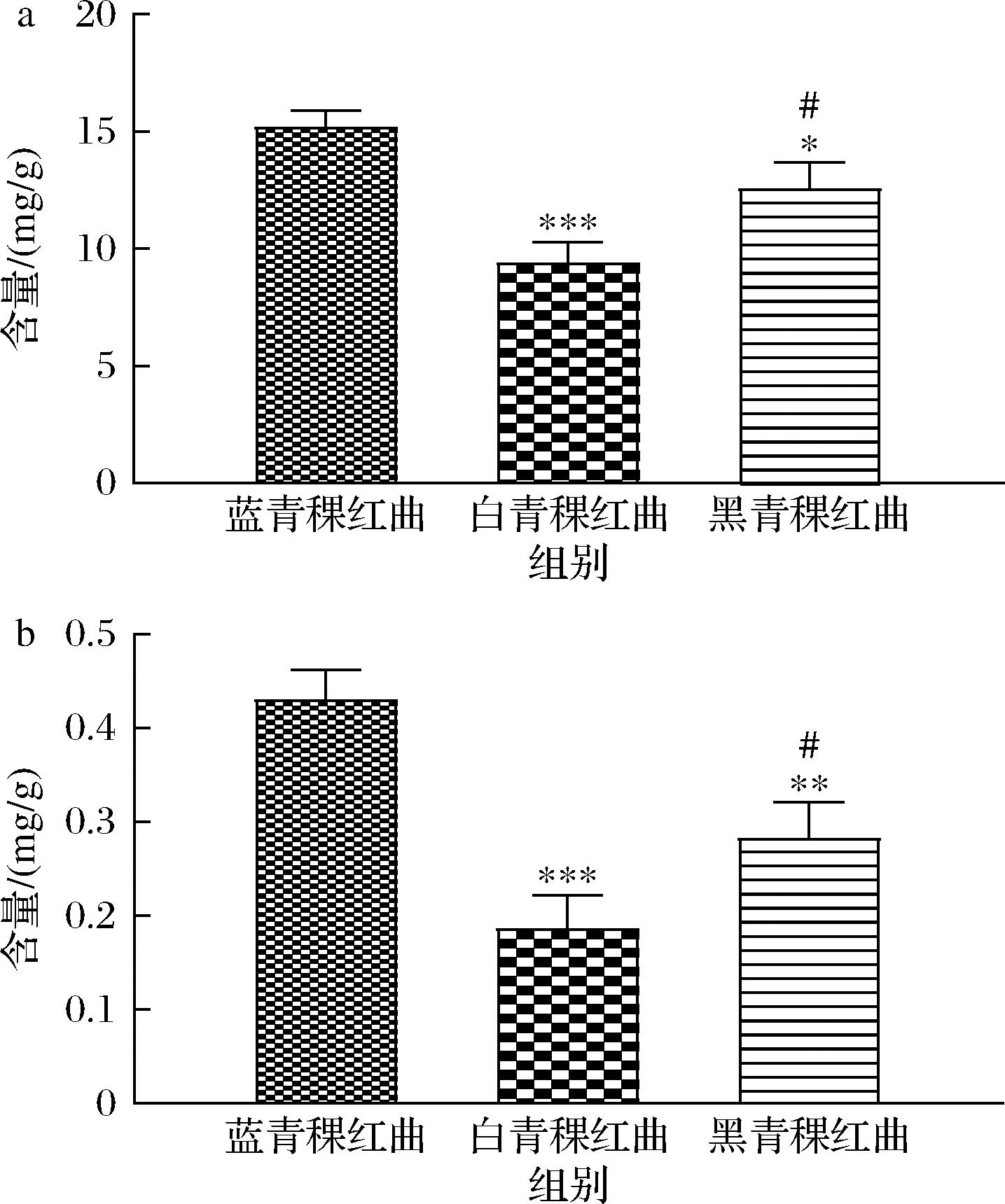
a-酸式洛伐他汀;b-内酯式洛伐他汀
图2 不同品种青稞发酵后青稞红曲中酸式和内酯式洛伐他汀含量比较
Fig.2 Comparison of acidic and lactone lovastatin contents in fermented highland barley Monascus from different highland barley varieties
注:蓝青稞红曲组与白青稞红曲组和黑青稞红曲组平均值对比,*,P<0.05;**,P<0.01;***,P<0.001(n=3);白青稞红曲组与黑青稞红曲组平均值对比,#,P<0.05(n=3)(下同)。
2.2 麦角甾醇的含量
麦角甾醇是在青稞红曲发酵过程中产生的一种重要的类维生素物质,其含量与真菌生物量存在正相关,它也是微生物细胞膜的关键成分之一,作为维生素D2的前体,麦角甾醇在紫外线照射下可发生结构转化生成维生素D2,维生素D2在人体中发挥着重要的生理作用,包括调节Ca和P的代谢以及影响细胞增殖和分化[20]。本研究采用HPLC法测定麦角甾醇含量。根据1.3.3节的方法获得麦角甾醇峰面积,计算回归方程为Y=2 284.2X-3 089.5,相关系数r为0.999 9,线性范围是5.86~750 μg/mL。方法学验证表明,样品中麦角甾醇与对照品峰保留时间一致,麦角甾醇色谱峰分离度好且附近无杂峰(图3);精密度试验中麦角甾醇峰面积的RSD为0.33%,显示了仪器的良好精密度,重复性试验中麦角甾醇峰面积的RSD为1.72%,在稳定性试验中,室温保存24 h的样品溶液的麦角甾醇峰面积RSD为1.68%,表明方法具有良好的重现性和溶液稳定性。加标回收试验中麦角甾醇的平均回收率为98.24%,RSD为1.54%。
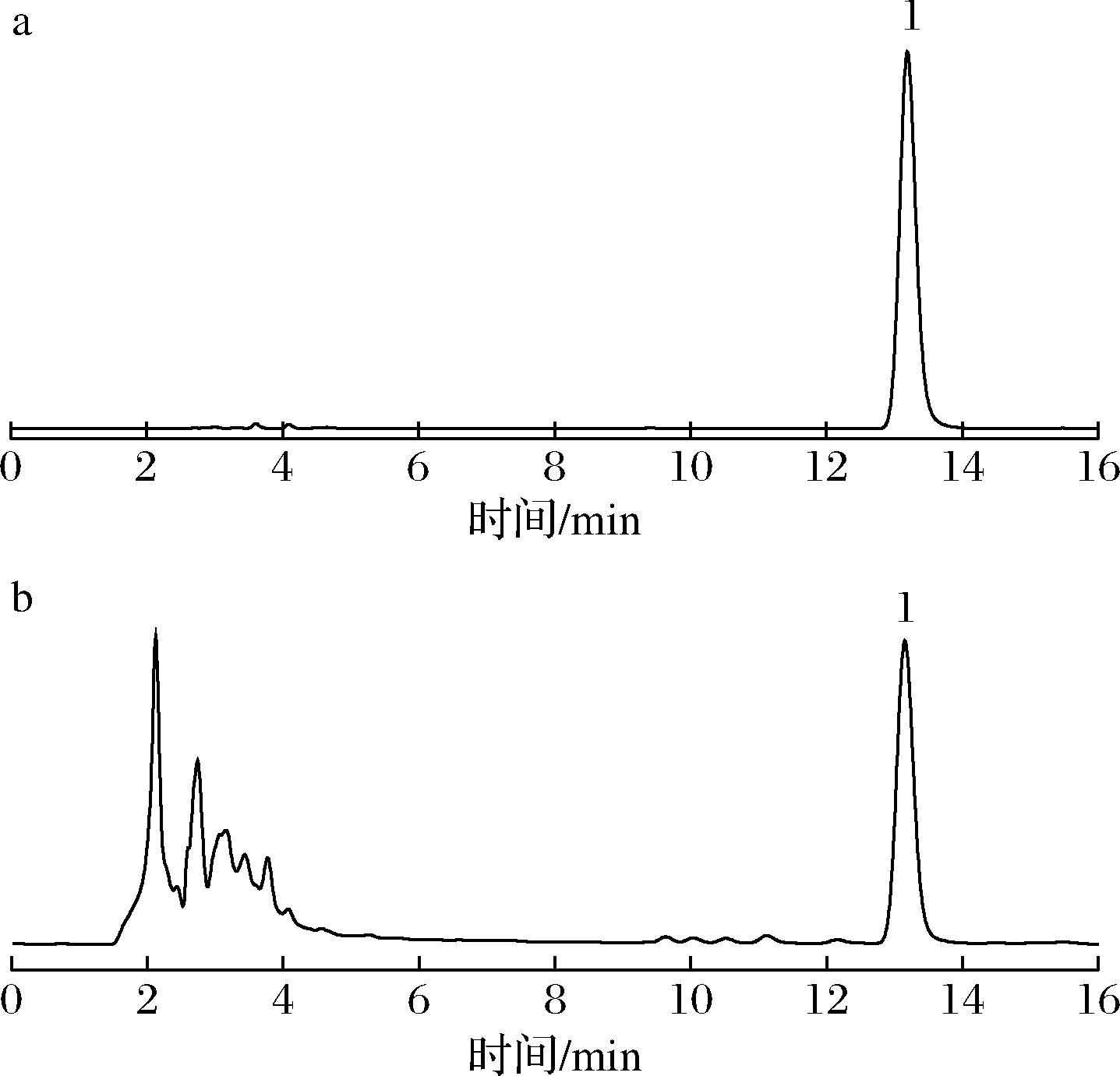
a-麦角甾醇对照品;b-样品
图3 麦角甾醇专属性试验色谱图
Fig.3 Chromatograms for specificity test of ergosterol
注:1-麦角甾醇。
该方法分析了不同品种青稞与其发酵青稞红曲样品中麦角甾醇的含量。发酵前,不同品种的青稞均不含有麦角甾醇,发酵后的不同品种青稞红曲均产生了麦角甾醇,蓝青稞、白青稞和黑青稞红曲中麦角甾醇含量分别为7.26~8.71 mg/g、2.49~3.90 mg/g 和4.50~5.32 mg/g。以发酵后的青稞红曲中麦角甾醇含量平均值对比(图4),蓝青稞红曲中麦角甾醇含量[(7.90±0.74) mg/g]显著高于白青稞红曲[(3.37±0.77) mg/g]、黑青稞红曲[(4.86±0.42) mg/g](P<0.05),蓝青稞红曲中麦角甾醇含量约为白、黑青稞红曲的2.3倍和1.6倍,黑青稞红曲中麦角甾醇含量与白青稞红曲相比无显著性差异(P>0.05)。
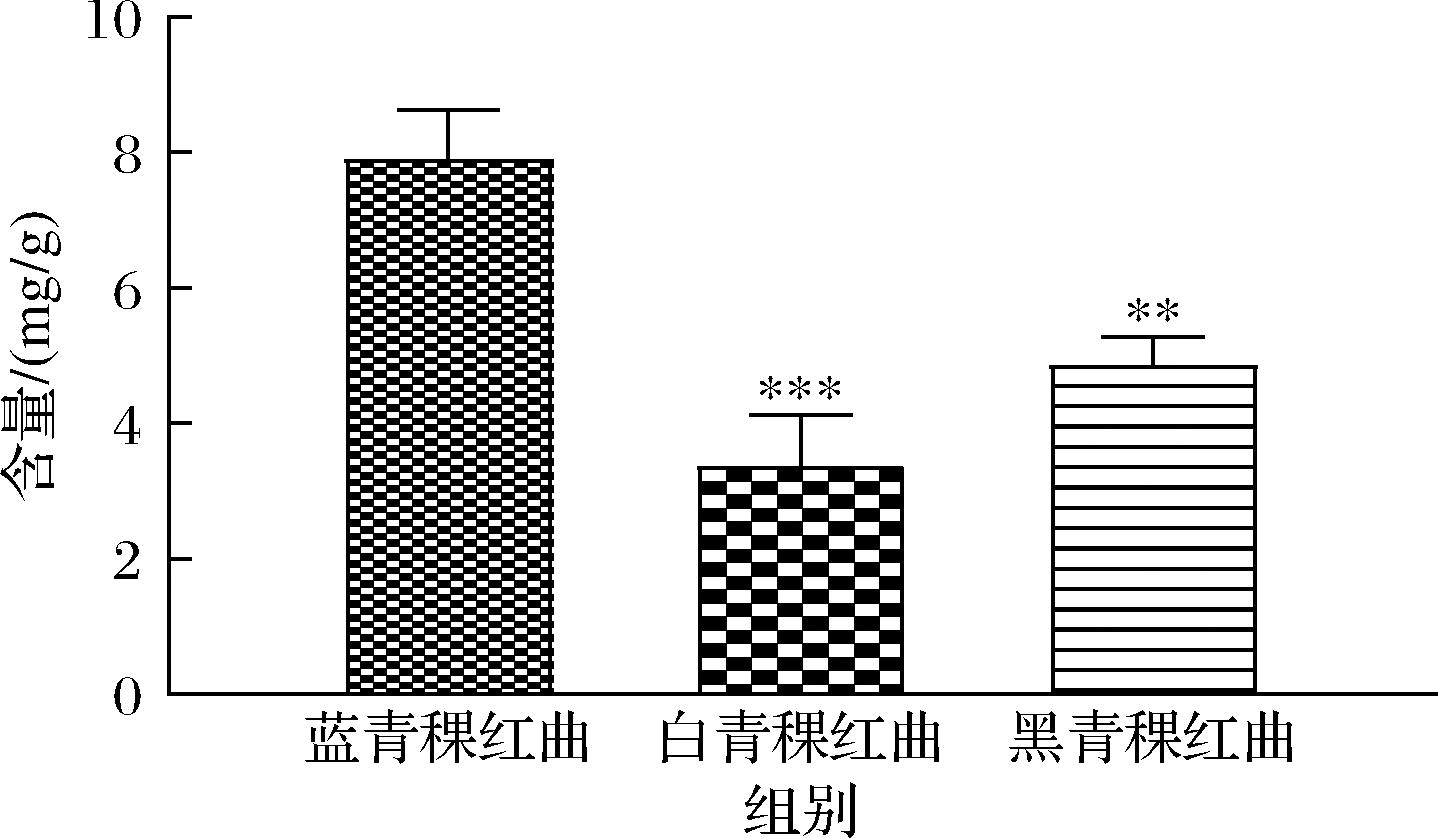
图4 不同品种青稞发酵后青稞红曲中麦角甾醇含量比较
Fig.4 Comparison of ergosterol content in fermented highland barley Monascus from different highland barley varieties
2.3 β-葡聚糖的含量
β-葡聚糖已被证明通过抑制肠道对膳食脂肪和胆固醇的吸收、促进胆酸排泄以及加速胆固醇向胆酸转化来降低血清胆固醇水平。此外,它还显示出潜在的抗癌和抗肿瘤生物活性。对β-葡聚糖标准溶液进行吸光度测量,并用超纯水和刚果红溶液校准空白吸光度至零。标准曲线回归方程为Y=0.004X-0.019 8,相关系数r为0.998 3,线性范围是40~400 μg/mL,表明β-葡聚糖在此范围内与吸光度呈线性关系。连续6次测量β-葡聚糖对照品溶液的吸光度,得到RSD为0.77%,证明仪器的精密度良好。分析6个青稞红曲样品溶液的重复性,吸光度RSD为0.49%,表明该方法的良好重复性。在2 h内不同时间点测定样品溶液,吸光度的RSD增加到16.21%,表明应在样品制备后尽快进行测量以确保准确性。加标回收试验中β-葡聚糖的平均回收率为98.60%,RSD为1.14%。
采用标准曲线法对不同品种青稞及其发酵青稞红曲样品中β-葡聚糖的含量进行了测定。结果显示不同品种的青稞均含有β-葡聚糖,品种不同β-葡聚糖的含量差异较大,蓝青稞、白青稞和黑青稞中β-葡聚糖含量分别为62.14~72.65 mg/g、48.02~53.37 mg/g 和54.43~60.37 mg/g,以不同品种青稞中β-葡聚糖含量平均值对比(图5),蓝青稞中β-葡聚糖含量[(68.24±5.96) mg/g]显著高于白青稞[(49.63±5.02) mg/g]、黑青稞[(58.26±4.39) mg/g](P<0.05),黑青稞中β-葡聚糖含量与白青稞相比无显著性差异(P>0.05)。
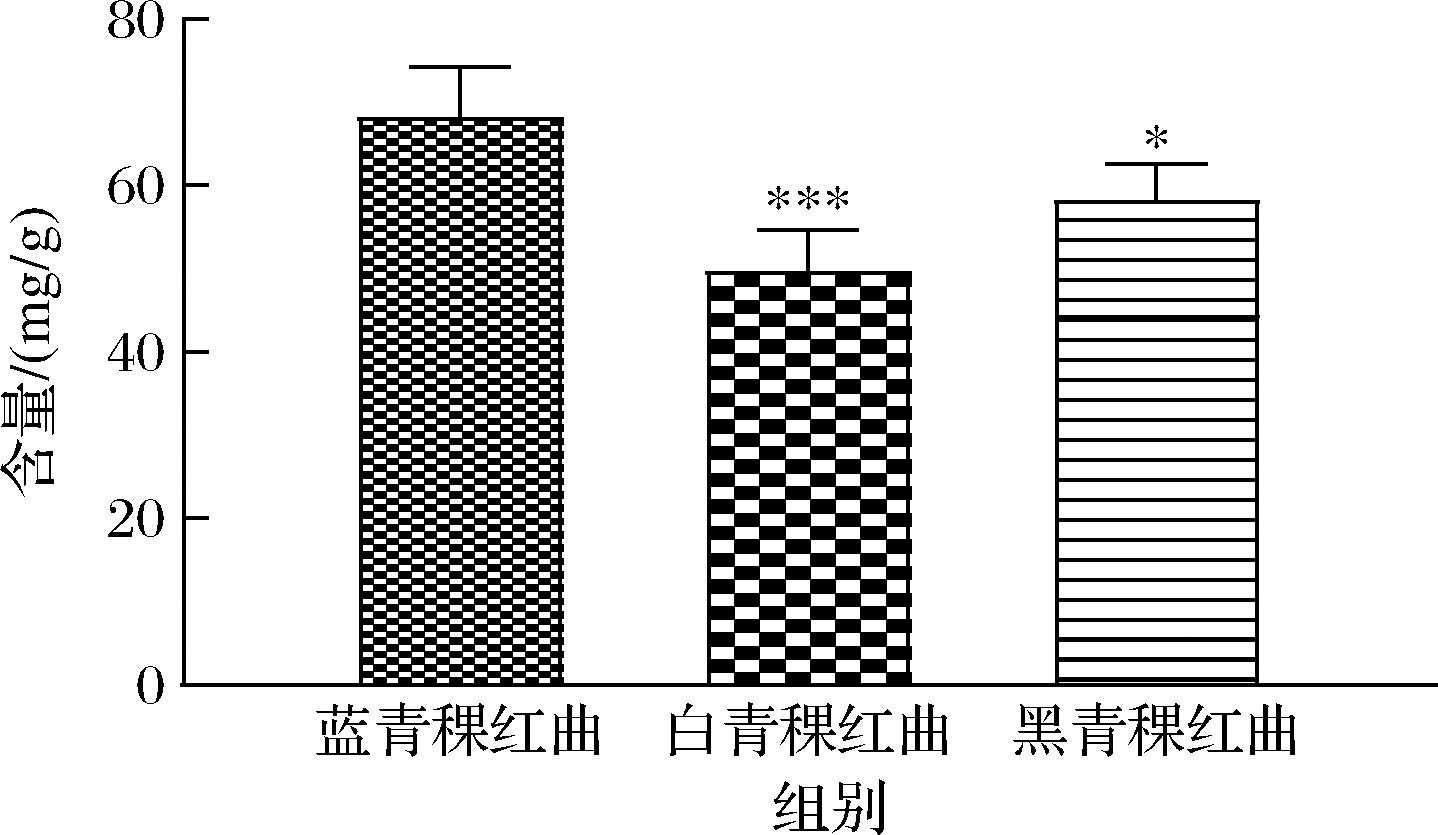
图5 不同品种青稞中β-葡聚糖含量比较
Fig.5 Comparison of β-glucan content in different highland barley varieties
不种品种青稞发酵后的青稞红曲中β-葡聚糖的含量显著降低,蓝青稞、白青稞和黑青稞红曲中β-葡聚糖含量分别为34.65~39.71 mg/g、19.11~23.27 mg/g 和22.52~26.22 mg/g。以发酵后的青稞红曲中β-葡聚糖含量平均值对比(图6),蓝青稞红曲中β-葡聚糖含量[(37.37±2.55) mg/g]显著高于白青稞红曲[(20.88±2.15) mg/g]、黑青稞红曲[(24.83±2.02) mg/g](P<0.05),蓝青稞红曲中β-葡聚糖含量约为白、黑青稞红曲的1.8倍和1.5倍,黑青稞红曲中β-葡聚糖含量与白青稞红曲相比无显著性差异(P>0.05)。
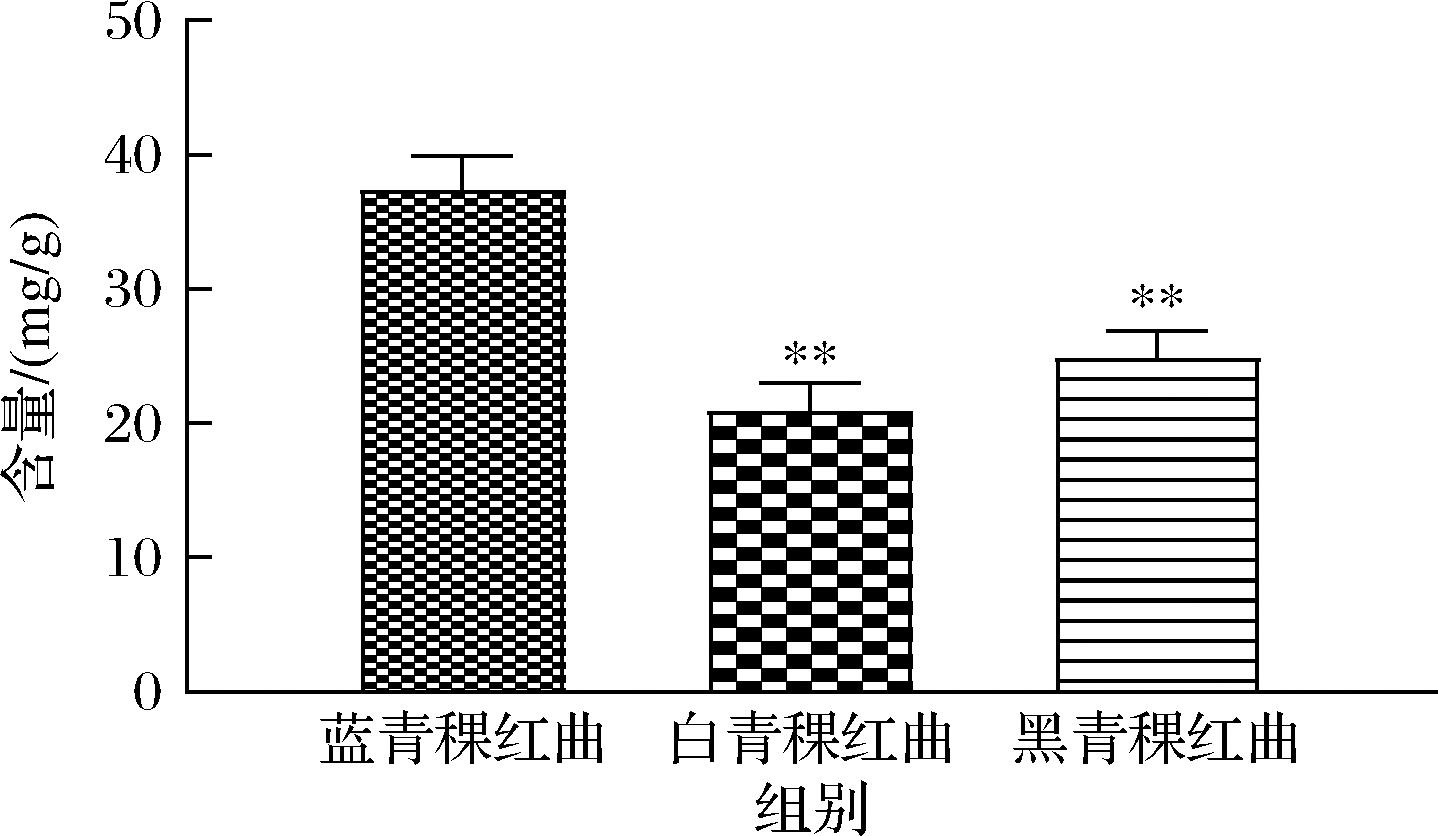
图6 不同品种青稞发酵后青稞红曲中β-葡聚糖含量比较
Fig.6 Comparison of β-glucan content in fermented highland barley Monascus from different highland barley varieties
3 讨论与结论
红曲霉在我国具有悠久的应用历史,主要用于生产药食两用产品红曲。2005年国家食品药品监督管理局发布《可用于保健食品的真菌菌种名单》明确将紫色红曲霉列为传统食用菌,可用于食品生产。当前研究多注重发酵工艺条件优化,而轻原料特性。红曲霉在固态发酵过程中,底物对其代谢产物的合成有着重要的影响。本实验以紫色红曲霉为菌种,不同品种的青稞(蓝、白、黑青稞)为底物发酵生产青稞红曲,以其主要活性成分(酸式和内酯式洛伐他汀、麦角甾醇及β-葡聚糖)为指标,考察青稞品种差异对发酵产物中主要活性成分变化的影响。
参照李雨恒等[15]麦角甾醇含量测定法提取时,考察了处理方法中乙醚的用量,发现乙醚用量增至15 mL时乙醚层更易分离,可显著提高分离效率;β-葡聚糖测定选择刚果红溶液浓度时,考察了不同量刚果红(0.01、0.03、0.05 g)溶于100 mL的0.1 mol/L的磷酸盐缓冲溶液(pH 8)的吸光度,结果显示0.03 g刚果红溶于100 mL的0.1 mol/L的磷酸盐缓冲溶液(pH 8)吸光度最佳,且吸光度值范围波动较小。此外,在β-葡聚糖含量测定的过程中发现刚果红溶液较不稳定,稳定性<2 h,因此,β-葡聚糖测定需使用新配刚果红溶液,以保证测定稳定性。
青稞在营养成分和物化性质上与大米等其他谷物存在显著差异,特别是在蛋白质、膳食纤维、β-葡聚糖、多酚类化合物等方面的含量均高于常用红曲的主要发酵原料大米,并且其青稞的淀粉糊化温度较高,抗性淀粉含量较高,糊粉层中膳食纤维含量也较高[21-23]。这些因素可能影响红曲霉的初级代谢和次级代谢水平,并导致发酵后的青稞红曲的相关真菌合成活性成分(如酸式/内酯式洛伐他汀、麦角甾醇和β-葡聚糖)较传统大米发酵的红曲米含量水平更高。目前有研究结果提示青稞红曲的酸式/内酯式洛伐他汀和麦角甾醇含量较红曲米显著增高[4],和本文的研究结果一致。
目前已报道的红曲米的主要活性成分含量分析结果显示,洛伐他汀平均含量在8 mg/g左右[24],其他研究也多显示常规生产销售的红曲米中洛伐他汀含量在1.5 mg/g左右[12,25]。与CHEN等[4]类似,本研究结果提示青稞红曲中洛伐他汀含量平均达到12.5 mg/g,均显著高于红曲米的含量,甚至高于一些菌种改造后的发酵红曲米的含量[26]。研究发现红曲米中麦角甾醇含量范围约为0.1~4 mg/g[15,25],而本研究中的青稞红曲的麦角甾醇含量达到2.49~8.71 mg/g。结果提示青稞红曲的麦角甾醇含量可能显著高于红曲米,并可能和更高含量的洛伐他汀成分配合,起到更加良好的调节血脂功能。此外,由于目前尚缺少红曲米中具体β-葡聚糖含量文献报道,本文无法比较2种红曲的该成分区别,将在下一步研究中开展相关工作。
青稞是麦类作物中β-葡聚糖含量最高的作物,其基质特性显著影响红曲霉发酵效能。发酵前,不同品种青稞中均未检出酸式和内酯式洛伐他汀及麦角甾醇,但β-葡聚糖含量差异显著(P<0.05)。红曲霉在固态发酵过程中,青稞作为发酵基质,其中β-葡聚糖的含量显著降解,但蓝青稞红曲残留量(34.65~39.71 mg/g)仍最高。β-葡聚糖的降解与红曲霉在发酵过程中分泌的β-葡聚糖酶活性直接相关,该酶可水解β-1,3-糖苷键,将大分子葡聚糖转化为葡萄糖,进而可能通过甲羟戊酸途径驱动洛伐他汀合成[27-28]。蓝青稞因初始β-葡聚糖含量(62.14~72.65 mg/g)显著高于白、黑青稞,其提供的充足碳源使发酵产物中洛伐他汀产量较白、黑青稞提高60%和20%(P<0.05),验证底物碳源充足性对次级代谢产物的正向调控。此外,目前发现红曲霉中洛伐他汀合成的底物主要在线粒体中首先合成产生[29-30],而青稞中的营养成分包括β-葡聚糖、膳食纤维等物质,相比红曲米中主要的淀粉类物质,更难直接通过糖酵解的方式代谢利用,需要提高线粒体的代谢效率以利用相关碳源,从而增高洛伐他汀相关前体物质的合成,并起到提升次级代谢产物合成,提高酸式和内酯式洛伐他汀合成的代谢作用。因此,本研究推测可能是青稞特有的成分和物化性质尤其是高含量β-葡聚糖特点,导致青稞红曲在发酵代谢过程中次级代谢作用的增强,并产生更多的洛伐他汀和麦角甾醇等活性物质。
综上所述,本研究证实蓝青稞因其高β-葡聚糖含量,作为发酵基质可显著提升青稞红曲中洛伐他汀与麦角甾醇的产量。这一发现为青稞红曲的原料筛选提供了直接依据,同时提示β-葡聚糖含量可作为预测青稞红曲品质的潜在指标,此外,也构建了“原料成分-终产物含量”多维质量评价体系,为青稞红曲产业化升级提供了理论依据。
[1] XIE J J, HONG Y, GU Z B, et al.Highland barley starch:Structures, properties, and applications[J].Foods, 2023, 12(2):387.
[2] 韩昕丽, 梁丹辉.我国青稞产业经济分析[J].中国食物与营养, 2024, 30(1):14-18.
HAN X L, LIANG D H.Economic analysis of China highland barley industry in China[J].Food and Nutrition in China, 2024, 30(1):14-18.
[3] 周红, 张杰, 张文刚, 等.青海黑青稞营养及活性成分分析与评价[J].核农学报, 2021, 35(7):1609-1618.
ZHOU H, ZHANG J, ZHANG W G, et al.Analysis and evaluation of the nutritional quality and active components of Qinghai black highland barley[J].Journal of Nuclear Agricultural Sciences, 2021, 35(7):1609-1618.
[4] CHEN J, ZHENG Q, ZHENG Z X, et al.Analysis of the differences in the chemical composition of Monascus rice and highland barley monascus[J].Food Function, 2022, 13(13):7000-7019.
[5] OBADI M, SUN J, XU B.Highland barley:Chemical composition, bioactive compounds, health effects, and applications[J].Food Research International, 2021, 140:110065.
[6] 吴海毓, 郑万财, 杨希娟, 等.基于代谢组学评价青稞红曲茶功能成分及其抗氧化活性的研究[J].食品与发酵工业, 2024,50(15):155-162.
WU H Y, ZHENG W C, YANG X J, et al.Metabolomics-based evaluation of functional constituents and their antioxidant activities in highland barley Monascus tea[J].Food and Fermentation Industries, 2024, 50(15):155-162.
[7] BUZZELLI L, SEGRETI A, DI GIOIA D, et al.Alternative lipid lowering strategies:State-of-the-art review of red yeast rice[J].Fitoterapia, 2024, 172:105719.
[8] 蒋沅岐, 董玉洁, 周福军, 等.红曲的化学成分、药理作用及临床应用研究进展[J].中草药, 2021, 52(23):7379-7388.
JIANG Y Q, DONG Y J, ZHOU F J, et al.Research progress on chemical constituents, pharmacological action and clinical application of Fermentum Rubrum[J].Chinese Traditional and Herbal Drugs, 2021, 52(23):7379-7388.
[9] CICERO A F G, FOGACCI F, BANACH M.Red yeast rice for hypercholesterolemia[J].Methodist DeBakey Cardiovascular Journal, 2019, 15(3):192-199.
[10] 陈发贵, 张丹, 刘敏, 等.高效液相色谱法测定青稞红曲中内酯式和酸式洛伐他汀的含量[J].中国酿造, 2016, 35(10):162-165.
CHEN F G, ZHANG D, LIU M, et al.Content determination of lovastatin and lovastatin acid in highland barley Monascus by HPLC[J].China Brewing, 2016, 35(10):162-165.
[11] 胡久平, 鄢平, 戚珊珊, 等.发酵条件对青稞红曲中Monacolin K和β-葡聚糖的影响[J].食品与发酵工业, 2017, 43(3):134-139.
HU J P, YAN P, QI S S, et al.The effect of fermentation conditions on the production of Monacolin K and β-glucan of hullessbarley Monascus[J].Food and Fermentation Industries, 2017, 43(3):134-139.
[12] 张星星, 毛清黎, 孙俊, 等.高效液相色谱法测定红曲发酵食品中洛伐他汀的研究[J].中国酿造, 2020, 39(5):193-196.
ZHANG X X, MAO Q L, SUN J, et al.Determination of lovastatin in Monascus fermented food by HPLC[J].China Brewing, 2020, 39(5):193-196.
[13] 尹昭晔, 孔炯炜, 赵婷, 等.HPLC法测定柳蘑麦角甾醇含量[J].食用菌, 2023, 45(1):70-71;75.
YIN Z Y, KONG J W, ZHAO T, et al.Study on determination of ergosterol in Trametes hirsute by HPLC[J].Edible Fungi, 2023, 45(1):70-71;75
[14] 王晓琴, 黄秀丽, 陈月景, 等.HPLC测定真菌及其制品中麦角甾醇含量[J].农学学报, 2021, 11(4):56-61.
WANG X Q, HUANG X L, CHEN Y J, et al.Determination of ergosterol in fungi and its products by HPLC[J].Journal of Agriculture, 2021, 11(4):56-61.
[15] 李雨恒, 孙晓东, 刘润璞, 等.高效液相色谱法测定自制红曲米中麦角固醇的含量[J].中国调味品, 2019, 44(10):129-131.
LI Y H, SUN X D, LIU R P, et al.Determination of ergosterol in home-made red koji rice by high performance liquid chromatography[J].China Condiment, 2019, 44(10):129-131.
[16] 刘书余, 陈晋元, 孙清平, 等.HPLC法同时测定地顶孢霉培养物中腺苷、虫草素和麦角甾醇含量[J].扬州大学学报(农业与生命科学版), 2022, 43(6):111-117;132.
LIU S Y, CHEN J Y, SUN Q P, et al.Simultaneous determination of adenosine, cordycepin and ergosterol in Acremoniumterricola culture by HPLC[J].Journal of Yangzhou University (Agricultural and Life Science Edition), 2022, 43(6):111-117;132.
[17] 毕继全, 王希通, 陈林伟, 等.萌芽黑青稞喷干粉的主要成分测定及HPLC指纹图谱的建立[J].中国食品学报, 2022, 22(9):293-303.
BI J Q, WANG X T, CHEN L W, et al.Determination of main components in sprouting black highland barley and establishment of its HPLC fingerprint[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(9):293-303.
[18] 曹桦强, 刘琛仪, 李赛芬, 等.刚果红法定量检测酵母β-葡聚糖的方法研究[J].食品与发酵工业, 2022, 48(9):261-266.
CAO H Q, LIU C Y, LI S F, et al.Study on quantitative determination of yeast β-glucan by Congo red[J].Food and Fermentation Industries, 2022, 48(9):261-266.
[19] SUHARNA N,WULANDARI N F,YULINERY T, et al.HPLC analysis on citrinin and lovastatin and their genes expression of two selected Monascus purpureus strains[J].IOP Conference Series:Earth and Environmental Science,2019, 308(1):012068.
[20] LI J J, ZHONG X J, WANG X, et al.Polyhydroxylated sterols from Monascus purpureus-fermented rice[J].Steroids,2020, 154:108546.
[21] 杨涛, 闵康, 曾亚文, 等.青稞和普通大麦全谷物功能成分差异分析[J].西南农业学报, 2015, 28(6):2360-2362.
YANG T, MIN K, ZENG Y W, et al.Difference analysis of functional components of whole grains between hull-less barley and normal barley[J].Southwest China Journal of Agricultural Sciences, 2015, 28(6):2360-2362.
[22] 康琳, 但沁, 季成军, 等.不同品种青稞全粉品质特性[J].食品研究与开发, 2025, 46(5):72-79.
KANG L, DAN Q, JI C J, et al.Quality characteristics of whole flour of different varieties of highland barley[J].Food Research and Development, 2025, 46(5):72-79.
[23] 王倩, 童亚男, 王丽丽, 等.青海、西藏主栽青稞品种营养品质及其淀粉糊化特性[J].食品工业科技, 2025,46(1):333-342.
WANG Q, TONG Y N, WANG L L, et al.Nutritional quality and starch gelatinization characteristics of main highland barley cultivars from Qinghai and Tibet[J].Science and Technology of Food Industry, 2025,46(1):333-342.
[24] 齐方圆, 任丹, 黄紫妍, 等.16个产地红曲中洛伐他汀及桔霉素测定[J].中成药, 2021, 43(4):948-953.
QI F Y, REN D, HUANG Z Y, et al.Determination of lovastatin and citrinin in red yeast rice from sixteen growing areas[J].Chinese Traditional Patent Medicine, 2021, 43(4):948-953.
[25] 吕思敏, 张丽婷, 何小冰, 等.功能性红曲米粉中洛伐他汀和辅酶Q10等功效成分的含量测定[J].广州化工, 2019, 47(18):92-95.
LYU S M, ZHANG L T, HE X B, et al.Determination of functional ingredients such as lovastatin and coenzyme Q10 in functional red yeast rice flour[J].Guangzhou Chemical Industry, 2019, 47(18):92-95.
[26] YUAN X S, GAO S, TAN Y D, et al.Production of red yeast rice rich in monacolin K by variable temperature solid fermentation of Monascus purpureus[J].RSC Advances, 2023, 13(39):27303-27308.
[27] LU W, XU X M.Research status and application prospects of Monascus sp.[J].Agricultural Science &Technology, 2015, 16(1):192-196.
[28] 张江宁, 杨春, 张玲, 等.红曲菌发酵特性研究[J].中国调味品, 2019, 44(2):88-90.
ZHANG J N, YANG C, ZHANG L, et al.Study on the fermentation characteristics of Monascus[J].China Condiment, 2019, 44(2):88-90.
[29] WU Z Y, ZHANG C, LIU Q, et al.Combinatorial mutagenesis and fermentation optimization biotechnologies synergistically enhance monacolin K content in functional red yeast rice[J].Frontiers in Microbiology, 2025, 16:1669985.
[30] SHAO Y C, LEI M, MAO Z J, et al.Insights into Monascus biology at the genetic level[J].Applied Microbiology and Biotechnology, 2014, 98(9):3911-3922.