真菌毒素是由霉菌产生的有毒次级代谢产物,通常具有相对较小的分子质量。迄今为止,科学家已鉴定出超过500种真菌毒素,但其中对人类和动物构成危害的仅有少数[1]。常见于淀粉类食物的真菌毒素包括脱氧雪腐镰刀菌烯醇(deoxynivalenol, DON)、玉米赤霉烯酮(zearalenone, ZEA)、伏马毒素(fumonisin, FUMs)、赭曲霉毒素A(ochratoxin A, OTA)和黄曲霉毒素(aflatoxin, AFs)[2]。真菌毒素摄入造成牲畜减产甚至死亡;此外,真菌毒素直接或间接(例如,牛奶中可能含有AFs残留)地通过食物链进入人体,并对人体造成危害。真菌毒素能够引起人和畜牧牲畜的生化、生理和病理变化;在人和动物中观察到的真菌毒素的危害包括致癌性、致畸性、免疫毒性、神经毒性、肝毒性、肾毒性、生殖和发育毒性、消化不良等[3]。
膳食和饲料中的真菌毒素暴露是一个全球性问题。每年世界上大约25%的收获作物受到真菌毒素的污染[3]。伴随着食品法规的逐渐完善,我国目前鲜有发生急性食品真菌毒素中毒案例,但长期低剂量暴露于真菌毒素对于食品安全、公共卫生和农业经济仍是巨大的挑战。产毒真菌很可能在农作物生长的时候就已经存在,并受昆虫啃食、降水量、温度和仓储环境等因素影响,在作物和食品中生长并产生毒素[4]。传统食品加工过程中,脱壳、浸泡、碾磨、热处理或挤压等程序对消除真菌毒素具有一定作用,但无法完全去除食物和饲料中的真菌毒素[5]。
基于食物饲料中真菌毒素污染问题频发、危害性大以及传统农艺和食品加工工艺难以去除的特点,研发真菌毒素的脱毒和解毒办法迫在眉睫。然而,由于真菌毒素在体内危害广泛、代谢产物及掩蔽形式众多,采用传统的体外细胞实验或基于色谱的方式无法准确鉴别其毒性降低效率。例如,铝硅酸盐在体外展示出对ZEA具有良好的脱毒效果但在动物实验中无效,表明体内和体外脱毒存在差异[6]。在我国,实验动物指为实验或其他科学目的而饲养的动物。动物实验能够准确且直观地评估物质对人类、动物或环境的毒性程度,因此被广泛应用于食品安全评价和毒理学研究。目前,动物实验已在真菌毒素毒性剂量、作用机制以及环境排放污染等方面发挥重要作用。在真菌毒素的脱毒和解毒研究领域也有诸多实验采用实验动物进行成效验证和机制探究。本文将从实验动物在真菌毒素脱毒与解毒中应用的角度,综述和总结动物品种及细胞品系选择。此外,本文还将从体外脱毒效果验证和体内解毒机制探究两方面对现有研究成果进行综述。
1 体内外实验选择
1.1 体内实验相关动物选择
用实验动物进行研究是检测化学物质的重要毒性特性的最可靠手段。常用于毒理学实验的实验动物种类繁多,包括大小鼠、狗、鱼类和线虫等。有关真菌毒素脱毒与解毒的研究往往应用于畜牧生产或食品安全领域,因此除了大小鼠等常用实验动物,还包括鸡、猪、牛和羊等畜牧动物。不同物种的动物对于真菌毒素的耐受程度和代谢速率具有显著差异。以OTA为例,猪、大鼠、兔和鸡对该毒素的吸收率分别为66%、56%、56%和40%[7]。新生大鼠、小鼠、雏鸡、猪和狗对OTA的半数致死剂量(LD50)分别为3.9、46~58、10.67、1 mg/kg体重和0.2 mg/kg体重。相似地,ZEA的毒性在不同物种间也存在显著差异。在小鼠、大鼠和豚鼠中分别为2 000、4 000、5 000 mg/kg体重以上[8]。90 d亚慢性口服毒性研究中猪和大鼠的无明显作用剂量分别为40、100 μg/kg[9]。此外,不同物种对真菌毒素的代谢物也不同。例如,暴露于ZEA后,人和猪体内的代谢物α-玉米赤霉醇(α-zearalenol,α- ZOL)较高,而家禽和反刍动物β-玉米赤霉醇(β- ZOL)占优势[10]。不同代谢物间的毒性和循环中的清除效率存在差异。物种间对真菌毒素代谢的差异与其消化道结构(例如,瘤胃发酵具有一定降解真菌毒素的能力)和胆汁酸循环等多方面因素相关[11]。因此,在实验设计上应当综合考虑物种间差异及解毒技术应用前景选择实验动物品种和设计实验中真菌毒素的给药剂量。
不同品系的动物由于遗传背景差异,对毒素的耐受程度存在显著不同。例如,研究表明,二噁英的半数致死剂量在不同大鼠品系之间可相差数百至近千倍。一些大鼠品系对致癌剂的耐受性较高,在某些情况下,致癌剂的有效剂量在不同品系之间可能存在超过70%的差异[12]。因此,选用不恰当的动物品系可能会错误地评估毒性或不准确地判断安全剂量水平;并使利用不同品系动物实验间的可比性降低。以大小鼠为例,常用于毒理学研究的大鼠品系为SD大鼠和Wistar大鼠;常用于毒理学研究的小鼠品系包括ICR小鼠(瑞士小鼠的一种)和CD-1小鼠(瑞士系封闭群小鼠)。值得注意的是,真菌毒素对特殊人群的影响近年来逐渐被关注。在这些研究中可以选用容易造成某类疾病模型的动物品系。例如,在探究DON和ZEA对高脂饮食诱导肥胖群体毒性的2项研究中,研究者分别选用了较易诱导肥胖的B6C3F1杂交小鼠和C57BL/6小鼠作为实验模型[13-14]。
1.2 体外实验相关细胞系选择
此外,体外实验也可以被用来评估真菌毒素的毒性,探究机制和解毒剂对真菌毒素的解毒作用。体外实验的好处在于操作简便、可控性强、伦理成本低。常用于检测的细胞系包括肝细胞系、肠上皮细胞系、肾细胞系等。这是因为目前绝大多数真菌毒素的作用机制是通过肝脏代谢、肠道吸收以及肾脏排泄。肝脏是毒素转化的主要器官,而黄曲霉毒素B1(AFB1)被广泛认为是强烈的肝毒素之一,对肝损伤和肝细胞癌的发展有很大影响。CHEN等[15]使用人肝细胞癌细胞系HepG2检测黄曲霉毒素发现在1 μg/mL的质量浓度下毒素会短期刺激肝细胞增强能量代谢以抵御毒性应激。其他的肝细胞系例如HepaRG也经常被使用,研究发现HepaRG和HepG2在对AFB1暴露下具有相近的敏感性,但是在低剂量AFB1处理下会出现更明显的肝脏毒性反应[16]。肠道吸收中体外实验主要选择Caco-2人结肠腺癌来源的上皮细胞系。DON和ZEA都会通过肠道对人体造成影响,可通过Caco-2细胞系进行相关实验。研究指出,ZEA会对肠道造成损伤,增加肠道屏障通透性,具体体现在肠道紧密连接蛋白Occludin和Claudin-4的表达下降[17],而DON也有类似的状况。同样,猪小肠上皮细胞IPEC-J2也被用于检测ZEA体外模型实验中[18]。OTA会通过肾脏排泄,肾小管对毒素的积累和排出有重大作用。OTA通过激活人肾近曲小管上皮细胞系HK-2的相关促炎细胞因子表达和中性粒细胞浸润诱导肾毒性[19-20]。人胚胎肾细胞系HEK-293也同样被使用,但其并不具备典型肾小管上皮细胞的功能特性,反而表现出上皮样细胞特征。在一些研究中适合作为“非靶细胞系”对比肝、肾、肠等靶细胞的毒性反应差异[21]。因此,根据研究目的的不同,可以通过不同方法结合使用来探究毒素对体外细胞毒性的全面评估,以提高结果的可靠性和可解释性。尽管如此,不可否认的是,由于体外实验仅关注毒素对特定细胞类型的影响,很难构建一个关于毒素在体内的循环模型,以评估毒素的整体影响(图1)。
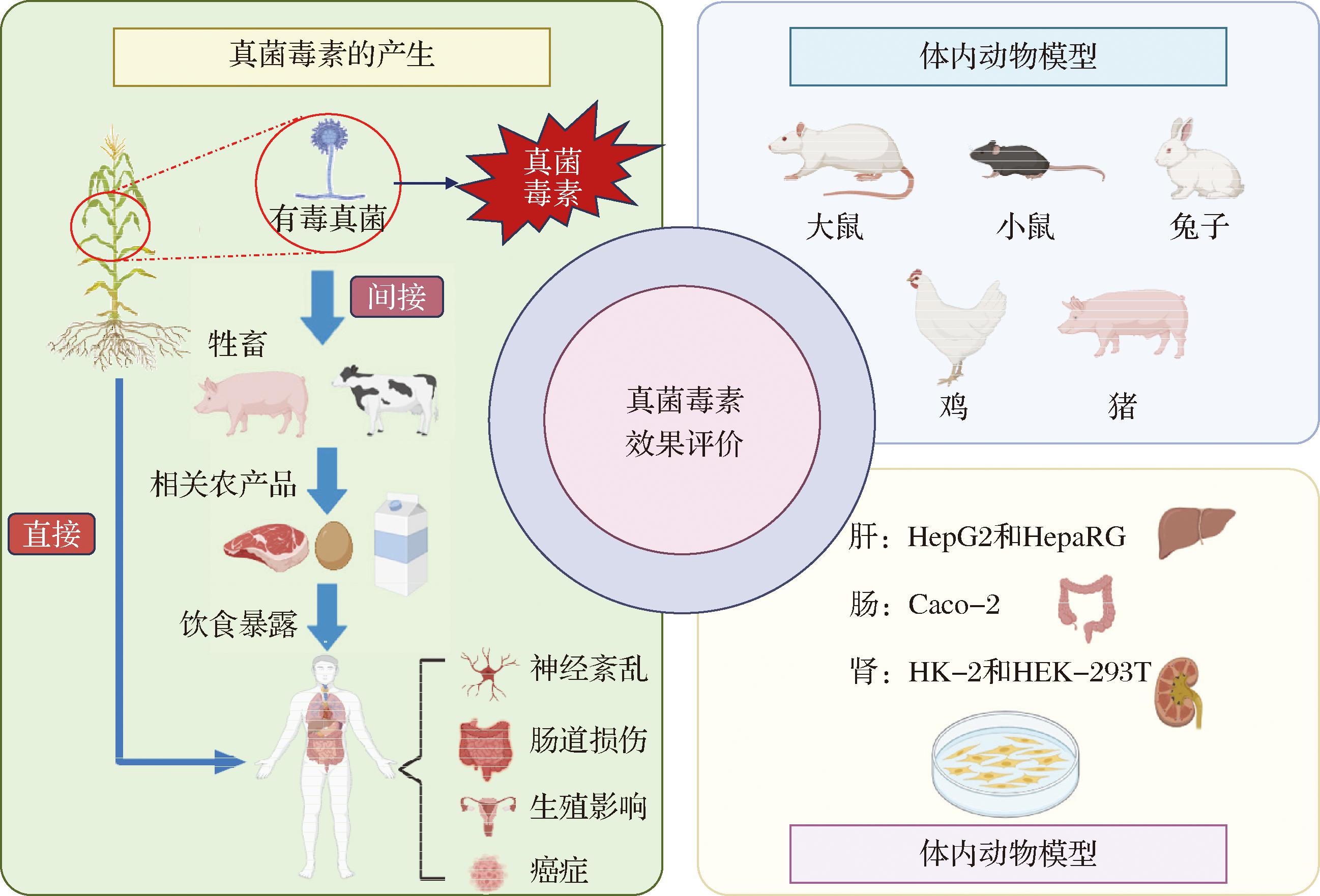
图1 真菌毒素来源与实验评价模型
Fig.1 Sources of mycotoxins and experimental evaluation models
2 通过动物实验验证体外脱毒效果
2.1 物理方法
2.1.1 吸附法
物理方面,吸附剂是当前研究较多的真菌毒素吸附和固定剂。它们将真菌毒素通过物理吸附、离子交换或氢键的作用将其结合或吸附到它们的层间空间、外表面和边缘,从而降低真菌毒素的毒害作用。沸石、磁性氧化石墨烯、磁性石墨烯、壳聚糖甚至于稻壳和榴莲皮均可以作为真菌毒素的吸附剂[22]。活性炭的多孔结构使其具有很大的比表面积,从而赋予其吸附容量大,性能稳定的特点。活性炭吸附的优点包括价格低廉,在较大范围的温度和酸碱条件下均适用,吸附速度快。然而活性炭的吸附不具有特异性,在脱毒过程中不仅会吸附真菌毒素,还会吸附各类食品营养组分,造成营养成分损失[23]。蒙脱石也是常见的用于真菌毒素脱毒的吸附剂,其特点是随温度升高,不仅能吸附黄曲霉毒素,还可以将其转化为毒性较小的其他形式。经过锰、铜等过度金属离子交换的蒙脱石或适当的热处理均能够提高AFB1转化为毒性较小化合物的效率。
在目前进行的相关动物实验中,吸附法通常被加入饲料,通过动物实验进行真菌毒素的检测。例如,一项以山羊为实验动物的研究中,在饲料中添加蒙脱石可显著降低瘤胃和乳汁中的AFs和ZEA含量,表明蒙脱石吸附了饲料中的真菌毒素[24]。然而,尽管体外实验证明活性炭对真菌毒素具有吸附作用,但是在断奶仔猪饲料中加入活性炭,无法完全有效保护它们免受伏马菌素b1的不良影响[25]。相似的,基于大鼠、牛、肉鸡、火鸡和水貂等动物开展的实验表明,经活性炭吸附的饲料中真菌毒素仍在动物体内具有毒性[26]。体内外实验的差异可能与真菌毒素的遮蔽形式或吸附剂在消化道内环境的有效性相关,并直接证明了动物实验在验证真菌毒素脱毒有效性方面的重要作用[27]。
2.1.2 热处理
热处理脱毒主要是通过高温破坏真菌毒素的分子结构,从而达到脱毒目的。利用高温脱毒是早期最常用的手段之一,其主要包括干燥、蒸煮、烘烤等。然而,部分真菌毒素具有较强耐热性,如黄曲霉素耐受温度高于235 ℃,对高温具有很强的抵抗力,因此简单的加热不能将其完全去除。有证据表明,调节pH延长加热时间似乎能提高其去除率。DON物理化学性质稳定,热处理仅能破坏其部分毒力,例如,当在pH 4.0、170 ℃处理60 min和在pH 7.0、170 ℃处理15 min条件下均只有部分DON被破坏;而当pH 10.0、120 ℃处理30 min或者170 ℃处理15 min,DON可被完全破坏[28]。
热处理操作简单,成本低,然而对于展青霉素(patulin,PAT)以及ZEA等多数耐热性强的真菌毒素,这使得传统物理热处理方法降解毒素效果较差。大部分情况下必须通过高温并结合调整pH等化学方法才能达到预期的脱毒效果,但会严重影响原材料品质。此外,新兴的物理方式包括加热、辐照、和冷等离子体在消除真菌毒素方面体现出良好潜力,但目前仍缺乏基于动物实验和细胞实验的体内外验证。
2.2 化学方法
化学脱毒可通过氧化、还原、酸碱作用或络合反应等方式破坏真菌毒素的化学结构和活性基团,从而降低毒性。例如,臭氧作为一种强氧化剂,能够降解多种真菌毒素。此外,部分真菌毒素(如ZEA、OTA、AFs)极性较强,可通过溶剂漂洗法(如丙酮、异丙醇、甲醇和乙腈等溶剂)去除,从而减少食品和饲料中的残留[29-30]。化学解毒法已被广泛应用于消除饲料中的真菌毒素。然而,体内外实验研究表明,部分化学脱毒方法可能导致食品中残留有毒化学物质(如萃取剂、氧化副产物),并造成食品营养成分的损失。例如,尽管臭氧能够有效地降低玉米粉中ZEA污染量,但其强氧化特性会改变玉米粉的过氧化值、脂肪酸谱和糊化特性[31],从而影响谷物的营养价值和风味。鼠、斑马鱼、秀丽隐杆线虫等动物实验表明,长期摄入或接触低剂量的萃取剂残留会导致生殖毒性和内分泌干扰[32];这些研究结果进一步证明了动物实验在评估真菌毒素脱毒方法安全性方面的重要作用。
2.3 生物方法
生物解毒技术是指通过微生物对食物或饲料中的霉菌进行吸附、酶解或生物转化等功能对其进行降解或清除。例如,从猪的直肠中筛选出1株乳杆菌(Lactobacillus spp.),由于其对玉米赤霉菌的细胞结构具有亲合力,通过吸附功能降低其生物利用度[33]。有研究指出,通过给25 d龄仔猪喂食经葡萄乳杆菌干酪乳酪杆菌、乳酸片球菌和戊糖片球菌发酵饲料,其肠道内的真菌毒素含量明显下降[34]。这一现象可能与其自身的代谢活性有关,也可能通过其分泌的胞外酶(如葡萄糖苷酶、脱氢酶等)对真菌毒素进行降解。值得注意的是,除了使用活性微生物,直接添加由微生物发酵产出的酶制剂也已成为生物脱毒研究的重要方向。例如,SUN等[35]研究表明,通过食品级表达体系在毕赤酵母(Pichia pastoris)中高效表达的漆酶PpLac1与AoLac2可显著降解AFB1与ZEA,其最优降解率分别达到78.51%和80.60%。此外,利用乳酸菌、酵母等细菌对畜禽养殖生产的真菌毒素(AFs、DON、OTA)具有明显的抑制作用,提高畜禽生产效率,促进畜禽健康[36]。应用真菌毒素结合剂也可显著减轻蛋鸡产蛋性能、鸡蛋品质和肝脏健康等不良效应[36]。通过动物试验,证实了微生物对真菌毒素的降解作用,揭示了从肠道中分离出的特殊微生物(如乳杆菌、双歧杆菌等)有望成为一种新型的抗真菌毒素制剂,用于饲料及食品的安全性(表1)。
表1 微生物及酶制剂在真菌毒素脱毒中的应用
Table 1 Applications of microorganisms and enzymes in mycotoxin detoxification

微生物/酶制剂解毒机制靶毒素动物实验模型参考文献乳杆菌(Lactobacillus spp.)吸附结合ZEAZEA猪、小鼠[33-34]双歧杆菌(Bifidobacterium spp.)分泌降解酶或竞争性黏附多种毒素猪[34]酵母表达漆酶PpLac1和AoLac2酶促降解ZEA, AFB1无动物实验[35]酵母细胞壁+蒙脱石复合制剂物理吸附和肠道屏障增强DON, AFB1, OTA蛋鸡[36]枯草芽孢杆菌+干酪乳酪杆菌等联合益生菌调节肠道菌群ZEA, AFB1猪[37]
3 利用实验动物探寻体内解毒机制
体内解毒旨在从分子机制和通路调控上,利用天然产物、益生菌等手段,缓解或拮抗真菌毒素的毒性作用。在动物体内,真菌毒素进入血液循环和致毒机制受到多方面因素的影响、具有复杂和多元化的调控网络。因此,在验证天然产物、益生菌和吸附剂缓解真菌毒素毒性的效果和机制不能只依靠在细胞层面上体外验证,必须通过实验动物进行体内探究。下文将从不同解毒机制的角度,分别介绍动物实验在探究真菌毒素的体内解毒方面取得的研究进展。
3.1 拮抗毒素作用靶点
真菌毒素的主要作用机制可能是修饰DNA模板,破坏转录过程,或抑制蛋白质合成中的翻译过程。在某些情况下,真菌毒素直接与酶蛋白或辅酶反应。因此,一些天然产物等小分子物质可以通过直接作用于真菌毒素的分子靶点,拮抗其毒性作用。例如,ZEA具有和动物雌激素(β雌二醇)类似的分子结构,与雌激素受体1 (estrogen receptor 1,ESR1)具有结合能力,从而发挥毒性作用。膳食补充水飞蓟素调控蛋白激酶[adenosine 5′-monophosphate (AMP)-activated protein kinase,AMPK]、3β-羟基类固醇脱氢酶(3β-hydroxysteroid dehydrogenase,HSD3B)和ESR1等基因位点,缓解ZEA在大鼠中造成的肝毒性和生殖毒性[38]。大蒜素[39]、褪黑素[40-41]和白藜芦醇[42]等多种天然产物被报道在体内具有解毒ZEA潜力。双氢青蒿素在仔猪中作通过在mRNA和蛋白水平下调TNF-α和NF-κB的表达,拮抗DON诱导的炎症增加,改善了DON对血清生化指标和炎性细胞因子水平、肝脏抗氧化能力、肝细胞凋亡和炎症反应的负面影响[43]。
此外,虽然传统毒素与新兴毒素在体内通常会发生协同作用以加强毒素毒性,但最新的研究发现,在特定的情况下,DON的毒性作用可能被镰刀菌毒素恩镰孢菌素(enniatins,ENNs)拮抗缓解。TANG等[44]的研究发现,ENNs在高浓度下可使HepG2细胞中的PI3K/Akt/FoxO通路激活,对凋亡相关基因Caspase-3、p53和Bax进行抑制,缓解DON的联合肝毒性。而YE等[45]在Caco-2模型中进一步发现ENNs在Ras/PI3K/Akt通路中起到调控作用降低活性氧(reactive oxygen species,ROS)水平和Ca2+紊乱,缓解DON导致的毒性作用。这类研究指出未来可尝试通过共暴露下的关键信号通路,探索多靶点协同拮抗解毒策略,缓解真菌毒素引发的毒性效应(图2)。
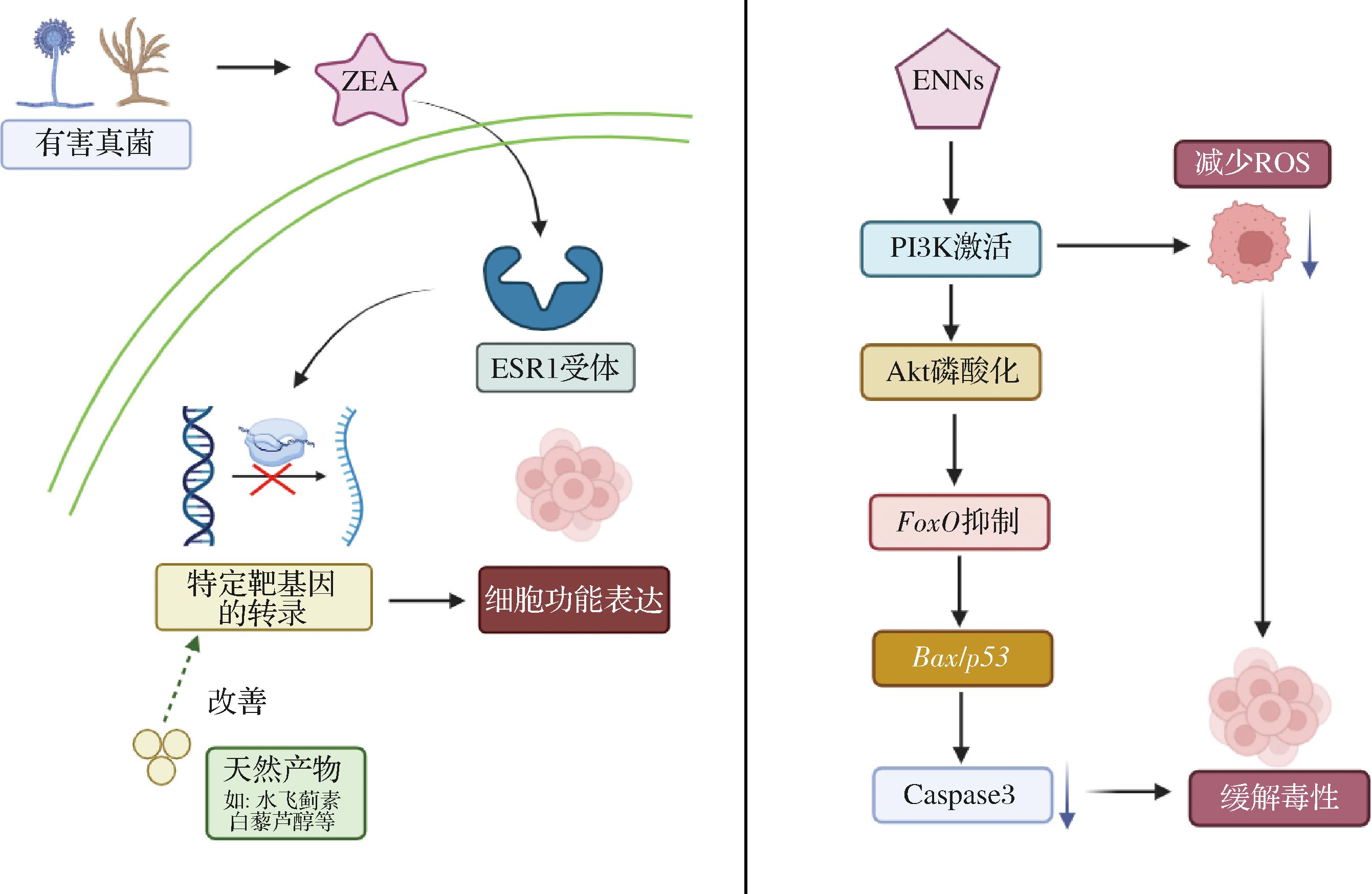
图2 拮抗毒素作用靶点与信号通路调控机制
Fig.2 Sources of mycotoxins and experimental evaluation models
3.2 缓解氧化应激
诱发氧化应激和产生ROS是真菌毒素引致细胞水平失衡,导致动物出现急性或慢性健康问题的主要原因之一。细胞由于其生理代谢或作为能够调节稳态功能的信号分子而产生ROS和活性氮(reactive nitrogen species,RNS)。真菌毒素诱导产生的自由基使体内自身调节系统失衡,从而导致活性氧过量并引发一系列破坏性影响[46]。迄今为止,通过在体内拮抗活性氧形成从而缓解真菌毒素毒性已在诸多动物实验中得到验证。N-乙酰半胱氨酸通过减少ZEA引起的氧化损伤和细胞凋亡来减轻它对猪的负面影响[47]。乳酸杆菌可减低脱氧雪腐镰刀菌烯醇对肉鸡肠道和肝脏造成的形态变化和氧化应激[48]。白藜芦醇在雄性C57BL/6 J小鼠中通过去除ROS拮抗了AFB1诱导的肝脏疾病的作用[49]。
最近的一项研究发现核受体PXR激动剂IPA可通过转录激活N6-甲基腺苷(m6A)去甲基酶FTO,降低Malat1 lncRNA的m6A修饰水平,从而减少其与NRF2的结合,解除对NRF2抗氧化转录活性的抑制,显著增强下游抗氧化酶如SOD1和CAT的表达,缓解DON诱导的肝损伤与氧化应激反应[50]。这构建了一个新型PXR-FTO-Malat1-NRF2抗氧化调控轴,展示了从表观调控、非编码RNA到抗氧化转录因子精细联动的新机制。
3.3 增强肠道屏障和菌群解毒能力
改善肠道健康是“解毒”的一个新思路。当真菌毒素从食物引入时,它们首先与胃肠道相互作用、肠屏障可作为对抗有害真菌毒素的过滤器、并且肠道菌群与胃肠道协同作用可保护宿主免受真菌毒素的有害作用[3]。一项以鸡为实验对象的研究表明,蒙脱石通过附着在肠道上对黄曲霉毒素G1(AFG1)进行吸附,增强肠黏膜内AFG1的吸附力,从而减低其在鸡体内的生物利用度并起到缓解毒性的作用[51]。联用4种益生菌,即枯草芽孢杆菌(Bacillus subtilis)、干酪乳酪杆菌(Lacticaseibacillus casei),产朊假丝酵母(Candida utilis)和米曲霉(Aspergillus oryzae),可通过缓解猪肠道炎症和细胞凋亡与ZEA的毒性拮抗[37]。褪黑素则通过恢复小鼠在OTA暴露下受损的肠道屏障功能,缓解其肝脏炎症、氧化应激和线粒体自噬[41]。
4 总结与展望
总之,真菌毒素具有分布广泛、毒性大、难以通过常规的食品加工手段有效去除的特性,对食品安全和畜牧生产造成危害。因此,在食用前通过物理、化学、生物的方法对真菌毒素脱毒;或者摄入后以拮抗毒素作用靶点、缓解氧化应激、增强肠道屏障和菌群解毒能力为机制对真菌毒素进行解毒是至关重要的。目前,虽然已有一些研究通过体外细胞培养等方式验证真菌毒素的脱毒和解毒的效果,但是由于真菌毒素结构的复杂性和代谢物的多变性以及其在人和动物体内复杂的机制网络,难以通过体外实验进行完备的评估[52]。因此,在真菌毒素的脱毒解毒方面,动物实验仍是最快捷有效的评价手段。
当前,已有大量的研究证实了多种抗真菌毒素在动物体内的脱毒和解毒效果。通过对天然产物、益生菌、小分子物质、氨基酸等生物活性成分的研究,发现天然产物、益生菌、小分子物质、氨基酸等在生物体内具有拮抗作用。但是,在活体水平上,一些具有较好的体外解毒技术(例如木炭吸附)并不能很好地消除其对机体的毒害作用,因此,动物试验在该领域的应用具有重要意义。此外,因不同种类、品种间的真菌毒素的代谢及灵敏度差别很大,很难通过试验结果进行横向对比。需要注意的是,不同物种、品系间的代谢机制差异使得试验结果难以直接横向对比,且解剖、生理、遗传背景差异也会影响动物试验映射人体的准确性。
在此背景下,真菌毒素解毒研究正逐步迈入多层级机制解析与精准调控的新阶段。未来的研究可结合毒素在多器官间的协同损伤机制,深入探讨其信号通路网络干预位点,特别是lncRNA、miRNA等非编码RNA在氧化应激和细胞凋亡调控中的作用。同时,干细胞模型、器官芯片、类器官培养等新兴体外模型,以及人工智能辅助的毒性预测、分子对接等技术手段,有望弥补传统动物实验周期长、成本高的不足,实现高通量、高精度的毒性机制研究与拮抗策略开发。
[1] 戴海蓉,梁思慧,王春民,等.同时检测食品中多种类真菌毒素的研究进展[J].中国食品学报,2022,22(8):398-415.
DAI H R, LIANG S H, WANG C M, et al.Research progress on simultaneous detection of multiple mycotoxins in food[J].Journal of Chinese Institute of Food Science and Technology, 2022,22(8):398-415.
[2] LIEW W P P, MOHD-REDZWAN S.Mycotoxin:Its impact on gut health and microbiota[J].Frontiers in Cellular and Infection Microbiology, 2018, 8:60.
[3] PLEADIN J, FRECE J, MARKOV K.Mycotoxins in food and feed[J].Advances in Food and Nutrition Research, 2019, 89:297-345.
[4] ZINGALES V, TARONCHER M, MARTINO P A, et al.Climate change and effects on molds and mycotoxins[J].Toxins, 2022, 14(7):445.
[5] AHMAD MIR S, DAR B N, AHMAD SHAH M, et al.Application of new technologies in decontamination of mycotoxins in cereal grains:Challenges, and perspectives[J].Food and Chemical Toxicology, 2021, 148:111976.
[6] AVANTAGGIATO G, GRECO D, D’ASCANIO V, et al.Advances and criticisms on the use of mycotoxin detoxifying agents[M].Mycotoxins in Food and Beverages.Boca Raton:CRC Press, 2021:122-153.
[7] YANG C, SONG G, LIM W.Effects of mycotoxin-contaminated feed on farm animals[J].Journal of Hazardous Materials, 2020, 389:122087.
[8] RAI A, DAS M, TRIPATHI A.Occurrence and toxicity of a Fusarium mycotoxin, Zearalenone[J].Critical Reviews in Food Science and Nutrition, 2020, 60(16):2710-2729.
[9] VAN DEN BRAND A D, BOKKERS B G H, TE BIESEBEEK J D, et al.Combined exposure to multiple mycotoxins:An example of using a tiered approach in a mixture risk assessment[J].Toxins, 2022, 14(5):303.
[10] TONINI C, OLIVEIRA M S, PARMEGGIANI E B, et al.Serological biomarkers of Zearalenone exposure in beef heifers receiving anti-mycotoxin additive[J].World Mycotoxin Journal, 2021, 14(3):357-366.
[11] HAN X, HUANGFU B X, XU T X, et al.Research progress of safety of Zearalenone:A review[J].Toxins, 2022, 14(6):386.
[12] BERCU J P, ZHANG S F, SOBOL Z, et al.Comparison of the transgenic rodent mutation assay, error corrected next generation duplex sequencing, and the alkaline comet assay to detect dose-related mutations following exposure to N-nitrosodiethylamine[J].Mutation Research.Genetic Toxicology and Environmental Mutagenesis, 2023, 891:503685.
[13] WANG T W, YE Y L, JI J, et al.Diet composition affects long-term Zearalenone exposure on the gut-blood-liver axis metabolic dysfunction in mice[J].Ecotoxicology and Environmental Safety, 2022, 236:113466.
[14] YUE J M, GUO D W, GAO X G, et al.Deoxynivalenol (vomitoxin)-induced anorexia is induced by the release of intestinal hormones in mice[J].Toxins, 2021, 13(8):512.
[15] CHEN X R, ABDALLAH M F, GROOTAERT C, et al.Bioenergetic status of the intestinal and hepatic cells after short term exposure to fumonisin B1 and aflatoxin B1[J].International Journal of Molecular Sciences, 2022, 23(13):6945.
[16] CHE L, HUANG J, LIN J X, et al.Aflatoxin B1 exposure triggers hepatic lipotoxicity via p53 and perilipin 2 interaction-mediated mitochondria-lipid droplet contacts:An in vitro and in vivo assessment[J].Journal of Hazardous Materials, 2023, 445:130584.
[17] ZHANG R Q, HUANGFU B X, XU T X, et al.Zearalenone enhances TSST-1 production by intestinal Staphylococcus and increases uterine immune stress in rats[J].Food and Chemical Toxicology, 2025, 196:115140.
[18] GUAN H Y, MA W X, WU Q, et al.Exploring the toxic effects of ZEA on IPEC-J2 cells from the inflammatory response and apoptosis[J].Animals, 2023, 13(17):2731.
[19] WANG S, REN H, FAN C, et al.Ochratoxin a induces renal cell ferroptosis by disrupting iron homeostasis and increasing ROS[J].Journal of Agricultural and Food Chemistry, 2024, 72(3):1734-1744.
[20] TANG J Y, ZENG J Y, CHEN L, et al.Farnesoid X receptor plays a key role in ochratoxin A-induced nephrotoxicity by targeting ferroptosis in vivo and in vitro[J].Journal of Agricultural and Food Chemistry, 2023, 71(39):14365-14378.
[21] RA I
I D, ZANDONA A, KATALINI
D, ZANDONA A, KATALINI M, et al.Assessing the potential synergistic/antagonistic effects of citrinin and cannabidiol on SH-SY5Y, HepG2, HEK293 cell lines, and human lymphocytes[J].Toxins, 2024, 16(12):534.
M, et al.Assessing the potential synergistic/antagonistic effects of citrinin and cannabidiol on SH-SY5Y, HepG2, HEK293 cell lines, and human lymphocytes[J].Toxins, 2024, 16(12):534.
[22] WU N, OU W, ZHANG Z D, et al.Recent advances in detoxification strategies for Zearalenone contamination in food and feed[J].Chinese Journal of Chemical Engineering, 2021, 30:168-177.
[23] 黄伟锋, 马传国, 陈小威, 等.吸附法消减真菌毒素的研究进展[J].食品工业科技, 2020,41(1):328-334.
HUANG W F, MA C G, CHEN X W, et al.Research progress of the elimination of mycotoxins by adsorption[J].Science and Technology of Food Industry, 2020,41(1):328-334.
[24] GOUDA G A, KHATTAB H M, ABDEL-WAHHAB M A, et al.Clay minerals as sorbents for mycotoxins in lactating goat’s diets:Intake, digestibility, blood chemistry, ruminal fermentation, milk yield and composition, and milk aflatoxin M1 content[J].Small Ruminant Research, 2019, 175:15-22.
[25] BHATTI S A, KHAN M Z, HASSAN Z U, et al.Comparative efficacy of Bentonite clay, activated charcoal and Trichosporon mycotoxinivorans in regulating the feed-to-tissue transfer of mycotoxins[J].Journal of the Science of Food and Agriculture, 2018, 98(3):884-890.
[26]  OLOVI
OLOVI R, PUVA
R, PUVA A N, CHELI F, et al.Decontamination of mycotoxin-contaminated feedstuffs and compound feed[J].Toxins, 2019, 11(11):617.
A N, CHELI F, et al.Decontamination of mycotoxin-contaminated feedstuffs and compound feed[J].Toxins, 2019, 11(11):617.
[27] KIHAL A, RODR GUEZ-PRADO M, CALSAMIGLIA S.The efficacy of mycotoxin binders to control mycotoxins in feeds and the potential risk of interactions with nutrient:A review[J].Journal of Animal Science, 2022, 100(11):skac328.
GUEZ-PRADO M, CALSAMIGLIA S.The efficacy of mycotoxin binders to control mycotoxins in feeds and the potential risk of interactions with nutrient:A review[J].Journal of Animal Science, 2022, 100(11):skac328.
[28] WOLF C E, BULLERMAN L B.Heat and pH alter the concentration of deoxynivalenol in an aqueous enviroment[J].Journal of Food Protection, 1998, 61(3):365-368.
[29] ISMAIL A, GONÇALVES B L, DE NEEFF D V, et al.Aflatoxin in foodstuffs:Occurrence and recent advances in decontamination[J].Food Research International, 2018, 113:74-85.
[30] GBASHI S, MADALA N E, DE SAEGER S, et al.Numerical optimization of temperature-time degradation of multiple mycotoxins[J].Food and Chemical Toxicology, 2019, 125:289-304.
[31] ALEXANDRE A P S, CASTANHA N, COSTA N S, et al.Ozone technology to reduce Zearalenone contamination in whole maize flour:Degradation kinetics and impact on quality[J].Journal of the Science of Food and Agriculture, 2019, 99(15):6814-6821.
[32] CHENG W L, YANG X, XUE H, et al.Reproductive toxicity of furfural acetone in Meloidogyne incognita and Caenorhabditis elegans[J].Cells, 2022, 11(3):401.
[33] VEGA M F, DIEGUEZ S N, RICCIO B, et al.Zearalenone adsorption capacity of lactic acid bacteria isolated from pigs[J].Brazilian Journal of Microbiology, 2017, 48(4):715-723.
[34] VADOPALAS L, RUZAUSKAS M, LELE V, et al.Combination of antimicrobial starters for feed fermentation:Influence on piglet feces microbiota and health and growth performance, including mycotoxin biotransformation in vivo[J].Frontiers in Veterinary Science, 2020, 7:528990.
[35] SUN Z, YOU Y X, XU H D, et al.Food-grade expression of two laccases in Pichia pastoris and study on their enzymatic degradation characteristics for mycotoxins[J].Journal of Agricultural and Food Chemistry, 2024.
[36] ZHAO L, FENG Y, WEI J T, et al.Mitigation effects of bentonite and yeast cell wall binders on AFB1, DON, and OTA induced changes in laying hen performance, egg quality, and health[J].Toxins, 2021, 13(2):156.
[37] HUANG W W, CHANG J, WANG P, et al.Effect of compound probiotics and mycotoxin degradation enzymes on alleviating cytotoxicity of swine jejunal epithelial cells induced by aflatoxin B1 and Zearalenone[J].Toxins, 2019, 11(1):12.
[38] GAO X, XIAO Z H, LIU M, et al.Dietary silymarin supplementation alleviates Zearalenone-induced hepatotoxicity and reproductive toxicity in rats[J].The Journal of Nutrition, 2018, 148(8):1209-1216.
[39] ABDEL-TAWWAB M, KHALIFA E, DIAB A M, et al.Dietary garlic and chitosan alleviated Zearalenone toxic effects on performance, immunity, and challenge of European sea bass, Dicentrarchus labrax, to Vibrio alginolyticus infection[J].Aquaculture International, 2020, 28(2):493-510.
[40] XU Y, ZHANG K H, SUN M H, et al.Protective effects of melatonin against Zearalenone toxicity on porcine embryos in vitro[J].Frontiers in Pharmacology, 2019, 10:327.
[41] ZHANG H, YAN A N, LIU X Y, et al.Melatonin ameliorates ochratoxin A induced liver inflammation, oxidative stress and mitophagy in mice involving in intestinal microbiota and restoring the intestinal barrier function[J].Journal of Hazardous Materials, 2021, 407:124489.
[42] VIRK P, AL-MUKHAIZEEM N A R, BIN MOREBAH S H, et al.Protective effect of resveratrol against toxicity induced by the mycotoxin, Zearalenone in a rat model[J].Food and Chemical Toxicology, 2020, 146:111840.
[43] LI J B, BAI Y S, MA K D, et al.Dihydroartemisinin alleviates deoxynivalenol induced liver apoptosis and inflammation in piglets[J].Ecotoxicology and Environmental Safety, 2022, 241:113811.
[44] TANG L Y, YE Y L, JI J, et al.PI3K/Akt/FoxO pathway mediates antagonistic toxicity in HepG2 cells coexposed to deoxynivalenol and enniatins[J].Journal of Agricultural and Food Chemistry, 2024, 72(14):8214-8224.
[45] YE Y L, TANG L Y, WANG J S, et al.Unexpected antagonism of deoxynivalenol and enniatins in intestinal toxicity through the Ras/PI3K/AKT signaling pathway[J].Toxicology, 2024, 508:153928.
[46] MAVROMMATIS A, GIAMOURI E, TAVRIZELOU S, et al.Impact of mycotoxins on animals’ oxidative status[J].Antioxidants, 2021, 10(2):214.
[47] CAO L, ZHAO J, XU J R, et al.N-acetylcysteine ameliorate cytotoxic injury in piglets Sertoli cells induced by Zearalenone and deoxynivalenol[J].Environmental Science and Pollution Research, 2021, 28(42):60276-60289.
[48] DE SOUZA M, BAPTISTA A A S, VALDIVIEZO M J J, et al.Lactobacillus spp.reduces morphological changes and oxidative stress induced by deoxynivalenol on the intestine and liver of broilers[J].Toxicon, 2020, 185:203-212.
[49] WU J M, GAN Z D, ZHUO R H, et al.Resveratrol attenuates aflatoxin B1-induced ROS formation and increase of m6A RNA methylation[J].Animals, 2020, 10(4):677.
[50] FENG Y, SHEN J K, LIN Z S, et al.PXR activation relieves deoxynivalenol-induced liver oxidative stress via Malat1 LncRNA m6A demethylation[J].Advanced Science, 2024, 11(25):e2308742.
[51] REJEB R, BAERE S, DEVREESE M, et al.Calcination improves the in vivo efficacy of a montmorillonite clay to bind aflatoxin G1 in broiler chickens:A toxicokinetic approach[J].Toxins, 2020, 12(10):660.
[52] ZHANG T Y, SUN X F, LI L, et al.Ochratoxin a exposure impairs porcine granulosa cell growth via the PI3K/AKT signaling pathway[J].Journal of Agricultural and Food Chemistry, 2019, 67(9):2679-2690.