“色、香、味”是食品的3个重要特性,色泽作为消费者的直接感官印象,在很大程度上决定其食欲和购买意愿[1]。食品着色剂的主要功能是赋予或改善食品色泽。不过,部分天然色素兼具生理活性功能和特殊的芳香气味,因此着色剂还具有提升食品品质和改善食品风味的功能[2]。GB 2760—2024《食品安全国家标准 食品添加剂使用标准》批准使用的食品着色剂共79种,按来源可分为合成着色剂和天然着色剂两大类。合成着色剂价格低廉,物理化学性质稳定,目前仍占据行业主导地位。然而,合成着色剂在环境中难以降解,生产过程易造成水体污染,引发环境问题[3]。此外,研究证实合成着色剂对人体健康存在潜在危害,可能引发过敏反应、结肠炎、脑损伤、癌症等疾病,引起了公众对其安全性质的广泛担忧[3]。鉴于此,日本和澳大利亚已明令禁止在食品中添加合成着色剂。
天然着色剂是指从动植物材料、微生物中提取,可赋予食品色泽的一大类色素物质。目前,GB 2760—2024《食品安全国家标准 食品添加剂使用标准》在列的天然着色剂约40种。鉴于天然着色剂大多源于自然界中的动植物和微生物资源,普遍认为具有较高的安全性。随着生活水平的提高,消费者更加注重健康安全和环保,天然着色剂的需求呈现持续增长的态势。当前,动植物和微生物材料提取仍是食品天然着色剂的主要生产方式。但是,动植物材料生长周期长,并受土地、气候制约,且原材料中色素含量低,提取工艺复杂,使得食品天然着色剂的生产面临巨大挑战。
微生物细胞结构简单、繁殖迅速,是生产天然产物的理想载体。改造微生物构建细胞工厂生产天然着色剂,不受时空和土地限制,是替代天然材料提取法,实现食品天然着色剂可持续生产的重要途径。近年来,随着代谢工程和合成生物学的迅速发展,基因表达原件逐步标准化,基因编辑、高通量筛选、酶的理性设计进化、组学技术不断更新迭代,大幅度提升了食品天然着色剂的微生物合成水平。本文聚焦微生物合成食品天然着色剂的最新研究进展,对代谢工程改造微生物合成食品天然着色剂的研究现状及其改造策略进行了梳理和总结,并对当前面临的问题和未来发展进行了合理的分析和展望,以期为食品天然着色剂生物合成研究者提供借鉴和参考,推动食品天然着色剂行业的健康和稳定发展。
1 天然着色剂特性及其合成途径
根据化学结构,食品天然着色剂大致可分为6类:黄酮类色素、类胡萝卜素、生物碱色素、聚酮类色素、蛋白类色素以及其他色素。同类天然色素具有共同前体物,因此针对某一色素的代谢工程改造策略可借鉴迁移至其他同类色素。图1为微生物中构建的各类代表性色素的生物合成代谢途径。
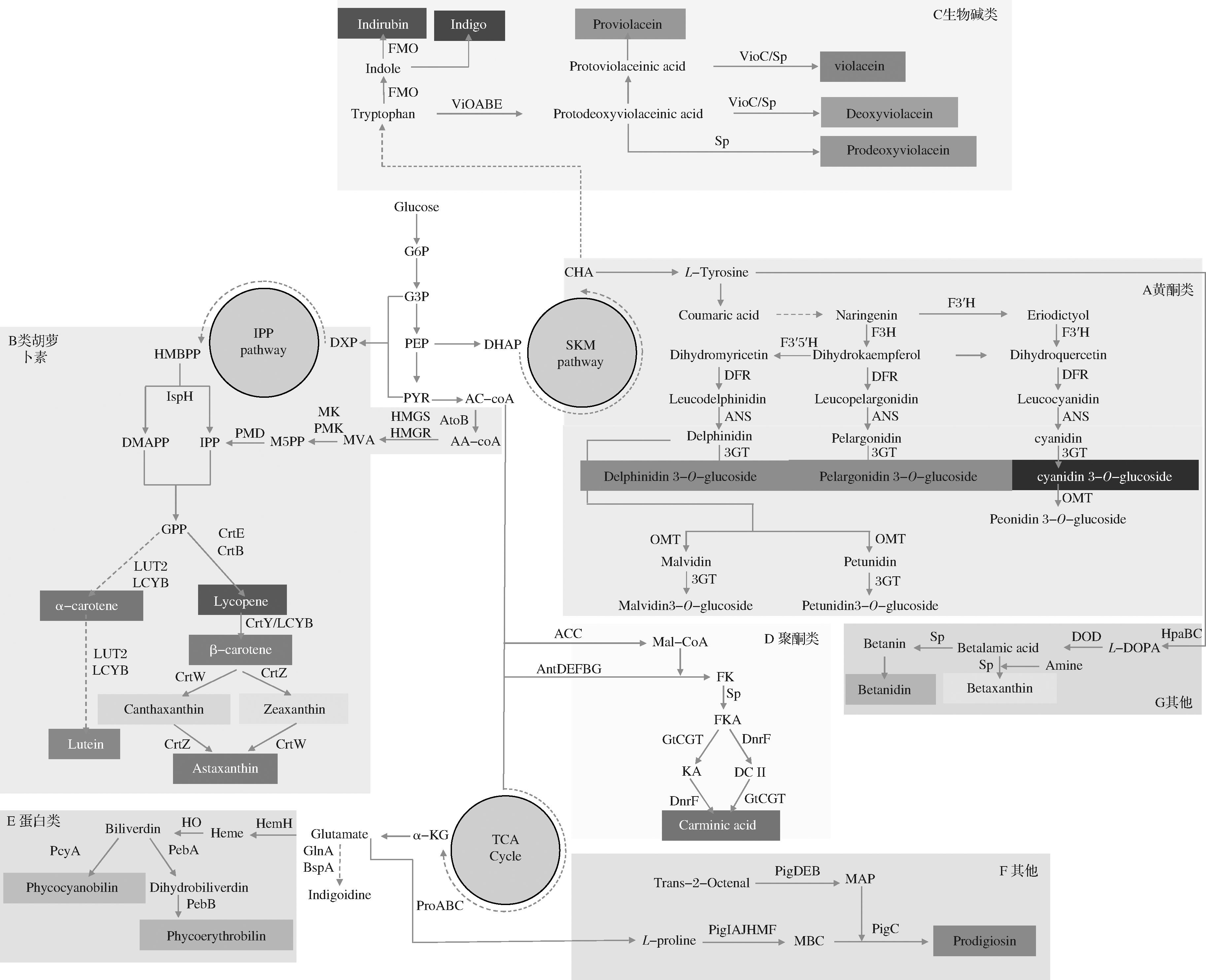
A-黄酮类;B-类胡萝卜素;C-生物碱类;D-聚酮类;E-蛋白类;F、G-其他
图1 代表性食品天然着色剂生物合成途径[4]
Fig.1 The biosynthetic pathways of the representative natural food colorants
注:α-carotene,α-胡萝卜素;β-carotene,β-胡萝卜素;amine,胺;astaxanthin,虾青素;betalamic acid,甜菜醛氨酸;betanidin,甜菜素配基;betanin,甜菜素;betaxanthin,甜菜黄素;biliverdin,胆绿素;canthaxanthin,角黄素;carminic acid,胭脂红酸;coumaric acid,香豆酸;cyanidin,矢车菊素;cyanidin 3-O-glucoside,矢车菊素-3-O-葡萄糖苷;dihydrokaempferol,香橙素;delphinidin,飞燕草素;delphinidin 3-O-glucoside,飞燕草素-3-O-葡萄糖苷;dihydrobiliverdin,二氢胆绿素;dihydromyricetin,二氢杨梅素;dihydroquercetin,二氢槲皮素;deoxyviolacein,脱氧紫色杆菌素;eriodictyol,圣草酚;glucose,葡萄糖;glutamate,谷氨酸;heme,血红素;indigo,靛蓝;indigoidine,天然蓝色素;indirubin,靛玉红;indole,吲哚;IPP pathway,异戊烯焦磷酸途径;leucocyanidin,无色矢车菊素;leucodelphinidin,无色飞燕草素;leucopelargonidin,无色天竺葵素;L-DOPA,L-多巴;L-proline,L-脯氨酸;L-tyrosine,L-酪氨酸;lutein,叶黄素;lycopene,番茄红素;malvidin,锦葵素;malvidin 3-O-glucoside,锦葵素-3-O-葡萄糖苷;naringenin,柚皮素;pelargonidin,天竺葵素;pelargonidin 3-O-glucoside,天竺葵素-3-O-葡萄糖苷;petunidin,矮牵牛素;petunidin 3-O-glucoside,矮牵牛素-3-O-葡萄糖苷;phycocyanobilin,藻蓝胆素;phycoerythrobilin,藻红胆素;prodeoxyviolacein,原脱氧紫色杆菌素;protodeoxyviolaceinic acid,原脱氧紫色杆菌酸;prodigiosin,灵菌红素;proviolacein,原紫色杆菌素;protoviolaceinic acid,原紫色杆菌酸;SKM pathway,莽草酸途径;trans-2-Octenal,反式-2-辛烯醛;TCA cycle,三羧酸循环;tryptophan,色氨酸;violacein,紫色杆菌素;zeaxanthin,玉米黄素。3GT(flavonoid 3-O-glucosyltransferase),类黄酮-3-O-葡萄糖基转移酶;5GT(5-O-glucosyltransferase),类黄酮-5-O-葡萄糖基转移酶;α-KG(α-ketoglutarate),α-酮戊二酸;AA-CoA(acetoacetyl-CoA),乙酰乙酰辅酶A;ACC(acetyl-CoA carboxylase complex),乙酰辅酶A羧化酶;Ac-CoA(acetyl-CoA),乙酰辅酶A;AntDEFBG(octaketide synthase complex),辛肽合成酶复合体;ANS(anthocyanidin synthase),花青素合成酶;AtoB(acetyl-CoA acetyltransferase),乙酰辅酶A酰基转移酶;BspA(phosphopantetheinyl transferase),磷酸泛酰巯基乙胺基转移酶;CHA(chorismate),分支酸;CrtB(phytoene synthase),八氢番茄红素合成酶;CrtE(geranylgeranyl pyrophosphate synthetase),牻牛儿基牻牛儿基焦磷酸合成酶;CrtW(β-carotene ketolase),β-胡萝卜素酮化酶;CrtY/LCYB(lycopene β-cyclase),番茄红素β-环化酶;CrtZ(β-carotene hydroxylase),β-胡萝卜素羟化酶;DAHP(3-deoxy-D-arabinoheptulosonate 7-phosphate),3-脱氧-D-阿拉伯-庚酮糖酸-7-磷酸;DFR(dihydroflavonol 4-reductase),二氢黄酮醇4-还原酶;DMAPP(dimethylallyl diphosphate),二甲烯丙基焦磷酸;DnrF(aklavinone 12-hydroxylase),阿克拉菌酮-12-羟化酶;DOD(DOPA 4,5-dioxygenase),4,5-多巴双加氧酶;DXP(1-deoxy-D-xylulose-5-phosphate),1-脱氧-D-木酮糖5-磷酸;F3H(flavanone-3-hydroxylase),黄酮烷-3-羟化酶;F3′H(flavonoid 3′-hydroxylase),类黄酮3′-羟化酶;F3′ 5′H(flavonoid 3′,5′-hydroylase),类黄酮3′ 5′-羟化酶;FK(flavokermesic acid),黄胭脂酮酸;FKA(flavokermisic acid anthrone),黄胭脂酮酸醌;FMO(flavin-containing monooxygenase),黄素单加氧酶;G3P(glyceraldehyde 3-phosphate),3-磷酸甘油醛;G6P(glucose 6-phosphate),葡萄糖-6-磷酸;GlnA(glutamine synthetase),谷氨酰胺合成酶;GPP(geranyl diphosphate),香叶基焦磷酸;GtCGT(C-glucosyltransferase),C-葡萄糖基转移酶;HMBPP(1-hydroxy-2-methyl-2-butenyl 4-diphosphate),1-羟基-2-甲基-2-丁烯基4-二磷酸;HMGR(hydroxymethylglutaryl-CoA reductase),羟甲基戊二酸单酰辅酶A还原酶;HMGS(hydroxymethylglutaryl-CoA synthase),羟甲基戊二酸单酰辅酶A合成酶;HO(heme oxygenase),血红素氧化酶;HpaBC(4-hydroxyphenylacetate 3-monooxygenase),酪氨酸羟化酶;IPP(isopentenyl diphosphate),异戊烯焦磷酸;IspH(1-hydroxy-2-methyl-2-(E)-butenyl 4-diphosphate reductase),1-羟基-2-甲基-2-(E)-丁烯基-4-焦磷酸还原酶;KA(kermesic acid),胭脂酮酸;LUT2(lycopene ε-cyclase),番茄红素ε-环化酶;M5PP(mevalonate-5-diphosphate),5-二磷酸甲羟戊酸;Mal-CoA(malonyl-CoA),丙酰辅酶A;MK(mevalonate kinase),甲羟戊酸激酶;MVA(mevalonate),甲羟戊酸;OMT(O-methyltransferase),O-甲基转移酶;PcyA(phycocyanobilin:ferredoxin oxidoreductase),藻胆蓝素:铁氧还蛋白氧化还原酶;PebA(15,16-dihydrobiliverdin:ferredoxin oxidoreductase),15,16-二羟基胆绿素:铁氧还蛋白氧化还原酶;PebB(phycoerythrobilin:ferredoxin oxidoreductase),藻胆红素:铁氧还蛋白氧化还原酶;PEP(phosphoenolpyruvate),磷酸烯醇式丙酮酸;PigA(L-prolyl-[peptidyl-carrier protein] dehydrogenase),L-脯氨酰-[肽酰载体蛋白]脱氢酶;PigB(2-acetyloctanal dehydrogenase),2-乙酰辛烯醛脱氢酶;PigC(prodigiosin/undecylprodigiosin synthetase),灵菌红素缩合酶;PigD(thiamine diphosphate dependent 2-acetyloctanal synthase),焦磷酸硫胺素依赖型3-乙酰辛烯醛合成酶;PigE(3-acetyloctanal aminotransferase),2-乙酰辛烯醛转氨酶;PigF(S-adenosyl-L-methionine-dependent methyl transferase PigF),S-腺苷甲硫氨酸依赖型甲基转移酶;PigH(4-hydroxy-2,2′-bipyrrole-5-methanol synthase),4-羟基-2,2二吡咯-5-甲醇合成酶;PigL(L-proline-[L-prolyl-carrier protein] ligase),L-脯氨酸:L-脯氨酰载体蛋白连接酶;PigJ(β-ketoacyl synthase PigJ),β-酮脂酰合成酶;PigM(putative NAD(P)H nitroreductase PigM),NAD(P)H依赖型硝基还原酶;PMD(phosphomevalonate decarboxylase),甲羟戊酸激焦磷酸脱羧酶;PMK(phosphomevalonate kinase),磷酸甲羟戊酸激酶;ProA(γ-glutamyl phosphate reductase),γ-谷氨酰磷酸还原酶;ProB(glutamate 5-kinase),谷氨酸5-激酶;ProC(pyrroline-5-carboxylate reductase),吡咯啉-5-羧酸还原酶;Sp(spontaneous),自发反应;VioA(flavin-dependent L-tryptophan oxidase),黄素依赖型L-色氨酸氧化酶;VioB(2-imino-3-(indol-3-yl)propanoate dimerase),2-亚氨基-3-(吲哚-3-基)丙酸二聚酶;VioC(violacein synthase),紫色杆菌素合酶;VioE(violacein biosynthesis enzyme),紫色杆菌素生物合成酶。
1.1 黄酮类色素
黄酮是以2-苯基苯并吡喃为母核衍生形成的一大类化合物。母核由2个酚环通过含氧杂环连接而成,其种类差异取决于杂环侧链上所连基团[5]。花青素是最主要的黄酮类色素,大多存在于植物果实和花中,其吸收光谱位于490~550 nm的可见光区,呈鲜红、紫色和粉色[6]。矢车菊素、牵牛花色素、天竺葵色素、芍药色素、锦葵色素、飞燕草色素是自然界中最常见的6种花青素。但是,天然花青素稳定性较差,易氧化,见光易分解,低pH和高温条件下易失活。研究表明,乙酰化或糖基化修饰可提高其稳定性[7]。除基本的着色功能外,花青素还具有良好的抗氧化、抗炎、抗癌等生理功效,是一种高品质的食品着色剂,在功能食品和营养保健品领域有着广泛的应用[8]。
花青素以分支酸途径代谢产物苯丙氨酸或酪氨酸为初始底物代谢合成,其合成途径可分为3个阶段(图1-A)。第一阶段,苯丙氨酸经苯丙氨酸裂解酶(phenylalanine ammonia lyase, PAL)、肉桂酸4-羟化酶(cinnamate-4-hydroxylase, C4H)、4-香豆酰辅酶A连接酶(4-coumarate CoA ligase, 4CL),或由酪氨酸经酪氨酸裂解酶(tyrosine ammonia-lyase, TAL)和4-香豆酰辅酶A连接酶相继催化生成4-香豆酰辅酶A。第二阶段,查尔酮合酶(chalcone synthase, CHS)催化4-香豆酰辅酶A与丙二酰辅酶A缩合生成查尔酮,后者在查尔酮异构酶(chalcone isomerase, CHI)、黄酮3-羟化酶(flavanone-3-hydroxylase, F3H)作用下生成香橙素。第三阶段,香橙素经类黄酮3′-羟化酶(flavonoid 3′-hydroxylase, F3′H)和类黄酮3′ 5′-羟化酶(flavonoid 3′,5′-hydroylase, F3′5′H)催化分别生成二氢槲皮素和二氢杨梅素,后者继续在二氢黄酮醇还原酶(dihydroflavonol 4-reductase, DFR)作用下生成无色花青素,即无色矢车菊素、无色天竺葵素、无色飞燕草素。无色花青素在花青素合成酶(anthocyanidin synthase, ANS)作用下生成有色花青素,即矢车菊素、天竺葵素、飞燕草素,三者经类黄酮-3-O-葡萄糖基转移酶(flavonoid 3-O-glucosyltransferase, 3GT)催化分别生成相应的糖苷——矢车菊素-3-O-葡萄糖苷、天竺葵素-3-O-葡萄糖苷、飞燕草素-3-O-葡萄糖苷。矢车菊素-3-O-葡萄糖苷经O-甲基转移酶催化后可生成芍药素-3-O-葡萄糖苷。同时,飞燕草素还可在O-甲基转移酶作用下生成锦葵素、矮牵牛素,后者经3GT催化分别生成锦葵素-3-O-葡萄糖苷、矮牵牛素-3-O-葡萄糖苷[9]。
1.2 类胡萝卜素
类胡萝卜素是一种应用广泛的脂溶性色素,属于四萜化合物。依据是否含有氧元素,可将其分为胡萝卜素(不含氧)和叶黄素类(含氧),前者包括番茄红素、α-胡萝卜素、β-胡萝卜素等,后者包括玉米黄素、虾青素、角黄素、黄体素等。天然类胡萝卜素呈现黄色、橙色至红色的不同色泽,其吸收波长为400~500 nm[10]。类胡萝卜素具有多种生理活性功能,例如,β-胡萝卜素在人体中可代谢生成维生素A与补充维生素A;此外,类胡萝卜素还具有抗氧化、抗肿瘤、预防心血管疾病等生理活性功能[11]。
如图1-B所示,类胡萝卜素的前体物为异戊烯基焦磷酸(isopentenyl diphosphate, IPP)及其异构体二甲基丙烯焦磷酸(dimethylallyl diphosphate, DMAPP),它们由糖酵解途径的中间代谢产物3-磷酸甘油醛、丙酮酸经甲羟戊酸(mevalonate, MVA)途径或2-C-甲基-D-赤藓糖醇-4-磷酸(2-C-methyl-D-erythritol-4-phosphate, MEP)途径生成,MVA途径主要存在于真核细胞的细胞质中,MEP途径大多存在于细菌及植物叶绿体内,也称为非甲羟戊酸途径[12]。在IPP异构酶作用下,IPP异构化为DMAPP,经牻牛儿基焦磷酸(geranylgeranyl diphosphate, GGPP)合成酶CrtE(GGPP synthase)催化,1分子DMAPP加上3分子IPP缩合生成GGPP。随后,2分子的GGPP经八氢番茄红素合酶(phytoene synthase, CrtB)催化缩合,生成八氢番茄红素,后者在八氢番茄红素脱氢酶(phytoene synthase, PSY)作用下连续脱氢,使共轭双键不断延长,生成番茄红素。番茄红素可在番茄红素β-环化酶(lycopene beta cyclase, CrtY/LCYB)作用下环化生成β-胡萝卜素,可在番茄红素ε-环化酶(lycopene ε-cyclase, LUT2)和LCYB作用下生成α-胡萝卜素。β-胡萝卜素经β-胡萝卜素羟化酶(β-carotene hydroxylase, CrtZ)催化可羟化形成玉米黄素,后者再经β-胡萝卜素酮化酶(β-carotene ketolase, CrtW)催化生成虾青素;此外,β-胡萝卜素还可在CrtW作用下生成角黄素,角黄素经CrtZ催化后亦可生成虾青素[13]。
1.3 生物碱色素
生物碱是自然界中广泛存在的一类含氮碱性有机化合物,大多为植物和微生物次级代谢产物。生物碱类色素通常具有复杂的环状结构,含有氧、氮原子,化学性质稳定,在不同的环境条件下仍能保持颜色和结构的稳定,但亦有部分生物碱色素在光照和高温下发生分解[14]。生物碱类色素大多具有明显的生理活性功能,如抗菌、抗氧化、抗癌、抗病毒等[15-16]。
按照最初前体物的来源,生物碱类色素可分为色氨酸衍生物(如靛蓝、紫色杆菌素、靛玉红),酪氨酸衍生物(如甜菜红)以及谷氨酸衍生物(如血红素和靛蓝素)。三羧酸循环中间产物α-酮戊二酸经谷氨酸脱氢酶、谷氨酰胺合成酶连续催化生成谷氨酰胺,随后2分子谷氨酰胺在磷酸泛酰巯基乙胺基转移酶(phosphopantetheinyl transferase, BpsA)作用下生成靛蓝素[17];同时,谷氨酸经谷氨酰-tRNA-还原酶(glutamyl-tRNA reductase, HemA)和谷氨酸-1-半醛-2,1-氨基变位酶(glutamate-1-semialdehyde 2,1-aminomutase, HemL)催化可生成血红素关键前体物——5-氨基乙酰丙酸,后者经过7步催化反应后可生成血红素[18]。色氨酸作为前体物,可在色氨酸酶α亚基(tryptophanase α subunit, tnaA)作用下生成吲哚,吲哚经黄素蛋白单加氧酶(flavin-containing monooxygenase, FMO)、细胞色素P450单加氧酶或加氧酶催化,可生成靛蓝和靛玉红[19]。同时,色氨酸可在黄素依赖性L-色氨酸氧化酶(flavin-dependent L-tryptophan oxidase, VioA)、2-亚氨基-3-(吲哚-3-基)丙酸二聚酶[2-imino-3-(indol-3-yl) propanoate dimerase, VioB]、紫色杆菌素生物合成酶(violacein biosynthesis enzyme, VioE)连续作用下,转化生成原脱氧紫色杆菌酸,后者经不同的分支代谢途径分别生成紫色杆菌素、脱氧紫色杆菌素、原脱氧紫色杆菌素、原紫色杆菌素[20]。酪氨酸经酪氨酸-3-羟化酶和多巴-4′ 5′-双加氧酶催化可生成甜菜醛氨酸,以菜醛氨酸为前体物,经2条不同的代谢途径可分别生成甜菜红素和甜菜黄素[21](图1-C)。
1.4 聚酮类色素
聚酮类化合物是一类广泛分布于植物、动物和微生物,结构多元化的次级代谢产物,由于其核心催化酶为聚酮合酶,因而称之为聚酮。常用聚酮类食品天然着色剂包括红曲色素、姜黄素、胭脂虫红等,其化学本质为含β-羰基骨架的次级代谢产物,经酰基缩合、环化及修饰形成显色结构(如芳香多烯、醌或烯酮)。依据分子发色团的电子结构特征和显色机制的不同,聚酮类色素可分为醌型、芳香型和离子型3类。醌型和芳香型聚酮色素脂溶性强,离子型聚酮色素水溶性好,醌型聚酮色素具有良好的耐酸性和光、热稳定性,适合果汁等液体酸性食品着色;芳香型聚酮亦具有良好的热稳定性和pH稳定性,可用于高温烘焙食品着色,但其发色团中的共轭多烯在光照条件下易氧化,光稳定性较差;离子型聚酮虽然光稳定性较差,并且pH耐受范围窄,但其生物活性强,如抗氧化、抗菌、抗肿瘤等,除用于食品着色外,也常用于医药和营养保健领域[22]。
聚酮类天然产物以乙酰辅酶A、丙二酰辅酶A或甲基丙二酰辅酶A为基本延伸单元,在聚酮合酶催化作用下连续缩合形成,其合成过程与脂肪酸合成过程类似[23]。聚酮合酶由数量不等的对称或非对称的二聚体模块组成,模块具有多个催化结构域,在聚酮链延伸过程中发挥不同的作用,如加载、延伸和卸载;同时,模块可通过多肽或离散的对接结构域连接形成装配线合成聚酮,模块和结构域的数量决定聚酮的化学结构和复杂程度[24]。根据聚酮合酶结构和催化机制的差异,可分为Ⅰ、Ⅱ、Ⅲ型聚酮合酶。Ⅰ型聚酮合酶通过聚酮链延伸和β-酮基修饰反应,主要合成大环内酯类和多烯类聚酮化合物,如红曲色素;Ⅱ型聚酮合酶多催化合成蒽环类芳香族聚酮,如放线紫红素;Ⅲ型聚酮合酶主要催化合成类黄酮、二苯乙烯和胭脂虫红酸(图1-D),如姜黄素[25]。
1.5 蛋白类色素
蛋白色素是指由蛋白质与非蛋白发色团共价或非共价结合形成的,具有特定颜色的复合物。食品天然着色剂中应用最为广泛的蛋白色素是藻胆蛋白,它主要存在于蓝藻、红藻等藻类生物中,其主要功能是参与光合作用,将吸收的光能传递给叶绿素。藻胆蛋白是一种水溶性强色素蛋白,含有α和β两个亚基,具有特定光吸收,依据其吸收光谱差异可分为藻红蛋白(吸收峰540~570 nm,呈红色)、藻蓝蛋白(吸收峰610~620 nm,呈蓝色)和别藻蓝蛋白(650~650 nm,呈蓝绿色)[26]。此外,藻胆蛋白还具有抗氧化、抗病毒、抗炎、抗肿瘤等生理活性功能,因此广泛应用于医药、化妆品和食品行业[27]。
藻胆蛋白的合成始于谷氨酸,谷氨酸经过系列催化反应生成血红素,在血红素加氧酶的作用下,血红素开环氧化形成胆绿素IX。胆绿素IX在不同的铁氧还蛋白依赖型胆绿素还原酶催化,分别生成发色团——藻蓝胆素、藻红胆素。最后,在不同的裂合酶,如藻胆蛋白裂合酶(chromophore lyase, CpcS/U)、藻蓝胆素裂合酶(phycocyanobilin lyase, CpcE/F),藻红胆素裂合酶(phycoerythrobilin lyase, CpeS/T)催化作用下,藻蓝胆素、藻红胆素的A环乙烯基与脱辅基蛋白半胱氨酸的巯基之间作用形成硫醚键,组装形成成熟的藻红蛋白、藻蓝蛋白、别藻红蛋白、别藻蓝蛋白[28](图1-E)。
1.6 其他色素
常用食品天然着色剂中,亦存在一些结构不符合前5类标准的着色剂,如甜菜红、灵菌红素等。灵菌红素是一种具有三吡咯环的红色素,其水溶性较差,酸性条件下显红色,吸收峰为530~550 nm,碱性条件下偏黄色,吸收峰为400~500 nm,除具有着色功能外,还具有抗癌、抗菌、抗真菌、止痛的生理活性功能[29]。
粘质沙雷氏菌(Serratia marcescens)是合成灵菌红素的主要微生物。2-甲基-3-戊基吡咯(2-methyl-3-amylpyrrole, MAP)和4-甲氧基2-,2-二吡咯-5-羧甲基乙醛(4-methoxy-2,2′-bipyrrole-5-carbaldehyde, MBC)是合成灵菌红素的直接前体物,二者在灵菌红素缩合酶(prodigiosin/undecylprodigiosin synthetase, PigC)催化作用下,缩合形成灵菌红素,因此PigC也是灵菌红素合成的关键酶。MAP的合成起源于脂肪酸氧化产物2-辛烯醛和丙酮酸,在2-乙酰辛烯醛合成酶(thiamine diphosphate dependent-3-acetyloctanal synthase PigD, PigD)催化作用下,丙酮酸发生脱羧,并将形成的2C单元转移至2-辛烯醛上,生成3-乙酰辛烷醛,随后经3-乙酰辛烯醛转氨酶(3-acetyloctanal aminotransferase, PigE)和2-乙酰辛烯醛脱氢酶(2-acetyloctanal dehydrogenase, PigB)催化生成MAP。MBC的合成则始于脯氨酸和丙酰辅酶A,经Pig基因簇中10个基因编码的酶催化,最终形成MBC(图1-F)[30]。
2 代谢工程提高食品天然着色剂产量改造策略
微生物发酵生产食品天然着色剂条件温和、经济环保、安全高效,是最具发展前景的食品天然着色剂生产方式。近年来,代谢工程和合成生物学技术飞速发展,为微生物发酵生产食品天然着色剂提供了良好的契机,研究者应用各种新技术和新策略,逐步提升了天然着色剂的发酵水平。本文对相关改造策略进行了梳理、归纳和总结,并在电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.044168)中列举了代表性天然着色剂的发酵水平。
2.1 优选底盘细胞
模式微生物遗传背景清楚,遗传操作方法成熟,是异源生产天然产物的优良底盘细胞。值得注意的是,一些非模式微生物,如解脂耶氏酵母、三孢布拉氏霉等,由于具有独特的生理特性,也常用作底盘细胞合成天然产物。因此,应当根据天然着色剂的合成途径,结合微生物的生理特性,选择合适的底盘细胞。例如,乙酰辅酶A是萜类物质合成的重要前体物,而解脂耶氏酵母的乙酰辅酶A代谢通量较高,可提供充足的乙酰辅酶A,因此常用于生产番茄红素、β-胡萝卜素、虾青素等萜类色素[31]。解脂耶氏酵母引入外源β-胡萝卜素合成途径后,通过增加β-胡萝卜合成途径关键基因拷贝数以及敲除细胞形态调控基因,成功将β-胡萝卜素产量提升至7.6 g/L[31]。同样以解脂耶氏酵母为底盘细胞,利用Rosetta和计算生物学方法模拟对茄红素环化酶CrtY进行改造,获得了1个突变体CrtYY27R,成功解除了番茄红素的底物抑制效应,继续过表达合成途径关键基因——羟甲基戊二酸单酰辅酶A还原酶(hydroxymethylglutaryl-CoA reductase, HMGR)、ERG12、异戊烯基焦磷酸异构酶(isopentenyl diphosphate delta isomerase, IDI)和法尼基焦磷酸合成酶(farnesyl diphosphate synthase, ERG20),并引入外源胆碱激酶(choline kinase, CK)和异戊烯基磷酸激酶(isopentenyl Phosphate Kinase, IPK)提高异戊醇利用效率,β-胡萝卜素产量达到39.5 g/L[32],远超模式微生物大肠杆菌3.2 g/L[33]和酿酒酵母2.06 g/L的最高发酵水平[34]。弱化解脂耶氏酵母牻牛儿基牻牛儿基焦磷酸合酶(geranylgeranyl pyrophosphate synthase, GGPPS),使碳代谢流转向番茄红素合成,联合应用系列代谢工程策略,3 L发酵罐分批补料发酵可产番茄红素17.6 g/L[32],而大肠杆菌的最高发酵水平仅为3.52 g/L[35]。
一些食品天然着色剂,如甜菜红、花青素、叶黄素等,都源自于植物或动物等真核生物,因此合成过程中需要细胞色素P450酶,但原核微生物中无等效的细胞色素P450酶,并且原核微生物中表达的外源细胞色素P450酶无法正确折叠,影响产物的合成。因此,合成这些着色剂,酿酒酵母、解脂耶氏酵母或丝状真菌等真核生物作为底盘细胞更具优势。在解脂耶氏酵母甜菜红苷工程菌中,过表达抗反馈抑制的3-脱氧-D-阿拉伯庚酮糖-7-磷酸合酶ARO4K221L和分支酸变位酶ARO7G141S,增加关键基因拷贝数,优化发酵工艺,5 L发酵罐水平可产甜菜红苷1 271 mg/L[36],而大肠杆菌甜菜红苷的最高发酵水平仅为150 mg/L[37]。
靛蓝素前体物为谷氨酸,谷氨酸代谢通量大的谷氨酸棒杆菌显然更适合生产靛蓝素。GHIFFARY等[17]以谷氨酸棒杆菌为底盘盘细胞,经过系列代谢工程改造后,5 L发酵罐分批补料发酵可产靛蓝素49.3 g/L,远高于大肠杆菌的最高发酵水平8.81 g/L[38]。
2.2 强化代谢流
确保前体物的充足供应是高效生产天然色素的前提和基础。然而,前体物往往并非底盘细胞正常生理活动所必需,代谢通量通常较低。因此,必须优化改造合成途径,提高代谢通量,确保前体的充足供应,常用的策略包括敲除竞争途径,过表达关键酶基因,解除负反馈调节,如敲除负反馈调节因子,以及引入反馈抗性酶解除负反馈等。敲除大肠杆菌靛蓝工程菌中的色氨酸合成负反馈调节因子trpR,靛蓝产量提高了12.5%,达到44.2 mg/L;随后,过表达具有抗反馈抑制特性的限速酶——3-脱氧-D-阿拉伯庚酮糖-7-磷酸合酶(3-deoxy-D-arabinoheptulosonate-7-phosphate synthase feedback resistance, AroGfbr)和邻氨基苯甲酸合酶(anthranilate synthase subunit feedback resistance, TrpEfbr),解除色氨酸的反馈抑制,靛蓝产量提高47%,达64.9 mg/L;在此基础上,过表达色氨酸合成途径的8个关键基因,靛蓝产量提高40%,达到90.8 mg/L;最后,敲除竞争途径丙酮酸脱氢酶基因(pyruvate kinase, pykAF),过表达转酮酶(transketolase 1, tktA),增加色氨酸合成的关键前体物——磷酸烯醇式丙酮酸和赤藓糖-4-磷酸的供给,靛蓝产量进一步提升至104 mg/L[39]。谷氨酸是合成靛蓝素的前体物,GHIFFARY等[17]过表达抗反馈抑制L-谷氨酰胺合成酶,解除其反馈抑制,增大了谷氨酰胺合成代谢流,靛蓝素产量由7.3 g/L提升至12.4 g/L;随后,过表达谷氨酸脱氢酶,弱化α-酮戊二酸脱氢酶,增大靶向谷氨酸的碳代谢流,最终改造的菌株5 L发酵罐分批补料发酵可产靛蓝素49.3 g/L。同样,KILDEGAARD等[40]通过截短羟甲基戊二酸单酰辅酶A(hydroxymethylglutaryl-CoA, HMG-CoA)还原酶N端跨膜结构域,解除其在翻译水平的反馈抑制,增大了β-胡萝卜素前体物IPP和DMAPP的代谢通量,使β-胡萝卜素产量提高了10.3倍;随后,通过截短角鲨烯合成酶(squalene synthase, ERG9)的启动子,下调角鲨烯竞争途径代谢通量,提高法尼基焦磷酸(farnesyl diphosphate, FPP)靶向β-胡萝卜素的代谢通量,β-胡萝卜素产量继续提升2.5倍,达797.1 mg/L。
2.3 模块工程
食品天然着色剂大多为次级代谢产物,其合成途径都较长,若外源基因与内源基因间以及上下游途径代谢流不平衡,将导致中间代谢产物积累,影响产物的合成效率。因此,可根据合成途径特点,将其分成多个独立的模块,分别在不同的质粒或不同的菌株中独立表达,并通过优化各模块表达或菌株共培养工艺,实现代谢平衡,从而促进代谢产物的合成。例如,将番茄红素合成途径分为上游甲羟戊酸途径、下游甲羟戊酸途径、番茄红素合成途径,使用3个强度不同的T7启动子突变体优化3个模块基因的表达,番茄红素产量迅速提升至107 mg/L[41]。ZHAO等[42]将大肠杆菌中构建的血红素合成途径分为2个模块,即合成前体物5-氨基乙酰丙酸的上游模块和以5-氨基乙酰丙酸为底物合成血红素的下游模块,通过优化上下游模块基因和下游模块的表达强度,将胞内血红素产量由0.1 mg/L提升至3.8 mg/L。JONES等[43]将花青素合成所需的15个外源基因按照功能分别在4株大肠杆菌中表达,并优化接种量调控表达,使天竺葵素-3-O-葡萄糖苷产量达到9.5 mg/L。采用相同的策略,RODRIGUES等[44]以阿魏酸为分节点,将姜黄素合成途径分成2个模块分别在2株大肠杆菌表达,共培养可产姜黄素43.2 μmol/L,较单菌发酵提高160%。
因此,将复杂的天然色素合成途径分成不同的模块进行调控表达或共培养可有效提高色素产量。
2.4 构建底物通道
对于由多个酶催化的级联代谢途径而言,并非编码这些酶的基因表达水平越高,产物合成效率就越高,关键是各个基因间的平衡表达,若基因表达不平衡,将导致代谢紊乱和有毒中间代谢产物的积累,影响细胞生长,进而降低产物的合成效率,这也是工程菌合成外源天然产物的一个瓶颈。底物通道则是解决这个瓶颈的关键。
底物通道是指用连接子将级联反应中各个相邻的酶连接在一起,使得上一步反应的产物直接作为底物进入下一步反应酶的活性中心,从而避免因为扩散导致酶与底物接触几率的降低而影响酶的催化效果,目前常用的底物通道技术包括蛋白支架、DNA支架、RNA支架、融合蛋白和可调基因间隔区(tunable intergenic region, TIGR)[45]。发光杆状菌(Photorhabdus luminescens)的CipB蛋白可以自发聚合形成胞内蛋白结晶包涵体,根据这一特性,将阿拉伯芥(Arabidopsis thaliana)来源番茄红素-ε-环化酶基因LUT2、β-胡萝卜素羟化酶3基因LUT5和P450还原酶基因ART2与cipB融合表达,使其自发聚合形成功能性蛋白结晶包涵体,使叶黄素产量提高2.41倍[46]。SHEN等[47]利用TIGR调控甲羟戊酸途径,提高前体物FPP的供给,玉米黄素产量提高了27.9%。Idi是类胡萝卜素上游合成途径的最后一步关键酶,催化IPP和DMAPP的转化,而CrtE则是催化类胡萝卜素下游合成途径第一步的酶,其催化类胡萝卜素前体物GGPP的合成,但是Idi在细胞质中,而CrtE则结合于膜上,因而导致IPP和DMAPP转移效率低。cAMP依赖性蛋白质激酶A的R亚基(RIDD)可与激酶锚定蛋白中的RIAD肽自组装形成蛋白纳米颗粒,将Idi与RIAD融合,CrtE与RIDD融合,二者自组装形成功能性纳米颗粒,将大肠杆菌类胡萝卜素产量提高了1.3倍,采用相同的策略,酿酒酵母番茄红素产量提高了58%,达到2.3 g/L[48]。光响应蛋白支架如FUSN-PixD、FUSN-PixE、FUSN-Cry2,可响应特定波长光,实现支架蛋白的聚集和分散,将代谢途径关键节点酶与光响应蛋白支架融合表达,可调控代谢流流向,从而实现不同产物的合成,以其调控脱氧紫色杆菌素的关键节点紫色杆菌素合酶基因(violacein synthase, vioC)和紫色杆菌素合成酶基因(violacein biosynthesis enzyme, vioE),将脱氧紫色杆菌素产量提高了6倍[49]。
2.5 提高辅因子供给
在食品天然着色剂生物合成过程中,大多需要氧化还原反应和激酶的参与。因此,通过代谢工程改造,提高还原型辅酶Ⅱ(nicotinamide adenine dinucleotide phosphate, NADPH)、三磷酸腺苷(adenosine triphosphate, ATP)等辅因子的供给,将促进食品天然着色剂的合成。大肠杆菌NADPH的来源途径主要有3条:磷酸戊糖途径、三羧酸循环和转氢酶催化还原型辅酶Ⅰ(nicotinamide adenine dinucleotide, NADH)生成NADPH。β-胡萝卜素的合成需要消耗大量的NADPH,ZHAO等[50]采用不同强度的启动子调控三羧酸循环的9个基因gltA、acnA、icd、sucAB、sucCD、sdhABCD、fumA、fumC、mdh,提升NADPH供给,结果发现均可提高β-胡萝卜素产量,sucAB、gltA和sdhABCD分别提高39%、35%和25%;继续调控磷酸戊糖途径基因tktA和talB,β-胡萝卜素产量提高16%和17%。NADH:泛醌氧化还原酶(NADH:ubiquinoneoxidoreductase, Nuo)的主要功能是形成质子电化学梯度,对于ATP的合成具有重要作用,用强启动子强化表达nuo,提高ATP的供给,使β-胡萝卜素产量提高21%。WU等[51]通过敲除NADPH消耗基因yjgB,过表达NADPH合成基因nadK,将β-胡萝卜素产量提高了34.9%,达266.24 mg/L。
2.6 高通量筛选
理性设计是提高目标产物产量的重要方法,但非理性策略同样是提升产量的重要途径,其关键在于从大规模突变文库中高通量筛选出高产菌株。食品天然着色剂具有特定颜色或荧光,且合成的色素大多积累于细胞膜或周质空间,因而菌落呈现相应的色泽,菌落颜色深浅与色素产量正相关。因此,通常策略是肉眼挑选深颜色菌落,微孔板发酵初筛,摇瓶发酵后利用HPLC等精密检测仪器测定色素产量复筛[52]。YANG等[53]构建靶向大肠杆菌全基因组的单链向导RNA(single guide RNA, sgRNA)文库,利用CRISPR干扰系统(CRISPR interference, CRISPRi)分别抑制1 858个基因的表达,挑出32个颜色较深的菌落复筛,鉴定到12个紫色杆菌素产量提高幅度超过3.5倍的靶标基因,最高产量达到5.19 g/L,这也是目前文献报道的最高水平;采用相同的策略,将靛蓝产量从108 mg/L成功提升至135 mg/L。此外,对于具有荧光特性的食品天然着色剂(如甜菜红、β-胡萝卜素、玉米黄素等),还可借助液滴微流控分选仪或流式细胞仪自动化、高通量筛选文库[54-55]。LIU等[56]借助流式细胞仪从数十万个β-胡萝卜素工程菌突变文库中筛选出16株高产菌株,其产量提升幅度达28%~166%,最优菌株5 L发酵罐分批补料发酵,β-胡萝卜素产量达9.4 g/L。
高通量筛选策略同样可用于食品天然着色剂合成酶进化文库的筛选。BIAN等[57]基于颜色深浅筛选番茄红素ε-环化酶进化文库,获得了催化效率大幅度提升的突变体mLCYEF61S,随后联合应用饱和突变和N端融合表达细胞膜锚定蛋白PMSeV-C,将α-胡萝卜素产量提高了4.9倍。ZHOU等[58]通过易错PCR构建了虾青素合成关键酶——β-胡萝卜素酮化酶和β-胡萝卜素羟化酶的共进化文库,基于菌落颜色深浅初筛和摇瓶复筛,对有益突变进行组合突变,虾青素产量提高了33%。
2.7 细胞膜工程
微生物合成的食品天然着色剂,一般亲水性天然色素分泌至培养基中,而疏水性色素则积累于周质空间或细胞膜上,有限的空间限制了疏水性色素产量的进一步提升,通过改造微生物提高细胞膜的表面积或存储空间是解决这一问题的关键。YANG等[59]通过抑制大肠杆菌的细胞分裂调控相关的基因、细胞壁合成或细胞形态维持相关基因,使大肠杆菌细胞变长变圆,增加细胞膜表面积;引入人源cavolin-1编码基因cav1形成膜内囊泡,增加胞内膜面积,抑制外膜蛋白、维持外膜/肽聚糖完整性相关和抗σ E因子编码基因,形成胞外囊泡,扩展胞外膜面积;最后,对有效基因靶点进行优化组合,最优菌的β-胡萝卜素和脱氧紫色杆菌素产量分别提高了18.4倍和10.9倍。电镜结果显示,工程菌确实变长变圆,细胞膜内外均呈现多个囊泡,增大了色素积累空间。基于相似的策略,利用CRISPRi系统抑制大肠杆菌细胞形态相关基因和膜蛋白基因,发现抑制形态维持相关mreB,pbp,ftsZ和rodZ和膜蛋白相关基因lpp、rcsF、bamB,虾青素产量提升幅度较大,对靶点进行优化组合,发现联合抑制lpp、bamB、rodZ可使虾青素产量提高53%。透射电镜检测发现,工程菌细胞变长变圆,增大了膜表面积,为虾青素积累提供了空间[60]。在β-胡萝卜素合成研究中,通过调控细胞形态和细胞膜合成相关基因,产量提高了2.9倍[61];通过构建人工囊泡运输系统,胞外β-胡萝卜素产量提高了24倍,总β-胡萝卜素产量提高了61%[62]。
尽管工程化改造微生物扩张生物膜,提升色素积累空间的策略可有效提高天然色素产量,但细胞膜表面积和周质空间扩张幅度有限,这也是疏水性天然色素普遍面临的瓶颈。因此,构建良好的转运系统,提升色素分泌至胞外培养基中的比例,将是突破这一瓶颈的关键。
2.8 优化发酵工艺
发酵条件的变化可影响基质传质效率、溶氧传递、胞内酶活力,甚至代谢方向,进而影响产物的合成。优化发酵工艺可为细胞合成产物提供合适的外部环境,从而提升产量。统计学方法是常用的发酵工艺优化策略。除此之外,还可根据产物和底盘细胞的特点优化发酵工艺。例如,两段发酵法,即将细胞生长与产物合成人为分为细胞生长和产物合成2个阶段,这种策略非常适合对底盘细胞具有毒性的天然色素的生产。紫色杆菌素抑制底盘细胞谷氨酸棒杆菌生长。在紫色杆菌素分批补料发酵过程中,前期30 ℃培养12 h,以细胞生长增殖为主,后期将发酵温度降低至20 ℃,保证外源合成酶蛋白的正确折叠,促进紫色杆菌素合成,利用这一策略,紫色杆菌素产量由1.12 g/L提升至5.44 g/L[63]。番茄红素合成后存储于细胞膜,影响细胞正常生长代谢,抑制细胞生长,进而影响番茄红素的合成。以温敏型启动子Gal4M9调控番茄红素外源合成途径,前期30 ℃培养,抑制外源途径转录,从而保证细胞充分生长;后期调整发酵温度至24 ℃,转录表达外源途径,合成番茄红素,工程菌的生物量和番茄红素产量分别提升44%和177%[64]。
此外,两相发酵工艺也可用于提升疏水性食品天然着色剂产量。两相发酵工艺是指在利用微生物发酵时,使微生物在两相(如水相和油相)中分别进行代谢反应,水相主要提供O2、营养物质和适宜的pH等环境因素,而油相则作为代谢产物的负载相,进行代谢产物的分离和纯化,从而有效解决产物在水相中不稳定,解除产物反馈抑制和对底盘细胞的毒性作用等问题,从而提升色素产量。例如,在虾青素工程大肠杆菌分批补料发酵时,添加肉豆蔻酸异丙酯为溶剂原位提取虾青素,产量较未添加时提高43%,达320 mg/L[65]。同样,番茄红素工程大肠杆菌分批补料发酵添加辛烷作为溶剂提取产物番茄红素,产量提高了98.9%,达到74.7 mg/L[66]。
3 展望
虽然合成食品着色剂价格低廉,物理化学性质稳定,但生产过程易引发环境问题,并对人体健康具有潜在危害,而食品天然着色剂则普遍认为安全,除基本着色功能外,还兼具抗氧化、抗炎、抗癌等生理活性功能。食品天然着色剂替代合成食品着色剂不仅是人们追求健康安全生活的内在需求,也是食品行业和社会发展的必然结果。然而,天然材料提取仍是当前食品天然着色剂的主要生产方式。由于原材料受土地、气候和季节影响,这一方式已无法满足日益增长的市场需求。代谢工程改造微生物生产食品天然着色剂不受时空限制,绿色安全高效,是实现食品天然着色剂可持续生产的重要途径。
本文聚焦代谢工程改造微生物促进食品天然着色剂合成的最新研究进展,对食品天然着色剂的合成途径和代谢工程改造策略进行了总结和梳理。综合分析发现,食品天然着色剂兼具有多种生理活性功能,并且微生物合成食品天然着色剂生产过程环保,改造微生物生产食品天然着色剂具有巨大的市场需求和发展潜力。对于非模式微生物来说,虽然当前测序和组学技术的发展,可以快速进行全基因组测序和基因注释,但其合成代谢调控机制仍不完全清晰,影响了非模式微生物底盘细胞的开发利用。为此,可利用进化关系相近的微生物基因组信息,通过机器学习和人工智能技术,构建基因组代谢模型,解析调控机制,促进非模式微生物底盘细胞的开发。理性设计在理论上可有效强化代谢流,但细胞代谢网络调控复杂,局部改变往往会造成整个代谢网络的扰动,影响改造效果,可通过多组学技术挖掘关键调控节点,优化代谢调控。此外,目标产物代谢通量的增加易导致中间代谢产物或目标代谢产物的积累,对细胞产生毒性作用,可采用动态调控技术减少中间代谢物积累,构建人工细胞器隔离外源途径,或将有毒产物合成途径区域化或定位到特定细胞器,不仅可减少产物毒性作用,还可将合成途径酶聚集于狭小的空间中,提高合成途径催化效率,促进产物合成。食品天然着色剂的特征颜色为高通量筛选提供了良好的基础,但仍存在假阳性、精准度差和自动化程度不高的问题,可从着色剂的光谱特征入手,如利用共聚焦拉曼光谱仪,提高筛选精度,利用微流控技术和细胞分选仪提升自动化操作。改造细胞膜可提高色素存储空间,但将色素分泌至胞外才是提高色素产量的长效机制,可构建产物转运系统或对产物进行修饰提高分泌效率。在发酵工艺优化方面,可以通过计算机模拟发酵,结合流体力学分析溶质扩散效率,以及自动化平行发酵技术优化发酵工艺。
此外,发酵过程和产物分离纯化成本较高亦是限制微生物合成食品天然着色剂市场化的主要障碍。近年来,计算生物学飞速发展,组学技术日益成熟,这为改造微生物生产食品天然着色剂奠定了良好的理论基础;得益于工程技术的迅速发展,高通量筛选方法不断更新迭代;机器学习和人工智能日新月异,且与代谢工程的交叉融合日益紧密。因此,可综合应用计算生物学方法以及组学、机器学习、人工智能、高通量筛选技术,指导构建高效微生物细胞工厂,进一步提高合成效率,从源头上降低成本。其次,以人工智能和机器人自动化为基础构建智能化发酵平台,逐步实现发酵过程的数字化、可视化,进一步优化发酵工艺过程,降低发酵过程成本。最后,借鉴现代分离技术的最新发展成果,开发廉价高效的分离纯化工艺,降低产物分离纯化成本。
从食品着色剂的发展历程来看,天然着色剂替代合成着色剂是社会发展的必然需求,综合利用代谢工程、合成生物学、人工智能、计算生物学、自动化等前沿科学技术,持续助力提升天然色素生产效率,降低生产成本,促进食品着色剂行业健康发展,将使人类健康与环境共同受益。
[1] SINGH T, PANDEY V K, DASH K K, et al.Natural bio-colorant and pigments:Sources and applications in food processing[J].Journal of Agriculture and Food Research, 2023, 12:100628.
[2] SAMANTA S, SARKAR T, CHAKRABORTY R.Multifunctional applications of natural colorants:Preservative, functional ingredient, and sports supplements[J].Biocatalysis and Agricultural Biotechnology, 2024, 56:103026.
[3] UPADHYAY D, JINDAL T, TRIPATHI A, et al.Impact of synthetic food colouring agents on aquatic ecosystems and human health[J].Uttar Pradesh Journal of Zoology, 2023, 44(13):17-37.
[4] THOMSEN P T, NIELSEN S R, BORODINA I.Recent advances in engineering microorganisms for the production of natural food colorants[J].Current Opinion in Chemical Biology, 2024, 81:102477.
[5] HWANG Y, NOH M H, JUNG G Y.Recent advancements in flavonoid production through engineering microbial systems[J].Biotechnology and Bioprocess Engineering, 2024, 29(5):792-805.
[6] SALAS E, DUE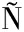 AS M, SCHWARZ M, et al.Characterization of pigments from different high speed countercurrent chromatography wine fractions[J].Journal of Agricultural and Food Chemistry, 2005, 53(11):4536-4546.
AS M, SCHWARZ M, et al.Characterization of pigments from different high speed countercurrent chromatography wine fractions[J].Journal of Agricultural and Food Chemistry, 2005, 53(11):4536-4546.
[7] ZHAO C L, YU Y Q, CHEN Z J, et al.Stability-increasing effects of anthocyanin glycosyl acylation[J].Food Chemistry, 2017, 214:119-128.
[8] PASDARAN A, ZARE M, HAMEDI A, et al.A review of the chemistry and biological activities of natural colorants, dyes, and pigments:Challenges, and opportunities for food, cosmetics, and pharmaceutical application[J].Chemistry &Biodiversity, 2023, 20(8):e202300561.
[9] TANAKA Y, OHMIYA A.Seeing is believing:Engineering anthocyanin and carotenoid biosynthetic pathways[J].Current Opinion in Biotechnology, 2008, 19(2):190-197.
[10] JOSHI K, KUMAR P, KATARIA R.Microbial carotenoid production and their potential applications as antioxidants:A current update[J].Process Biochemistry, 2023, 128:190-205.
[11] MELÉNDEZ-MART NEZ A J, MANDI
NEZ A J, MANDI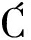 A I, BANTIS F, et al.A comprehensive review on carotenoids in foods and feeds:Status quo, applications, patents, and research needs[J].Critical Reviews in Food Science and Nutrition, 2022, 62(8):1999-2049.
A I, BANTIS F, et al.A comprehensive review on carotenoids in foods and feeds:Status quo, applications, patents, and research needs[J].Critical Reviews in Food Science and Nutrition, 2022, 62(8):1999-2049.
[12] MEGANATHAN R.Ubiquinone biosynthesis in microorganisms [J].FEMS Microbiology Letters, 2001, 203(2):131-139.
[13] EUN H, YUP L.Metabolic engineering and fermentation of microorganisms for carotenoids production[J].Current Opinion in Biotechnology, 2024, 87:103104.
[14] 王萍, 闫明哲.红甜菜色素稳定性影响因素研究进展[J].食品与生物技术学报, 2021, 40(7):19-29.
WANG P, YAN M Z.Research advances on influencing factors of betalains stability in red beet[J].Journal of Food Science and Biotechnology, 2021, 40(7):19-29.
[15] YANG L, LI X Y, HUANG W, et al.Pharmacological properties of indirubin and its derivatives[J].Biomedicine &Pharmacotherapy, 2022, 151:113112.
[16] THIRUVENGADAM M, CHUNG I M, SAMYNATHAN R, et al.A comprehensive review of beetroot (Beta vulgaris L.) bioactive components in the food and pharmaceutical industries[J].Critical Reviews in Food Science and Nutrition, 2024, 64(3):708-739.
[17] GHIFFARY M R, PRABOWO C P S, SHARMA K, et al.High-level production of the natural blue pigment indigoidine from metabolically engineered Corynebacterium glutamicum for sustainable fabric dyes [J].ACS Sustainable Chemistry &Engineering, 2021, 9(19):6613-6622.
[18] WANG S, YIN Z R, FAN Y, et al.Engineering Corynebacterium glutamicum with effective heme supply for the synthesis of high-activity hemoglobins and myoglobins[J].Journal of Agricultural and Food Chemistry, 2025, 73(24):15235-15244.
[19] KAYASTHA S, SAGWAN-BARKDOLL L, ANTEROLA A, et al.Developing synthetic microbes to produce indirubin-derivatives[J].Biocatalysis and Agricultural Biotechnology, 2021, 37:102162.
[20] 李仁瀚, 张乐乐, 刘春立, 等.基于紫色杆菌素生物合成途径的L-色氨酸生物传感器的构建[J].生物技术通报, 2023, 39(10):80-92.
LI R H, ZHANG L L, LIU C L, et al.Development of an L-tryptophan biosensor based on the violacein biosynthesis pathway[J].Biotechnology Bulletin, 2023, 39(10):80-92.
[21] 于思礼, 刘雪, 张昭宇, 等.甜菜素的生物合成及其代谢调控进展 [J].中国生物工程杂志, 2018, 38(8):84-91.
YU S L, LIU X, ZHANG Z Y, et al.Advances of betalains biosynthesis and metabolic regulation [J].China Biotechnology, 2018, 38(8):84-91.
[22] ROBERTSEN H L, MUSIOL-KROLL E M.Actinomycete-derived polyketides as a source of antibiotics and lead structures for the development of new antimicrobial drugs [J].Antibiotics, 2019, 8(4):157.
[23] ZHANG L H, HASHIMOTO T, QIN B, et al.Characterization of giant modular PKSs provides insight into genetic mechanism for structural diversification of aminopolyol polyketides[J].Angewandte Chemie International Edition, 2017, 56(7):1740-1745.
[24] 张华茜, 刘伟, 杜春梅.聚酮合酶的催化机制及聚酮类化合物的组合生物合成 [J].中国生物化学与分子生物学报, 2023, 39(3):400-412.
ZHANG H Q, LIU W, DU C M.Catalytic mechanisms of polyketide synthases and combinatorial biosynthesis of polyketides [J].Chinese Journal of Biochemistry and Molecular Biology, 2023, 39(3):400-412.
[25] NIVINA A, YUET K P, HSU J, et al.Evolution and diversity of assembly-line polyketide synthases [J].Chemical Reviews, 2019, 119(24):12524-12547.
[26] DERBEL H, ELLEUCH J, TOUNSI L, et al.Improvement of biomass and phycoerythrin production by a strain of Rhodomonas sp.isolated from the Tunisian coast of Sidi mansour[J].Biomolecules, 2022, 12(7):885.
[27] TOUNSI L, BEN HLIMA H, HENTATI F, et al.Microalgae:A promising source of bioactive phycobiliproteins[J].Marine Drugs, 2023, 21(8):440.
[28] SRIVASTAVA A, KALWANI M, CHAKDAR H, et al.Biosynthesis and biotechnological interventions for commercial production of microalgal pigments:A review[J].Bioresource Technology, 2022, 352:127071.
[29] LU Y L, LIU D R, JIANG R H, et al.Prodigiosin:Unveiling the crimson wonder - a comprehensive journey from diverse bioactivity to synthesis and yield enhancement[J].Frontiers in Microbiology, 2024, 15:1412776.
[30] 谭文章, 商俊杰, 魏云林.粘质沙雷氏菌中灵杆菌素合成因素探究进展[J].基因组学与应用生物学, 2021, 40(4):1711-1718.
TAN W Z, SHANG J J, WEI Y L.Current exploring status of factors involved in biological synthesis of prodigiosin in Serratia marcescens [J].Genomics and Applied Biology, 2021, 40(4):1711-1718.
[31] LIU M M, ZHANG J, YE J R, et al.Morphological and metabolic engineering of Yarrowia lipolytica to increase β-carotene production[J].ACS Synthetic Biology, 2021, 10(12):3551-3560.
[32] MA Y S, LIU N, GREISEN P, et al.Removal of lycopene substrate inhibition enables high carotenoid productivity in Yarrowia lipolytica[J].Nature Communications, 2022, 13:572.
[33] YANG J M, GUO L Z.Biosynthesis of β-carotene in engineered E.coli using the MEP and MVA pathways [J].Microbial Cell Factories, 2014, 13:160.
[34] LIN P, ZHANG L P, DU G C, et al.Construction of Saccharomyces cerevisiae platform strain for the biosynthesis of carotenoids and apocarotenoids[J].Journal of Agricultural and Food Chemistry, 2025, 73(15):9187-9196.
[35] SUN T, MIAO L T, LI Q Y, et al.Production of lycopene by metabolically-engineered Escherichia coli [J].Biotechnology Letters, 2014, 36(7):1515-1522.
[36] THOMSEN P T, MERAMO S, NINIVAGGI L, et al.Beet red food colourant can be produced more sustainably with engineered Yarrowia lipolytica [J].Nature Microbiology, 2023, 8(12):2290-2303.
[37] GUERRERO-RUBIO M A, L PEZ-LLORCA R, HENAREJOS-ESCUDERO P, et al.Scaled-up biotechnological production of individual betalains in a microbial system[J].Microbial Biotechnology, 2019, 12(5):993-1002.
PEZ-LLORCA R, HENAREJOS-ESCUDERO P, et al.Scaled-up biotechnological production of individual betalains in a microbial system[J].Microbial Biotechnology, 2019, 12(5):993-1002.
[38] XU F C, GAGE D, ZHAN J X.Efficient production of indigoidine in Escherichia coli[J].Journal of Industrial Microbiology &Biotechnology, 2015, 42(8):1149-1155.
[39] DU J K, YANG D, LUO Z W, et al.Metabolic engineering of Escherichia coli for the production of indirubin from glucose[J].Journal of Biotechnology, 2018, 267:19-28.
[40] KILDEGAARD K R, ADIEGO-PÉREZ B, DOMÉNECH BELDA D, et al.Engineering of Yarrowia lipolytica for production of astaxanthin[J].Synthetic and Systems Biotechnology, 2017, 2(4):287-294.
[41] ZHANG C Q, CHEN X X, LINDLEY N D, et al.A “plug-n-play” modular metabolic system for the production of apocarotenoids[J].Biotechnology and Bioengineering, 2018, 115(1):174-183.
[42] ZHAO X R, CHOI K R, LEE S Y.Metabolic engineering of Escherichia coli for secretory production of free haem [J].Nature Catalysis, 2018, 1(9):720-728.
[43] JONES J A, VERNACCHIO V R, COLLINS S M, et al.Complete biosynthesis of anthocyanins using E.coli polycultures [J].mBio, 2017,8(3):e00621-17.
[44] RODRIGUES J L, GOMES D, RODRIGUES L R.A combinatorial approach to optimize the production of curcuminoids from tyrosine in Escherichia coli [J].Frontiers in Bioengineering and Biotechnology, 2020, 8:59.
[45] PERCIVAL ZHANG Y H.Substrate channeling and enzyme complexes for biotechnological applications[J].Biotechnology Advances, 2011, 29(6):715-725.
[46] PARK S Y, EUN H, LEE M H, et al.Metabolic engineering of Escherichia coli with electron channelling for the production of natural products [J].Nature Catalysis, 2022, 5(8):726-737.
[47] SHEN H J, CHENG B Y, ZHANG Y M, et al.Dynamic control of the mevalonate pathway expression for improved zeaxanthin production in Escherichia coli and comparative proteome analysis [J].Metabolic Engineering, 2016, 38:180-190.
[48] KANG W, MA T, LIU M, et al.Modular enzyme assembly for enhanced cascade biocatalysis and metabolic flux [J].Nature Communications, 2019, 10:4248.
[49] ZHAO E M, SUEK N, WILSON M Z, et al.Light-based control of metabolic flux through assembly of synthetic organelles [J].Nature Chemical Biology, 2019, 15(6):589-597.
[50] ZHAO J, LI Q Y, SUN T, et al.Engineering central metabolic modules of Escherichia coli for improving β-carotene production[J].Metabolic Engineering, 2013, 17:42-50.
[51] WU Y Q, YAN P P, LI Y, et al.Enhancing β-carotene production in Escherichia coli by perturbing central carbon metabolism and improving the NADPH supply[J].Frontiers in Bioengineering and Biotechnology, 2020, 8:585.
[52] YUZBASHEVA E Y, TARATYNOVA M O, FEDYAEVA I M, et al.Large-scale bioproduction of natural astaxanthin in Yarrowia lipolytica [J].Bioresource Technology Reports, 2023, 21:101289.
[53] YANG D, YOO S M, GU C D, et al.Expanded synthetic small regulatory RNA expression platforms for rapid and multiplex gene expression knockdown[J].Metabolic Engineering, 2019, 54:180-190.
[54] BABAEI M, THOMSEN P T, DYEKJ☞R J D, et al.Combinatorial engineering of betalain biosynthesis pathway in yeast Saccharomyces cerevisiae[J].Biotechnology for Biofuels and Bioproducts, 2023, 16(1):128.
[55] BOWMAN E K, ALPER H S.Microdroplet-assisted screening of biomolecule production for metabolic engineering applications [J].Trends in Biotechnology, 2020, 38(7):701-714.
[56] LIU M M, ZHANG J, LIU X Q, et al.Rapid gene target tracking for enhancing β-carotene production using flow cytometry-based high-throughput screening in Yarrowia lipolytica[J].Applied and Environmental Microbiology, 2022, 88(19):e01149-22.
[57] BIAN Q, ZHOU P P, YAO Z, et al.Heterologous biosynthesis of lutein in S.cerevisiae enabled by temporospatial pathway control [J].Metabolic Engineering, 2021, 67:19-28.
[58] ZHOU P P, LI M, SHEN B, et al.Directed coevolution of β-carotene ketolase and hydroxylase and its application in temperature-regulated biosynthesis of astaxanthin [J].Journal of Agricultural and Food Chemistry, 2019, 67(4):1072-1080.
[59] YANG D, PARK S Y, LEE S Y.Production of rainbow colorants by metabolically engineered Escherichia coli[J].Advanced Science, 2021, 8(13):2100743.
[60] LU Q, LIU J Z.Enhanced astaxanthin production in Escherichia coli via morphology and oxidative stress engineering[J].Journal of Agricultural and Food Chemistry, 2019, 67(42):11703-11709.
[61] WU T, YE L J, ZHAO D D, et al.Membrane engineering - A novel strategy to enhance the production and accumulation of β-carotene in Escherichia coli[J].Metabolic Engineering, 2017, 43(Pt A):85-91.
[62] WU T, LI S W, YE L J, et al.Engineering an artificial membrane vesicle trafficking system (AMVTS) for the excretion of β-carotene in Escherichia coli[J].ACS Synthetic Biology, 2019, 8(5):1037-1046.
[63] SUN H N, ZHAO D D, XIONG B, et al.Engineering Corynebacterium glutamicum for violacein hyper production[J].Microbial Cell Factories, 2016, 15(1):148.
[64] ZHOU P P, XIE W P, YAO Z, et al.Development of a temperature-responsive yeast cell factory using engineered Gal4 as a protein switch[J].Biotechnology and Bioengineering, 2018, 115(5):1321-1330.
[65] ZHANG C Q, SEOW V Y, CHEN X X, et al.Multidimensional heuristic process for high-yield production of astaxanthin and fragrance molecules in Escherichia coli [J].Nature Communications, 2018, 9:1858.
[66] GALLEGO-JARA J, DE DIEGO T, DEL REAL  , et al.Lycopene overproduction and in situ extraction in organic-aqueous culture systems using a metabolically engineered Escherichia coli[J].AMB Express, 2015, 5(1):65.
, et al.Lycopene overproduction and in situ extraction in organic-aqueous culture systems using a metabolically engineered Escherichia coli[J].AMB Express, 2015, 5(1):65.