癌症作为全球面临的重大健康挑战之一,2022年全球有近2 000万新发癌症病例和近1 000万癌症死亡病例,预计到2050年,每年的癌症人数将达到3 500万[1]。随着癌症发病率的逐年攀升及消费者对食品天然化、功能化需求的日益增长,开发兼具疾病防治的天然活性成分成为跨学科研究的热点。天然黄酮属于多酚类化合物,主要存在于膳食植物和药用植物中,因其多靶点、低毒性和广泛的生物活性,在抗癌药物研发中备受关注。各种体外和体内研究表明,天然类黄酮具有多种抗癌作用[2]。
牡荆素作为一种C-糖苷化黄酮,广泛存在于山楂、绿豆、西番莲和小麦叶[3]等植物中。其多元化的生物活性已通过现代药理学研究得到系统验证,包括抗氧化、抗炎、神经保护、抗菌、抗癌及调节脂代谢等作用[4]。值得注意的是,其抗癌活性因多靶点调控特性成为近年研究热点,已在乳腺癌[5]、肝癌[6]及结直肠癌等模型中展现出显著抗癌疗效。然而,牡荆素的水溶性差、稳定性低,生物利用度不高,严重限制其在食品和医药领域的应用。目前,为提高牡荆素的应用性,研究者们积极探索稳态化递送系统,如使用纳米乳液[7]、纳米颗粒[8]、磷脂复合物、脂质体[9]以及外泌体[10]等,以提高其生物利用度和靶向功能,推动其在功能性食品开发中的应用。尤其是在当前消费者对天然、安全食品成分需求日益增长的背景下,牡荆素在精准营养领域具有广阔的应用前景。本综述旨在梳理牡荆素的抗癌机制、吸收代谢、稳态化递送形式及其在食品领域中的应用。通过对现有研究的总结和分析,为进一步开发牡荆素作为抗癌药物和功能性食品成分提供理论基础。表1展示了牡荆素的理化结构及其主要性质。
表1 牡荆素的理化结构及其主要性质
Table 1 Physicochemical structure and main properties of vitexin
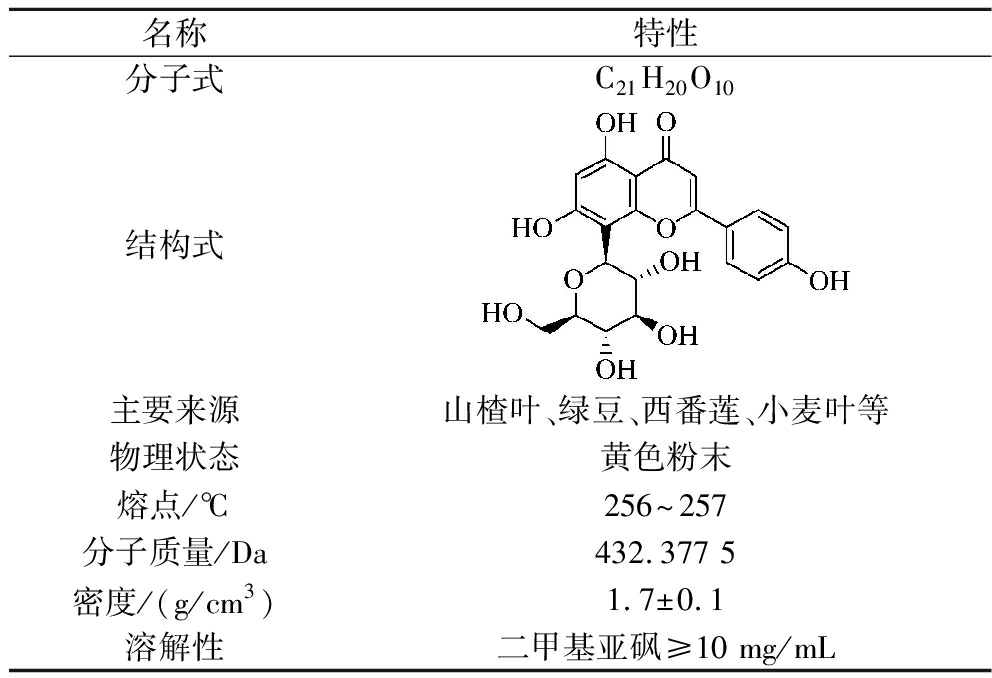
名称特性分子式C21H20O10结构式主要来源山楂叶、绿豆、西番莲、小麦叶等物理状态黄色粉末熔点/℃256~257分子质量/Da432.377 5密度/(g/cm3)1.7±0.1溶解性二甲基亚砜≥10 mg/mL
1 牡荆素的抗癌活性及其机制
恶性肿瘤(即癌症)是全球范围内导致死亡的主要原因之一,大量研究表明,天然多酚物质具有抗肿瘤活性,在癌症治疗中副作用小,安全性高。其中,牡荆素作为黄酮类化合物具有较好的抑制肿瘤生长作用,包括结直肠癌、乳腺癌、口腔癌、肝癌等。ZHANG等[11]从谷糠中提取出由12种化合物组成的总多酚,结合分子对接、MTT筛选和结合体内模型发现牡荆素和丁香酸是抑制乳腺癌的主要活性成分。此外,牡荆素可以通过诱导癌细胞凋亡、抗肿瘤血管生成、抑制肿瘤迁移和侵袭,以及自噬作用增强抗肿瘤作用(图1)。目前也有不少研究将牡荆素和不同的药物结合以实现协同抗癌作用,如CHEN等[12]将牡荆素与阿司匹林联合治疗以实现结肠癌治疗。
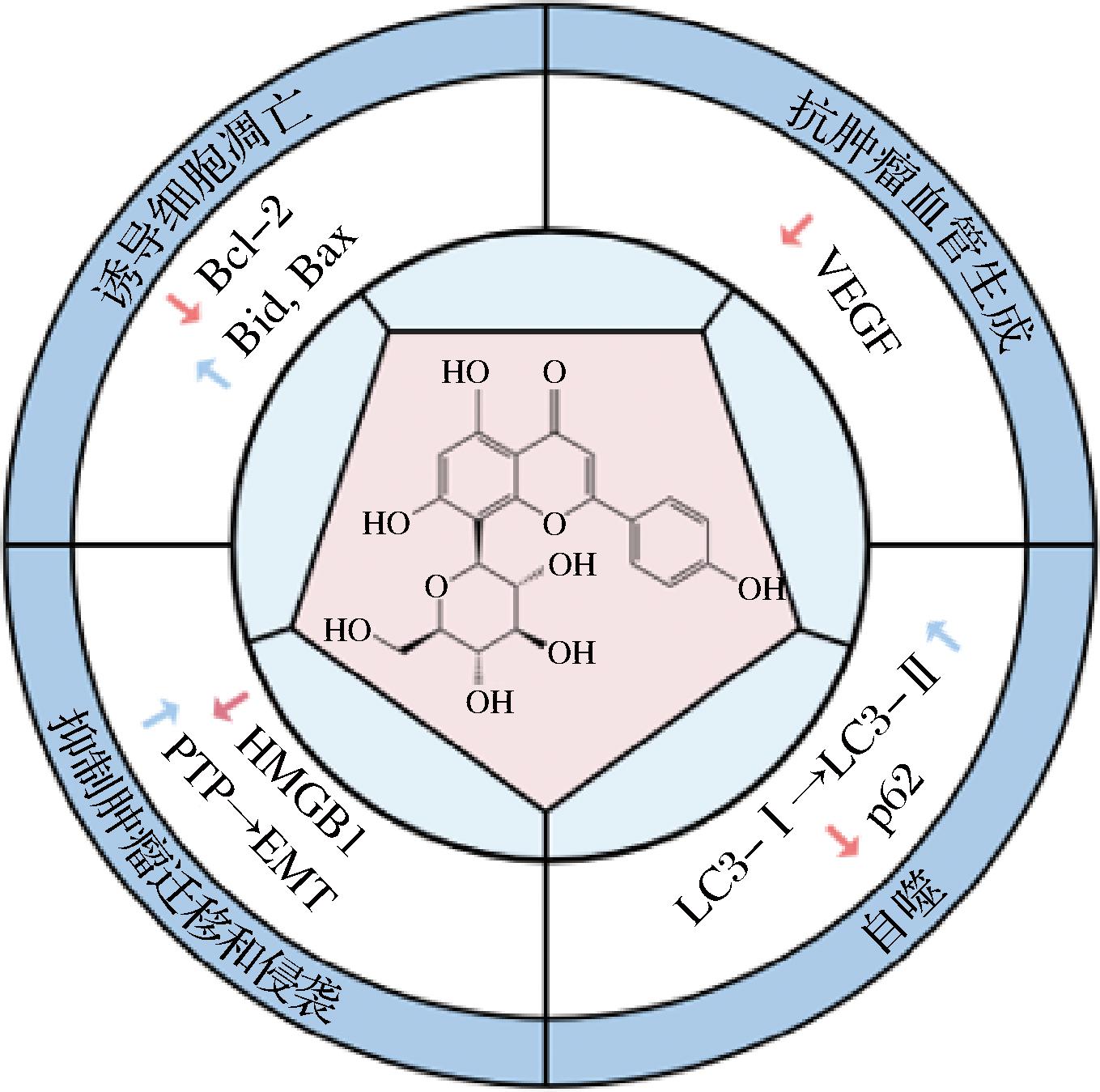
图1 牡荆素主要抗癌活性作用
Fig.1 Major anticancer effects of vitexin
注:红色箭头代表下调,蓝色箭头代表上调。Bcl-2,B淋巴细胞瘤-2;Bid、Bax,促凋亡蛋白;VEGF,血管内皮生长因子;HMGB1,高迁移率族蛋白 B1;PTP,蛋白酪氨酸磷酸酶;EMT,上皮-间质转化;LC3,酵母自噬相关蛋白;p62,自噬受体蛋白。
1.1 牡荆素抗肿瘤作用及机制
1.1.1 诱导细胞凋亡
细胞凋亡作为一种程序性细胞死亡机制,对癌症治疗至关重要。主要包括内源性途径(线粒体途径)和外源性途径(死亡受体途径)。内源性途径通过线粒体释放细胞色素c,激活半胱天冬酶(Caspase)级联反应,其调控核心在于B淋巴细胞瘤-2(B-cell lymphoma-2, Bcl-2)家族蛋白的平衡。然而,外源性途径通过死亡配体(如FasL)触发Caspase的激活,并通过tBID蛋白与线粒体途径协同促进凋亡。
牡荆素主要通过激活Caspase-3/Caspase-9级联反应,上调促凋亡蛋白Bax表达,同时下调抗凋亡蛋白Bcl-2水平,诱导乳腺癌(MA782、MCF-7、T47D、MDA-MB-435 s)、PC-3前列腺、HepG2肝癌及HeLa宫颈肿瘤细胞的程序性死亡[13]。值得注意的是,在人组织细胞淋巴瘤U937细胞模型中,牡荆素处理组同样观察到Bcl-2蛋白水平显著降低,并伴随Caspase-3/Caspase-9活化程度的剂量依赖性增强[14]。此外,牡荆素还可作为治疗食管癌治疗剂,通过上调抑癌蛋白p53并下调Bcl-2,诱导细胞凋亡。如表2所示,牡荆素诱导细胞凋亡过程主要是由Bcl-2/Bax比例的降低及Caspase激活介导。另一方面,牡荆素通过多通路协同机制发挥广谱抗肿瘤作用,包括:1)调控PI3K/AKT-Nrf2通路抑制膀胱尿路上皮癌的恶性增殖,诱导细胞凋亡[15];2)通过抑制 PI3K/AKT/mTOR通路,诱导非小细胞肺癌A549细胞凋亡[16],激活胃癌细胞自噬进程从而诱导凋亡[17];3)通过JNK、p53、STAT3和JAK/STAT3等信号通路来调控细胞凋亡。
表2 牡荆素对不同癌细胞的细胞凋亡作用及主要机制
Table 2 Apoptotic effect and mechanism of vitexin on different cancer cells

癌症类型细胞类型机制信号通路文献乳腺癌MA7824T1激活Caspase,上调Bax,下调Bcl-2激活iNOS巨噬细胞,增加全身性CD3+CD8+T细胞和CD45、CD8细胞—[13][18]肺癌A549H1975上调Bax和Caspase-3,下调Bcl-2上调Bax,下调Bcl-2,Beclin-1和LC3-II水平升高PI3K/AKT/mTORJNK[16][19]胃癌GCp-PI3K、p-AKT和p-mTOR表达显著降低PI3K/AKT/mTOR[17]肝癌SK-Hep1、Hepa1-6HepG2、Hep3B、HCCLM3 和 PLC/PRF5激活Caspase-3,下调Bcl-2激活Caspase-3,上调Bax,下调Bcl-2JNK STAT3[6][20]口腔癌OC2上调p53、p21和Baxp53[21]食管癌EC-109上调p53,下调Bcl-2—[22]胶质母细胞瘤U251p-JAK1、p-JAK3和p-STAT3蛋白表达降低JAK/STAT3[23]
注:—代表无相关信息。
1.1.2 抗肿瘤血管生成
肿瘤的发生和转移依赖于新生血管的形成,因此抑制肿瘤血管生成是治疗癌症的重要策略。血管内皮生长因子(vascular endothelial growth factor, VEGF)是关键驱动因子,通过与受体VEGFR-2结合,诱导内皮细胞增殖、迁移和存活。许多的天然产物,包括牡荆素,可以通过不同的机制来抑制肿瘤血管的生成:抑制PI3K/AKT通路,显著下调VEGFA和FGF2表达水平,进而抑制子宫内膜癌细胞增殖及血管生成。而且抑制VEGFA/VEGFR2信号传导减少宫颈癌的细胞增殖、迁移、侵袭和血管生成[24]。此外,靶向Akt/FOXO3a通路降低VEGF表达,从而抑制肝癌细胞增殖与血管生成[25]。同时,热休克蛋白Hsp90会通过多种途径促进肿瘤血管生成和转移。因此,牡荆素有潜力靶向Hsp90从而抑制肿瘤血管生成。
1.1.3 抑制肿瘤迁移和侵袭
牡荆素不仅可抑制肿瘤血管生成,还可抑制肿瘤迁移和侵袭。肿瘤转移的抑制主要依赖于阻碍上皮间质转化(epithelial-mesenchymal transition, EMT)进程,包括上皮细胞标志物的上调和间充质细胞标志物的下调。在人胃腺癌细胞系AGS(CRL-1739)的研究中,牡荆素显著增加了E-钙黏蛋白(E-cadherin, E-CAD)的表达,并以剂量依赖性降低E-CAD、基质金属蛋白酶MMP9和MMP2水平来抑制胃癌细胞的迁移、侵袭和EMT[26]。此外,STAT3信号通路的异常激活驱动肝癌细胞恶性进展,而牡荆素通过蛋白酪氨酸磷酸酶依赖的STAT3去磷酸化及DNA结合抑制,直接阻断其转录活性,同时,牡荆素拮抗CXCL12的促转移功能,进一步抑制肝癌细胞侵袭,证实其作为STAT3/CXCL12双靶点抑制剂的治疗潜力[27]。
1.1.4 自噬
自噬作为细胞进化保守的自我降解机制,在肿瘤生物学中呈现双重调控特性,早期抑制肿瘤发生与转移,晚期则维持癌细胞代谢稳态。目前,研究发现自噬与凋亡通路通过关键蛋白复合物(如Beclin1-Bcl-2、UVRAG-Bif-1及ATG12-Mcl-1)形成动态互作网络。其中,微观相关蛋白轻链3(microtubule-associated protein light chain 3, LC3)是自噬的特异性标志物,而LC3-I向LC3-II的转化过程是监测自噬活性的重要指标[27]。除此之外,牡荆素在结肠癌细胞(HCT-116)中通过双重机制抑制肿瘤生长:一方面通过剂量依赖性下调自噬相关蛋白家族及Beclin-1表达,抑制LC3-I向LC3-II的转化,阻断自噬通量;另一方面激活Caspase级联调控Bcl-2家族蛋白,形成自噬抑制与凋亡激活的协同效应[28]。此外,用天然木脂素牡荆素6处理的14种不同肿瘤细胞系中JNK磷酸化触发自噬标志物(Beclin-1/LC3-II),并上调了p-Bcl-2和p-C-Jun的表达,抑制癌细胞增殖[19]。
1.2 牡荆素在体内的吸收和代谢
牡荆素在体内吸收代谢特性与独特的C-葡萄糖苷结构密切相关。经口服后,C-糖苷键的特殊稳定性使其对消化道酸性环境及消化酶具有显著抗性,导致其在小肠段的吸收效率较低。未被吸收的牡荆素主要转运至结肠区域,在此处经历肠道菌群介导的双重生物转化:一方面通过特异性β-葡萄糖苷酶催化实现糖基水解生成苷元芹菜素。另一方面,经杂环C环的氧化开环反应代谢为原儿茶酸等低分子质量酚酸类产物[29](图2)。除此之外,静脉注射牡荆素到大鼠体内后,肝肾对牡荆素具有很高的摄取率[30]。吸收后的牡荆素及其代谢产物在肝脏经历Ⅰ期代谢途径(氧化、还原、甲基化、CH2O损失和CO损失)和Ⅱ期代谢途径(乙酰化、谷氨酰胺共轭和葡萄糖醛酸共轭),生成水溶性代谢物(如牡荆素葡萄糖醛酸苷),最终通过肾脏(尿液)和胆汁(粪便)排泄[31]。然而,牡荆素的低生物利用受限于首过效应和肠道代谢效率,其药效可能源于原型药与代谢产物的协同作用,未来可优化通过递送系统联合调控肠道菌群策略以提升其生物利用度与靶向性。
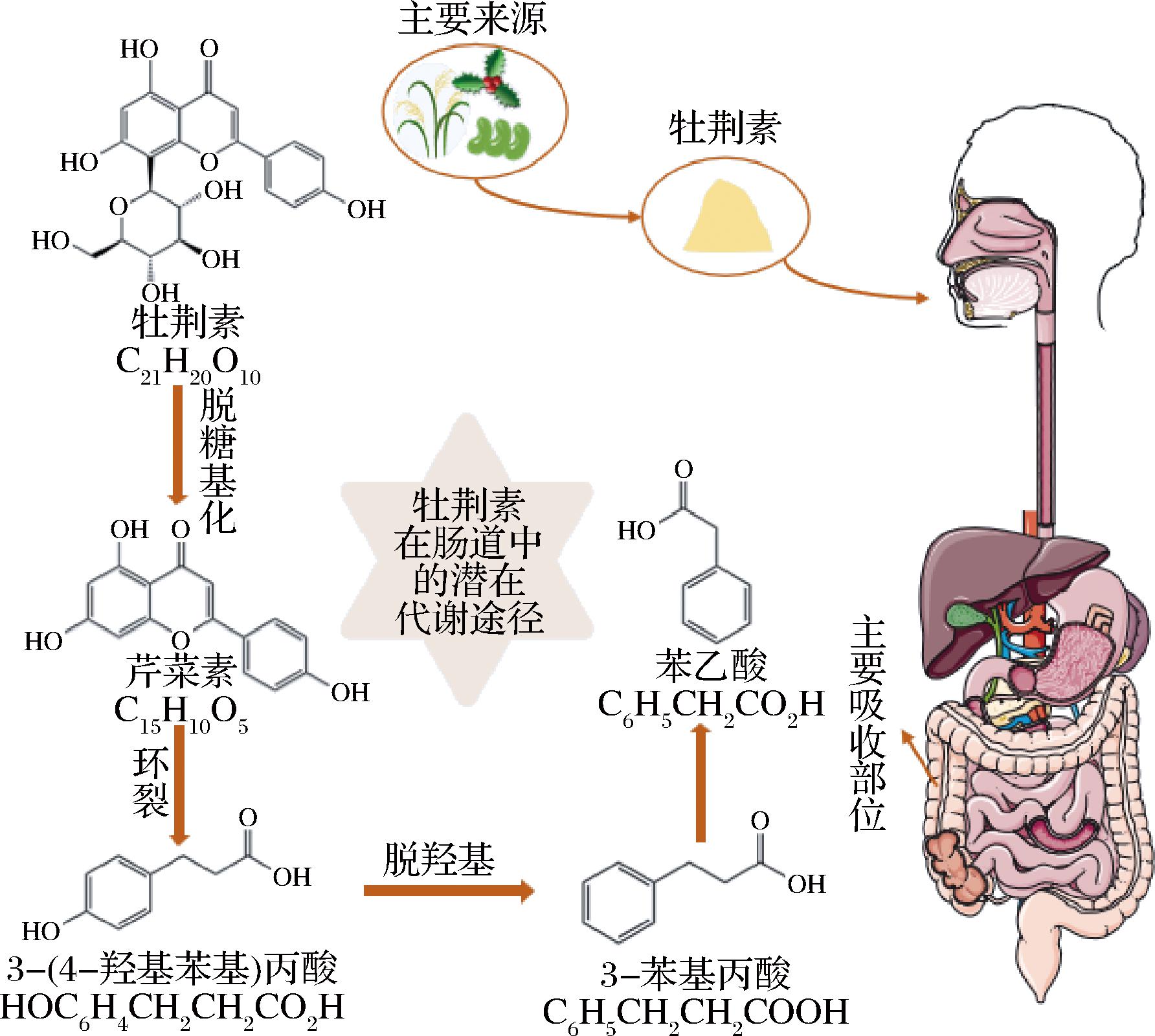
图2 牡荆素在人体内潜在的吸收代谢途径
Fig.2 Potential absorption and metabolism pathways of vitexin in human body
2 牡荆素稳态化递送及其发展
由于牡荆素水溶性差、肠道通透性差,口服生物利用度有限,牡荆素的利用受到限制。为提高牡荆素生物活性、溶解度、稳定性以及靶向性,开发稳态化牡荆素递送系统已成为重要解决策略。目前,牡荆素的递送形式主要有纳米乳剂、纳米颗粒、磷脂复合物以及脂质体,可调控牡荆素在胃肠道的消化吸收,扩展其应用范围。除此之外,外泌体是细胞分泌的纳米颗粒,借助天然磷脂双分子层结构,可作为一种潜在递送牡荆素的新型递送系统,提高多酚的靶向性和生物利用度[32]。图3展示了牡荆素主要来源及其代表性稳态化递送系统。
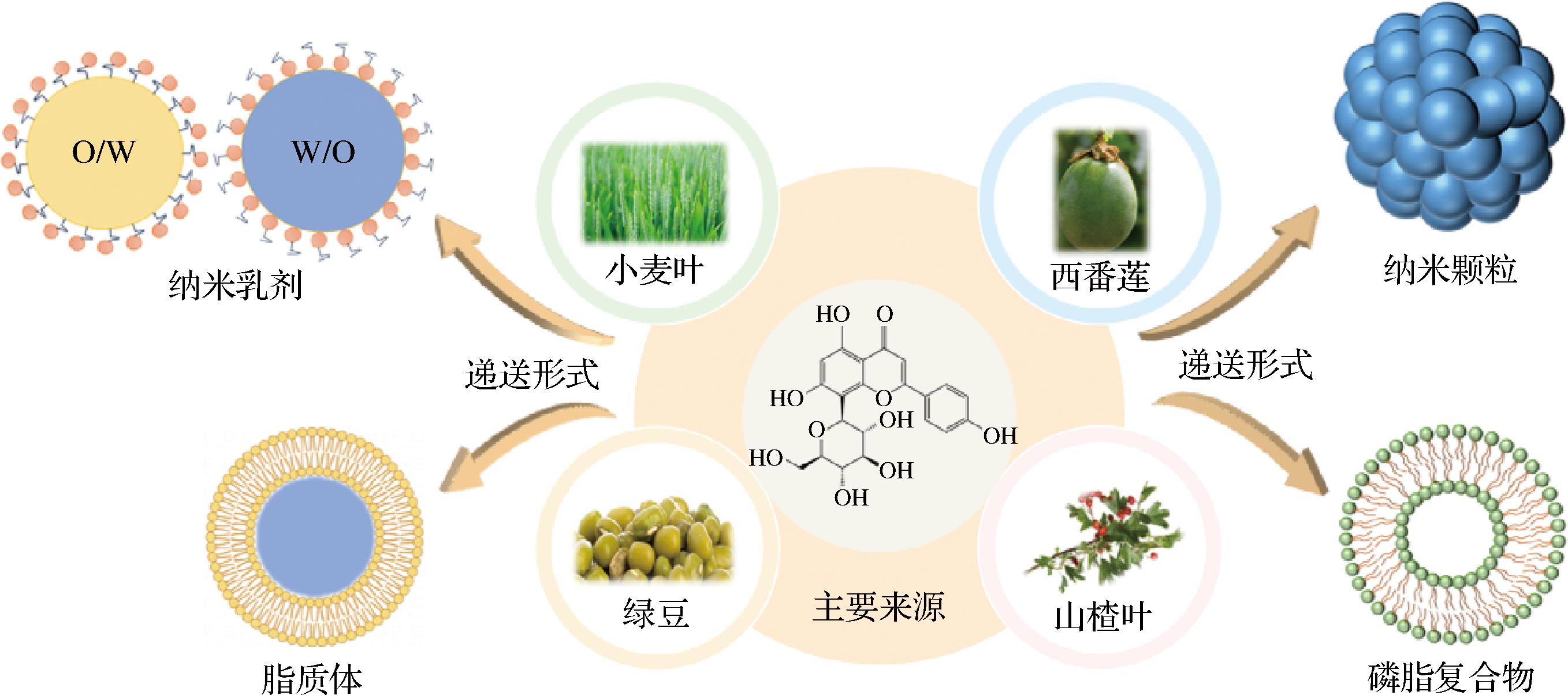
图3 牡荆素主要来源及其代表性稳态化递送系统
Fig.3 Primary sources of vitexin and their representative stabilized delivery systems
2.1 纳米乳剂
纳米乳剂是一种动力学稳定且液滴尺寸为纳米级的胶体体系,利用表面活性剂的稳定作用,将互不相溶的油相与水相结合形成均匀分散系统,其可以通过高能法(高压均质、超声波等)和低能法(低能乳化、相反转法等)制备而成。常见的简单纳米乳剂类型有油包水(water/oil, W/O)和水包油(oil/water, O/W)类型,能够改善牡荆素的溶解性和生物活性。CHOMCHOEY等[33]采用不同浓度的中链甘油三酯和椰子油作为分散油相,吐温-80和卵磷脂的混合物作为乳化剂,通过高压均质技术制备了负载牡荆素的纳米乳液,具有较好的抗液滴聚集性和相分离稳定性,实现了对牡荆素的高包埋率(88%~90%),有效保护牡荆素在胃肠道消化过程中的降解,为疏水性活性成分的递送系统设计提供了重要的理论依据。此外,YOKSAN等[8]使用O/W乳液结合离子凝胶化制备载有牡荆素的壳聚糖-三磷酸五钠纳米颗粒,有效提高了牡荆素在水中的分散稳定性,能够通过极端的胃肠道环境将牡荆素输送到小肠靶点。此外,CHE ZAIN等[7]采用棕榈油为油相,结合亲脂性乳化剂聚甘油蓖麻醇酸酯成功制备了稳定的W/O型初乳,实现牡荆素黄酮C-糖苷富集提取物的高效包封(88.44%),增强了其抗氧化活性和伤口愈合能力。
2.2 纳米颗粒
纳米颗粒的尺寸通常在1~100 nm,不同形状的纳米颗粒具有不同的理化特性。为解决牡荆素的水溶性和分散稳定性差以及在胃肠道中的吸收效果较差等关键问题,可以开发多种纳米颗粒以改善其吸收率。例如,将牡荆素包封在绿豆分离蛋白中,通过pH转移法和超声波处理,显著提高牡荆素的溶解度和生物利用度[34]。靶向杯状细胞肽CSKSSDYQC(CSK) 修饰的N-三甲基壳聚糖包覆的大豆肽双层纳米颗粒,逐层组装提高牡荆素的生物利用度,避免牡荆素在胃部过早释放[35]。利用纳米喷雾干燥法制备藻酸盐纳米颗粒系统,其经口服灌胃后有效改善牡荆素在胃中过早释放[36]。改性壳聚糖和三聚磷酸盐包埋牡荆素的纳米颗粒不仅增强牡荆素在胃肠道中的消化,还表现出抗氧化活性[37]。此外,纳米颗粒递送系统还具有靶向递送牡荆素至特定组织或细胞。YANG等[38]开发了叶酸修饰的聚己内酯-聚乙二醇-聚己内酯[poly(ε-caprolactone)-poly(ethylene glycol)-poly(ε-caprolactone),PCEC]共聚物纳米颗粒,用于靶向递送厚朴酚至鼻咽癌细胞,可能有助于靶向递送牡荆素至特定癌细胞发挥抗癌活性。
2.3 磷脂复合物
磷脂复合物是一种将磷脂酰胆碱(phosphatidylcholine, PC)和植物成分结合的递送形式,增强植物成分的吸收和利用。PC具有亲水性的头部和亲脂性的尾部,使其能够与水溶性和脂溶性成分相互作用。磷脂复合物通过将植物提取物包裹在磷脂中,改善其脂溶性和穿透细胞膜的能力。采用磷脂复合物技术有效增强了牡荆素的水溶性,提高了其在胃肠道消化过程中的口服生物利用度[39]。
2.4 脂质体
脂质体是由磷脂双分子层组成的球形囊泡,内部包裹着水性空间。它具有良好的生物相容性,可以封装亲水性和疏水性物质,保护物质成分免受降解,并提高其在靶部位的浓度。常见的脂质体制备方法包括反相蒸发技术、注射技术、微流控法、薄膜水合法等。利用微流控技术制备的牡荆素/吲哚菁绿脂质体,与游离的牡荆素相比,可增加牡荆素的释放,有效提高了颗粒之间的分散性[9]。包被聚乙二醇(polyethylene glycol,PEG)的牡荆素脂质体可用于治疗肝硬化[40],证实脂质体包埋与PEG涂层是提高牡荆素生物利用度和药代动力学行为的有效策略。此外,由非离子表面活性剂组成的囊泡也可作为靶向递送系统,既保持了脂质体的药物靶向优势,又克服了脂质体不稳定性的问题,提高了药物生物利用度。MALATHI等[41]开发了一种靶向囊泡系统的内皮生长因子受体(epidermal growth factor receptor,EGFR)来递送阿霉素和牡荆素治疗乳腺癌,载有牡荆素的囊泡递送体在4T1细胞诱导的乳腺癌小鼠模型中具有明显的抗肿瘤活性,同时对乳腺组织发挥潜在抗炎作用。
2.5 外泌体
外泌体是细胞分泌的直径约30~150 nm的胞外囊泡,携带蛋白质、RNA、脂质等生物活性分子,介导细胞间通讯,参与免疫调节、肿瘤转移、组织修复等过程,是疾病诊断标志物和靶向治疗的潜在载体,其来源广泛,包括体液、植物、水果和牛奶。最新研究表明,利用牛奶源性外泌体共载姜黄素与白藜芦醇,成功实现了乳腺靶向递送,并显著增强对乳腺癌细胞的抗增殖作用[42]。基于其天然的靶向特性与优异的生物相容性,负载牡荆素的外泌体可能是一种规避传统递送系统免疫清除问题的新型高效递送载体。
3 牡荆素在食品领域中的应用
牡荆素作为一种天然多靶点活性分子,其多元化的生物活性已在研究中得到广泛证实,包括抗炎作用、清除活性氧(reactive oxygen species, ROS)/活性氮(reactive nitrogen species, RNS)自由基实现抗氧化保护、诱导肿瘤细胞凋亡的抗癌机制,以及调节β-淀粉样蛋白沉积的神经保护功等作用[43],是一种具有延缓衰老、干预代谢综合征等定向健康效应的潜在活性因子,作为食品补充剂改善食品性能,有助于功能性食品开发。此外,它还作为共激发小分子用于果实保鲜领域,调节果实衰老,提升果实保鲜品质(图4)。
图4 牡荆素在食品领域中的应用
Fig.4 Applications of vitexin in food industry
3.1 功能性食品开发
美拉德反应作为食品加工中提升感官特性的重要手段,其产生的晚期糖基化终末产物(advanced glycation end products, AGEs)在热加工与贮藏过程中过量积累,已被证实会引发食品感官品质劣变并破坏肠道稳态[44]。NI等[45]通过构建牛血清白蛋白-果糖和牛血清白蛋白-甲基乙二醛两种糖基化模型,证实牡荆素能够捕获活性羰基物质抑制AGEs生成,并通过空间位阻效应改变蛋白质的糖化修饰位点分布,为开发精准型抗糖化剂提供了新思路。目前,以精制淀粉为主导的膳食结构引发的代谢综合征问题日益严峻。NIU等[46]通过超声波辅助分子组装技术成功构建了牡荆素-稻米淀粉V型复合物,提高抗性淀粉含量至41.8%,为开发低升糖指数功能食品奠定理论基础。此外,研究人员利用反溶剂法将牡荆素-鼠李糖苷包埋在玉米醇溶蛋白-果胶纳米颗粒,有效降低了血清总胆固醇和三酰甘油水平、炎症和脂肪的沉积,并且抑制了天冬氨酸转氨酶和丙氨酸转氨酶的活性,显著改善了高脂饮食诱导的脂质代谢紊乱[47],为功能性食品纳米递送系统提供了新思路,有助于开发具有多种生物活性的功能性食品。
3.2 水果保鲜应用
采后果皮发生褐变主要的机制包括能量供应不足和ROS爆发。过度的ROS积累会破坏膜的完整性,诱导果实衰老。YANG等[48]采用1 mmol/L牡荆素处理荔枝,发现其能够特异性上调自噬相关基因(LcATG2、LcATG5和LcATG8)的表达水平,激活细胞自噬机制,有效缓解氧化应激损伤,维持细胞稳态,延缓果实衰老。
3.3 膳食补充剂应用
植物发酵蔬菜营养丰富,具有多种潜在健康益处。目前,研究发现蔬菜发酵过程中有益菌能将牡荆素代谢成小分子多酚(例如糖苷配基),提高酚类化合物水平,增强产物生物活性。此外,富含牡荆素的发酵蔬菜可以增加乳酸菌,抑制有害细菌,并增强抗氧化活性[49],表明牡荆素在未来可作为原料和补充剂,具有提高发酵食品的生物活力的潜力。
4 结论与展望
牡荆素作为一种天然多酚化合物,在抗癌领域展现出巨大的潜力,其抗癌机制主要通过诱导细胞凋亡、抗肿瘤血管生成、抑制肿瘤迁移和侵袭、调节自噬实现。然而,由于牡荆素具有水溶性差、稳定性低、肠道通透性有限等问题,应用多种稳态化递送系统,如纳米乳液、纳米颗粒、脂质体等,能够有效改善牡荆素的水溶性和稳定性,提高生物利用度,改善其体内分布,实现靶向抗癌效果。此外,牡荆素作为一种生物活性小分子,具有丰富的食用价值和营养价值,在功能食品开发、水果保鲜应用、改善食品性能等方面应用具有良好的发展前景。但还有许多亟待解决的问题:1)深入开展牡荆素及其递送系统药代动力学与长期安全性评价研究工作;2)开发系列耐受高温、高热的牡荆素纳米递送体,以提高活性分子在食品加工和储存过程中的稳定性;3)开发具有高效靶向特异性的牡荆素复合纳米载体,同时可结合光热疗法和光动力学疗法实现抗肿瘤作用。总之,设计和开发牡荆素的稳态化递送系统,不仅能够拓宽牡荆素在食品领域的应用范围,更能实现营养成分的精准递送与可控释放,进一步推动牡荆素在食品工业中的产业化应用。
[1] BRAY F, LAVERSANNE M, SUNG H, et al.Global cancer statistics 2022:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J].CA:A Cancer Journal for Clinicians, 2024, 74(3):229-263.
[2] KOPUSTINSKIENE D M, JAKSTAS V, SAVICKAS A, et al.Flavonoids as anticancer agents[J].Nutrients, 2020, 12(2):457.
[3] LI W X, LIU X Y, MA Y, et al.Changes in physio-biochemical metabolism, phenolics and antioxidant capacity during germination of different wheat varieties[J].Food Chemistry:X, 2024, 22:101429.
[4] PENG Y, GAN R Y, LI H B, et al.Absorption, metabolism, and bioactivity of vitexin:Recent advances in understanding the efficacy of an important nutraceutical[J].Critical Reviews in Food Science and Nutrition, 2021, 61(6):1049-1064.
[5] WU T H, XIANG M, LI Y J, et al.Exploration of the pharmacological mechanism of vitexicarpin against triple-negative breast cancer in network pharmacology[J].Frontiers in Bioscience, 2023, 28(12):341.
[6] HE J D, WANG Z, LI S P, et al.Vitexin suppresses autophagy to induce apoptosis in hepatocellular carcinoma via activation of the JNK signaling pathway[J].Oncotarget, 2016, 7(51):84520-84532.
[7] CHE ZAIN M S, SHAARI K, LEE S Y, et al.Development and evaluation of hydrogel-thickened nanoemulsion containing orientin, isoorientin, vitexin and isovitexin as an antioxidant wound dressing[J].Journal of Cluster Science, 2024, 35(2):635-656.
[8] YOKSAN R, NOIVOIL N.Fabrication, characterization and in vitro release of vitexin-loaded chitosan nanoparticles[J].Journal of Polymers and the Environment, 2024, 32(4):1557-1572.
[9] CAO X, LIU Q, ADU-FRIMPONG M, et al.Microfluidic generation of near-infrared photothermal vitexin/ICG liposome with amplified photodynamic therapy[J].AAPS PharmSciTech, 2023, 24(4):82.
[10] MOON B, CHANG S.Exosome as a delivery vehicle for cancer therapy[J].Cells, 2022, 11(3):316.
[11] ZHANG L C, LA X Q, TIAN J M, et al.The phytochemical vitexin and syringic acid derived from foxtail fillet bran inhibit breast cancer cells proliferation via GRP78/SREBP-1/SCD1 signaling axis[J].Journal of Functional Foods, 2021, 85:104620.
[12] CHEN D S, CHEN Y, HUANG F, et al.The underlying regulatory mechanisms of colorectal carcinoma by combining Vitexin and Aspirin:Based on systems biology, molecular docking, molecular dynamics simulation, and in vitro study[J].Frontiers in Endocrinology, 2023, 14:1147132.
[13] ZHOU Y J, LIU Y E, CAO J G, et al.Vitexins, nature-derived lignan compounds, induce apoptosis and suppress tumor growth[J].Clinical Cancer Research, 2009, 15(16):5161-5169.
[14] LEE C Y, CHIEN Y S, CHIU T H, et al.Apoptosis triggered by vitexin in U937 human leukemia cells via a mitochondrial signaling pathway[J].Oncology Reports, 2012, 28(5):1883-1888.
[15] WANG C, JIANG H M.Vitexin induces apoptosis and ferroptosis and suppresses malignant proliferation and invasion of bladder urothelial carcinoma through PI3K/AKT-Nrf2 axis[J].Letters in Drug Design &Discovery, 2024, 21(11):2135-2147.
[16] LIU X L, JIANG Q F, LIU H M, et al.Vitexin induces apoptosis through mitochondrial pathway and PI3K/Akt/mTOR signaling in human non-small cell lung cancer A549 cells[J].Biological Research, 2019, 52(1):7.
[17] JIASHU LU M M, LEI YU M M, YING MA M M, et al.Vitexin inhibits the proliferation and promotes the apoptosis of gastric cancer cells via phosphatidylinositol-3-kinase (PI3K)/protein kinase B (Akt)/the mammalian target of rapamycin (mTOR) signaling pathway[J].Journal of Biomaterials and Tissue Engineering, 2020, 10(12):1843-1850.
[18] CHEN Y E, YUAN X, PEI C Y, et al.Vitexin alleviates breast tumor in mice via skewing TAMs toward an iNOS+ profile orchestrating effective CD8+ T cell activation[J].Journal of Functional Foods, 2022, 95:105190.
[19] ZHOU J, HU H Y, LONG J P, et al.Vitexin 6, a novel lignan, induces autophagy and apoptosis by activating the Jun N-terminal kinase pathway[J].Anti-Cancer Drugs, 2013, 24(9):928-936.
[20] LEE J H, MOHAN C D, SHANMUGAM M K, et al.Vitexin abrogates invasion and survival of hepatocellular carcinoma cells through targeting STAT3 signaling pathway[J].Biochimie, 2020, 175:58-68.
[21] YANG S H, LIAO P H, PAN Y F, et al.The novel p53-dependent metastatic and apoptotic pathway induced by vitexin in human oral cancer OC2 cells[J].Phytotherapy Research, 2013, 27(8):1154-1161.
[22] AN F, WANG S H, TIAN Q Q, et al.Effects of orientin and vitexin from Trollius chinensis on the growth and apoptosis of esophageal cancer EC-109 cells[J].Oncology Letters, 2015, 10(4):2627-2633.
[23] HUANG J X, ZHOU Y N, ZHONG X Z, et al.Effects of vitexin, a natural flavonoid glycoside, on the proliferation, invasion, and apoptosis of human U251 glioblastoma cells[J].Oxidative Medicine and Cellular Longevity, 2022, 2022(1):3129155.
[24] WANG Q, ZHANG J, YE J, et al.Vitexin exerts anti-tumor and anti-angiogensis effects on cervical cancer through VEGFA/VEGFR2 pathway [J].European Journal of Gynaecological Oncology, 2022, 43(4):86-91.
[25] WANG J G, ZHENG X X, ZENG G Y, et al.Purified vitexin compound 1 inhibits growth and angiogenesis through activation of FOXO3a by inactivation of Akt in hepatocellular carcinoma[J].International Journal of Molecular Medicine, 2014, 33(2):441-448.
[26] ZHOU P, ZHENG Z H, WAN T, et al.Vitexin inhibits gastric cancer growth and metastasis through HMGB1-mediated inactivation of the PI3K/AKT/mTOR/HIF-1α signaling pathway[J].Journal of Gastric Cancer, 2021, 21(4):439-456.
[27] LI W, ZHOU Y, YANG J, et al.Curcumin induces apoptotic cell death and protective autophagy in human gastric cancer cells[J].Oncology Reports, 2017, 37(6):3459-3466.
[28] BHARDWAJ M, CHO H J, PAUL S, et al.Vitexin induces apoptosis by suppressing autophagy in multi-drug resistant colorectal cancer cells[J].Oncotarget, 2017, 9(3):3278-3291.
[29] BRAUNE A, BLAUT M.Intestinal bacterium Eubacterium cellulosolvens deglycosylates flavonoid C- and O-glucosides[J].Applied and Environmental Microbiology, 2012, 78(22):8151-8153.
[30] 童成亮, 刘晓东.牡荆素在大鼠体内的药代动力学[J].中国药科大学学报, 2007, 38(1):65-68.
TONG C L, LIU X D.Pharmacokinetics of vitexin in rats[J].Journal of China Pharmaceutical University, 2007, 38(1):65-68.
[31] LIAO M, CHENG X Y, DIAO X P, et al.Metabolites identificaion of two bioactive constituents in Trollius ledebourii in rats using ultra-high-performance liquid chromatography coupled to quadrupole time-of-flight mass spectrometry[J].Journal of Chromatography B, 2017, 1068:297-312.
[32] CHEN H Z, WANG L Y, ZENG X L, et al.Exosomes, a new star for targeted delivery[J].Frontiers in Cell and Developmental Biology, 2021, 9:751079.
[33] CHOMCHOEY S, KLONGDEE S, PEANPARKDEE M, et al.Fabrication and characterization of nanoemulsions for encapsulation and delivery of vitexin:Antioxidant activity, storage stability and in vitro digestibility[J].Journal of the Science of Food and Agriculture, 2023, 103(5):2532-2543.
[34] RODKLONGTAN A, DUMRONGCHAI T, CHITPRASERT P.Ultrasound-assisted pH-shifted mung bean protein isolate nanoparticles in calcium carbonate microparticles for oral delivery of vitexin[J].Journal of Food Science, 2025, 90(2):e70032.
[35] LI S, LV H Y, CHEN Y, et al.N-trimethyl chitosan coated targeting nanoparticles improve the oral bioavailability and antioxidant activity of vitexin[J].Carbohydrate Polymers, 2022, 286:119273.
[36] SHAEDI N, NAHARUDIN I, CHOO C Y, et al.Design of oral intestinal-specific alginate-vitexin nanoparticulate system to modulate blood glucose level of diabetic rats[J].Carbohydrate Polymers, 2021, 254:117312.
[37] YOKSAN R, TOWONGPHAICHAYONTE P.Vitexin-loaded poly(ethylene glycol) methyl ether-grafted chitosan/alginate nanoparticles:Preparation, physicochemical properties and in vitro release behaviors[J].Journal of the Science of Food and Agriculture, 2024, 104(2):956-966.
[38] YANG B, NI X L, CHEN L X, et al.Honokiol-loaded polymeric nanoparticles:An active targeting drug delivery system for the treatment of nasopharyngeal carcinoma[J].Drug Delivery, 2017, 24(1):660-669.
[39] PEANPARKDEE M, YOOYING R.Enhancement of solubility, thermal stability and bioaccessibility of vitexin using phosphatidylcholine-based phytosome[J].NFS Journal, 2023, 31:28-38.
[40] FAROOQ A, IQBAL A, RANA N F, et al.A novel sprague-dawley rat model presents improved NASH/NAFLD symptoms with PEG coated vitexin liposomes[J].International Journal of Molecular Sciences, 2022, 23(6):3131.
[41] MALATHI S, SISILA V, SINGARAVEL V, et al.Epidermal growth factor receptor targeted doxorubicin and vitexin loaded niosomes for enhanced breast cancer therapy[J].Materials Advances, 2023, 4(21):5224-5237.
[42] GONZ LEZ-SARR
LEZ-SARR AS A, IGLESIAS-AGUIRRE C E, CORTÉS-MART
AS A, IGLESIAS-AGUIRRE C E, CORTÉS-MART N A, et al.Milk-derived exosomes as nanocarriers to deliver curcumin and resveratrol in breast tissue and enhance their anticancer activity[J].International Journal of Molecular Sciences, 2022, 23(5):2860.
N A, et al.Milk-derived exosomes as nanocarriers to deliver curcumin and resveratrol in breast tissue and enhance their anticancer activity[J].International Journal of Molecular Sciences, 2022, 23(5):2860.
[43] BABAEI F, MOAFIZAD A, DARVISHVAND Z, et al.Review of the effects of vitexin in oxidative stress-related diseases[J].Food Science &Nutrition, 2020, 8(6):2569-2580.
[44] SHI B S, GUO X, LIU H Y, et al.Dissecting Maillard reaction production in fried foods:Formation mechanisms, sensory characteristic attribution, control strategy, and gut homeostasis regulation[J].Food Chemistry, 2024, 438:137994.
[45] NI M T, SONG X, PAN J H, et al.Vitexin inhibits protein glycation through structural protection, methylglyoxal trapping, and alteration of glycation site[J].Journal of Agricultural and Food Chemistry, 2021, 69(8):2462-2476.
[46] NIU R J, RAZA H, WANG M F.Introducing vitexin in rice starch using ultrasound to enhance V-type resistant starch[J].LWT, 2025, 215:117287.
[47] HUANG X, HU X P, LI S H, et al.Vitexin-rhamnoside encapsulated with zein-pectin nanoparticles relieved high-fat diet induced lipid metabolism disorders in mice by altering the gut microbiota[J].International Journal of Biological Macromolecules, 2024, 264:130704.
[48] YANG Q X, SHI D D, REN Y L, et al.Vitexin is a potential postharvest treatment for ameliorating litchi fruit pericarp browning by regulating autophagy[J].Postharvest Biology and Technology, 2024, 216:113061.
[49] NGAMSAMER C, MUANGNOI C, TONGKHAO K, et al.Potential health benefits of fermented vegetables with additions of Lacticaseibacillus rhamnosus GG and polyphenol vitexin based on their antioxidant properties and prohealth profiles[J].Foods, 2024, 13(7):982.