5-氨基乙酰丙酸(5-aminolevulinic,5-ALA)是维生素B12、血红素、叶绿素和细胞色素等生物合成途径的关键代谢前体,广泛存在于细菌、真菌及动植物细胞中,其中血红素和叶绿素是光合作用和呼吸作用中重要的载体[1]。因其独特的化学结构和广泛的生物活性,在多个领域展现出重要的应用价值与开发前景。近年来,随着对其生物化学特性的深入研究,5-ALA在医疗和农业领域的应用逐渐受到关注,并成为跨学科研究的热点。作为一种安全、选择性和渗透性好的光动力学药物在医学领域逐渐得到了重视。目前,已经应用于癌症的诊断和治疗[2]。在农业上,已经成为一种无公害的绿色农药,作为除草剂、植物生长调节剂等[3]。同时,也是工业上一些有机物合成的中间体。
自然界中的很多微生物、植物和动物都可以天然合成5-ALA,合成途径有2条:碳四(C4)途径和碳五(C5)途径。C5途径中,谷氨酸是5-ALA合成的直接前体物。谷氨酰tRNA合成酶催化谷氨酸生成谷氨酰tRNA。影响C5途径效率的关键酶是谷氨酰tRNA还原酶,谷氨酰tRNA在该酶的作用下还原为谷氨酰半醛。最后一步在谷氨酰半醛氨基转移酶的催化下生成5-ALA[4]。C4途径主要存在于动物、真菌,以及非硫光合细菌中,在由hemA基因编码的5-ALA合成酶(5-aminolevulinic acid aynthase,ALAS)催化下,由1分子甘氨酸和1分子琥珀酰辅酶A缩合生成1分子5-ALA[5]。ALAS是一种5-磷酸吡哆醛(pyridoxal 5′-phosphate,PLP)依赖性同源二聚体,它属于α级PLP依赖性酶的氧氨合酶亚组[6-7],是5-ALA合成途径中的关键酶。不同细菌间的ALAS大小较接近,处于43~55 kDa。ALAS包括3个结构域:N端结构域、C端结构域、α端催化域,通过形成连接紧密的同源二聚体发挥功能[8]。
荚膜红杆菌(Rhodobacter capsulatus)ALAS的晶体结构为底物结合和催化提供了结构基础。KAUFHOLZ等[9]为了阐明ALAS活性位点中单个氨基酸残基在底物识别、底物定位、催化和蛋白结构重排中的功能作用,对氨基酸残基Arg21、Thr83、Asn85和Ile86进行动力学测定,分析其功能。HE等[10]选择了来自R.capsulatus的ALAS(RC ALAS)进行半胱氨酸靶向突变,成功构建了多个变体,其中RC-C201A变体表现出显著的特性,在谷氨酸棒杆菌(Corynebacterium glutamicum)中过表达RC-C201A变体时,5-ALA的产量比野生型提高了21.6%,酶活力提高了3.8%。DU等[11]对来源于R.capsulatus的ALAS进行突变,获得了突变体I325M/V390Y/H391I,其比活性比野生型增加了7倍。
利用C4途径,在工程化宿主中导入异源高活力的ALAS实现5-ALA的生物合成是近年来的研究热点[12],并在2024年取得较大突破:WANG等[13]在大肠杆菌(Escherichia coli)中表达来源于Rhodopseudomonas palustris的hemA,调节其启动子、突变R97H、T317I,增强5-ALA外排、弱化hemB,经过改善辅因子合成和供应,加强三羧酸循环通量,提高应变耐受性,增强5-ALA外排和减弱ALA下游通量等一系列代谢工程策略,在5 L发酵罐中,通过补加甘氨酸进行发酵,5-ALA的产量达到58.54 g/L;ZHOU等[14]通过在基因组水平上鉴定并分别敲除E.coli的sucCD、GCSP、pta-ackA、poxB,共表达noxE与gfp,优化辅因子,弱化hemB,上调5-ALA转运蛋白EamA,最终在5 L生物反应器中将5-ALA滴度提高到21.82 g/L。在氧化还原系统上,协调优化了其他辅因子的转录水平,将5-ALA产量提高到63.39 g/L,为目前报道5-ALA的最高产量。
本研究对R.capsulatus来源的ALAS(RC ALAS)进行了改造,通过定点突变技术筛选产量较高的突变体Rc/I361V,并对其进行动力学测定,然后将其在大肠杆菌中进行异源表达;采用代谢工程的策略,以敲除了大肠杆菌中编码的琥珀酰辅酶A合成酶的sucCD基因的E. coli W3110(DE3)为出发菌株,弱化了参与甘氨酸裂解酶系统的gcsH基因,敲除甘氨酸代谢关键基因kbL、丙酮酸代谢途径poxB基因,促进5-ALA途径通量,为高产5-ALA大肠杆菌菌株的工业应用奠定基础。
1 材料与方法
1.1 材料
1.1.1 主要试剂
同源重组连接酶试剂盒,北京庄盟国际基因科技有限公司;PCR高保真酶,TaKaRa公司;琼脂糖凝胶DNA回收试剂盒、小量质粒提取试剂盒、硫酸卡那霉素(kanamycin,Kan)、氨苄青霉素钠(ampicillin sodium,Amp)、壮观霉素等抗生素,异丙基-β-D-硫代半乳糖苷(isopropyl β-D-thiogalactopyranoside,IPTG)、核酸染料等试剂,上海生工生物工程股份有限公司;LB普通培养基,Gen Star公司;葡萄糖、甘氨酸、冰醋酸、高氯酸、乙酰丙酮等试剂(分析纯),国药集团化学试剂有限公司。
1.1.2 菌株、质粒和培养基
出发菌株E.coli W3110、大肠杆菌E.coli DH5α、大肠杆菌E.coli BL21(DE3)和质粒RC hemA-pET 21a均为实验室保藏。本研究中的菌株及质粒命名见表1。
表1 文中所用菌株和质粒
Table 1 Strains and plasmids used in this study

菌株特性来源E.coli DH5α感受态细胞实验室保藏E.coli BL21(DE3)感受态细胞实验室保藏RC hemA BL21(DE3)含有RC hemA-pET21a质粒的E.coli BL21(DE3) 本研究构建RC/I361V BL21(DE3)[其余含有突变体的E.coli BL21(DE3)同RC/I361V BL21(DE3)命名]含有RC/I361V质粒的E.coli BL21(DE3)本研究构建E.coli W3110(DE3)野生型菌株实验室保藏S162在E.coli W3110 (DE3)上敲除sucCD基因实验室保藏S163菌株S162的 gcsH基因的S67突变为A本研究构建S164敲除S163上的kbL基因本研究构建S165敲除S164上的poxB基因本研究构建RC/I361V S162含有RC/I361V质粒的S162菌株本研究构建RC/I361V S163含有RC/I361V质粒的S163菌株本研究构建RC/I361V S164含有RC/I361V质粒的S164菌株本研究构建RC/I361V S165含有RC/I361V质粒的S165菌株本研究构建质粒说明来源RC hemA-pET21a表达RC hemA基因GenBank: KU687108.1实验室保藏RC/I361V(其余突变体同I361V命名质粒)RC hemA基因的I361突变为V本研究构建
LB培养基(g/L):酵母粉5,蛋白胨10,NaCl 10 (固体培养基加入13 g/L的琼脂粉)。
TB培养基(g/L):酵母粉24,蛋白胨12,NaCl 10,KH2PO4 2.2,K2HPO4 9.4,甘油4 mL。
1.1.3 PCR引物设计
本研究中PCR扩增所用引物由上海生工生物公司合成,序列见表2。
表2 文中所用引物
Table 2 Primers used in this study

引物名称引物序列(5′-3′)F375A-FGTCTGCGTGCGACCCCGTCTCCGGTTCACGACCTGAAACAGATCF375A-RACGGGGTCGCACGCAGACGTTCGGTACCACGCGGAACGN85A-FGTACCCGTGCTATCTCTGGTACCACCGCTTACCACCN85A-RCAGAGATAGCACGGGTACCACCAGAACCAGCACCAAR84A-FGGTGGTACCGCTAACATCTCTGGTACCACCGCTTACCACR84A-RGATGTTAGCGGTACCACCAGAACCAGCACCAACAR374A-FACGTCTGGCGTTCACCCCGTCTCCGGTTCACGACCTGAAACAGR374A-RGGGGTGAACGCCAGACGTTCGGTACCACGCGGAACGS277C-FCATCTTCTGCACCTCTCTGCCGCCGGCTATCGCS277-RGAGAGGTGCAGAAGATGAAACCCGGAGCGTAAGAACGAACAGT83C-FTGGTGGTTGCCGTAACATCTCTGGTACCACCGCTTACCACT83C-RTGTTACGGCAACCACCAGAACCAGCACCAACAGCTTCCAGAGI361V-FTTCAGCCGGTGAACTTCCCGACCGTTCCGCGTGGTACCI361V-RGGGAAGTTCACCGGCTGAACGTAAACACCGTAGTCAGACAGCAGsucCD-sgRNATCCTAGGTATAATACTAGTGGGGACTTTCCACTCAGAACGTTTTAGAGCTAGAAATAGCgcsH/S67A-FAAAGCGGCGGCGGACATTTATGCGCCAGTAAGCGGgcsH/S67A-FAAATGTCCGCCGCCGCTTTTACCGATTCGGgcsH-sgRNATCCTAGGTATAATACTAGTGTGAACAGCGAACCGTATGCGTTTTAGAGCTAGAAATAGCkbL-sgRNATCCTAGGTATAATACTAGTATTGGCGCGTATCAGGTGAGGTTTTAGAGCTAGAAATAGCpoxB- sgRNATCCTAGGTATAATACTAGTGCGATGGAGATGAAAGCTGGGTTTTAGAGCTAGAAATAGCsgRNA-RACTAGTATTATACCTAGGACTGAGCTAGCT
1.2 方法
1.2.1 RC ALAS定点突变及筛选
以RC hemA质粒为模板分别使用定点突变引物进行PCR,用In-Fusion试剂盒进行重组连接,从转化平板挑取形态大小均一的单菌落测序验证。测序成功后将质粒转入E.coli BL21(DE3)摇瓶发酵验证,从平板上挑取单菌落接入含有Amp (100 μg/mL)抗性的4 mL LB液体培养基,37 ℃、200 r/min培养6 h,转接含20 mL氨苄抗性的LB培养基中,待OD600值达到0.6~0.8时加入0.2 mmoI/L IPTG,28 ℃、200 r/min继续培养12 h,测定发酵液中5-ALA的浓度。
1.2.2 5-ALA及甘氨酸浓度的测定
将发酵液12 000 r/min离心10 min除去菌体,并将上清液稀释至适宜浓度。取稀释后液体或标准品20 μL,加入200 μL的1 moI/L乙酸钠溶液及20 μL的乙酰丙酮。100 ℃反应15 min。冷却至室温后加入100 μL Ehrlich’s试剂[1 g 4-(二甲氨基)苯甲醛加入8 mL体积分数70%的高氯酸后冰乙酸定容至50 mL],反应2 min,在554 nm下测量吸光度,根据标准曲线计算5-ALA的浓度[15]。
取40 μL发酵液上清样品或标品,加入160 μL 0.2 moI/L NaHCO3和200 μL体积分数10 mmoI/L丹磺酰氯乙腈溶液,混合30 ℃反应30 min,加入400 μL 0.12 mmoI/L HCl溶液,通过0.22 μm滤膜过滤,并使用C18色谱柱(250 mm×4.6 mm,5 μm)通过高效液相色谱分析,进样量5 μL,流速1.0 mL/min,检测波长338 nm,柱温30 ℃。流动相A:25% 50 mmoI/L乙腈溶液。流动相B:75%磷酸钾溶液(pH 6.0)。
1.2.3 RC ALAS及突变体RC/I136V动力学参数测定
分别挑取RC hemA BL21(DE3)及RC/I361V B21(DE3)的单菌落接种到4 mL摇菌管里,37 ℃、200 r/min培养6 h,转接含20 mL的LB培养基中,待OD600值达到0.6~0.8时加入0.2 mmol/L IPTG,28 ℃、200 r/min继续培养12 h后,于4 ℃、10 000 r/min离心20 min。菌体收集后用50 mmol/L Tris-HCl缓冲液(pH 7.5)洗涤2次,冰上超声波破碎,将破碎液于4 ℃、12 000 r/min离心30 min,取上清液即为ALAS粗酶液,使用AKTA蛋白纯化系统及Ni柱(His TrapTM FF,GE Healthcare)进行亲和层析纯化。用50 mmol/L磷酸盐缓冲液(pH 7.4)平衡Ni柱3~5个柱体积。将粗酶液加载到Ni柱上。用平衡缓冲液洗脱非特异性结合的蛋白,然后用含有不同浓度咪唑的洗脱缓冲液进行线性梯度洗脱(如5%~100% B液),收集洗脱峰,超滤浓缩之后采用BCA法测定蛋白质浓度,并进行酶动力学参数测定,酶催化反应体系:40 μL 甘氨酸(0.1~15 mmol/L)、80 μL纯化ALAS、80 μL琥珀酰辅酶A(0.1 mmol/L)、4 μL PLP(10 mg/mL)。ALAS加入PLP后4 ℃孵育1 h后加入底物,37 ℃反应1 h,测定反应液中5-ALA的浓度。酶活力则定义为:37 ℃下每分钟催化形成1 μmol 5-ALA的酶量为1 U。
1.2.4 大肠杆菌基因突变株的构建
使用CRISPR/Cas9(clustered regularly interspaced short palindromic repeats-Cas9)基因编辑技术敲除基因[13],利用网站https://zlab.bio/guide-design-resources设计sgRNA,通过PCR构建到质粒pECgRNA上。选择被敲基因上下游各40 bp合成80 bp同源片段,overlap PCR合成gcsH带有S67A[16]突变的1 000 bp的同源片段。将带有pEcCas9质粒的大肠杆菌制作成感受态细胞,加入3 μL重组的sgRNA质粒以及15 μL同源片段与感受态预混3 min。通过电转化后,涂布于卡那霉素加壮观霉素的双抗性平板上(加阿拉伯糖),37 ℃过夜培养,挑取单菌落做PCR验证。阳性克隆消除sgRNA(使用鼠李糖消除)和pEcCas9(使用蔗糖消除)。
1.2.5 基因缺失突变株的发酵
将敲除成功的宿主制备成感受态,将RC/I361V质粒通过电转化转入改造后的宿主,将其涂布于含Amp抗性的平板上过夜培养,从平板上挑取单菌落接入含有Amp (100 μg/mL)抗性的4 mL LB液体培养基,37 ℃、200 r/min培养6 h,转接含20 mL氨苄抗性的TB培养基中,37 ℃、200 r/min培养至OD600值达到0.6~0.8时加入0.2 mmoI/L IPTG,补加2 g/L的甘氨酸到培养基,28 ℃、200 r/min继续培养12 h,测定发酵液中5-ALA的浓度和甘氨酸的残留量。5-ALA及甘氨酸的测定方法同1.2.2节。
2 结果与分析
2.1 高活性RC ALAS突变体筛选及动力学参数测定
根据RC ALAS的晶体结构(PDB数据库编号:2BWO),选取了底物结合口袋周围的5个氨基酸残基R374、F375、N85、R84和I361进行突变并发酵验证,结果如图1-a所示,突变体Rc/N85A、Rc/I361C和RC/I361V转入E.coli BL21(DE3)后的5-ALA产量显著高于野生型。进而对I361位点进行了饱和突变,结果如图1-b所示,361位点的亮氨酸残基I突变为天冬酰胺N、半胱氨酸C、苏氨酸T、谷氨酰胺Q及缬氨酸V等氨基酸残基时,转入E.coli BL21(DE3)后的5-ALA产量显著提高,其中RC/I361V BL21(DE3)的产量为野生型的2.5倍。基于蛋白晶体分析,如图2所示,361~372位氨基酸残基构成的loop区与琥珀酰辅酶A位置接近,其中365位苏氨酸残基(T365)对琥珀酰辅酶A结合起到至关重要的作用[17],处在loop端位I361残基的突变,可能改变loop的构象,提高底物与酶的结合能力。
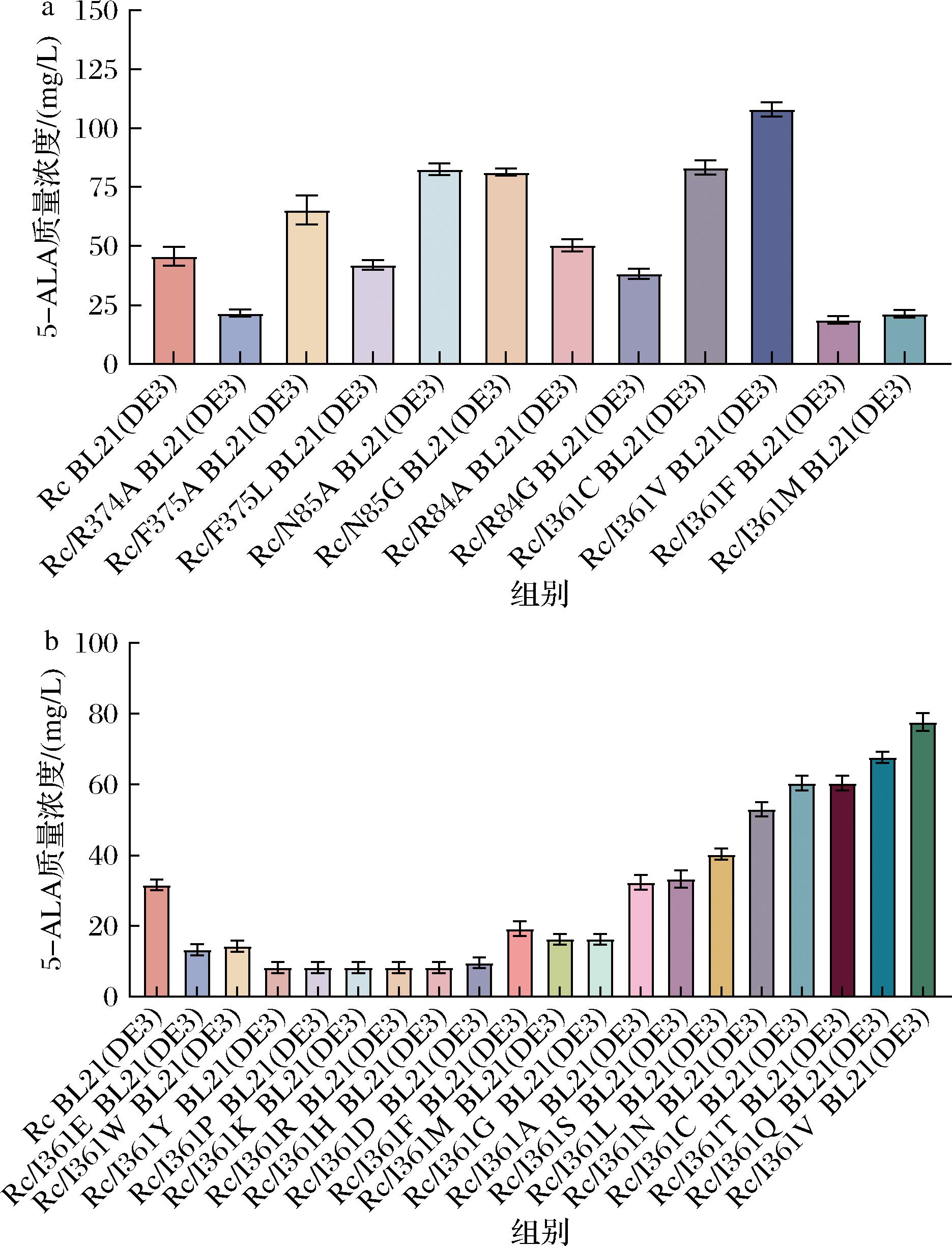
a-RC ALAS突变体的发酵验证;b-RC/I361饱和突变体的发酵验证
图1 RC ALAS突变体的筛选
Fig.1 Screening of RC ALAS mutants
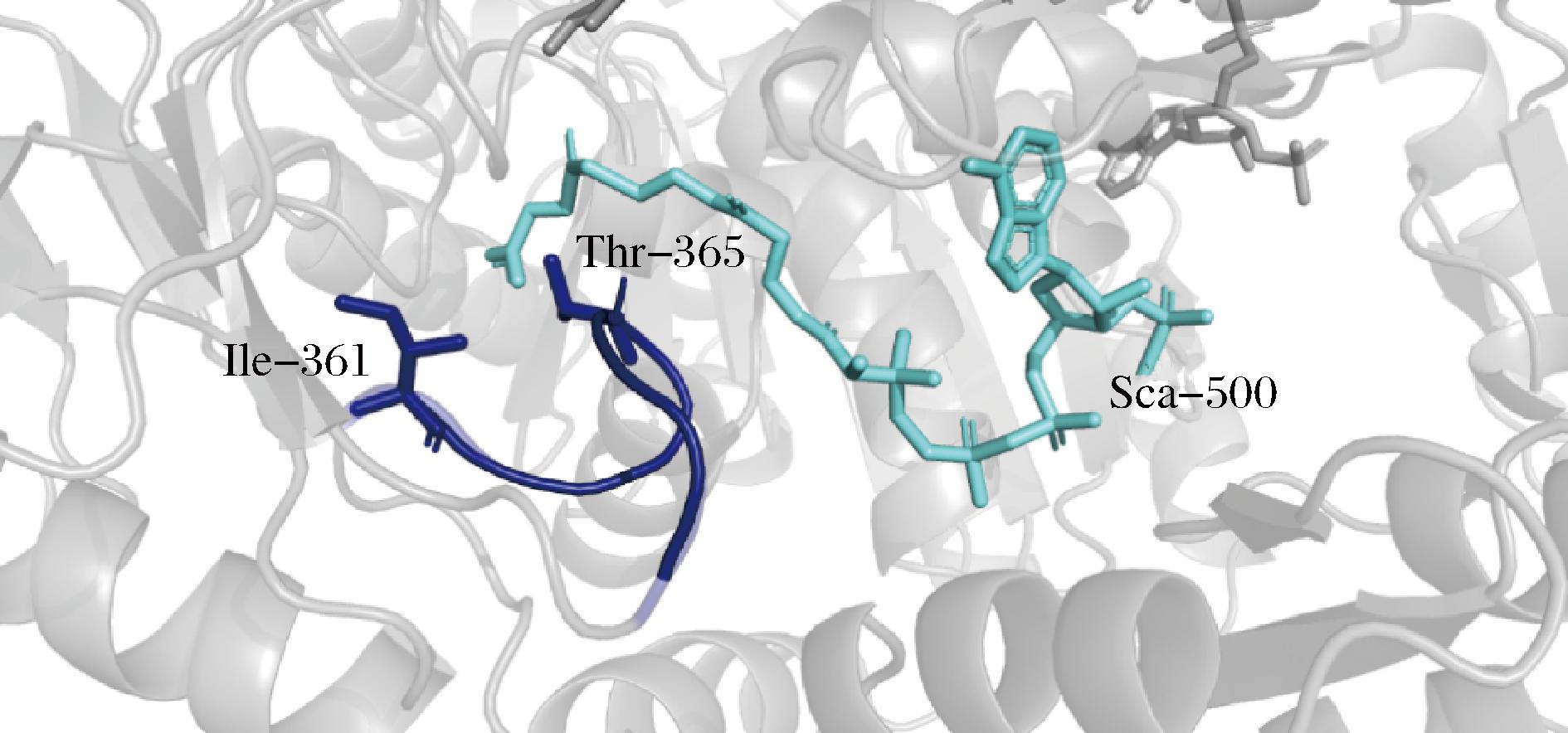
图2 RC ALAS 361~372位氨基酸残基构成的loop区
Fig.2 Loop region composed of amino acid residues 361~372 of RC ALAS
对突变体RC/I361V的酶动力学参数进行了测定,结果如表3所示,相较于野生型RC ALAS,突变体RC/I361V的Km值略有下降,Kcat值显著提高,由5.71 s-1提高到14.46 s-1,最大反应速率Vmax是野生型2.53倍。
表3 RC ALAS和RC/I361V ALAS催化的gly动力学参数
Table 3 Kinetic parameters of gly induced by RC ALAS and RC/I361V ALAS

酶比酶活力/(U/mg)Km/(mmol/L)Vmax/(μmol/min)Kcat/s-1Kcat/Km/[L/(mmol·s)]RC ALAS154.550.171.605.7133.59RC ALAS/I361V373.640.144.0514.46103.32
2.2 kbL及poxB缺失突变株的构建
利用CRISPR技术,在菌株S163中敲除甘氨酸代谢途径kbL基因和编码丙酮酸脱氢酶poxB基因,转化子PCR验证结果如图3-a所示,野生型大肠杆菌kbL基因片段大小为2 200 bp,图3-b的poxB基因片段大小为2 100 bp;而kbL基因缺失的菌株中目的条带大小为1 200 bp,poxB基因缺失的菌株中目的条带大小为500 bp,根据条带大小挑选正确转化子并分别命名为S164和S165。
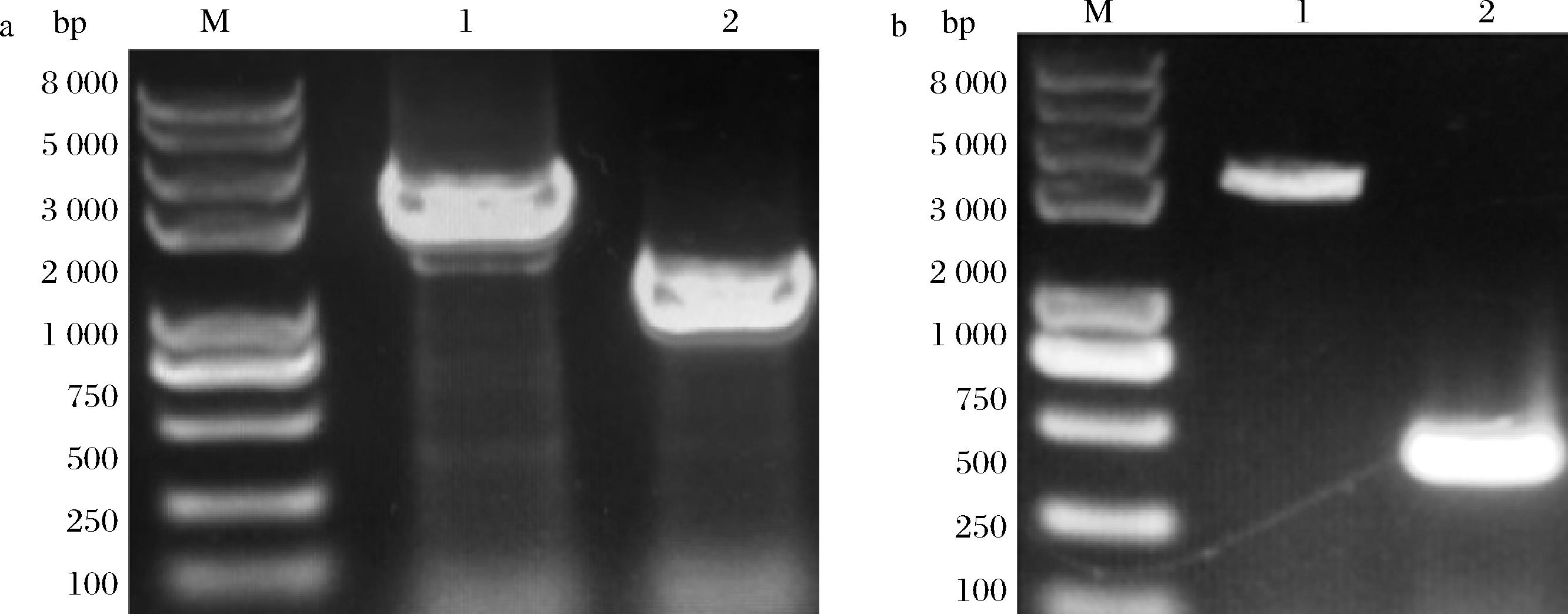
a-M: 8K DNA marker电泳条带;1, 2: kbL基因及被敲除后的PCR产物条带; b-M: 8K DNA marker电泳条带;1,2: poxB基因及被敲除后的PCR产物条带。
图3 kbL和poxB缺失突变株的菌落PCR验证
Fig.3 Bacterial colony PCR validation of kbL and poxB deletion mutant strains
2.3 弱化gcsH基因对5-ALA积累的影响
甘氨酸是利用C4途径合成5-ALA的重要前体,本研究围绕甘氨酸代谢途径来改造大肠杆菌,以敲除了大肠杆菌中编码的琥珀酰辅酶A合成酶的sucCD基因的E.coli W3110(DE3)为出发菌株,以期积累琥珀酰辅酶A[18],菌株命名为S162。
甘氨酸裂解酶系是大肠杆菌降解甘氨酸的主要途径,是由H、P、T和L蛋白组成多酶反应体系,在辅酶四氢叶酸的存在下,将甘氨酸降解为1分子5,10-亚甲基四氢叶酸和1分子CO2和游离氨,并生成1分子还原力。其中H蛋白作为穿梭蛋白,是连接P蛋白与T蛋白的催化中心。前期尝试对gcsH基因进行敲除,但菌株生长不稳定,故对H蛋白67位丝氨酸残基突变为丙氨酸,降低其催化活力[16],得到S163菌株。
为了测试弱化gcsH基因对5-ALA积累的影响,首先将前期筛选出产量较高的突变体hemA质粒RC/I361V转入改造后的S163菌株,28 ℃下添加2 g/L甘氨酸培养,测定各菌株发酵液的5-ALA产量及甘氨酸残留量。结果如图4所示,弱化gcsH的RC/I361V S163菌株中5-ALA的产量达到了1 g/L,比对照菌株RC/I361V S162(0.61 g/L)提高了64%,外源甘氨酸的利用减少了18%。该结果表明弱化gcsH基因有助于5-ALA的积累。如图5所示,摇瓶发酵实验结果表明,菌株RC/I361V S163的OD600值较出发菌株RC/I361V S162减少了15%,gcsH基因对菌株影响较小。
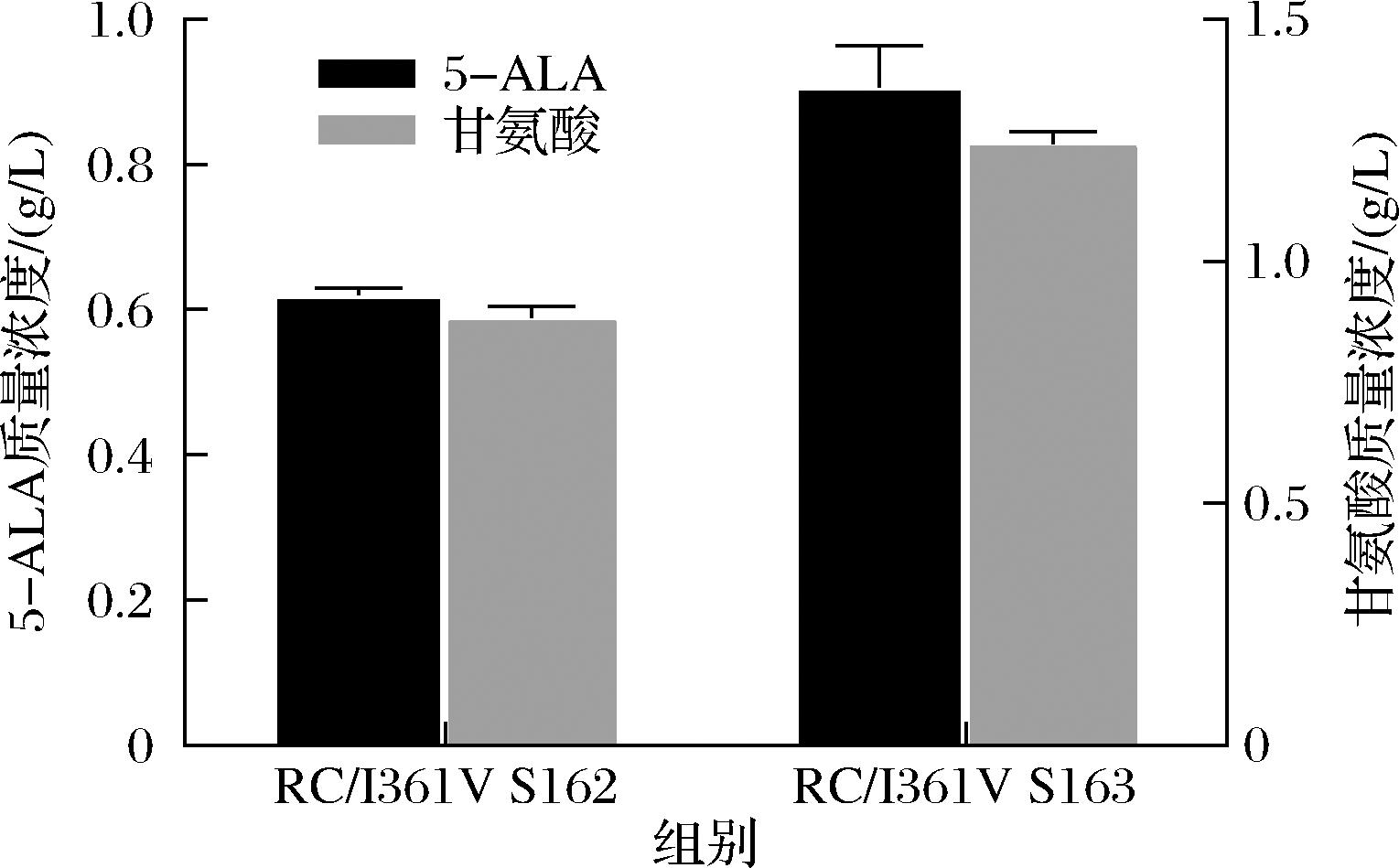
图4 摇瓶发酵验证弱化gcsH基因对5-ALA积累的影响
Fig.4 Effect of weaken gcsH gene on 5-ALA accumulation in erlenmeyer flasks
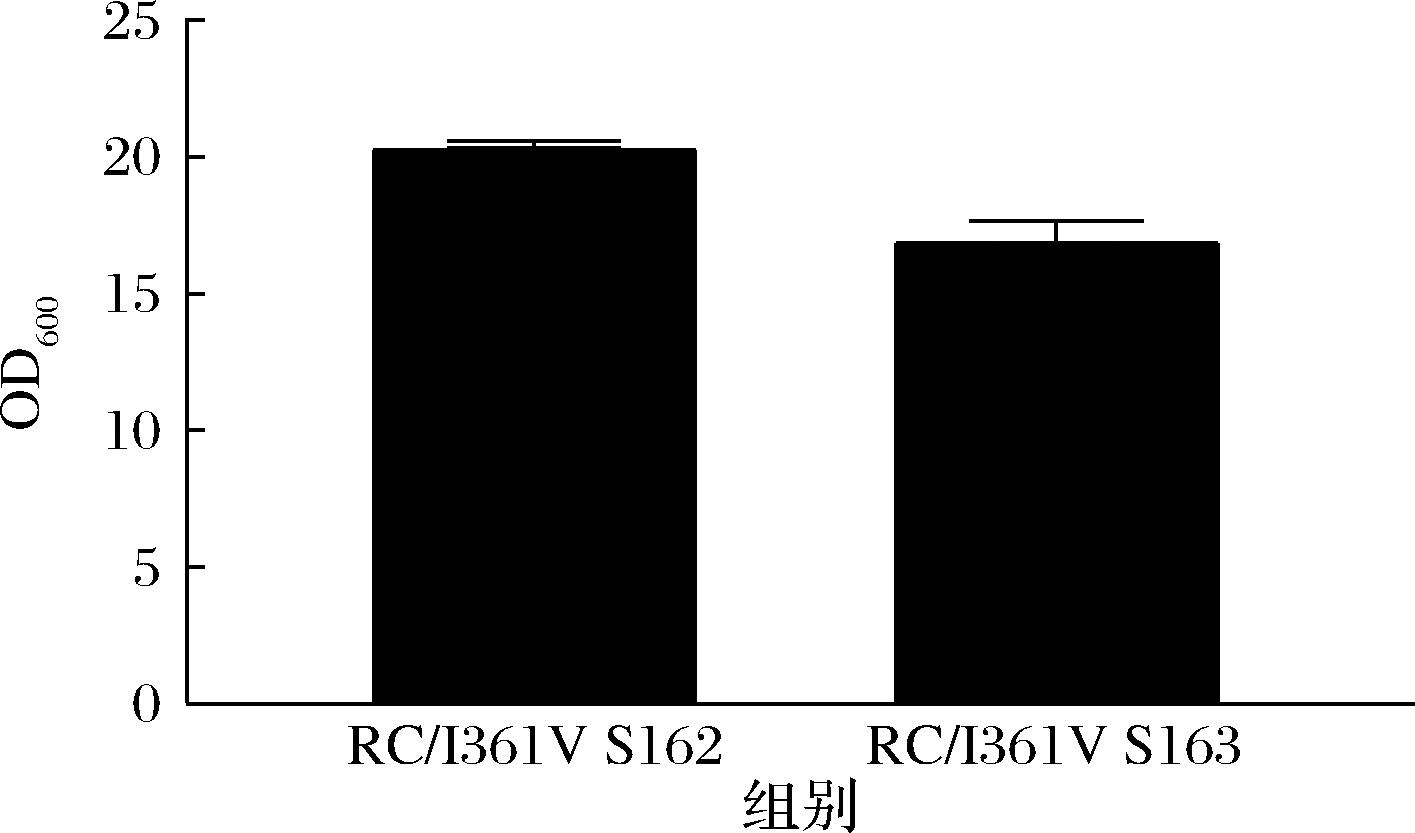
图5 摇瓶发酵验证弱化gcsH基因对菌株生长特性的影响
Fig.5 Effect of weaken gcsH gene on growth characteristics of bacterial strains in erlenmeyer flasks
2.4 敲除kbL基因对5-ALA积累的影响
kbL是编码甘氨酸C-乙酰转移酶的基因,主要控制甘氨酸到苏氨酸的相互转化,敲除kbL可以实现大肠杆菌胞内甘氨酸积累,其具体代谢途径如图6所示,在S163上继续敲除kbL基因得到S164菌株。
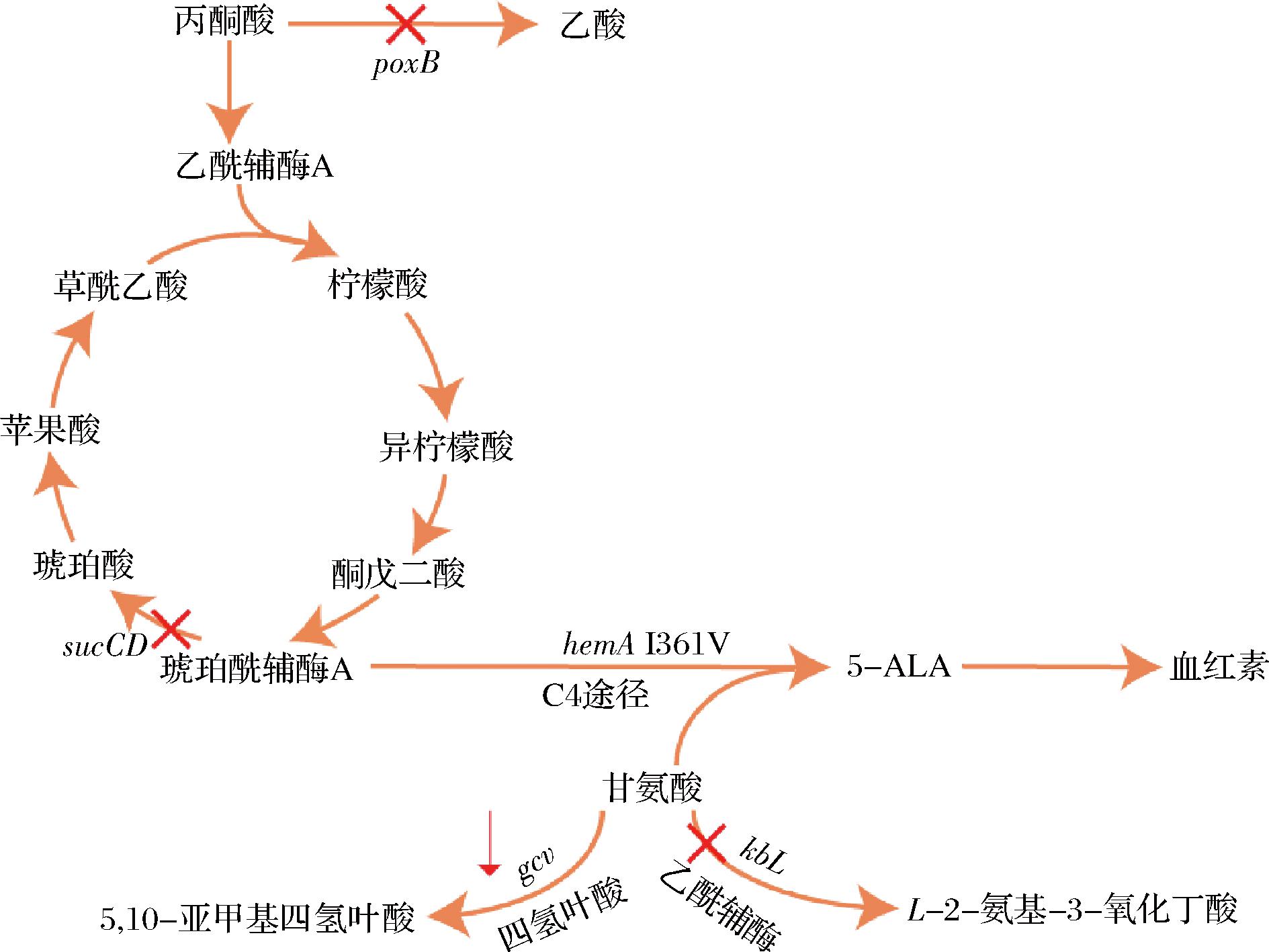
图6 5-ALA天然合成途径及代谢调控示意图
Fig.6 Schematic diagram of natural synthesis pathway and metabolic regulation of 5-ALA
为了测试敲除kbL对5-ALA积累的影响,将RC/I361V突变体转化S164中,28 ℃下添加2 g/L甘氨酸培养,测定各菌株发酵液的5-ALA产量及甘氨酸残留量。结果如图7所示,弱化了gcsH和敲除kbL的RC/I361V S164菌株中5-ALA的产量达到了1.5 g/L,比对照菌株RC/I361V S162提高了1.45倍,外源甘氨酸的利用减少了21%。该结果表明敲除kbL基因有助于5-ALA的积累。
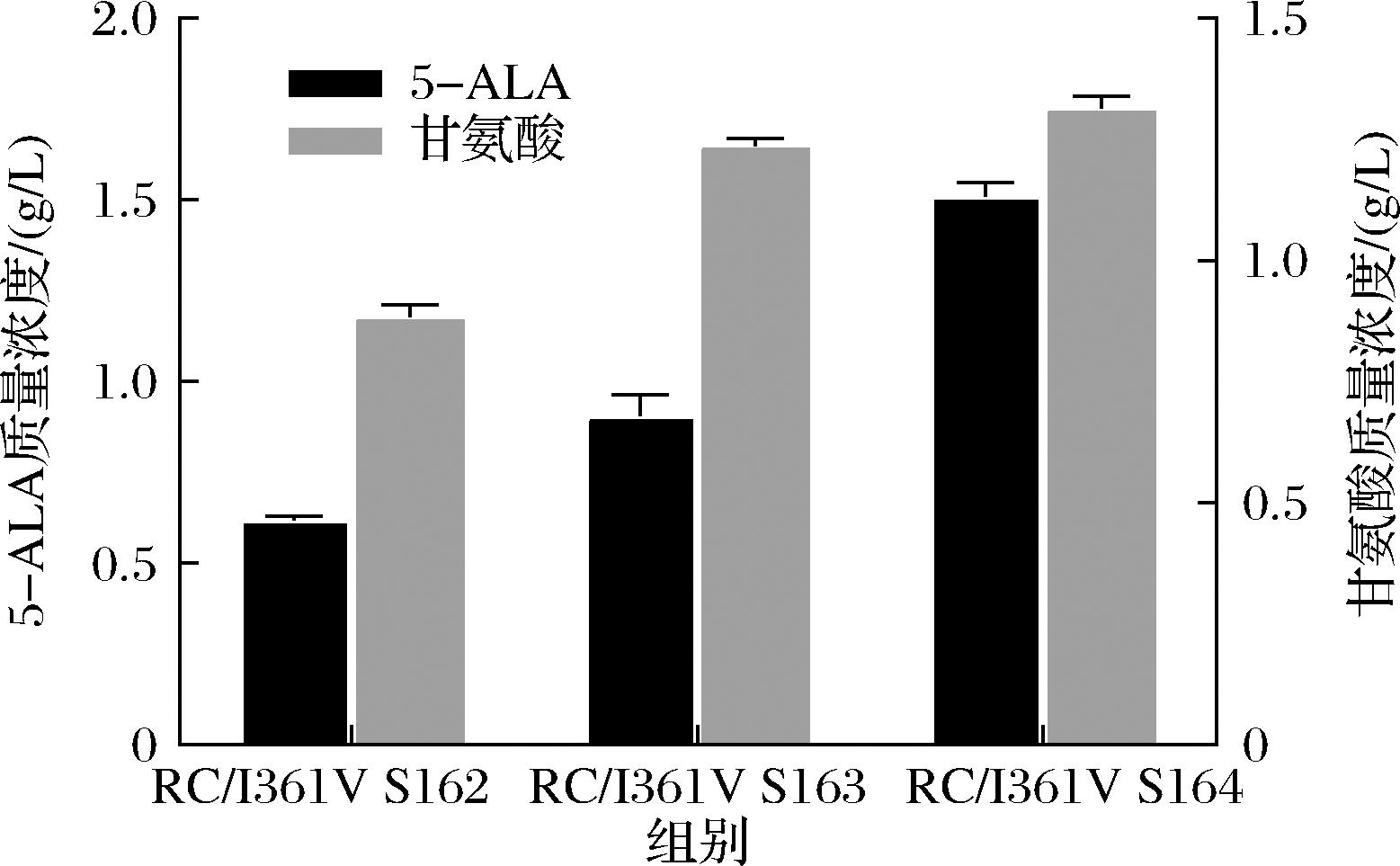
图7 摇瓶发酵验证弱化gcsH基因和敲除kbL对5-ALA积累的影响
Fig.7 Effect of weaken gcsH gene and knockout kbL on 5-ALA accumulation in erlenmeyer flasks
如图8所示,摇瓶发酵实验结果表明,摇瓶发酵实验结果表明,菌株RC/I361V S164与出发菌株RC/I361V S162生长无明显差异。
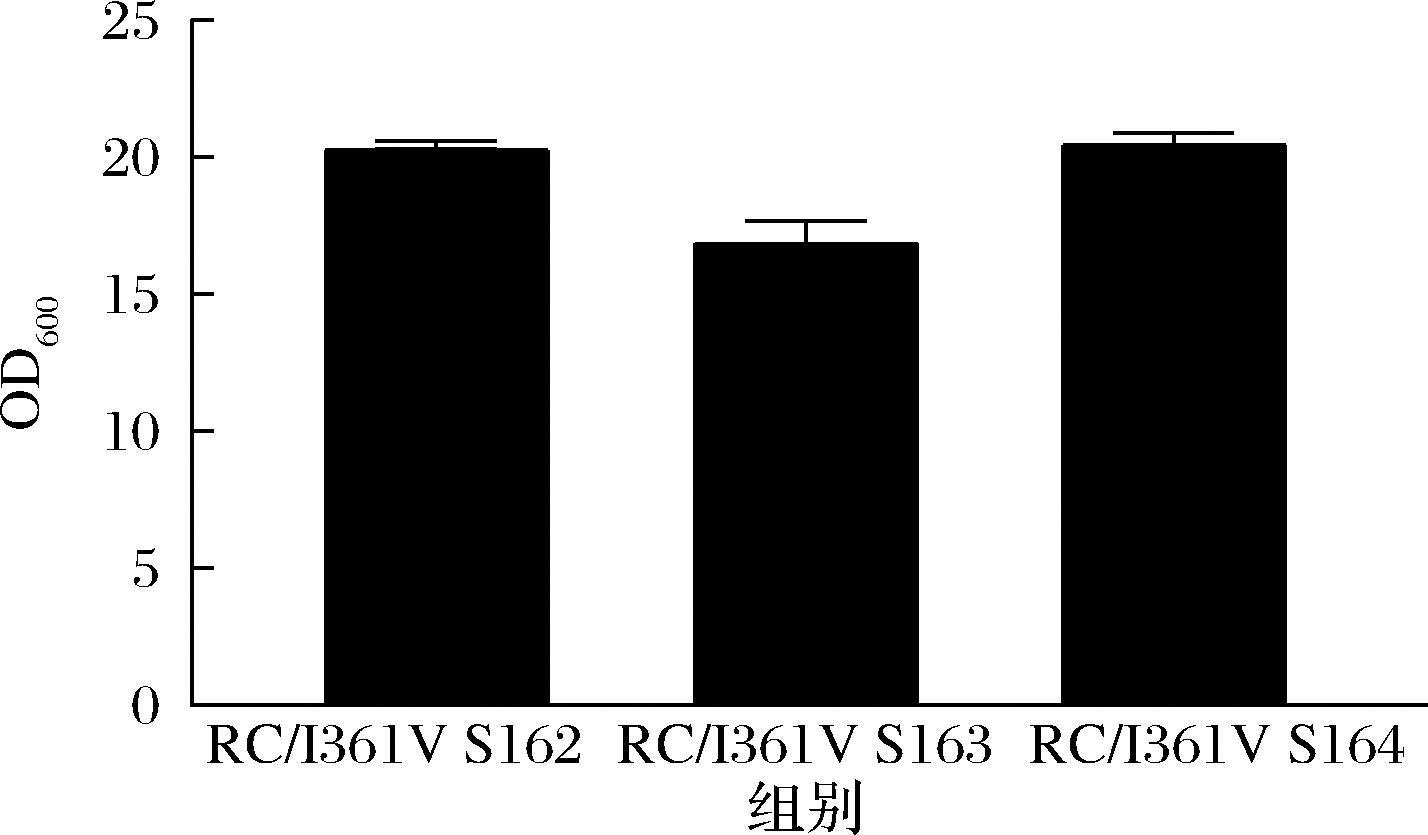
图8 摇瓶发酵验证弱化gcsH基因和敲除kbL对菌株生长特性的影响
Fig.8 Effect of weaken gcsH gene and knockout kbL on growth characteristics of bacterial strains in erlenmeyer flasks
2.5 敲除poxB对5-ALA积累的影响
poxB编码丙酮酸脱氢酶,控制丙酮酸代谢下游生产乙酸的途径,敲除poxB基因可以显著减少大肠杆菌在发酵过程中乙酸的积累并提高三羧酸循环的通量,在S164上继续敲除poxB基因得到S165菌株。
将RC/I361V突变体质粒转入改造后的S165菌株,28 ℃下添加2 g/L甘氨酸培养,测定各菌株发酵液的5-ALA产量及甘氨酸残留量,结果如图9所示,5-ALA产量由(S162)0.61 g/L提高到(S165)2.01 g/L,且培养基中甘氨酸的剩余量逐步提高,对比RC/I361V S162外源甘氨酸的利用减少了51%。说明甘氨酸的消耗逐步降低,这为后续5-ALA生物合成中降低甘氨酸用量提供了新的思路。
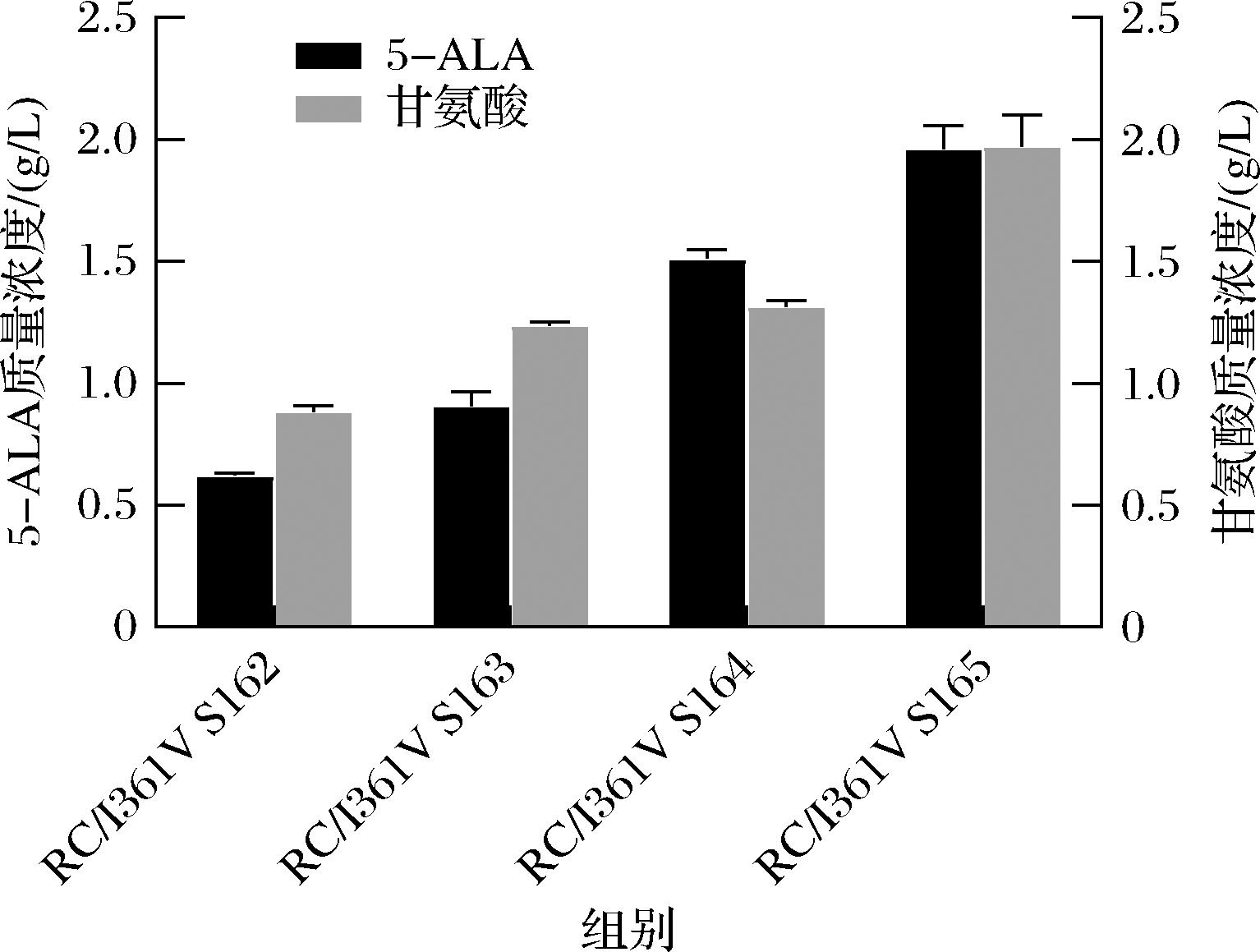
图9 摇瓶发酵验证弱化gcsH基因和敲除kbL、poxB对5-ALA积累的影响
Fig.9 Effect of weaken gcsH gene and knockout kbL and poxB on 5-ALA accumulation in erlenmeyer flasks
如图10所示,摇瓶发酵实验结果表明,摇瓶发酵实验结果表明,菌株RC/I361V S165与出发菌株RC/I361V S162生长无明显差异。
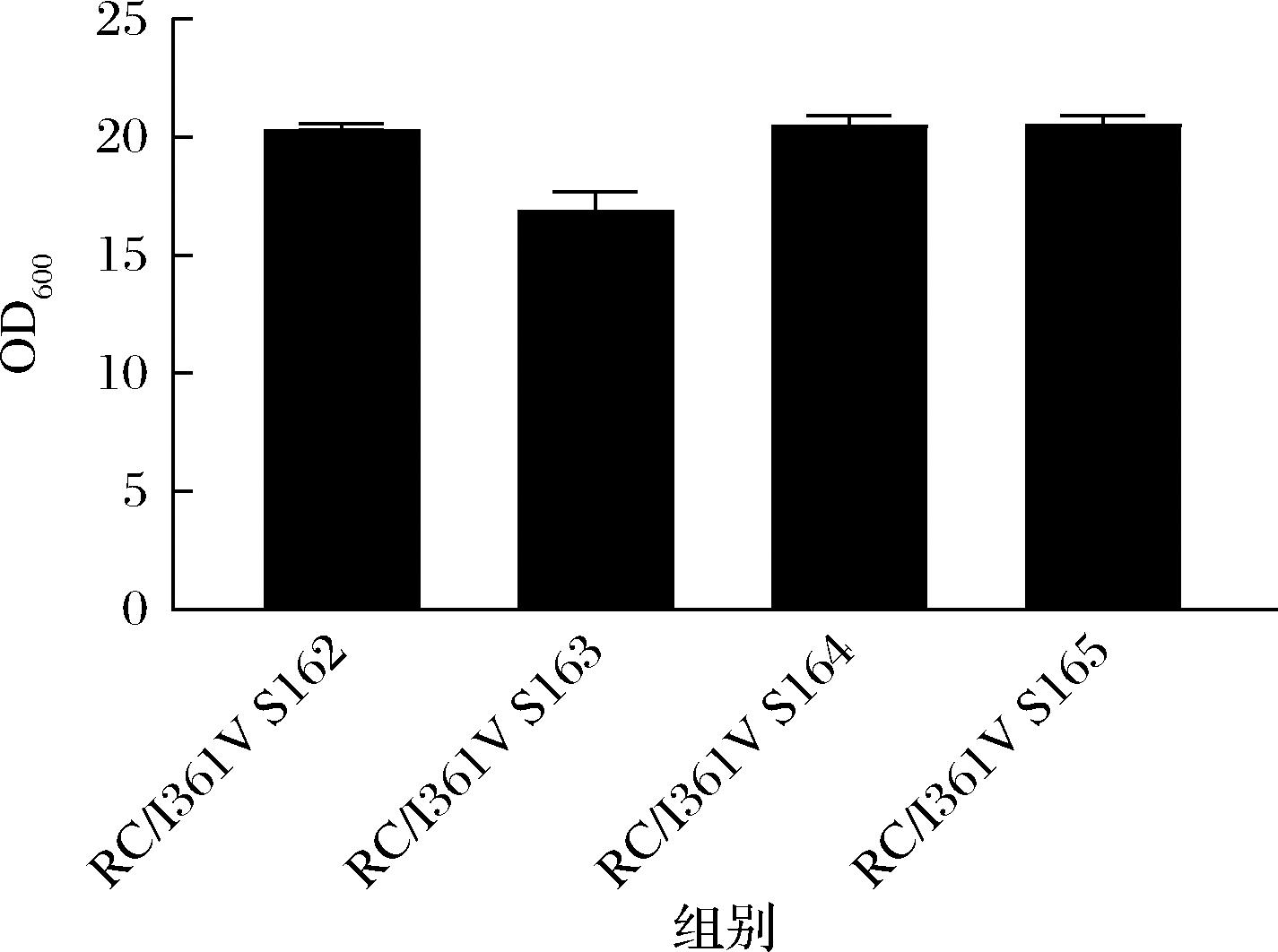
图10 摇瓶发酵验证弱化gcsH基因和敲除kbL、poxB对菌株生长特性的影响
Fig.10 Effect of weaken gcsH gene and knockout kbL and poxB on growth characteristics of bacterial strains in erlenmeyer flasks
3 结论与讨论
本文先对来源于R.capsulatus的ALAS进行改造,通过定点突变RC ALAS活性位点周围的氨基酸残基,筛选得到酶活力提高1.5倍的突变体RC/I361V,结果证明通过突变RC ALAS活性点的氨基酸来改变其结构特征和空间构象可以实现酶活力的提高,为未来对ALAS的改造提供了新的设计思路。然后通过对E.coli中5-ALA的合成及前体甘氨酸的代谢途径进行分析,提出弱化gcsH基因,敲除甘氨酸代谢途径kbL基因和编码丙酮酸脱氢酶poxB基因有利于5-ALA合成的设想。通过弱化gcsH基因和敲除甘氨酸代谢途径kbL基因,可以减少甘氨酸的代谢分流,使得更多的甘氨酸用于5-ALA的合成。敲除poxB基因可以显著降低乙酸的合成,减少丙酮酸的消耗,增加流向三羧酸循环的碳通量。这有助于提高细胞内的ATP和还原力(NADH/NADPH)水平,从而为5-ALA的合成提供更多的能量和前体物质。通过实验证实了弱化gcsH基因,敲除甘氨酸代谢途径kbL基因和编码丙酮酸脱氢酶poxB基因均可以显著提高菌株积累5-ALA的能力,弱化gcsH的RC/I361V S163菌株中5-ALA的产量达到了1 g/L,比对照菌株RC/I361V S162提高了64%;弱化了gcsH和敲除kbL的RC/I361V S164菌株中5-ALA的产量达到了1.5 g/L,比对照菌株RC/I361V S162提高了1.45倍;在此基础上敲除poxB得到S165菌株,RC/I361V S165的摇瓶产量达到2.01 g/L。对于甘氨酸的代谢改造,显著降低了菌株消耗外源添加甘氨酸的量,提高了菌株合成5-ALA的能力。
甘氨酸是利用C4途径合成5-ALA的重要前体,大肠杆菌中甘氨酸的合成和代谢与一碳代谢密切相关,如敲除由丝氨酸合成甘氨酸glyA基因细胞无法生长,敲除甘氨酸裂解酶系的H蛋白细胞生长也不稳定[14]。在培养基中外源添加甘氨酸会使得细胞利用甘氨酸生成一碳单位及还原力,且过量的甘氨酸还会影响细胞生长[19]。本研究通过对甘氨酸裂解酶系H蛋白进行点突变改造,降低其降解甘氨酸的能力;阻断甘氨酸向苏氨酸的转化,同时减少乙酰辅酶A的消耗。虽然改造后的重组菌株摇瓶发酵5-ALA的产量比之目前研究最高的产量还有很大的提高空间,但是本研究在提高5-ALA产量的同时,降低了甘氨酸消耗,为后续5-ALA生物合成中甘氨酸的有效利用提供了新的思路。
[1] 安玉涵, 马伊丹, 杨佳, 等.5-氨基乙酰丙酸(5-ALA)的生物学作用及其在动物生产中的应用[J].饲料研究, 2023, 46(19):150-154.
AN Y H, MA Y D, YANG J, et al.Biological function of 5-aminolevulinic acid(5-ALA) and its application in animals production[J].Feed Research, 2023, 46(19):150-154.
[2] 高艳霞, 刘睿, 刘南南, 等.5-氨基乙酰丙酸及其前体药物介导的光动力疗法在恶性肿瘤治疗中的应用研究进展[J].山东医药, 2022, 62(8):90-94.
GAO Y X, LIU R, LIU N N, et al.Progress in the application of 5- aminolevulinic acid and its prodrug mediated photodynamic therapy in the treatment of malignant tumors[J].Shandong Medical Journal, 2022, 62(8):90-94.
[3] 魏敏华, 李宇虹, 张佳蓉, 等.代谢工程构建谷氨酸棒杆菌合成5-氨基乙酰丙酸[J].食品与发酵工业, 2022, 48(14):9-15.
WEI M H, LI Y H, ZHANG J R, et al.Metabolic engineering of Corynebacterium glutamicum chassis for biosynthesis of 5-aminolevulinic acid[J].Food and Fermentation Industries, 2022, 48(14):9-15.
[4] 王帅, 张乐乐, 刘恩昊, 等.5-氨基乙酰丙酸的生物合成及应用研究进展[J].天津化工, 2023, 37(S2):77-81.
WANG S, ZHANG L L, LIU E H, et al.Progress in biosynthesis and application of 5-aminolevulinic acid[J].Tianjin Chemical Industry, 2023, 37(S2):77-81.
[5] DING W W, WENG H J, DU G C, et al.5-Aminolevulinic acid production from inexpensive glucose by engineering the C4 pathway in Escherichia coli[J].Journal of Industrial Microbiology &Biotechnology, 2017, 44(8):1127-1135.
[6] CHRISTEN P, MEHTA P K, SANDMEIER E.Molecular evolution of pyridoxal-5′-phosphate-dependent enzymes[C].Biochemistry of Vitamin B6 and PQQ.Basel:Springer, 1994:9-13.
[7] MEHTA P K, CHRISTEN P.Homology of 1-aminocyclopropane-1-carboxylate synthase, 8-amino-7-oxononanoate synthase, 2-amino-6-caprolactam racemase, 2, 2-dialkylglycine decarboxylase, glutamate-1-semialdehyde 2, 1-aminomutase and isopenicillin-N-epimerase with aminotransferases[J].Biochemical and Biophysical Research Communications, 1994, 198(1):138-143.
[8] FERREIRA G C, NEAME P J, DAILEY H A.Heme biosynthesis in mammalian systems:Evidence of a Schiff base linkage between the pyridoxal 5′-phosphate cofactor and a lysine residue in 5-aminolevulinate synthase[J].Protein Science, 1993, 2(11):1959-1965.
[9] KAUFHOLZ A L, HUNTER G A, FERREIRA G C, et al.Aminolaevulinic acid synthase of Rhodobacter capsulatus:High-resolution kinetic investigation of the structural basis for substrate binding and catalysis[J].The Biochemical Journal, 2013, 451(2):205-216.
[10] HE G M, JIANG M R, CUI Z Z, et al.Construction of 5-aminolevulinic acid synthase variants by cysteine-targeted mutation to release heme inhibition[J].Journal of Bioscience and Bioengineering, 2022, 134(5):416-423.
[11] DU S, ZHENG N, ZHANG Z H, et al.Rational design engineering of 5-aminolevulinate synthase with activity and stability enhancement[J].Journal of Agricultural and Food Chemistry, 2025, 73(3):1892-1901.
[12] 陈久洲, 王钰, 蒲伟, 等.5-氨基乙酰丙酸生物合成技术的发展及展望[J].合成生物学, 2021, 2(6):1000-1016.
CHEN J Z, WANG Y, PU W, et al.Advances and perspective on bioproduction of 5-aminolevulinic acid[J].Synthetic Biology Journal, 2021, 2(6):1000-1016.
[13] WANG Q, JIA M J, LI H J, et al.Design of a genetically encoded biosensor for high-throughput screening and engineering 5-aminolevulinic acid hyper-producing Escherichia coli[J].ACS Sustainable Chemistry &Engineering, 2024, 12(12):4846-4857.
[14] ZHOU H M, ZHANG C Y, LI Z L, et al.Systematic development of a highly efficient cell factory for 5-aminolevulinic acid production[J].Trends in Biotechnology, 2024, 42(11):1479-1502.
[15] MAUZERALL D, GRANICK S.The occurrence and determination of delta-amino-levulinic acid and porphobilinogen in urine[J].The Journal of Biological Chemistry, 1956, 219(1):435-446.
[16] ZHANG H, LI Y C, NIE J L, et al.Structure-based dynamic analysis of the glycine cleavage system suggests key residues for control of a key reaction step[J].Communications Biology, 2020, 3:756.
[17] ASTNER I, SCHULZE J O, VAN DEN HEUVEL J, et al.Crystal structure of 5-aminolevulinate synthase, the first enzyme of heme biosynthesis, and its link to XLSA in humans[J].The EMBO Journal, 2005, 24(18):3166-3177.
[18] 蒲伟, 陈久洲, 孙村民, 等.琥珀酸脱氢酶或琥珀酰辅酶A合成酶缺失促进大肠杆菌积累5-氨基乙酰丙酸[J].生物工程学报, 2013, 29(10):1494-1503.
PU W, CHEN J Z, SUN C M, et al.Deficiency of succinic dehydrogenase or succinyl-CoA synthetase enhances the production of 5-aminolevulinic acid in recombinant Escherichia coli[J].Chinese Journal of Biotechnology, 2013, 29(10):1494-1503.
[19] 李凤辰, 段纪甫, 宫衡.氨基酸对大肠杆菌BL21生长影响的研究[J].工业微生物, 2013, 43(3):29-31.
LI F C, DUAN J F, GONG H.Effects of amino acid on growth of Escherichia coli BL21[J].Industrial Microbiology, 2013, 43(3):29-31.