色醇(tryptophol,IET)是色氨酸(L-tryptophan,Trp)的衍生物,广泛存在于自然界中。在植物中,IET可作为生长因子调节植物生长;在自然微生物群落中,可作为群体感应分子参与细胞间通讯,并表现出抗菌活性;此外,它还具有诱导细胞凋亡、抗肿瘤等生物活性[1]。同时IET所具有的吲哚结构和可修饰的羟乙基结构,使其衍生物能够成为合成一系列具备显著药理特性化合物[如具抗肿瘤、抗菌和抗氧化特性的植物来源化合物毒扁豆次碱(physovenine)、一种白坚木属单萜吲哚类生物碱(goniomitine)等]的关键中间体[2]。因此,IET在农业生产、临床研究等多个领域展现出潜在的应用价值。
目前尚未有工业化规模的单独生产IET案例。但由于吲哚结构在医药分子中的重要性及吲哚化学的不断发展,IET及其衍生物的市场需求巨大,主流生产方式全部为化学合成[2],IET衍生物的生产规模可达到公斤级[3]。尽管利用化学合成方法,IET的产率最高可达95%[4],但仍存在副产物积累难以去除、催化反应工艺复杂以及生产能耗大等问题。为适应当前绿色环保、可持续发展的需求,生物法合成IET是一种理想的替代方案。酵母内源的艾利希途径(Ehrlich pathway)[5-6]能够将芳香族氨基酸经过三步反应转化为对应高级醇,因此酵母已成为目前生产IET最常用的底盘菌种,如一种接合酵母(Zygosaccharomyces priorianus)[7]和汉逊德巴利酵母(Debaryomyces hansenii)[8]。然而,目前大部分生物法合成IET的研究仍集中于通过外源添加Trp作为底物,与廉价的碳源相比,原料成本较高,难以实现工业化生产。
本团队先前研究已成功构建一株酿酒酵母(Saccharomyces cerevisiae)菌株,实现以葡萄糖为碳源合成IET[1],5 L补料分批发酵后可达1.04 g/L,是目前生物法从头合成IET的最高产量,且超过此前报道的微生物首次从头合成IET产量的2倍以上[9]。该研究还证明,内源Trp代谢通量不足是酵母中从未实现IET高效从头合成的主要原因。该菌株通过同时过表达TRP1、TRP2S65R, S76L、TRP3-5这5个Trp合成相关基因(其中S65R、S76L为解除TRP2的反馈抑制突变位点),显著提高了Trp的代谢通量,进而有效提升了IET的产量。然而酿酒酵母中Trp合成的相关代谢途径的调控机制尚不成熟,仍需深入研究[10];此外,除了调控Trp合成模块外,该菌株还对艾利希途径及芳香族氨基酸合成途径进行了调控,共涉及4个代谢模块。因此该工程菌株内已负担多重遗传改造,想在此基础上进一步提升IET的产量面临较大挑战。
为解决上述问题,本研究引入共培养策略[11-12],通过劳动分工将较长的代谢途径模块化分割,并将不同模块的代谢任务分配给适宜的微生物种群,从而降低单菌株的代谢负担,同时利用各个种群的天然代谢优势,提升目标产物的合成效率,目前已有大量研究成功构建能够合成复杂化合物的微生物群落[13-14]。针对IET合成,本研究设计微生物群落如图1所示,Trp作为一种小分子化合物,可通过被动扩散或主动运输跨越细胞膜,因此被确定为群落内的中间代谢产物。基于此,以Trp合成为节点,将IET合成途径划分为2个模块:上游模块从碳源合成Trp,下游模块从Trp合成IET。
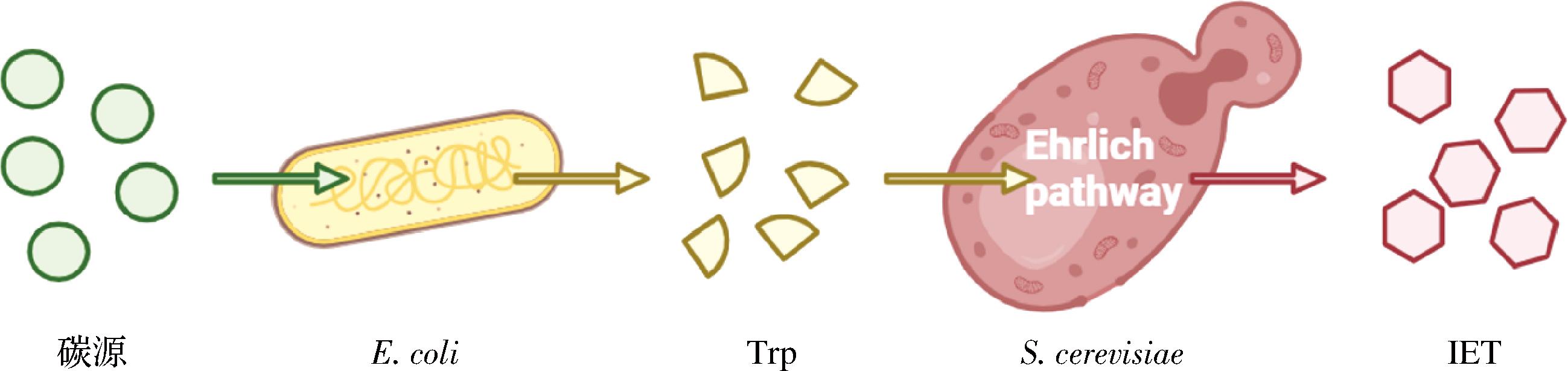
图1 从头合成IET的微生物群落设计
Fig.1 Design of a microbial consortium for de novo biosynthesis of IET
在上游模块,选择大肠杆菌(Escherichia coli)作为底盘菌株。大肠杆菌在Trp代谢研究中具有成熟的机制、完善的理论基础以及基因编辑的便利性,且已有大量研究通过代谢工程优化其Trp生产,并实现了工业级产量[15-16],因此成为理想的Trp生产平台。在下游模块,酿酒酵母负责Trp转化为IET的代谢任务。酿酒酵母不仅具有天然的艾利希途径,能将Trp转化为IET,而且作为真核生物,具备完整的蛋白质加工与翻译系统、代谢分区明确的细胞器,且比起其他具有艾利希途径的真核微生物,具备更成熟的基因编辑工具,这些优势使其在合成复杂结构化合物方面具有独特的优势[17]。
本研究首先通过相关基因的过表达构建上下游模块的2个底盘菌株,使其具备合成Trp和IET的能力;然后探究共培养群落的生产能力,并对群落整体组成进行优化,包括优化接种比例和接种量,最终成功构建能够从头合成IET的微生物群落。本研究为IET的生物合成提供了一种新的研究思路。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株、质粒与引物
大肠杆菌BL21(DE3)用作扩增大肠杆菌目标基因和Trp生产的出发菌株,DH5α用于质粒的构建与质粒保存。酿酒酵母BY4741用作扩增酿酒酵母目标基因及IET生产的出发菌株。
本实验构建和使用的菌株和质粒如表1、表2所示,设计的引物如表3所示。
表1 本研究构建和使用的菌株
Table 1 Strains in this study
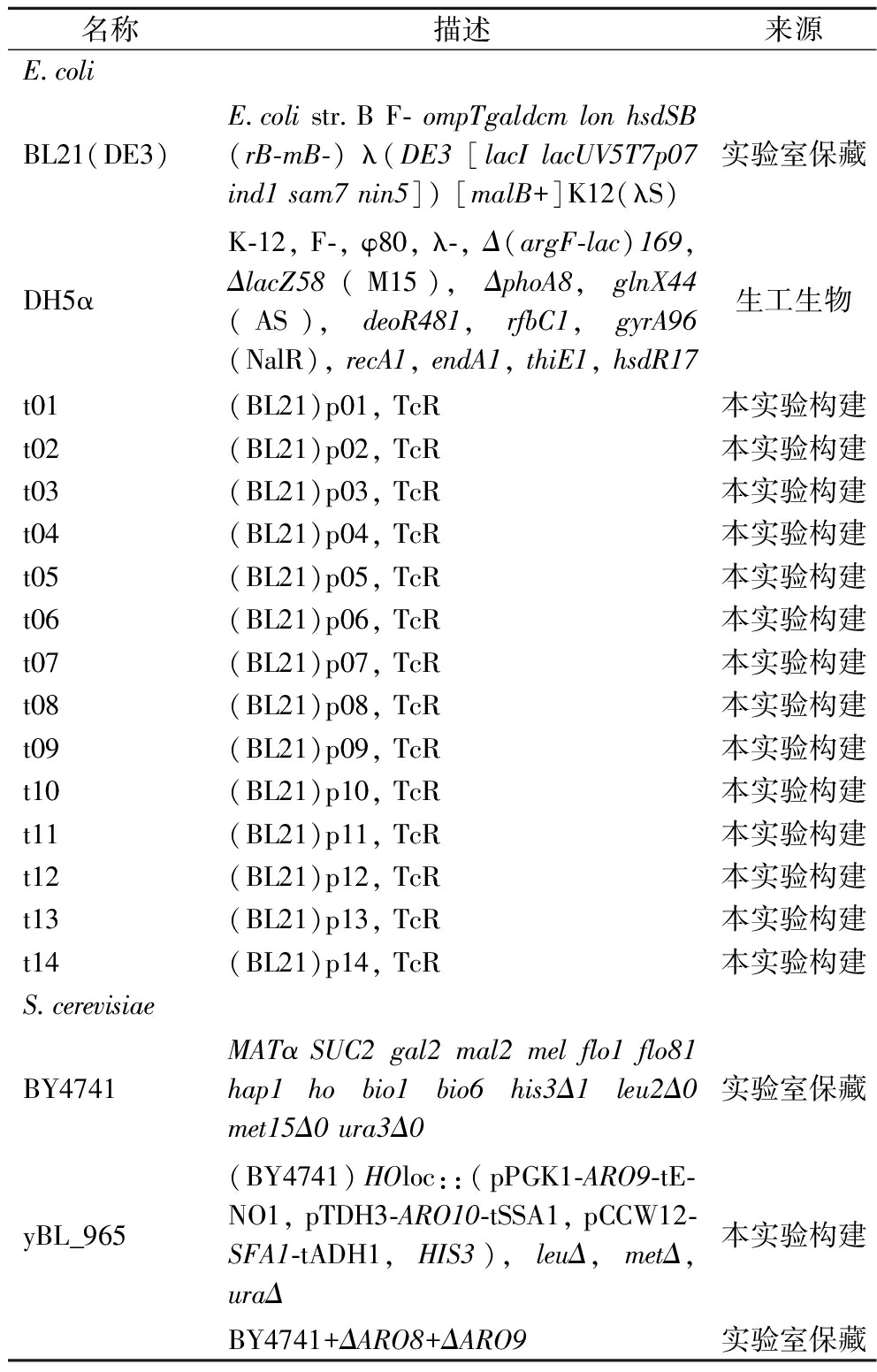
名称描述来源E.coliBL21(DE3)E.coli str.B F- ompTgaldcm lon hsdSB(rB-mB-) λ(DE3 [lacI lacUV5T7p07 ind1 sam7 nin5]) [malB+]K12(λS)实验室保藏DH5αK-12, F-, φ80, λ-, Δ(argF-lac)169, ΔlacZ58(M15), ΔphoA8, glnX44(AS), deoR481, rfbC1, gyrA96(NalR), recA1, endA1, thiE1, hsdR17生工生物t01(BL21)p01, TcR本实验构建t02(BL21)p02, TcR本实验构建t03(BL21)p03, TcR本实验构建t04(BL21)p04, TcR本实验构建t05(BL21)p05, TcR本实验构建t06(BL21)p06, TcR本实验构建t07(BL21)p07, TcR本实验构建t08(BL21)p08, TcR本实验构建t09(BL21)p09, TcR本实验构建t10(BL21)p10, TcR本实验构建t11(BL21)p11, TcR本实验构建t12(BL21)p12, TcR本实验构建t13(BL21)p13, TcR本实验构建t14(BL21)p14, TcR本实验构建S.cerevisiaeBY4741MATα SUC2 gal2 mal2 mel flo1 flo81 hap1 ho bio1 bio6 his3Δ1 leu2Δ0 met15Δ0 ura3Δ0实验室保藏yBL_965(BY4741)HOloc::(pPGK1-ARO9-tE-NO1, pTDH3-ARO10-tSSA1, pCCW12-SFA1-tADH1, HIS3), leuΔ, metΔ, uraΔ本实验构建BY4741+ΔARO8+ΔARO9实验室保藏
表2 本研究构建和使用的质粒
Table 2 Plasmids in this study
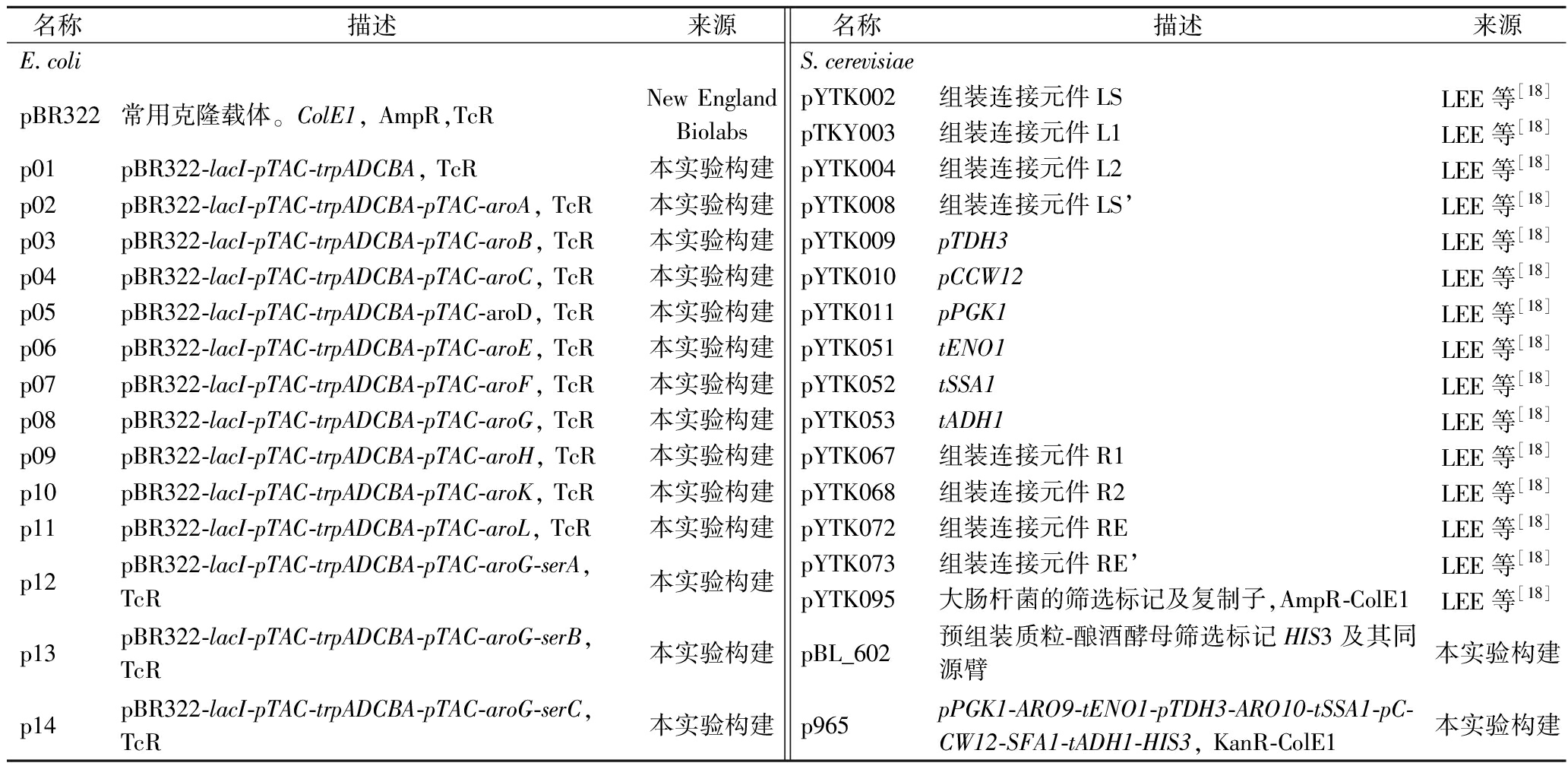
名称描述来源名称描述来源E.colipBR322常用克隆载体。ColE1, AmpR,TcRNew England Biolabsp01pBR322-lacI-pTAC-trpADCBA, TcR本实验构建p02pBR322-lacI-pTAC-trpADCBA-pTAC-aroA, TcR本实验构建p03pBR322-lacI-pTAC-trpADCBA-pTAC-aroB, TcR本实验构建p04pBR322-lacI-pTAC-trpADCBA-pTAC-aroC, TcR本实验构建p05pBR322-lacI-pTAC-trpADCBA-pTAC-aroD, TcR本实验构建p06pBR322-lacI-pTAC-trpADCBA-pTAC-aroE, TcR本实验构建p07pBR322-lacI-pTAC-trpADCBA-pTAC-aroF, TcR本实验构建p08pBR322-lacI-pTAC-trpADCBA-pTAC-aroG, TcR本实验构建p09pBR322-lacI-pTAC-trpADCBA-pTAC-aroH, TcR本实验构建p10pBR322-lacI-pTAC-trpADCBA-pTAC-aroK, TcR本实验构建p11pBR322-lacI-pTAC-trpADCBA-pTAC-aroL, TcR本实验构建p12pBR322-lacI-pTAC-trpADCBA-pTAC-aroG-serA, TcR本实验构建p13pBR322-lacI-pTAC-trpADCBA-pTAC-aroG-serB, TcR本实验构建p14pBR322-lacI-pTAC-trpADCBA-pTAC-aroG-serC, TcR本实验构建S.cerevisiaepYTK002组装连接元件LSLEE等[18]pTKY003组装连接元件L1LEE等[18]pYTK004组装连接元件L2LEE等[18]pYTK008组装连接元件LS’LEE等[18]pYTK009pTDH3LEE等[18]pYTK010pCCW12LEE等[18]pYTK011pPGK1LEE等[18]pYTK051tENO1LEE等[18]pYTK052tSSA1LEE等[18]pYTK053tADH1LEE等[18]pYTK067组装连接元件R1LEE等[18]pYTK068组装连接元件R2LEE等[18]pYTK072组装连接元件RELEE等[18]pYTK073组装连接元件RE’LEE等[18]pYTK095大肠杆菌的筛选标记及复制子,AmpR-ColE1LEE等[18]pBL_602预组装质粒-酿酒酵母筛选标记HIS3及其同源臂本实验构建p965pPGK1-ARO9-tENO1-pTDH3-ARO10-tSSA1-pC-CW12-SFA1-tADH1-HIS3, KanR-ColE1本实验构建
表3 本研究使用的引物
Table 3 Primers used in this study
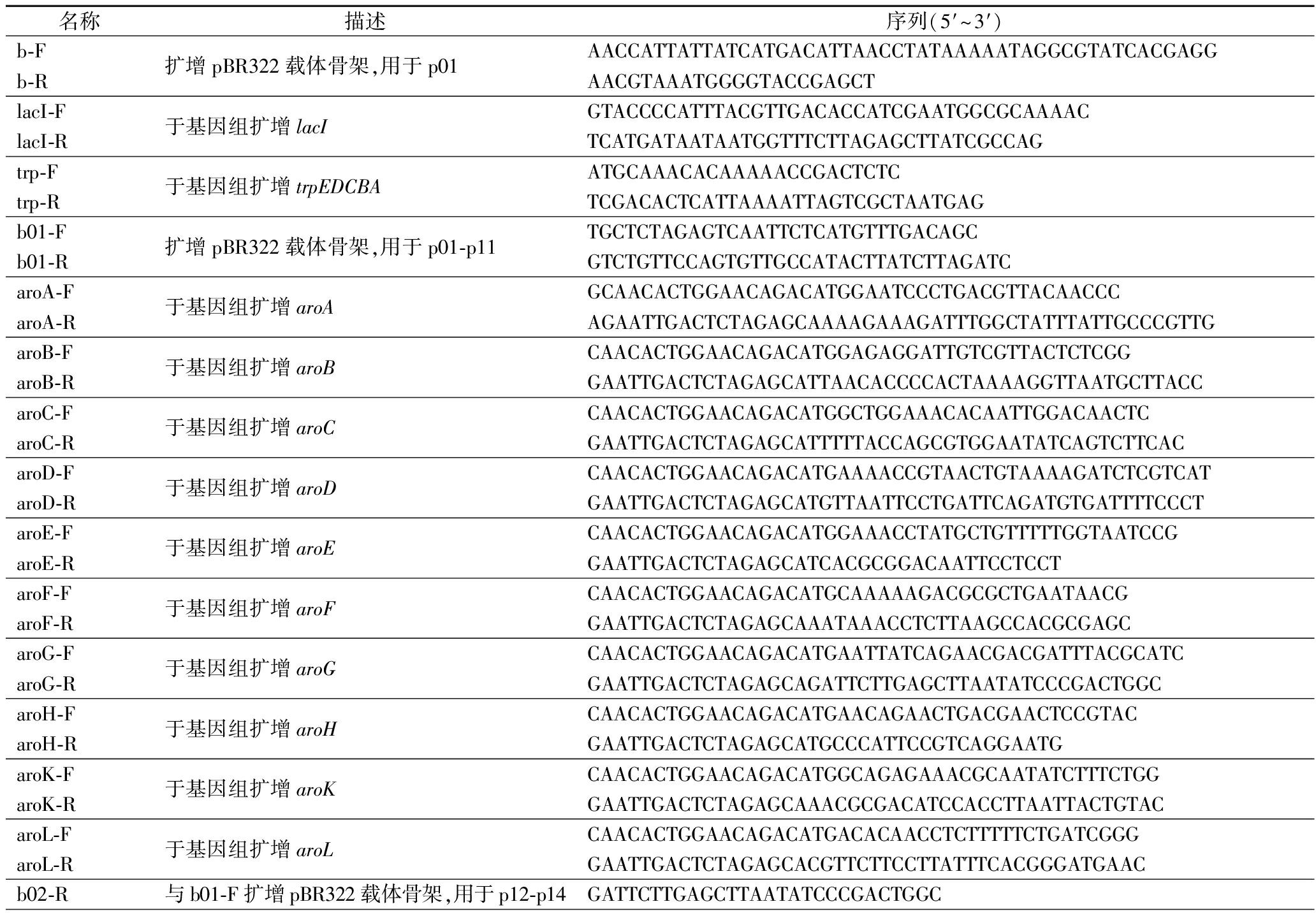
名称描述序列(5′~3′)b-Fb-R扩增pBR322载体骨架,用于p01AACCATTATTATCATGACATTAACCTATAAAAATAGGCGTATCACGAGGAACGTAAATGGGGTACCGAGCTlacI-FlacI-R于基因组扩增lacIGTACCCCATTTACGTTGACACCATCGAATGGCGCAAAACTCATGATAATAATGGTTTCTTAGAGCTTATCGCCAGtrp-Ftrp-R于基因组扩增trpEDCBAATGCAAACACAAAAACCGACTCTCTCGACACTCATTAAAATTAGTCGCTAATGAGb01-Fb01-R扩增pBR322载体骨架,用于p01-p11TGCTCTAGAGTCAATTCTCATGTTTGACAGCGTCTGTTCCAGTGTTGCCATACTTATCTTAGATCaroA-FaroA-R于基因组扩增aroAGCAACACTGGAACAGACATGGAATCCCTGACGTTACAACCCAGAATTGACTCTAGAGCAAAAGAAAGATTTGGCTATTTATTGCCCGTTGaroB-FaroB-R于基因组扩增aroBCAACACTGGAACAGACATGGAGAGGATTGTCGTTACTCTCGGGAATTGACTCTAGAGCATTAACACCCCACTAAAAGGTTAATGCTTACCaroC-FaroC-R于基因组扩增aroCCAACACTGGAACAGACATGGCTGGAAACACAATTGGACAACTCGAATTGACTCTAGAGCATTTTTACCAGCGTGGAATATCAGTCTTCACaroD-FaroD-R于基因组扩增aroDCAACACTGGAACAGACATGAAAACCGTAACTGTAAAAGATCTCGTCATGAATTGACTCTAGAGCATGTTAATTCCTGATTCAGATGTGATTTTCCCTaroE-FaroE-R于基因组扩增aroECAACACTGGAACAGACATGGAAACCTATGCTGTTTTTGGTAATCCGGAATTGACTCTAGAGCATCACGCGGACAATTCCTCCTaroF-FaroF-R于基因组扩增aroFCAACACTGGAACAGACATGCAAAAAGACGCGCTGAATAACGGAATTGACTCTAGAGCAAATAAACCTCTTAAGCCACGCGAGCaroG-FaroG-R于基因组扩增aroGCAACACTGGAACAGACATGAATTATCAGAACGACGATTTACGCATCGAATTGACTCTAGAGCAGATTCTTGAGCTTAATATCCCGACTGGCaroH-FaroH-R于基因组扩增aroHCAACACTGGAACAGACATGAACAGAACTGACGAACTCCGTACGAATTGACTCTAGAGCATGCCCATTCCGTCAGGAATGaroK-FaroK-R于基因组扩增aroKCAACACTGGAACAGACATGGCAGAGAAACGCAATATCTTTCTGGGAATTGACTCTAGAGCAAACGCGACATCCACCTTAATTACTGTACaroL-FaroL-R于基因组扩增aroLCAACACTGGAACAGACATGACACAACCTCTTTTTCTGATCGGGGAATTGACTCTAGAGCACGTTCTTCCTTATTTCACGGGATGAACb02-R与b01-F扩增pBR322载体骨架,用于p12-p14GATTCTTGAGCTTAATATCCCGACTGGC
续表3

名称描述序列(5′~3′)serA-FserA-R于基因组扩增serATATTAAGCTCAAGAATCCGACGCAAACGTTCATATTGCCGGAATTGACTCTAGAGCAGCAACGCGGCAACGGTserB-FserB-R于基因组扩增serBTATTAAGCTCAAGAATCTTATTTTCCCTGCTTCGAACGATTTTACAGGGAATTGACTCTAGAGCAGGTGTACCTCGTTAATGCTGTGCCserC-FserC-R于基因组扩增serCTATTAAGCTCAAGAATCACAGGAATAATGTATTACCTGTGGTCGCGAATTGACTCTAGAGCAGAACTCAACTCTCTACAACAGAAATAAAAACCCCARO9-FARO9-R于基因组扩增ARO9GCATCGTCTCATCGGTCTCATATGACTGCTGGTTCTGCCATGCCGTCTCAGGTCTCAGGATCCACTTTTATAGTTGTCAAAAAATTCTTTTATGCCARO10-FARO10-R于基因组扩增ARO10GCATCGTCTCATCGGTCTCATATGGCACCTGTTACAATTGAAAAGTATGCCGTCTCAGGTCTCAGGATCCTTTTTTATTTCTTTTAAGTGCCGCTGCSFA1-FSFA1-R于基因组扩增SFA1GCATCGTCTCATCGGTCTCATATGTCCGCCGCTACTGTTATGCCGTCTCAGGTCTCAGGATCCTTTTATTTCATCAGACTTCAAGACGGTTC
1.1.2 试剂与培养基
培养基(g/L):大肠杆菌单独培养使用LB培养基(酵母粉5、蛋白胨10、NaCl 10);酿酒酵母单独培养使用YTD培养基(酵母粉10、蛋白胨20、葡萄糖20);大肠杆菌与酿酒酵母混合培养所用培养基命名为YTNa培养基(酵母粉17.5、蛋白胨15、NaCl 5、葡萄糖10[19])。
高保真DNA聚合酶:Fly,用于扩增基因组上目标片段,来自TransGen Biotech;Phanta Flash #P510,用于扩增载体质粒的骨架部分,来自Vazyme。
同源重组连接酶:MultiF,ABclonal。
抗生素与诱导剂:四环素50 μg/mL、IPTG 1 mmol/L、氨苄青霉素50 μg/mL。
1.2 仪器与设备
LC-20AT 高效液相色谱-紫外检测器,日本SHIMADZU公司;Tmax Bio 5L发酵罐,天木生物科技有限公司。
1.3 实验方法
1.3.1 质粒构建
大肠杆菌内的质粒构建方法为重叠延伸PCR和同源组装,酿酒酵母内的质粒构建方法及工具盒Yeast Toolkit(YTK)参考LEE等[18],构建流程示意图如图2-b、图5-a所示。
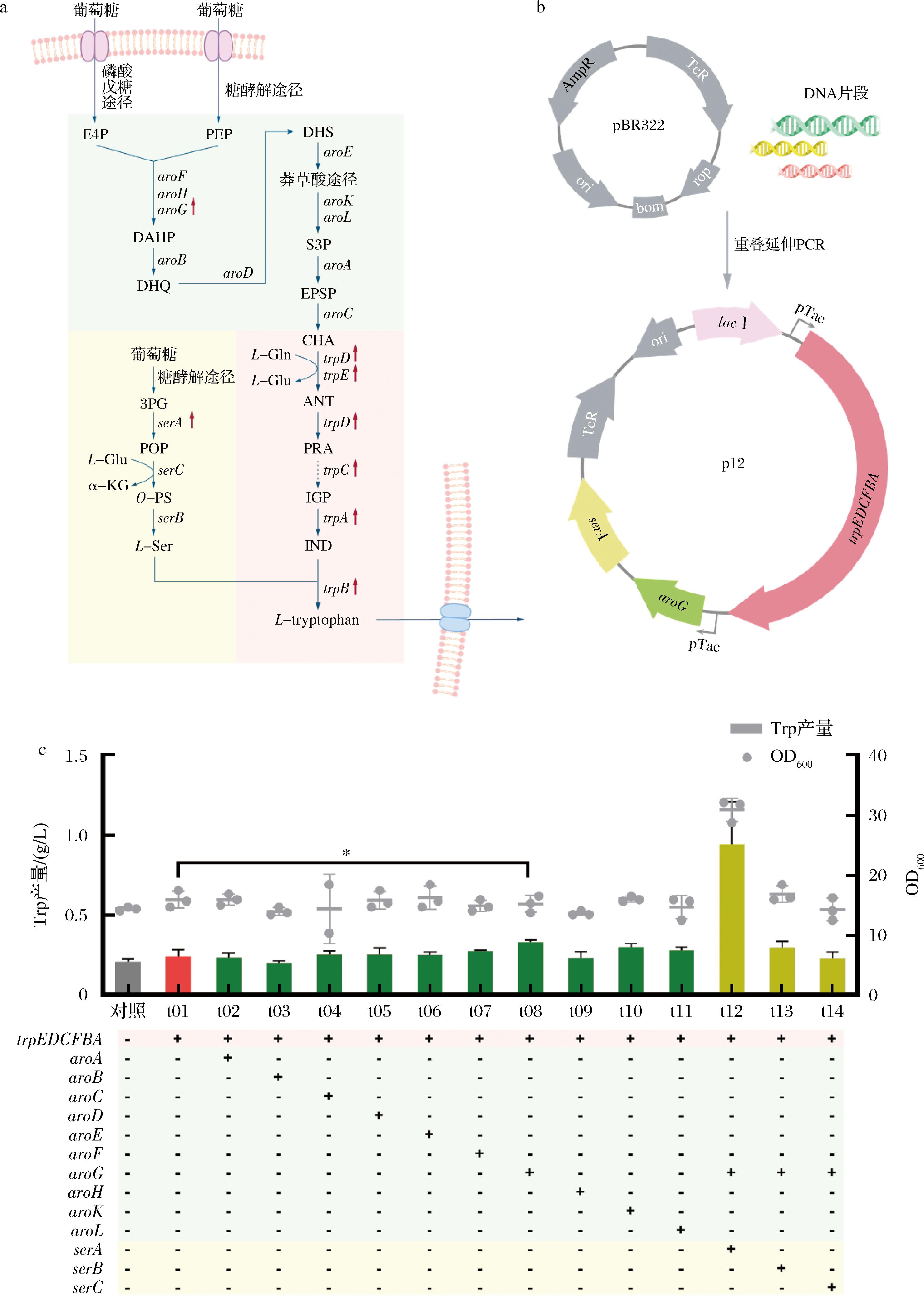
a-大肠杆菌内Trp合成代谢途径;b-质粒p01~p14的构建流程,图中以最终用于底盘菌株的质粒p12为例;c-分步过表达Trp合成相关基因对Trp产量的影响
图2 用于微生物群落上游模块的大肠杆菌底盘菌株的构建
Fig.2 Construction of the E.coli chassis strain for the first module in the microbial consortium
注:图2-a中缩略词释义如下:E4P:D-erythrose-4-phosphate, D-赤藓糖-4-磷酸;PEP:phosphoenolpyruvate, 磷酸烯醇式丙酮酸;DAHP:3-deoxy-D-arabino-heptulosonate-7-phosphate, 3-脱氧-D-阿拉伯庚酮糖酸-7-磷酸;DHQ:3-dehydroquinate, 3-脱氢奎尼酸;DHS:3-dehydroshikimate, 3-脱氢莽草酸;shikimate:莽草酸;S3P:shikimate-3-phosphate, 莽草酸-3-磷酸;EPSP:5-enolpyruvol-shikimate-3-phosphate, 5-烯醇丙酮酸莽草酸-3-磷酸;CHA:chorismate, 分支酸;ANT:anthranilate, 邻氨基苯甲酸;PRA:N-(5-phosphoribosyl)-anthranilate, N-(5-磷酸核糖)-邻氨基苯甲酸;IGP:(1S,2R)-1-C-(indol-3-yl)glycerol 3-phophate, (1S,2R)-1-C-(吲哚-3-基)甘油-3-磷酸;IND:indole, 吲哚;3PG:3-phospho-D-glycerate, 3-磷酸-D-甘油酸;POP:3-phosphooxypyruvate, 3-磷酸氧丙酮酸;O-PS:O-phosphol-L-serine, O-磷酸-L-丝氨酸;L-Ser:L-serine, L-丝氨酸;*表示P<0.05;**表示P< 0.01;***表示P<0.001(下同)。
1.3.2 摇瓶发酵
使用250 mL摇瓶,装液量50 mL,相似的表达发酵体系的格式在下文中简化为“50/250 mL摇瓶”。
1.3.2.1 大肠杆菌单独培养
挑取平板上生长良好的单菌落于2 mL LB培养基,10 mL摇菌管37 ℃、220 r/min过夜培养;种子液以2%体积分数接种于LB培养基,并添加四环素(50 μg/mL),37 ℃培养2 h;加入诱导剂IPTG(1 mmol/L),降低温度至30 ℃开始发酵,发酵周期72 h。
1.3.2.2 酿酒酵母单独培养
挑取平板上生长良好的单菌落于5 mL YTD培养基,50 mL离心管30 ℃ 220 r/min过夜培养;种子液以2%体积分数接种于YTD培养基,30 ℃发酵72 h。
1.3.2.3 大肠杆菌与酿酒酵母共培养
种子液的培养方式与单培养时相同,大肠杆菌与酿酒酵母种子液以1∶1体积比、2%接种量接种于YTNa培养基,37 ℃培养2 h;加入诱导剂IPTG,降低温度至30 ℃开始发酵,发酵周期72 h。
1.3.3 发酵罐发酵
一级种子液:分别挑取大肠杆菌、酿酒酵母的单菌落于LB、YTD(5/50 mL离心管),最适温度过夜培养。
二级种子液:将大肠杆菌、酿酒酵母的一级种子液分别以1%、5%接种于发酵培养基YTNa扩大培养,按照接种比例与接种量确定合适的培养体系,最适温度过夜培养,用于发酵罐接种。本实验最终以285/1 000 mL摇瓶、36/250 mL摇瓶培养二级种子液。
发酵罐参数与控制:5 L发酵罐补料分批发酵,装液量2.5 L。控制pH值为7.0(30%氨水与1 mmol/L磷酸),空气通量为1 vvm,溶氧量为30%,转速为300~800 r/min。接种后以37 ℃培养,待OD600增长到20左右,降低温度至30 ℃,添加IPTG诱导,发酵72 h。当溶氧量>50%,以12.5 g/(L·h)流速流加葡萄糖。
1.3.4 代谢产物的定量检测
高效液相色谱-紫外检测器定量分析发酵液中的IET与Trp含量,液相色谱柱:Shim-pack GIST C18柱(5 μm,150 mm×4.6 mm)。
发酵液前处理:发酵液高速离心,取上清液与无水乙醇以等体积比充分混匀,13 500 r/min离心5 min,取上清液进样检测。
HPLC分析方法—同时检测IET与Trp:水相A为含1%(体积分数)乙腈的20 mmol/L KH2PO4,有机相B为乙腈。总流速1 mL/min,检测双波长为276、215 nm,柱温箱30 ℃。流动相B在0~6 min从0%线性增加到10%,6~25 min线性增加到60%,25~26 min降低到0%,26~32 min维持在0%。Trp出峰时间为10.5 min,IET出峰时间为19.4 min。
HPLC分析方法—仅检测Trp:水相C为0.1%(体积分数)甲酸,有机相D为甲醇。总流速0.8 mL/min,检测波长270 nm,柱温箱40 ℃。流动相D在0~15 min从20%线性增加到60%,15~16 min线性下降到20%,16~24 min维持在20%。Trp出峰时间为5.8 min。
2 结果与分析
2.1 上游模块-大肠杆菌底盘菌株t12的构建与表征
大肠杆菌内Trp合成代谢途径如图2-a所示,将其分为3个模块:1)从E4P与PEP缩合DAHP,DAHP进入CHA途径生成分支酸。这个模块是Trp合成的前驱反应,其中DAHP的缩合是Trp合成的关键,CHA是芳香族氨基酸(色氨酸、酪氨酸、苯丙氨酸)合成代谢途径的第1个分支点。2)CHA在trpE、trpD、trpC、trpB、trpA编码的一系列酶催化下合成Trp。trpEDCBA为大肠杆菌基因组内的一个基因簇,其表达受到Trp浓度的反馈抑制调控。3)丝氨酸的合成代谢。丝氨酸作为Trp合成的最后一步反应的底物,与吲哚结合后合成Trp。
如图2-c所示,在BL21中分步过表达3个代谢模块的基因,模块(1)和(2)中基因的过表达对Trp产量影响很小,除了菌株t08的Trp终产量达0.33 g/L,比出发菌株增加了37.5%,其余菌株与出发菌株t01的Trp产量(0.24 g/L)均没有显著差异。而模块(3)中serA基因的过表达显著提升了Trp产量,菌株t12的Trp产量达到0.94 g/L,比过表达serA之前增加了1.85倍,说明模块(3)提供的丝氨酸是Trp合成的关键影响因素,CHEN等[20]的研究也得出了相同的结论。最终联合过表达trpEDCBA、aroG与serA的菌株t12Trp产量达到出发菌株的457%,因此选择该大肠杆菌t12作为上游模块底盘菌株。
在发酵过程中还发现四环素的不同盐型对大肠杆菌的生长和生产有一定影响,如图3所示,使用盐酸四环素时,大肠杆菌底盘菌株t12的目标产物Trp浓度更高,是使用普通四环素时的1.59倍,且菌株的生长也并未受到显著的抑制,因此后续实验均使用盐酸盐四环素。需要指出的是,本实验的发酵条件与文中其余不同,体系为24孔板,装液量2 mL,发酵时间缩短至48 h,因此Trp产量和OD均有所下降。
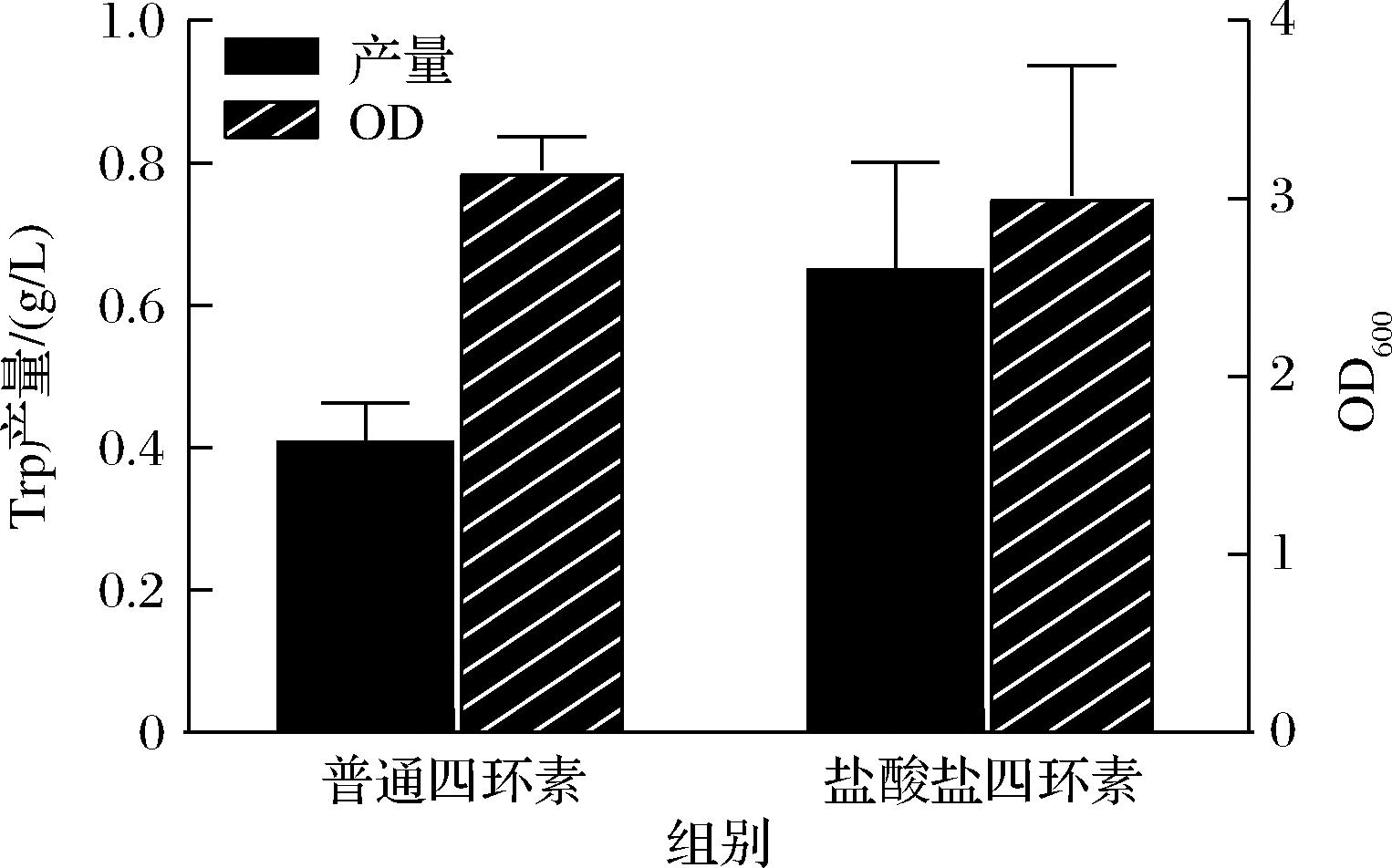
图3 不同盐型四环素对大肠杆菌t12生长和生产的影响
Fig.3 Influence of different salt forms of tetracycline on the growth and production of E.coli strain t12
将t12在摇瓶中发酵,如图4所示,发酵72 h后Trp产量可达到0.91 g/L。而野生型菌株BL21几乎没有合成Trp的能力,其Trp终产量低于培养基中原有的Trp,这说明发酵过程中BL21消耗的Trp量远多于合成的量,同时也表明了经代谢通路强化的重组菌株t12具备作为共培养群落上游模块的能力,能够为下游模块提供多余的底物Trp。
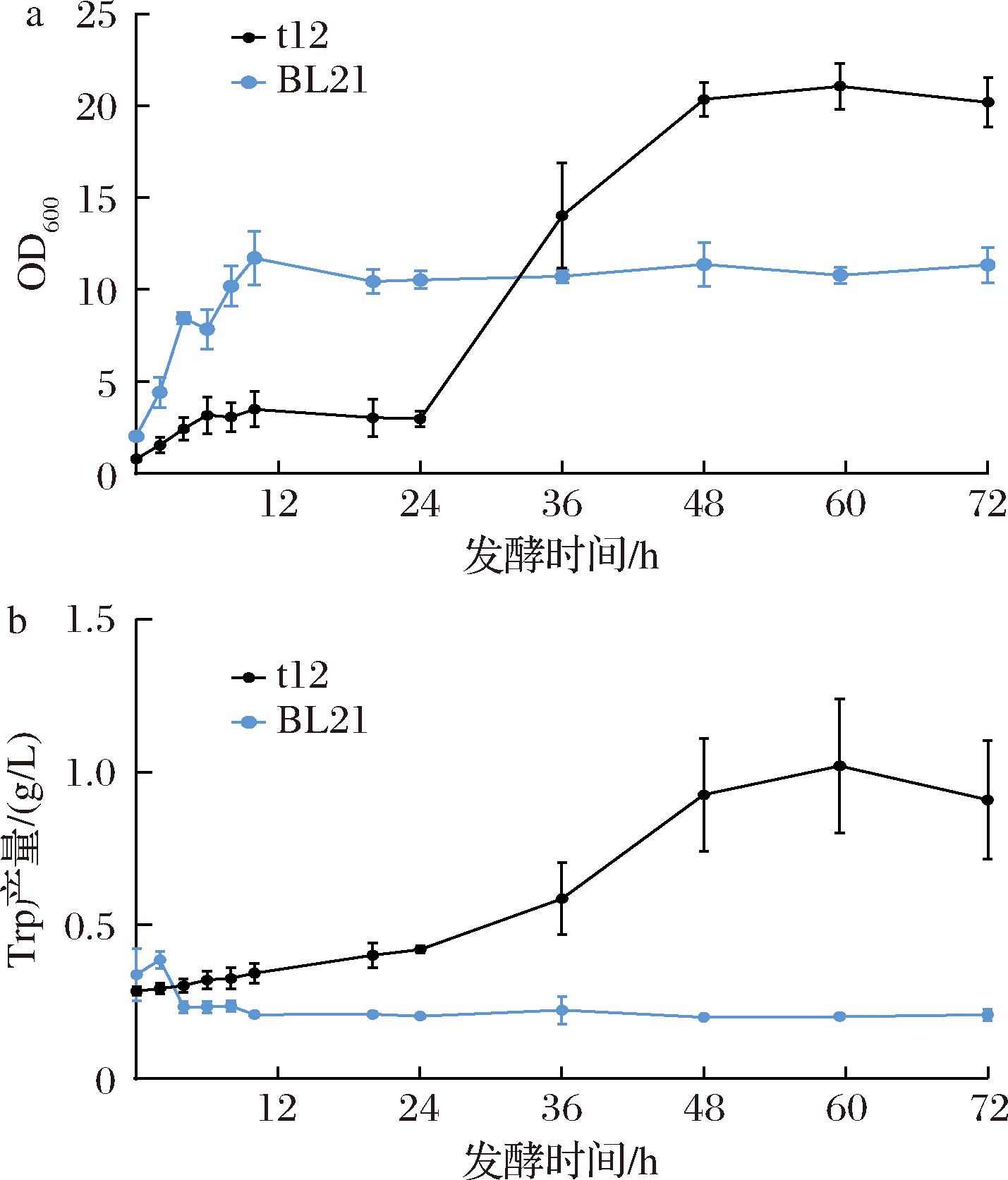
a-大肠杆菌发酵72 h的生长曲线;b-大肠杆菌发酵72 h的Trp含量变化
图4 上游模块大肠杆菌底盘菌株的表征
Fig.4 Characterization of the E.coli chassis strain in the first module
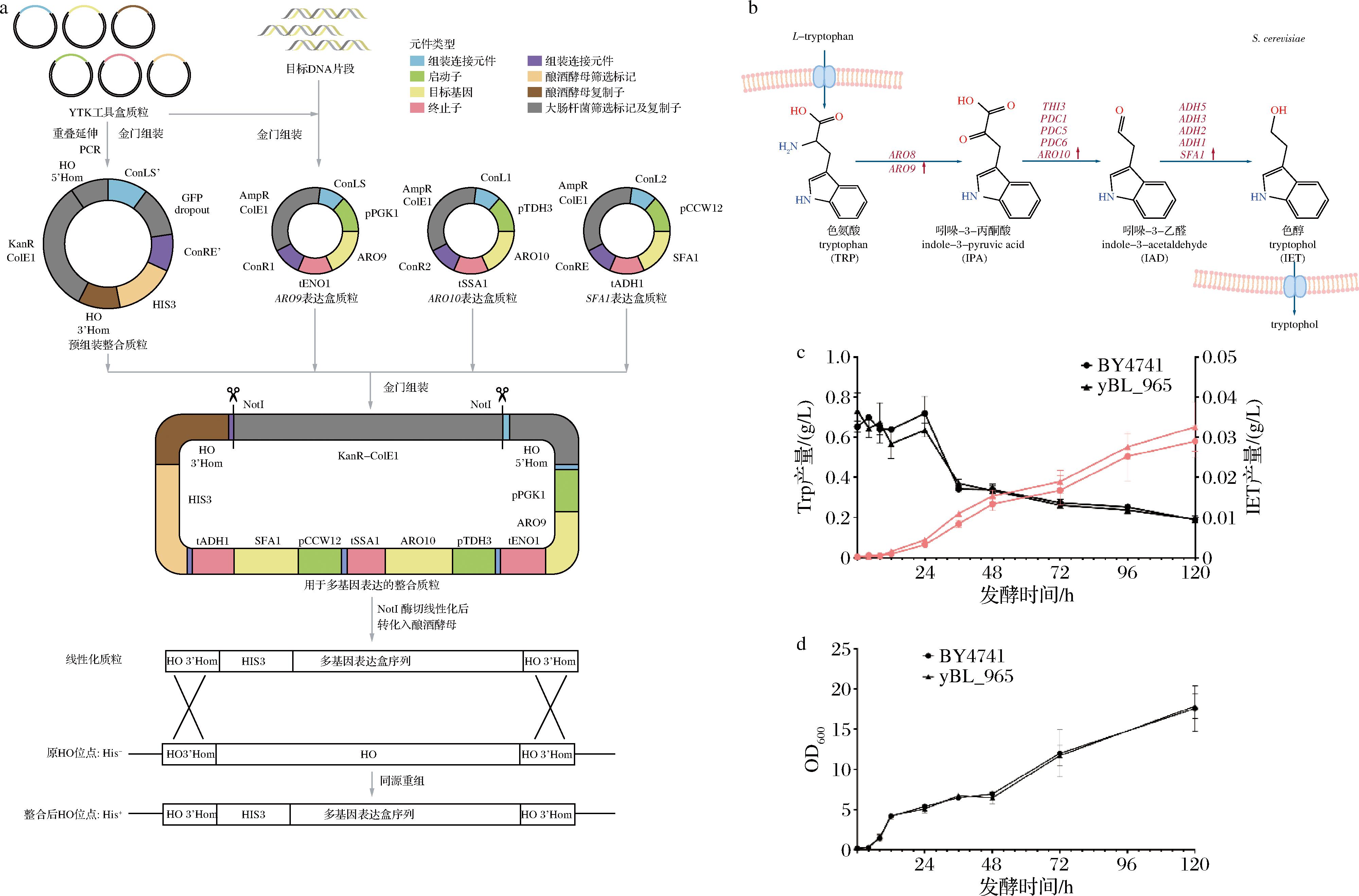
a-质粒p965的构建流程;b-酿酒酵母通过Ehrlich途径将Trp转化为IET;c,d-下游模块酿酒酵母底盘菌株的代谢表征
图5 用于微生物群落下游模块的酿酒酵母底盘菌株的构建
Fig.5 Construction of the S.cerevisiae chassis strain for the second module in the microbial consortium
2.2 下游模块-酿酒酵母底盘菌株yBL_965的构建与表征
在本团队前期的研究中[21],通过对野生型酿酒酵母BY4741内艾利希途径的逐步过表达进行系统优化,发现于Trp转化为IET的生物过程中(图5-b),ARO9、ARO10和SFA1的联合过表达是最优的基因组合。因此构建质粒内同时包含这3个基因,均以组成型强启动子表达,最终表达盒基因型为pPGK1-ARO9-tENO1-pTDH3-ARO10-tSSA1-pCCW12-SFA1-tADH1-HIS3,组氨酸为酵母的营养缺陷筛选标记。将整个表达盒整合到BY4741的同一个位点HO上(菌株构建流程如图5-a所示),得到菌株yBL_965,作为下游模块的底盘菌株。
在摇瓶中对该酵母菌株yBL_965进行发酵过程表征,在培养基内额外添加5 mmol/L Trp单菌发酵,结果如图5-c、图5-d所示,yBL_965的最终IET产量为0.03 g/L,比出发菌株提高了约12%,而生长情况和出发菌株几乎一致,可作为IET合成群落的下游模块出发菌株。
2.3 大肠杆菌与酿酒酵母共培养
为验证构建的群落的可行性,即考察中间代谢物Trp是否能由上游模块合成,并被下游模块吸收转化为IET,在此将设计构建的IET合成群落(t12+yBL_965)与不同Trp/IET合成能力的大肠杆菌/酿酒酵母组成的共培养体系进行对比,其中酵母菌株BY4741+ΔARO8+ΔARO9利用CRISPR-Cas9技术敲除了Trp向IET转化的第一步反应关键酶,无法合成IET。
不同共培养体系发酵的结果如图6-a所示,揭示了上游模块与下游模块的代谢强度共同决定了群落的整体IET生产能力。上下游模块强度均为最强的工程群落(t12+yBL_965)表现出最高的IET产量,达0.095 g/L。相比之下,(t12+BY4741)因其下游模块强度较低,IET产量受限,仅为0.057 g/L。而上游模块代谢强度过低的(BL21+yBL_965)则因为Trp产量不足限制了IET的进一步合成,其产量仅为0.039 g/L。与之相比,当t12作为上游底盘菌株时,其合成的更多Trp被yBL_965转化为IET,同时回答了中间代谢物Trp的流通问题,证明了本研究构建的工程群落内代谢链畅通,上游模块合成的Trp能渗透至下游模块并被进一步转化为IET,最终能将碳源直接转化为IET。
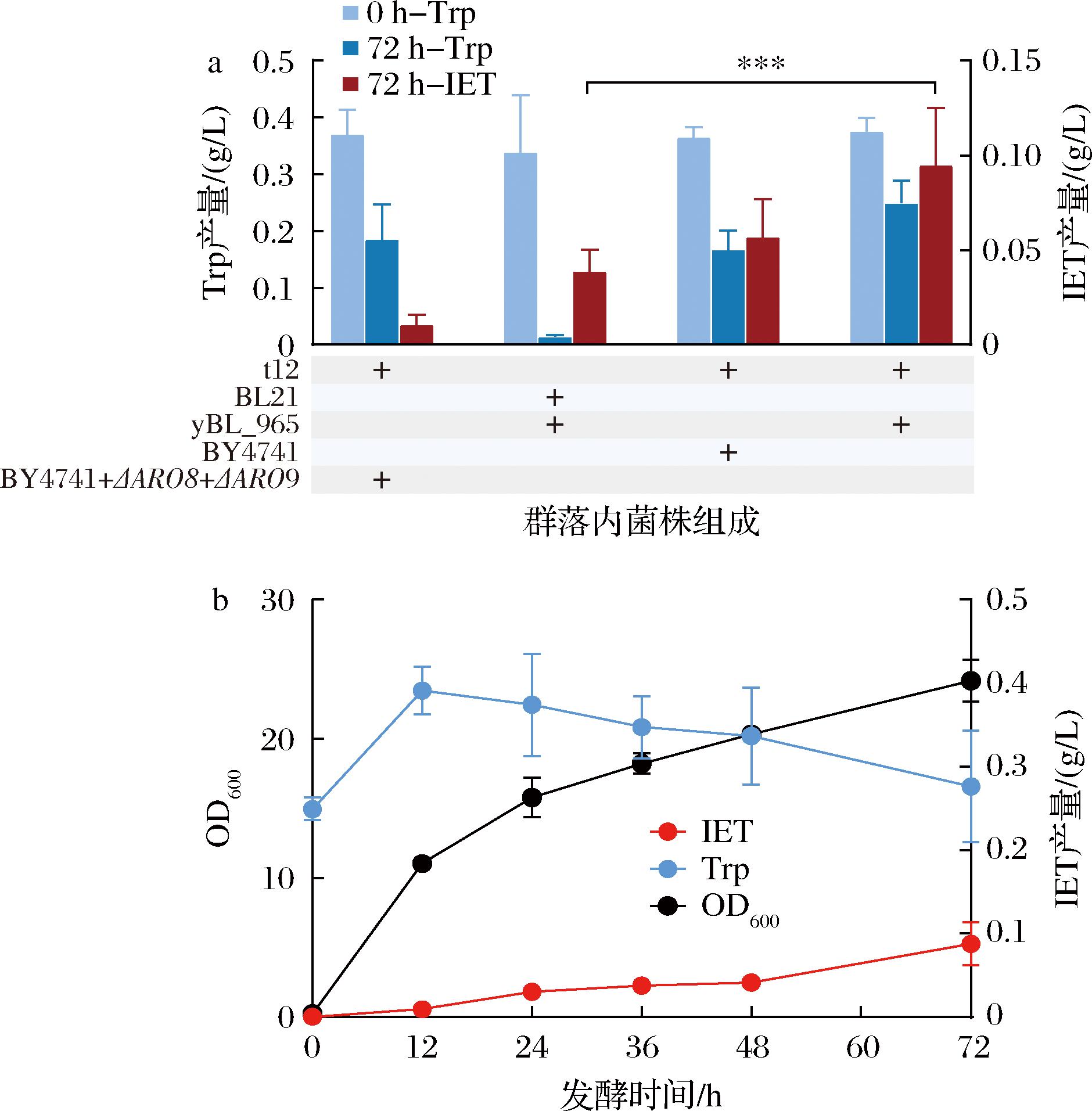
a-共培养群落的代谢可行性验证;b-共培养群落(t12+yBL_965)的生长与产量曲线
图6 共培养群落的可行性验证与表征
Fig.6 Feasibility validation and characterization of the engineered microbial consortium
于摇瓶内进行发酵过程表征,结果如图6-b,该群落在发酵72 h后IET产量可达0.087 g/L,为yBL_965在添加充足底物单独培养时的2倍以上。
2.3.1 合成群落的发酵条件优化
为测试由上述2株底盘菌株组成的共培养群落的最大IET生产能力,在培养基内额外添加0~10 mmol/L不同浓度的Trp后进行共培养。结果如图7-a所示,当添加1 mmol/L Trp时,群落的IET产量显著增加,提高了约60%,说明群落的上游模块有进一步增强的空间。因此推测改变群落发酵时的初始接种比例,当上游模块的菌体数量增加时,上游代谢强度可得到增强,从而增加上游产物Trp的合成量,进而提升IET产量。
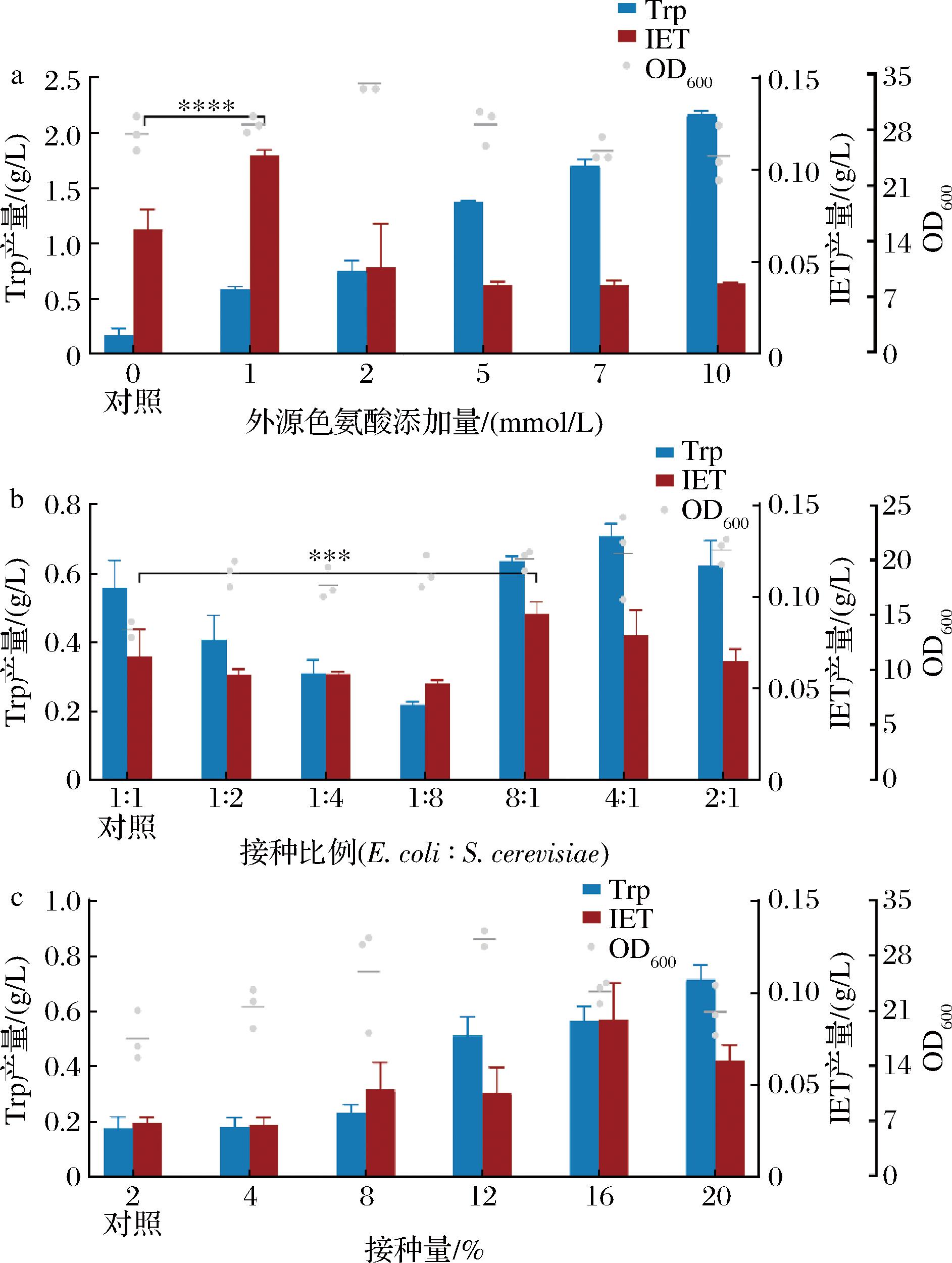
a-添加底物Trp验证群落的最大IET生产能力;b-初始接种比例对群落IET产量的影响;c-接种量对群落IET产量的影响
图7 共培养群落的发酵条件优化
Fig.7 Investigating the impact of fermentation conditions on IET production
注:****表示P<0.000 1。
固定总接种量为2%,将大肠杆菌与酿酒酵母以不同比例接种入发酵培养基,如图7-b所示,大肠杆菌比例的提高确实能够增强上游模块的代谢强度并提高群落的IET产量,其中以大肠杆菌、酿酒酵母8∶1体积比接种时IET产量最高,提高了约34%。
随后固定8∶1的初始接种比例,改变菌体的总接种量,如图7-c所示,发现接种量的提高也能够提高群落的IET生产能力,当接种量16%时,最终IET产量提升至原来的2.9倍。更高的接种量反而使IET的产量降低,这是由于积累的Trp抑制了酵母的生长,而酵母的体积较大且在发酵后期生长占优,因此贡献大部分OD值,酵母的生长受抑制会引起明显的OD600减少。高浓度Trp引起的抑制酵母生长在图7-a中也可观察到。
尽管不同批次的实验之间IET产量并不稳定,但该群落的IET产量始终无法通过优化群落内的菌体数量和比例达到显著性提升。且在这3次实验中均发现过量的Trp在培养基中积累,无法转化为IET,因此怀疑目前下游模块存在代谢瓶颈。
2.3.2 外源添加艾利希途径的反应底物及辅因子
下游模块的详细代谢途径如图8-a所示,艾利希途径的三步反应中都需要其他底物或辅因子参与酶催化反应,其中α-酮戊二酸、3-(4-联苯基)-2-氧代丙酸作为氨基受体协助第一步转氨反应,硫胺素是第二步脱羧反应中脱羧酶的辅酶,NADH作为电子供体,为第三步脱氢反应提供还原力,将吲哚-3-乙醛还原为IET。
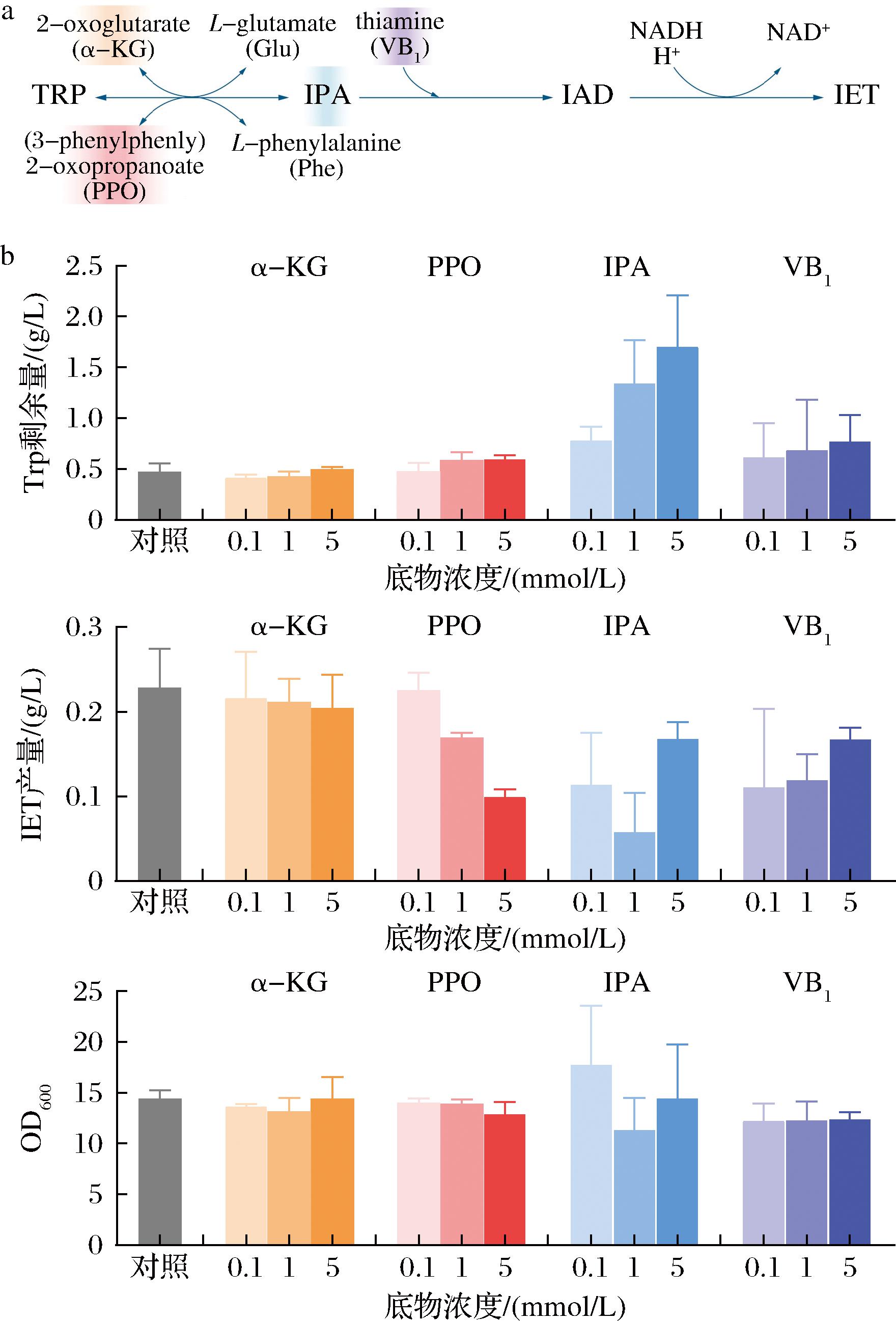
a-艾利希途径中的辅因子代谢(颜色标注的物质在实验中进行了添加);b-4种辅因子和中间代谢物的添加对yBL_965单菌发酵的影响
图8 艾利希途径的底物及辅因子对群落产量的影响
Fig.8 Impact of Ehrlich pathway substrates and cofactors on the IET production of the microbial consortium
注:α-KG,α-酮戊二酸;PPO,3-(4-联苯基)-2-氧代丙酸;IPA,吲哚-3-丙酮酸;VB1,硫胺素;NADH,烟酰胺腺嘌呤二核苷酸-还原态;IAD,吲哚-3-乙醛。
在培养基中分别添加这4种底物或辅因子进行共培养:α-酮戊二酸、3-(4-联苯基)-2-氧代丙酸、吲哚-3-丙酮酸(indole-3-pyruvic acid, IPA)、硫胺素,探究是否因为其中几种物质的缺乏导致下游生产强度太弱。其中吲哚-3-乙醛因为标准品价格昂贵且理化性质不稳定,NADH不能被跨膜吸收,在此不做验证。结果如图8-b所示,以上4种底物及辅因子的添加并未对群落的IET产量产生正向的影响,除了α-酮戊二酸,其他物质的添加均抑制了IET的合成;吲哚-3-丙酮酸的过量添加甚至导致底物Trp增加,推测这是由于第一步可逆的转氨反应中,逆向反应速率大于正向反应速率导致。由此可以判断,目前群落的下游模块代谢瓶颈并不是由于途径中的这些辅因子和中间代谢物缺乏引起的。
2.3.3 共培养5 L补料分批发酵
将共培养群落(t12+yBL_965)以上述所得最佳发酵条件(接种比例8∶1,接种量16%)进行5 L体系放大发酵,结果如图9所示,最终本实验构建的合成群落以葡萄糖为碳源时,可合成约0.23 g/L IET,比摇瓶体系增加了2倍以上,比酵母yBL_965在添加底物Trp单独发酵时提高了7倍以上。
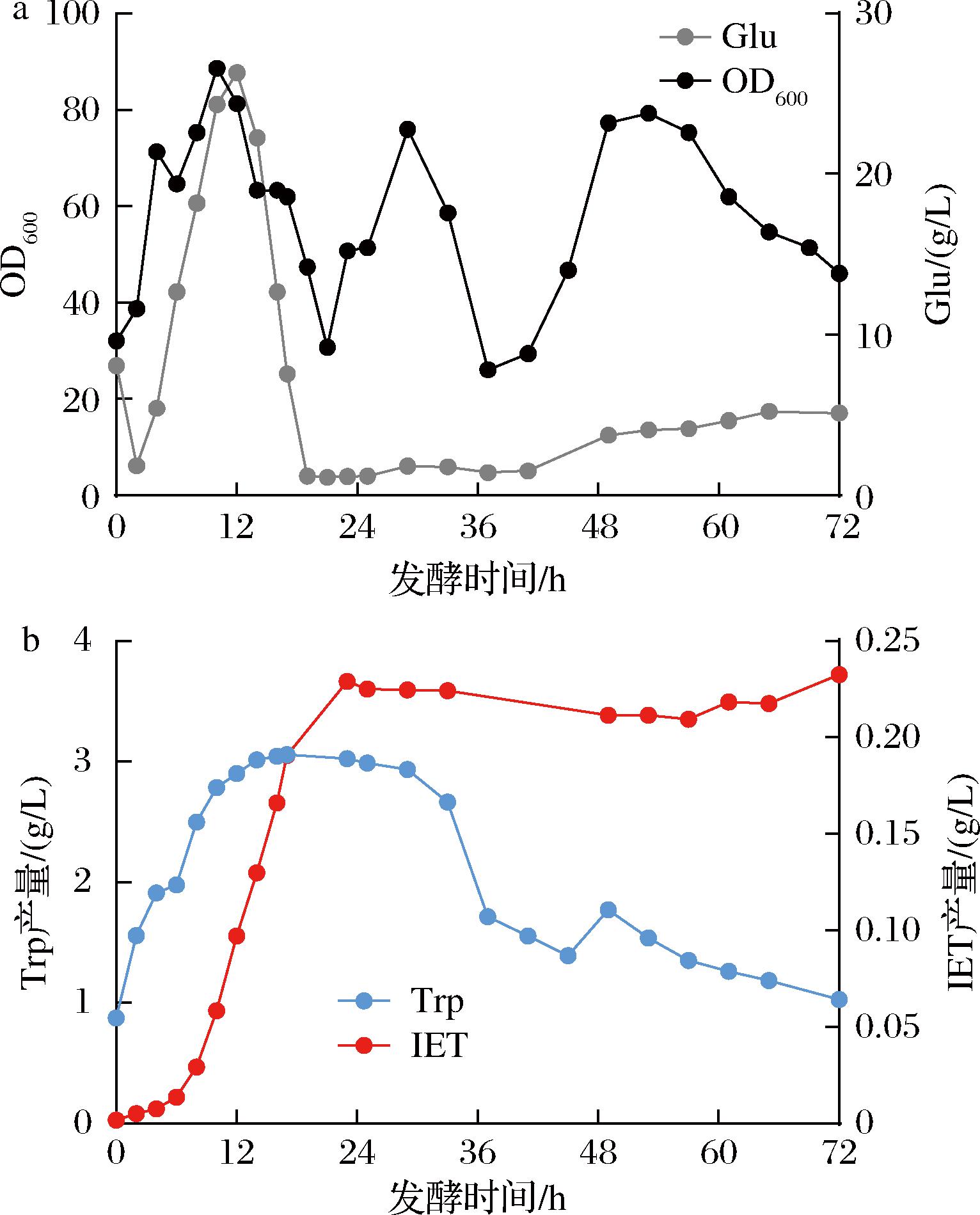
a-生长曲线与葡萄糖浓度变化;b-Trp及IET含量变化
图9 共培养群落的补料分批发酵
Fig.9 5-L fed-batch fermentation of the engineered microbial consortium
值得注意的是,本合成群落在放大的发酵罐体系中并不稳定,整体的生长呈现剧烈波动。推测为以下2个方面原因:1)当前补糖策略与溶氧水平直接关联,可能导致短时间补充高浓度葡萄糖进入发酵体系,如开始发酵的2~12 h,而这很有可能引起酵母的Crabtree效应,进而产生大量乙醇,抑制甚至毒害菌体生长;2)目前发酵罐的控制参数并不适配混合体系的培养,需要进一步探索出基于两菌生长特性的最适控制方法,如分阶段控温、控糖等;3)混菌培养较单菌培养较低的稳定性随培养环境的复杂度提升而暴露出来,需要优化种间关系使群落内部达到相互依赖或相互促进的关系。推测目前群落内由于碳源单一而存在竞争关系,导致大肠杆菌或酿酒酵母均无法在最优条件下生长代谢,后续可以通过改变碳源种类、构建种间的营养缺陷互补配对等方法尝试改善,提升群落的稳定性。
3 结论与讨论
鉴于IET较为复杂的合成代谢途径,即使对于内源存在艾利希途径的酵母来说,在单菌株内高效合成IET仍存在较大挑战。采用共培养策略,本研究将长步的IET合成途径模块化,分配给大肠杆菌与酿酒酵母。在野生型BL21中转入trpEDCBA,aroG与serA联合过表达的质粒,大肠杆菌菌株t12的Trp产量达到0.91 g/L;在野生型BY4741中同时整合ARO9、ARO10、SFA1的表达盒,酿酒酵母菌株yBL_965的IET产量达到0.03 g/L;2株底盘菌株构成的微生物群落以8∶1初始接种比例、16%接种量在5 L发酵罐内可生产IET 0.23 g/L,比yBL_965外源添加底物Trp单独发酵时提高了7倍以上。为生物法从头合成IET以及其他芳香族氨基酸衍生物提供了有效的参考方向。
然而目前该群落中仍然存在较多问题:1)目前的群落IET产量还未能达到同时调控Trp与IET合成途径的酿酒酵母单菌发酵产量[1],是因为下游模块的代谢强度较弱,底物Trp积累无法被高效转化,虽然已经排除了下游反应辅因子或底物缺乏的问题,但具体的原因尚未研究清楚。推测有可能是下游模块中Trp跨膜向酵母胞内运输的效率太低,导致底物在胞外积累无法被有效吸收利用。2)在5 L发酵罐体系内的IET产量相对250 mL摇瓶的产量提升幅度较小,且OD600波动较大可能是由于发酵控制参数不合适,或者是群落的稳定性和鲁棒性较差,有待进一步优化发酵过程的控制参数及发酵条件,比如更改补糖策略、更换碳源,或者调控2个模块的生长和生产发酵的顺序与阶段;对于群落稳定性,还需要观测发酵过程中的种群比例变化及生长抑制物的产生,从而判断群落内的种群关系,进而进行针对性的代谢调控和发酵条件改变。
[1] LI Y, SUN J Z, FU Z H, et al.Engineering the L-tryptophan metabolism for efficient de novo biosynthesis of tryptophol in Saccharomyces cerevisiae[J].Biotechnology for Biofuels and Bioproducts, 2024, 17(1):130.
[2] PALMIERI A, PETRINI M.Tryptophol and derivatives:Natural occurrence and applications to the synthesis of bioactive compounds[J].Natural Product Reports, 2019, 36(3):490-530.
[3] LV Y W, YU Z Q, SU W K.A continuous kilogram-scale process for the manufacture of 7-ethyltryptophol[J].Organic Process Research &Development, 2011, 15(2):471-475.
[4] DUBHASHE Y R, SAWANT V M, GAIKAR V G.Process intensification of continuous flow synthesis of tryptophol[J].Industrial &Engineering Chemistry Research, 2018, 57(8):2787-2796.
[5] HAZELWOOD L A, DARAN J M, VAN MARIS A J A, et al.The Ehrlich pathway for fusel alcohol production:A century of research on Saccharomyces cerevisiae metabolism[J].Applied and Environmental Microbiology, 2008, 74(8):2259-2266.
[6] MAGASANIK B, KAISER C A.Nitrogen regulation in Saccharomyces cerevisiae[J].Gene, 2002, 290(1-2):1-18.
[7] ROSAZZA J P, JUHL R, DAVIS P.Tryptophol formation by Zygosaccharomyces priorianus[J].Applied Microbiology, 1973, 26(1):98-105.
[8] GORI K, KNUDSEN P B, NIELSEN K F, et al.Alcohol-based quorum sensing plays a role in adhesion and sliding motility of the yeast Debaryomyces hansenii[J].FEMS Yeast Research, 2011, 11(8):643-652.
[9] KONG S J, ZHANG J B, LI X, et al.De novo biosynthesis of indole-3-ethanol and indole-3-ethanol acetate in engineered Escherichia coli[J].Biochemical Engineering Journal, 2020, 154:107432.
[10] REN X R, WEI Y, ZHAO H L, et al.A comprehensive review and comparison of L-tryptophan biosynthesis in Saccharomyces cerevisiae and Escherichia coli[J].Frontiers in Bioengineering and Biotechnology, 2023, 11:1261832.
[11] ROELL G W, ZHA J, CARR R R, et al.Engineering microbial consortia by division of labor[J].Microbial Cell Factories, 2019, 18(1):35.
[12] DUNCKER K E, HOLMES Z A, YOU L C.Engineered microbial consortia:Strategies and applications[J].Microbial Cell Factories, 2021, 20(1):211.
[13] YUAN S F, YI X N, JOHNSTON T G, et al.De novo resveratrol production through modular engineering of an Escherichia coli-Saccharomyces cerevisiae co-culture[J].Microbial Cell Factories, 2020, 19(1):143.
[14] LIU Y Y, QIN R L, JIA X Q.Design and construction of an artificial labor-division consortium for phenanthrene degradation with three-functional modules[J].Chemosphere, 2024, 366:143439.
[15] XIONG B, ZHU Y D, TIAN D G, et al.Flux redistribution of central carbon metabolism for efficient production of L-tryptophan in Escherichia coli[J].Biotechnology and Bioengineering, 2021, 118(3):1393-1404.
[16] DING S, CHEN X L, GAO C, et al.Modular engineering of Escherichia coli for high-level production of L-tryptophan[J].Chinese Journal of Biotechnology, 2023, 39(6):2359-2374.
[17] PARAPOULI M, VASILEIADIS A, AFENDRA A S, et al.Saccharomyces cerevisiae and its industrial applications[J].AIMS Microbiology, 2020, 6(1):1-31.
[18] LEE M E, DELOACHE W C, CERVANTES B, et al.A highly characterized yeast toolkit for modular, multipart assembly[J].ACS Synthetic Biology, 2015, 4(9):975-986.
[19] LIU Y J, SONG D, HU H T, et al.De novo production of hydroxytyrosol by Saccharomyces cerevisiae-Escherichia coli coculture engineering[J].ACS Synthetic Biology, 2022, 11(9):3067-3077.
[20] CHEN L, ZENG A P.Rational design and metabolic analysis of Escherichia coli for effective production of L-tryptophan at high concentration[J].Applied Microbiology and Biotechnology, 2017, 101(2):559-568.
[21] 孙井震, 何玙冰, 杨卫华, 等.酿酒酵母过表达Ehrlich途径基因高效合成色醇[J].食品与发酵工业, 2022, 48(24):16-23.
SUN J Z, HE Y B, YANG W H, et al.Efficient synthesis of indole-3-ethanol in Saccharomyces cerevisiae by overexpression of Ehrlich pathway genes[J].Food and Fermentation Industries, 2022, 48(24):16-23.