γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种非蛋白氨基酸,又称4-氨基丁酸。它广泛存在于植物、动物和微生物中。GABA具有抑制神经兴奋、抗焦虑和抑郁、改善睡眠质量、降血压等多种功能[1-2],因此GABA被广泛应用于医药、食品等领域。目前用于合成GABA的方法主要有化学合成法和微生物合成法。化学合成法具有反应条件严格、产生有毒的副产物等缺陷,微生物合成法与化学合成法相比,具有环境友好、操作安全的优势。
谷氨酸棒杆菌(Corynebacterium glutamicum)是一种革兰氏阳性菌,其产物通常被认为是安全的。相比于其他的GABA合成菌株乳酸菌(Lactobacillus)、大肠杆菌(Escherichia coli)等,谷氨酸棒杆菌能够自身合成并提供GABA合成所需的前体物质L-谷氨酸。通过在谷氨酸棒杆菌中引入异源的由gad基因编码的谷氨酸脱羧酶(glutamate decarboxylase,GAD),L-谷氨酸会在该酶的催化下发生脱羧反应生成GABA。通常GAD的最适pH值为4.0~5.0,而谷氨酸棒杆菌生长和生产L-谷氨酸的最适pH值为7.0~7.5。来源于泡菜乳杆菌(Lactobacillus senmaizukei)的GAD(LsGAD)是在偏中性pH条件下具有较好活性的GAD,最适pH值为5.5,在谷氨酸棒杆菌KCTC1852中LsGAD催化L-谷氨酸最终获得42.5 g/L GABA[3]。利用在偏中性条件下具有活性的GAD很好地缓解了谷氨酸棒杆菌生长和GABA生产所需pH之间的矛盾。但是在谷氨酸棒杆菌中,胞内和胞外的pH值存在差异性,在胞外pH变化为酸性条件时,胞内会启动一系列反应来维持pH的稳定,以使细胞能够继续生存[4]。因此,胞内的pH变化可能不适合GAD活性的发挥。并且,前体L-谷氨酸对其自身合成过程存在反馈抑制作用,因此L-谷氨酸的高产依赖于其向细胞外的有效快速分泌,而分泌后又导致细胞内表达的GAD合成GABA时所需底物L-谷氨酸不足。此外,谷氨酸棒杆菌中还存在以GabP为主的GABA摄取系统和以α-酮戊二酸脱氢酶复合物(α-ketoglutarate dehydrogenase complex,ODHC)为主的前体L-谷氨酸合成的竞争途径,这些途径的存在减少了前体L-谷氨酸和GABA的积累[5-7]。这些问题都限制了谷氨酸棒杆菌GABA的高效合成。
微生物表面展示技术是一种通过将靶蛋白融合到细胞表面锚定基序的N-或C-末端上从而将靶蛋白展示在细胞表面上的技术,具有提高酶稳定性和胞外底物接触效率的优势。锚定基序的选择对于表面展示有效性非常重要。用于谷氨酸棒杆菌表面展示的锚定基序主要分为外源蛋白、分枝菌酸层蛋白和膜蛋白以及这些蛋白中的一段特定基序。目前有研究利用膜蛋白NCgl2775[8]和C端截短型的NCgl1221[9]将α-淀粉酶展示在谷氨酸棒杆菌细胞表面上,也有研究利用分枝菌酸层蛋白PorH、PorB、PorC[10]、NCgl1307[8]、NCgl1337S[11]等将α-淀粉酶、木聚糖酶等展示在细胞表面上,以将细胞无法摄取利用的淀粉、木聚糖等生物大分子在细胞外进行酶解,产生细胞可吸收利用的葡萄糖、木糖等生物小分子,从而解决这些物质吸收受限的问题。
本研究以LsGAD为靶蛋白,利用不同的锚定基序将LsGAD展示在谷氨酸棒杆菌的细胞表面上,从而使LsGAD在更适宜的胞外偏酸性环境中发挥催化作用,并将不断分泌到胞外的前体L-谷氨酸直接转化成胞外的GABA。然后优化表面展示策略,以提高表面展示效率,最后阻断谷氨酸棒杆菌中的GABA摄取途径,从而改善GABA在胞外的积累。这些研究为在谷氨酸棒杆菌中生产GABA提供了新的策略和思路。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
本研究所用菌株和质粒分别见表1和表2。大肠杆菌JM109为质粒构建的宿主菌。谷氨酸棒杆菌ATCC 13032及其实验室已构建的pknG缺失菌株G0为生产GABA的初始菌株。
表1 本研究中所使用的菌株
Table 1 Bacterial strains used in this study
续表1

名称特性来源G-HLC.glutamicum ATCC 13032 harboring p5-porHL-gad本研究构建G-HHC.glutamicum ATCC 13032 harboring p5-porHHis-gad本研究构建G-HdC.glutamicum ATCC 13032 harboring p5-porH-gad-dKEJ本研究构建G-HgC.glutamicum ATCC 13032 harboring p5-porH-gad-gSL本研究构建G0C.glutamicum ATCC 13032 ΔpknG[7]G1G0 ΔgabP本研究构建G1-HLG1 harboring p5-porHL-gad 本研究构建
表2 本研究中所使用的质粒
Table 2 Plasmids used in this study

名称特性来源pJYW-5Constitutive expression vector of C.glu-tamicum carrying promoter PtacM,Kmr[12]p5-LsgadpJYW-5 carrying Lsgad本研究构建p5-37S-gadpJYW-5 carrying NCgl1337S-displayed Lsgad本研究构建p5-21ΔC-gadpJYW-5 carrying C-terminally truncated NCgl1221-displayed Lsgad本研究构建p5-porH-gadpJYW-5 carrying porH-displayed Lsgad本研究构建p5-porB-gadpJYW-5 carrying porB-displayed Lsgad本研究构建p5-07-gadpJYW-5 carrying NCgl1307-displayed Lsgad本研究构建p5-75-gadpJYW-5 carrying NCgl2775-displayed Lsgad本研究构建pJYW-5-R4a-gadB2-R4a-gadB1mutpJYW-5 carrying gadB2-gadB1mut with the RBS sequence of R4a[13]p5-porH-B2pJYW-5 carrying porH-displayedgadB2本研究构建p5-porH-B1mpJYW-5 carrying porH-displayedgadB1mut本研究构建p5-porHL-gadpJYW-5 carrying porH-displayed Lsgad with longer linker本研究构建p5-porHHis-gadpJYW-5 carrying porH-displayed Lsgad with linker with His·tag本研究构建p5-dKEJpJYW-5 carrying dnaK-grpE-dnaJ本研究构建p5-gSLpJYW-5 carrying groES-groEL本研究构建p5-porH-gad-dKEJpJYW-5 carrying porH-displayed Lsgad and dnaK-grpE-dnaJ本研究构建p5-porH-gad-gSLpJYW-5 carrying porH-displayed Lsgad and groES-groEL本研究构建pSYN2gabP基因敲除用质粒[5]
1.1.1 主要培养基
LB培养基(g/L):NaCl 5、胰蛋白胨5、酵母提取物2.5。
LBB培养基(g/L):胰蛋白胨5、酵母提取物2.5、NaCl 5和脑心浸液18.5。
1.2 仪器与设备
752紫外分光光度计,上海舜宇恒平科学仪器有限公司;SBA-40E生物传感分析仪,山东省科学院生物研究所;DELTA 320型pH计,METTLER TOLEDO科技(中国)有限公司;1200高效液相色谱仪,美国Agilent公司;Hypersil 00S-2 C18分析柱(250 mm×4.6 mm,5 μm),赛默飞世尔科技公司。
1.3 实验方法
1.3.1 质粒和菌株的构建
1.3.1.1 基础型表面展示质粒和菌株的构建
本研究所用引物见表3。将Lsgad进行密码子优化和合成,利用引物Lsgad-L/Lsgad-R扩增Lsgad,并通过一步克隆插入经酶切处理过的pJYW-5载体中,获得质粒p5-Lsgad,将质粒p5-Lsgad转化至谷氨酸棒杆菌ATCC 13032中,获得菌株G-N。以谷氨酸棒杆菌ATCC 13032基因组为模板,分别利用引物对NCgl1337S-F/NCgl1337S-R、NCgl1221(ΔC)-F/NCgl1221(ΔC)-R、PorH-F/PorH-R、PorB-F/PorB-R、NCgl1307-F/NCgl1307-R和NCgl2775-F/NCgl2775-R扩增6种不同的锚定基序NCgl1337S、NCgl1221ΔC、porH、porB、NCgl1307和NCgl2775;以p5-Lsgad为模板,分别利用引物对Lsgad(37H)-F/Lsgad-R、Lsgad(ΔC2775)-F/Lsgad-R、Lsgad(1307)-F/Lsgad-R(BamHⅠ) 和Lsgad(Linker3)-F/Lsgad-R(BamHⅠ)扩增Lsgad,将获得的6种锚定基序利用重叠延伸PCR分别与对应的Lsgad融合,并插入经酶切处理过的pJYW-5载体中,产生6种不同的表面展示质粒p5-37S-gad、p5-21ΔC-gad、p5-porH-gad、p5-porB-gad、p5-07-gad和p5-75-gad。将这6种表面展示质粒分别转化至谷氨酸棒杆菌ATCC 13032中,获得6种表面展示菌株G-37、G-21、G-H、G-B、G-07和G-75。
表3 本研究中所使用的引物
Table 3 Primers used in this study

引物引物序列(3′-5′)Lsgad-LGGGGCCCGTTAACGGATCGAAAGGAGAGGATTGATGTCCAAGAACGACCAGGALsgad-RACTCTAGAGAGCTCGAATTCCTAGCGAACGGTGGTCTTGTNCgl1337S-FGGGCCCGTTAACGGATCGAAAGGAGAGGATTGATGGCTCAGCGAAAACTGGCNCgl1337S-RTCCTGGTCGTTCTTGGACATGCTGCCACCTCCACCGCTACCGCCGCCTCCAGCCACACCACCACTTGAGGLsgad(37H)-FATGTCCAAGAACGACCAGGANCgl1221(ΔC)-FGGGCCCGTTAACGGATCGAAAGGAGAGGATTGATGCGTATTATCAAGCAGCGNCgl1221(ΔC)-RACATGCTGCCACCTCCACCGCTACCGCCGCCTCCCACCGTAGTGGGCACTGTCATPorH-FGGGCCCGTTAACGGATCGAAAGGAGAGGATTGATGGATCTTTCCCTTCTCAAPorH-RTCCTGGTCGTTCTTGGACATGCTGCCACCTCCACCGCTACCGCCGCCTCCGGAAGAGAAGTTATCCAGATPorB-FTTAAGGGGCCCGTTAACGGAAAGGAGAGGATTGATGAAGCTTTCACACCGCATPorB-RCACTGCCTCCGCCACCACTACCGCCGCCTCCGGAAGAGAAGTTGGAGGACANCgl1307-FGCCTTAAGGGGCCCGTTAGAAAGGAGAGGATTGTTGAAGGATTACGCGGTGCANCgl1307-RCCGCCGCCTCCGTTCAGTTCTTCACGGCATTLsgad(1307)-FCTGAACGGAGGCGGCGGTAGCGGTGGAGGTGGCAGCATGTCCAAGAACGACCALsgad-R(BamHⅠ)GAGAGCTCGAATTCGTCGACCTAGCGAACGGTGGTCTTGTNCgl2775-FGCCTTAAGGGGCCCGTTAGAAAGGAGAGGATTGATGAGGAAAACCATCACCGNCgl2775-RTGGACATGCTGCCACCTCCACCGCTACCGCCGCCTCCTCCGTTGTCGATGAGGTTGGLsgad(ΔC2775)-FTGGAGGTGGCAGCATGTCCAAGAACGACCAGGAPorH(B2)-RTCCTGATCGTTTTTATTCATGCTGCCACCTCCACCGCTACCGCCGCCTCCGGAAGAGAAGTTATCCAGATgadB2(PorH)-FGGTGGCAGCATGAATAAAAACGATCAGGgadB2(SalⅠ)-RACTCTAGAGAGCTCGAATTCTTAACTTCGAACGGTGGTCTgadB1mut-FTAGTGGTGGCGGAGGCAGTGGTGGAGGCGGAAGTATGGCTATGTTGTATGGAAgadB1mut(SalⅠ)-RACTCTAGAGAGCTCGAATTCTTAGTGCGTGAACCCGTATTPorH(Linker3)-RCACTGCCTCCGCCACCACTACCGCCGCCTCCGGAAGAGAAGTTATCCAGATTLsgad(Linker3)-FTAGTGGTGGCGGAGGCAGTGGTGGAGGCGGAAGTATGTCCAAGAACGACCAPorH(His)-RCACCAGGCCGCTGCTGTGATGATGATGATGATGGCTGCTGCCCATGCTACCTCCTCCACCGCTALsgad(His)-FATCACAGCAGCGGCCTGGTGCGCGGCAGCCATATGTCCAAGAACGACCAdKEJ-FCAATTGCGGCCGCCTTAAGGGAAAGGAGAGGATTGATGGGACGTGCAGTAGGAATdKEJ-RTCGACGGATCCGTTAACGCTAGCGGTTCTGGCCCGCLs-dg-FCACCGTTCGCTAGGAATTCGTGAGCTGTTGACAATTAATCLs-dKEJ-RCCTGCAGGTATACTCTAGAGCTAGCGGTTCTGGCCCGCCgSL-FAAGGGGCCCGTTAACGGATCCGAAAGGAGAGGATTAGTGGCAAACGTCAACATCAAgSL-RACTCTAGAGAGCTCGAATTTTAGTGGTGATGATGTCCTGCLs-gSL-RCCTGCAGGTATACTCTAGAGTTAGTGGTGATGATGTCCTG
以质粒pJYW-5-R4a-gadB2-R4a-gadB1mut[13]为模板,分别利用引物对gadB2(PorH)-F/gadB2(SalⅠ)-R和gadB1mut-F/gadB1mut(SalⅠ)-R扩增基因gadB2和基因gadB1mut;以谷氨酸棒杆菌ATCC 13032基因组为模板,分别利用引物对PorH-F/PorH(B2)-R和PorH-F/PorH(Linker3)-R扩增porH,与上述方法相同,将扩增得到的gadB2和gadB1mut分别与对应的porH进行融合并插入经酶切处理过的pJYW-5载体中,获得质粒p5-porH-B2和p5-porH-B1m。将这2种表面展示质粒分别转化至谷氨酸棒杆菌ATCC 13032中,获得菌株G-HB2和G-HBm。
1.3.1.2 改进型表面展示质粒和菌株的构建
将锚定基序和目的蛋白LsGAD之间的接头序列由(G4S)2延长至(G4S)3。以谷氨酸棒杆菌ATCC 13032基因组为模板,利用引物对PorH-F/PorH(Linker3)-R扩增porH;以p5-Lsgad为模板,利用引物对Lsgad(Linker3)-F/Lsgad-R扩增Lsgad,与上述方法相同,构建了质粒p5-porHL-gad;利用引物对PorH-F/PorH(His)-R和Lsgad(His)-F/Lsgad-R将来源于载体pET-28a(+)的含有His·Tag的片段与序列(G4S)2连接,以延长接头序列,构建了质粒p5-porHHis-gad。将这2个表面展示质粒分别转化至谷氨酸棒杆菌ATCC 13032,获得2个表面展示菌株G-HL和G-HH。
以谷氨酸棒杆菌ATCC 13032基因组为模板,利用引物对dKEJ-F/dKEJ-R扩增dnaK-grpE-dnaJ(即dKEJ)基因,以谷氨酸棒杆菌SN01基因组为模板,利用引物对gSL-F/gSL-R扩增groES-groEL(即gSL)基因,分别将蛋白质分子伴侣基因dKEJ和gSL插入经酶切处理过的pJYW-5载体上,获得质粒p5-dKEJ和p5-gSL。然后分别以质粒p5-dKEJ和p5-gSL为模板,分别利用引物对Ls-dg-F/Ls-dKEJ-R和Ls-dg-F/Ls-gSL-R扩增PtacM-dnaK-grpE-dnaJ(即PtacM-dKEJ)片段和PtacM-groES-groEL(即PtacM-gSL)片段,将获得的PtacM-dKEJ和PtacM-gSL分别插入经酶切处理过的p5-porH-gad质粒上,最终获得质粒p5-porH-gad-dKEJ和p5-porH-gad-gSL,将获得的2个质粒分别转化至谷氨酸棒杆菌ATCC 13032,获得菌株G-Hd和G-Hg。
1.3.1.3 生产GABA的代谢工程重组菌株的构建
基于文献[5]的方法对谷氨酸棒杆菌的基因组进行编辑。将gabP敲除质粒pSYN2[5]转化到菌株G0中,经过同源重组和Cre-loxP位点特异性重组,产生gabP缺失菌株G1,将质粒p5-porHL-gad转化至菌株G1中,获得重组菌株G1-HL。
1.3.2 重组谷氨酸棒杆菌的GABA发酵生产
种子培养基和发酵培养基的配制参考文献[13]的方法。
谷氨酸棒杆菌在活化后接入种子培养基中,在30 ℃和200 r/min条件下预培养8 h,按初始OD562值1.9将种子液转接到含有30 mL发酵培养基的500 mL带挡板摇瓶中,并通过调节pH法或不调节pH法在30 ℃和200 r/min条件下培养至72 h。对于调节pH法,初始pH值为7.2,初始尿素质量浓度为4 g/L。在10~24 h的发酵过程中,每2 h检测一次pH值,当pH值降至6.5以下时,补加2 g/L的尿素。对于不调节pH法,初始pH值为6.0,初始尿素质量浓度为6 g/L。在发酵12 h时,同时加入7 g/L尿素和7 g/L (NH4)2SO4溶液。在发酵过程中,每12 h取1 mL发酵液,以测定OD562值、残糖浓度、pH值以及L-谷氨酸和GABA的含量。
1.3.3 GAD活力测定方法
酶活力的测定方法和酶活单位的定义参考文献[13]的方法。表面展示菌株的细胞悬浮液直接用作酶溶液。
1.4 数据处理
使用Excel进行数据统计并分析,使用GraphPad prism进行制图。
2 结果与分析
2.1 利用不同锚定基序表面展示LsGAD对GABA生产的影响
在谷氨酸棒杆菌摇瓶发酵生产GABA的过程中,初始pH值为7.2,随着发酵前期L-谷氨酸的不断积累和分泌,在发酵中期pH值不断降低至5.0~5.7。当胞外pH变化为酸性时,胞内的pH会由于pH维稳机制的存在而与胞外的pH存在差异,比胞外更偏向中性pH,而GAD的最适pH一般为酸性,这使得在胞内表达的GAD不能更好地发挥活性。另外大量的前体物质L-谷氨酸在细胞生长过程中被分泌到胞外,这导致胞内表达的GAD在合成GABA时所需的底物L-谷氨酸不足。本研究中,通过表面展示技术将LsGAD展示在谷氨酸棒杆菌的细胞表面上,从而使LsGAD在更合适的酸性环境中发挥作用,同时将不断分泌到胞外的L-谷氨酸直接转化为目的产物GABA,无需再进行GABA从胞内到胞外的转运,以改善GABA的合成效率。
锚定基序NCgl1221是含4个跨膜区的通道蛋白,负责L-谷氨酸分泌,其全长型和截短型NCgl1221ΔC的C末端均位于细胞外。C端截短后,NCgl1221蛋白结构改变,促使L-谷氨酸持续输出,且不影响膜张力,有利于L-谷氨酸的生产和积累[9]。分枝菌酸层蛋白NCgl1337经O-分枝菌酰化修饰后锚定于细胞表面,使用其全长型作为锚定基序时,因尺寸大导致空间位阻大,表面展示效果不如截短型NCgl1337[11]。位于谷氨酸棒杆菌分枝菌酸层的孔蛋白,参与亲水性小分子的摄取和通过,由于它们的分子质量小(约10 kDa),其与靶蛋白形成的融合蛋白更易展示于细胞表面[10]。最近研究人员通过基因组挖掘技术发现了其他一些新型锚定基序,如NCgl1307和NCgl2775,均能成功将靶蛋白展示于谷氨酸棒杆菌细胞表面且效果更佳[8]。因此,本研究选择了6种不同的锚定基序NCgl1337S、NCgl1221ΔC、PorH、PorB、NCgl1307和NCgl2775,将它们分别与LsGAD的N-末端进行融合,分别获得表面展示菌株G-37、G-21、G-H、G-B、G-07和G-75。将质粒p5-Lsgad转化至谷氨酸棒杆菌ATCC 13032中,获得胞内表达LsGAD的菌株G-N。
在不调节pH的发酵方式下进行锚定基序的筛选,结果如图1所示。分别含有锚定基序PorH和NCgl1307的菌株G-H和G-07表现出了一定的GABA生产能力,虽然菌株G-H的生长速度和葡萄糖消耗速度慢于菌株G-07(图1-a),但是菌株G-H产生1.7 g/L GABA,略高于菌株G-07(1.1 g/L GABA)(图1-b)。与胞内表达LsGAD的菌株G-N(10.9 g/L GABA)相比,虽然菌株G-H和G-07在表面展示LsGAD后GABA生产能力显著下降,但仍然展现出一定的GABA生产潜力。此外,LsGAD与锚定基序NCgl1337S和NCgl1221ΔC的融合表达严重影响了菌株G-37和G-21的生长、葡萄糖消耗和L-谷氨酸合成,并且这2个菌株不产生GABA。LsGAD与锚定基序NCgl2775的融合虽然促进了菌株G-75的生长和L-谷氨酸合成,但L-谷氨酸无法转化为GABA。LsGAD与锚定基序PorB的融合不会显著影响菌株G-B的生长和L-谷氨酸合成,但也没有合成出GABA。
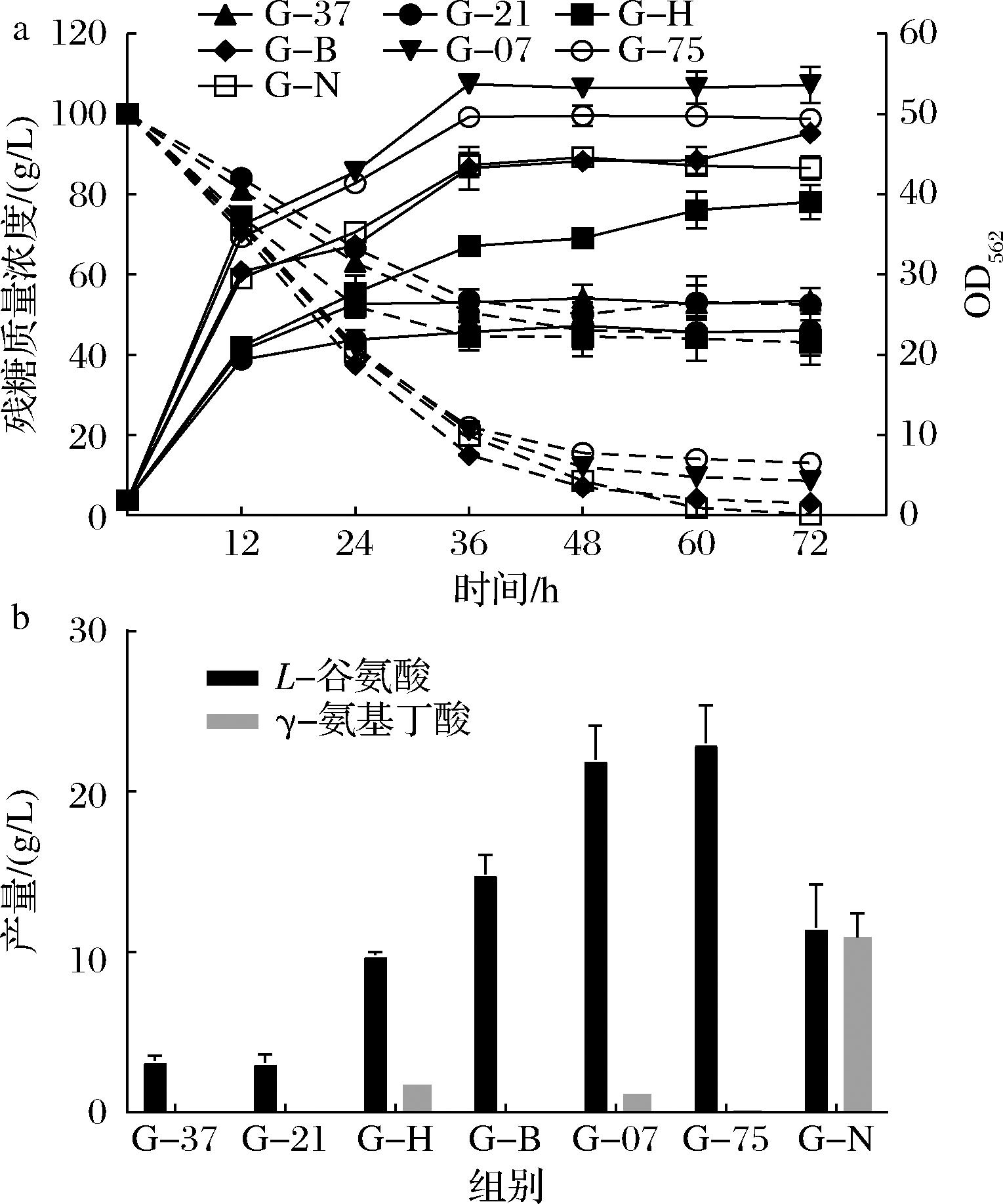
a-不同表面展示菌株的细胞生长和葡萄糖消耗情况;b-不同表面展示菌株的L-谷氨酸和GABA的产量
图1 在谷氨酸棒杆菌中不同锚定基序对LsGAD的表面展示和GABA生产的影响
Fig.1 Effect of different anchoring motifs on surface display of LsGAD and GABA production in C.glutamicum ATCC13032
注:虚线-残糖浓度,实线-细胞生长,下同。
靶蛋白在细胞表面的展示效率受许多因素影响,包括靶蛋白的尺寸、锚定基序、融合蛋白之间的接头序列、融合蛋白能否正确折叠等[14]。LsGAD表面展示后GABA产量显著降低,可能是由于融合后的LsGAD不能正确折叠。融合蛋白之间的接头序列在表面展示的功效中起着至关重要的作用,不合适的接头序列会影响融合蛋白的正确折叠。分子伴侣能够帮助新生蛋白质正确折叠。因此,本研究后续将着手对锚定基序PorH表面展示GAD的改进策略加以探究。
2.2 探究锚定基序PorH对不同GAD进行表面展示的效果
对于表面展示技术,除了锚定基序以外,靶蛋白的尺寸对表面展示效率也有着较强的影响。较小尺寸的靶蛋白通常更容易被展示在细胞表面上,因为在通过细胞膜的转运过程受到的阻碍相对较小,能够更顺利地穿越膜结构,从而更容易到达细胞表面,而较大尺寸的靶蛋白在转运过程中可能会因为较大的体积而受到阻碍,从而影响靶蛋白的转运效率和降低表面展示效率[15]。不同来源的GAD具有不同的蛋白质结构和亚基数目,来自于大肠杆菌的GAD为六聚体[16],来源于短乳杆菌(Lactobacillus brevis)CGMCC 1306的GAD为二聚体[17]。本实验室之前筛选出的短乳杆菌Lb85有2种谷氨酸脱羧酶GadB1(由gadB1基因编码)和GadB2(由gadB2基因编码),这2种酶的最适pH值为4.0~5.0,且GadB2的GABA生产能力优于GadB1[18]。为了适合GABA的生产,本研究又获得了pH活性范围拓宽的突变型GadB1T17I/D294G/E312S/Q346H(即GadB1mut)[19]。GadB1mut、GadB2和LsGAD序列与来源于大肠杆菌的GAD的一致性分别为41%、34.9%和35.3%,与来源于短乳杆菌CGMCC 1306的GAD的一致性分别为98.5%、49.6%和49%。
已有研究在大肠杆菌中成功对来源于Pyrococcus horikoshii的单体蛋白质GadB进行表面展示并生产出5.35 g/L GABA[20]。为了探究不同尺寸的GAD对表面展示效率的影响,本研究利用锚定基序PorH对GadB2和GadB1mut分别进行了表面展示。在不调节pH的发酵方式下,结果显示菌株G-HB2和G-HB1m的生长正常且葡萄糖消耗情况相似(图2-a),菌株G-HB2产生了0.3 g/L GABA,而G-HB1m没有产生GABA(图2-b),这可能是由于GadB2的活性优于GadB1mut。与过去在胞内表达GadB2和GadB1mut生产GABA的结果相比[21],表面展示后的GABA生产效率显著下降。与LsGAD的表面展示效率相比,GadB2和GadB1mut的表面展示效率更低,这可能是由于LsGAD比GadB2和GadB1mut具有更宽的pH活性范围[22]。因此LsGAD仍然是比较适宜的用于GABA生产的表面展示靶蛋白。
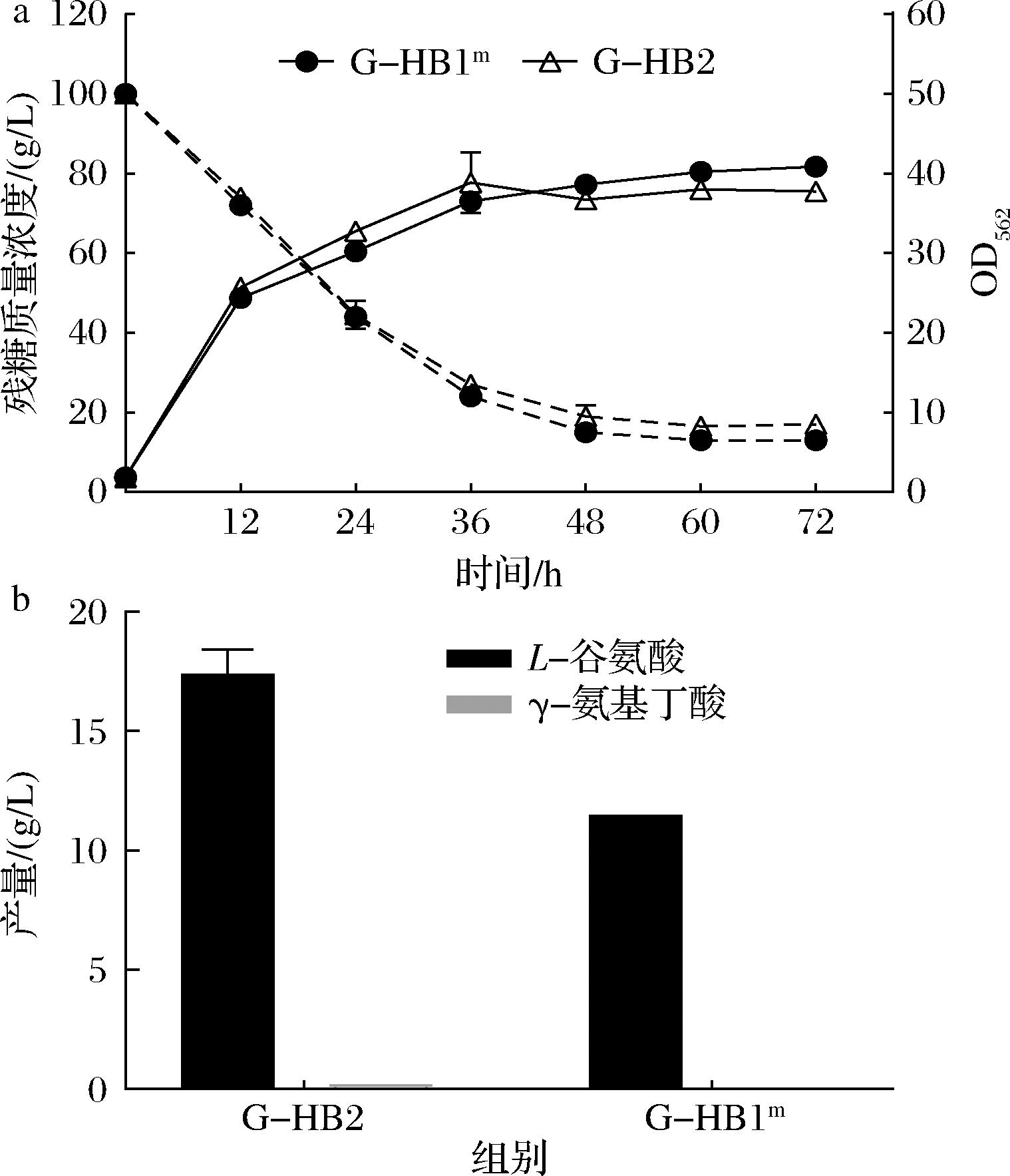
a-菌株G-HB2和G-HB1m的细胞生长和葡萄糖消耗情况;b-菌株G-HB2和G-HB1m的L-谷氨酸和GABA产量
图2 在谷氨酸棒杆菌中锚定基序PorH对GadB2和GadB1mut表面展示的影响
Fig.2 Effect of anchoring motif PorH on surface display of GadB2 and GadB1mut in C.glutamicum ATCC13032
2.3 延长接头序列以优化表面展示效率
融合蛋白之间的接头序列对融合蛋白的正确折叠具有重要的影响。适当长度的接头序列可以为融合蛋白提供足够的空间,从而使各个结构域能够独立折叠,减少相互干扰,增加融合蛋白正确折叠的概率和正常发挥功能。LsGAD与锚定基序的融合导致GABA产量显著下降,可能是由于接头序列的长度不合适而影响了LsGAD的折叠和功能发挥。因此,本研究首先通过将接头序列从最初使用的(G4S)2延伸为具有15个氨基酸的(G4S)3,构建了一个具有PorH锚定基序的接头序列延长的表面展示菌株,即G-HL。其次,本研究在原有接头序列的基础上,通过连接来源于质粒pET-28a(+)的含有His·Tag的片段,将接头序列延伸至29个氨基酸的长度,构建了另外一个具有PorH锚定基序的接头序列延长的表面展示菌株,即G-HH。
在不调节pH的发酵方式下,表面展示菌株G-HL和G-HH的生长正常且葡萄糖消耗情况没有显著差异(图3-a)。菌株G-HL和G-HH分别获得2.1 g/L和1.1 g/L GABA(图3-b)。与未延长接头序列的菌株G-H相比,菌株G-HL的GABA产量提升,而菌株G-HH的GABA产量下降。因此本研究对菌株G-HL中的LsGAD进行了酶活性测定,结果表明在延长接头序列后,锚定基序PorH表面展示的LsGAD的酶活性由G-H的3.24 U/g DCW增加为G-HL的6.05 U/g DCW。这表明延伸接头序列为(G4S)3的策略对于优化表面展示的效率、促进靶蛋白LsGAD的正确折叠是有效的。
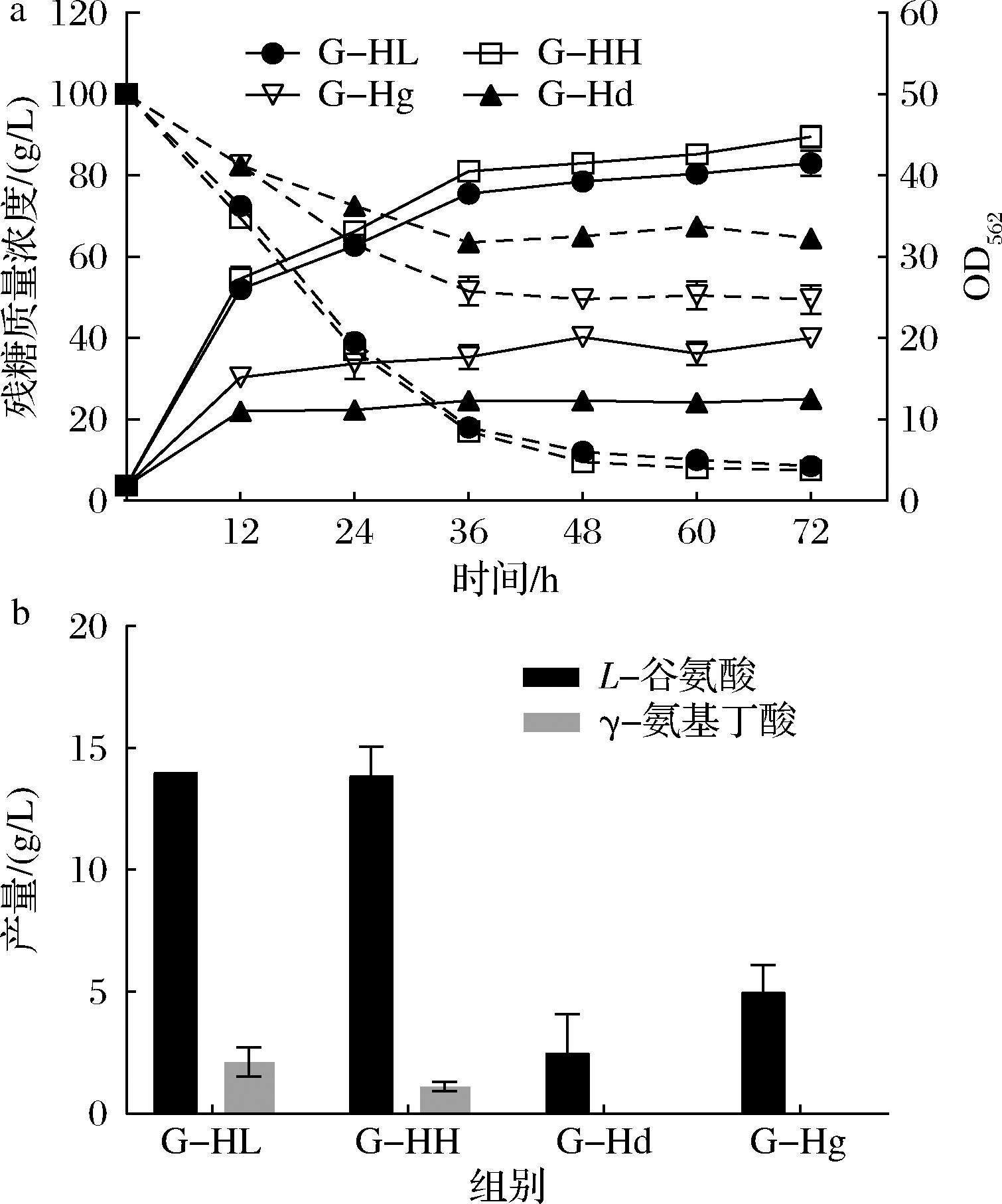
a-不同菌株的细胞生长和葡萄糖消耗情况;b-不同菌株的L-谷氨酸和GABA产量
图3 延长接头序列或与分子伴侣共表达对LsGAD表面展示的影响
Fig.3 Effect of extending linker sequences or co-expressing with molecular chaperones on surface display of LsGAD
2.4 融合蛋白和分子伴侣共表达以优化表面展示效率
分子伴侣是一类与其他蛋白质相互作用并帮助其进行折叠和组装的蛋白质,但是不作为最终功能结构的一部分。分子伴侣主要具有促进折叠和防止蛋白质聚集的功能。分子伴侣与靶蛋白共同作用时,可以帮助靶蛋白增强构象和功能的稳定性,以增强目的产物的生产[23]。在本研究中,表面展示后GABA产量显著下降,这可能是由于锚定基序和LsGAD组成的融合蛋白出现了折叠错误或聚集的情况,为了促进融合蛋白的折叠,考虑利用谷氨酸棒杆菌本身的分子伴侣GroEL-GroES复合物和DnaK-GrpE-DnaJ复合物[24]分别与融合蛋白进行共表达,获得了菌株G-Hg和G-Hd。在不调节pH的发酵方式下,结果表明,在融合蛋白和分子伴侣共表达后,菌株G-Hg和G-Hd的生长和葡萄糖摄取均受到了严重抑制(图3-a),L-谷氨酸的积累较少,且均未产生任何的GABA(图3-b)。之前的一项研究结果表明,分子伴侣的表达对细胞的生长有轻微的抑制[24],本研究中出现的显著抑制可能是由于融合蛋白和分子伴侣的表达强度较强,且融合蛋白结构复杂,它们的合成都需要消耗大量的能量和氨基酸,这增加了代谢负担,抑制了细胞生长。
2.5 改善发酵方式以优化表面展示效率
展示于细胞表面的LsGAD与胞外发酵环境直接接触,其酶活性受胞外发酵环境的显著影响。最初不调节pH的发酵方式会任由发酵过程中pH发生大幅变化,从而影响LsGAD的酶活性和GABA的生产。因此本研究又通过在发酵10~24 h过程中添加尿素来调控培养的pH值,以此保障谷氨酸棒杆菌的正常生长以及L-谷氨酸的有效积累。当发酵进行到24 h之后,凭借酸性L-谷氨酸的持续积累,pH值会自然而然地下降至酸性水平(图4-a),使得LsGAD被激活,为后续转化合成GABA的反应创造了条件。
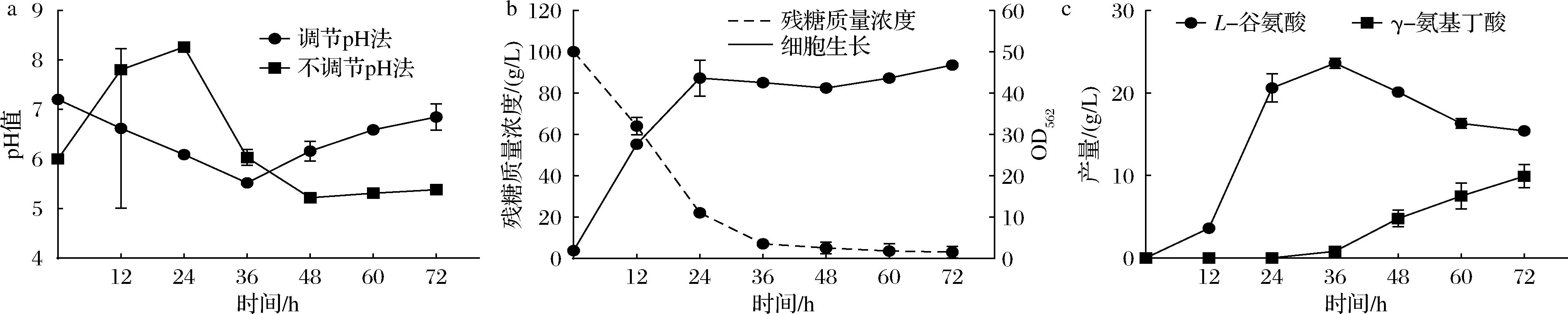
a-调节pH法和不调节pH法在发酵过程中pH的变化;b-菌株G-HL的细胞生长和葡萄糖消耗情况;c-菌株G-HL的L-谷氨酸和GABA产量
图4 调节pH的发酵方式对优化后的表面展示菌株G-HL生产GABA的影响
Fig.4 Effect of pH-adjusted fermentation mode on GABA production by optimized surface-displayed strain G-HL
利用调节pH的方式对上述研究中获得的最优表面展示菌株G-HL进行摇瓶培养,研究结果表明,与未调节pH的对照组(图3-a)相比,该菌株的生长和葡萄糖消耗未受到显著影响(图4-b)。同时,GABA的产量显著增加至9.9 g/L(图4-c),比不调节pH条件下的产量高约3.61倍。在发酵过程中,L-谷氨酸的质量浓度在24~36 h内达到最高水平,为21~24 g/L(图4-c)。随后,其浓度逐渐下降并转化为GABA。这一结果与SHI等[21]的研究结果一致,表明在调节pH的发酵方式下,可以有效促进发酵早期L-谷氨酸的积累和后期GABA的生成。进一步分析发现,通过在发酵的早期阶段补充尿素以保持中性pH,可以使得合成L-谷氨酸的关键酶L-谷氨酸脱氢酶以最佳活性发挥作用,这导致了更高水平的L-谷氨酸积累。积累的L-谷氨酸随后可以被低pH下激活的GAD转化为GABA,从而为改善GABA的生产提供了有力支持。
2.6 阻断GABA摄取途径以提高GABA产量
在谷氨酸棒杆菌中,L-谷氨酸的碳流来自于α-酮戊二酸(α-ketoglutarate,α-KG)节点,ODHC是在该节点与L-谷氨酸合成相竞争的主要酶。OdhI蛋白能够抑制ODHC,丝氨酸/苏氨酸蛋白激酶PknG通过使OdhI发生磷酸化,从而使其失去抑制活性(图5-a)。已有研究表明,PknG(由pknG基因编码)的缺失能够降低ODHC的活性,使更多的α-KG节点的碳通量能够分配到L-谷氨酸和GABA的合成途径中。有研究发现pknG缺失的谷氨酸棒杆菌ATCC 13032在生物反应器中发酵72 h后,L-谷氨酸含量从34.7 g/L增加至44.8 g/L,GABA产量从19.4 g/L增加至30.2 g/L[6-7]。YAO等[25]通过破坏谷氨酸棒杆菌CGY700中的PknG,使GABA的摇瓶发酵产量从19.14 g/L增加至20.84 g/L。这些结果表明,敲除pknG是一种有效的策略,可以提高GABA的合成效率。此外,由gabP基因编码的GABA渗透酶GabP是谷氨酸棒杆菌中存在的唯一一种GABA特异性转运蛋白,负责将胞外的GABA转运回胞内,使其作为碳氮源被重新利用[5](图5-b)。在NI等[5]的研究中,gabP缺失菌株在发酵72~84 h期间,GABA降解量约0.8 g/L,明显低于野生型菌株的3.9 g/L GABA。这表明,阻断GABA摄取途径可以有效减少GABA的降解,增加其在胞外的积累。因此,为了增强前体L-谷氨酸的供应和阻断GABA的重新摄取,以pknG缺失的菌株G0作为底盘菌株,再敲除gabP基因,获得菌株G1。然后将最佳表面展示质粒p5-porHL-gad转化至菌株G1中,获得GABA生产菌株G1-HL。
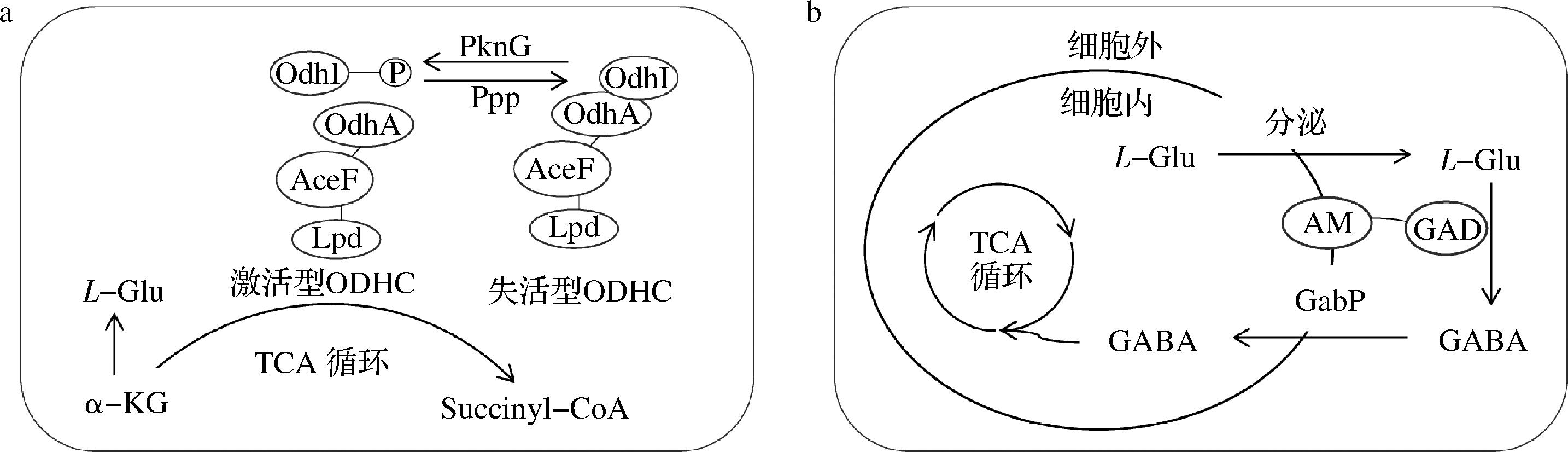
a-PknG对ODHC的调控作用;b-GabP对GABA的转运
图5 PknG对ODHC的调控作用以及GabP对GABA的转运
Fig.5 Regulation of ODHC by PknG and transport of GABA by GabP
注:OdhI:α-酮戊二酸脱氢酶抑制剂;AceF:二氢硫辛酰琥珀酰转移酶;Lpd:二氢硫辛酸脱氢酶;OdhA:α-酮戊二酸脱氢酶;Ppp:磷蛋白磷酸酶;Succinyl-CoA:琥珀酰辅酶A;AM:锚定基序。
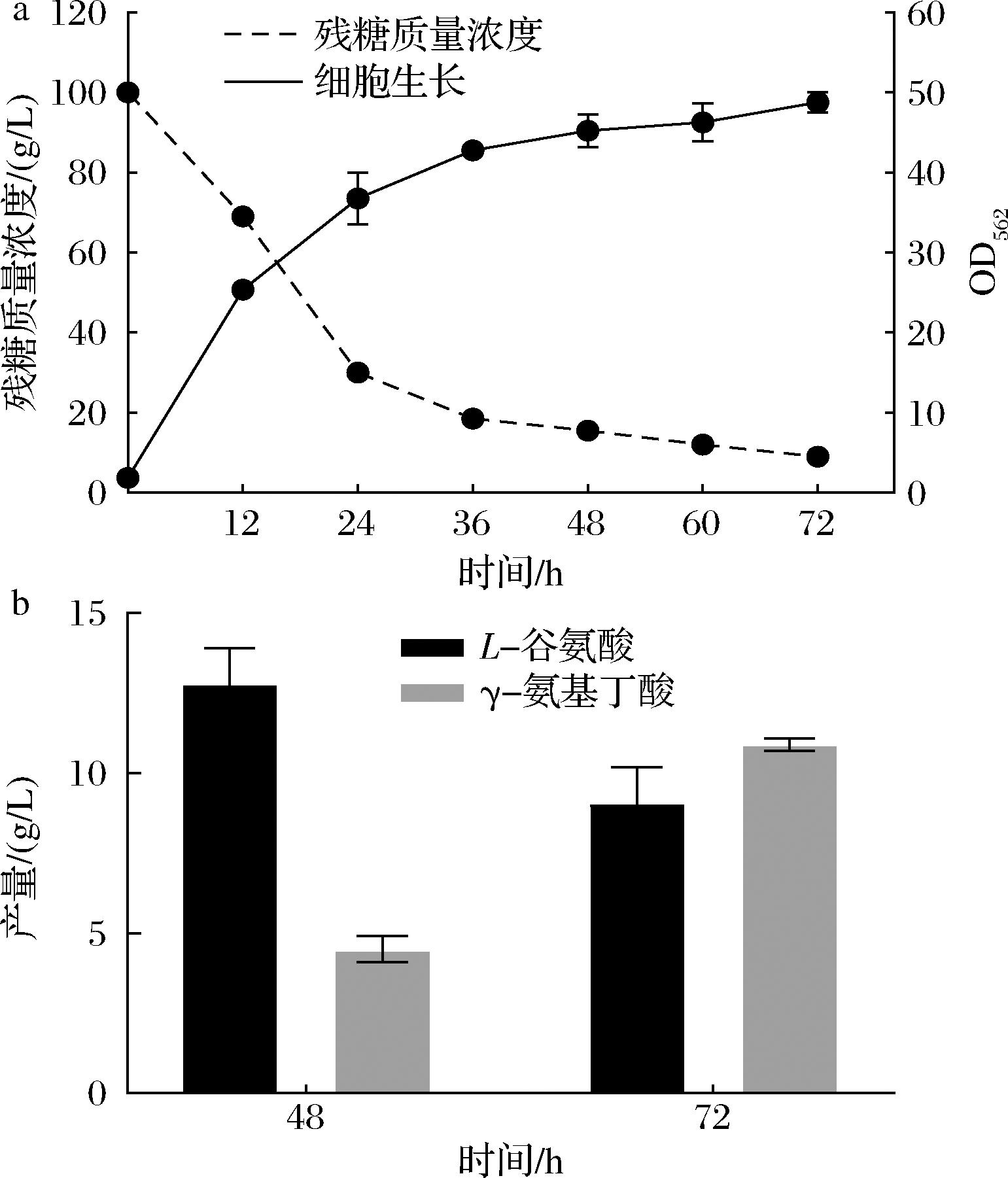
a-菌株G1-HL的细胞生长和葡萄糖消耗情况;b-菌株G1-HL的L-谷氨酸和GABA产量
图6 代谢工程重组菌株G1-HL在调节pH的发酵方式下进行的GABA生产
Fig.6 GABA production by metabolically engineered recombinant strain G1-HL under pH-adjusted fermentation mode
在调节pH的发酵方式下进行摇瓶培养,结果表明,菌株G1-HL生长良好,葡萄糖在72 h后基本消耗殆尽(图6-a)。在48~72 h,L-谷氨酸的含量由12.8 g/L降低至9.1 g/L,GABA的含量从4.5 g/L增加至10.9 g/L(图6-b)。L-谷氨酸在发酵过程中不断被转化为GABA。与在野生型ATCC 13032中表达p5-porHL-gad的菌株G-HL(9.9 g/L GABA)相比(图4-c),最终的GABA产量有所提高。与之前的研究结果[5-6]一致,pknG和gabP基因的缺失能改善GABA的生产。
3 结论与讨论
本研究创新性地将LsGAD通过不同的锚定基序展示在谷氨酸棒杆菌的细胞表面上,并通过延长接头序列的方式对表面展示策略进行了改进和优化,使LsGAD能够在更有利的酸性环境中发挥作用,产生了2.1 g/L GABA。在此基础上,进一步改进了发酵方式。通过调节pH的发酵方式,使胞外环境pH的变化更加适合细胞的生长以及GAD活性的发挥,这一改进将GABA的产量显著提升至9.9 g/L,验证了发酵时pH调节方式对于提高GABA生产的重要性。最终,通过阻断GABA的摄取途径,有效地增加了GABA的积累,重组菌株G1-HL成功获得了10.9 g/L的GABA。虽然该产量仍然低于通过改造分枝菌酸层以增强前体L-谷氨酸摄取等多种方式获得的最高摇瓶产量(52.36 g/L)[26],但这些研究证明了表面展示策略合成GABA的有效性,为后续的工业生产提供了有力的参考。在未来的研究中,可以通过选择和设计更合适的锚定基序以及接头序列,来进一步改善GAD的表面展示效果,提升GABA的产量。综上所述,本研究为谷氨酸棒杆菌展示GAD和生产GABA提供了一种新的策略。这一策略不仅有助于提高GABA的产量,还为谷氨酸棒杆菌中其他产物的代谢工程研究提供了有益的借鉴,具有广阔的应用前景。
[1] LUO H Z, LIU Z, XIE F, et al.Microbial production of gamma-aminobutyric acid:Applications, state-of-the-art achievements, and future perspectives[J].Critical Reviews in Biotechnology, 2021, 41(4):491-512.
[2] 俞德慧, 杨杨, 陈凤莲, 等.γ-氨基丁酸及其在谷物发酵食品中的研究进展[J].食品与发酵工业, 2022, 48(11):290-296.
YU D H, YANG Y, CHEN F L, et al.Research progress of γ-aminobutyric acid in cereal fermented food[J].Food and Fermentation Industries, 2022, 48(11):290-296.
[3] SON J, BARITUGO K A, SOHN Y J, et al.Production of γ-aminobutyrate (GABA) in recombinant Corynebacterium glutamicum by expression of glutamate decarboxylase active at neutral pH[J].ACS Omega, 2022, 7(33):29106-29115.
[4] T UBER S, BLÖBAUM L, WENDISCH V F, et al.Growth response and recovery of Corynebacterium glutamicum colonies on single-cell level upon defined pH stress pulses[J].Frontiers in Microbiology, 2021, 12:711893.
UBER S, BLÖBAUM L, WENDISCH V F, et al.Growth response and recovery of Corynebacterium glutamicum colonies on single-cell level upon defined pH stress pulses[J].Frontiers in Microbiology, 2021, 12:711893.
[5] NI Y L, SHI F, WANG N N.Specific γ-aminobutyric acid decomposition by gabP and gabT under neutral pH in recombinant Corynebacterium glutamicum[J].Biotechnology Letters, 2015, 37(11):2219-2227.
[6] SUNDERMEYER L, BOSCO G, GUJAR S, et al.Characteristics of the GlnH and GlnX signal transduction proteins controlling PknG-mediated phosphorylation of OdhI and 2-oxoglutarate dehydrogenase activity in Corynebacterium glutamicum[J].Microbiology Spectrum, 2022, 10(6):e02677-22.
[7] 王楠楠, 倪亚兰, 史锋.敲除pknG提高谷氨酸棒杆菌L-谷氨酸和GABA产量[J].食品与生物技术学报, 2017, 36(2):187-193.
WANG N N, NI Y L, SHI F.Deletion of pknG improves the production of L-glutamate and GABA in recombinant corynbacterium glutamicum[J].Journal of Food Science and Biotechnology, 2017, 36(2):187-193.
[8] LIN K R, ZHAO N N, CAI Y H, et al.Genome-scale mining of novel anchor proteins of Corynebacterium glutamicum[J].Frontiers in Microbiology, 2022, 12:677702.
[9] YAO W J, CHU C L, DENG X Z, et al.Display of α-amylase on the surface of Corynebacterium glutamicum cells by using NCgl1221 as the anchoring protein, and production of glutamate from starch[J].Archives of Microbiology, 2009, 191(10):751-759.
[10] TATENO T, HATADA K, TANAKA T, et al.Development of novel cell surface display in Corynebacterium glutamicum using porin[J].Applied Microbiology and Biotechnology, 2009, 84(4):733-739.
[11] CHOI J W, YIM S S, JEONG K J.Development of a potential protein display platform in Corynebacterium glutamicum using mycolic acid layer protein, NCgl1337, as an anchoring motif[J].Biotechnology Journal, 2018, 13(2):1700509.
[12] HU J Y, LI Y Y, ZHANG H L, et al.Construction of a novel expression system for use in Corynebacterium glutamicum[J].Plasmid, 2014, 75:18-26.
[13] SHI F, LUAN M Y, LI Y F.Ribosomal binding site sequences and promoters for expressing glutamate decarboxylase and producing γ-aminobutyrate in Corynebacterium glutamicum[J].AMB Express, 2018, 8(1):61.
[14] ZHANG C M, CHEN H Y, ZHU Y P, et al.Saccharomyces cerevisiae cell surface display technology:Strategies for improvement and applications[J].Frontiers in Bioengineering and Biotechnology, 2022, 10:1056804.
[15] GAO K P, YU K X, SUN J N, et al.Engineering an Escherichia coli surface display platform based on an autotransporter from Stenotrophomonas maltophilia:Autodisplay of enzymes with low to high molecular weight[J].Journal of Biotechnology, 2025, 398:97-104.
[16] CAPITANI G, DE BIASE D, AURIZI C, et al.Crystal structure and functional analysis of Escherichia coli glutamate decarboxylase[J].The EMBO Journal, 2003, 22(16):4027-4037.
[17] HUANG J, FANG H, GAI Z C, et al.Lactobacillus brevis CGMCC 1306 glutamate decarboxylase:Crystal structure and functional analysis[J].Biochemical and Biophysical Research Communications, 2018, 503(3):1703-1709.
[18] SHI F, LI Y X.Synthesis of γ-aminobutyric acid by expressing Lactobacillus brevis-derived glutamate decarboxylase in the Corynebacterium glutamicum strain ATCC 13032[J].Biotechnology Letters, 2011, 33(12):2469-2474.
[19] SHI F, XIE Y L, JIANG J J, et al.Directed evolution and mutagenesis of glutamate decarboxylase from Lactobacillus brevis Lb85 to broaden the range of its activity toward a near-neutral pH[J].Enzyme and Microbial Technology, 2014, 61-62:35-43.
[20] SOMASUNDARAM S, JEONG J, KUMARAVEL A, et al.Whole-cell display of Pyrococcus horikoshii glutamate decarboxylase in Escherichia coli for high-titer extracellular gamma-aminobutyric acid production[J].Journal of Industrial Microbiology &Biotechnology, 2021, 48(7-8):kuab039.
[21] SHI F, JIANG J J, LI Y F, et al.Enhancement of γ-aminobutyric acid production in recombinant Corynebacterium glutamicum by co-expressing two glutamate decarboxylase genes from Lactobacillus brevis[J].Journal of Industrial Microbiology &Biotechnology, 2013, 40(11):1285-1296.
[22] TANG C D, LI X, SHI H L, et al.Efficient expression of novel glutamate decarboxylases and high level production of γ-aminobutyric acid catalyzed by engineered Escherichia coli[J].International Journal of Biological Macromolecules, 2020, 160:372-379.
[23] FATIMA K, NAQVI F, YOUNAS H.A review:Molecular chaperone-mediated folding, unfolding and disaggregation of expressed recombinant proteins[J].Cell Biochemistry and Biophysics, 2021, 79(2):153-174.
[24] WANG Y L, LIU X X, LI Y, et al.Enhanced production of recombinant proteins in Corynebacterium glutamicum using a molecular chaperone[J].The Journal of General and Applied Microbiology, 2023, 69(1):34-44.
[25] YAO C Z, SHI F, WANG X Y.Chromosomal editing of Corynebacterium glutamicum ATCC 13032 to produce gamma-aminobutyric acid[J].Biotechnology and Applied Biochemistry, 2023, 70(1):7-21.
[26] WANG Y, YAO C Z, HUANG D Y, et al.Metabolic engineering of Corynebacterium glutamicum CGY-PG-304 for promoting gamma-aminobutyric acid production[J].Systems Microbiology and Biomanufacturing, 2024, 4(3):915-927.