新霉素主要是由费氏链霉菌代谢糖类物质通过磷酸戊糖途径转化生产的氨基糖苷类抗生素[1],被广泛用于医药和农业领域,如农作物疾病防控、呼吸道和胃肠道细菌感染的治疗等[2]。菌种性能好坏是决定新霉素产量和质量的核心因素,菌种选育成功的关键是获得多样性的突变子库和开发高通量的筛选方法,而对于庞大的突变子库,开发高通量筛选方法至关重要[3]。目前研究人员主要通过现代诱变技术和结合合成路径的分子改造技术来获得大量的费氏链霉菌突变子,但主要还是通过抗性平板等来筛选正向突变子[4]。虽然高通量的筛选技术如流式细胞仪[5-6]、液滴微流控技术[7]等广泛应用于微生物细胞的快速筛选,但多半是基于荧光信号,且在链霉菌中应用较少。近年来,研究人员通过由基因编码的蛋白质或RNA元件(如转录因子[8]和核糖开关)普遍存在,这类生物分子能够通过构象变化感知胞内特定代谢物的浓度变化,进而调控下游基因的信号输出功能[9],如图1所示。基于此原理构建的代谢物生物传感器,通过生物识别元件将目标化合物浓度转化为荧光信号、细胞活性或代谢通路调控等可视化指标,其作用机制类似于微生物体内的精密监测仪表。这类合成生物学工具不仅能实时监测胞内代谢物动态变化,也为代谢工程优化提供了重要技术手段。
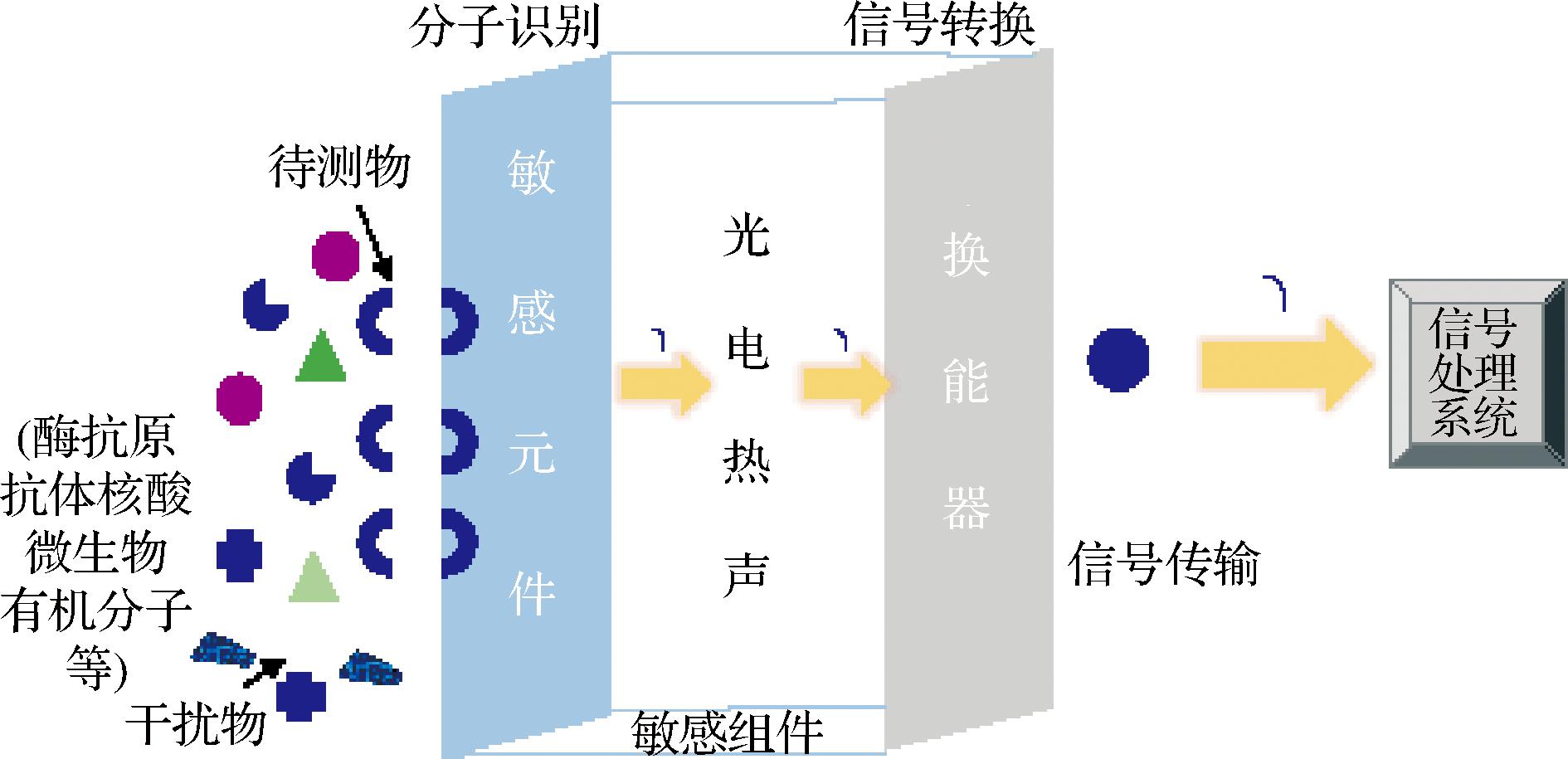
图1 生物传感器原理图
Fig.1 Schematic diagram of a biosensor
天然核糖开关RNA元件通常位于mRNA的5′端非编码区的一段高度保守的序列,其含有2个功能域:适体结构域(aptamer domain, AD)和表达结构域(expression domain, EPD)[10]。适体结构域特异性的结合目标代谢物后发生构象变化,引起了表达结构域形成选择性的茎环结构,从而引起下游相关基因表达水平的变化[11-14]。核糖开关首次由WINKLER等[15]于2002 年在大肠杆菌中发现,维生素B12转运蛋白mRNA的5′端非编码区的一段高度保守的序列结合5′-脱氧腺苷钴胺素后,该保守序列构象的改变阻断了核糖体结合到核糖体结合位点,调控了维生素B12转运蛋白的翻译。YOU等[16]构建的Spinach核糖开关通过与配体结合而激发荧光特性,其荧光强度和结合的亲和力呈正比。上述成功应用核糖开关构建生物传感器调控基因的表达为构建响应新霉素的核糖开关生物传感器筛选高产费氏链霉菌奠定了方法学基础。
目前微生物传感器主要有转录因子依赖型和核糖开关依赖型。费氏链霉菌内源和外源的转录因子能够特异性响应新霉素的报道不常见,而研究者在大肠杆菌中较为透彻地研究了能够特异性响应新霉素B的核糖开关N1[17-18]。因此,我们基于N1和基因线路原理尝试构建能够响应新霉素B[19-20]的生物传感器,为新霉素B高产菌株费氏链霉菌的高通量筛选提供技术方法。
1 材料与方法
1.1 材料
1.1.1 化学试剂和培养基
高保真DNA聚合酶(2×Phanta Max Master Mix)、同源重组酶C115(ClonExpress MultiS One Step Cloning Kit C115),南京诺唯赞生物科技股份有限公司;限制性核酸内切酶BamH I、Not I 、 EcoR V,赛默飞世尔科技公司;DNA Marker、质粒提取试剂盒、胶回收试剂盒,生工生物工程(上海)股份有限公司。
LB 固体培养基(g/L):酵母粉5,NaCl 10,蛋白胨10,琼脂 2%,pH 7.0;
LB液体培养基(g/L):蛋白胨10,NaCl 10,酵母粉5,pH 7.0;
YEME种子培养基(g/L):蔗糖103,麦芽粉3,葡萄糖10,酵母粉3,蛋白胨5, pH 7.0;
发酵培养基(g/L):可溶性淀粉 70,花生饼粉 28,酵母提取物 6,(NH4)2SO4 6,葡萄糖20,玉米浆 2.5,胰蛋白胨 9,中温豆饼粉5,NaCl 4.5,高温淀粉酶0.26,Na2HPO4 0.14,CaCO3 4,豆油 3,pH 6.8~7.3;
MS培养基(g/L):葡萄糖 10,牛肉膏 1,胰蛋白 3,玉米浆 3,NaCl 5,琼脂 20。
1.1.2 引物、质粒和菌株
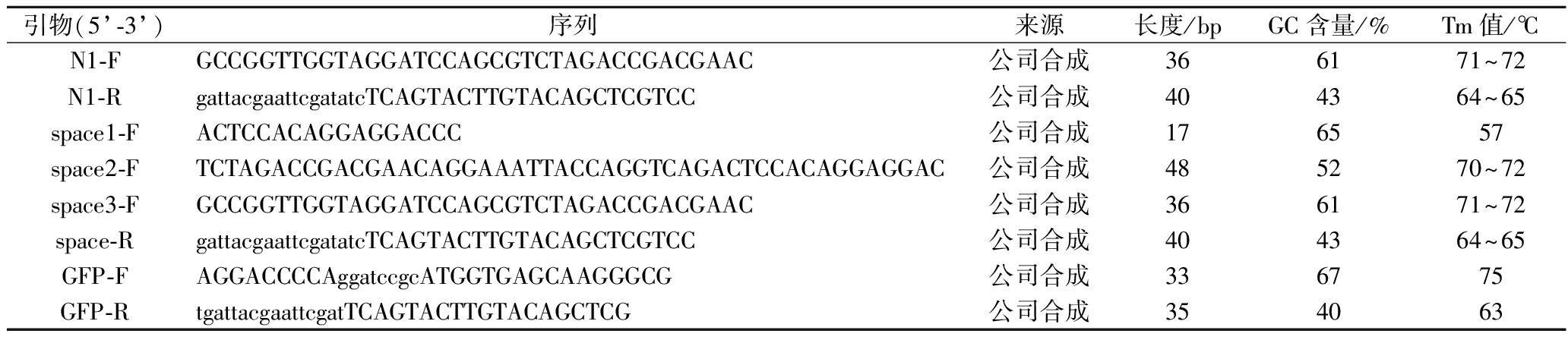
实验中所用的引物、质粒和菌株如表1、表2所示。
表1 引物
Table 1 Primers
引物(5’-3’)序列来源长度/bpGC含量/%Tm值/℃N1-FGCCGGTTGGTAGGATCCAGCGTCTAGACCGACGAAC公司合成366171~72N1-RgattacgaattcgatatcTCAGTACTTGTACAGCTCGTCC公司合成404364~65space1-FACTCCACAGGAGGACCC公司合成176557space2-FTCTAGACCGACGAACAGGAAATTACCAGGTCAGACTCCACAGGAGGAC公司合成485270~72space3-FGCCGGTTGGTAGGATCCAGCGTCTAGACCGACGAAC公司合成366171~72space-RgattacgaattcgatatcTCAGTACTTGTACAGCTCGTCC公司合成404364~65GFP-FAGGACCCCAggatccgcATGGTGAGCAAGGGCG公司合成336775GFP-RtgattacgaattcgatTCAGTACTTGTACAGCTCG公司合成354063
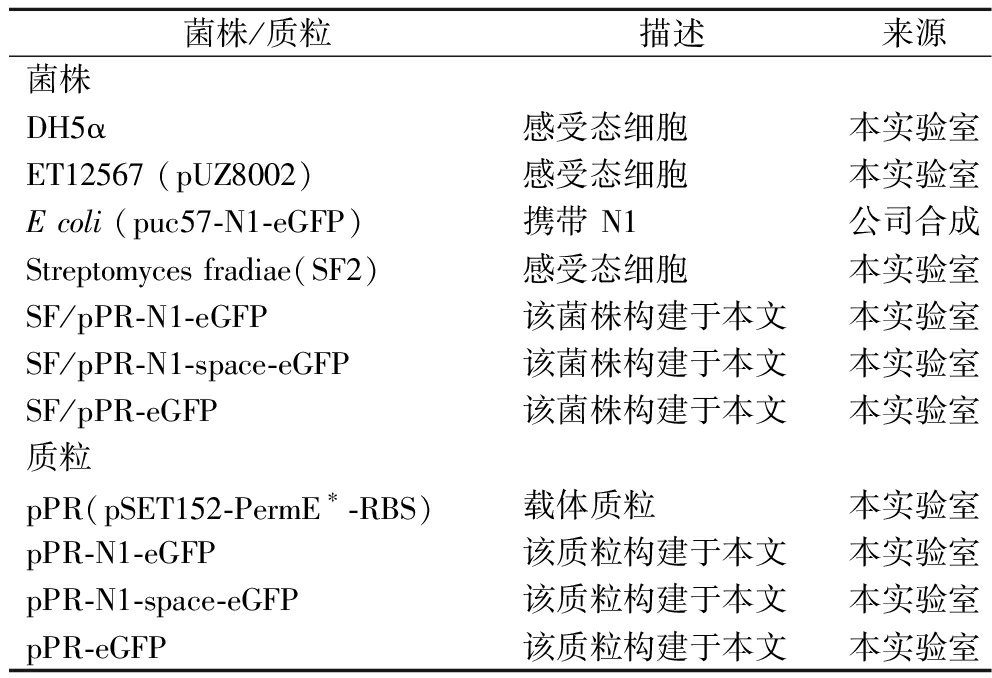
表2 质粒和菌株
Table 2 Strains and plasmids
菌株/质粒描述来源菌株DH5α感受态细胞本实验室ET12567 (pUZ8002)感受态细胞本实验室E coli (puc57-N1-eGFP)携带 N1公司合成Streptomyces fradiae(SF2)感受态细胞本实验室SF/pPR-N1-eGFP该菌株构建于本文本实验室SF/pPR-N1-space-eGFP该菌株构建于本文本实验室SF/pPR-eGFP该菌株构建于本文本实验室质粒pPR(pSET152-PermE∗-RBS)载体质粒本实验室pPR-N1-eGFP该质粒构建于本文本实验室pPR-N1-space-eGFP该质粒构建于本文本实验室pPR-eGFP该质粒构建于本文本实验室
1.2 实验方法
1.2.1 重组新霉素核糖开关质粒的构建
N1基因由金斯瑞生物科技有限公司合成,以puc 57为载体合成基因,利用高保真酶进行PCR扩增并回收得到线性化片段N1-GFP(启动子原件ermE#-1),通过无缝克隆技术与通过EcoR V和BamH I双切酶带有安普抗性的质粒pPR获得重组质粒pPR-N1-GFP。基因N1的聚合酶链式反应扩增得平末端。
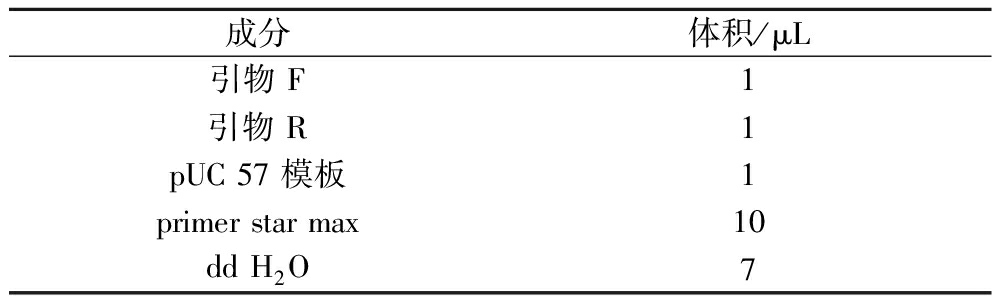
以克隆质粒pUC 57 为模板,在合适的反应体系和条件下(表3)用正反引物 PCR 得到平末端基因N1-eGFP序列。用1.0%的琼脂糖凝胶电泳验证 PCR 扩增产物并回收N1-eGFP基因。
表3 PCR反应体系
Table 3 System of PCR reaction
成分体积/μL引物 F1引物 R1pUC 57 模板1primer star max10dd H2O7
提取质粒pPR并用BamH I和EcoR V酶切后回收得到线性片段。
用含50 μg/mL的安普霉素(apramycin,Apr)培养在含2%琼脂的LB平板上划线获得pset152单菌落,在培养箱中37 ℃培养12~18 h。挑取长势良好的单菌落于LB液体培养基中,200 r/min,37 ℃培养4~8 h,然后提取质粒pPR。在表4的酶切体系下,1%的琼脂糖凝胶电泳验证并回收线性片段。
表4 BamH I和EcoR V酶切反应体系
Table 4 System of digestion of BamH I and EcoR V
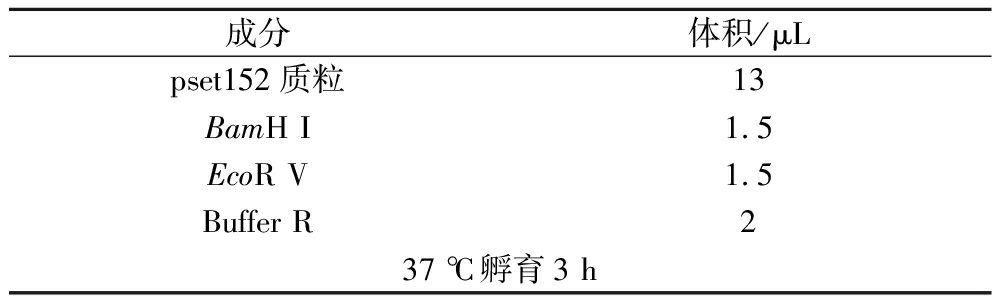
成分体积/μLpset152质粒13BamH I1.5EcoR V1.5Buffer R237 ℃孵育3 h
一步克隆构建重组 ET12567[DH5a(pPR-N1-eGFP)]。
在合适的同源重组体系和反应条件下(表5),将线性载体片段和目的基因N1-eGFP,通过同源重组原理获得表达质粒pPR-N1-eGFP,进而转化到感受态DH5a中;筛选得到重组子后,挑取长势良好的菌落,重新活化后提取表达质粒pPR-N1-eGFP,将质粒转化到感受态ET12567中。
表5 重组大肠杆菌的构建
Table 5 Construction of strain E.coli DH5a(pPR-N1-eGFP)
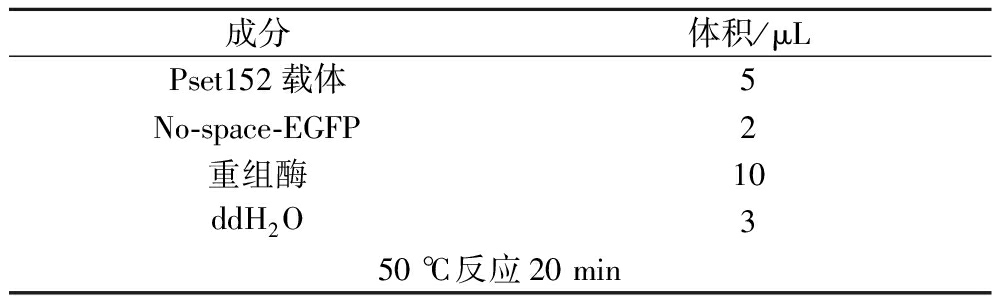
成分体积/μLPset152载体5No-space-EGFP2重组酶10ddH2O350 ℃反应20 min
为了探究RBS和N1核糖开关之间的碱基是否对新霉素与核糖开关亲和性有影响或者对荧光强度起正相关或负相关,所以对比设计增加14 bp的碱基space,以pPR-N1-eGFP为模板,重新设计引物扩增并回收,同样通过无缝克隆技术与通过EcoR V和BamH I双切酶带有安普抗性的质粒pPR获得重组质粒pPR-N1-space-eGFP(启动子原件ermE#),并设计空白对照pPR-eGFP(启动子原件ermE#-2)。将重组基因转至DH5α感受态,然后转化至ET12567感受态中,具体步骤参考ermE#-1,工程菌启动子元件示意如图2所示。
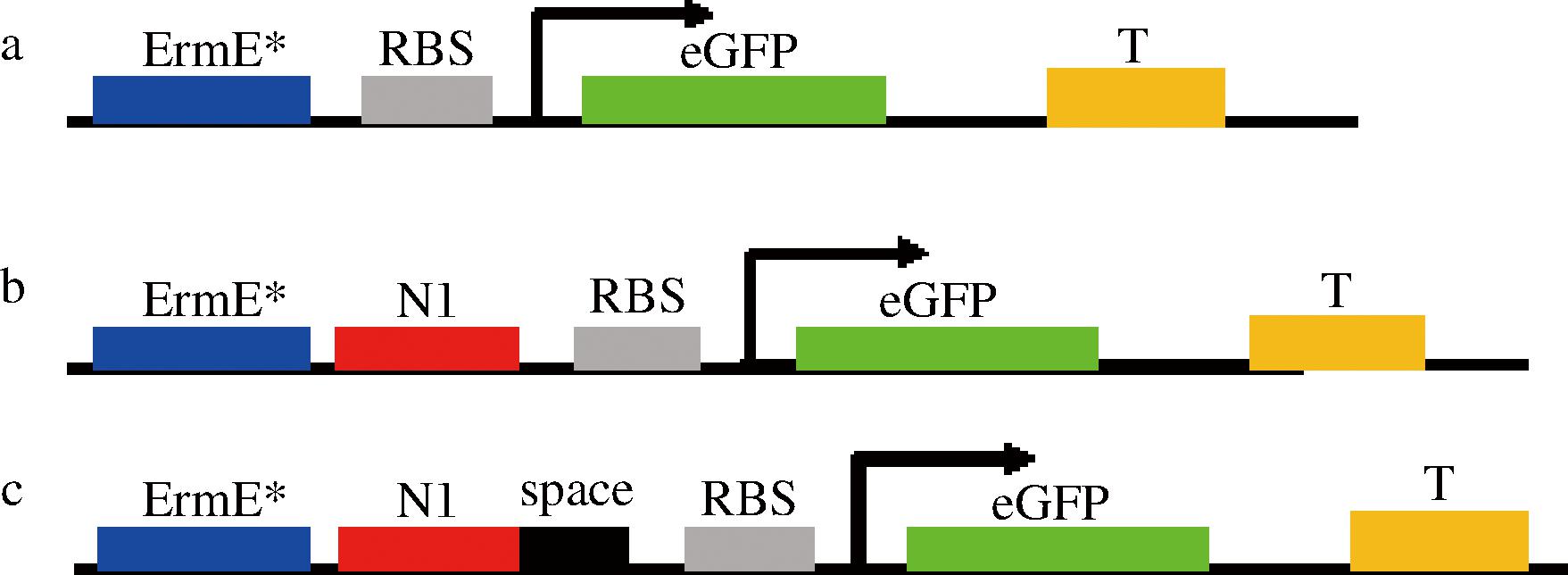
a-启动子原件ermE#-2;b-启动子原件ermE#-1;c-启动子原件ermE#
图2 工程菌株启动子元件示意图
Fig.2 Schematic diagram of the original promoter of the engineered strain
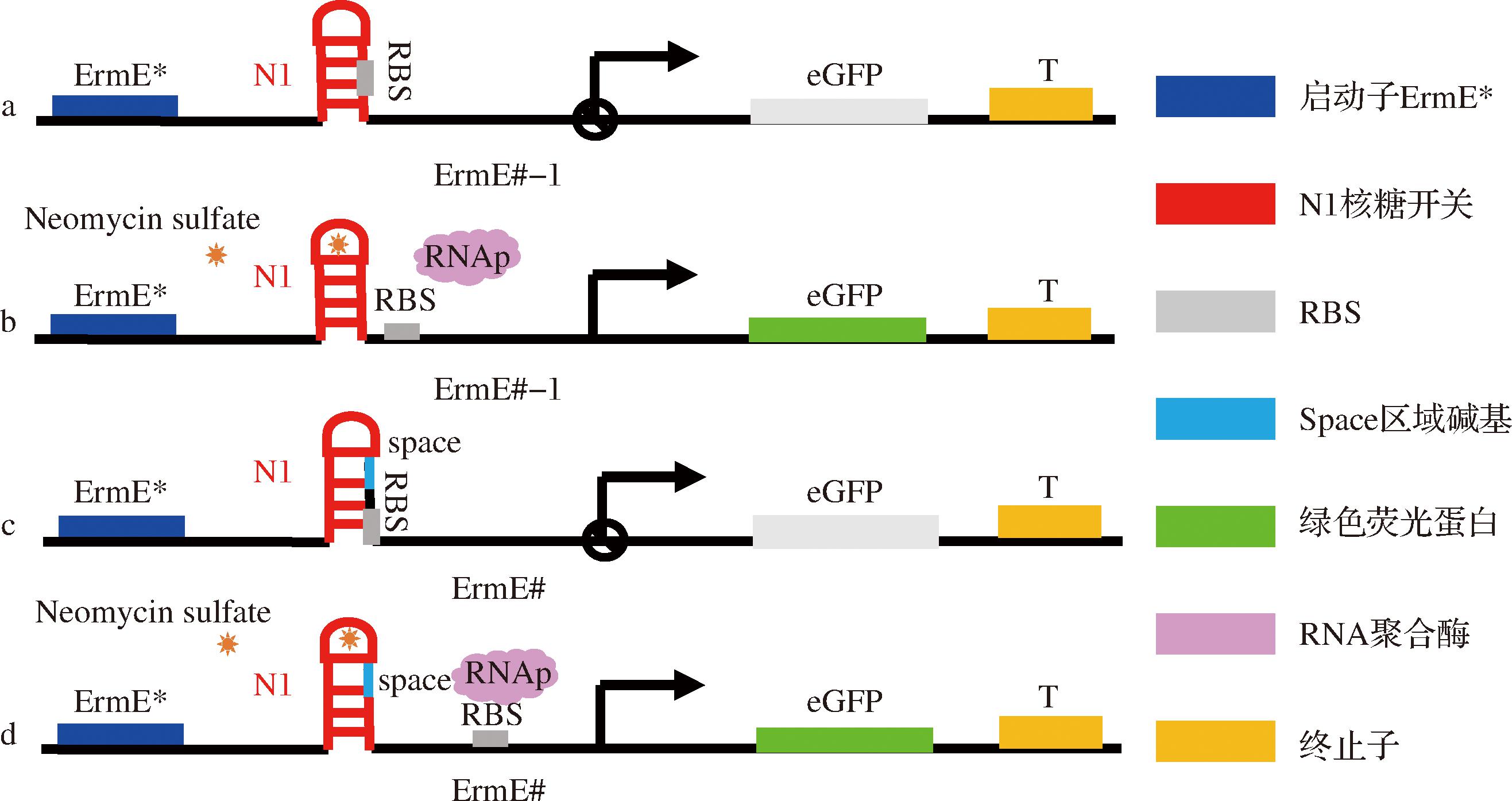
a-启动子元件ermE#-1;b-启动子元件ermE#-1与新霉素配体结合图;c-启动子元件ermE#;d-启动子元件ermE#与新霉素配体结合图
图3 启动子元件ermE#-1、ermE#的设计原理Fig.3 Design principles of promoter components ermE#-1 and ermE#
1.2.2 新霉素核糖开关工程菌株构建
1.2.2.1 供体的制备
含有转移质粒的大肠杆菌供体细胞的培养与转接培养。挑取单个菌落至含有相应抗生素(含50 μg/mL安普霉素、25 μg/mL卡那霉素和25 μg/mL氯霉素)的LB液体培养基中过夜培养(37 ℃、200 r/min)。以1∶100的比例接种至50 mL的含有相同抗生素的LB液体培养基中,摇床6~8 h,离心收集,用等量的LB液体培养基冲洗2~3次(除去抗生素),重悬至LB液体培养基中。
1.2.2.2 受体的制备
受体细胞费氏链霉菌孢子的热激。将MS固体培养基上培养的费氏链霉菌孢子用棉签刮取至3~5 mL YEME种子培养基中,用移液器吹打,并放在振荡器中使孢子散开,用2层纱布过滤,50 ℃热激10 min后摇床放置2~3 h预培养(35 ℃、220 r/min和75%湿度)。
1.2.2.3 接合转移
供体细胞-受体细胞的混合物进行平板涂布与培养。将LB液体培养基的大肠杆菌细胞(稀释至OD值为0.4~0.6)和热激后的孢子进行混合,再在摇床培养0.5 h,并稀释5倍,涂布于含有10 mmol/L MgCl2的MS固体平板上,30 ℃倒置培养18 h,用1 mL含1 mg/mL Apr和0.5 mg/mL甲氧苄啶(trimethoprim,Tmp)的无菌水覆盖平板,吹干后培养7~9 d长出接合子[17]。
1.2.2.4 结合子的PCR验证
刮取少量结合子至1.5 mL离心管,加入100 μL无菌水并放入金属浴煮沸10 min后,12 000 r/min条件下离心5 min。以上清液当模板,使用相应引物进行PCR验证。
1.2.3 新霉素核糖开关工程菌株的表征
1.2.3.1 工程菌株生长特性及荧光强度分析
将4株菌株(SF/pPR-N1-eGFP、SF/pPR-N1-space-eGFP、SF/pPR-eGFP、SF-2)于无菌条件下挑取成熟菌丝体接种于种子培养基,置于恒温恒湿摇床培养(35 ℃、220 r/min和75%湿度),每隔10 h取样2 mL测定OD值后12 000 r/min离心10 min,弃上清液,将沉淀置于80 ℃的烘箱中过夜烘干,检测其干重。经40 h培养后SF/pPR-N1-space-eGFP处于对数中期,其余菌株呈相对滞后的增殖动力学特征),进行菌丝体收集、缓冲液洗涤及重悬处理。激光共聚焦显微镜(10×物镜,Ex:488 nm/Em:510 nm)成像参数标准化:激光功率13%,电压为710 V。
1.2.3.2 工程菌株的摇瓶发酵验证
将费氏霉菌工程菌株单菌落接种于YEME种子培养基中进行40 h预培养。随后将菌液转移至发酵培养基,在恒定温湿度参数控制下维持7 d发酵周期。发酵终止后,取1 mL样本经8 000 r/min处理8 min,所得上清液按1∶50体积比用无菌水稀释后进行HPLC分析。摇瓶发酵体系参数设置为:250 mL锥形瓶装载30 mL培养基,1%接种量,控制摇床运行参数恒定[21]。
1.2.3.3 内外源新霉素对SF/pPR-N1-space-eGFP菌株荧光强度的影响
从固体平板上挑取SF/pPR-N1-space-eGFP菌株单菌落孢子接种于YEME种子培养基内,依据其生长曲线的趋势取2 mL样液直接破碎后每隔10 h用荧光分光光度计测量1次荧光值。超声波细胞破碎仪的功率270 W,报警温度50 ℃,工作总时间10 min。
将SF/pPR-N1-space-eGFP接种于YEME种子培养基内,取对数生长期的种子液(摇床培养40 h),于50 mL离心管内,4 ℃离心收集菌体,用YEME种子培养基清洗3次后,稀释,测定OD600值,使其范围在0.4~0.8。配制0、5、10、25、50、100、200、300、400 mmol/L梯度浓度的新霉素溶液。取2 mL菌液于10 mL离心管内,设置3组平行,并分别添加2 μL不同梯度浓度的抗生素,放置摇床培养24 h。一轮培养后得出的大致最适浓度范围再进一步缩小浓度范围,使用0、2、4、8、16、32、64、100 mmol/L再次测量。
将SF/pPR-N1-space-eGFP接种于YEME种子培养基内,摇床培养40 h,清洗3次后,稀释,测定OD600值,使其范围在0.4~0.8,加入64 mmol/L的新霉素,每隔2 h取菌液破碎,监测24 h内的荧光变化。
1.2.3.4 SF/pPR-N1-space-eGFP菌株摇瓶发酵过程中荧光强度及效价分析
从平板上分别挑取单菌落于YEME种子培养基培养48 h,以1%的接种量加入含有30 mL发酵培养基的250 mL锥形瓶中,在恒温恒湿摇床中发酵7 d,用于测量每日效价的摇瓶安置于不同摇床,设置平行实验,保证每瓶发酵液只取1次,不会因连续取样使发酵液减少致效价产生影响。每次取2 mL,离心后取上清液为胞外分泌,测试其荧光值及效价;取沉淀后清洗3次,使用超声波细胞破碎仪破碎后为胞内分泌,测试其荧光值及效价。发酵结束后进行HPLC检测。采用柱前衍生化HPLC法测定新霉素效价,方法参考文献[22]。
1.2.3.5 基于核糖开关生物传感器优化平板孢子生成条件
除发酵培养基组分外,固体培养基组分对费氏链霉菌菌株效价也有着同样重要的影响,本次实验以固体培养基中琼脂浓度,链霉素的抗性浓度和pH值设计三因素五水平的正交实验优化SF/pPR-N1-space-eGFP的效价。
在数学学科的相关理论中,正交法主要是在数理统计、概率论和线性代数为基础的前提下,选用标准的正交化作为试验设计原理而进行相关的设计试验,选取对新霉素B的效价具有影响的3个因素琼脂浓度,链霉素浓度和pH。每个因素确定5个水平,利用L25(56)正交试验,以新霉素B的效价、胞内荧光值为考察指标,确定最佳工艺,正交试验因素与水平设计见表6。
表6 正交试验因素与水平设计
Table 6 Orthogonal test factors and horizontal design

因素水平12345A 琼脂浓度/(g/L)1.21.51.82.12.4B 链霉素浓度/(g/L)0581015C pH值7.37.47.57.67.7
2 结果与分析
2.1 新霉素核糖开关工程菌株的构建
2.1.1 重组质粒的构建
为了进一步验证基因线路构建结合新霉素的费氏链霉菌核糖开关工程菌株,本文通过在底盘费氏链霉菌SF-2中得到的3株重组菌株,并结合绿色荧光蛋白对工程菌株比较表征和摇瓶发酵研究其对于新霉素产量的影响。首先设计对应其相应片段的扩增引物,利用高保真酶2×PrimeSTAR Max DNA Polymerase获得所需核糖开关的目标DNA片段。而后使用DNA 胶回收试剂盒回收得到纯化的基因片段,-20 ℃保存备用。
首先根据1.2.1节所述方法,分别构建重组质粒 pPR-N1-eGFP、pPR-N1-space-eGFP和pPR-eGFP,并通过化学转化至接合转移供体菌株E.coli ET12567中。在初始构建的菌株中,由于未引入14 bp非编码间隔序列,核糖开关N1的茎环结构与RBS区域空间距离过近。当新霉素B诱导发夹结构展开时,RNA聚合酶的庞大体积与残留茎环结构产生空间位阻,导致RBS结合位点被部分遮蔽,造成核糖体识别效率下降,降低基因线路的灵敏度与特异性。通过引入特定设计的间隔序列延长核糖开关N1下游结构域,使RBS位点完全暴露于转录复合物作用范围,该优化策略成功提升了核糖体结合效率,使生物传感器的信号响应幅度实现显著增强。核糖开关启动子元件如图3所示。将转化后的菌落接入含安普霉素抗性的LB液体培养基过夜培养然后提取质粒测序,测序结果与实验预测结果对比二者完全一致,表明3个重组质粒构建成功。
2.1.2 新霉素核糖开关工程菌株构建及验证
将含有核糖开关和对照组的重组质粒的供体菌株大肠杆菌ET12567(pUZ8002)与受体菌株弗氏链霉菌SF-2进行接合转移,并涂布于安普霉素和甲氧苄啶抗性平板上进行筛选得到接合子。将接合子按照1.2.2.3节方法处理,经验证结果与预想一致,如图4所示。表明重组质粒均已成功导入费氏链霉菌SF-2中。
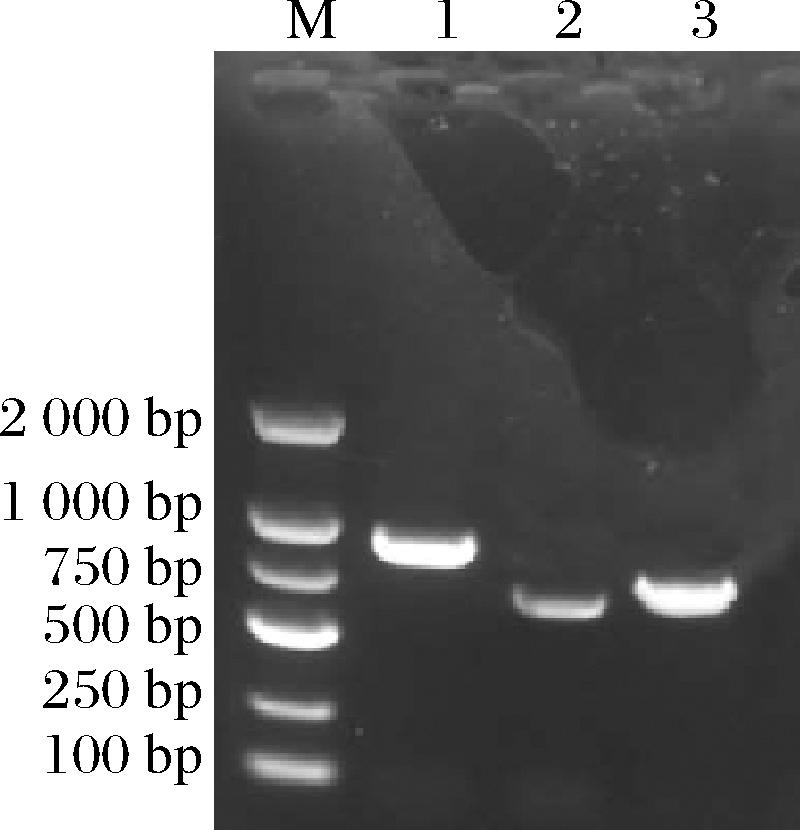
1-SF/pPR-N1-space-eGFP;2-SF/pPR-eGFP;3-SF/pPR-N1-eGFP。
图4 接合子PCR阳性克隆验证Fig.4 Verification of PCR positive clones of zygotes
2.2 新霉素核糖开关工程菌株的表征
2.2.1 工程菌株生长特性及荧光强度分析
采用YEME液体培养基,通过生物量干重与光密度(OD600)双变量联用策略,对重组费氏链霉菌工程菌株及野生型菌株(SF-2)进行生长表型表征。如图5所示,各菌株生长曲线呈现显著分化特征。其中,SF/pPR-eGFP与SF-2呈现相似的生长动力学特征,其典型四阶段表现为:0~24 h为延滞期,24~64 h进入对数生长期,64~72 h过渡至稳定期,72 h后进入衰亡期。
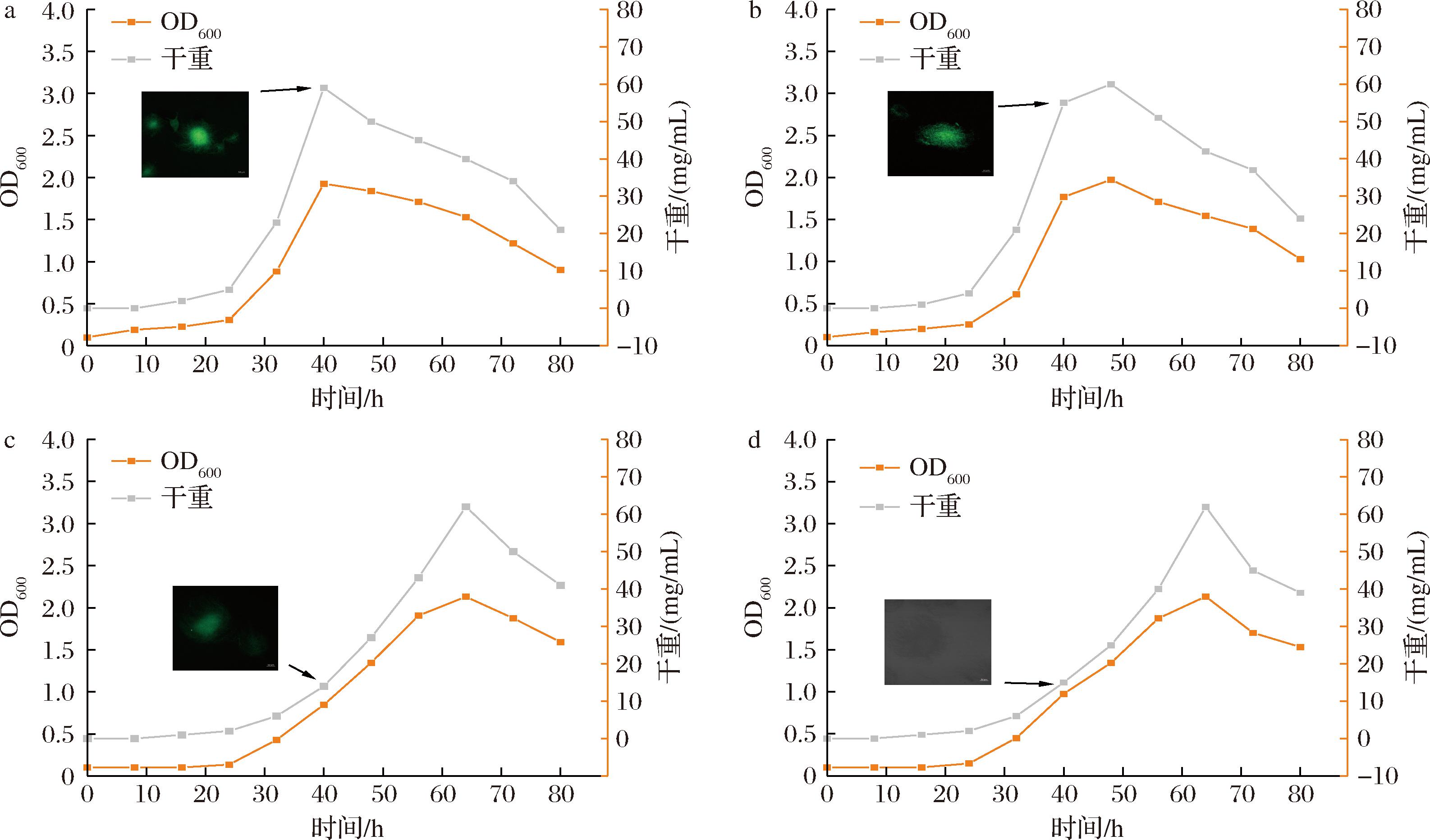
a-SF/pPR-N1-space-eGFP;b-SF/pPR-N1-eGFP;c-SF/pPR-eGFP;d-SF-2
图5 工程菌与原始菌生长曲线图与40 h时的荧光图Fig.5 Growth curves of engineering bacteria and primitive bacteria and fluorescence patterns at 40 h
相较于野生型,携带新霉素核糖开关调控元件的工程菌株SF/pPR-N1-space-eGFP与SF/pPR-N1-eGFP表现出显著提升的生物合成活性:1)延滞期缩短至18 h;2)对数生长期比生长速率提升;3)提前12 h进入稳定期。且工程菌株的DCWmax值较野生型有所降低,该现象与对数生长期时间压缩导致的生物量积累效率下降相关,同时印证了5′-UTR调控元件(space区域)对菌株代谢负荷的优化作用。根据次级代谢产物合成理论,工程菌株提前进入稳定期与新霉素B的生物合成窗口期前移具有正向关联性。
如图5所示,SF/pPR-N1-space-eGFP呈现显著增强的荧光信号强度,较SF/pPR-N1-eGFP提升明显,而SF/pPR-eGFP荧光较弱及SF-2均未检测到特异性荧光。该数据证实,space区域的碱基序列优化可显著增强核糖开关适配体结构域与新霉素配体的结合亲和力,进而提高转录调控效率。工程菌株在种子阶段即表现出新霉素B前体的微量合成,其配体依赖性荧光激活机制为后续高通量筛选提供了理论依据。
2.2.2 工程菌株的摇瓶发酵验证
通过将上述获得的3株工程菌株进行摇瓶发酵并测定新霉素的产量发现,相对于出发菌株SF-2,3株工程菌经摇瓶发酵7 d之后,测定的新霉素产量达到了7 943、6 849、7 029 U/mL,相对于SF-2分别提高了20%、3.5%和6.3%。如图6所示,相对于SF/pPR-N1-space-eGFP,SF/pPR-N1-eGFP、SF/pPR-eGFP对于新霉素B发酵效价没有明显提升。这部分结果说明,核糖开关N1对费氏链霉菌新霉素的发酵调控可能发挥着重要的作用,且通过2组实验证明,带有启动子元件ermE#的工程菌SF/pPR-N1-space-eGFP与新霉素B的响应灵敏度和特异性更强,符合设计实验的初衷。
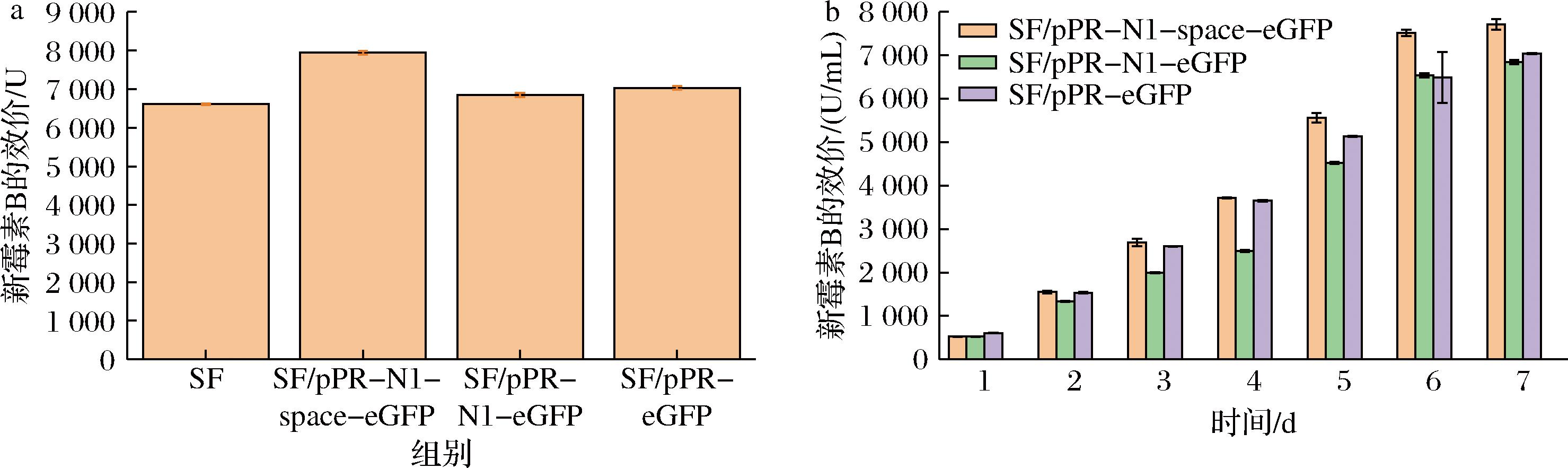
a-SF-2 中分别表达的工程菌效价;b-工程菌株发酵曲线
图6 原始菌SF-2及其表达工程菌发酵新霉素B效价
Fig.6 Comparative analysis of neomycin B production titers in wild-type Streptomyces SF-2 and its genetically engineered expression strain
2.2.3 内外源新霉素对SF/pPR-N1-space-eGFP菌株荧光强度的影响
如图7-a所示,工程菌株SF/pPR-N1-space-eGFP内源性合成的新霉素B可特异性激活核糖开关调控元件,通过配体-适配体结构域结合触发eGFP报告基因表达,其荧光动力学曲线显示,经超声波破碎处理的种子液胞内荧光强度随培养时间呈非线性增长模式。值得注意的是,在培养后期观察到荧光增幅速率显著下降,此现象可能与高密度发酵体系中出现的生物承载极限相关:1)三维培养空间限制导致细胞接触抑制效应;2)碳氮源营养底物呈现限制性消耗;3)细胞死亡率超过增殖速率。上述代谢应激状态与HPLC检测的日际效价动态共同验证了本研究的理论预测模型。
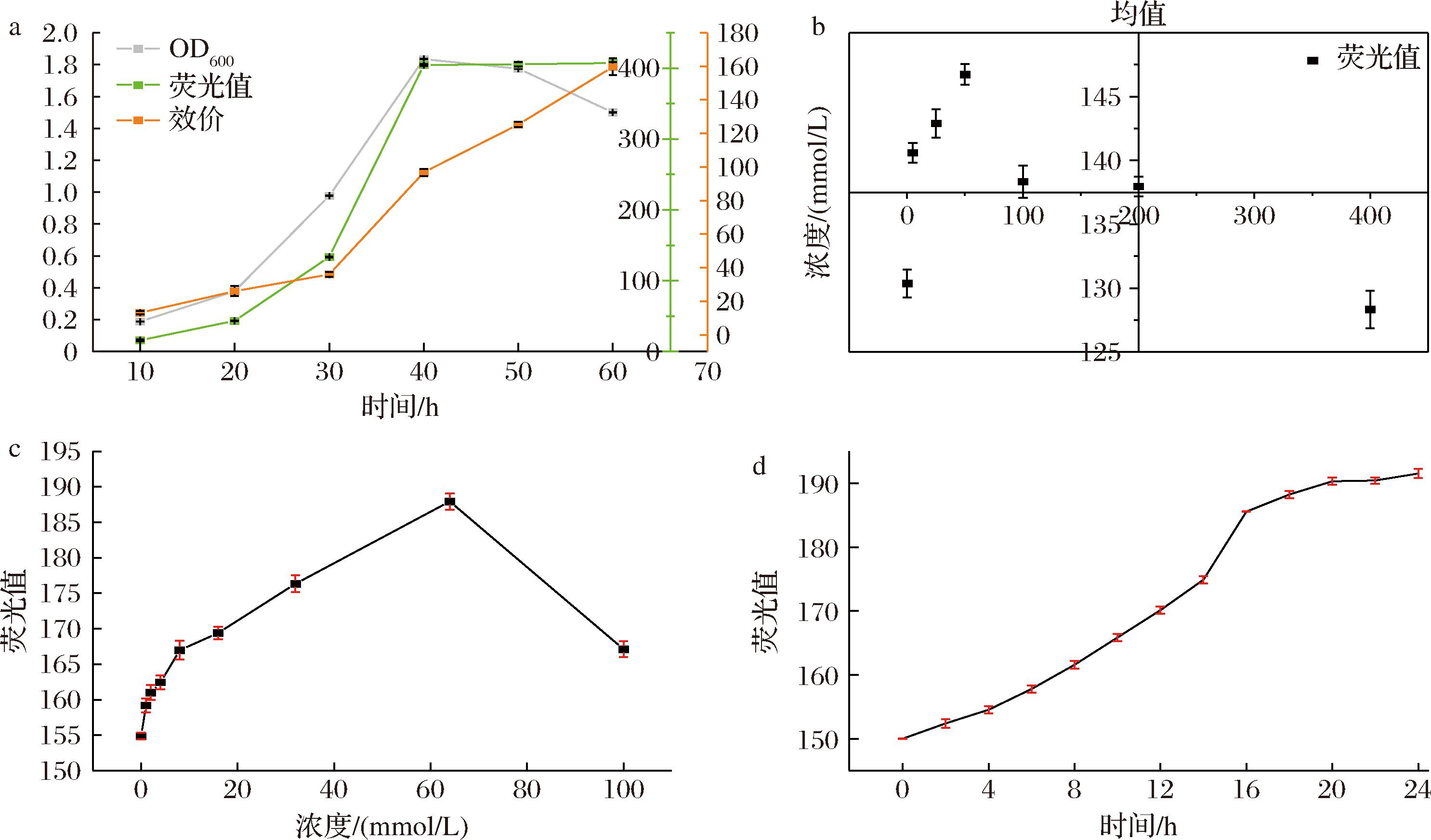
a-0~50 h内源新霉素产生响应核糖开关的荧光值、OD600值与效价;b-外源新霉素0~400 mmol/L添加荧光值变化图;c-外源新霉素0~100 mmol/L添加荧光值变化图;d-0~24 h内64 mmol/L外源新霉素添加胞内外荧光值变化图
图7 内外源新霉素对SF/pPR-N1-space-eGFP菌株荧光强度的影响
Fig.7 Fluorescence response of S.SF/pPR-N1-eGFP to endo-/exogenous neomycin for conciseness
在外源新霉素诱导优化实验中,采用宽域浓度梯度(0~400 mmol/L)进行初步剂量效应分析(图7-b),发现荧光响应值在50~100 mmol/L区间呈现显著剂量依赖性增强。基于此,进一步通过等比级数梯度稀释法建立精细浓度矩阵(图7-c),确定核糖开关系统的最适诱导浓度为64 mmol/L。于最适诱导浓度64 mmol/L下的工程菌株在24 h内的胞内外荧光值变化(图7-d),如图所示荧光值激增的时间在14~16 h,该优化参数为后续发酵过程的诱导策略提供了参考依据。
2.2.4 SF/pPR-N1-space-eGFP菌株摇瓶发酵过程中荧光强度及效价分析
经优化后的实验方法描述如下:每日采集发酵液样本进行离心分离(10 000 r/min,15 min,4 ℃),收集上清液作为胞外代谢产物样本,分别用于胞外生物效价测定及菌体自溶释放的绿色荧光蛋白定量分析。对离心沉淀物用缓冲液洗涤3次后重悬至初始体积,经超声波细胞破碎仪处理以裂解菌体,随后离心获得胞内可溶性组分,该组分主要包含胞内积累的eGFP表达产物及微量未完成跨膜转运的新霉素B。
如图8所示,胞内荧光强度随发酵时间延长呈现显著累积效应,而胞外荧光信号自第3发酵日起出现统计学显著下降。经初步验证,该现象可能与发酵液中色素类次级代谢产物积累导致的吸光度干扰相关,其具体作用机制尚需通过代谢组学分析进一步阐明。此结果与前期摇瓶发酵实验数据具有显著相关性,验证了本研究所构建的核糖开关调控型生物传感器系统的有效性。实验数据证实,该传感器可通过eGFP荧光信号强度与新霉素B产量之间的线性关系,实现发酵周期内新霉素B高产菌株的高通量筛选,满足工业菌种选育的定量需求。
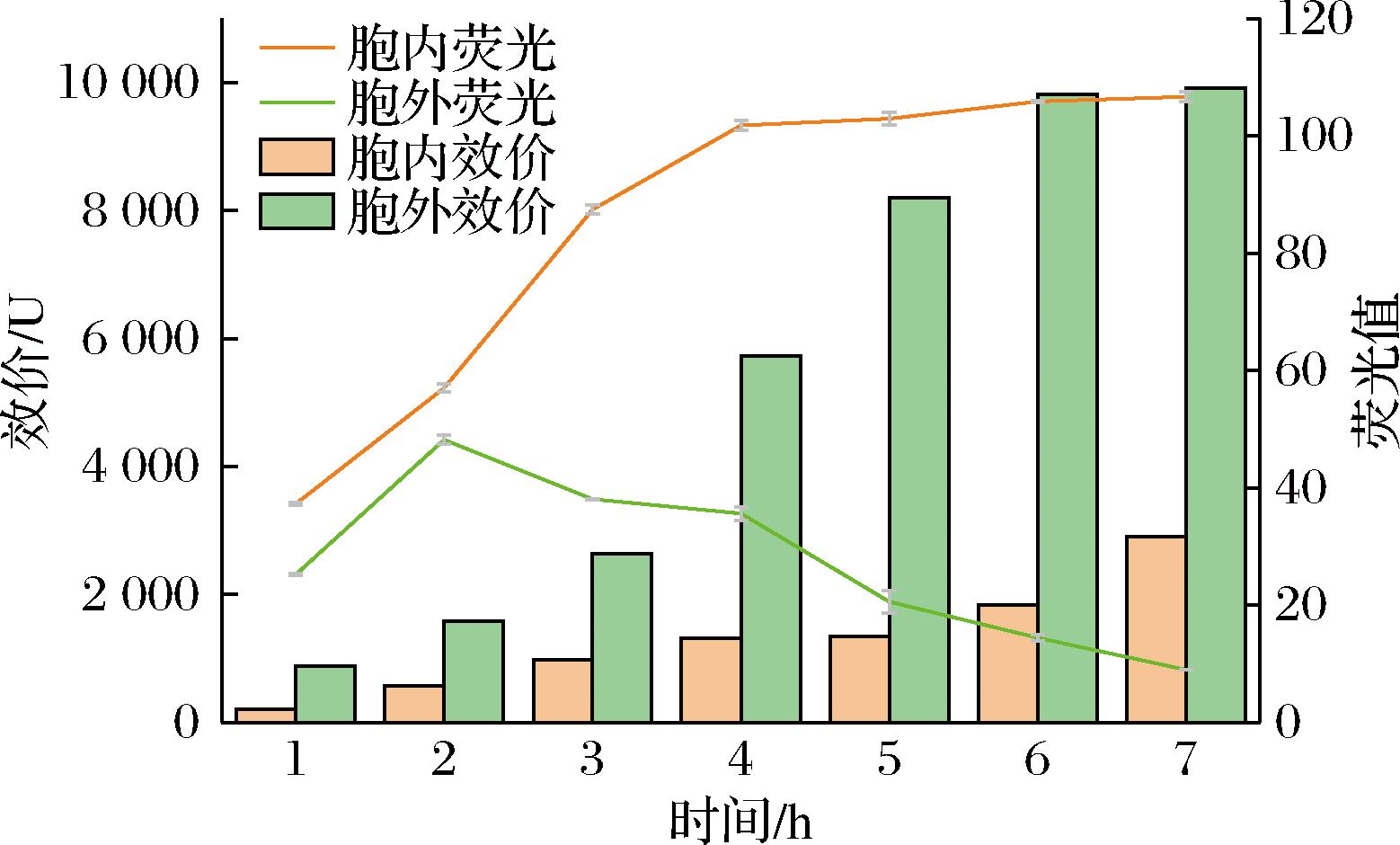
图8 SF/pPR-N1-space-eGFP发酵过程中每天胞内胞外的荧光值和效价图
Fig.8 Daily intracellular and extracellular fluorescence values and titer profiles during the fermentation process of SF/pPR-N1-space-eGFP
2.2.5 SF/pPR-N1-space-eGFP菌株摇瓶发酵过程中荧光强度及效价分析
选取对新霉素B的效价具有影响的3个因素琼脂浓度、链霉素浓度和pH。其中通过链霉素压力筛选获得高抗性工业菌株(如提高发酵过程稳定性);琼脂基质微结构通过三维孔隙协同调控渗透压梯度与氧传递,定向优化菌丝分化;pH的动态平衡则通过调控跨膜电势差与酶活力稳态,直接影响前体物质摄取及产物的胞外分泌。以新霉素B的效价和胞内荧光值为考察指标,确定最佳工艺,结果如表7所示。
表7 正交试验方案及结果
Table 7 Orthogonal test scheme and results
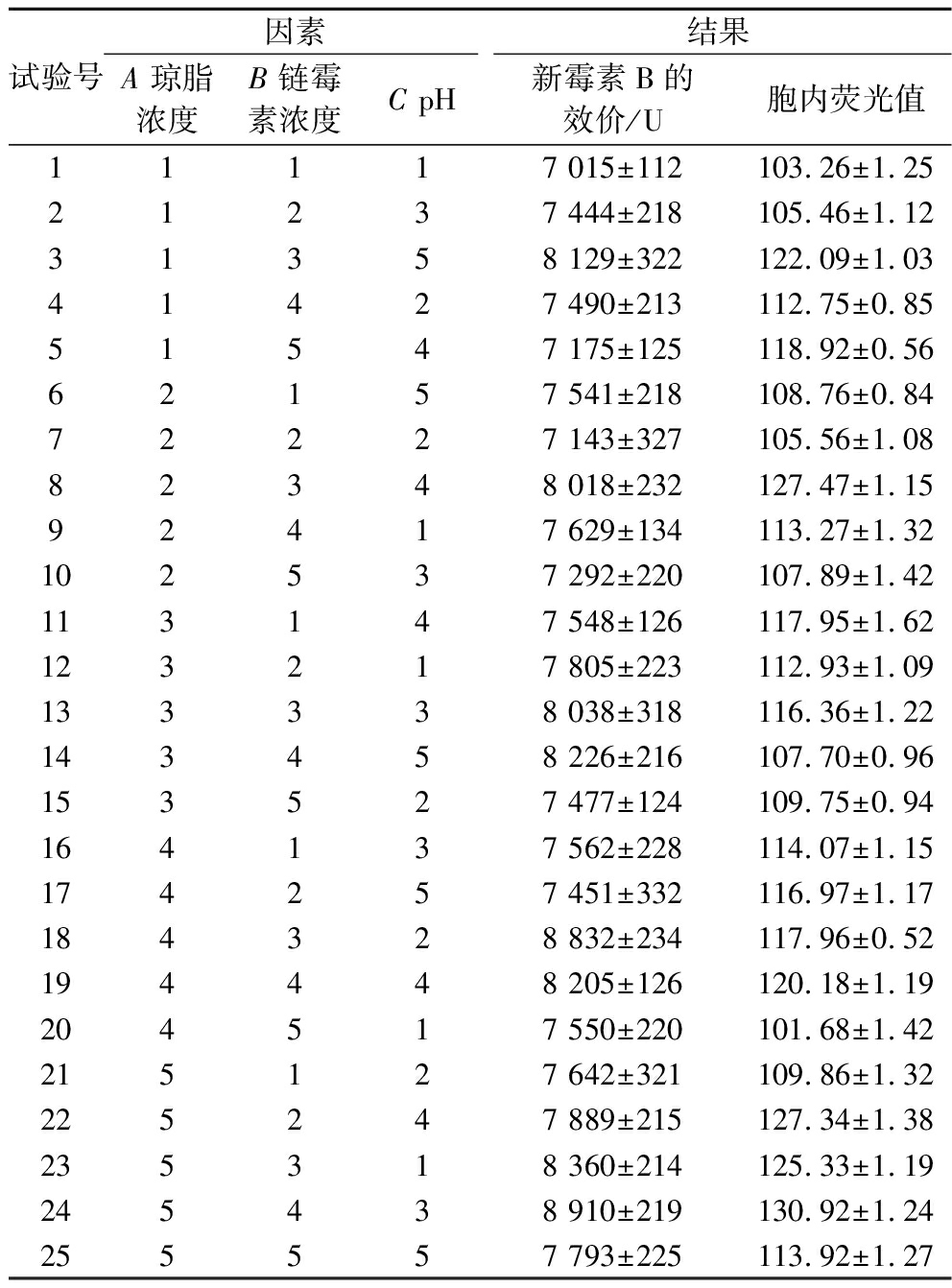
试验号因素结果A 琼脂浓度B 链霉素浓度C pH 新霉素B的效价/U胞内荧光值11117 015±112103.26±1.2521237 444±218105.46±1.1231358 129±322122.09±1.0341427 490±213112.75±0.8551547 175±125118.92±0.5662157 541±218108.76±0.8472227 143±327105.56±1.0882348 018±232127.47±1.1592417 629±134113.27±1.32102537 292±220107.89±1.42113147 548±126117.95±1.62123217 805±223112.93±1.09133338 038±318116.36±1.22143458 226±216107.70±0.96153527 477±124109.75±0.94164137 562±228114.07±1.15174257 451±332116.97±1.17184328 832±234117.96±0.52194448 205±126120.18±1.19204517 550±220101.68±1.42215127 642±321109.86±1.32225247 889±215127.34±1.38235318 360±214125.33±1.19245438 910±219130.92±1.24255557 793±225113.92±1.27
由表8中新霉素B的效价极差(r值)分析可知,3个因素对新霉素B的效价的影响程度依次为B>A>C,即链霉素浓度>琼脂浓度>pH, 从k1、k2、k3、k4、k5的大小分析得出,感官评分的最优条件为A5B4C3。
表8 各因素对新霉素B的效价的极差分析
Table 8 Analysis of the extreme difference of each factor on the calibration price of neomycin B
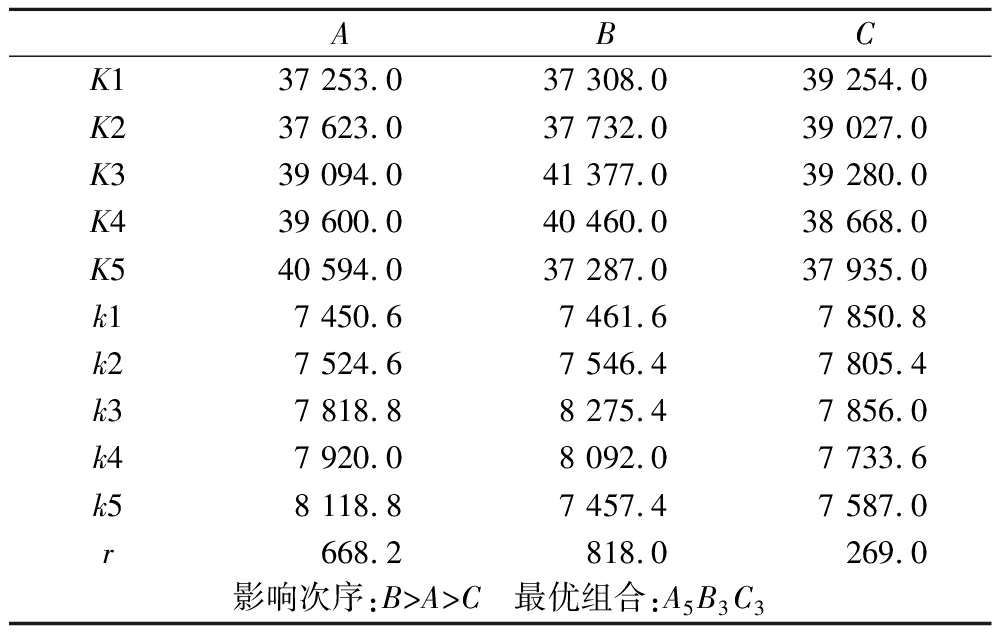
ABCK137 253.0 37 308.0 39 254.0 K237 623.0 37 732.0 39 027.0 K339 094.0 41 377.0 39 280.0 K439 600.0 40 460.0 38 668.0 K540 594.0 37 287.0 37 935.0 k17 450.6 7 461.6 7 850.8 k27 524.6 7 546.4 7 805.4 k37 818.8 8 275.4 7 856.0 k47 920.0 8 092.0 7 733.6 k58 118.8 7 457.4 7 587.0 r668.2 818.0 269.0 影响次序:B>A>C 最优组合:A5B3C3
由表9中极差(r值)分析可知,3个因素对胞内荧光值的影响程度依次为B>C>A,即链霉素浓度>pH>琼脂浓度,以胞内荧光值最大值为优化目标,从k1、k2、k3、k4、k5的大小分析得出,胞内荧光值的最优条件为A5B3C4。
表9 各因素对胞内荧光值的极差分析
Table 9 Range analysis of intracellular fluorescence value by various factors
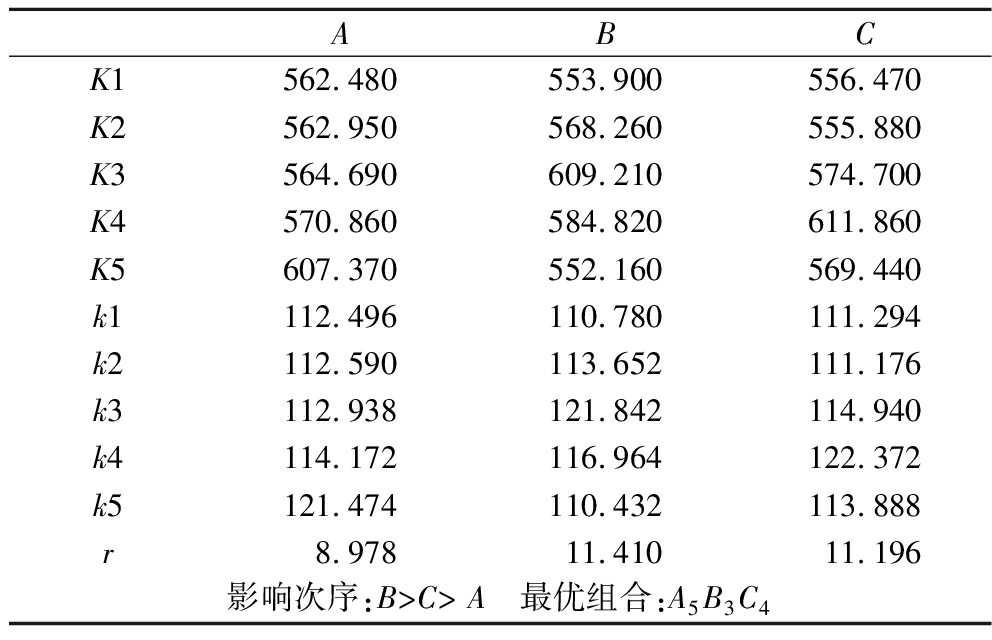
ABCK1562.480 553.900 556.470 K2562.950 568.260 555.880 K3564.690 609.210 574.700 K4570.860 584.820 611.860 K5607.370 552.160 569.440 k1112.496 110.780 111.294 k2112.590 113.652 111.176 k3112.938 121.842 114.940 k4114.172 116.964 122.372 k5121.474 110.432 113.888 r8.978 11.410 11.196 影响次序:B>C> A 最优组合:A5B3C4
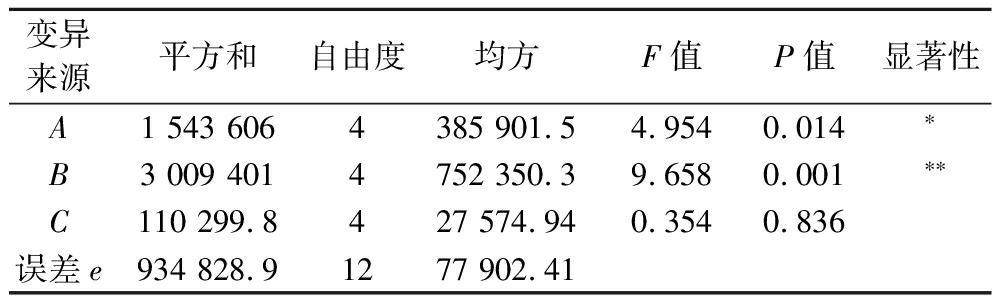
由表10可知,通过计算各因素以及误差的离差平方和,然后求出自由度、均方、F值,并进行F检验。新霉素B的效价方差分析结果如表10所示,从表10的方差分析结果表中,可以看出,链霉素浓度对新霉素B的效价影响极显著(P<0.01),琼脂浓度对新霉素B的效价影响显著(P<0.05),pH对新霉素B的效价影响不显著(P>0.05)。通过分析3个因素的F值可知,3个因素的影响次序为链霉素浓度>琼脂浓度>pH,综合考虑3个因素对新霉素B的效价的影响,得到最优组合为A5B3C3,即当琼脂浓度为2.4 g/L,链霉素浓度为8 g/L,pH值为7.5时新霉素B的效价最大。
表10 各因素对新霉素B的效价的方差分析结果
Table 10 ANOVA results of each factor on the calibration price of neomycin B
变异来源平方和自由度均方F值P值显著性A1 543 6064385 901.54.9540.014∗B3 009 4014752 350.39.6580.001∗∗C110 299.8427 574.940.3540.836误差e934 828.91277 902.41
注:**,具有极显著影响(P<0.01),*,具有显著影响(P<0.05)(下同)。
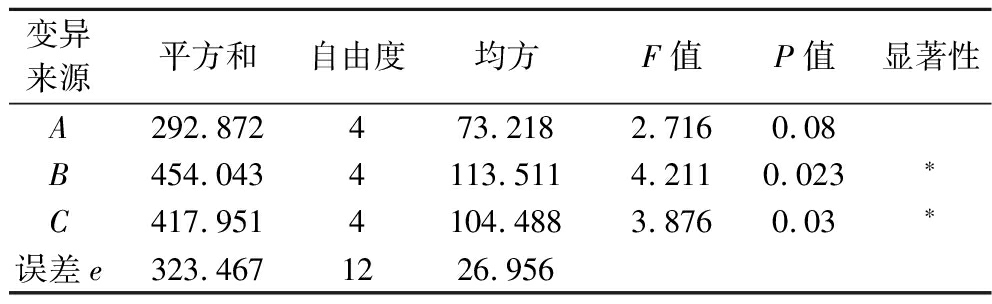
对胞内荧光值进行方差分析,方差分析结果如表11所示,链霉素浓度、pH对胞内荧光值具有显著影响(P<0.05),琼脂浓度对胞内荧光值的影响不显著(P>0.05),通过分析3个因素的F值可知,3个因素的影响次序为链霉素浓度>pH>琼脂浓度,综合考虑3个因素对胞内荧光值的影响,得到最优组合为A5B3C4,即当琼脂浓度为2.4 g/L,链霉素浓度为8 g/L,pH值为7.6时胞内荧光值最大。
表11 各因素对胞内荧光值的方差分析结果
Table 11 ANOVA results of each factor on intracellular fluorescence value
变异来源平方和自由度均方F值P值显著性A292.872473.2182.7160.08B454.0434113.5114.2110.023∗C417.9514104.4883.8760.03∗误差e323.4671226.956
综合考虑3个因素对新霉素B的效价、胞内荧光值的影响,得到最优组合为A5B3C4,即当琼脂浓度为2.4 g/L,链霉素浓度为8 g/L,pH值为7.6时胞内荧光值最大。
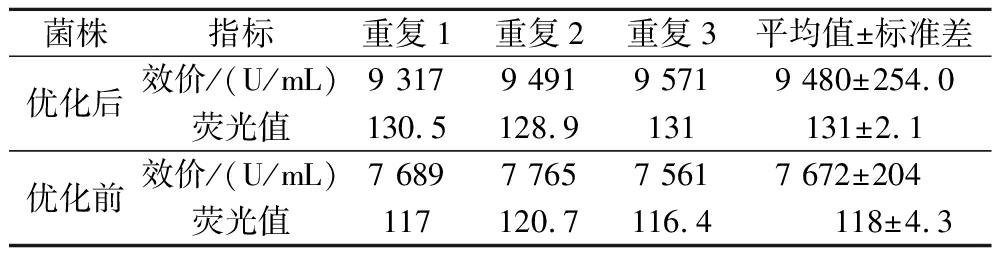
在此最优条件下,对SF/pPR-N1-space-eGFP菌株做3组平行摇瓶发酵验证,如表12所示,得到平均效价为9 480 U/mL,其均值范围约为254 U/mL,比出发菌株SF提高了43%,较优化前的SF/pPR-N1-space-eGFP菌株提高了23%;平均荧光值为131,较优化前的SF/pPR-N1-space-eGFP菌株提高了11%。
表12 培养基优化前后SF/pPR-N1-space-eGFP菌株效价与荧光值的差异比较
Table 12 Comparative analysis of the efficacy and fluorescence values of SF/pPR-N1-space-eGFP strains before and after medium optimization
菌株指标重复1重复2重复3平均值±标准差优化后效价/(U/mL)9 3179 4919 5719 480±254.0荧光值130.5128.9131131±2.1优化前效价/(U/mL)7 6897 7657 5617 672±204 荧光值117120.7116.4118±4.3
3 结论与讨论
本文首次基于在费氏链霉菌核糖开关动态构象与基因线路空间适配原理,设计出高灵敏度新霉素B生物传感器,突破传统传感元件响应效率瓶颈,创新性引入space序列优化调控元件空间排布,显著提升RBS与RNAp结合效率与信号信噪比,为复杂代谢产物的实时监测提供新型工具。得到了合成新霉素能力更强的菌株SF/pPR-N1-eGFP也探索了在不同培养条件下的表征情况;得到了当琼脂浓度为2.4 g/L,链霉素浓度为8 g/L,pH 7.6时新霉素B的效价和胞内荧光值最大,并在最优条件下,通过平行实验后得到平均效价为9 480 U/mL。较出发菌株SF在原始培养基条件下发酵的新霉素效价6 612 U/mL提高了43%。本研究通过跨学科技术融合与系统性工程优化,为不同场景下高产新霉素费氏链霉菌株的高通量筛选提供了新思路和新方法,也为链霉菌属其他次级代谢产物的高效筛选提供参考。
[1] HOMA S T.Neomycin, an inhibitor of phosphoinositide hydrolysis, inhibits the resumption of bovine oocyte spontaneous meiotic maturation[J].The Journal of Experimental Zoology, 1991, 258(1):95-103.
[2] VADASSERY J, REICHELT M, JIMENEZ-ALEMAN G H, et al.Neomycin inhibition of (+)-7-Iso-jasmonoyl-L-isoleucine accumulation and signaling[J].Journal of Chemical Ecology, 2014, 40(7):676-686.
[3] WU Y H, JIN H, YU Q, et al.Optimizing genome editing efficiency in Streptomyces fradiae via a CRISPR/Cas9n-mediated editing system[J].Applied and Environmental Microbiology, 2025, 91(2):e01953-24.
[4] 孙俊峰, 王珊, 刘鹏飞, 等.费氏链霉菌遗传操作体系的优化与应用[J].中国抗生素杂志, 2021, 46(2):128-133.
SUN J F, WANG S, LIU P F, et al.Optimization and application of genetic manipulation system of Streptomyces fradiae[J].Chinese Journal of Antibiotics, 2021, 46(2):128-133.
[5] MANOHAR S M, SHAH P, NAIR A.Flow cytometry:Principles, applications and recent advances[J].Bioanalysis, 2021, 13(3):181-198.
[6] MANHAS K R, BLATTMAN J N.Flow cytometry analysis of immune cell responses[J].Methods in Molecular Biology, 2023, 2597:105-120.
[7] SHAO C M, CHI J J, SHANG L R, et al.Droplet microfluidics-based biomedical microcarriers[J].Acta Biomaterialia, 2022, 138:21-33.
[8] 程一晗, 李翔飞, 韩如梦, 等.转录因子NeyR调控弗氏链霉菌新霉素的生物合成[J].食品与发酵工业, 2024, 50(24):84-90.
CHENG Y H, LI X F, HAN R M, et al.Transcription factor NeyR enhances neomycin synthesis in Streptomyces fradiae[J].Food and Fermentation Industries, 2024, 50(24):84-90.
[9] WANG X C, WILSON S C, HAMMOND M C.Next-generation RNA-based fluorescent biosensors enable anaerobic detection of cyclic di-GMP[J].Nucleic Acids Research, 2016, 44(17):e139.
[10] 韩祥东, 刘薇, 吴存祥, 等.核糖开关与基因表达调控[J].中国生物化学与分子生物学报, 2011, 27(12):1094-1100.
HAN X D, LIU W, WU C X, et al.Riboswitch in gene expression regulation[J].Chinese Journal of Biochemistry and Molecular Biology, 2011, 27(12):1094-1100.
[11] BARRICK J E, BREAKER R R.The distributions, mechanisms, and structures of metabolite-binding riboswitches[J].Genome Biology, 2007, 8(11):R239.
[12] BREAKER R R.Complex riboswitches[J].Science, 2008, 319(5871):1795-1797.
[13] TOPP S, GALLIVAN J P.Emerging applications of riboswitches in chemical biology[J].ACS Chemical Biology, 2010, 5(1):139-148.
[14] GONG S, DU C Y, WANG Y L.Regulation of the thiamine pyrophosphate (TPP)-sensing riboswitch in NMT1 mRNA from Neurospora crassa[J].FEBS Letters, 2020, 594(4):625-635.
[15] WINKLER W, NAHVI A, BREAKER R R.Thiamine derivatives bind messenger RNAs directly to regulate bacterial gene expression[J].Nature, 2002, 419(6910):952-956.
[16] YOU M X, LITKE J L, JAFFREY S R.Imaging metabolite dynamics in living cells using a Spinach-based riboswitch[J].PNAS, 2015, 112(21):E2756-E2765.
[17] KULIK M, MORI T, SUGITA Y, et al.Molecular mechanisms for dynamic regulation of N1 riboswitch by aminoglycosides[J].Nucleic Acids Research, 2018, 46(19):9960-9970.
[18] ![]() P, KULIK M, RE S Y, et al.Mutations of N1 riboswitch affect its dynamics and recognition by neomycin through conformational selection[J].Frontiers in Molecular Biosciences, 2021, 8:633130.
P, KULIK M, RE S Y, et al.Mutations of N1 riboswitch affect its dynamics and recognition by neomycin through conformational selection[J].Frontiers in Molecular Biosciences, 2021, 8:633130.
[19] LI X F, YU F, WANG F, et al.Point mutation of V252 in neomycin C epimerase enlarges substrate-binding pocket and improves neomycin B accumulation in Streptomyces fradiae[J].Bioresources and Bioprocessing, 2022, 9(1):123.
[20] LI X F, YU F, LIU K, et al.Uncovering the effects of ammonium sulfate on neomycin B biosynthesis in Streptomyces fradiae SF-2[J].Fermentation, 2022, 8(12):678.
[21] 魏萌, 李娟, 唐文丽, 等.大肠杆菌-链霉菌接合转移实验在职业院校教学中的应用与思考[J].生物学通报, 2023, 58(5):36-40.
WEI M, LI J, TANG W L, et al.Application and thinking of the experiment of Escherichia coli and Streptomyces albus conjugation transfer in vocational college teaching[J].Bulletin of Biology, 2023, 58(5):36-40.
[22] 余飞, 孙俊峰, 刘鹏飞, 等.弗氏链霉菌产硫酸新霉素高通量选育模型的建立及优化[J].食品与发酵工业, 2019, 45(8):162-167;177.
YU F, SUN J F, LIU P F, et al.A high-throughput screening method for selecting Streptomyces fradiae mutants with improved neomycin yield and its optimization[J].Food and Fermentation Industries, 2019, 45(8):162-167;177.