免疫系统通过免疫监控、免疫防御与免疫调节功能使宿主免受多种病原体侵害与威胁[1]。婴幼儿免疫发育过程复杂且动态,受到多种因素的影响,包括遗传、环境、营养和感染等[2]。由于负责免疫监控和调节的适应性免疫系统尚未发育完全[3],生命早期免疫防御主要依靠先天性免疫系统,这种免疫状态使婴幼儿在生长发育过程中面临多种病毒的威胁[4]。I型干扰素(type I interferons,IFN-I)是一类重要的细胞因子,主要在抗病毒免疫反应中发挥作用。由于干扰素α/β受体在所有有核细胞上都能表达,这让IFN-I能有效诱导广泛的全身抗病毒状态。研究发现宿主在免疫稳态状态下会保持低水平的IFN-I产生,能使细胞对其他细胞因子做出有效的后续反应。其中,相比于干扰素-α,干扰素β(interferon-β,IFN-β)在IFN-I家族中专注于保护性免疫,其在生命早期免疫成熟中发挥关键作用[5]。因此,调节IFN-β可能成为预防婴幼儿病毒性感染的潜在途径。
人体肠道菌群是稳态IFN-I表达的主要调节器,共生微生物可以通过影响浆细胞样树突状细胞产生稳态IFN-I并调节经典树突状细胞的反应,从而增强了宿主对病毒感染的抵抗力[6]。目前的研究发现,益生菌干预能够通过调节肠道菌群、刺激免疫细胞等多种途径调节免疫稳态,从而实现抗病毒等保护作用。KUMOVA等[7]的研究发现,对新生小鼠进行鼻腔鼠李糖乳酪杆菌GG处理可提高新生小鼠感染流感病毒后的存活率。此外,有研究使用副干酪乳酪杆菌MI29干预IFNAR1-/-小鼠,证明其可通过IFN-I发挥预防流感病毒的免疫保护作用,且同种对照菌株无效果,证明抗病毒作用具有菌株特异性[8]。因此,体外筛选具有抗病毒作用的益生菌至关重要,能够为后续动物实验缩小范围。小鼠骨髓源树突状细胞(bone marrow-derived dendritic cells,BMDC)作为一种重要的细胞模型,能够模拟体内树突状细胞的功能,用于研究各种免疫反应机制以及评估药物或化合物的免疫调节潜力。在MARIMAN等[9]的研究中,BMDC模型被用来验证益生菌的促炎和抗炎作用。同时,已有不少研究使用BMDC模型进行抗病毒评价。例如,STEFAN等[10]通过测定脆弱拟杆菌荚膜多糖诱导BMDC分泌IFN-β的能力来研究肠道共生菌对病毒感染的抗性。
婴幼儿的免疫发育不完全与肠道环境独特性会限制益生菌干预的效果及方式[11]。婴儿最初的微生物主要来自母亲,同时高度依赖于饮食、生活方式、环境因素和年龄等多种因素[12-13],与非母体菌株相比,母婴源菌株(婴儿肠道菌群、母亲肠道菌群、母乳)具备婴幼儿肠道生态适应性、与宿主免疫系统的协同进化等特征[14]。此外,益生菌在宿主体内发挥作用依赖于其适应肠道生态系统的能力。肠道适应能力包括克服胃酸、胆汁和渗透压等环境挑战以确保其生存和定殖[15]。同时,益生菌能够利用肠道中的多种碳源(如乳糖、低聚糖、膳食纤维等)作为能量来源,增强其在肠道内的存活率和定殖能力,形成竞争优势[16]。肠道黏附能力也被认为是鉴定潜在益生菌的关键标准,因为益生菌可以通过黏附占据肠道表面受体位点与致病菌竞争结合位点和营养物质,从而阻止致病菌的定殖;并且益生菌通过黏附能够在肠道中长期停留而不被快速排出,提高其生物利用度和功能持久性[17]。因此,本文以母婴源益生菌为研究对象,基于体外益生特性评价以及BMDC模型筛选具备婴幼儿肠道适应性和潜在免疫保护作用的益生菌菌株,进一步探究了所选菌株的不同形式刺激不同周龄来源的BMDC分泌IFN-β的能力,以期为抗病毒感染益生菌筛选及开发提供理论和技术参考。
1 材料与方法
1.1 实验菌株
本研究共选用7株双歧杆菌、5株乳杆菌、1株戊糖片球菌以及1株参比菌动物双歧杆菌乳亚种BB12,涉及的菌株包括短双歧杆菌、两歧双歧杆菌、长双歧杆菌、动物双歧杆菌乳亚种、格氏乳杆菌、鼠李糖乳酪杆菌和戊糖片球菌。实验菌株分离自中国无锡地区孕妇及婴幼儿肠道和母乳,菌株保藏于江南大学食品学院生物技术中心菌种保藏库,菌株信息表见表1。其中3株格氏乳杆菌和1株鼠李糖乳酪杆菌BB6L9已在先前的研究中报道过[18]。
表1 13株母婴源菌株基本信息
Table 1 Basic information of 13 strains of probiotics from mothers and infants
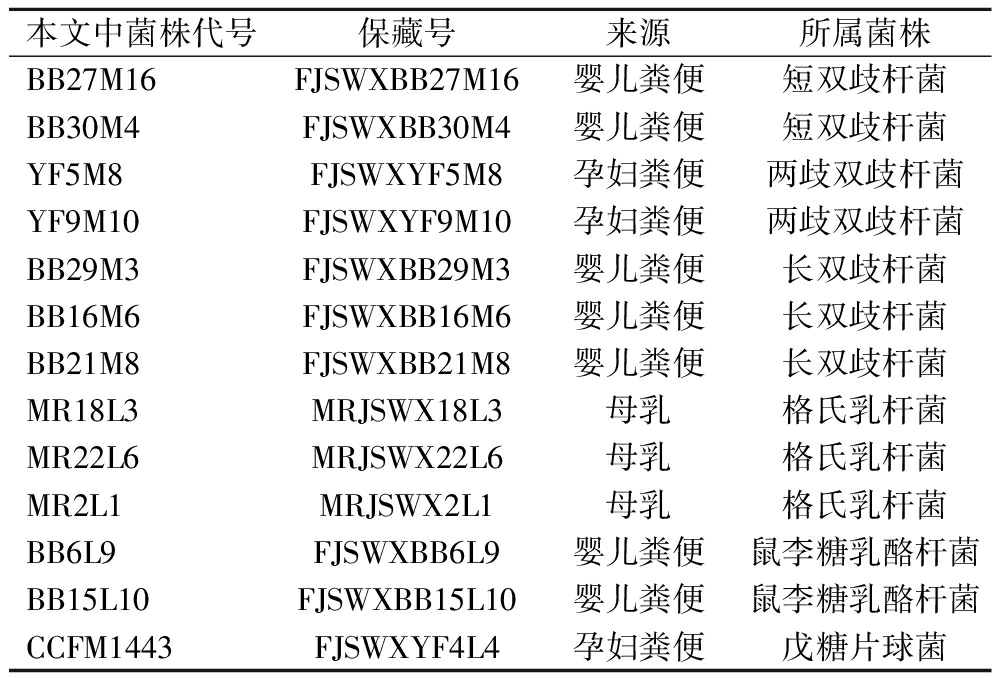
本文中菌株代号保藏号来源所属菌株BB27M16FJSWXBB27M16婴儿粪便短双歧杆菌BB30M4FJSWXBB30M4婴儿粪便短双歧杆菌YF5M8FJSWXYF5M8孕妇粪便两歧双歧杆菌YF9M10FJSWXYF9M10孕妇粪便两歧双歧杆菌BB29M3FJSWXBB29M3婴儿粪便长双歧杆菌BB16M6FJSWXBB16M6婴儿粪便长双歧杆菌BB21M8FJSWXBB21M8婴儿粪便长双歧杆菌MR18L3MRJSWX18L3母乳格氏乳杆菌MR22L6MRJSWX22L6母乳格氏乳杆菌MR2L1MRJSWX2L1母乳格氏乳杆菌BB6L9FJSWXBB6L9婴儿粪便鼠李糖乳酪杆菌BB15L10FJSWXBB15L10婴儿粪便鼠李糖乳酪杆菌CCFM1443FJSWXYF4L4孕妇粪便戊糖片球菌
1.2 实验细胞
研究中使用HT-29细胞进行肠道黏附实验,细胞购自中国科学院细胞库。BMDC分离自4、6、10周龄雌性C57BL/6J小鼠,实验方案已由江苏省血吸虫病防治研究所伦理委员会审核通过(批准号:IACUC-JIPD-2023-179)。
1.3 实验方法
1.3.1 菌株活化
将保存在-80 ℃的菌株化冻,接种环蘸取少量菌液于mMRS固体培养基上划线,37 ℃厌氧培养48 h。长出菌落后,挑取单菌落接种于5 mL mMRS液体管中,37 ℃厌氧培养18~24 h,随后按10 mL/L接种量传代培养。
1.3.2 具有促进BMDC产生IFN-β作用的母婴益生菌筛选
根据屈定武[19]的研究,在体外培养和诱导BMDC。简而言之,从4周龄C57BL/6J小鼠的股骨及胫骨采集细胞,用红细胞裂解缓冲液处理,并在直径10 cm培养皿中以2×106个细胞/皿的密度进行培养。培养基由RPMI 1640基础培养基、10 mmol/L HEPES缓冲液、10%(体积分数,下同)胎牛血清、2 mmol/L L-谷氨酰胺、1%青霉素-链霉素溶液和50 mmol/L 2-巯基乙醇组成,并添加20 ng/mL粒细胞-巨噬细胞集落刺激因子和10 ng/mL白细胞介素-4(interleukin-4,IL-4)。第3天,细胞进行半量换液,此后隔天换液,第9天获得悬浮和松散黏附的细胞。将细胞以106个/mL的密度将其置于96孔圆底培养板中,每孔200 μL。每孔中加入200 μL菌悬液(107 CFU /mL)与BMDC共培养,37 ℃ 5% CO2条件下孵育24 h,用ELISA试剂盒测定培养液上清液中IFN-β的水平,每株菌3个平行。
1.3.3 生长曲线及代时测定
将活化两代的菌株按2%的体积比例接种至mMRS培养基中,混匀后接种至96孔板中,每株菌3个平行。放置于37 ℃厌氧培养箱生长曲线检测仪中,每15 min检测1次OD600值,共培养18 h。以菌株生长时间为横坐标,OD600值为纵坐标绘制菌株生长曲线。根据生长曲线得到菌株的指数生长期,选取指数期开始和结束的2个时间点的数据用于计算代时,通过比较代时,判断菌株生长能力的强弱。按公式(1)计算:
(1)
式中:G,代时,h;t1,菌株生长进入指数期的时间点;t2,菌株指数期生长结束的时间点;OD1、OD2,t1、t2时刻测定菌悬液的OD值。
1.3.4 耐酸耐胆盐能力测定
参考文献[20-21]的方法对菌株耐酸耐胆盐能力进行评价。制备模拟胃液和模拟肠液:将3 mg/mL胃蛋白酶悬浮在无菌生理盐水(9 g/L,下同)中,并调节pH值为3.0;将3 g/L的胆盐和1 mg/mL的胰蛋白酶溶解在无菌生理盐水中,调整pH值为8.0。将培养好的菌体悬浮在模拟胃液/肠液中,37 ℃厌氧孵育3 h(模拟胃液)/4 h(模拟肠液)。在孵育前后取等量的菌悬液,将菌悬液用无菌生理盐水连续稀释,用mMRS琼脂涂布板法测定活菌数。37 ℃厌氧培养48 h,比较3 h/4 h的CFU计数与0 h的CFU计数,计算存活率。
1.3.5 糖利用能力测定
根据WATSON等[22]的方法测试了菌株对婴儿配方奶粉中常见的5种碳源(唾液酸、酵母葡聚糖、岩藻基乳糖、低聚果糖和低聚半乳糖)的利用能力。
1.3.6 抗菌活性测定
根据BNFAGA等[23]的方法略作修改,选择金黄色葡萄球菌、单增李斯特菌、大肠杆菌和鼠伤寒沙门氏菌作为致病菌进行体外抗菌活性测定。用mMRS培养基培养24 h的细菌上清液进行抑菌试验。实验菌株的无细胞培养上清液(cell-free culture supernatant,CFCS)通过5 000×g离心20 min后,用NaOH溶液调pH值至6.2~6.4,在超净工作台中用0.22 μm过滤器收集。将LB肉汤中培养的4株病原菌原液各吸取100 μL至固体LB平板上,涂布均匀至无水迹。随后在琼脂上钻8 mm直径的孔,将70 μL 的CFCS转移到相应的孔中。正置放入厌氧培养箱培养48 h,测量孔周围无生长抑制带(直径,mm)。以mMRS液体培养基为阴性对照,每株菌做3个平行。
1.3.7 肠道黏附能力测定
根据李刘若兰[24]的方法测定实验菌株对HT-29细胞的黏附能力。用细胞增殖示踪荧光探针cFDA-SE和二甲基亚砜配制1 mmol/L的荧光染色储备液,制备携带荧光染料的菌悬液,并调整菌悬液浓度为108 CFU/mL。
用PBS冲洗HT-29细胞2次,在12孔板中接种实验菌株,每孔1 mL,每株菌接种4个孔。在5% CO2、37 ℃条件下孵育4 h,PBS洗3次去除未黏附的细菌或分泌物;每株菌的其中3个孔加入250 μL胰酶(2.5 g/L EDTA)进行消化,37 ℃静置10 min后,加入完全培养基终止消化,收集细胞悬液,5 000×g离心10 min,去上清液,用培养基重悬,使用荧光分光光度计测量荧光强度。每株菌的剩余一个孔加入1 mL的甲醇溶液,静置10 min进行固定,吸去甲醇,待风干后用于荧光拍照。
1.3.8 戊糖片球菌CCFM1443活菌与热杀菌对不同周龄来源BMDC的调节能力
将活菌在金属浴98 ℃处理20 min得到热杀菌。采用4、6和10周龄来源的BMDC与菌株共培养,方法同1.3.2节。
1.4 数据处理
使用GraphPad Prism v9.3.0软件进行数据分析。连续变量数据表示为“平均值±标准差”,使用单因素方差分析分析数据,将P<0.05作为阈值来判别组间的显著性差异。
2 结果
2.1 13株母婴源益生菌与BMDC共培养产生IFN-β的水平
如图1所示,7株双歧杆菌中仅有长双歧杆菌BB16M6能刺激BMDC分泌IFN-β,且质量浓度较低,为16.10 pg/mL。3株格氏乳杆菌、2株鼠李糖乳酪杆菌和戊糖片球菌CCFM1443均能促进BMDC产生IFN-β。其中,格氏乳杆菌MR18L3和戊糖片球菌CCFM1443促进IFN-β分泌的能力显著强于其他菌株,戊糖片球菌CCFM1443刺激BMDC产生IFN-β的水平在13株菌中最高,质量浓度高达174.13 pg/mL。
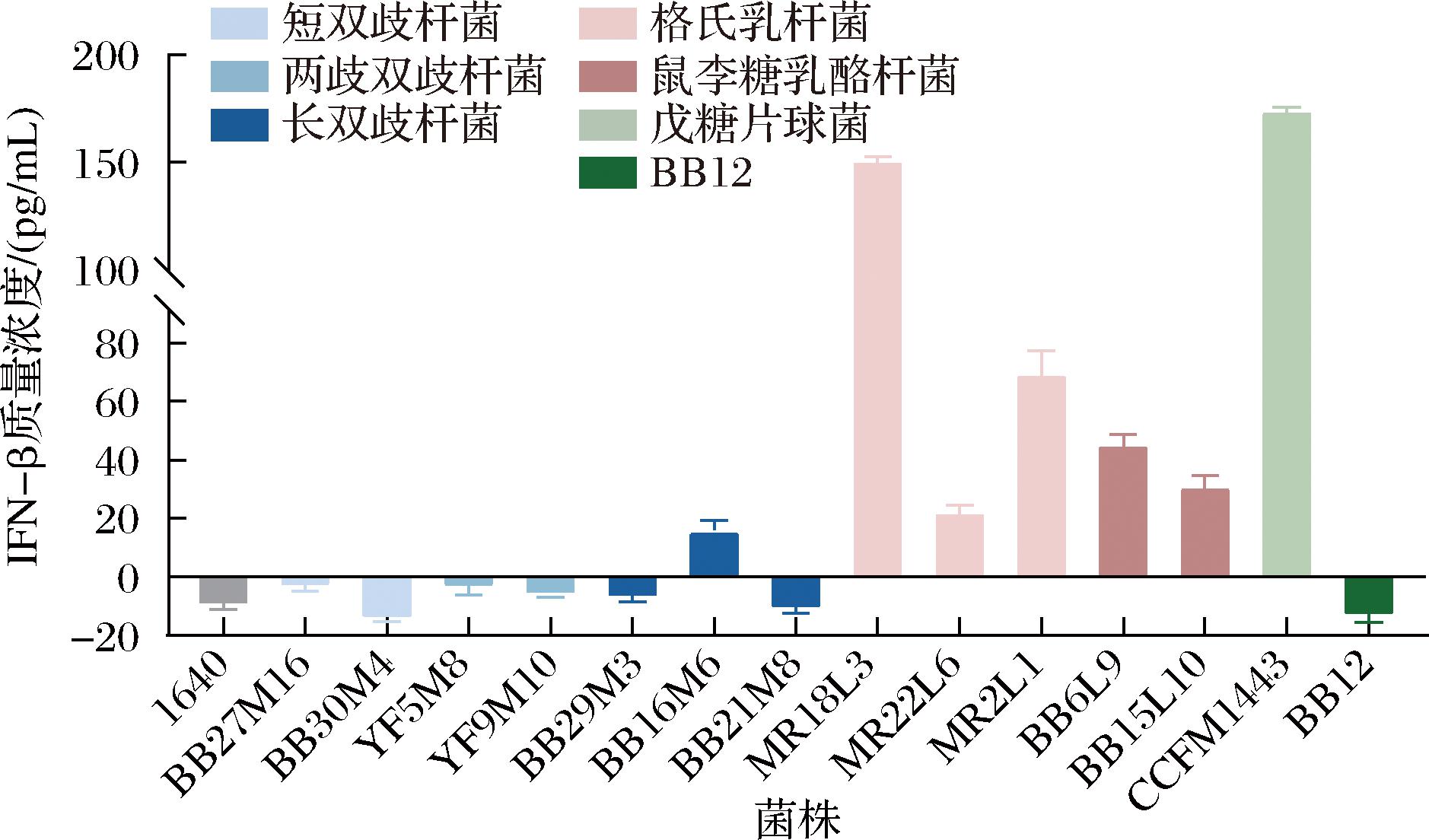
图1 14株菌促进BMDC分泌IFN-β的水平
Fig.1 Levels of IFN-β secretion promoted by 14 bacterial strains in BMDC
2.2 菌株的生长曲线与代时
13株母婴源益生菌及BB12的生长曲线和代时如图2所示,戊糖片球菌CCFM1443的代时最短(G=2.03 h),生长速率最快。两歧双歧杆菌YF5M8、长双歧杆菌BB29M3和格氏乳杆菌MR2L1的代时>5 h,表明这3株菌的生长速率较慢。当菌株生长至稳定期,戊糖片球菌CCFM1443的OD600值>1.0,代表菌株生长能力较强。
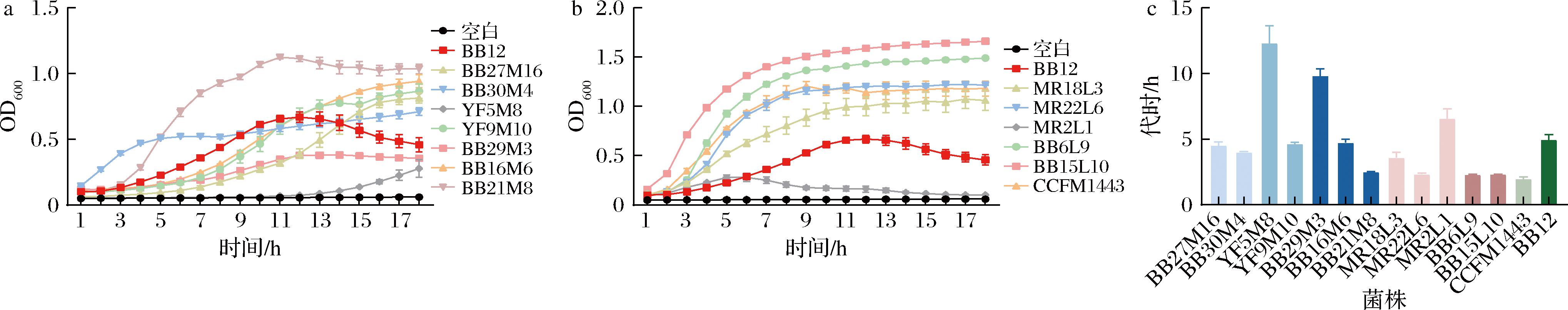
a-7株双歧杆菌生长曲线图;b-5株乳杆菌及1株戊糖片球菌生长曲线图;c-代时图
图2 生长曲线及代时
Fig.2 Growth curve and generation time
2.3 菌株耐受模拟胃液和模拟肠液的能力
在本研究中,根据菌落计数测定了13株菌在模拟胃液(pH=3.0)和模拟肠液(pH=8.0)条件下的存活率。结果显示,模拟胃液实验中,戊糖片球菌CCFM1443的存活率为36.42%,耐酸性强于长双歧杆菌BB16M6(存活率为3.46%)和格氏乳杆菌MR22L6(存活率为10.59%),但也弱于76.92%的实验菌株(图3-a)。在模拟肠液条件下,如图3-b所示,13株菌的存活率均有不同程度的下降。戊糖片球菌CCFM1443的耐受性最强,存活率高达30.06%;有5株菌株的耐胆盐存活率低于1%,表明其胆盐耐受能力较差。
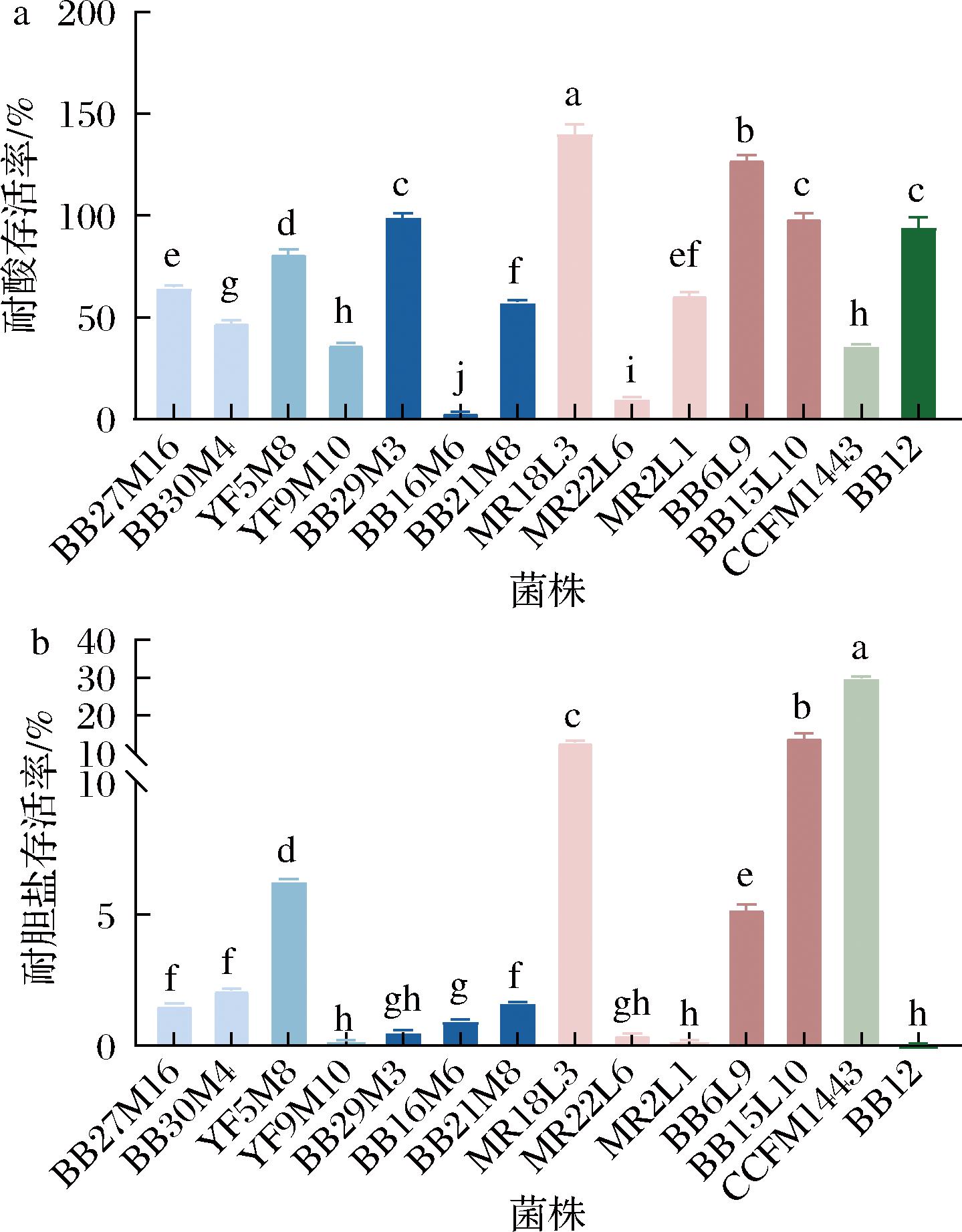
a-菌株在模拟胃液中的存活率;b-菌株在模拟肠液中的存活率
图3 菌株对模拟胃液和模拟肠液的耐受性
Fig.3 Strain tolerance to simulated gastric fluid and simulated intestinal fluid
注:不同的字母表示存在显著性差异(P<0.05)(下同)。
2.4 菌株对不同碳源的利用能力
在婴儿配方奶粉中常见的5种碳源条件下,所有菌株都能利用低聚果糖、低聚半乳糖和N-乙酰神经氨酸,但菌株利用程度不同。如图4所示,在以酵母β-葡聚糖为唯一碳源时,戊糖片球菌CCFM1443和7株双歧杆菌均不能生长。此外,戊糖片球菌CCFM1443对低聚果糖的利用程度最高,其次是N-乙酰神经氨酸和低聚半乳糖。相较于5株乳杆菌,戊糖片球菌CCFM1443对不同碳源的利用种类减少,但对低聚果糖和N-乙酰神经氨酸的利用能力强于5株乳杆菌。
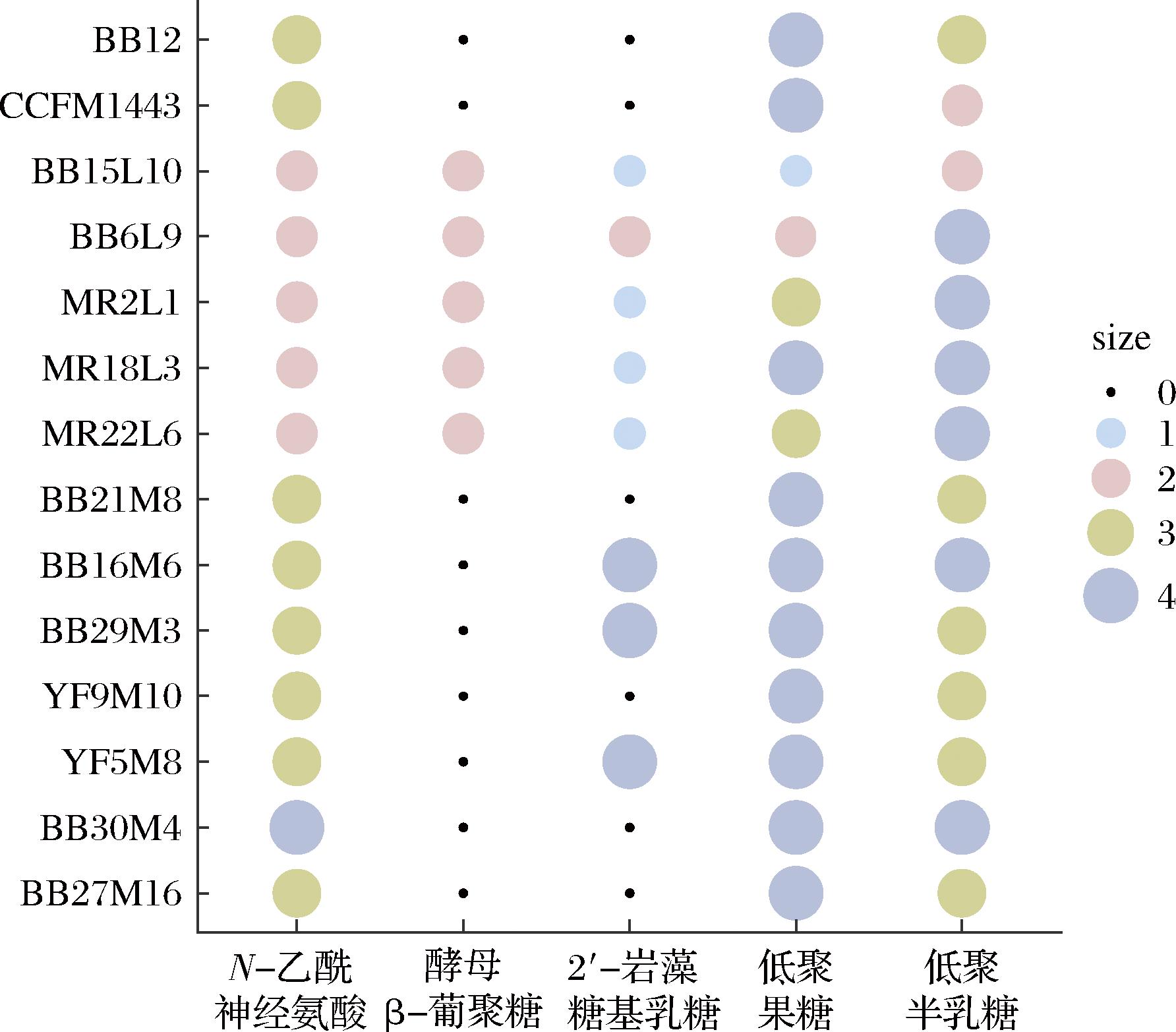
图4 菌株对5种碳水化合物的利用能力
Fig.4 The ability of strains to utilize five carbohydrate
注:“0”代表不能利用该碳源,随着分数的增加,利用糖的能力逐渐增强。
2.5 菌株的抗菌活性
如表2所示,13株菌中仅有戊糖片球菌CCFM1443对金黄色葡萄球菌展现了抑制能力,且有30.77%的菌株对4种致病菌均无抑制能力,7株双歧杆菌均无法抑制单增李斯特菌,表明实验菌株的抑菌活性较差。相较于其余12株菌株,戊糖片球菌CCFM1443能抑制3种致病菌的生长,表现出更强的抑菌广谱性。
表2 益生菌候选物对4种致病菌的抑制能力
Table 2 Inhibitory ability of probiotic candidates against four pathogenic bacteria
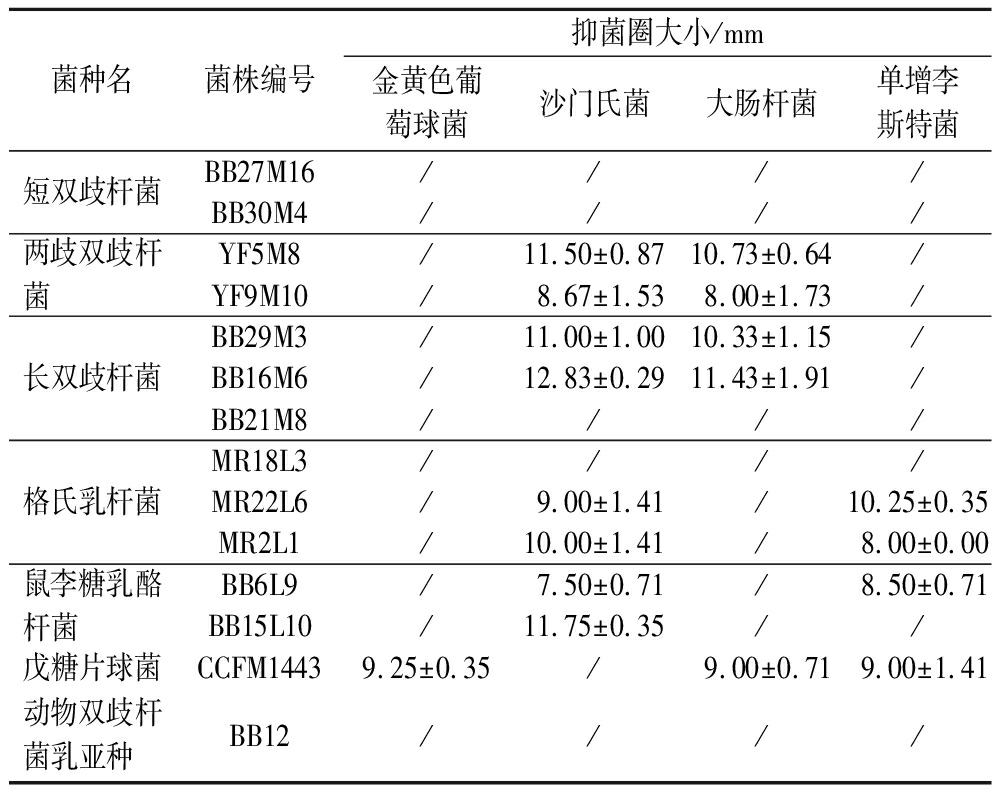
菌种名菌株编号抑菌圈大小/mm金黄色葡萄球菌沙门氏菌大肠杆菌单增李斯特菌短双歧杆菌BB27M16////BB30M4////两歧双歧杆菌YF5M8/11.50±0.8710.73±0.64/YF9M10/8.67±1.538.00±1.73/长双歧杆菌BB29M3/11.00±1.0010.33±1.15/BB16M6/12.83±0.2911.43±1.91/BB21M8////格氏乳杆菌MR18L3////MR22L6/9.00±1.41/10.25±0.35MR2L1/10.00±1.41/8.00±0.00鼠李糖乳酪杆菌BB6L9/7.50±0.71/8.50±0.71BB15L10/11.75±0.35//戊糖片球菌CCFM14439.25±0.35/9.00±0.719.00±1.41动物双歧杆菌乳亚种BB12////
注:“/”表示菌株对致病菌无抑制作用。
2.6 菌株对HT-29细胞的黏附能力
如图5-a所示,戊糖片球菌CCFM1443黏附率仅次于格氏乳杆菌,为11.02%,高于69.3%的实验菌株。3株格氏乳杆菌的肠道黏附能力远大于其他菌株,其中MR2L1的黏附率高达22.86%。通过荧光倒置显微镜拍摄了戊糖片球菌CCFM1443对HT-29细胞的黏附情况(图5-b),结果显示,带绿色荧光标记的戊糖片球菌CCFM1443与HT-29细胞的分布重叠,显示出菌株与细胞的良好结合,表明戊糖片球菌CCFM1443对HT-29细胞表现出较强的黏附能力。
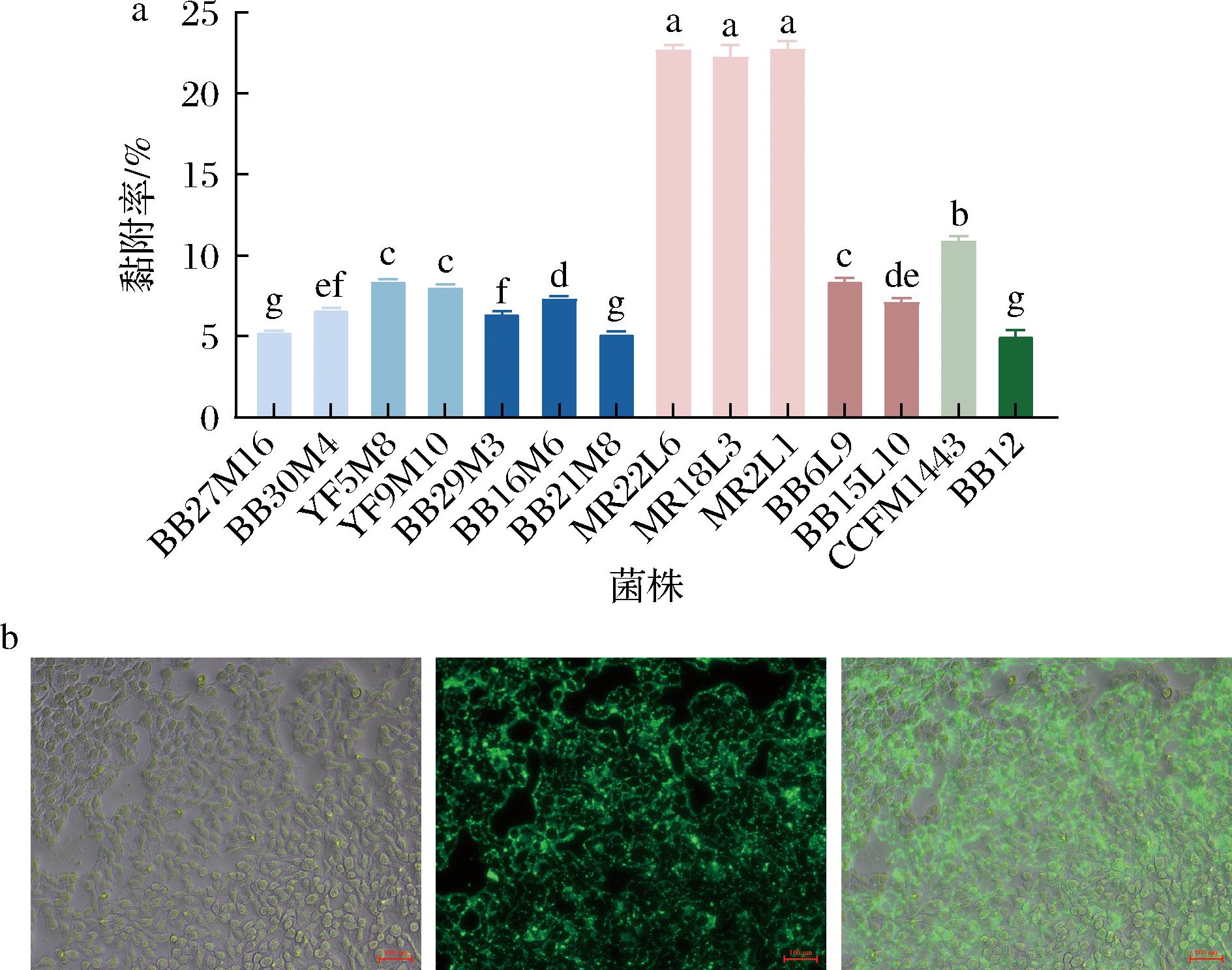
a-14株菌的肠道黏附率;b-戊糖片球菌CCFM1443黏附实验的荧光、明场和合成图像(20×)
图5 候选菌株对HT-29细胞的黏附能力
Fig.5 Adhesion ability of candidate strains to HT-29 cells
2.7 戊糖片球菌CCFM1443与BMDCs共培养产生IFN-β的水平
在BMDC模型细胞初步筛选母婴源益生菌实验中,戊糖片球菌CCFM1443的免疫调节能力最强。结合5项基础益生特性测试发现,戊糖片球菌CCFM1443在实验菌株中生长速率最快、具有良好的耐酸耐胆盐能力和抗菌活性,同时能较好地利用多种碳源和有较强的肠道黏附能力,展现出优秀的体外益生特性。因此对戊糖片球菌CCFM1443展开进一步的体外细胞功能性探究,结果如图6所示,戊糖片球菌CCFM1443热杀菌的调节能力显著强于活菌;在3个周龄的小鼠BMDC中,热杀菌没有显著差异,戊糖片球菌CCFM1443活菌对6周龄小鼠BMDC的刺激作用最强,显著高于对10周龄小鼠BMDC的促进作用。
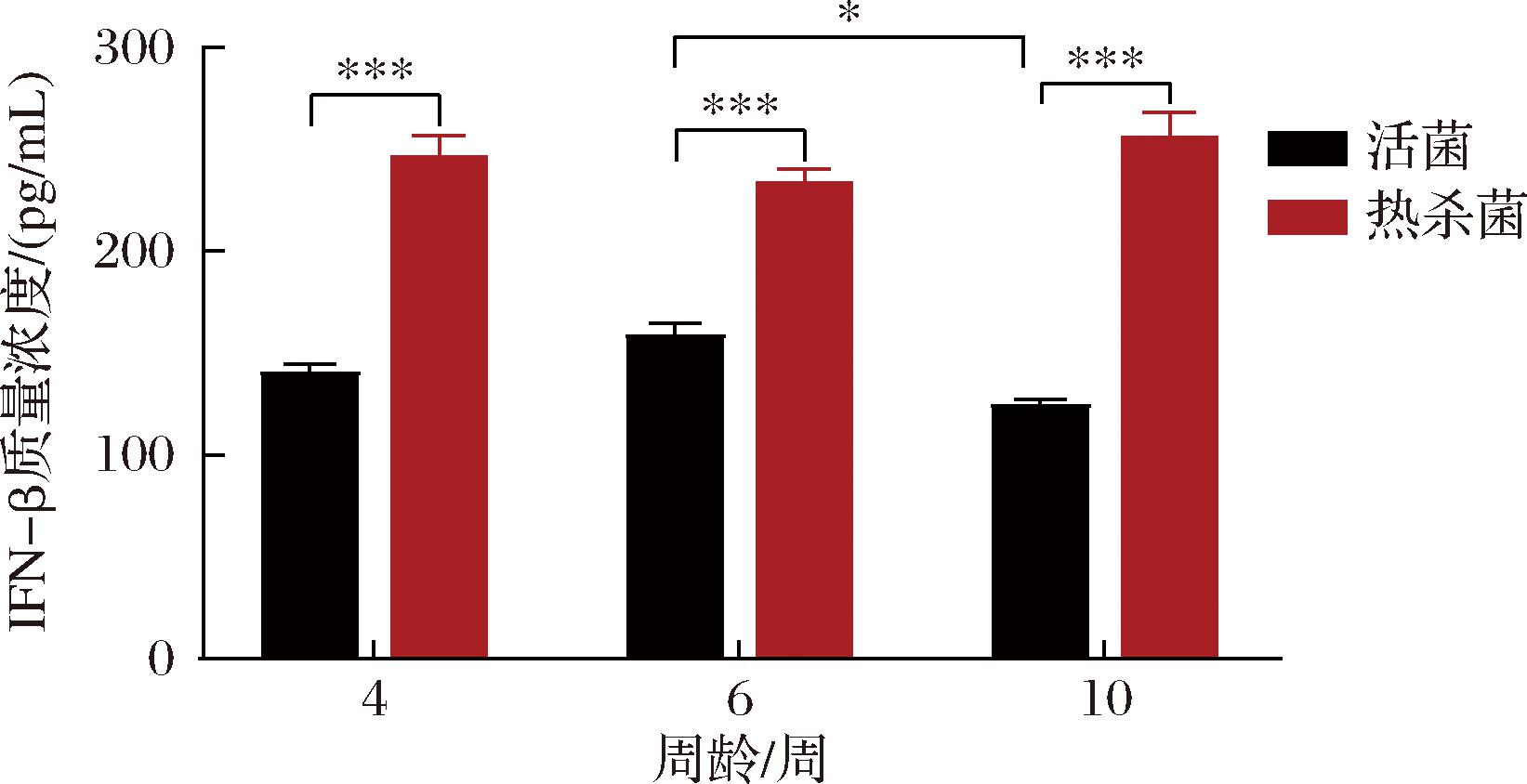
图6 戊糖片球菌CCFM1443活菌和热杀菌促进不同周龄来源的BMDCs分泌IFN-β的水平
Fig.6 Live and heat-killed Pediococcus pentosaceus CCFM1443 promote the secretion of IFN-β by BMDCs from different ages
注:*代表P< 0.05,***代表P< 0.001。
3 讨论
据报道,益生菌如双歧杆菌和乳杆菌对病毒感染具有免疫调节和预防作用[7,25-26]。BMDC作为一种重要的细胞模型,能够模拟体内树突状细胞的功能,用于研究各种免疫反应机制以及评估药物或化合物的免疫调节潜力[9-10]。本文通过BMDC模型在体外筛选能够促进BMDC分泌IFN-β的菌株,发现双歧杆菌刺激BMDC产生IFN-β的效果具有菌株特异性,乳杆菌和戊糖片球菌均能在体外展现免疫调节能力。其中,戊糖片球菌CCFM1443的作用最强,格氏乳杆菌MR18L3次之。体外BMDC实验提示戊糖片球菌CCFM1443可能通过调节IFN-β成为预防病毒等感染的潜在益生菌。
微生物典型生长曲线分为延滞期(适应期)、对数期、稳定期和衰亡期4个时期,通过测定菌株的生长曲线可以为优化培养条件、设计发酵工艺提供理论依据。生长曲线及代时结果显示,戊糖片球菌CCFM1443的生长速率最快,且稳定期的生物量较高,具备良好的生产特性基础。益生菌进入人体后必须克服胃肠道的不良环境才能存活。在一定时间内对胃液的低pH值和肠液中胆盐的良好耐受性是选择益生菌的重要标准之一。因此,耐酸和耐胆盐实验已被用作从大量菌株中初步筛选潜在益生菌的方法[27-28]。本实验中,84.62%的菌株在模拟胃液条件下的存活率高于30%,模拟胃液条件下61.54%的菌株存活率高于1%。其中戊糖片球菌CCFM1443的耐胆盐能力最强,存活率高达30.06%,能更好地耐受肠液环境。
当细菌到达肠道时,益生菌微生物黏附于肠黏膜是定植的先决条件[29]。体外黏附试验被认为可以反映益生菌菌株暂时在人体肠道中存活的能力[30]。HT-29是一种常用的人类结肠腺癌细胞系,其形态和功能特征与正常肠细胞相似,是已被广泛用作研究肠细胞功能的体外模型。实验结果表明,13株菌均能黏附在HT-29细胞表面,但黏附能力存在差异,菌株的黏附率最低为5.26%,最高可达22.86%,戊糖片球菌CCFM1443仅次于3株格氏乳杆菌。造成差异的原因是益生菌的表面因子在黏附中起重要作用,研究发现菌株的表面因子(如胞外多糖[31]、黏附蛋白[32]等)可能通过与上皮细胞的特异性结合提高菌株的黏附能力。益生菌在肠道内定植后,可通过释放各种抗菌物质(包括有机酸和细菌素)抑制肠道致病菌的生长,从而维持肠道稳态[33-34]。在本研究中,戊糖片球菌CCFM1443展现出良好的抗菌能力,对金黄色葡萄球菌、大肠杆菌和单增李斯特菌均有抑菌活性。现有研究表明,包括戊糖片球菌在内的多种益生菌抗菌物质可以通过破坏细胞膜完整性[35]、增加细胞膜通透性[36]、影响代谢途径[37]等方式抑制病原菌的生长和繁殖。
肠道微生物利用营养物质的能力在一定程度上决定了它们在肠道中驻留和生存的能力,而利用独特的碳水化合物或更有效地利用它们有助于细菌扩张和定居新的生态位[38-39]。许多细菌在混合碳源中生长时优先利用葡萄糖。本实验中,选择了除葡萄糖外5种常见的婴儿配方奶粉添加碳源作为唯一碳源进行实验,选择在婴幼儿肠道中更有竞争优势的菌株,以评估菌株对这些碳源的利用能力,为未来婴儿配方奶粉的设计提供参考,也可将筛选出的菌株与其高效利用的碳源组合应用,开发为潜在的合生元制剂。结果表明,所有实验菌株均能利用至少3种碳源。其中,戊糖片球菌CCFM1443能利用低聚果糖、低聚半乳糖和N-乙酰神经氨酸,不能利用酵母β-葡聚糖和2′-岩藻糖基乳糖。与本文结果一致,UNBAN等[40]分离的戊糖片球菌CMY9也能利用低聚果糖和低聚半乳糖,并且对低聚果糖的利用程度高于低聚半乳糖。
通过BMDC模型初步探究了13株母婴源益生菌的免疫调节能力,结合体外益生特性实验发现,戊糖片球菌CCFM1443促进BMDC分泌IFN-β的能力最强,并且具有良好的益生特性。因此,对戊糖片球菌CCFM1443展开进一步研究。先前研究发现,除了活菌形式,植物乳植杆菌、干酪乳酪杆菌和戊糖乳杆菌等益生菌的热杀菌也能增强对流感病毒的免疫保护[41-43]。本文分别使用活菌和热杀菌来进行菌株潜在抗病毒能力评价,结果表明热杀菌促进BMDC分泌IFN-β的能力强于活菌,提示戊糖片球菌CCFM1443可能作为后生元调节宿主免疫反应。由于生命早期免疫系统尚未完全成熟,新生儿和幼儿更容易受到感染,肠道菌群有助于免疫系统的发育[44]。随着年龄的增长,免疫系统逐渐成熟,肠道菌群也趋于稳定。本文也探究了戊糖片球菌CCFM1443对4、6、10周龄小鼠BMDC的调节作用,发现菌株均能有效调节BMDC分泌IFN-β,表明戊糖片球菌CCFM1443可能对不同时期的宿主均有免疫保护作用。
4 结论
本研究旨在通过体外基础特性评价和BMDC模型筛选具有婴幼儿肠道适应性和潜在免疫保护作用的母婴源益生菌菌株。经过BMDC实验和5项益生特性实验筛选得到一株戊糖片球菌CCFM1443,其具备优秀的生长能力、胆盐耐受性、抗菌活性、肠道黏附能力和体外调节免疫细胞的能力,为母婴源益生菌具有潜在调节免疫作用提供了新的证据。未来将进一步探究戊糖片球菌CCFM1443在体内预防感染、提供免疫保护的作用效果,为后续开发提高婴幼儿免疫水平的母婴益生菌产品提供新的策略。
[1] BRODIN P, DAVIS M M.Human immune system variation[J].Nature Reviews Immunology, 2017, 17(1):21-29.
[2] 汪姝敏, 翟齐啸.婴幼儿肠道菌群的发育、成熟及影响因素研究进展[J].乳业科学与技术, 2022, 45(1):38-47.
WANG S M, ZHAI Q X.Development and maturation of the intestinal flora during infancy and early childhood and influencing factors[J].Journal of Dairy Science and Technology, 2022, 45(1):38-47.
[3] ADKINS B, LECLERC C, MARSHALL-CLARKE S.Neonatal adaptive immunity comes of age[J].Nature Reviews Immunology, 2004, 4(7):553-564.
[4] LEVY O.Innate immunity of the newborn:Basic mechanisms and clinical correlates[J].Nature Reviews Immunology, 2007, 7(5):379-390.
[5] HOOFTMAN A, PEACE C G, RYAN D G, et al.Macrophage fumarate hydratase restrains mtRNA-mediated interferon production[J].Nature, 2023, 615(7952):490-498.
[6] SCHAUPP L, MUTH S, ROGELL L, et al.Microbiota-induced type I interferons instruct a poised basal state of dendritic cells[J].Cell, 2020, 181(5):1080-1096.e19.
[7] KUMOVA O K, FIKE A J, THAYER J L, et al.Lung transcriptional unresponsiveness and loss of early influenza virus control in infected neonates is prevented by intranasal Lactobacillus rhamnosus GG[J].PLoS Pathogens, 2019, 15(10):e1008072.
[8] KIM S, LEE S, KIM T Y, et al.Newly isolated Lactobacillus paracasei strain modulates lung immunity and improves the capacity to cope with influenza virus infection[J].Microbiome, 2023, 11(1):260.
[9] MARIMAN R, KREMER B, KONING F, et al.The probiotic mixture VSL#3 mediates both pro- and anti-inflammatory responses in bone marrow-derived dendritic cells from C57BL/6 and BALB/c mice[J].British Journal of Nutrition, 2014, 112(7):1088-1097.
[10] STEFAN K L, KIM M V, IWASAKI A, et al.Commensal microbiota modulation of natural resistance to virus infection[J].Cell, 2020, 183(5):1312-1324.e10.
[11] 李双祁. 母乳来源益生菌的筛选和益生作用研究[D].广州:广东工业大学, 2022.
LI S Q.Research on screening and probiotic effects of probiotics derived from breast milk[D].Guangzhou:Guangdong University of Technology, 2022.
[12] BARKER-TEJEDA T C, ZUBELDIA-VARELA E, MAC AS-CAMERO A, et al.Comparative characterization of the infant gut microbiome and their maternal lineage by a multi-omics approach[J].Nature Communications, 2024, 15:3004.
AS-CAMERO A, et al.Comparative characterization of the infant gut microbiome and their maternal lineage by a multi-omics approach[J].Nature Communications, 2024, 15:3004.
[13] 梅丽亚, 郑雪丽, 李佳豪, 等.母乳源乳酸菌调节肠道稳态的研究进展及产业化应用[J].食品与发酵工业,2025,51(12):424-432.
MEI L Y, ZHENG X L, LI J H, et al.Research progress and industrial application of breast milk-derived lactic acid bacteria in regulating intestinal homeostasis[J].Food and Fermentation Industries, 2025,51(12):424-432.
[14] 于俊娟, 王秋玉.母婴源益生菌的研究与开发进展 [J].食品安全导刊, 2024, (25):148-150;154.
YU J J, WANG Q Y.Research and development progress of probiotics of maternal and infant origin[J].China Food Safety Magazine, 2024(25):148-150;154.
[15] ZHANG Z W, LV J L, PAN L, et al.Roles and applications of probiotic Lactobacillus strains[J].Applied Microbiology and Biotechnology, 2018, 102(19):8135-8143.
[16] WANG H, HUANG X J, TAN H Z, et al.Interaction between dietary fiber and bifidobacteria in promoting intestinal health[J].Food Chemistry, 2022, 393:133407.
[17] MONTEAGUDO-MERA A, RASTALL R A, GIBSON G R, et al.Adhesion mechanisms mediated by probiotics and prebiotics and their potential impact on human health[J].Applied Microbiology and Biotechnology, 2019, 103(16):6463-6472.
[18] SHENTU J Q, ZHENG C D, WANG S M, et al.In vitro screening and identification of Lactobacilli with potential probiotic characteristics from breast milk and infant feces[J].Food Nutrition, 2025, 1(1):100009.
[19] 屈定武. 两歧双歧杆菌对TNBS诱导型结肠炎的缓解作用及机制探究[D].无锡:江南大学, 2023.
QU D W.Relieving effect and mechanism of Bifidobacterium bifidum on TNBS-induced colitis[D].Wuxi:Jiangnan University, 2023.
[20] RANADHEERA C S, EVANS C A, ADAMS M C, et al.In vitro analysis of gastrointestinal tolerance and intestinal cell adhesion of probiotics in goat’s milk ice cream and yogurt[J].Food Research International, 2012, 49(2):619-625.
[21] RANADHEERA C S, EVANS C A, ADAMS M C, et al.Effect of dairy probiotic combinations on in vitro gastrointestinal tolerance, intestinal epithelial cell adhesion and cytokine secretion[J].Journal of Functional Foods, 2014, 8:18-25.
[22] WATSON D, MOTHERWAY M O, SCHOTERMAN M C, et al.Selective carbohydrate utilization by lactobacilli and bifidobacteria[J].Journal of Applied Microbiology, 2013, 114(4):1132-1146.
[23] BNFAGA A A, LEE K W, THAN L T L, et al.Antimicrobial and immunoregulatory effects of Lactobacillus delbrueckii 45E against genitourinary pathogens[J].Journal of Biomedical Science, 2023, 30(1):19.
[24] 李刘若兰. 人体肠道中长双歧杆菌占据属内丰度优势的机制解析及筛选方法开发[D].无锡:江南大学, 2023.
LI L R L.Mechanism analysis and screening method development of Bifidobacterium longum occupying of the abundance dominance within the genus in the human gut[D].Wuxi:Jiangnan University, 2023.
[25] MAHOOTI M, ABDOLALIPOUR E, SALEHZADEH A, et al.Immunomodulatory and prophylactic effects of Bifidobacterium bifidum probiotic strain on influenza infection in mice[J].World Journal of Microbiology and Biotechnology, 2019, 35(6):91.
[26] XING J H, SHI C W, SUN M J, et al.Lactiplantibacillus plantarum 0111 protects against influenza virus by modulating intestinal microbial-mediated immune responses[J].Frontiers in Microbiology, 2022, 13:820484.
[27] DING W R, SHI C, CHEN M, et al.Screening for lactic acid bacteria in traditional fermented Tibetan yak milk and evaluating their probiotic and cholesterol-lowering potentials in rats fed a high-cholesterol diet[J].Journal of Functional Foods, 2017, 32:324-332.
[28] DAMODHARAN K, LEE Y S, PALANIYANDI S A, et al.Preliminary probiotic and technological characterization of Pediococcus pentosaceus strain KID7 and in vivo assessment of its cholesterol-lowering activity[J].Frontiers in Microbiology, 2015, 6:768.
[29] ZHENG Y X, ZHAO J R, NIE X Y, et al.Mutual adhesion of Lactobacillus spp.to intestinal cells:A review of perspectives on surface layer proteins and cell surface receptors[J].International Journal of Biological Macromolecules, 2024, 282(Pt 4):137031.
[30] BLUM S, RENIERO R, SCHIFFRIN E J, et al.Adhesion studies for probiotics:Need for validation and refinement[J].Trends in Food Science &Technology, 1999, 10(12):405-410.
[31] ZENG Z, ZUO F L, MARCOTTE H.Putative adhesion factors in vaginal Lactobacillus gasseri DSM 14869:Functional characterization[J].Applied and Environmental Microbiology, 2019, 85(19):e00800-19.
[32] QIAN G R, ZANG H, TANG J T, et al.Lactobacillus gasseri ATCC33323 affects the intestinal mucosal barrier to ameliorate DSS-induced colitis through the NR1I3- mediated regulation of E-cadherin[J].PLoS Pathogens, 2024, 20(9):e1012541.
[33] LIU B H, ZHONG X X, LIU Z Y, et al.Probiotic potential and safety assessment of Lactiplantibacillus plantarum cqf-43 and whole-genome sequence analysis[J].International Journal of Molecular Sciences.
[34] JIANG Y H, YANG R S, LIN Y C, et al.Assessment of the safety and probiotic characteristics of Lactobacillus salivarius CGMCC20700 based on whole-genome sequencing and phenotypic analysis[J].Frontiers in Microbiology, 2023, 14:1120263.
[35] SOUNDHARRAJAN I, KIM D, KUPPUSAMY P, et al.Probiotic and Triticale silage fermentation potential of Pediococcus pentosaceus and Lactobacillus brevis and their impacts on pathogenic bacteria[J].Microorganisms.
[36] XU C, FU Y Y, LIU F, et al.Purification and antimicrobial mechanism of a novel bacteriocin produced by Lactobacillus rhamnosus 1.0320[J].LWT, 2021, 137:110338.
[37] WANG S, ZHANG Y J, MANDLAA, et al.Properties and mechanism of the antimicrobial peptide APT produced by Lactobacillus ALAC-4[J].LWT, 2022, 165:113713.
[38] REGMI A, BOYD E F.Carbohydrate metabolic systems present on genomic islands are lost and gained in Vibrio parahaemolyticus[J].BMC Microbiology, 2019, 19(1):112.
[39] ALTERMANN E, KLAENHAMMER T R.Group-specific comparison of four lactobacilli isolated from human sources using differential blast analysis[J].Genes &Nutrition, 2011, 6(3):319-340.
[40] UNBAN K, CHAICHANA W, BAIPONG S, et al.Probiotic and antioxidant properties of lactic acid bacteria isolated from indigenous fermented tea leaves (miang) of north Thailand and promising application in synbiotic formulation[J].Fermentation, 2021, 7(3):195.
[41] KOBAYASHI N, SAITO T, UEMATSU T, et al.Oral administration of heat-killed Lactobacillus pentosus strain b240 augments protection against influenza virus infection in mice[J].International Immunopharmacology, 2011, 11(2):199-203.
[42] MAEDA N, NAKAMURA R, HIROSE Y, et al.Oral administration of heat-killed Lactobacillus plantarum L-137 enhances protection against influenza virus infection by stimulation of type I interferon production in mice[J].International Immunopharmacology, 2009, 9(9):1 122-1 125.
[43] JUNG Y J, LEE Y T, LE NGO V, et al.Heat-killed Lactobacillus casei confers broad protection against influenza A virus primary infection and develops heterosubtypic immunity against future secondary infection[J].Scientific Reports, 2017, 7:17360.
[44] SANIDAD K Z, AMIR M, ANANTHANARAYANAN A, et al.Maternal gut microbiome-induced IgG regulates neonatal gut microbiome and immunity[J].Science Immunology, 2022, 7(72):eabh3816.