龋齿是全球范围内最常见的口腔疾病之一。据全国口腔卫生报道,截止到2022年,全球有约25亿人患有龋齿。龋齿的初期无明显症状,但若不及时治疗,病变继续发展形成龋洞,从而继发牙髓炎、根尖周炎等并发症,且龋洞不会自行愈合,其发展的最终结果是牙齿丧失[1]。
龋齿的发生与口腔菌群密切相关,牙菌斑生物膜是细菌在口腔中存在的主要生态形式[2]。龋齿发生时,可以从牙菌斑生物膜中分离出变异链球菌,该菌有很强的产酸和耐酸性,可以利用饮食中的碳水化合物产酸,引起口腔局部pH值降低,导致牙面脱矿化。同时变异链球菌能够产生表面抗原Ⅰ/Ⅱ和水不溶性葡聚糖,从而促进细菌对牙面和其他细菌的黏附[3]。此外,变异链球菌可以在喂食富含蔗糖饮食的动物中诱导龋齿的形成,是目前公认的引发龋齿的主要病原体[4]。
此外,白色念珠菌在龋齿病变部位中的检出率高达97%[5],也是口腔中常见的致龋性真菌。白色念珠菌能黏附于牙齿表面,产生的菌丝可侵袭牙本质小管,引起牙体硬组织脱矿[6]。白色念珠菌与变异链球菌之间存在相互作用,可以通过上调糖代谢影响变异链球菌的定植、增殖及代谢酸的能力,而同时变异链球菌影响白色念珠菌的生存、致龋毒力、共聚集和黏附力,二者的相互作用是形成生物膜导致龋齿的重要推动因素[7]。
益生菌是一种足量摄入后对宿主健康有益的活性微生物[8],能够通过调节肠道微生物及免疫系统来发挥改善作用[9]。近年来,科学界对益生菌在口腔健康中的潜在作用表现出了极大的兴趣。研究表明,益生菌可通过分泌抑菌物质降低口腔致病菌生物膜的生成量[10],改善口腔微生态平衡[11]等多种途径来提升口腔健康。如鼠李糖乳酪杆菌[12]、唾液联合乳杆菌[13]、植物乳植杆菌[14]及戊糖乳杆菌[15]等多种菌株可以抑制变异链球菌和白色念珠菌的生长,并影响其生物膜的生成,在龋齿的预防中发挥了积极作用。
大鼠龋齿模型为研究龋齿及其干预措施提供了有效的实验平台。本研究通过变异链球菌和白色念珠菌侵染建立大鼠龋齿模型,评估由鼠李糖乳酪杆菌CCFM1070和唾液联合乳杆菌CCFM1215结合其他辅料组成的复合益生菌对大鼠龋齿的改善作用,从减少口腔致病菌、龋齿损坏程度等方面来评判该复合益生菌对龋齿的缓解作用,为益生菌在龋齿预治应用中提供更多的可能性。
1 材料与方法
1.1 实验菌株及样品
变异链球菌ATCC25175,中国普通微生物菌种保藏管理中心;白色念珠菌O501,分离自患龋儿童的牙菌斑。
复合益生菌及辅料,无锡特殊食品与营养健康研究院有限公司,复合益生菌主要成分见表1,辅料由不含益生菌的其他成分组成。复合益生菌均为0.5 g/片,于-20 ℃保存,动物实验前检测其活菌数,取0.5 g复合益生菌磨成粉末,加1 mL水涡旋混匀使其融化并进行活菌计数,结果为1.9×109 CFU/g。
表1 复合益生菌成分表
Table 1 Composition of composite probiotics
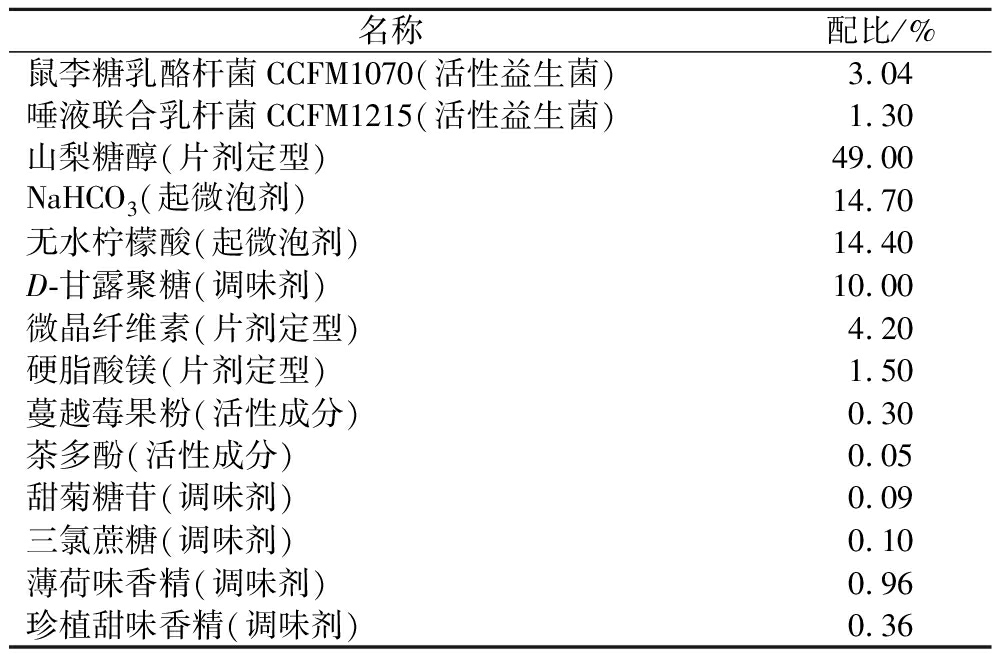
名称配比/%鼠李糖乳酪杆菌CCFM1070(活性益生菌)3.04唾液联合乳杆菌CCFM1215(活性益生菌)1.30山梨糖醇(片剂定型)49.00NaHCO3(起微泡剂)14.70无水柠檬酸(起微泡剂)14.40D-甘露聚糖(调味剂)10.00微晶纤维素(片剂定型)4.20硬脂酸镁(片剂定型)1.50蔓越莓果粉(活性成分)0.30茶多酚(活性成分)0.05甜菊糖苷(调味剂)0.09三氯蔗糖(调味剂)0.10薄荷味香精(调味剂)0.96珍植甜味香精(调味剂)0.36
1.2 实验材料与试剂
0.2 g/L洗必泰(氯己定)、蔗糖、无水乙醇,国药集团化学试剂有限公司;紫脲酸铵,上海生工生物工程股份有限公司;脑心浸液(brain heart infusion,BHI)培养基、BIGGY培养基、甘露醇氯化钠琼脂(mannitol salt agar,MSA)培养基、亚碲酸钾,青岛海博生物科技有限公司;异氟烷,上海博飞美科化学科技有限公司。
1 mL一次性注射器,无锡市宇寿医疗器械有限公司;一次性无菌棉拭子,深圳市东之星医疗科技有限公司;15 C手术刀,英国Swann-Morton公司。
1.3 培养基
BHI培养基(g/L):BHI培养基成品38.5,115 ℃高压灭菌20 min;用于变异链球菌的分离和培养。
MSA培养基(g/L):MSA培养基成品236, 115 ℃高压灭菌20 min,用于变异链球菌的计数。
YPD培养基(g/L):葡萄糖20、蛋白胨20、酵母粉10,115 ℃高压灭菌20 min,用于白色念珠菌的分离和培养。
BIGGY培养基:称取成品45.0 g,加热搅拌溶解于1 000 mL蒸馏水中,煮沸不要超过1 min,用于白色念珠菌的计数。
1.4 实验动物与饲料
3周龄SPF级Wistar雄性大鼠30只,体重60~80 g,北京维通利华实验动物技术有限公司,生产许可证号SCXK(京)2012-0001。动物实验方案获得江苏省血吸虫病防治研究所伦理委员会批准(伦理批号为IACUC-JIPD-2023-117)。致龋饲料Diet 2000,南通特洛菲饲料科技有限公司。
1.5 实验仪器与设备
CLS 100X型体视显微镜,徕卡(新加坡)公司;Quantum GX型小动物活体成像系统,美国Perkin Elmer公司;Sorvall MX120 +型超高速离心机,美国Thermo Fisher公司;MCB-900V型超净工作台,中科美菱低温科技股份有限公司;GR60DA型高温高压灭菌锅,美国ZEALWAY公司;SHP-250型生化培养箱,上海森信实验仪器有限公司。
1.6 实验方法
1.6.1 实验菌株准备
变异链球菌:将保存于甘油管中的变异链球菌于BHI固体培养基上划线活化,挑取单菌落接种于BHI液体培养基中,37 ℃培养24 h,活化2代后,将其浓度调整为1×108 CFU/mL。
白色念珠菌:将保存于甘油管中的白色念珠菌于YPD固体培养基上划线活化,挑取单菌落接种于YPD液体培养基中,37 ℃培养24 h,活化2代后,调整浓度为1×107 CFU/mL。
1.6.2 动物实验设计
大鼠首先喂食常规饲料3 d以适应新环境。为防止内源性微生物的影响,所有大鼠连续4 d喂食含有125 mg/L氨苄西林的水和普通饲料,随后,将大鼠随机分为5组:空白组、模型组、洗必泰组、辅料组及复合益生菌组,每组6只。整个实验周期共42 d,实验流程见图1。
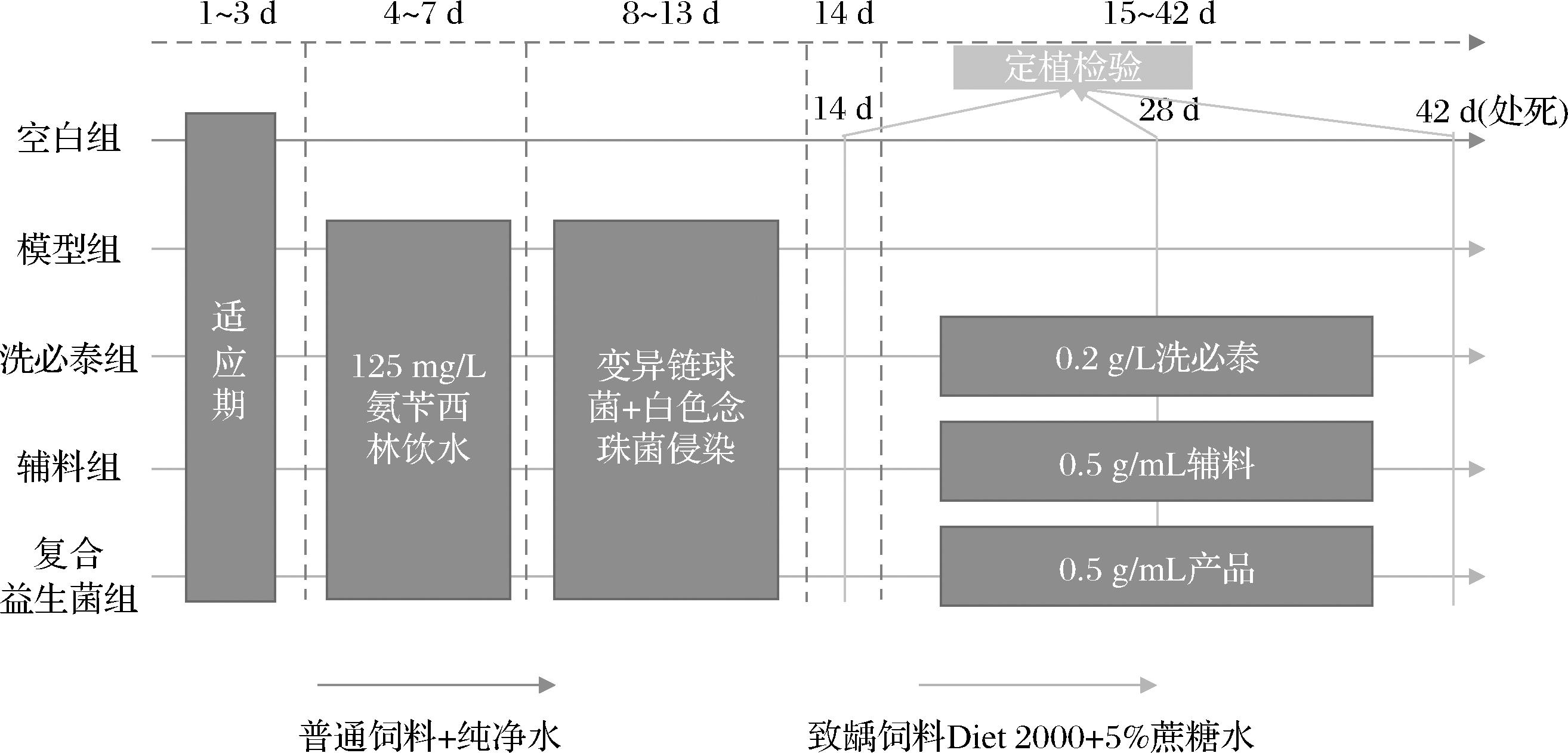
图1 实验流程图
Fig.1 Experimental flowchart
第8天开始,空白组饲喂普通饲料和纯净水,其余组大鼠均饲喂致龋饲料Diet 2000和50 g/L蔗糖水。除空白组外,其余组别于第8~13天连续6 d侵染变异链球菌和白色念珠菌,操作方法根据ZHANG等[16]的方式进行修改:使用无菌注射器分别吸取变异链球菌(108 CFU/mL)和白色念珠菌(107 CFU/mL)的菌悬液各1 mL,先后对大鼠两侧磨牙进行缓慢冲洗,并禁食禁水0.5 h[17],以避免食物或水对细菌的机械性清除,从而促进细菌在牙齿表面的黏附与定植。实验第14天用无菌棉拭子采集口腔唾液样本,以确认变异链球菌和白色念珠菌在口腔中定植。模型组除采样外不做任何处理直至实验结束。
洗必泰组、辅料组及复合益生菌组在实验第8~14天与模型组步骤相同。从第15天开始,连续4周,每周5次分别用0.2 g/L的洗必泰、0.5 g/mL辅料以及0.5 g/mL复合益生菌冲牙。干预2周(实验第28天)和干预4周(实验第42天)后用无菌棉拭子采集口腔唾液样本,进行致病菌定植检验。
1.6.3 大鼠体重测定
实验期间,每周对大鼠进行称重,比较各组大鼠生长情况。
1.6.4 大鼠口腔致病菌计数
实验期间共采集3次唾液样本:第一次取样在第14天,即致病菌干预结束时,作为致龋菌的定植检验;第二次取样在实验干预2周后,即实验第28天;第3次取样在实验干预4周后,即第42天(大鼠处死前)。用无菌棉拭子在大鼠牙面来回旋转获取唾液样本,将拭子保存于1 mL生理盐水中,而后将含有唾液样本的生理盐水进行梯度稀释并使用倾注平板法进行活菌计数。该实验操作在4 h内完成。活菌计数共用到2种固体平板,变异链球菌的计数使用添加了10 mg/L亚碲酸钾的MSA培养基,白色念珠菌的计数用BIGGY平板。
1.6.5 大鼠牙釉质体积测定
实验结束后,异氟烷麻醉大鼠并处死,分离大鼠下颌骨,剔除颌骨周围所有软组织,在体积分数10%多聚甲醛中浸泡72 h,取出清洗晾干。将大鼠上颌骨样本使用Micro-CT影像系统进行X射线扫描成像,具体方法为:在90 kV、88 μA下,以18 μm/像素的分辨率,通过360°的旋转,曝光时间240 ms进行扫描[18]。使用Skyscan CT-analyzer软件重建下颌骨的三维图像,以固定阈值将牙釉质与下颌骨分离并计算牙釉质的体积。
1.6.6 大鼠龋齿评分
将大鼠磨牙浸泡于4 g/L紫脲酸铵染液中,12 h后取出,用清水洗净并晾干,用超薄金刚砂片将磨牙纵向切为两半,在体视显微镜下观察大鼠磨牙龋损情况,采用Keyes评分对龋齿进行打分[19]。
1.7 统计分析
采用SPSS 25.0 软件对数据进行统计学分析。各组间的显著性差异采用Duncan检验进行单因素方差分析;采用Graphpad Prism 8.0软件进行绘图。结果表示为”平均值±标准误差”。
2 结果与讨论
2.1 大鼠体重
如图2所示,整个实验期间各组大鼠体重稳步增长,模型组与各干预组大鼠体重增长量均无统计学差异,说明益生菌干预不会影响大鼠体重。
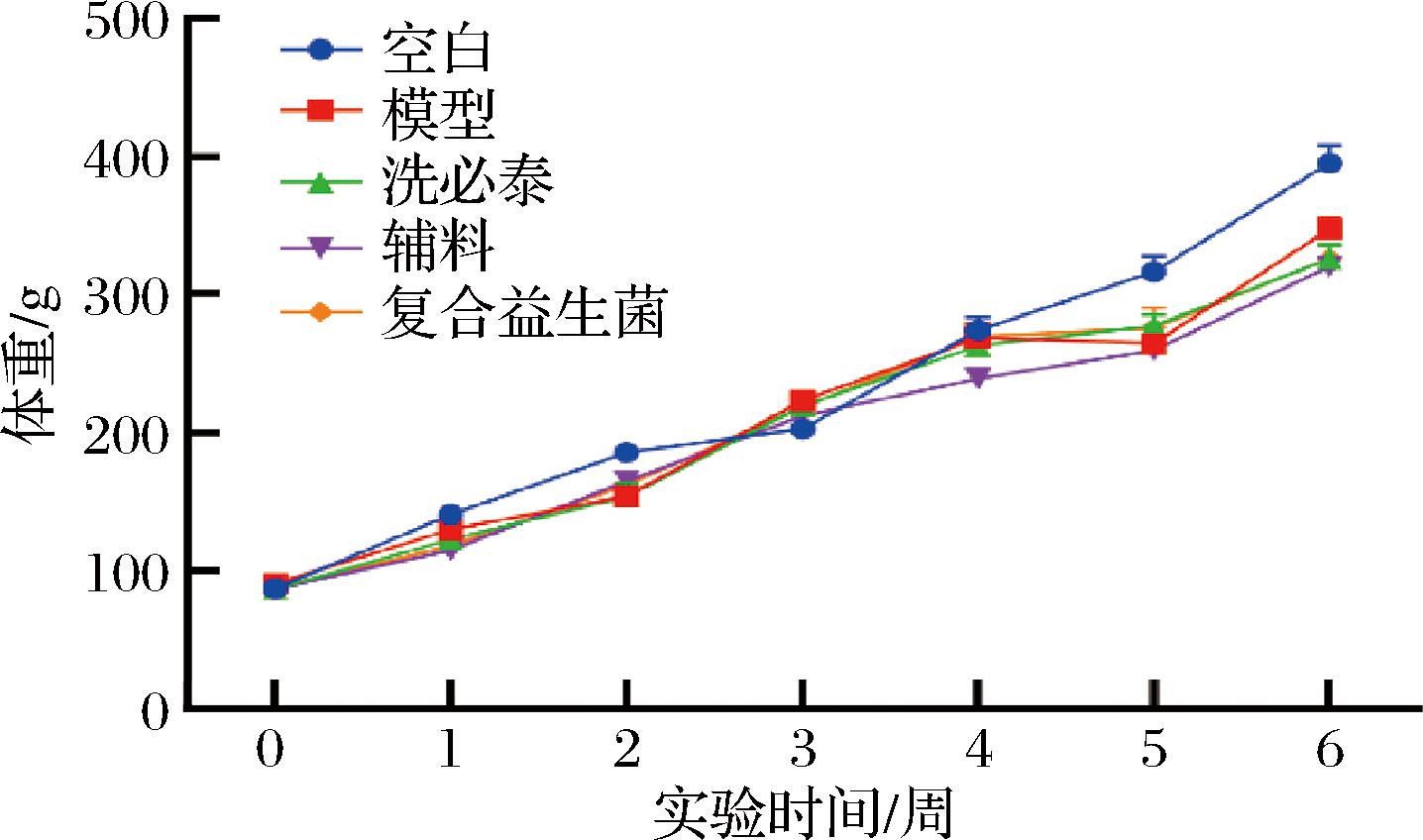
图2 大鼠体重变化
Fig.2 Changes in body weight of rats
2.2 大鼠口腔中致病菌数量变化
实验期间,共进行了3次口腔唾液采样,对变异链球菌及白色念珠菌进行了计数,结果如图3所示。在3次计数中,空白组均未检测到变异链球菌和白色念珠菌存在。
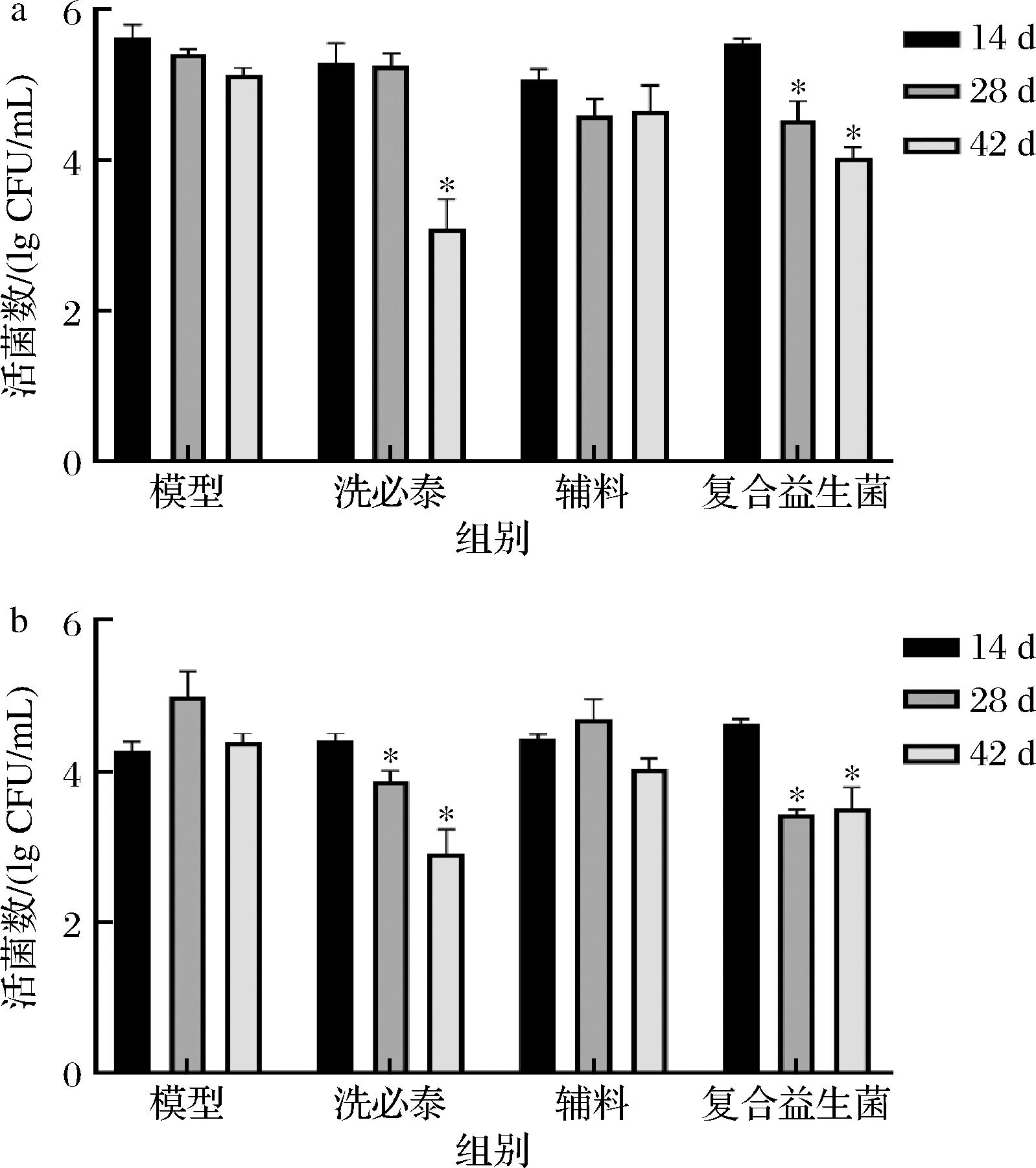
a-变异链球菌;b-白色念珠菌
图3 大鼠口腔中变异链球菌和白色念珠菌数量变化
Fig.3 Changes in the quantity of Streptococcus mutans and Candida albicans in the oral cavity of rats
注:*为与14 d相比差异显著(P<0.05)。
致龋菌侵染口腔结束后(实验第14天),各组大鼠口腔内变异链球菌的数量均在5.00 lg CFU/mL以上,且模型组全程活菌数保持在5.00 lg CFU/mL以上,说明该菌在大鼠口腔内定植成功。洗必泰干预2周后(28 d),变异链球菌数量没有显著变化,但是干预4周后(42 d),显著下降至(3.08±0.40) lg CFU/mL(P<0.05),说明洗必泰需要较长时间的干预才能抑制大鼠口腔内的变异链球菌的生长。洗必泰会改变细菌渗透压释放细胞质组分,高浓度的洗必泰可在短期内产生较好的杀菌效果[20],而本研究中使用较低浓度的洗必泰(0.02%),因而抑菌效果的发挥比较缓慢。复合益生菌组在干预2周后,变异链球菌数量由(5.55±0.06) lg CFU/mL降低至(4.53±0.25) lg CFU/mL(P<0.05),干预4周后,进一步降低至(4.03±0.14) lg CFU/mL(P<0.05)。这说明本研究使用的复合益生菌可在短期内对口腔致病菌进行一定程度的抑制,并且可以发挥长效抑制作用。这种抑菌效应可能源于益生菌的多重作用机制:初期(干预2周)的快速抑制可能主要源于鼠李糖乳酪杆菌分泌抑菌物质(如抗菌肽)对变异链球菌活性的直接抑制[12],同时通过分泌生物表面活性剂破坏其生物膜三维结构[21],此外,唾液联合乳杆菌可以靶向抑制磷酸烯醇式丙酮酸磷酸转移酶系统以及2个ATP结合转运蛋白功能来减少变异链球菌生物膜的形成[13];随着干预时间延长至4周,益生菌通过占据口腔黏膜黏附位点、竞争性消耗唾液中的必需营养物质(如葡萄糖和氨基酸)形成生态位优势[22],同时调节口腔微生物群落平衡,并激活宿主免疫应答,最终通过生态调控与免疫协同途径实现长效抑菌效果[23]。本研究使用的辅料对变异链球菌数量没有显著影响。
对白色念珠菌的计数结果显示,致病菌侵染结束后(第14天),各组白色念珠菌数量均在4.50 lg CFU/mL左右,且模型组中该菌的数量在实验全程未降低,说明该菌在大鼠口腔内定植成功。经过干预后,洗必泰组和复合益生菌组白色念珠菌出现数量级下降。其中,洗必泰组表现为稳步下降趋势,在致病菌冲洗结束时(14 d),白色念珠菌数量为(4.41±0.09) lg CFU/mL,干预2周后(28 d)下降到(3.87±0.13) lg CFU/mL(P<0.05),干预4周后(42 d)下降至(2.91±0.32) lg CFU/mL(P<0.05),这说明使用0.02%的洗必泰后可以在短期内抑制白色念珠菌的增殖,且长效抑制作用较好。复合益生菌组在干预2周后(28 d),白色念珠菌数量由(4.62±0.07) lg CFU/mL下降至(3.42±0.07) lg CFU/mL(P<0.05),但是在干预4周后(42 d),该菌的数量没有出现进一步下降。此现象可能反映益生菌-真菌的微生态博弈:在干预初期,益生菌可以通过代谢产物(如短链脂肪酸)降低局部pH从而抑制白色念珠菌毒力因子,也可以干扰白色念珠菌生物膜发育和菌丝分化[24];在干预后期,白色念珠菌通过上调应激响应基因(如CAP1、MRR1)增强耐药性[25],而益生菌通过激活宿主固有免疫实现持续调控。这种动态平衡提示益生菌可能更适用于预防性干预而非根治性治疗。辅料组的白色念珠菌数量无显著变化。
2.3 大鼠牙釉质体积分析
牙菌斑中的致龋菌会通过代谢食物残渣中的可发酵碳水化合物(如糖)产酸,降低局部pH值,溶解并破坏牙釉质和牙本质中的矿物质,引发龋齿[26]。因此,牙釉质体积与龋损程度呈负相关。Micro-CT扫描技术可以根据组织的密度,使用不同的密度阈值来分割每个组织。利用这种方法,我们将大鼠下颌骨进行三维重建,以固定阈值将牙釉质与牙本质分离,从而计算牙釉质体积以评估龋齿的严重程度。
从下颌骨的3D重建图(图4-A)中可以看到,空白组牙釉质完整,无龋洞;模型组存在釉质缺失情况,有较大龋洞。经过洗必泰或复合益生菌干预后,牙釉质损失程度减轻,尤其是复合益生菌组,从剥离的牙釉质图来看,其完整度与空白组无异。
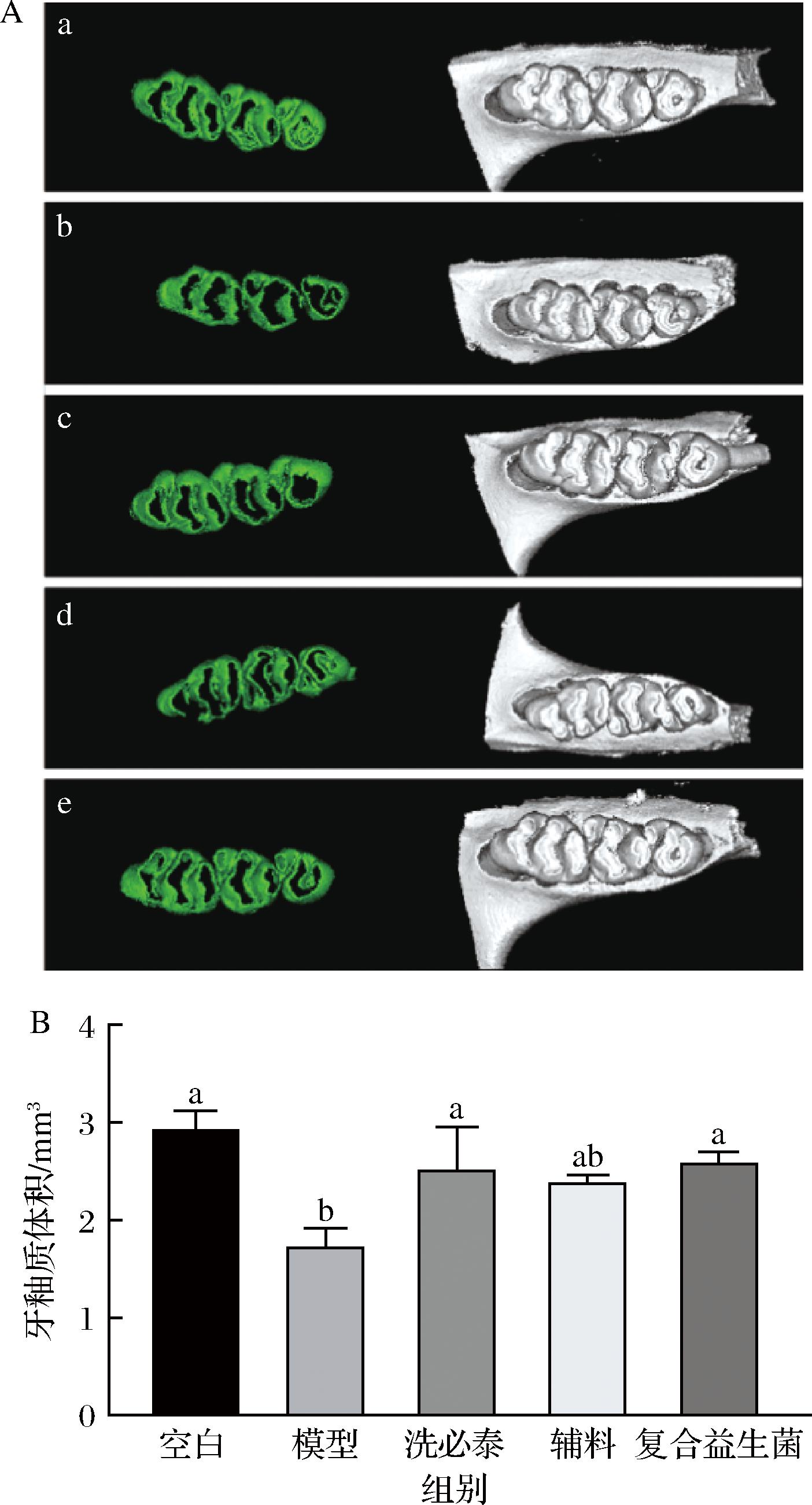
A-三维重建图;B-牙釉质体积
图4 大鼠磨牙的三维重建图及牙釉质体积
Fig.4 The 3D reconstruction image of the rat’s molar and the volume of enamel
注:A图中a-空白组;b-模型组;c-洗必泰组;d-辅料组;e-复合益生菌组。(绿色为牙釉质)B图中不同小写字母表示有显著性差异(P<0.05)(下同)。
对牙釉质体积进行定量分析(图4-B),空白组牙釉质体积为(2.93±0.19) mm3,而模型组牙釉质体积显著降低至(1.75±0.17) mm3(P<0.05),说明龋齿模型建立成功。经过干预后,洗必泰组和复合益生菌组牙釉质体积都显著升高,分别为(2.54±0.42) mm3和(2.61±0.09) mm3(P<0.05)。郑志瑶等[27]使用发酵粘液乳杆菌和洗必泰干预龋齿大鼠时,发现益生菌组大鼠牙釉质体积显著增加,而洗必泰组牙釉质体积没有显著变化。复合益生菌组牙釉质体积的升高可能与益生菌的多重保护机制有关,一方面通过产生抗菌物质与致龋菌竞争黏附位点从而减少致龋菌的定植,另一方面其代谢产物可调节口腔pH值并促进钙磷沉积[28]。近期研究发现,鼠李糖乳酪杆菌[12]、短乳杆菌[29]等益生菌可以增强牙釉质对脱矿的抵抗力,使钙和磷的质量百分比以及钙/磷比值恢复到基础水平。值得注意的是,本研究中洗必泰组牙釉质体积也显著增高,这可能是因为洗必泰作为广谱抗菌剂,可以通过破坏细菌细胞壁及抑制蛋白质合成来发挥抗菌作用,从而保护牙釉质[30]。本研究中辅料组牙釉质体积(2.39±0.06) mm3也有所升高,尽管与模型组的差异未达统计学显著性(P>0.05),但其体积值的升高提示辅料可能对延缓脱矿存在潜在干预效应。推测其机制可能与辅料中NaHCO3的碱性缓冲作用相关,NaHCO3可能通过中和菌斑糖酵解产生的酸,升高唾液pH,延缓脱矿。这一推论得到金燕[31]的研究支持,其研究证明NaHCO3具有增加釉质抗酸性、抑制釉质脱矿和促进脱矿釉质再矿化的作用。
2.4 大鼠龋齿评分
龋损的牙体硬组织会由于脱矿而使微小孔隙增多,可以被紫脲酸铵染色剂染成红色[32]。用体视显微镜观察染色后的大鼠牙齿,结果见图5。空白组磨牙光滑面、纵切面的窝沟及邻面均没有被染上颜色,说明空白组无龋损(图5-a)。而模型组光滑面被染成红色且面积较大,纵切面显示所有磨牙的窝沟均被染成红色,部分邻面也被染色(图5-b)。经过洗必泰和复合益生菌干预后,大鼠磨牙的光滑面、邻面及窝沟染色程度都有所下降,但是辅料组邻面及窝沟面染色程度变化不明显。
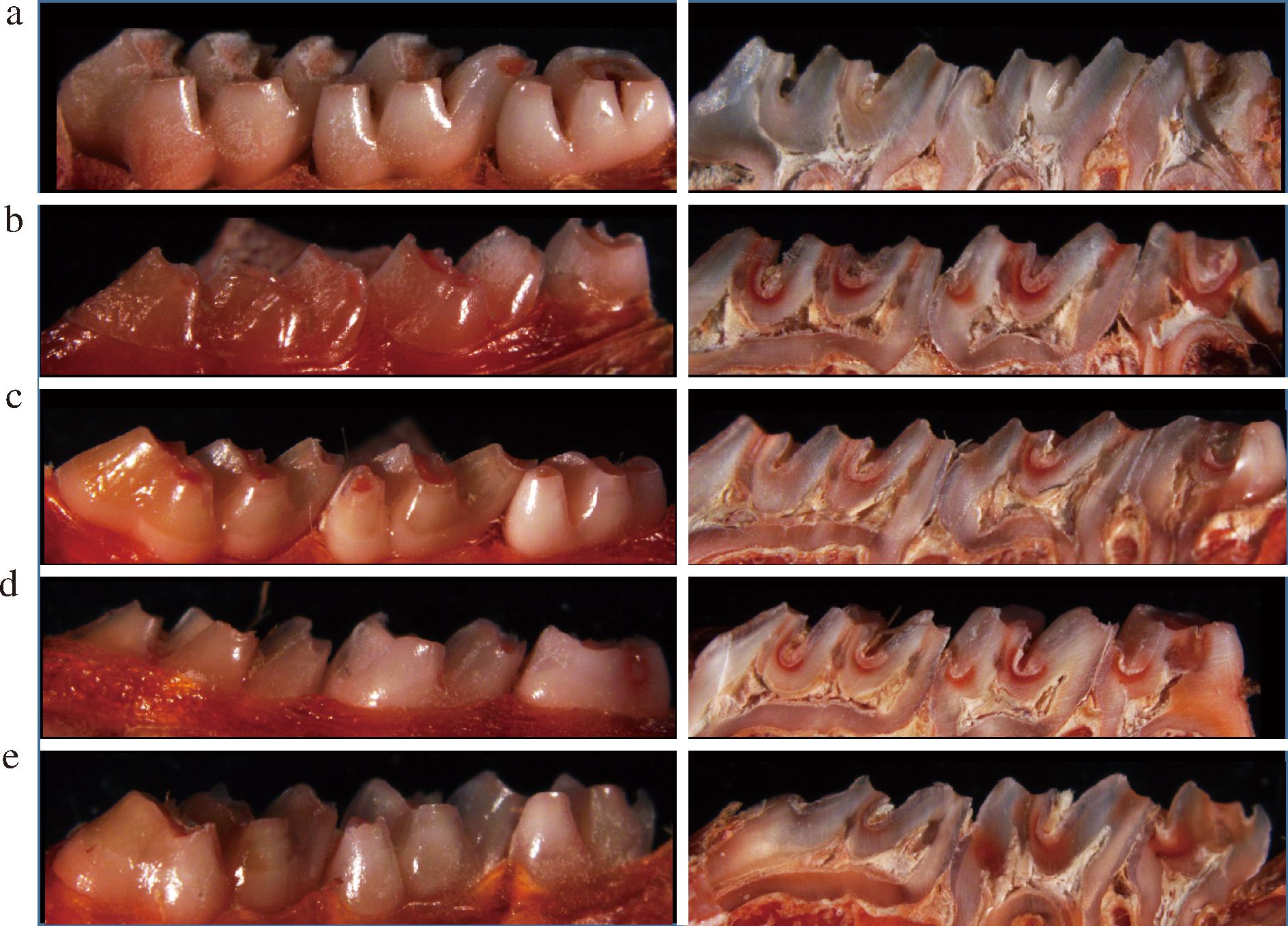
a-空白组;b-模型组;c-洗必泰组;d-辅料组;e-复合益生菌组
图5 染色后大鼠磨牙及其纵切面
Fig.5 Stained rat molars and their cross-sections
Keyes评分法将龋齿病变分为4个等级:光滑面釉质龋(E级)、牙本质浅龋(Ds级)、牙本质中层龋(Dm级)和牙本质深层龋(Dx级)。E代表仅出现牙釉质龋损;Ds代表牙本质中有1/4的部分出现龋损,位于牙釉质与牙髓腔之间;Dm则表示1/4~3/4的牙本质出现龋损;而Dx则意味着龋齿的病变已经超过3/4的牙本质区域[19]。这一评分系统有助于对龋齿的严重程度进行量化评估,分值越高,龋损越严重。
光滑面龋齿Keyes评分见表2,窝沟面龋齿评分见表3。光滑面龋和窝沟龋总得分(E)最低的依次为复合益生菌组(12.33±1.71)、洗必泰组(14.25±2.56)、辅料组(17.83±1.56)、模型组(23.67±1.20)。其中,复合益生菌组和洗必泰组的总得分都显著低于模型组(P<0.05),说明本次研究所用复合益生菌和洗必泰都可以有效改善龋损,复合益生菌的效果更好。
表2 龋齿评分表(光滑面龋)
Table 2 The caries scores (smooth-surface caries)
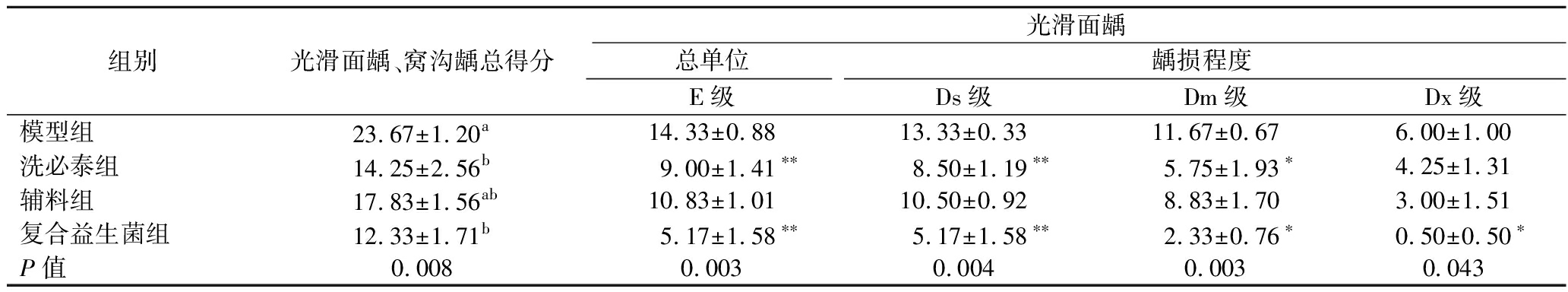
组别光滑面龋、窝沟龋总得分光滑面龋总单位龋损程度E级Ds级Dm级Dx级模型组23.67±1.20a14.33±0.8813.33±0.3311.67±0.676.00±1.00洗必泰组14.25±2.56b9.00±1.41∗∗8.50±1.19∗∗5.75±1.93∗4.25±1.31辅料组17.83±1.56ab10.83±1.0110.50±0.928.83±1.703.00±1.51复合益生菌组12.33±1.71b5.17±1.58∗∗5.17±1.58∗∗2.33±0.76∗0.50±0.50∗P值0.0080.0030.0040.0030.043
注:表中不同小写字母表示组间有显著性差异,*表示同模型组相比P<0.05,**表示同模型组相比P<0.01(下同)。
表3 龋齿评分表(窝沟龋)
Table 3 The caries scores (sulcal caries)
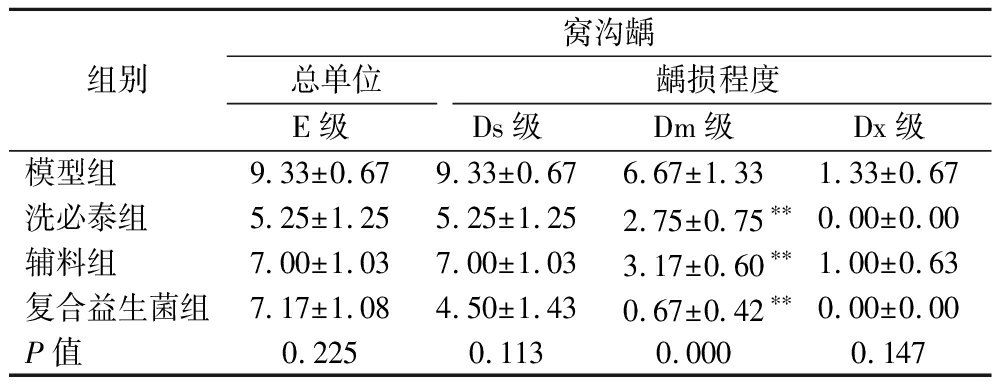
组别窝沟龋总单位龋损程度E级Ds级Dm级Dx级模型组9.33±0.679.33±0.676.67±1.331.33±0.67洗必泰组5.25±1.255.25±1.252.75±0.75∗∗0.00±0.00辅料组7.00±1.037.00±1.033.17±0.60∗∗1.00±0.63复合益生菌组7.17±1.084.50±1.430.67±0.42∗∗0.00±0.00P值0.2250.1130.0000.147
从光滑面龋的评分结果来看,复合益生菌组和洗必泰组都可以显著降低光滑面E级、Ds级和Dm级的评分,但是复合益生菌组的评分更低,而且只有复合益生菌可以显著改善Dx级的龋损,这说明洗必泰对龋损深度发展的抑制作用没有益生菌效果好。奚彧等[33]研究得到类似结果,即益生菌可显著减轻光滑面龋,且效果优于洗必泰。辅料组对光滑面龋没有显著改善效果,但是其评分也有所降低,这可能是由于辅料组中含有蔓越莓粉[34]和茶多酚[35]等成分,这些成分被证明可以防治龋齿,但是由于这些成分含量较低,所以防龋效果不明显。
从窝沟龋的评分结果来看,洗必泰、辅料及复合益生菌可以降低E级、Ds级的评分,但是与模型组相比没有显著差异,说明它们对窝沟浅龋的改善的作用不大。但是洗必泰、辅料和复合益生菌都可以显著降低窝沟Dm级龋的发生,其中效果最好的是复合益生菌组,评分从(6.67±1.33)降低至(0.67±0.42)(P<0.01)。说明这3种物质在阻止窝沟龋的深层发展均有一定效果,复合益生菌的效果最好。CHEN等[12]也观察到类似的结果,鼠李糖乳酪杆菌可以减少矿物质流失,从而使大鼠牙本质Dm级龋严重程度显著降低。
以上结果说明,本复合益生菌可以延缓光滑面龋和窝沟龋的发生发展。这可能是鼠李糖乳酪杆菌和唾液联合乳杆菌可以在口腔内定植,从而共聚集致龋菌,并且通过下调负责生物膜生成的gftB及gtfC等基因的表达,减少病原菌生物膜胞外多糖的合成,使生物膜更松散、多孔,进而延缓龋齿的发生和发展[36]。
3 结论
本研究通过建立大鼠龋齿模型,发现由鼠李糖乳酪杆菌CCFM1070和唾液联合乳杆菌CCFM1215组成的复合益生菌可以显著降低大鼠口腔中变异链球菌和白色念珠菌的数量,减少牙釉质的损失,并且降低光滑面各级龋齿评分及窝沟面中层龋的评分,说明该复合益生菌对龋齿的改善有积极作用,可以作为龋齿预防及辅助治疗手段。
[1] MATHUR V P, DHILLON J K.Dental caries:A disease which needs attention[J].The Indian Journal of Pediatrics, 2018, 85(3):202-206.
[2] 高文佳, 谢元栋, 李春望, 等.变异链球菌与口腔致龋微生物相互作用的研究进展[J].国际老年医学杂志, 2024, 45(2):242-246.
GAO W J, XIE Y D, LI C W, et al.Recent advances in research on interactions between Streptococcus mutans and oral cariogenic microorganisms[J].International Journal of Geriatrics, 2024, 45(2):242-246.
[3] 陈冬茹, 林焕彩.变异链球菌致龋机制研究新进展[J].四川大学学报(医学版), 2022, 53(2):208-213.
CHEN D R, LIN H C.Research updates:Cariogenic mechanism of Streptococcus mutans[J].Journal of Sichuan University (Medical Sciences), 2022, 53(2):208-213.
[4] THAYUMANAVAN T, HARISH B S, SUBASHKUMAR R, et al.Streptococcus mutans biofilms in the establishment of dental caries:A review[J].3 Biotech, 2025, 15(3):62.
[5] SCHULZ M N, ANSARI F, HOSSAIN H, et al.Verleichende PCR-typisierung von Candida albicans aus der mundhöhle und dem magen-darm trakt[J].Oralprophylaxe &Kinderzahnheilkunde, 2005, 27:139-143.
[6] EV L D, DAMÉ-TEIXEIRA N, DO T, et al.The role of Candida albicans in root caries biofilms:An RNA-seq analysis[J].Journal of Applied Oral Science, 2020, 28:e20190578.
[7] 吴冠希, 聂华, 朱雅男.口腔致龋生物膜中白色念珠菌与变异链球菌交互作用机制研究进展[J].北京口腔医学, 2023, 31(6):440-443.
WU G X, NIE H, ZHU Y N.Research progress on the interaction mechanism between Candida albicans and Streptococcus mutans in oral cariogenic biofilm[J].Beijing Journal of Stomatology, 2023, 31(6):440-443.
[8] 张倩霞, 王胜朝.益生菌与口腔微生态调控的研究进展[J].微生物学通报, 2021, 48(6):2195-2202.
ZHANG Q X, WANG S C.Probiotics and regulation of oral microecology:A review[J].Microbiology China, 2021, 48(6):2195-2202.
[9] KIM S K, GUEVARRA R B, KIM Y T, et al.Role of probiotics in human gut microbiome-associated diseases[J].Journal of Microbiology and Biotechnology, 2019, 29(9):1335-1340.
[10] 刘诚敬. 口腔微生物及益生菌对口腔疾病的防治[J].罕少疾病杂志, 2024, 31(2):1-2;8.
LIU C J.Prevention and treatment of oral diseases by oral microorganisms and probiotics[J].Journal of Rare and Uncommon Diseases, 2024, 31(2):1-2;8.
[11] HAN N N, JIA L, SU Y Y, et al.Lactobacillus reuteri extracts promoted wound healing via PI3K/AKT/β-catenin/TGFβ1 pathway[J].Stem Cell Research &Therapy, 2019, 10(1):243.
[12] CHEN Y Y, HAO Y, CHEN J, et al.Lacticaseibacillus rhamnosus inhibits the development of dental caries in rat caries model and in vitro[J].Journal of Dentistry, 2024, 149:105278.
[13] MA N, YANG W, CHEN B R, et al.Exploration of the primary antibiofilm substance and mechanism employed by Lactobacillus salivarius ATCC 11741 to inhibit biofilm of Streptococcus mutans[J].Frontiers in Cellular and Infection Microbiology, 2025, 15:1535539.
[14] YANG W, JIANG M X, CHEN B R, et al.Study the effect of Lactobacillus plantarum ATCC 14917 for caries prevention and anti-obesity[J].Frontiers in Nutrition, 2024, 11:1511660.
[15] GU M K, CHO J H, SUH J W, et al.Potential oral probiotic Lactobacillus pentosus MJM60383 inhibits Streptococcus mutans biofilm formation by inhibiting sucrose decomposition[J].Journal of Oral Microbiology, 2023, 15(1):2161179.
[16] ZHANG Q X, QIN S J, HUANG Y, et al.Inhibitory and preventive effects of Lactobacillus plantarum FB-T9 on dental caries in rats[J].Journal of Oral Microbiology, 2020, 12(1):1703883.
[17] 王晓敏, 余小琴, 刘飞.光动力疗法对大鼠龋齿模型防龋效果及牙髓组织的影响及相关机制研究[J].临床和实验医学杂志, 2021, 20(10):1051-1055.
WANG X M, YU X Q, LIU F.Effect of photodynamic therapy on caries prevention and pulp tissue of rat dental caries model[J].Journal of Clinical and Experimental Medicine, 2021, 20(10):1051-1055.
[18] GASQUE K C S, FOSTER B L, KUSS P, et al.Improvement of the skeletal and dental hypophosphatasia phenotype in Alpl-/- mice by administration of soluble (non-targeted) chimeric alkaline phosphatase[J].Bone, 2015, 72:137-147.
[19] KEYES P H.Dental caries in the molar teeth of rats:II.A method for diagnosing and scoring several types of lesions simultaneously[J].Journal of Dental Research, 1958, 37(6):1088-1099.
[20] ZOU X Y, ZHENG X, LIANG Y H, et al.Expert consensus on irrigation and intracanal medication in root canal therapy[J].International Journal of Oral Science, 2024, 16:23.
[21] JUNG H Y, CAI J N, YOO S C, et al.Collagen peptide in a combinatorial treatment with Lactobacillus rhamnosus inhibits the cariogenic properties of Streptococcus mutans:An in vitro study[J].International Journal of Molecular Sciences, 2022, 23(3):1860.
[22] LUO S C, WEI S M, LUO X T, et al.How probiotics, prebiotics, synbiotics, and postbiotics prevent dental caries:An oral microbiota perspective[J].NPJ Biofilms and Microbiomes, 2024, 10(1):14.
[23] ZHU Y M, WANG Y, ZHANG S Y, et al.Association of polymicrobial interactions with dental caries development and prevention[J].Frontiers in Microbiology, 2023, 14:1162380.
[24] 吴婧楠, 刘绍兰, 杨建勋.益生菌抗真菌作用机制研究进展[J].中国微生态学杂志, 2019, 31(1):116-118;125.
WU J N, LIU S L, YANG J X.Progress in research on the mechanisms of antifungal action of probiotics[J].Chinese Journal of Microecology, 2019, 31(1):116-118;125.
[25] 黄海, 王彦, 李莹, 等.白念珠菌的应激反应与耐药性[J].第二军医大学学报, 2010, 31(11):1239-1243.
HUANG H, WANG Y, LI Y, et al.Stress response and drug resistance of Candida albicans[J].Academic Journal of Second Military Medical University, 2010, 31(11):1239-1243.
[26] ROBERTS W E, MANGUM J E, SCHNEIDER P M.Pathophysiology of demineralization, part II:Enamel white spots, cavitated caries, and bone infection[J].Current Osteoporosis Reports, 2022, 20(1):106-119.
[27] 郑志瑶, 陈彩玲, 陈作国, 等.预防龋齿益生菌的筛选及对大鼠龋齿改善效果的评价[J].食品与发酵工业, 2025, 51(7):82-88.
ZHENG Z Y, CHEN C L, CHEN Z G, et al.Screening of probiotics for preventing dental caries and evaluating the effectiveness in improving dental caries in rats[J].Food and Fermentation Industries 2025, 51(7):82-88.
[28] ZHANG J Y, WANG Q, DUAN Z.Preventive effects of probiotics on dental caries in vitro and in vivo[J].BMC Oral Health, 2024, 24(1):915.
[29] ALTAMURA S, AUGELLO F R, ORTU E, et al.Efficacy of the probiotic L.brevis in counteracting the demineralizing process of the tooth enamel surface:Results from an in vitro study[J].Biomolecules, 2024, 14(5):605.
[30] KODGI V, SHETTY P, THIMMAIAH C, et al.Comparative assessment of antimicrobial activity of propolis and chlorhexidine on salivary isolates of Candida albicans and Streptococcus mutans in children with severe early childhood caries:An in vitro study[J].International Journal of Clinical Pediatric Dentistry, 2024, 17(5):591-595.
[31] 金燕. 碳酸氢钠溶液对人牙釉质抗酸性及早期龋再矿化作用的实验研究[D].南昌:南昌大学, 2003.
JIN Y.The effect of sodium bicarbonate solution on the acidresistance of human enamel and remineralizationof early caries:An in vitro study[D].Nanchang:Nanchang University, 2003.
[32] 曹茜茜, 叶倩琳, 周立波, 等.人参皂苷Rh2抑制致龋菌生物膜的实验研究[J].口腔医学研究, 2018, 34(12):1302-1306.
CAO Q Q, YE Q L, ZHOU L B, et al.Study on inhibitory effect of ginsenoside Rh2 on cariogenic bacteria biofilms[J].Journal of Oral Science Research, 2018, 34(12):1302-1306.
[33] 奚彧, 董权锋, 张秋香, 等.益生菌组合物对大鼠龋齿的预防作用[J].中国微生态学杂志, 2022, 34(11):1306-1313;1319.
XI Y, DONG Q F, ZHANG Q X, et al.Preventory effect of probiotics combination on rat dental caries[J].Chinese Journal of Microecology, 2022, 34(11):1306-1313;1319.
[34] 刘小涵, 王远亮.蔓越莓中的植物化合物及其抑菌机理研究进展[J].食品与机械, 2020, 36(11):202-205;210.
LIU X H, WANG Y L.Progress on phytochemicals and antimicrobial mechanism of cranberry[J].Food &Machinery, 2020, 36(11):202-205;210.
[35] MELOK A L, LEE L H, MOHAMED YUSSOF S A, et al.Green tea polyphenol epigallocatechin-3-gallate-stearate inhibits the growth of Streptococcus mutans:A promising new approach in caries prevention[J].Dentistry Journal, 2018, 6(3):38.
[36] BRETZ W A, CORBY P M A, HART T C, et al.Dental caries and microbial acid production in twins[J].Caries Research, 2005, 39(3):168-172.