贻贝足丝蛋白(mussel foot protein,Mfp)在海洋贻贝足丝腺中产生并贮存,使贻贝能够在水生环境中黏附和生存,具有出色的黏附能力、防水性能和生物降解性[1]。贻贝足丝至少由20种蛋白组成,主要分为起黏附作用的黏附界面蛋白、起结构支撑和连接作用的线基质蛋白(proximal matrix thread core protein,PMTP)和胶原蛋白前体(precursor collagen,preCol),如图1-a所示。其蛋白质的分子质量范围为5(Mfp-3中)~240 kDa(preCol-D中),均具有相似的等电点(isoelectric point,pI),并含有翻译后修饰的氨基酸3,4-二羟基苯基丙氨酸(3,4-dihydroxyphenylalanine,DOPA)[2-3],这些特性增强了贻贝足丝蛋白的黏附功能[4]。由于其无毒性、无免疫原性以及具备抗氧化和抗炎特性[5-6],贻贝足丝蛋白在生物材料和化妆品领域中有巨大应用潜力[7]。
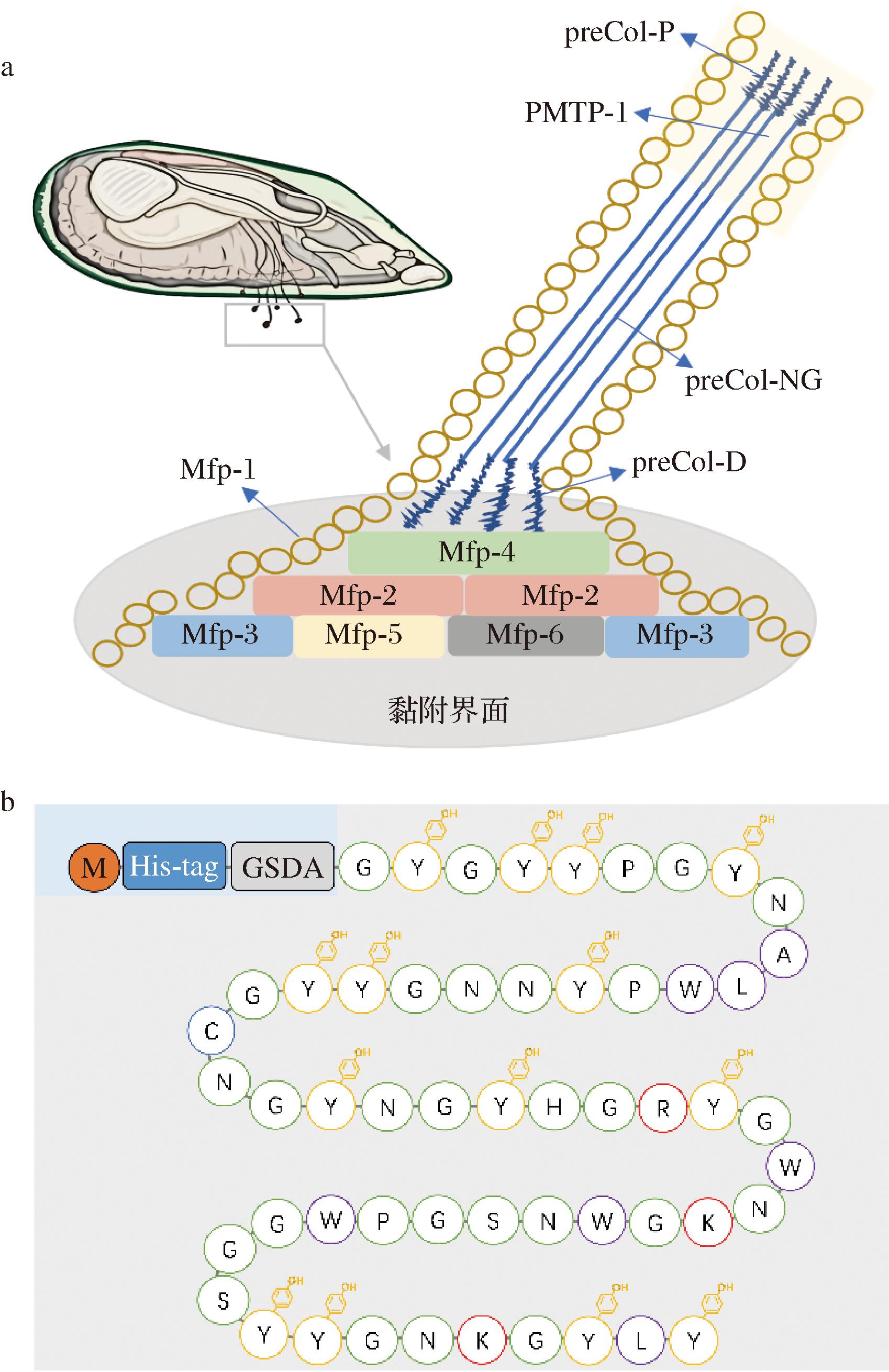
a-贻贝足丝蛋白结构示意图;b-重组表达Mcofp-3氨基酸序列示意图
图1 贻贝蛋白结构和氨基酸序列示意图
Fig.1 Schematic diagram of the structure of the mussel foot protein and amino acid sequence
注:preCol和PMTP在不同区域有不同的命名,-D、-NG、-P分别表示距离黏附界面的由近及远,PMTP-1是线基质蛋白的其中一种。
目前,贻贝足丝蛋白主要通过直接从天然贻贝组织中提取[8],该提取方法依赖贻贝原料,消耗率高,杂质多,目标产物得率低,提取1 g贻贝足丝蛋白混合物需要约10 000只贻贝,且难以分离单一类型的贻贝足丝蛋白,大大限制了贻贝足丝蛋白的广泛应用[9]。利用基因工程生产重组表达已成为获取贻贝足丝蛋白的有效的替代方法[10]。重组表达策略已在大肠杆菌(Escherichia coli)[11-12]、毕赤酵母(Pichia pastoris)[13]、酿酒酵母(Saccharomyces cerevisiae)[14]等微生物中得到了验证。相比之下,酵母作为真核表达系统,虽能进行复杂的翻译后修饰,但其生长周期较长且培养成本较高。大肠杆菌作为合成生物学中常用的模式菌株,具有生长速度快、培养条件简单、基因操作体系成熟、重组蛋白易于提取与纯化等优势。SEONG等[15]利用密码子优化策略,在大肠杆菌中重组Mgfp-5产量达50 mg/L,Mgfp-3A产量达47 mg/L[16];LEE等[17]将Mefp-1的七肽重复序列与大肠杆菌中的截短OmpA信号肽融合,表达量达到147 mg/L;袁升[18]利用融合表达策略,将贻贝蛋白与哺乳动物TDP43LC结构域蛋白质融合表达,Mgfp-5最终表达量达200.8 mg/L,是目前报道的最高水平;吕玉伟等[19]则通过优化蛋白质纯化制备条件,显著提高了蛋白产物得率水平。尽管目前已经实现了多种不同类型贻贝足丝蛋白在微生物中的重组表达,但由于表达条件不适合、表达元件不匹配以及纯化方式的复杂性,限制了贻贝足丝蛋白的工业化应用[20]。
本研究通过多种策略组合优化,实现了厚壳贻贝(Mytilus coruscus)来源的Mcofp-3在大肠杆菌中的高效重组表达。首先通过密码子优化表达,确定了Mcofp-3在大肠杆菌中以包涵体形式表达,初始产量为158.6 mg/L,离心纯化后目的蛋白占比超过85%;并对发酵培养条件进行3因素5水平的正交优化,在优化的表达条件下,重组Mcofp-3表达量达到303.3 mg/L;接着,通过载体优化、启动子及RBS工程多策略组合最终最优表达菌株产量达到484.2 mg/L。在此基础上,通过5-L发酵罐放大培养优化,在37 h后,Mcofp-3表达水平为1 720 mg/L。本研究结果实现了贻贝足丝蛋白短周期的高效生产,为其规模化工业化生产奠定了基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与质粒
本实验所有的质粒构建均在E.coli JM109菌株中进行,E.coli BL21(DE3)为贻贝足丝蛋白的表达菌株。选择商业化质粒pET-32a(+)用于扩增目的基因。菌株均由本实验室保存。
贻贝足丝蛋白编码基因Mcofp-3由生工生物工程(上海)股份有限公司合成,连接在商业化质粒pET-32a(+)上。构建得到重组质粒pET32a-Mcofp3;在上述表达贻贝足丝蛋白的质粒编码基因的N端删除促溶标签TrxA、纯化标签6*His、促溶标签S-Tag,构建得到重组质粒pET32a-ΔTag-Mcofp3。用于质粒构建的相关表达框元件及引物碱基序列分别见表1、表2。
表1 表达框优化元件碱基序列
Table 1 Expression frame optimization element base sequences

表2 引物碱基序列
Table 2 Sequence of primer bases

1.1.2 实验试剂
蛋白胨、酵母粉,美国OXIOD公司;各类氨基酸标准品、异丙基-β-D-硫代半乳糖苷(isopropyl β-D-thiogalactoside,IPTG)、硫酸卡那霉素(kanamycin,Kana)、氨苄青霉素(ampicillin,Amp)、氯霉素(chloramphenicol,Cm),上海生工生物工程公司。
1.1.3 培养基
LB培养基(g/L):酵母粉5,胰蛋白胨10,NaCl 10;LB固体培养基中需另加15 g/L琼脂粉。
TB培养基(g/L):甘油5,酵母粉12,蛋白胨24,磷酸氢二钾12.52,磷酸二氢钾2.3。
无机盐培养基(g/L):甘油10,磷酸氢二铵6,磷酸二氢钾10.5,柠檬酸1.7;灭菌锅灭菌;微量元素10 mL/L,过滤灭菌;硫酸镁1.68,单独灭菌;使用时加入。其中微量元素母液配方(g/L):五水合硫酸铜3,四水合硫酸锰0.5,四硼酸钠0.23,氯化钙2,七水合硫酸锌10,七水合硫酸亚铁5.25,七钼酸铵0.1。
1.2 仪器与设备
UV2450紫外分光光度计,日本×Shimadzu公司产品;蒸汽灭菌器,致微(厦门)公司产品;ZQTY-70台式振荡培养箱,上海知楚仪器有限公司产品;Avanti J-26XP低温高速冷冻离心机,美国Beckman公司产品;VCX750超声破碎仪,美国 Sonics 公司产品;5-L全自动发酵罐,迪必尔上海生物工程有限公司产品。
1.3 实验方法
1.3.1 摇瓶发酵
挑取平板上的单菌落,接种于5 mL液体LB培养基,于37 ℃、220 r/min过夜培养。按OD600值为0.05 接种量将种子液接种于含有50 mL摇瓶培养基(LB)的500 mL摇瓶中,37 ℃、220 r/min培养2 h,待菌体OD600值为0.6~0.8时,添加终浓度为1 mmol/L的IPTG,并继续控制温度37 ℃,摇床诱导培养6 h。发酵前,培养基中添加Amp,终质量浓度均为100 mg/L。其中,细胞菌体量测量方法:菌液稀释适当倍数后,使用分光光度计测定OD600值。发酵优化后,摇瓶培养基替换为TB培养基、转接培养1 h后诱导、IPTG浓度0.4 mmol/L;表达框优化后,抗生素替换为终质量浓度15 mg/L的Cm。
1.3.2 发酵罐发酵
发酵优化和表达框优化后,挑取单菌落接种于5 mL液体LB培养基中,37 ℃、220 r/min过夜培养。再将500 μL培养液接种于50 mL TB培养基中,37 ℃、220 r/min培养11 h。然后将200 mL种子液接种到装有2-L TB培养基的5-L发酵罐中,在37 ℃、pH值为6.9±0.1、溶氧电极参数35%左右的条件下发酵,培养菌体OD600值至10时,添加终浓度为0.4 mmol/L的IPTG诱导培养,发酵过程以455 g/L氨水控制pH。各培养过程中,添加终质量浓度为15 mg/L的Cm。定时取样检测菌体生长情况、贻贝足丝蛋白表达量。初始转速设定为220 r/min,通过调整通气量使溶氧电极参数维持在35%。随着菌体生长,耗氧量增加,通过联动控制搅拌转速和通气量,使溶氧电极参数稳定保持在35%。
1.3.3 蛋白表达与测定
设含有空白质粒pET-32a(+)的E.coli BL21(DE3)菌落作为阴性对照,培养阳性单克隆E.coli BL21-pET32a-Mcofp3至OD600值为0.6~0.8时,加入IPTG至终浓度1.0 mmol/L,诱导后继续培养6 h。6 000 r/min,8 min离心收集1.0 mL菌液细胞,使用20 mmol/L Tris-HCl洗涤重悬2次,随后冰上超声破壁。4 ℃,12 000 r/min,离心20 min,分别取上清液、沉淀,再用20 mmol/L Tris-HCl重悬沉淀。通过对上清液、重悬液SDS-PAGE分析贻贝足丝蛋白的表达情况。
当贻贝足丝蛋白以可溶形式表达,通过Ni柱亲和纯化。重组菌株发酵结束后,取菌液于4 ℃、6 000 r/min条件下离心8 min,弃上清液,留菌体。使用20 mmol/L Tris-HCl (pH值为7.5)洗涤菌体1~2次后,调节菌液浓度至OD600值为10.0,经超声或者高压匀浆破碎后,于4 ℃、12 000 r/min条件下离心20 min,保留上清液,使用0.45 μm滤膜过滤后备用,即待纯化样品。使用AKTA蛋白纯化系统进行Ni柱亲和层析。首先使用50 mL纯化液A(50 mmol/L Tris-HCl, 150 mmol/L NaCl, pH值为7.5)平衡Ni-His Trap FF柱,后进行待纯化样品上样,最后使用适当浓度的纯化液B(50 mmol/L Tris-HCl,150 mmol/L NaCl, 500 mmol/L 咪唑, pH 7.5)进行蛋白除杂和洗脱。
当贻贝足丝蛋白以包涵体形式表达,将发酵液于6 000 r/min,离心8 min后取菌体沉淀,用20 mmol/L Tris-HCl重悬,破碎细胞后,在12 000 r/min转速下离心20 min取沉淀,获得包涵体混合物。再用525 g/L乙酸重悬,低温4 ℃存放过夜。最后通过12 000 r/min,20 min离心,取上清液,获得复溶于乙酸的贻贝足丝蛋白[21]。
酸水解氨基酸分析:根据SDS-PAGE中存在的双条带,分别分析氨基酸组成。将蛋白质样品与浓盐酸(6 mol/L)混合,在110 ℃的密闭条件下水解16~24 h,使蛋白质降解为游离氨基酸。水解产物经离心或过滤去除杂质后,通过HPLC或氨基酸自动分析仪进行分离和定量[22]。
半定量测定:基于SDS-PAGE评估蛋白表达水平。通过凝胶电泳分离蛋白质后,利用图像处理软件(如Image J)测量蛋白条带的灰度值,以7.5 kDa左右特异性条带为目标,灰度值反映了蛋白的相对含量。为确保准确性,需设置已知蛋白浓度样品的灰度值作为比较基准,并且注意上样量、曝光时间等操作要素均一致[23-24]。首先,使用照胶仪在统一参数下采集SDS-PAGE蛋白胶图像。随后,利用Image J软件对采集到的图像进行灰度分析。在分析过程中,确保框选的灰度分析面积一致,并比较总灰度分析值IntDen。
全定量测定:纯化后的蛋白,使用Bradford法测蛋白浓度。分别配制1 500、1 000、750、500、250、125、0 mg/L的蛋白标准样品,依据在A595nm处吸光值不同分别测定的各个浓度下对应的吸光值,以蛋白标准样品的吸光值为横坐标,对应蛋白标准样品的浓度为纵坐标,绘制标准曲线。根据待测蛋白浓度样品的吸光值,根据上述标准曲线,可换算出对应贻贝足丝蛋白的表达量。
2 结果与分析
2.1 Mcofp-3在大肠杆菌中的重组表达
2.1.1 重组Mcofp-3的表达形式确认
将贻贝足丝蛋白Mcofp-3序列进行密码子优化后(图1-b),构建到质粒pET-32a(+)上,获得重组质粒pET32a-Mcofp3,如图2-a所示。将重组质粒化学转化至E.coli BL21(DE3)感受态细胞中,获得E.coli BL21-pET32a-Mcofp3。对上述菌株进行摇瓶发酵培养,SDS-PAGE蛋白凝胶电泳实验结果表明,E.coli BL21-pET32a-Mcofp3以可溶形式表达贻贝足丝蛋白,分子质量为24 kDa,与预测结果一致,表达量为57 mg/L,如图2-b所示。
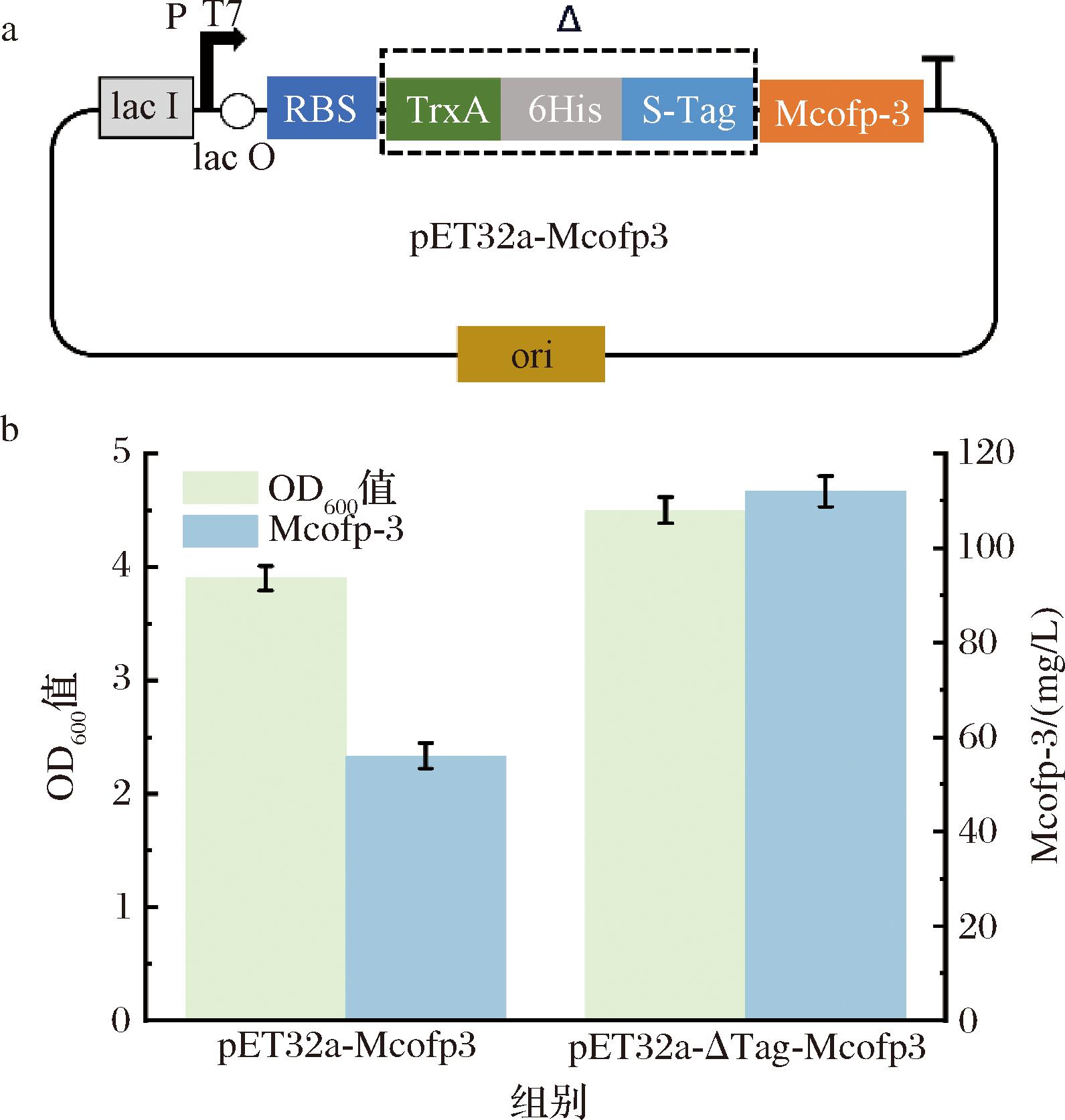
a-质粒构建示意图;b-OD600值及Mcofp-3蛋白表达量
图2 可溶表达与包涵体表达形式对比
Fig.2 Comparison of soluble expression and inclusion body expression
通过去除N端促溶标签TrxA、纯化标签6*His和促溶标签S-Tag获得贻贝足丝蛋白重组质粒pET32a-ΔTag-Mcofp3。对应重组菌株E.coli BL21-pET32a-ΔTag-Mcofp3的摇瓶发酵培养结果表明,无标签的Mcofp-3显示为包涵体表达形式,分别在7.5 kDa和15 kDa大小附近有明显的表达,与预测的单体和二聚体形式一致,测定蛋白浓度后,确定表达量为110 mg/L。贻贝足丝蛋白Mcofp-3无固定结构,在以包涵体形式表达,通过复溶复性不影响其功能,且具有离心后纯化的便捷优势,因此选择以包涵体形式表达Mcofp-3。
2.1.2 重组表达Mcofp-3单体和二聚体的鉴定
当以包涵体形式表达Mcofp-3时,SDS-PAGE蛋白凝胶电泳与空白对照相比出现双条带。查阅文献得知,可能由于氨基酸侧链参与多种非共价相互作用,部分蛋白表达会形成多聚体[2]。为了确定SDS-PAGE中显示的2个条带均为重组Mcofp-3单体和二聚体表达形式,分别将对应的蛋白条带进行胶回收后,通过酸水解测定氨基酸组成是否吻合。如图3所示,结果表明2个条带对应的蛋白质为同种氨基酸比例组合,结合分子质量大小对比,可以确定重组Mcofp-3的表达为单体和二聚体形式。其中,样品中各种氨基酸的相对含量是基于检出浓度,并以甲硫氨酸为基准(设定为1)进行比例换算得出的。由于Mcofp-3序列中仅包含一个甲硫氨酸,因此将其设定为1以便进行比例换算。
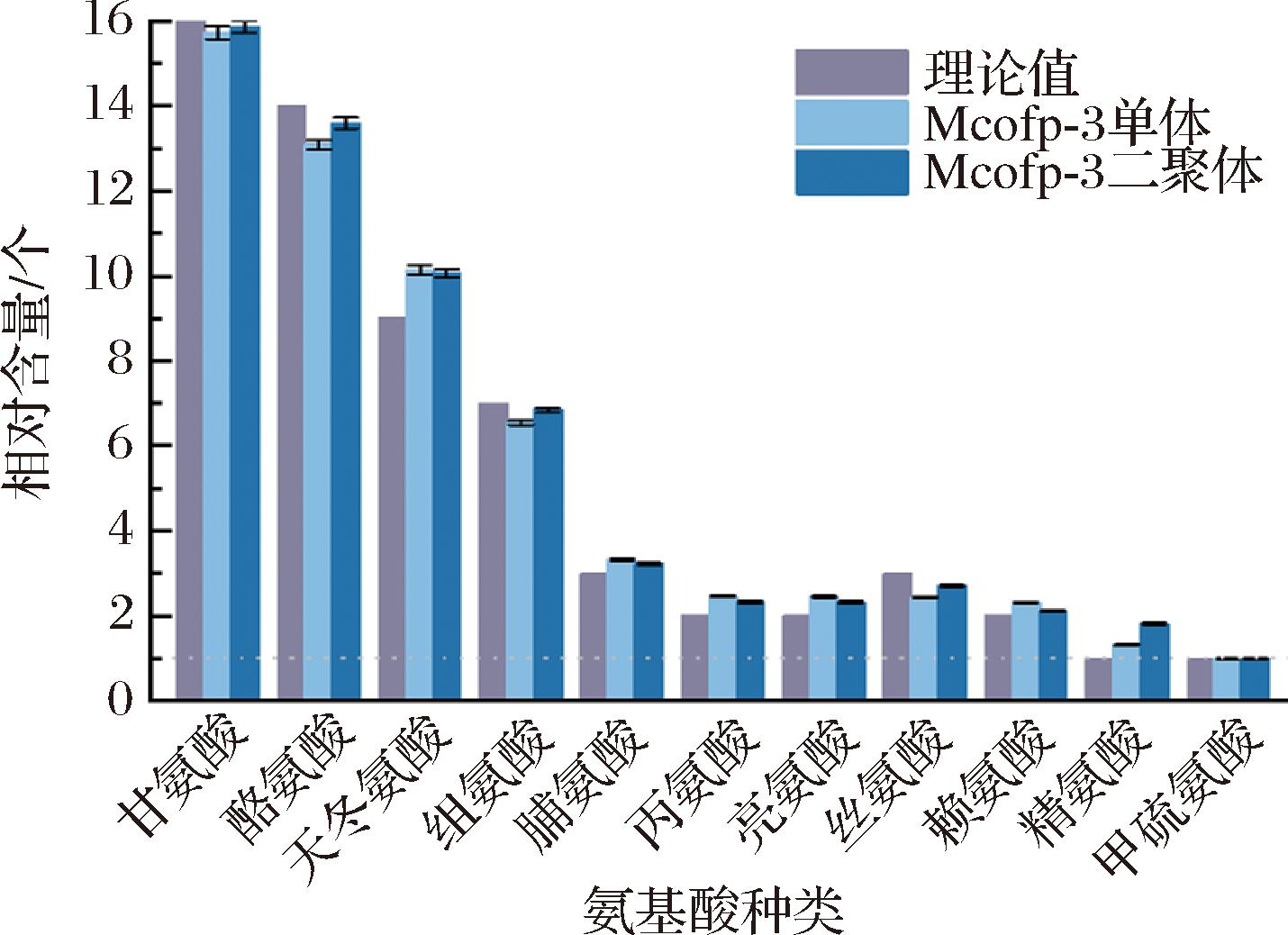
图3 酸水解氨基酸结果比对
Fig.3 Comparison of the results of acid hydrolysis of amino acids
2.1.3 重组Mcofp-3表达的分阶段取样分析
初始发酵条件为全部以LB为培养基,转接2 h后诱导,诱导剂IPTG浓度为1 mmol/L。通过定时取样进行SDS-PAGE蛋白凝胶电泳实验并进行灰度分析,在表达初期,Mcofp-3单体表达形式有较高比例,随后逐渐下降。最终结果表明,摇瓶条件下重组表达Mcofp-3在22 h表达量达到最高,为159 mg/L。此外,通过破碎菌体,在10 000 r/min,4 ℃条件下离心10 min,舍弃上清液,随后重悬后,重复以上步骤2次离心,测得离心纯化后的Mcofp-3比例在初始表达时最高,达到89.5%,第24 h时为86.4%,如图4所示。该结果表明,利用包涵体形式表达贻贝足丝蛋白可以通过简单离心获得较高纯度的重组蛋白,相比较可溶蛋白表达形式在纯化步骤上有明显优势。
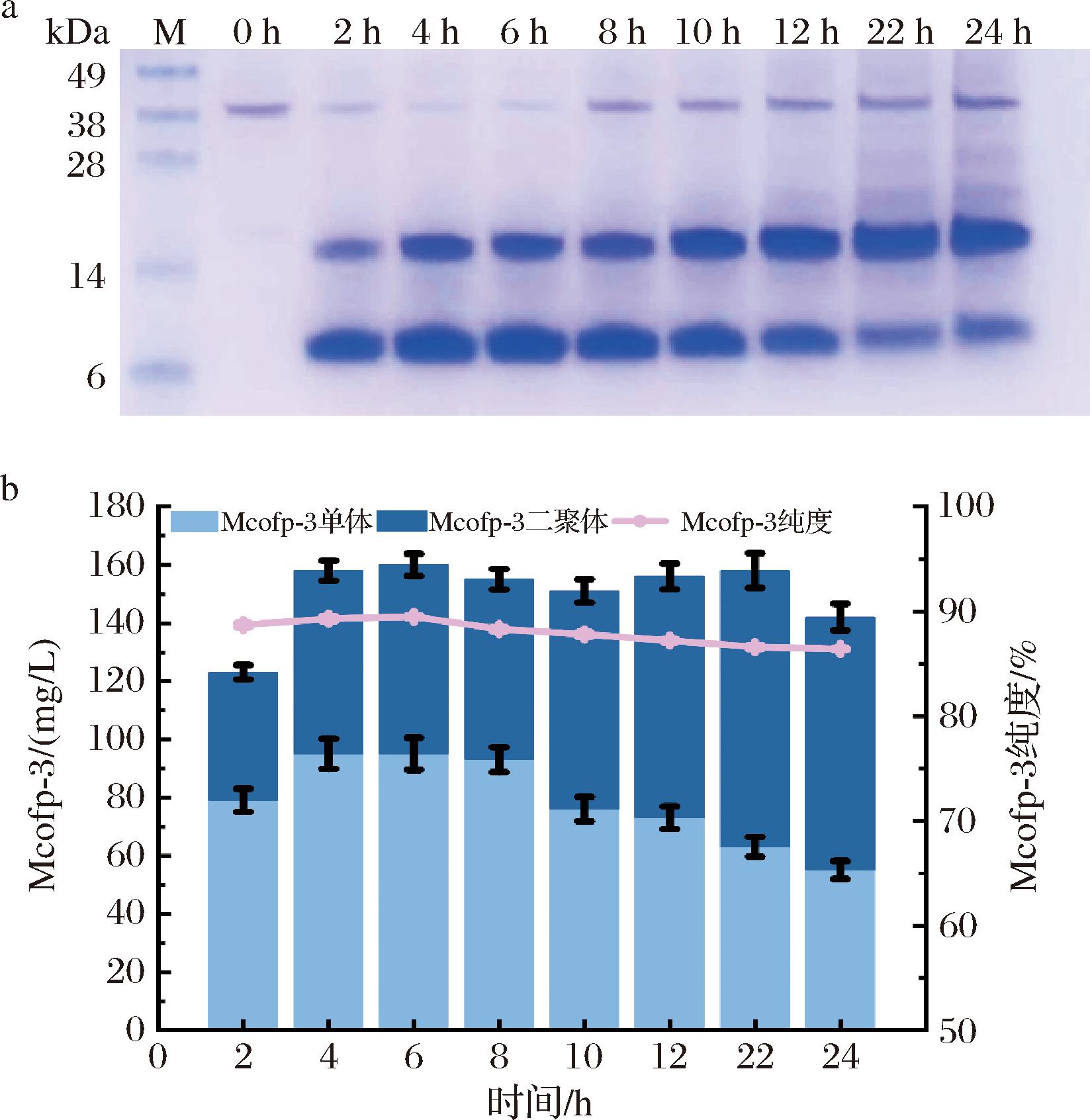
M表示Marker。
a-SDS-PAGE凝胶电泳;b-Mcofp-3蛋白表达量
图4 Mcofp-3表达情况分析
Fig.4 Analysis of Mcofp-3 expression
2.2 重组Mcofp-3表达的培养条件优化
发酵过程需要添加诱导剂IPTG诱导蛋白表达,诱导剂浓度过低,菌体表达目的蛋白强度低,诱导剂浓度过高不利于菌体正常生长和代谢。同时,诱导时机以及诱导温度都会对重组蛋白的表达有显著影响[19]。基于此,本研究拟采取正交组合诱导时间、诱导剂添加量与诱导温度的策略,制定3因素5水平混合水平正交表,L25(53),适用于3个因素5水平的实验,筛选出最优发酵参数,进而提高贻贝足丝蛋白表达量[25-26]。正交试验设计如表3所示。以单位体积发酵液破壁处理后进行SDS-PAGE蛋白凝胶电泳实验,以贻贝足丝蛋白对应条带灰度分析结果作为考察指标,使用软件Design Expert展开3因素5水平正交试验并迸行分析,分析各个因素对贻贝足丝蛋白合成的影响,结果如表4所示。
表3 正交试验设计因素及水平
Table 3 Orthogonal test design factors and levels
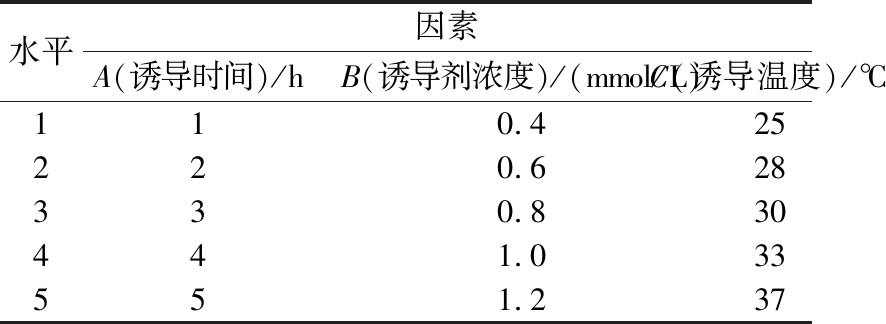
水平因素A(诱导时间)/hB(诱导剂浓度)/(mmol/L)C(诱导温度)/℃110.425220.628330.830441.033551.237
表4 正交试验结果
Table 4 Results of orthogonal tests
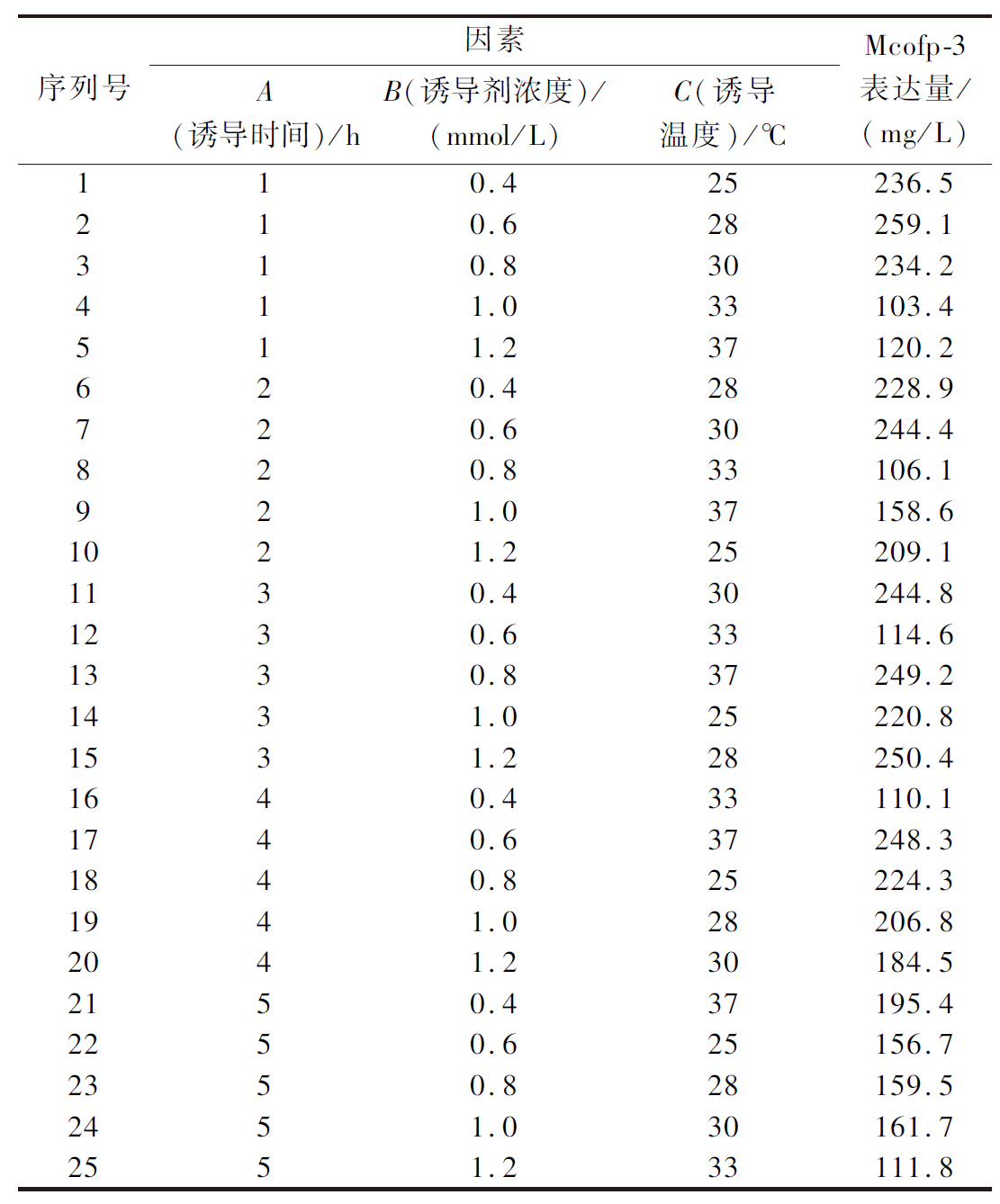
序列号因素A(诱导时间)/hB(诱导剂浓度)/(mmol/L)C(诱导温度)/℃Mcofp-3表达量/(mg/L)110.425236.5210.628259.1310.830234.2411.033103.4511.237120.2620.428228.9720.630244.4820.833106.1921.037158.61021.225209.11130.430244.81230.633114.61330.837249.21431.025220.81531.228250.41640.433110.11740.637248.31840.825224.31941.028206.82041.230184.52150.437195.42250.625156.72350.828159.52451.030161.72551.233111.8
由重组贻贝足丝蛋白表达发酵正交试验数据和极差分析(表5)可知,各因素影响的主次顺序为:诱导温度>诱导时间>诱导剂浓度(C>A>B)。在25个组合中,实验最优组合为序列号2,即控制诱导时间1 h,诱导剂浓度0.6 mmol/L,诱导温度28 ℃,Mcofp-3的表达量最高,达到259.1 mg/L,与原发酵条件下的表达量158.6 mg/L相比(序列号9:诱导时间2 h,诱导剂浓度1 mmol/L,诱导温度37 ℃),提升至1.63倍。并通过Design Expert对最优参数进行预测,预测条件为诱导时间1 h,诱导剂浓度0.4 mmol/L,诱导温度37 ℃。对正交试验筛选出的最优参数及预测参数进行重复实验,验证预测参数蛋白表达量达268.6 mg/L。
表5 正交试验极差分析
Table 5 Analysis of variance of orthogonal tests
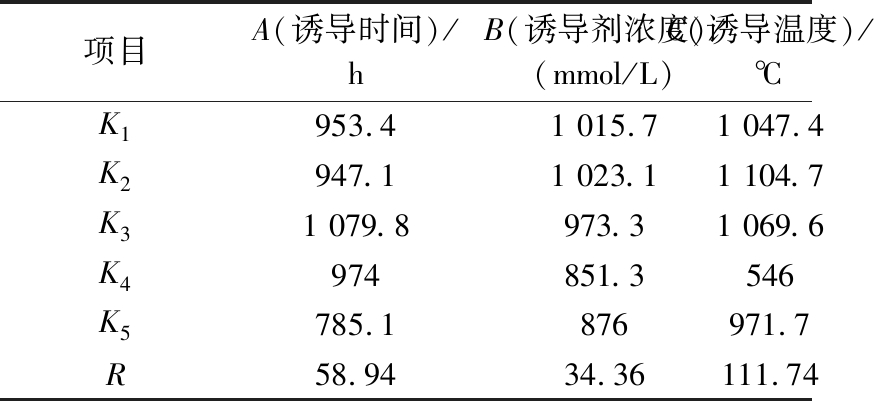
项目A(诱导时间)/hB(诱导剂浓度)/(mmol/L)C(诱导温度)/℃K1953.41 015.71 047.4K2947.11 023.11 104.7K31 079.8973.31 069.6K4974851.3546K5785.1876971.7R58.9434.36111.74
对比LB、TB、无机盐培养基条件下,菌体的生长情况及贻贝足丝蛋白表达情况。研究发现当培养基为TB时,菌体OD600值最高,同时菌体贻贝足丝蛋白表达量最高,达303.3 mg/L。因此选择把诱导时间1 h,诱导剂浓度0.4 mmol/L,诱导温度37 ℃,TB培养基作为之后发酵条件。
2.3 重组Mcofp-3表达元件的多策略组合优化
合理的表达元件组合是实现Mcofp-3的高效重组表达的关键。首先通过质粒表达重组蛋白,载体的复制子、启动子、RBS等表达元件通过调控目的基因的拷贝数、转录和翻译速率,从而最终影响目的蛋白的表达量[10]。初始使用的质粒载体为pET-32a(+)构建系统,采用T7启动子进行启动,初始RBS (https://www.denovodna.com)网站计算为25 455 au[27-28]。接下来,通过逐步替换不同梯度强度的复制子(表达框)、启动子和RBS元件,筛选出最优组合,以期提高Mcofp-3的最终表达量(图5)。
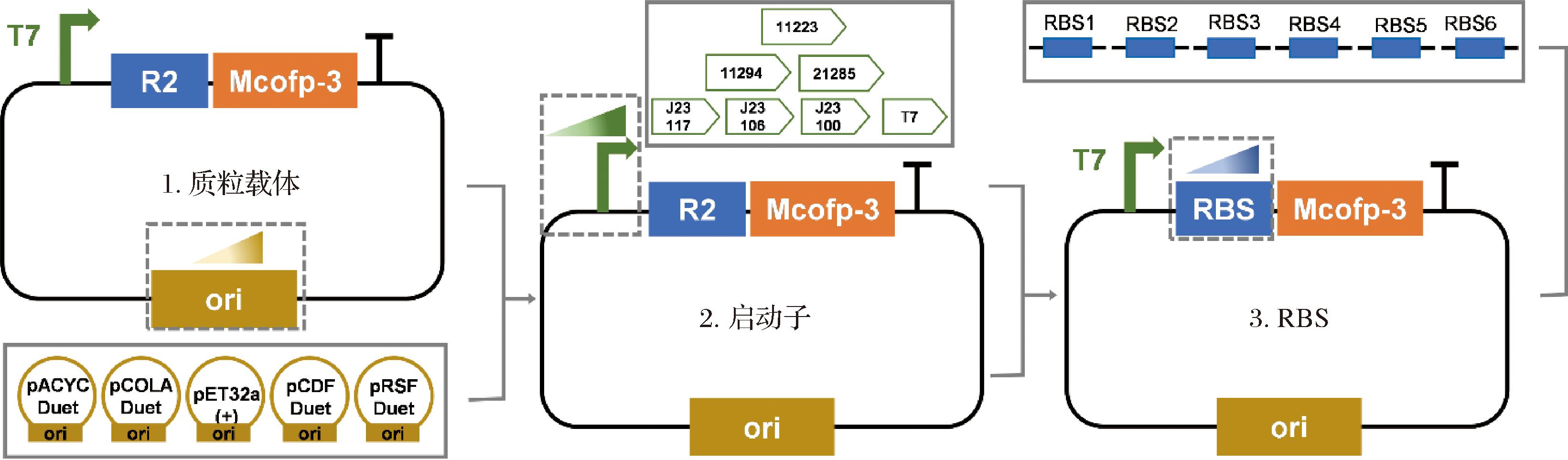
图5 表达框元件优化策略示意图
Fig.5 Schematic representation of the optimization strategy for expression frame components
2.3.1 重组Mcofp-3表达载体筛选优化
不同质粒载体拷贝数不同,从而影响目的蛋白表达水平。选择不同拷贝数载体表达Mcofp-3,拷贝数由低到高包括pACYCDuet、pCOLADuet、pET-32a(+)、pCDFDuet、pRSFDuet。通过一步法克隆与线性化的载体连接,分别获得重组质粒pACYCDuet-Mcofp3、pCOLADuet-Mcofp3、pET32a-Mcofp3、pCDFDuet-Mcofp3、pRSFDuet-Mcofp3,将上述质粒化学转化至E.coli BL21(DE3)感受态细胞中,获得对应工程菌株。
对上述菌株进行摇瓶发酵培养,测定发酵结束的贻贝足丝蛋白产量。BL21-pACYCDuet-Mcofp3、BL21-pCOLADuet-Mcofp3、BL21-pET32a-Mcofp3、BL21-pCDFDuet-Mcofp3发酵产量分别为334.2、251.9、303.3、255.8 mg/L。可见,选用pACYCDuet载体表达量最高(图6)。尽管pRSFDuet质粒的拷贝数最高,但是Mcofp-3表达量反而是零,分析主要可能由于表达元件不适配,如RBS与pRSFDuet质粒不匹配,进而影响翻译效率。
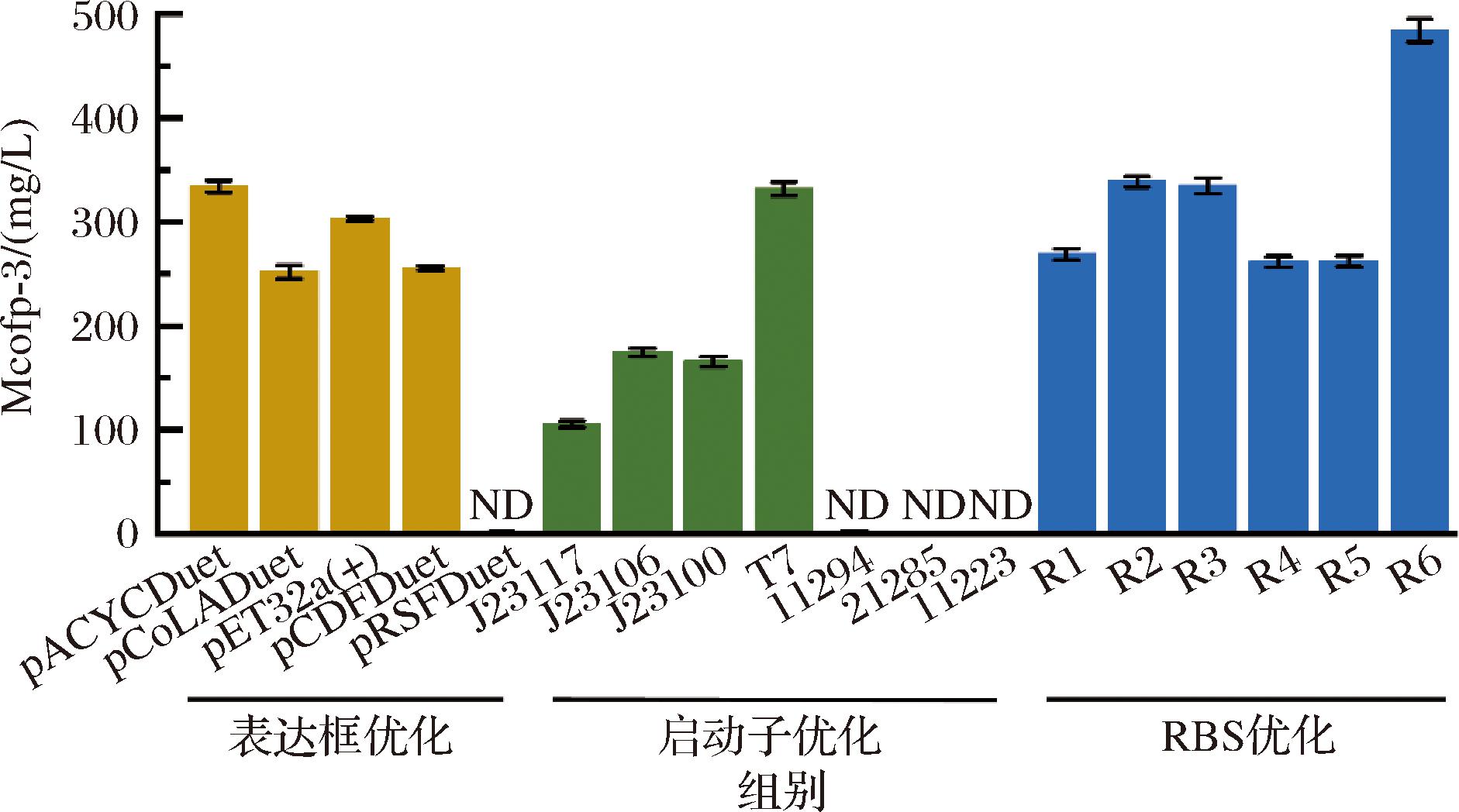
图6 表达框优化后Mcofp-3表达量
Fig.6 Mcofp-3 expression after expression frame optimization
注:ND表示为没有表达。
2.3.2 启动子策略优化重组Mcofp-3的表达
由于组成型启动子无需添加IPTG诱导更可使菌体维持更好的生长状态,同时保证表达的稳定性和一致性,节省成本,适用于高密度发酵。因此考虑替换不同转录强度的组成型启动子表达Mcofp-3,包括常用组成型启动子(转录由低到高:J23117、J23106、J23100)和本课题组设计的大肠杆菌人工组成型启动子(转录强度由低到高:11 223、11 294、21 285)[29-30]。通过一步法克隆与线性化pACYCDuet载体连接,分别获得重组质粒pACYCDuet-J23117-Mcofp3、pACYCDuet-J23106-Mcofp3、pACYCDuet-J23100-Mcofp3、pACYCDuet-T7-Mcofp3、pACYCDuet-11223-Mcofp3、pACYCDuet-11294-Mcofp3、pACYCDuet-21285-Mcofp3,将上述质粒化学转化至E.coli BL21(DE3)感受态细胞中,获得对应工程菌株。
对上述菌株进行摇瓶发酵培养,测定发酵结束的Mcofp-3产量。BL21-pACYCDuet-J23117-Mcofp3、BL21-pACYCDuet-J23106-Mcofp3、BL21-pACYCDuet-J23100- Mcofp3、BL21-pACYCDuet-T7-Mcofp3产量分别为105.8、175.6、169.2、331.9 mg/L,其余菌株未测得蛋白表达量。可见,选用T7启动子表达量最高(图6)。
2.3.3 RBS策略优化重组Mcofp-3的表达
基于在线网站RBS Calculator v2.1(https://www.denovodna.com)计算重组质粒pACYCDuet-T7-Mcofp3表达贻贝足丝蛋白时,RBS对应的翻译起始速率为25 455 au(R2)。通过预测生成5条具有不同翻译速率的RBS序列,从低到高分别为R1(10 000 au)、R3(50 000 au)、R4(100 000 au)、R5(200 000 au)、R6(300 000 au) [31]。将构建的重组质粒pACYCDuet-T7-Mcofp3中RBS序列分别替换成R1、R3、R4、R5、R6,分别获得重组质粒pACYCDuet-T7-R1-Mcofp3、pACYCDuet-T7-R3-Mcofp3、pACYCDuet-T7-R4-Mcofp3、pACYCDuet-T7-R5-Mcofp3、pACYCDuet-T7-R6-Mcofp3。将构建好的质粒分别化学转化至E.coli BL21(DE3)感受态细胞中,获得对应工程菌株。
对上述菌株进行摇瓶发酵培养,发酵结束后测定贻贝足丝蛋白的产量。工程菌BL21-pACYCDuet-T7-R1-Mcofp3、BL21-pACYCDuet-T7-R2-Mcofp3、BL21-pACYCDuet-T7-R3-Mcofp3、BL21-pACYCDuet-R4-Mcofp3、BL21-pACYCDuet-T7-R5-Mcofp3、BL21-pACYCDuet-T7-R6-Mcofp3同时摇瓶发酵,贻贝足丝蛋白表达量分别为268.9、338.8、334.6、261.6、262.1、484.2 mg/L。可见,选用预测后最高翻译速率RBS,蛋白表达量最高(图6)。
综上所述,最终确定以pACYCDuet为质粒载体、T7为载体启动子并替换最高翻译速率的RBS6。
2.4 5-L发酵罐分批补料发酵生产贻贝足丝蛋白Mcofp-3
为了评估贻贝足丝蛋白工程菌在经发酵优化、表达框优化后,规模化生产的潜力[10],根据前期研究,选定最优菌株E.coli BL21-pACYCDuet-T7-R6-Mcofp3在5-L发酵罐中进行补料发酵。鉴于产物生长偶联特性,采取TB培养基进行发酵,在营养丰富条件下,菌体生长OD600值可达到更高水平,从而提高贻贝足丝蛋白的合成。
如图7所示,菌体在前14 h生长迅速,OD600值超过35,随后14~30 h菌体生长缓慢,最高OD600值超过45,37 h之后趋于稳定,并稳步降低。蛋白积累与生长偶联,前30 h一直在累计增加。随着OD600值达到最高值开始缓慢降低时,蛋白积累显示出一定的滞后性,蛋白表达量在37 h达到最高。随着菌体缓慢裂解,蛋白积累量达到最高值也逐渐趋于稳定。发酵培养37 h,贻贝足丝蛋白产量达到1 720 mg/L,产率为46.49 mg/(L·h), 在较短周期内实现了贻贝足丝蛋白的高效生产,为实现稳定可靠的大规模产业化提供了更大可能。
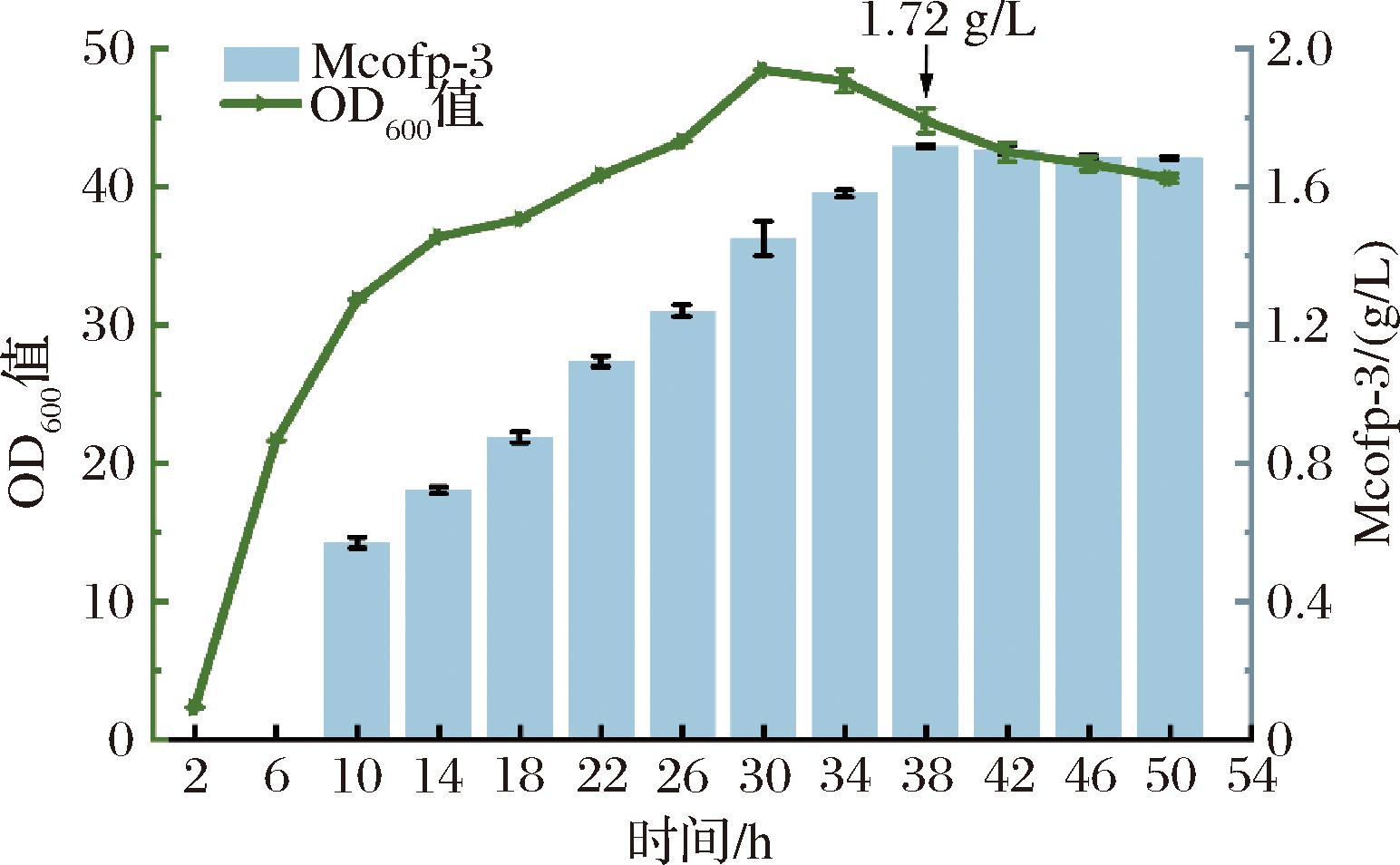
图7 5-L发酵罐分批补料发酵过程曲线图
Fig.7 Time courses of Mcofp-3 production under fed-batch fermentation in 5-L fermentor
3 结论与讨论
厚壳贻贝足丝蛋白Mcofp-3基因被成功克隆后,在大肠杆菌、酵母表达系统中实现了重组表达和功能分析[20],为后续研究奠定了基础。尽管对作用机理和应用研究已日益深入[18],但是因贻贝足丝蛋白Mcofp-3的表达量不足,其大规模生产仍面临挑战。本研究通过在大肠杆菌中构建贻贝足丝蛋白工程菌株多策略组合优化,实现了贻贝足丝蛋白Mcofp-3的高效合成。通过优化发酵条件和表达元件组合,显著提高了以包涵体形式在E.coli BL21(DE3)中表达的Mcofp-3蛋白产量,最终,在5-L发酵罐中达到了1 720 mg/L,产率为46.49 mg/(L·h),表现出优越的生产效率。此外,以包涵体形式表达的Mcofp-3通过简单离心复溶比例超过85%。研究为贻贝足丝蛋白的工业化生产提供了有效的技术路径,将来结合课题组前期的细菌酪氨酸酶表达基础[32],进一步对贻贝足丝蛋白实现DOPA修饰,增强贻贝足丝蛋白黏附等相关功能,推动贻贝足丝蛋白在医药和食品化妆品领域的广泛应用。
[1] XU S C, KANG M Z, XIN X L, et al.Design principles and application research of mussel-inspired materials:A review[J].Journal of Environmental Chemical Engineering, 2024, 12(1):111655.
[2] GUO Q, CHEN J S, WANG J L, et al.Recent progress in synthesis and application of mussel-inspired adhesives[J].Nanoscale, 2020, 12(3):1307-1324.
[3] ZWIES C, VARGAS RODR GUEZ
GUEZ  M, NAUMANN M, et al.Alternative strategies for the recombinant synthesis, DOPA modification and analysis of mussel foot proteins-A case study for Mefp-3 from Mytilus edulis[J].Protein Expression and Purification, 2024, 219:106483.
M, NAUMANN M, et al.Alternative strategies for the recombinant synthesis, DOPA modification and analysis of mussel foot proteins-A case study for Mefp-3 from Mytilus edulis[J].Protein Expression and Purification, 2024, 219:106483.
[4] PRIEMEL T, PALIA R, BABYCH M, et al.Compartmentalized processing of catechols during mussel Byssus fabrication determines the destiny of DOPA[J].Proceedings of the National Academy of Sciences of the United States of America, 2020, 117(14):7613-7621.
[5] WANG X E, LIAO Z, YANG Q M, et al.Characterization of a novel antioxidant byssal protein from Mytilus coruscus foot[J].International Journal of Biological Macromolecules, 2024, 273:133095.
[6] WANG Z, FANG Y, ZENG Y, et al.Immunomodulatory peptides from thick-shelled mussel (Mytilus coruscus):Isolation, identification, molecular docking and immunomodulatory effects on RAW264.7 cells[J].Food Bioscience, 2024, 59:103874.
[7] LI K, XU Z T, LIU X X, et al.Mussel foot inspired bionic adhesive material enhanced by a reconstructed in vitro system for interfacial adhesion[J].Chemical Engineering Journal, 2023, 452:139580.
[8] CASTILLO J J, SHANBHAG B K, HE L.Food Bioactives:Extraction and Biotechnology Applications [M].Cham:Springer International Publishing, 2017:111-135.
[9] WANG J, SCHEIBEL T.Recombinant production of mussel Byssus inspired proteins[J].Biotechnology Journal, 2018, 13(12):1800146.
[10] ESKANDARI A, NEZHAD N G, LEOW T C, et al.Essential factors, advanced strategies, challenges, and approaches involved for efficient expression of recombinant proteins in Escherichia coli[J].Archives of Microbiology, 2024, 206(4):152.
[11] WANG X Y, FENG X X, XUE R, et al.Promoting soluble expression of hybrid mussel foot proteins by SUMO-TrxA tags for production of mussel glue[J].International Journal of Biological Macromolecules, 2023, 225:840-847.
[12] XUE R, WANG J, HUANG W W, et al.Efficient production of recombinant hybrid mussel proteins with improved adhesion[J].International Journal of Biological Macromolecules, 2025, 289:139937.
[13] BOLGHARI N, SHAHSAVARANI H, ANVARI M, et al.A novel recombinant chimeric bio-adhesive protein consisting of mussel foot protein 3, 5, gas vesicle protein A, and CsgA curli protein expressed in Pichia pastoris[J].AMB Express, 2022, 12(1):23.
[14] CASTRO J M, BIANCHI V A, PASCUAL M M, et al.Immune and biochemical responses in hemolymph and gills of the Patagonian freshwater mussel Diplodon chilensis, against two microbiological challenges:Saccharomyces cerevisiae and Escherichia coli[J].Journal of Invertebrate Pathology, 2018, 157:36-44.
[15] SEONG C,GYUN K, LIM S, et al.Recombinant mussel adhesive protein fp-5 (MAP fp-5) as a bulk bioadhesive and surface coating material[J].Biofouling, 2011, 27(7):729-737.
[16] YANG B, GYUN K,HYUN S, et al.A comparative study on the bulk adhesive strength of the recombinant mussel adhesive protein fp-3[J].Biofouling, 2013, 29(5):483-490.
[17] LEE S J, HAN Y H, NAM B H, et al.A novel expression system for recombinant marine mussel adhesive protein Mefp1 using a truncated OmpA signal peptide[J].Molecules and Cells, 2008, 26(1):34-40.
[18] 袁升. 贻贝足丝蛋白Mgfp-5及其融合蛋白在大肠杆菌中的表达和粘附性能研究 [D].武汉:华中科技大学, 2021.YUAN S.Expression and adhesion of mussel foot silk protein Mgfp-5 and its fusion protein in Escherichia coli[D].Wuhan:Huazhong University of Science and Technology, 2021.
[19] 吕玉伟, 吕亚维, 杨泽熵, 等.贻贝蛋白Mgfp-5的原核表达与纯化[J].西北大学学报(自然科学版), 2016, 46(3):390-396.LYU Y W,LV Y W,YANG Z S,et al.Prokaryotic expression and purification of Mytilus galloprovincialis foot protein-5[J].Journal of Northwest University (Natural Science Edition), 2016, 46(3):390-396.
[20] 李楠楠. 厚壳贻贝足丝蛋白分子多样性及重组表达分析 [D].舟山:浙江海洋大学, 2012.LI N N.Molecular diversity and recombinant expression analysis of Mytilus coruscus foot protein[D].Zhoushan:Zhejiang Ocean University, 2012.
[21] CHOI B H, CHEONG H, KEE J, et al.Highly purified mussel adhesive protein to secure biosafety for in vivo applications[J].Microbial Cell Factories, 2014, 13(1):52.
[22] GEHRKE C W, WALL L L Sr, ABSHEER J S, et al.Sample preparation for chromatography of amino acids:Acid hydrolysis of proteins[J].Journal of Association of Official Analytical Chemists, 1985, 68(5):811-821.
[23] ZHOU H Y, WU W J, NIU K, et al.Enhanced L-methionine production by genetically engineered Escherichia coli through fermentation optimization[J].3 Biotech, 2019, 9(3):96.
[24] CHEN Z, ZHOU P, ZHAO Z J, et al.Enhanced production of L-serine in Escherichia coli by fermentation process optimization and transcriptome sequencing[J].Biochemical Engineering Journal, 2023, 200:109109.
[25] 陈佳敏, 王阳, 堵国成, 等.优化前体供给与细胞膜通透性强化大肠杆菌合成麦角硫因[J].食品与生物技术学报, 2022, 41(8):43-52.CHEN J M, WANG Y, DU G C, et al.Enhancement of ergothioneine synthesis in Escherichia coli via optimization of precursor supply and cell membrane permeability[J].Journal of Food Science and Biotechnology, 2022, 41(8):43-52.
[26] ZHOU Y L, LU Z H, WANG X, et al.Genetic engineering modification and fermentation optimization for extracellular production of recombinant proteins using Escherichia coli[J].Applied Microbiology and Biotechnology, 2018, 102(4):1545-1556.
[27] ZHANG Y, GUO M L, ZHANG X Y, et al.Multiple optimizations of recombinant plasmid for improving expression of Hepatitis B core antigen in Escherichia coli[J].Protein Expression and Purification, 2022, 198:106127.
[28] SANTOS S P O, GARCÉS L F S, SILVA F S R, et al.Engineering an optimized expression operating unit for improved recombinant protein production in Escherichia coli[J].Protein Expression and Purification, 2022, 199:106150.
[29] WANG Y, LIU Q T, WENG H J, et al.Construction of synthetic promoters by assembling the sigma factor binding -35 and -10 boxes[J].Biotechnology Journal, 2019, 14(1):1800298.
[30] HUANG Y K, YU C H, NG I S.Precise strength prediction of endogenous promoters from Escherichia coli and J-series promoters by artificial intelligence[J].Journal of the Taiwan Institute of Chemical Engineers, 2024, 160:105211.
[31] WANG D A, CHEN J M, WANG Y, et al.Engineering Escherichia coli for high-yield production of ectoine[J].Green Chemical Engineering, 2023, 4(2):217-223.
[32] 郑依琳, 胥睿睿, 王阳, 等.细菌酪氨酸酶高效异源表达及其在生物染发和丝素多肽多巴修饰中的应用[J].生物工程学报, 2024, 40(9):3083-3102.ZHENG Y L, XU R R, WANG Y, et al.Heterologous expression of bacterial tyrosinase and its applications in biological hair dyeing and DOPA modification of hydrolyzed silk fibroin[J].Chinese Journal of Biotechnology, 2024, 40(9):3083-3102.