人乳寡糖(human milk oligosaccharides,HMOs)是人乳中仅次于乳糖和脂类的第三大固体成分,含量丰富且种类多达200余种,为一类复杂且不易消化的非营养性碳水化合物,在婴幼儿的发育中发挥着重要作用[1]。目前,婴幼儿配方奶粉多以牛、羊乳为基料,其寡糖含量显著低于人乳,因此,在配方奶粉中添加HMOs对婴幼儿的健康具有显著益处。其中,3-岩藻糖基乳糖(3-fucosyllactose,3-FL)是人乳寡糖中的一种重要成分,在人乳寡糖中的含量约为5%[2],具有调节肠道菌群、提供免疫支持和促进大脑发育等作用[3]。随着3-FL功能的不断明确,其制备工艺也在持续开发,为将来的应用奠定了基础[4]。
目前,3-FL的生产方法包括化学法、酶法和微生物发酵法。化学法反应步骤冗长且涉及毒性试剂的使用,不适合在食品工业中应用;酶法合成虽然精确,但因底物价格昂贵且获取困难,难以支持大规模生产;微生物发酵法具有合成条件温和、成本低等优势,正在受到越来越多的关注[3]。现阶段,3-FL生产多以大肠杆菌作为底盘细胞,例如,CHEN等[5]通过过表达manC、manB、gmd和wcaG增加GDP(鸟苷二磷酸,guanosine)-L-岩藻糖供应,筛选得新的3-岩藻糖基转移酶(1,3-fucosyltransferases,α-1,3-Fut)FutM2,使大肠杆菌重组菌的3-FL产量达到20.3 g/L。DU等[6]在此基础上通过引入转运蛋白促进3-FL的外排,酶工程改造FutM2提高其催化性能的策略,将3-FL产量提升至52.1 g/L,为目前报道的最高产量。虽然大肠杆菌具有较高的3-FL生产能力,但其在发酵中可能产生内毒素,且易感染噬菌体,故开发食品安全型微生物来生产3-FL具有重要意义。酵母是发酵工业中常用的微生物,尤其在食药品行业中具有显著优势,利用酵母作为底盘细胞进行生产可以有效规避大肠杆菌发酵中产生内毒素等问题,提高食品的安全性,目前已有多篇文献报道使用酵母来合成2′-岩藻糖基乳糖(2′-FL)[7-9],这对于3-FL合成的研究也具有参考价值。XU等[10]在酿酒酵母中构建了基于信息素反应途径的自诱导基因表达系统,用于3-FL的生产,摇瓶产量达2.36 g/L,发酵罐产量达20.91 g/L,首次完成了3-FL在酵母中的合成,也是目前唯一报道的使用酵母作为底盘细胞合成3-FL的研究,可以说,目前对于3-FL在酵母中合成的研究还相对薄弱。解脂耶氏酵母(Yarrowia lipolytica)是近年来研究和应用的热门底盘细胞之一,随着适用于该酵母的如基因编辑、基因表达调控等合成生物学技术的成熟,Y.lipolytica已被转化为生产多种精细化学品的细胞工厂,此外,其出色的适应多种极端环境的能力,使其成为工业实际生产的理想宿主[11]。同酿酒酵母相比,Y.lipolytica的磷酸戊糖途径通量更高,通常能更有效地再生NADPH,这有利于获得更高含量的3-FL合成前体GDP-L-岩藻糖,此外,酿酒酵母以葡萄糖作为底物时,容易积累大量的乙醇,不利于目标产物的生成[10,12]。HOLLANDS等[13]在解脂耶氏酵母中完成了2′-FL代谢通路的构建,2′-FL和3-FL的合成途径类似,均以GDP-L-岩藻糖和乳糖为前体物质,仅在岩藻糖基转移酶上存在差异:2′-FL由2′-岩藻糖基转移酶合成,而3-FL则由3-岩藻糖基转移酶催化生成。
本研究构建了一株Y.lipolytica菌株,用于合成3-FL。通过引入来自Kluyveromyces lactis的lac12,来自Mortierella alpina的gmd和gmer,来自Neobacillus cucumis的fut3Bc,实现了3-FL的从头合成[10,13]。随后,通过过表达合成途径中的关键基因,确定了3-FL在Y.lipolytica中合成的限速步骤为由Fut3Bc催化GDP-L-岩藻糖和乳糖合成3-FL的反应,之后通过对Fut3Bc添加小泛素相关修饰蛋白(small ubiquitin-related modifier,SUMO)标签,随机整合多拷贝SUMO-fut3Bc,过表达pgl基因以增强辅因子NADPH供应的策略,最终获得了一株摇瓶产量为2.84 g/L,发酵罐产量为14.70 g/L的重组Y.lipolytica菌株。本研究开拓了3-FL在酵母中生产的可能性,也为人乳寡糖细胞工厂的构建提供了参考。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
本研究所用的出发菌株是实验室保存的Y.lipolytica Po1f(MatA, Leu2-270, URA3-302, xpr2-322, axp-2)。
1.1.2 主要试剂
2×Phanta Flash Master Mix(Dye Plus)、2×Rapid Taq Master Mix、ClonExpress Ultra One Step Cloning Kit V2(C116)、FastPure Gel DNA Extraction Mini Kit(DC301)、FastPure Plasmid Mini Kit(DC201),南京诺唯赞生物科技有限公司;QuickCut限制性快切酶、DNA Maker,Takara宝生物工程(大连)有限公司;基因、引物合成及测序,苏州金唯智生物科技有限公司;3-岩藻糖基乳糖标准品,上海麦克林生化科技有限公司;FROZEN-EZ酵母转化试剂盒,美国Zymo Research公司。
1.1.3 培养基
LB培养基(g/L):蛋白胨10、酵母粉5、氯化钠10;YPD培养基(g/L):蛋白胨20、酵母粉10、葡萄糖20;YNB(yeast nitrogen base)培养基(g/L):酵母氮源基础培养基6.7、葡萄糖20,尿嘧啶0.1,酪蛋白水解物2(用于补充亮氨酸),10%(体积分数)Na+/K+磷酸缓冲液,其中尿嘧啶和酪蛋白水解物根据需要添加;液体发酵培养基中补充终质量浓度为5 g/L的乳糖;通过添加2%(质量分数)琼脂粉制备固体培养基。
Na+/K+磷酸缓冲液:一定体积的500 mmol/L的KH2PO4和500 mmol/L的Na2HPO4·12H2O混合,调节pH值为6.8。
1.2 仪器与设备
电子天平、ST3100型pH计,奥豪斯公司;离心机,Thermo UltiMate 3000液相色谱系统,赛默飞世尔科技公司;Votex2涡旋振荡混匀器,德国艾卡公司;UV-6100紫外-可见光分光光度计,上海元析仪器有限公司;AIRTECH VS-1306超净工作台,苏州安泰空气技术有限公司;DYY-6C核酸电泳仪,北京六一生物科技有限公司;冰箱,安徽中科都菱有限公司;QWZY-C3组合式摇床,太仓市强文实验设备有限公司;MINI Space凝胶成像系统,上海天能科技有限公司;SB5200TD超声波清洗机,宁波新芝生物科技股份有限公司;BG-160恒温培养箱、DK-8D水浴锅,上海博迅医疗生物仪器股份有限公司;恒温金属浴,上海一恒科技有限公司;微量紫外-可见光分光光度计,普睿博仪器有限公司;ETC-811 PCR仪,北京东胜创新生物科技有限公司;CT90A灭菌锅,上海伯能仪器有限公司;溶氧电极、pH电极,梅特勒托利多国际有限公司;T&J-Atype 5 L台式玻璃发酵罐,迪必尔生物工程(上海)有限公司。
1.3 实验方法
1.3.1 质粒构建和菌株构建
本研究所用质粒和引物详细信息如表1和表2所示,质粒构建主要采用一步克隆法连接;pFutM1、pFutM2、pFut3Bc、pFutA、pm3FT、pHpM32委托苏州金唯智生物科技有限公司在pGmer的BamH Ⅰ和Hind Ⅲ酶切位点之间插入密码子优化后的相关基因;以pLGG为模板,通过引物Lac12-F、Lac12-R克隆lac12基因表达框,以pFutM1为模板,Fut-F、Fut-R克隆futM1表达框,EcoR Ⅰ酶切pLGG获得载体,组装成pLGGF1,同理构建pLGGF2、pLGGF3;以Y.lipolytica Po1f基因组为模板,通过引物Pmi40-F、Pmi40-R克隆pmi40,BamH Ⅰ和Hind Ⅲ双酶切pGmer 获得载体,组装成pPmi40,同理构建pSec53、pPsa1、pZwf1、pPgl、pGnd1;以pSUMO为模板,通过引物SUMO-F、SUMO-R克隆SUMO标签,以pFut3Bc为模板,通过引物Fut3Bc-F、Fut3Bc-R克隆载体,组装成pSF3,同理构建pXF3、pTF3,以pFut3Bc为模板,通过引物Avi-F、Avi-R克隆pFut3Bc组装成pAF3;同pLGGF1构建方法构建pLGGSF3;以pSF3为模板,通过引物SF3-F、SF3-R克隆SUMO-fut3Bc基因,以p16/28S-rRNA为模板,通过引物tLIP-F、pTEF-R克隆载体,组装成pRS;以pZwf1为模板,通过引物Co-F、Co-R克隆zwf1表达框,以pRS为模版,通过引物R2-F、R2-R克隆载体,组装成pRSZ,同理构建pRSP、pRSG。
表1 本研究所用质粒
Table 1 Plasmids used in this study

表2 本研究所用引物
Table 2 Primers used in this study

本研究所用菌株详细信息如表3所示,Y.lipolytica菌株的构建采用FROZEN-EZ酵母转化试剂盒转化法:挑取单菌落过夜培养,次日接种1 mL菌液于装有10 mL新鲜YPD培养基中培养至OD600nm=0.8~1.0;取2.5 mL菌液,3 000 r/min离心4 min,弃上清液;2.5 mL EZ1重悬,3 000 r/min离心4 min,弃上清液;250 mL EZ2重悬,分装成50 mL一支;加入5 mL质粒或线性化DNA片段,加入500 mL EZ3,30 ℃孵育45 min,期间2~3次翻转混匀;取50~100 mL涂布YNB筛选平板。
表3 本研究所用菌株
Table 3 Strains used in this study

1.3.2 发酵方法
摇瓶发酵:将菌株接种到装有10 mL YPD/YNB液体培养基的50 mL摇瓶中,在30 ℃、220 r/min条件下培养24 h制备种子液,转接至装有25 mL YPD/YNB(含5 g/L乳糖)液体发酵培养基的250 mL摇瓶中,接种量为5%(体积分数),30 ℃、220 r/min培养96 h。
5 L发酵罐发酵:将于固体平板活化的菌株,接种到装有10 mL YPD液体培养基的50 mL摇瓶中,30 ℃、220 r/min培养24 h制备一级种子液,接种5%(体积分数)至装有30 mL YPD液体培养基的250 mL摇瓶中,30 ℃、220 r/min培养96 h制备二级种子液,装有1.5 L含有20 g/L酵母粉和40 g/L蛋白胨的发酵罐和167 mL质量浓度为500 g/L的葡萄糖分别灭菌,待冷却后往发酵罐中加入葡萄糖溶液和种子液,控制发酵温度在30 ℃,通过5 mol/L的NaOH控制pH值在5.5,通过控制搅拌速度将溶氧控制在15%~25%,通气量维持在2 vvm。发酵过程中,流加500 g/L的葡萄糖和200 g/L的乳糖。
1.3.3 产物检测
对于胞外3-FL的检测,取1 mL发酵液于1.5 mL离心管中,12 000 r/min离心10 min后取上清液,经0.22 mm滤膜过滤后进行HPLC检测。采用Dikma CarboPac H+(300 mm×8.0 mm,6 mm)色谱柱,流动相为0.5‰(体积分数)硫酸,柱温50 ℃,流速0.8 mL/min,进样量10 μL,示差折光检测器在35 ℃进行检测。对于3-FL总量的检测,取1 mL发酵液于1.5 mL离心管中,沸水浴10 min,后续操作同胞外3-FL的检测,胞内3-FL含量为二者之差。
LC-MS检测委托江南大学食品科学与技术国家重点实验室进行。
2 结果与分析
2.1 3-FL代谢途径的构建
如图1所示,Y.lipolytica需要引入外源的GDP-甘露糖-4,6-脱水酶、GDP-L-岩藻糖合酶使得GDP-D-甘露糖转化成GDP-L-岩藻糖,需要引入外源的乳糖转运蛋白使得乳糖转运进胞内[13]。本研究采用实验室前期构建的含有K.lactis来源的lac12基因表达框,M.alpina来源的gmd和gmer基因表达框的质粒pLGG,将其线性化后整合至Po1f基因组,获得重组菌LGG。
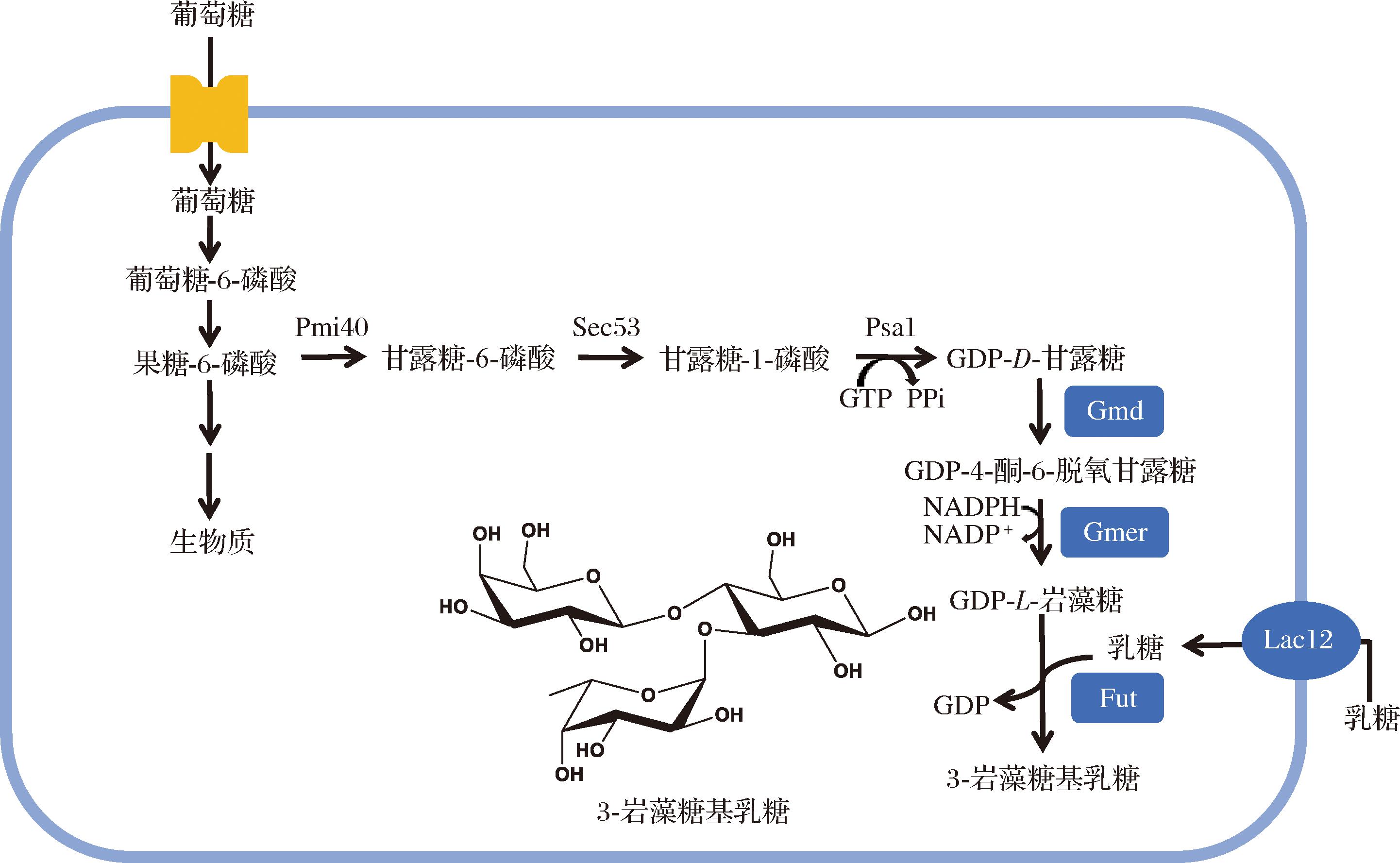
图1 Y.lipolytica中3-FL的代谢途径
Fig.1 Metabolic pathway of 3-FL in Y.lipolytica
注:Pmi40为甘露糖-6-磷酸异构酶;Sec53为磷酸甘露糖变位酶;Psa1为甘露糖-1-磷酸鸟苷转移酶;Gmd为GDP-D-甘露糖-4,6-脱水酶;Gmer为GDP-L-岩藻糖合酶;Lac12为乳糖转运蛋白;Fut为3-岩藻糖基转移酶;其中Lac12来源于K. lactis;Gmd和Gmer来源于M.alpina;Fut来源于N.cucumis。
岩藻糖基转移酶属于Leloir糖基转移酶(leloir glycosyltransferase)家族,以核苷酸活化糖为糖基供体进行糖基化反应的具体机制为催化L-岩藻糖基从GDP-L-岩藻糖转移到受体底物上[14]。3-岩藻糖基转移酶是该家族的一种关键酶,可用于生产3-FL。目前研究最多的3-岩藻糖基转移酶来源于幽门螺杆菌,其中一些的结构已被阐明,如FutA包含3个功能区域:N-末端的催化结构域、带负电荷的C-末端尾部,以及由7个氨基酸残基重复单元组成的中间区域[4,15]。近年来,更多来源3-岩藻糖基转移酶被研究,如CHEN等[5]筛选了多种不同来源的3-岩藻糖基转移酶,发现了一种在大肠杆菌中更高效的α1,3-Fut,为3-FL生产提供了新的可能性。
为了寻找适合在Y.lipolytica中高效发挥作用的3-岩藻糖基转移酶,本研究筛选了6种不同来源的α1,3-Fut,分别为:Bacteroidaceae bacterium来源的FutM1(MBO5664686.1)[5]、Bacteroides gallinaceum来源的FutM2(WP_204430034.1)[5]、N.cucumis来源的Fut3Bc(WP_101650151.1)[10]、H.pylori来源的FutA[16]、H.pylori来源的HpM32(PDB:5ZOI)[17]和H.pylori来源的m3FT[18]。以上α1,3-Fut基因经密码子优化后,在重组菌LGG中游离表达,分别得到菌株F1、F2、F3、F4、F5、F6。在YNB液体培养基发酵后,进行HPLC和LC-MS检测(图2),结果显示,F1、F2、F3菌株能产生3-FL,而F4、F5和F6菌株未检测到3-FL的合成。实验表明,大肠杆菌中广泛应用的幽门螺杆菌来源的3-岩藻糖基转移酶[4]在Y.lipolytica中无法正常发挥作用。这一结果反映出异源基因在不同宿主中的表达效果可能存在显著差异,也进一步验证了筛选适合宿主的3-岩藻糖基转移酶的必要性。本研究通过筛选得到了适合Y.lipolytica的3-FL合成关键酶,为其进一步应用奠定了基础。
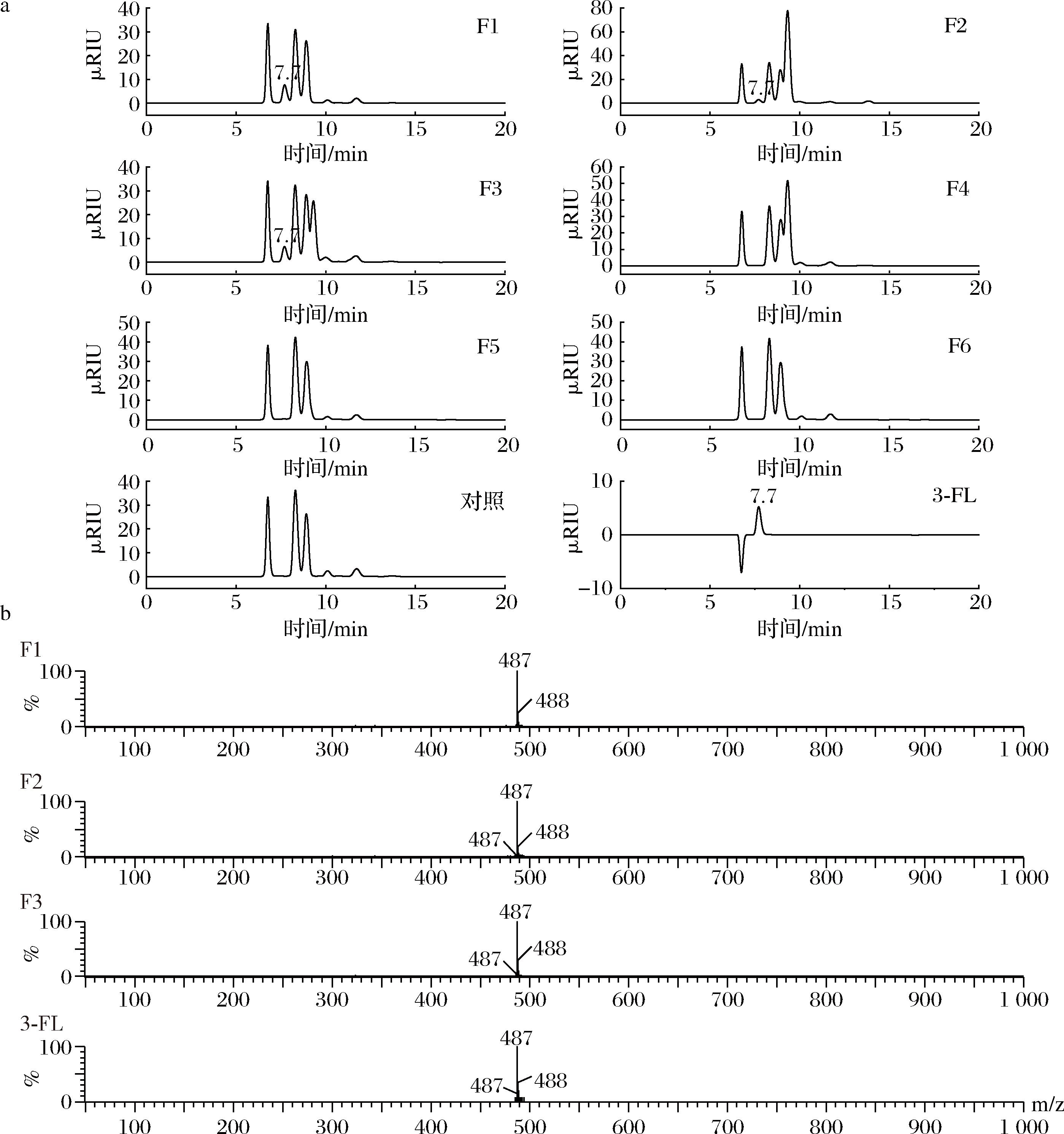
a-F1、F2、F3、F4、F5、F6发酵液、对照组以及3-FL标品的HPLC图谱;b-F1、F2、F3发酵液和3-FL标品的LC-MS图谱
图2 LGG菌株游离表达3-岩藻糖基转移酶合成3-FL的HPLC和LC-MS检测结果
Fig.2 HPLC and LC-MS detection of episomal 1,3-Fut expression in strain LGG for the synthesis of 3-FL
随后,将lac12、gmd、gmer和futM1、futM2、fut3Bc分别串联构建质粒pLGGF1、pLGGF2和pLGGF3,线性化后整合到Po1f基因组中,分别获得重组菌LGGF1、LGGF2和LGGF3。YPD液体培养基发酵后检测结果显示LGGF3的3-FL产量最高(图3),达0.66 g/L,这表明N.cucumis来源的Fut3Bc在Y.lipolytica中更适合用于3-FL的合成。进一步分析发现,在96 h的发酵液中,LGGF3的胞外3-FL产量为0.56 g/L,胞内产量为0.1 g/L,胞内产量占总产量的15.2%。这一结果表明,虽然大部分3-FL被成功分泌到胞外,但仍有一定比例的3-FL积累在胞内,因此在后续研究中可以进一步优化分泌路径,以提高3-FL的分泌效率。
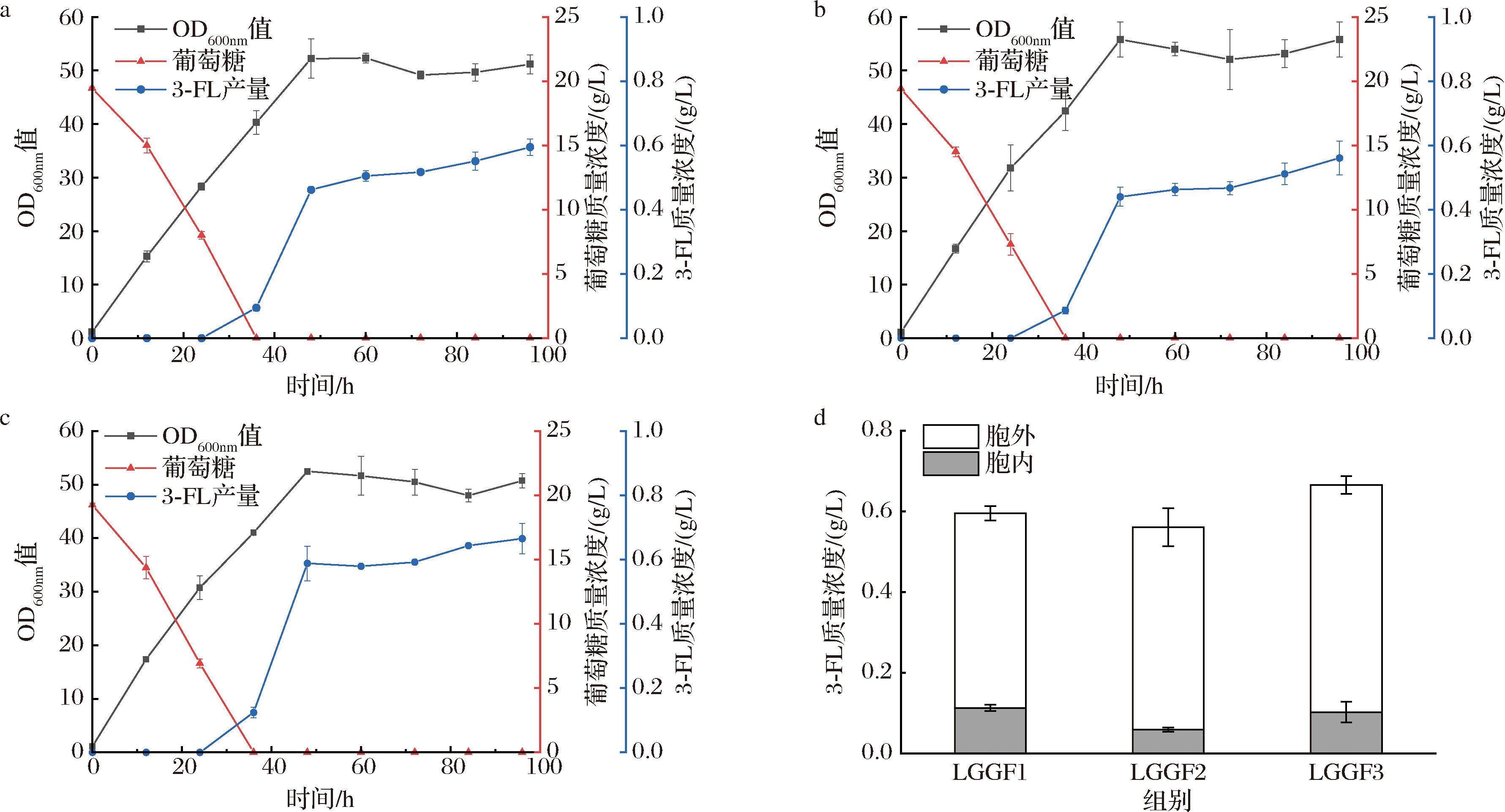
a-LGGF1发酵结果;b-LGGF2发酵结果;c-LGGF3发酵结果;d-96 h时LGGF1、LGGF2、LGGF3发酵液中产物的胞内胞外分布情况
图3 整合表达3-岩藻糖基转移酶的发酵结果
Fig.3 Fermentation results of integrated expression of α-1,3-Fut
2.2 3-FL代谢途径限速步骤的判断
寻找代谢途径中的限速步骤对于定向改造菌株提高产物产量有重要意义,而基因过表达是该方向常用的研究策略。如图1所示,3-FL代谢途径中的关键基因包括pmi40、sec53、psa1、gmd、gmer、lac12和fut3Bc。为研究限速步骤,本研究将上述基因分别构建到质粒上并在菌株LGGF3中游离表达,以实现基因对目的基因的过表达(图4)。结果显示,过表达pmi40、sec53、psa1、gmd、gmer和lac12时,3-FL的产量为0.43~0.58 g/L,与空白对照相比差距不大。而当过表达fut3Bc时,3-FL的产量显著提升至0.89 g/L,较空白对照提高了97.8%。这一结果表明,代谢路径的最后一步,即Fut3Bc催化GDP-L-岩藻糖和乳糖合成3-FL的反应,是3-FL合成的限速步骤,这一发现为后续的菌株优化提供了重要的参考方向。
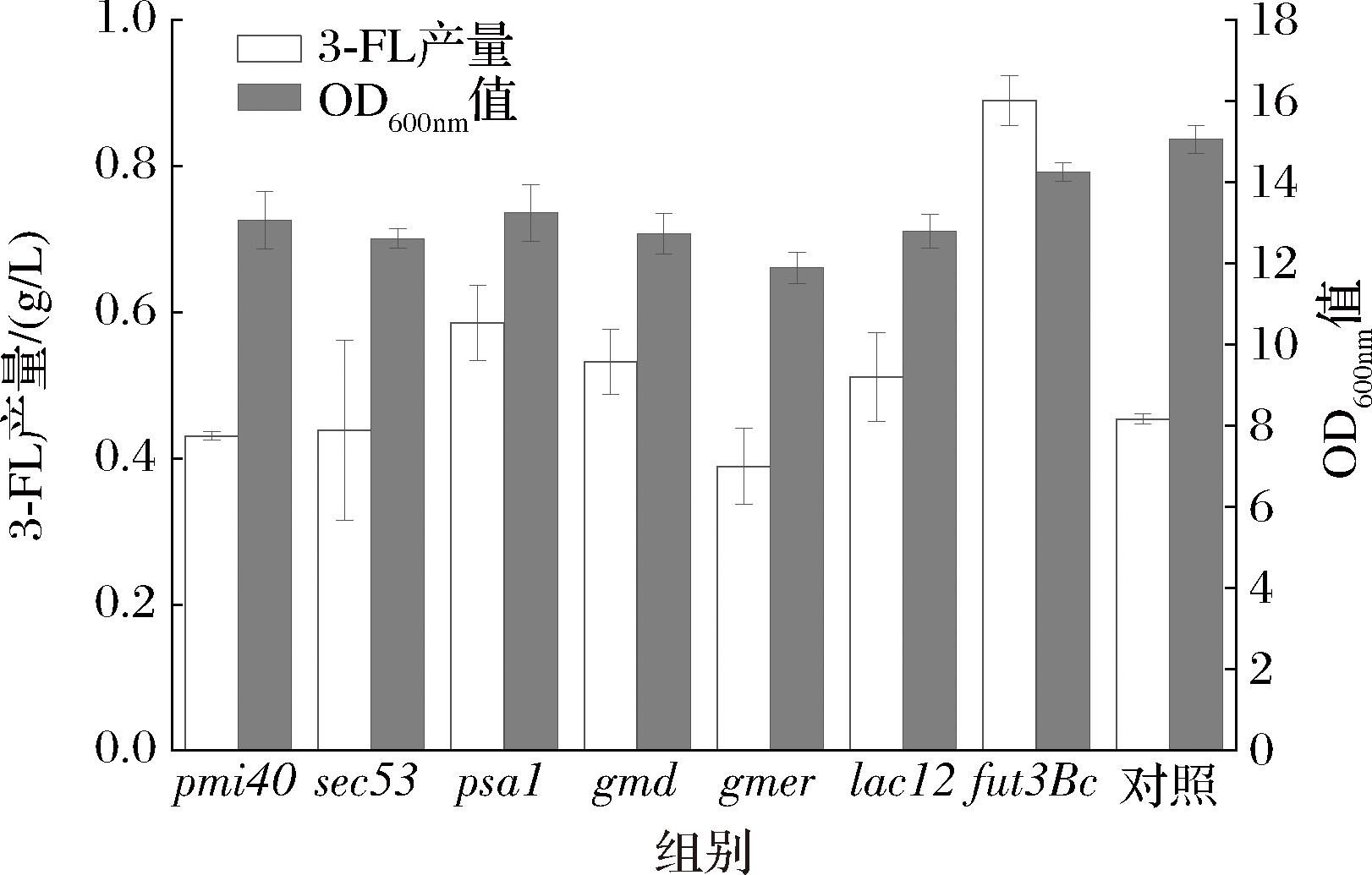
图4 过表达3-FL代谢途径中的关键基因
Fig.4 Overexpression of key genes in 3-FL metabolic pathway
2.3 对Fut3Bc添加蛋白标签并多拷贝
异源表达的3-岩藻糖基转移酶在微生物发酵法生产3-FL过程中普遍存在溶解性差的问题。CHOI等[19]和XIE等[15]通过截短α1,3-Fut的疏水C末端提升了该蛋白的溶解性,提高了3-FL的生产效率。HOLLANDS等[13]在Y.lipolytica中使用SUMO蛋白标签,提升了2′-岩藻糖基转移酶的溶解性,获得了更高的2′-FL产量。
本研究明确了3-FL合成的限速步骤为代谢途径的最后一步(Fut3Bc催化的反应)。基于已有研究表明合适的蛋白标签可以提高蛋白的表达水平、稳定性以及溶解性,本研究尝试将其与Fut3Bc融合表达以提高3-FL的产量,选择了SUMO、防冻蛋白 AXX 的逆序列蛋白(XXA)[20]、硫氧还蛋白(thioredoxin A,TrxA)和Avi标签(avidin-binding tag,Avi)4种蛋白标签,在LGG中进行游离表达(图5),结果显示,SUMO标签的效果最好,3-FL产量达到1.26 g/L,较空白对照相提升了168%;Avi标签效果效果略差于SUMO标签,但对3-FL产量也有显著提升;TrxA标签对于3-FL产量没有明显影响;XXA标签则使得Fut3Bc丧失了合成3-FL的能力。以上结果表明,由于原核生物和真核生物在蛋白质翻译和修饰过程中的差异,某些在大肠杆菌中效果较好的标签可能不适合在Y.lipolytica中与Fut3Bc融合表达用于3-FL的合成[21]。这一发现为优化Fut3Bc的表达策略提供了新的思路,也为酵母中蛋白质工程的应用研究提供了重要参考。
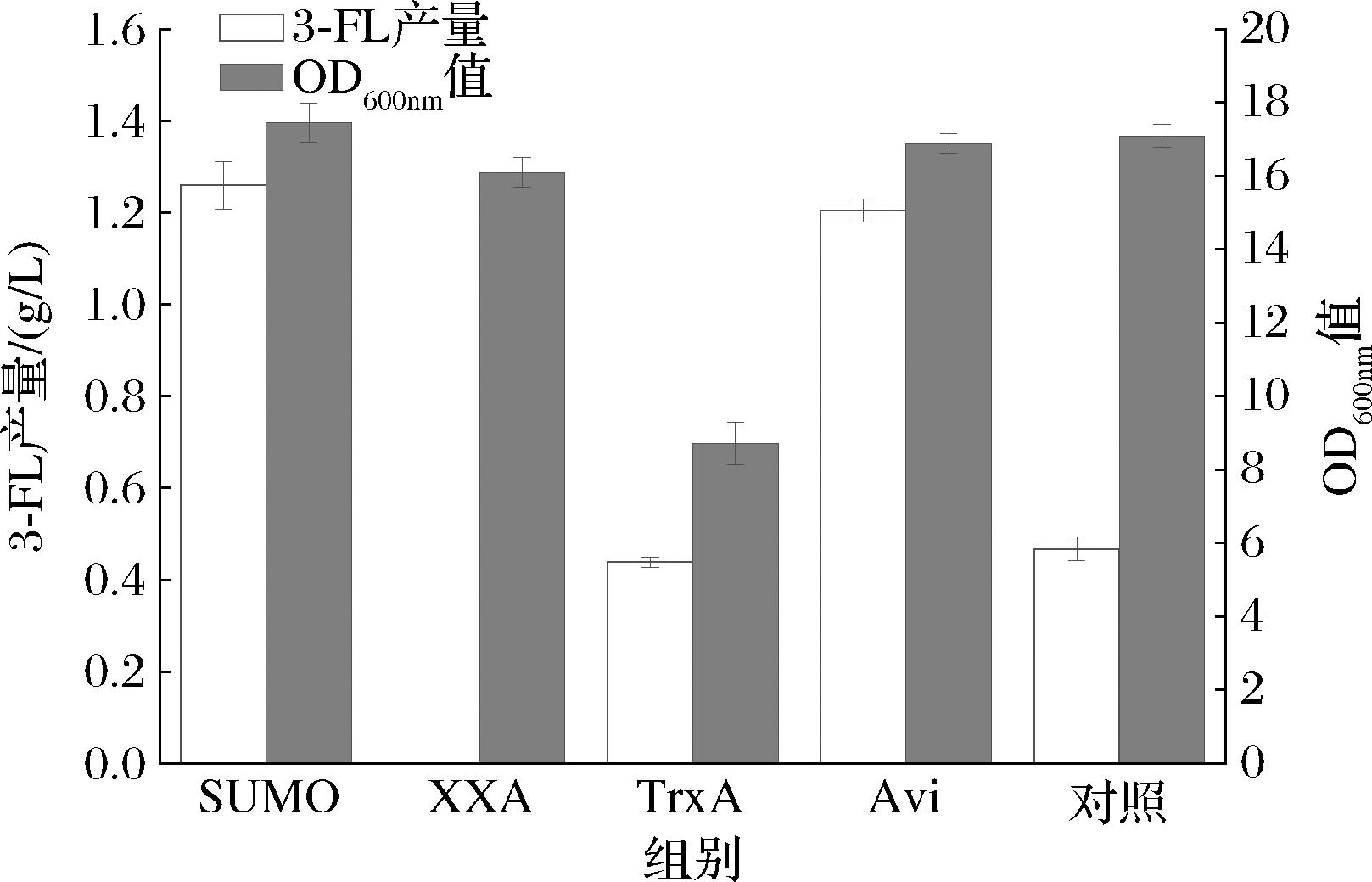
图5 Fut3Bc添加蛋白标签
Fig.5 Fut3Bc with protein tags
随后,将lac12、gmd、gmer以及SUMO-fut3Bc整合至Po1f基因组中,获得重组菌LGGSF3。发酵结果如图6所示,LGGSF3的3-FL产量达到1.25 g/L,较LGGF3提升了89.4%,表明在Fut3Bc前添加SUMO标签无论是质粒表达还是基因组整合表达,均可显著提升3-FL产量。
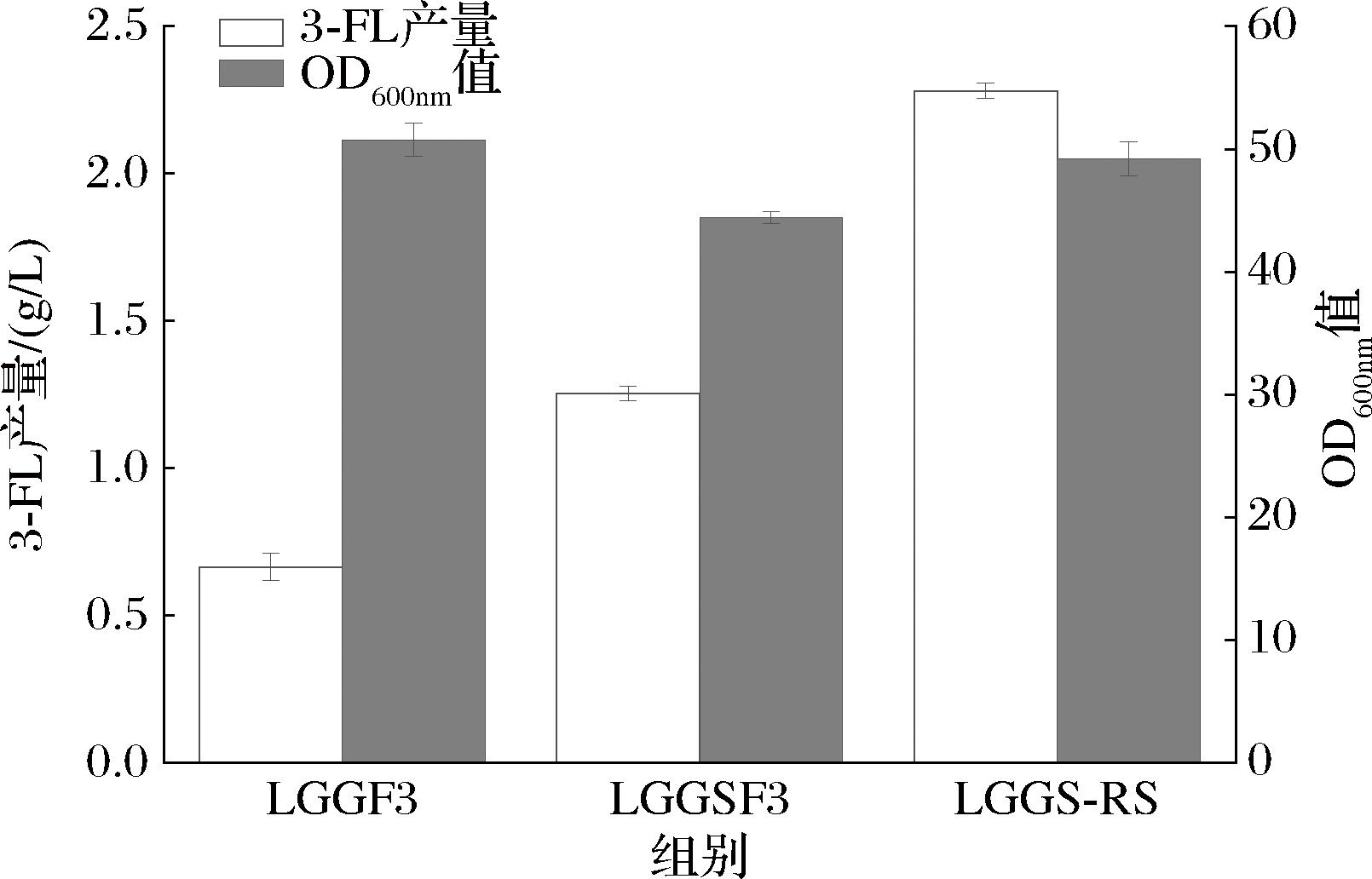
图6 整合表达SUMO-fut3Bc并在此基础上对SUMO-fut3Bc进行多拷贝
Fig.6 Integrated expression of SUMO-fut3Bc and make multiple copies of SUMO-fut3Bc on this basis
此外,已有研究表明,多拷贝表达目标基因可以有效提升代谢产物产量[22]。在Y.lipolytica中,多拷贝的核糖体rRNA基因簇提供了理想的多基因整合位点。根据该重复区域的基因序列,设计同源整合区域,可实现目标基因在基因组内的多拷贝整合。本研究利用16S和28S rRNA基因序列作为同源臂,随机整合SUMO-fut3Bc,构建了菌株LGGS-RS。发酵结果显示,LGGS-RS的3-FL产量达到2.28 g/L,较LGGSF3提升了82.4%,较LGGF3提升了245%。这些结果进一步验证了SUMO标签和多拷贝整合在Y.lipolytica中提升3-FL产量的有效性,为进一步开发高效的3-FL微生物生产体系提供了重要参考。
2.4 优化氧化还原辅因子供应模块
3-FL的代谢路径中涉及氧化还原酶催化的关键反应(由Gmer催化GDP-4-酮-6-脱氧甘露糖生成GDP-L-岩藻糖),该过程需要NADPH作为辅因子。已有研究表明,增强NADPH供应可以有效提高3-FL产量[16,23]。在磷酸戊糖途径(pentose phosphate pathway,PPP)中,zwf1、pgl和gnd1基因的表达可直接或间接影响NADPH的产生。其中,Zwf1为葡萄糖-6-磷酸脱氢酶,Gnd1为6-磷酸葡萄糖酸脱氢酶,Pgl为6-磷酸葡萄糖酸内酯酶,催化6-磷酸葡萄糖酸-δ-内酯水解为6-磷酸葡萄糖酸,是PPP途径总的第二步,也是Zwf1和Gnd1所催化反应的中间步骤。已有研究表明,Zwf1和Gnd1催化的反应是酵母中NADPH生成的重要来源,而Pgl催化的反应则可能成为途径的限速步骤[22,24]。基于此,本研究在LGGS-RS菌株的基础上,随机整合多拷贝zwf1、pgl和gnd1基因,期望通过增强NADPH的再生进一步提升3-FL的产量。发酵结果如图7所示,过表达pgl的菌株3-FL产量达到2.84 g/L,较LGGS-RS提升了24.6%,效果最好;过表达gnd1的菌株3-FL产量为2.42 g/L,提升了6.1%,效果不如pgl;而过表达zwf1对3-FL产量无显著影响。这表明在该代谢体系下,pgl催化的反应可能为PPP途径中的限速步骤,而过表达pgl可以增加PPP途径的通量,从而增加NADPH的供应,进而实现3-FL产量的提升。
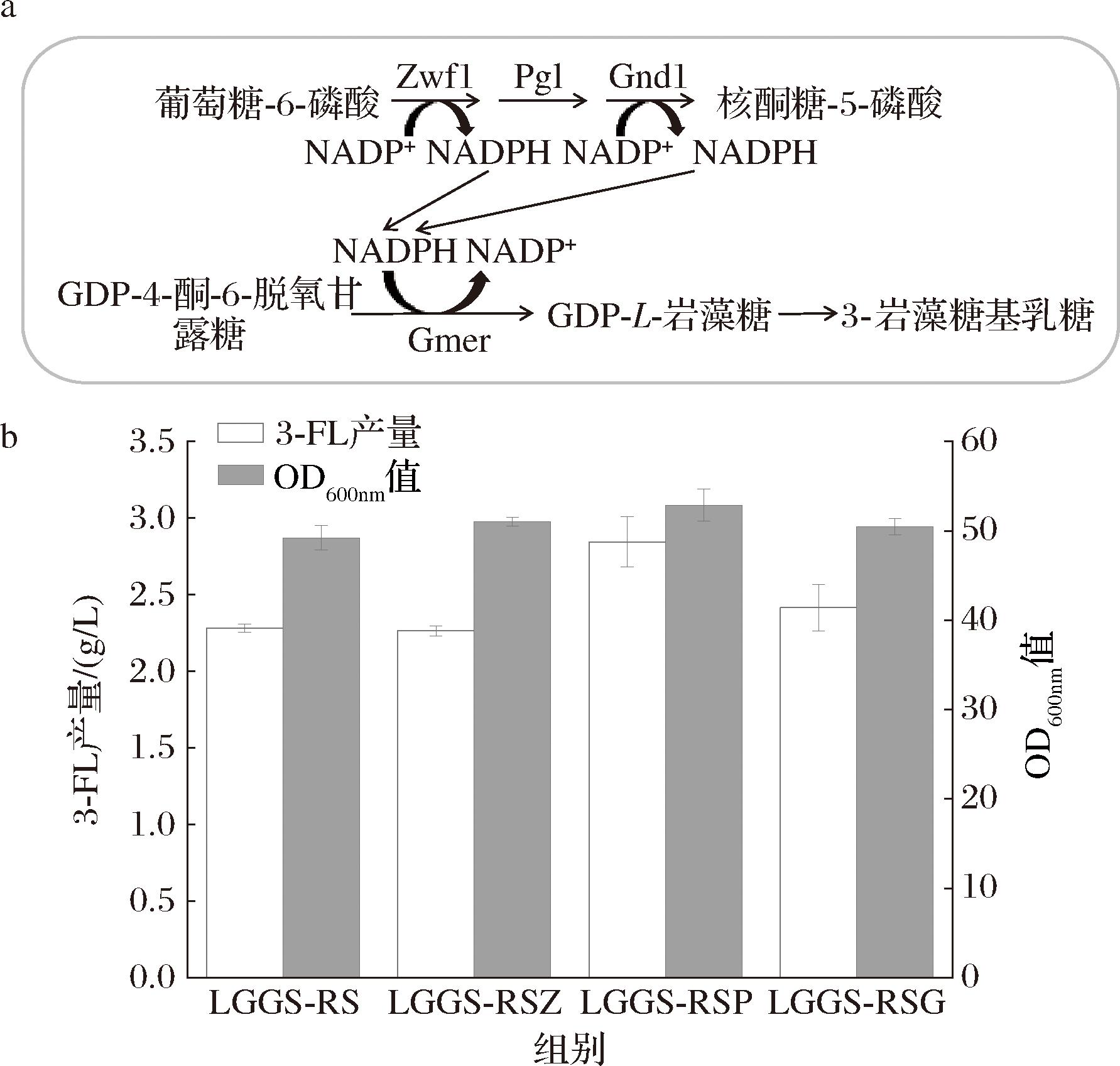
a-NADPH再生途径示意图;b-LGGS-RS基础上增加zwf1、pgl、gnd1拷贝数
图7 优化NADPH供应模块提高3-FL产量
Fig.7 Improving 3-FL production by optimizing NADPH supply module
注:LGGS-RSZ菌株过表达zwf1基因、LGGS-RSP菌株过表达pgl基因、LGGS-RSG菌株过表达gnd1基因。
2.5 发酵罐补料分批发酵
为了进一步研究重组菌株的生产性能,在5 L发酵罐中对菌株LGGS-RSP进行补料分批发酵,结果如图8所示,在12 h开始流加200 g/L的乳糖,在18 h葡萄糖将要耗尽时流加500 g/L的葡萄糖,结果显示,3-FL在对数生长期迅速积累,在60 h时质量浓度达14.70 g/L,生产效率为0.245 g/(L·h),5 L发酵罐产量约为摇瓶的5倍。
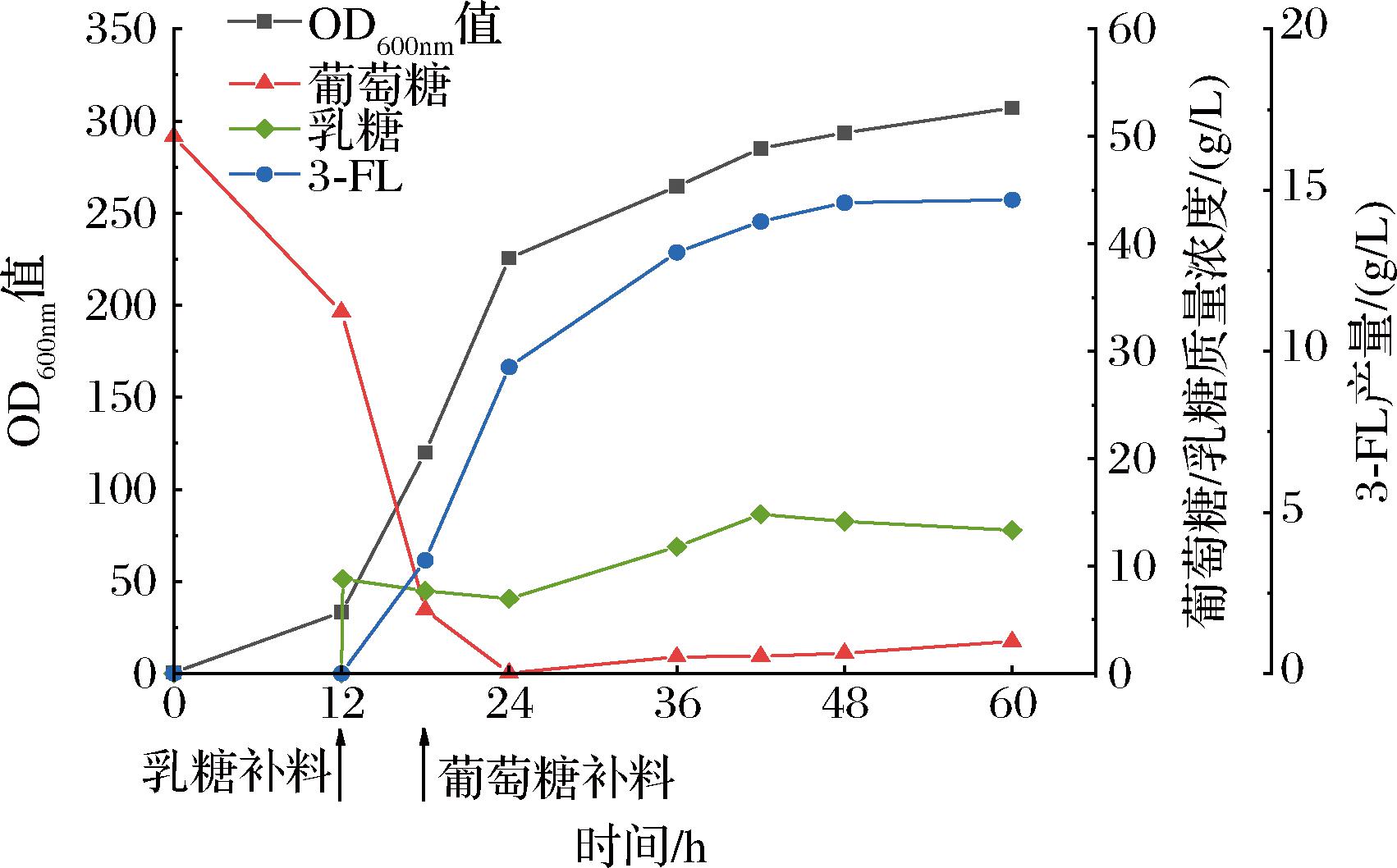
图8 5 L发酵罐补料分批发酵
Fig.8 Fed-batch fermentation in a 5 L fermentor
同XU等[10]在酿酒酵母中合成3-FL的研究相比,本研究重组菌株的摇瓶产量2.84 g/L高于其2.36 g/L,发酵罐产量14.70 g/L低于其20.91 g/L。不过,其产物积累于36 h后的平稳期阶段,发酵周期为108 h,生产效率为0.19 g/(L·h),低于本研究,故从生产效率的角度看,本研究所构建的菌株具有优势。
3 结论与讨论
作为人乳寡糖的重要组成部分,3-FL在婴儿的发育过程中发挥着重要作用,其在促进消化健康等方面的功能已被广泛研究,并被美国食品药品监督管理局批准为一般认可安全(Generally Recognized as Safe,GRAS),凭借其独特的生物学功能和安全性,3-FL展现出较大的商业化应用潜力[3-4]。本研究首次以Y.lipolytica作为底盘细胞,成功构建了3-FL的代谢通路。通过系统筛选,确定了适合在Y.lipolytica中高效发挥作用的3-岩藻糖基转移酶Fut3Bc。同时,研究明确了3-FL合成代谢的限速步骤为代谢通路的最后一步,即由Fut3Bc催化GDP-L-岩藻糖和乳糖合成3-FL的反应。
随后,本研究针对3-FL合成代谢通路的限速步骤进行了菌株改造。首先是对Fut3Bc添加蛋白标签,发现SUMO标签效果最佳,这一结果同HOLLANDS等[13]对2′-岩藻糖基转移酶添加SUMO标签的研究结果相似,这在一定程度上表明SUMO标签适合应用在Y.lipolytica中;之后对SUMO-fut3Bc进行了多拷贝整合,显著提升了3-FL的产量,同LGGF3相比,提升幅度达到245%。由于3-FL的代谢途径中涉及NADPH参与的氧化还原反应,本研究通过过表达PPP途径中的pgl基因来加强NADPH的供应以实现3-FL产量的进一步提升,最终得到的LGGS-RSP菌株摇瓶产量为2.84 g/L,发酵罐产量为14.70 g/L。虽然发酵罐产量不及酿酒酵母重组菌株,但本研究所构建的菌株在生产效率上具有一定的优势。此外,本研究发现尽管大部分3-FL被排到了胞外,但在胞内仍然存在相对较高的比例,这表明未来可以尝试引入转运蛋白以促进胞内产物的外排,从而进一步提升3-FL产量。后续,针对3-FL合成的相关竞争途径实施抑制策略,也可能对产量提升起到积极作用。虽然目前3-FL的产量尚未达到工业化生产的要求,但本研究成功实现了Y.lipolytica中3-FL的高效合成,开辟了利用酵母生产3-FL的新途径,为构建人乳寡糖细胞工厂提供了重要的理论依据和实践参考,也为开发高效、经济的3-FL工业化生产方案奠定了基础。
[1] ZHOU Y L, SUN H, LI K F, et al.Dynamic changes in human milk oligosaccharides in Chinese population:A systematic review and meta-analysis[J].Nutrients, 2021, 13(9):2912.
[2] BYCH K, MIK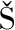 M H, JOHANSON T, et al.Production of HMOs using microbial hosts:From cell engineering to large scale production[J].Current Opinion in Biotechnology, 2019, 56:130-137.
M H, JOHANSON T, et al.Production of HMOs using microbial hosts:From cell engineering to large scale production[J].Current Opinion in Biotechnology, 2019, 56:130-137.
[3] DU Z H, LI Z Y, GUANG C E, et al.Recent advances of 3-fucosyllactose in health effects and production[J].Archives of Microbiology, 2024, 206(9):378.
[4] LI Z Y, ZHU Y Y, NI D W, et al.Occurrence, functional properties, and preparation of 3-fucosyllactose, one of the smallest human milk oligosaccharides[J].Critical Reviews in Food Science and Nutrition, 2023, 63(28):9364-9378.
[5] CHEN G, WU H, ZHU Y Y, et al.Glycosyltransferase from Bacteroides gallinaceum is a novel a-1,3-fucosyltransferase that can be used for 3-fucosyllactose production in vivo by metabolically engineered Escherichia coli[J].Journal of Agricultural and Food Chemistry, 2022, 70(6):1934-1942.
[6] DU Z H, ZHU Y Y, LU Z, et al.Combinatorial optimization strategies for 3-fucosyllactose hyperproduction in Escherichia coli[J].Journal of Agricultural and Food Chemistry, 2024, 72(25):14191-14198.
[7] LEE J W, KWAK S, LIU J J, et al.Enhanced 2′-fucosyllactose production by engineered Saccharomyces cerevisiae using xylose as a co-substrate[J].Metabolic Engineering, 2020, 62:322-329.
[8] LIU J J, KWAK S, PATHANIBUL P, et al.Biosynthesis of a functional human milk oligosaccharide, 2′-fucosyllactose, and l-fucose using engineered Saccharomyces cerevisiae[J].ACS Synthetic Biology, 2018, 7(11):2529-2536.
[9] YU S, LIU J J, YUN E J, et al.Production of a human milk oligosaccharide 2'-fucosyllactose by metabolically engineered Saccharomyces cerevisiae[J].Microbial Cell Factories, 2018, 17(1):101.
[10] XU M Y, SUN M T, MENG X F, et al.Engineering pheromone-mediated quorum sensing with enhanced response output increases fucosyllactose production in Saccharomyces cerevisiae[J].ACS Synthetic Biology, 2023, 12(1):238-248.
[11] LIU H H, JI X J, HUANG H.Biotechnological applications of Yarrowia lipolytica:Past, present and future[J].Biotechnology Advances, 2015, 33(8):1522-1546.
[12] BLANK L M, LEHMBECK F, SAUER U.Metabolic-flux and network analysis in fourteen hemiascomycetous yeasts[J].FEMS Yeast Research, 2005, 5(6-7):545-558.
[13] HOLLANDS K, BARON C M, GIBSON K J, et al.Engineering two species of yeast as cell factories for 2′-fucosyllactose[J].Metabolic Engineering, 2019, 52:232-242.
[14] FAIJES M, CASTEJ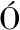 N-VILATERSANA M, VAL-CID C, et al.Enzymatic and cell factory approaches to the production of human milk oligosaccharides[J].Biotechnology Advances, 2019, 37(5):667-697.
N-VILATERSANA M, VAL-CID C, et al.Enzymatic and cell factory approaches to the production of human milk oligosaccharides[J].Biotechnology Advances, 2019, 37(5):667-697.
[15] XIE Y K, WU X Y, FU C, et al.Rational design of an a-1,3-fucosyltransferase for the biosynthesis of 3-fucosyllactose in Bacillus subtilis ATCC 6051a via de novo GDP-l-fucose pathway[J].Journal of Agricultural and Food Chemistry, 2024, 72(2):1178-1189.
[16] HUANG D, YANG K X, LIU J, et al.Metabolic engineering of Escherichia coli for the production of 2′-fucosyllactose and 3-fucosyllactose through modular pathway enhancement[J].Metabolic Engineering, 2017, 41:23-38.
[17] LI M L, LI C C, LUO Y J, et al.Multi-level metabolic engineering of Escherichia coli for high-titer biosynthesis of 2′-fucosyllactose and 3-fucosyllactose[J].Microbial Biotechnology, 2022, 15(12):2970-2981.
[18] NI Z J, WU J Y LI Z K, et al.Enhanced bioproduction of fucosylated oligosaccharide 3-fucosyllactose in engineered Escherichia coli with an improved de novo pathway[J].Bioscience, Biotechnology, and Biochemistry, 2021, 85(7):1772-1781.
[19] CHOI Y H, KIM J H, PARK B S, et al.Solubilization and iterative saturation mutagenesis of a1,3-fucosyltransferase from Helicobacter pylori to enhance its catalytic efficiency[J].Biotechnology and Bioengineering, 2016, 113(8):1666-1675.
[20] XIE X, WU P, HUANG X C, et al.Retro-protein XXA is a remarkable solubilizing fusion tag for inclusion bodies[J].Microbial Cell Factories, 2022, 21(1):51.
[21] LIN L, GONG M Y, LIU Y F, et al.Combinatorial metabolic engineering of Escherichia coli for de novo production of 2′-fucosyllactose[J].Bioresource Technology, 2022, 351:126949.
[22] ZHANG Y, ZHANG X J, LIU H Y, et al.Efficient production of 2′-fucosyllactose in unconventional yeast Yarrowia lipolytica[J].Synthetic and Systems Biotechnology, 2023, 8(4):716-723.
[23] HUANG H Y, YU W W, XU X H, et al.Combinatorial engineering of Escherichia coli for enhancing 3-fucosyllactose production[J].American Chemical Society Synthetic Biology, 2024, 13(6):1866-1878.
[24] CHENG H L, WANG S Q, BILAL M, et al.Identification, characterization of two NADPH-dependent erythrose reductases in the yeast Yarrowia lipolytica and improvement of erythritol productivity using metabolic engineering[J].Microbial Cell Factories, 2018, 17(1):133.