柿原花青素(persimmon proanthocyanidin,PPAs)是从柿属植物中提取的一类天然多酚类化合物,具有独特的化学结构和显著的生物活性[1]。其中,原翠雀定结构占58.7%,棓酰化程度高达72.4%,A型和B型连接共存,特征结构单元包括A型连接ECG二聚体和A型连接EGCG二聚体等[2](图1)。AKAGI等[3]确定表没食子儿茶素-3-O-没食子酸酯(epigallocatechin gallate,EGCG)是其主要结构单元。近年研究表明,PPAs不仅展现出强大的自由基清除能力和抗炎特性,还在调节脂代谢、抑制肿瘤细胞增殖及改善心血管功能等方面表现出潜在应用价值[4]。但PPAs的生物利用率较低,这源于其高聚合度与分子质量限制了其在肠道中的吸收,且其与黏蛋白、脂质等物质的结合减少游离态的产生以及环境因素也会影响其生物利用率。
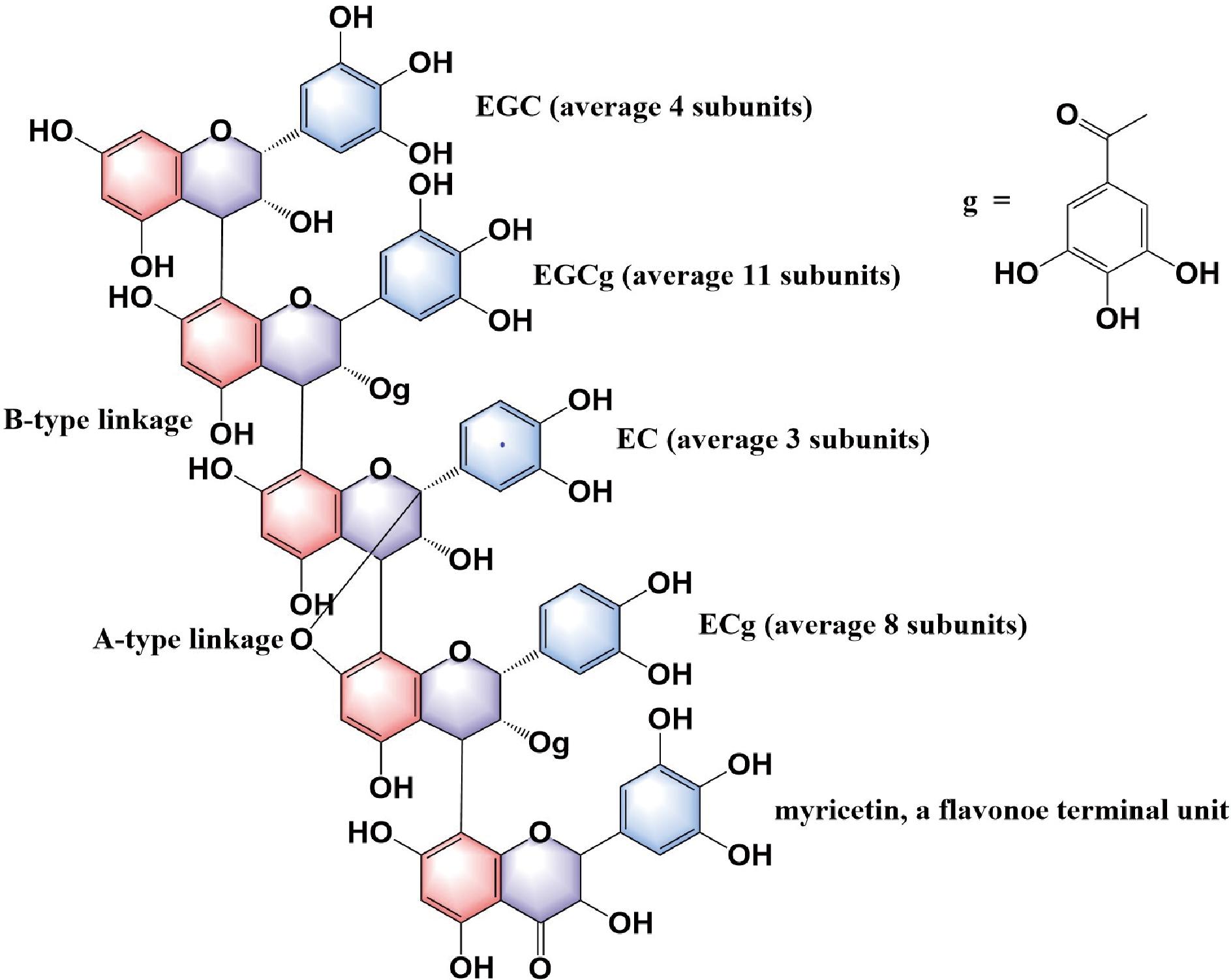
图1 柿原花青素结构[5]
Fig.1 Structure of persimmon proanthocyanidins
注:EGC:表没食子儿茶素,epigallocatechin;EGCg:表没食子儿茶素没食子酸酯,epigallocatechin gallate;EC:表儿茶素,epicatechin; ECg:表儿茶素没食子酸酯,epicatechin gallate。
肠上皮屏障赋予肠上皮选择通透性和抵御病原体侵袭等功能,其功能障碍与肠道通透性改变和炎症的发生密切相关。通过探寻天然活性成分的抗炎机制,并对肠屏障损伤进行干预受到学界的广泛关注。以原花青素为代表的多酚类物质,通过调控炎症因子表达、抑制氧化应激通路等多重作用机制,在改善肠屏障损伤方面展现出独特优势[6],这为开发新型个性化功能性食品提供了科学依据。
目前,研究人员已建有多种氧化应激模型,如孙雅望[7]利用脂多糖(lipopolysaccharide,LPS)诱导牛乳腺上皮细胞建立氧化应激模型以探究不同浓度LPS诱导对牛乳腺上皮细胞的影响。任李梅[8]利用LPS诱导RAW264.7细胞建立炎症模型研究人参根提取物及其有效成分对于抗炎、抗氧化的保护作用以及其作用机制。AMARASIRI等[9]使用人结直肠腺癌细胞来探索吲哚丙烯酸对LPS诱导的炎症的保护作用。表皮生长因子受体(epidermal growth factor receptor,EGFR)位于细胞膜脂质筏区域,在调节细胞增殖、分化以及炎症发生等生理生化过程中发挥重要作用[10]。过度激活EGFR将影响细胞外调节蛋白激酶(extracellular regulated protein kinases 1/2,ERK1/2)相关信号的传导,从而干扰紧密连接紧密连接蛋白-1(zonula occludens-1,ZO-1)等和黏蛋白的表达水平,导致肠上皮屏障损伤[11]。尽管已有大量研究通过建立细胞损伤模型来探索活性物质的相关调控机制,但PPAs对肠道屏障损伤的修复或缓解机制仍不清晰,通过探寻功能因子与肠屏障稳态相互影响的关联机制,有助于阐明原花青素在肠道中所发挥的健康效应,并为创制适合特殊人群食用的专用型膳食提供理论依据。
1 材料和方法
1.1 材料与试剂
低糖杜尔贝科改良伊格尔培养基(Dulbecco’s modified eagle medium, DMEM)、胎牛血清(fetal bovine serum, FBS)、胰蛋白酶-EDTA(乙二胺四乙酸,ethylenediaminetetraacetic acid)(0.25%,质量分数),上海达特希尔生物科技有限公司;双抗、抗荧光衰减封片剂、二甲亚砜(dimethyl sulfoxide,DMSO)、多聚甲醛,大连美仑生物技术有限公司;甲基噻唑基二苯基四氮唑溴盐(methylthiazolyldiphenyl-tetrazolium bromide assay,MTT)、碘化丙啶(propidium iodide staining solution, PI)染色剂,北京索莱宝科技有限公司;LPS,西格玛奥德里奇(上海)贸易有限公司;NO试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒、丙二醛(malondialdehyde,MDA)试剂盒、乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒、碱性磷酸酶(alkaline phosphatase,AKP)试剂盒,南京建成生物有限公司;ZO-1多克隆抗体、Fluorescein (FITC)-标记的山羊抗兔IgG(H+L),武汉三鹰生物技术有限公司;PBS缓冲液,实验室自配(g/L):0.144 KH2PO4,9 NaCl,0.795 Na2HPO4 · 7H2O,试剂均来源于天津市大茂化学试剂厂;二喹啉甲酸(bicinchoninic acid,BCA)试剂盒、 0.1%Tween(质量分数),碧云天生物技术有限公司;PBST(含0.1% Tween,质量分数),兰杰柯科技有限公司。
1.2 仪器与设备
Tecan Spark 20M多功能微孔板读数仪,奥地利Tecan有限公司;Beckman CytoFLEX S流式细胞仪,贝克曼库尔特有限公司;YXQ-5OA高压灭菌锅,上海博讯医疗生物科技有限公司;SW-CJ-1FD无菌操作台,苏州净化设备有限公司;3111型CO2培养箱,赛默飞世尔科技公司;H1650-W台式高速冷冻离心机、HH-2恒温水浴锅,湖南湘仪实验室仪器开发有限公司;FV3000激光共聚焦显微镜,奥林巴斯(中国)有限公司。
1.3 实验方法
1.3.1 PPAs制备
参考ZOU等[12]的方法稍作修改,将采摘的柿果在100 ℃的开水中热烫5 min,置于-20 ℃冷冻保存备用。本文所采用的浸提液为1%(体积分数)的盐酸-甲醇,按料液比1∶8(g∶mL)于80 ℃冷凝回流重复提取3次,每次40 min,合并浸提液,35 ℃旋蒸浓缩去除甲醇;浓缩液经AB-8大孔树脂吸附40 min,后经去离子水、15%(质量分数)乙醇溶液对糖类、低分子质量酚类化合物等杂质进行去除,再采用95%(质量分数)乙醇洗脱,收集洗脱液进行旋转蒸发去除乙醇,真空冷冻干燥后得到PPAs样品。以甲醛沉淀法测得PPAs的纯度为96.52%(质量分数),经检测所得PPAs平均聚合度为26,平均分子质量为10.7 kDa[5]。
1.3.2 细胞复苏与培养
将冻存的Caco-2细胞转入37 ℃的恒温水浴锅中孵育,并顺时针摇动使其快速融化后2 500 r/min离心3 min,弃去上清液,加1 mL的10%(体积分数)FBS-DMEM培养液,轻轻吹打,待细胞重悬后转移到培养瓶中,加入11 mL完全培养基,再次轻轻吹打使细胞均匀,置于37 ℃、5%(体积分数)的CO2培养箱中培养,次日换液,同时每天观察和记录细胞的生长状态。
1.3.3 存活率检测
使用MTT法评估PPAs的细胞毒性。将胰酶消化后的Caco-2细胞接种至96孔板,接种密度为8 000个/孔,每梯度浓度做6孔重复,待细胞贴壁后,换无血清培养基同化12 h,设置空白组、对照组及实验组,实验组添加含有不同质量浓度PPAs(5、15、30、45、60、75、90 μg/mL)的培养液,对照组添加含有等浓度DMSO的培养基代替,空白组则不含细胞,干预24 h,然后加0.5 mg/mL的MTT检测液150 μL,培养箱孵育4 h后移除MTT,每孔加入150 μL的DMSO后置于酶标仪37 ℃振荡10 min,于490 nm波长处测定每个吸光度,细胞存活率的计算如公式(1)所示:
细胞存活率![]()
(1)
1.3.4 LPS诱导实验
取对数生长期的Caco-2细胞接种于12孔培养板,待细胞贴壁后,更换无血清培养基同化12 h,空白组加入2 mL完全培养基,诱导组和干预组则加入2 mL含LPS(终质量浓度100 μg/mL)的完全培养基,干预组则同时加入含不同浓度PPAs(终质量浓度分别为5、15、30、45 μg/mL)的完全培养基,24 h后观察细胞损伤状态,并检测培养液及细胞中氧化应激相关指标。
1.3.5 LDH、AKP活力的测定
取对数生长期的Caco-2细胞接种于6孔培养板,待细胞贴壁后,PBS清洗3遍,更换无血清培养基同化12 h,空白组、LPS组和PPAs组继续使用不含酚红的完全培养液孵育24 h,吸取细胞培养液,1 000 r/min离心10 min,取上清液用于检测AKP及LDH的活力。使用BCA试剂盒来测量细胞样本中的蛋白质浓度,并以mg prot/mL作为计算单位。
通过使用LDH试剂盒来测量培养液中LDH的活力,并在波长为450 nm的条件下对各个孔的吸光度进行测量,LDH活力数值的计算如公式(2)所示:
培养液中LDH的活力/(U/g prot)=![]() 酚标准品浓度(0.2 μmol/mL)÷待测样品蛋白浓度/(g prot/mL)
酚标准品浓度(0.2 μmol/mL)÷待测样品蛋白浓度/(g prot/mL)
(2)
利用AKP测定试剂盒测定培养液中AKP的活力,在波长520 nm下检测各孔吸光度值,AKP活力的计算如公式(3)所示:
培养液中AKP的活力/(金氏单位/g prot)=![]() 酚标准品浓度(0.1 mg/mL)÷待测样品蛋白浓度/(g prot/mL)
酚标准品浓度(0.1 mg/mL)÷待测样品蛋白浓度/(g prot/mL)
(3)
1.3.6 SOD活力测定
以1.3.5节所述方法收集细胞后,采用黄嘌呤氧化酶法测定SOD的活力,加入提取液,超声破碎细胞,在4 ℃,8 000×g条件下离心10 min,取上清液,置于冰上,待测。利用SOD试剂盒来测定细胞内总SOD活力,并在波长为550 nm的地方测量各孔的吸光度,细胞中总SOD活力值的计算如公式(4)所示:
细胞中总SOD活力值/(U/mg prot)=![]() 相同均浆浓度下的蛋白含量/(mg prot/mL)
相同均浆浓度下的蛋白含量/(mg prot/mL)
(4)
使用BCA试剂盒来测量细胞样本中的蛋白质浓度,并以mg prot/mL作为计算单位。
1.3.7 MDA含量测定
以1.3.5节所述方法收集细胞后,用超声粉碎机粉碎,功率1 200 W,每次5 s,间隔10 s反复进行粉碎3~5次。按照试剂盒的规定,设置空白孔、标准孔、测定孔以及对照孔,并按顺序加入各反应液。将离心管密封完全,用针在离心管盖子上扎一小孔,充分混匀,95 ℃水浴40 min,取出后流水冷却,3 500 r/min,离心10 min,取上清液,置于酶标仪在490 nm波长处测定每个吸光度,完成对于Caco-2细胞内MDA含量的测定,计算如公式(5)所示:
细胞中MDA含量![]() 标准品浓度(10 nmol/mL)÷待测样本蛋白浓度/(mg prot/mL)
标准品浓度(10 nmol/mL)÷待测样本蛋白浓度/(mg prot/mL)
(5)
使用BCA试剂盒测量细胞样本中蛋白质浓度,并以mg prot/mL作为计算单位。
1.3.8 NO的测定
以1.3.5节所述方法收集细胞后,根据NO试剂盒的说明书测定细胞内NO含量,按步骤加入样本和R1、R2混合试剂,37 ℃水浴60 min,加入R3、R4试剂,抽提室温静置40 min,3 500~4 000 r/min,离心10 min,取上清液,加入显色剂,静置10 min,于550 nm波长下检测吸光度从而计算出NO含量。
1.3.9 流式细胞仪测定
参考于志辉等[13]的方法稍作修改。以1.3.5节所述方法收集细胞,然后用PI染色0.5 h,用流式细胞仪对细胞凋亡的情况进行检测。
1.3.10 实时逆转录聚合酶链式反应(real-time reverse transcription polymerase chain reaction,real-time RT-PCR)检测
参考慈小燕等[14]的方法稍作修改。以1.3.5节所述方法处理细胞后,使用Total RNA Extractor裂解液将细胞收集,细胞密度为2×105/样,委托生工生物工程(上海)股份有限公司进行检测。检测采用RT-PCR技术,数据分析采用ΔΔCt法,以GAPDH为内参基因(表1)。每组实验重复3次。
表1 EGFR相关基因引物序列
Table 1 The primer sequence of EGFR related genes

基因引物序列GAPDHForward5′-AGAAGGCTGGGGCTCATTTG-3′Reverse5′-AGGGGCCATCCACAGTCTTC-3′EGFRForward5′-CGTTTGGGAGTTGATGACCTTTG-3′Reverse5′-CACGGAACTTTGGGCGACTATC-3′ERK1/2Forward5′-TCAACACCACCTGCGACCTT-3′Reverse5′-GCGTAGCCACATACTCCGTCA-3′NF-κBForward5′-AGCAAATAGACGAGCTCCGA-3′Reverse5′-TCGGTAAAGCTGAGTTTGCG-3′
1.3.11 ZO-1蛋白免疫荧光染色
参照刘欢等[15]的方法稍作修改。以1.3.5节所述方法处理细胞后,弃去培养液,PBS清洗3遍,使用4%(质量分数)多聚甲醛溶液常温固定20 min,PBS洗3次。在0.1%(质量分数)Triton X-100孵育10 min,PBS洗3次。添加封闭溶液孵育1 h。吸弃封闭液,用抗体稀释缓冲液稀释ZO-1多克隆抗体。设置空白对照(在不加一抗的抗体稀释缓冲液中培养),常温孵育1 h,用1×PBST清洗3次,每次5 min。加入用抗体稀释缓冲液稀释的FITC标记的山羊抗兔IgG(H+L),并在黑暗的环境中室温孵育1 h。用PBST清洗3次,每次5 min。用封片剂将样本封固在单孔培养板中,用激光共聚焦显微镜(confocal laser scanning microscopy,CLSM)进行观察,使用Image J软件对荧光强度进行统计分析。
1.4 数据处理
使用IBM SPSS Statistics 26软件对数据进行显著性分析,并利用origin 2021软件制作统计图。完成方差齐性检验后,使用Tukey’s多重检验评估各组分差异,在P<0.05时认定存在显著性差异,显著程度:a>b>c>d>e>f。
2 结果与分析
2.1 毒性作用评价
目前,MTT染色法是广泛采用的细胞毒性检测技术,由于死细胞内缺乏琥珀酸脱氢酶,无法将MTT还原,因此甲臜的产生量仅与样本中活细胞的数量成正比[16]。由图2可知,高质量浓度的PPAs(>60 μg/mL)处理后均会显著降低Caco-2细胞的存活率,PPAs干预质量浓度选为0~45 μg/mL最为适宜。
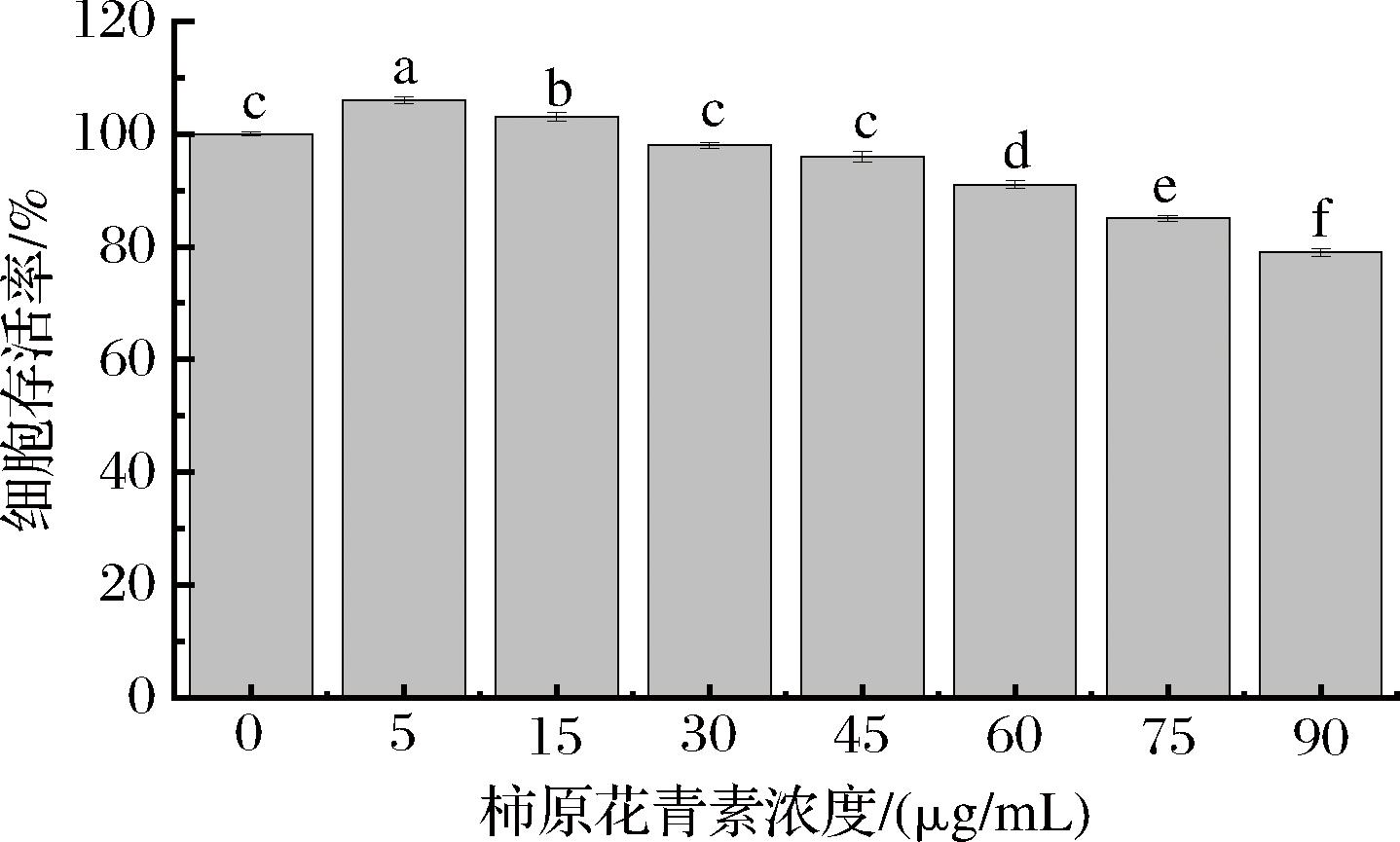
图2 PPAs对于Caco-2细胞存活率的影响
Fig.2 Effect of PPAs on the survival rate of Caco-2 cells
注:图中不同字母表示显著性差异(P<0.05)(下同)。
2.2 细胞通透性评价
AKP是一种在Caco-2细胞单层形成过程中分化出来的刷状缘的标志性酶。LDH是一种在机体受损时会释放的物质,当细胞受到严重的损伤时,其释放量也会相应增加。PAN等[17]使用原花青素处理TM3细胞,通过检测LDH发现原花青素可以有效减轻细胞损伤。Caco-2细胞在LPS的刺激下,细胞培养上清中的AKP和LDH的含量均有显著升高(P<0.05),表明LPS对Caco-2细胞有明显的损伤作用。而在PPAs干预组中,Caco-2细胞培养液中LDH和AKP的活力随PPAs干预浓度的增加均显著降低(图3),表明PPAs可有效改善Caco-2细胞的通透性,能使Caco-2细胞损伤明显减轻。
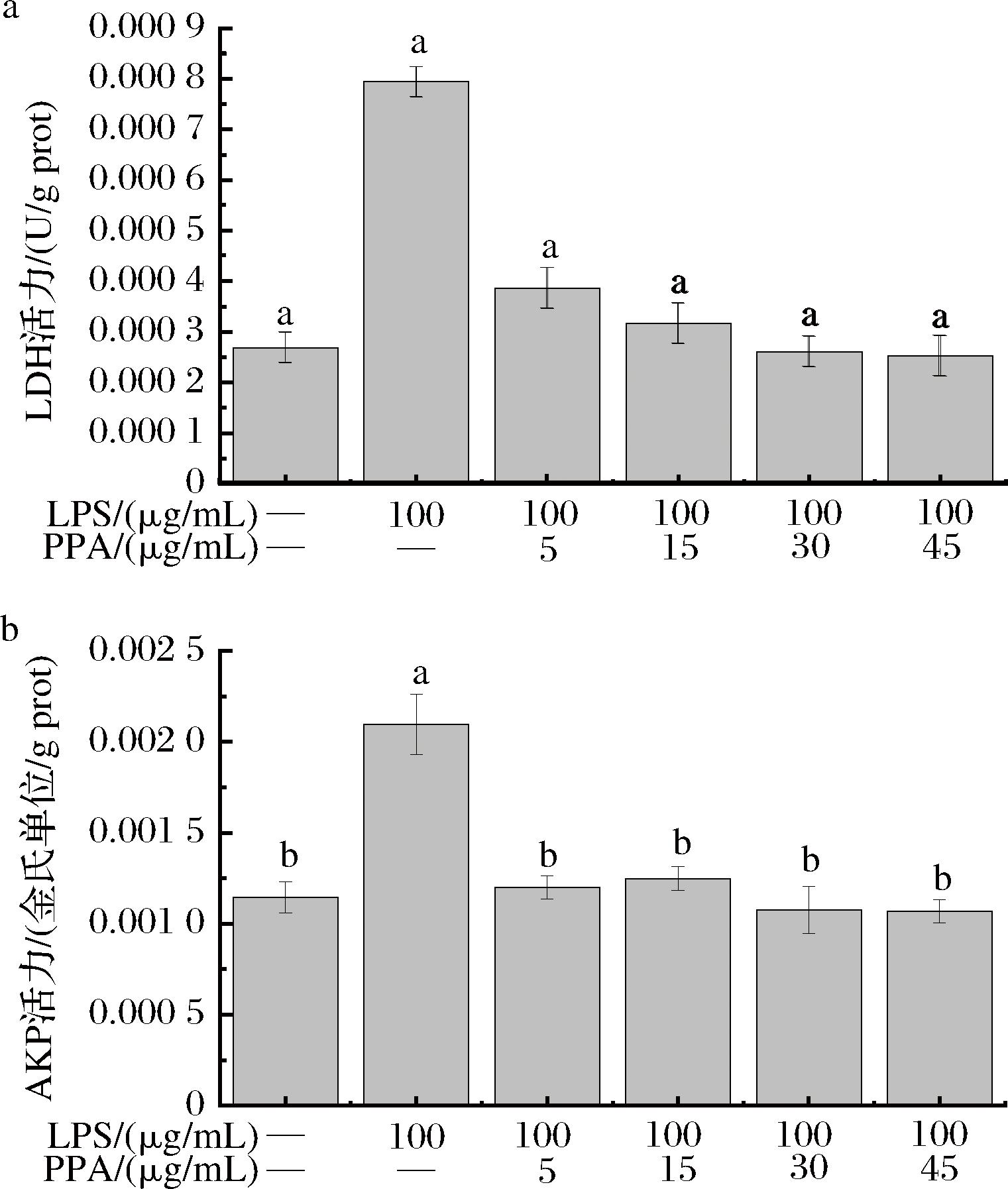
a-LDH活力;b-AKP活力
图3 PPAs对LPS诱导的Caco-2细胞液中LDH和AKP活力的影响
Fig.3 Effect of PPAs on LDH and AKP activity in LPS-induced Caco-2 cell supernatant
注:—表示未添加(下同)。
2.3 SOD活力影响评价
SOD可有效应对机体氧化应激,缓解机体衰老、抗炎症、增加机体免疫与抗辐射的功能[18]。将不同浓度PPAs加入经LPS诱导后的Caco-2细胞内后,总SOD活力的变化如图4所示。相较于对照组不同浓度PPAs处理的Caco-2细胞均与对照组有显著降低(P<0.05)。随着浓度的上升,细胞内总SOD活力也有显著上升,故总SOD活力与PPAs浓度呈明显正相关。结果显示,PPAs可有效增加Caco-2细胞内总SOD活力,对细胞损伤有明显的修复作用。
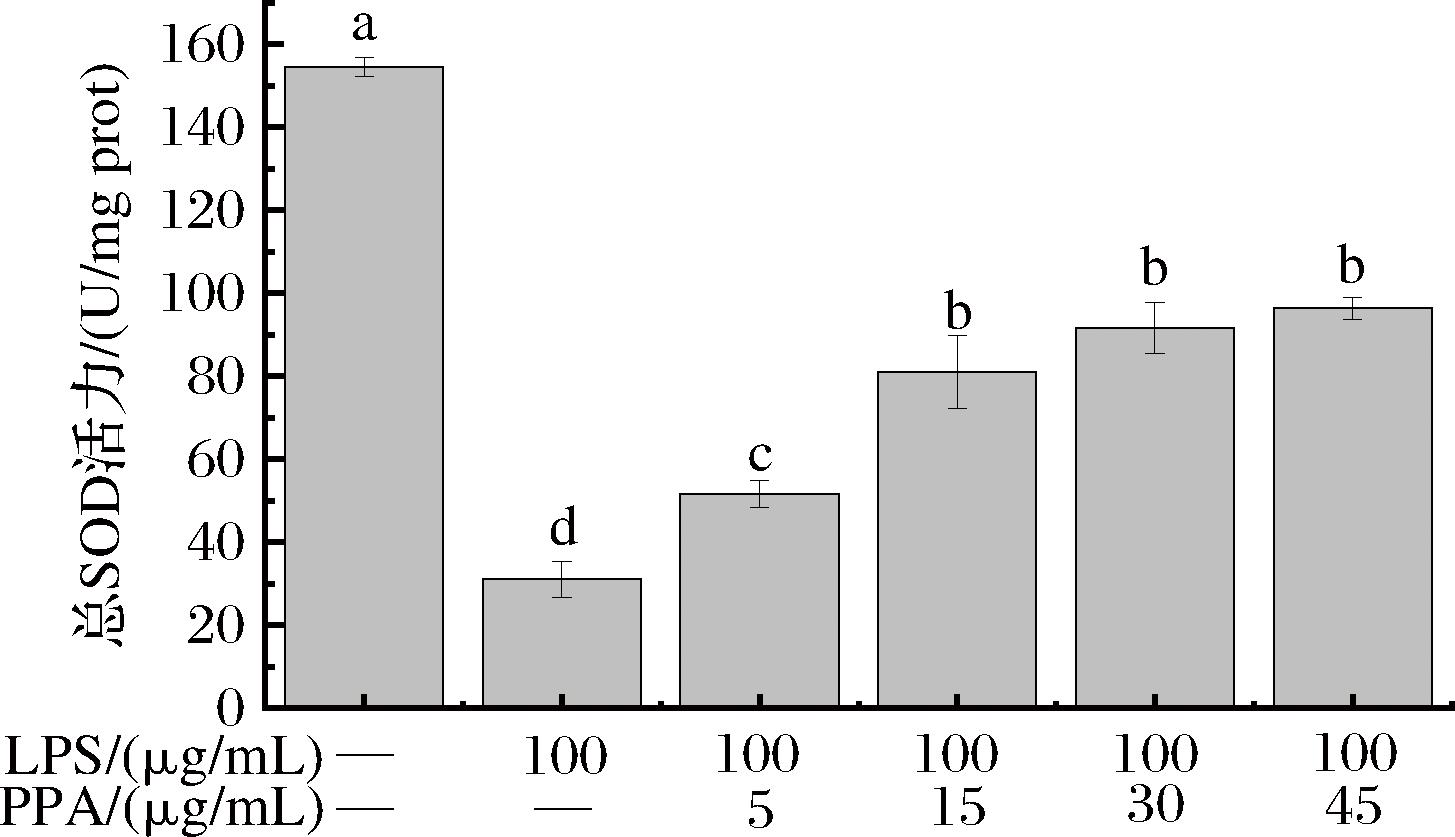
图4 PPAs对LPS诱导的Caco-2细胞内总SOD活力的影响
Fig.4 Effect of PPAs on total SOD activity of Caco-2 cells induced by LPS
2.4 MDA含量影响评价
人体是否处于氧化损伤状态,通常可以借助MDA反映氧化损伤的程度。当细胞损伤程度减轻时,MDA会处于较低水平状态[19]。在Caco-2细胞中,MDA含量的上升表明细胞已进入受损阶段(图5)。将不同浓度PPAs加入到经LPS诱导的Caco-2细胞中后,细胞内MDA的含量与PPAs浓度呈反比,随着PPAs浓度的不断增加,Caco-2细胞内的MDA含量先迅速下降后呈平稳趋势。对比空白对照组的数据说明细胞受到氧化损伤时,MDA水平会显著升高(P<0.05)。在PPAs干预组,Caco-2细胞内MDA含量显著下降(P<0.05),表明PPAs对于Caco-2细胞的氧化损伤有显著的修复作用。
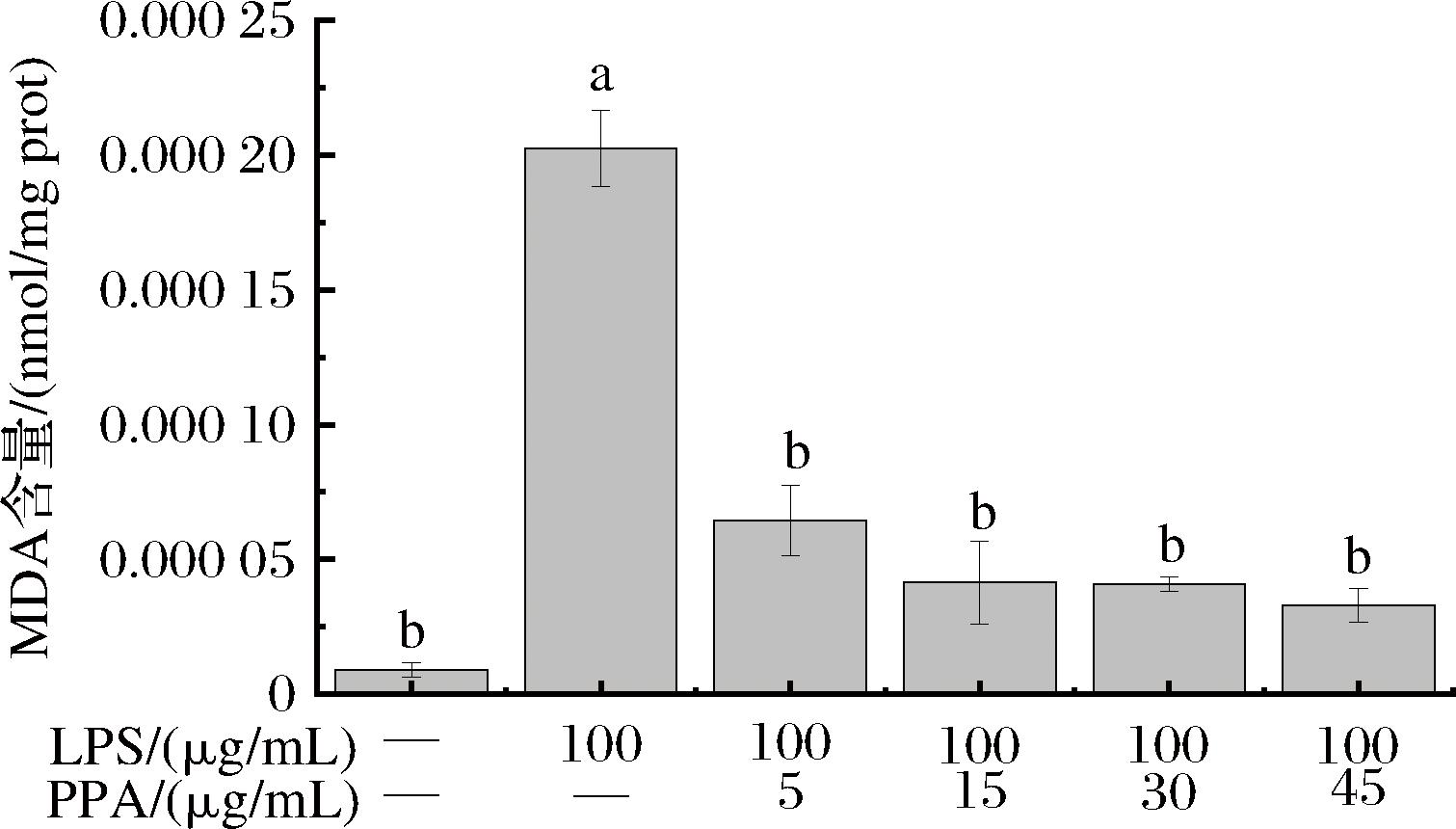
图5 PPAs对LPS诱导的Caco-2细胞内MDA含量的影响
Fig.5 Effect of PPAs on MDA content of Caco-2 cells induced by LPS
2.5 NO含量影响评价
NO是一种具有高度化学活性的自由基,若出现异常,可能会导致相关疾病的出现。陈素领等[20]研究了大黄素可以减轻NO自由基对神经细胞的损伤。如图6所示,使用LPS诱导Caco-2细胞后,与对照组相比,体系中NO含量是对照组的24倍,显著升高(P<0.05)。PPAs的干预使得Caco-2细胞中NO含量均有所下降。故PPAs有助于显著降低LPS诱发的细胞氧化损伤。
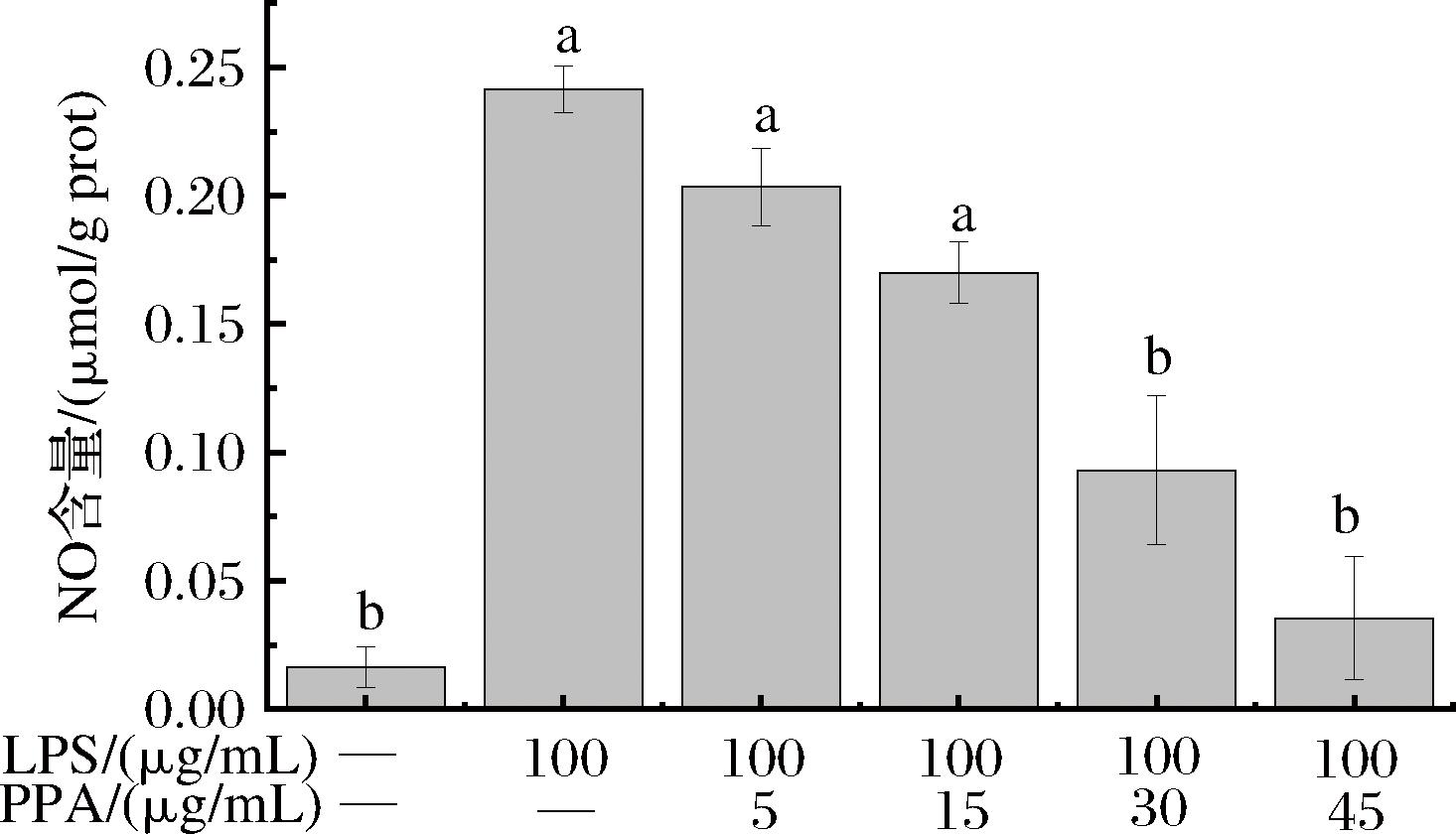
图6 PPAs对LPS诱导的Caco-2细胞内NO含量的影响
Fig.6 Effect of PPAs on NO content of Caco-2 cells induced by LPS
2.6 流式细胞仪检测分析
细胞凋亡是一种由细胞基因发生自主、有序死亡的一种生理过程[21],如图7所示,相比于空白组,LPS诱导组的受损细胞占比增加至5.97%,经不同浓度PPAs干预后,受损细胞明显减少,未受损细胞数量增加。流式细胞仪结果进一步证实PPAs的添加改善了LPS对Caco-2细胞带来的氧化损伤。张莲莲等[22]也采用流式细胞术研究了蓝莓原花青素抗氧化应激血管损伤的机制,其研究结果表明蓝莓原花青素同样具有一定的抗氧化性。
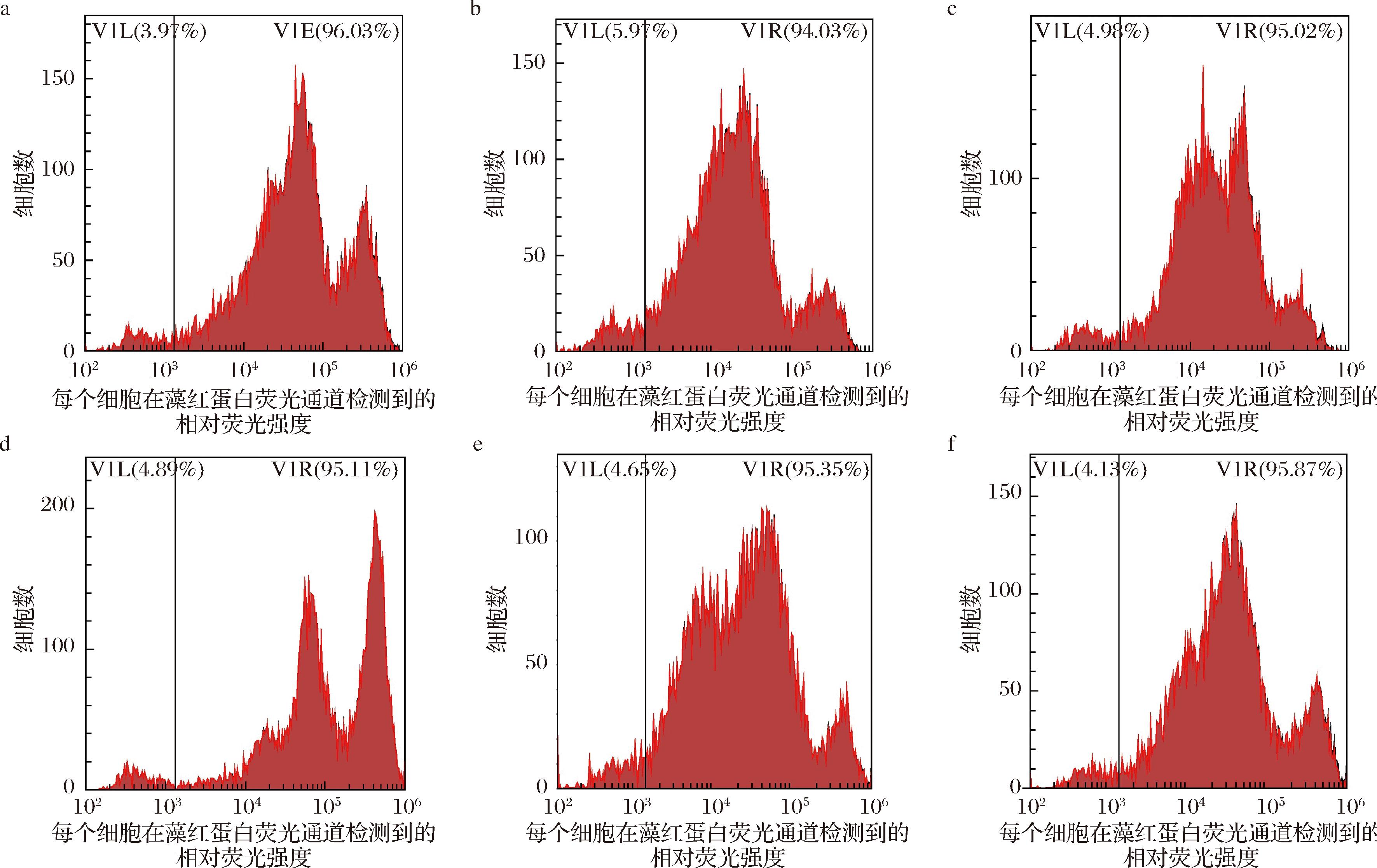
a-空白组;b-对照组(LPS);c-LPS+PPA5 μg/mL;d-LPS+PPA15 μg/mL;e-LPS+PPA30 μg/mL;f-LPS+PPA45 μg/mL
图7 PPAs对LPS诱导的Caco-2细胞凋亡的影响
Fig.7 Effect of PPAs on the apoptosis of Caco-2 cells induced by LPS
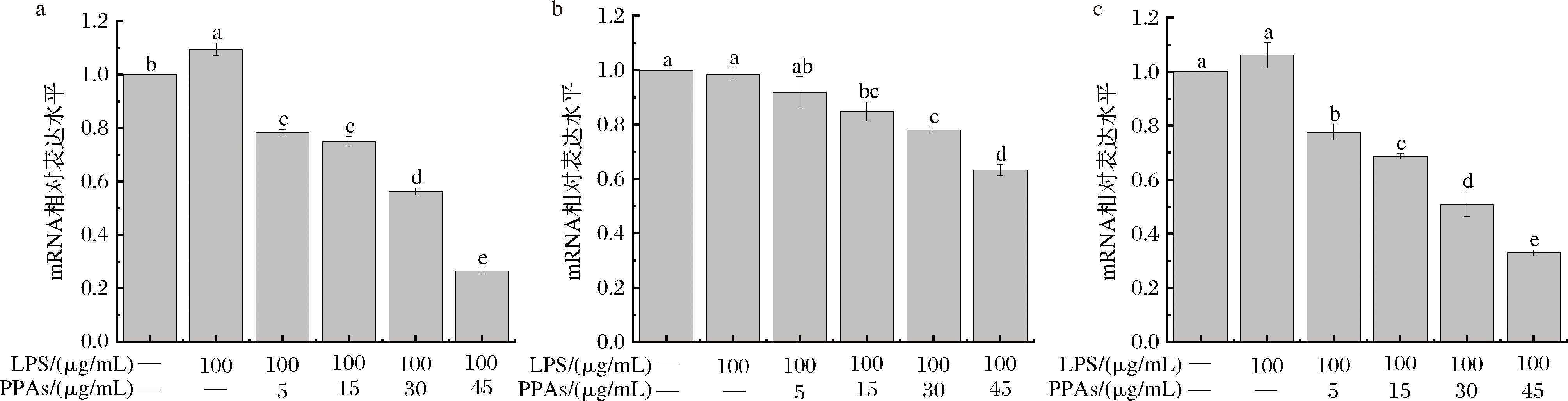
a-EGFR;b-ERK1/2;c-NF-κB
图8 PPAs对LPS诱导的Caco-2细胞EGFR信号通路相关基因表达的影响
Fig.8 Effects of PPAs on gene expression related to EGFR signaling pathway in Caco-2 cells induced by LPS
2.7 real-time RT-PCR结果分析
已有研究发现EGFR可以通过调控胞外信号调控激酶(ERK1/2)、核因子(NF-κB)而发挥多种生理功效。张秀娟等[23]也通过使用QRT-PCR进行葡萄籽原花青素预处理对LPS诱导的人牙龈上皮细胞(human gingival epithelial cells,HGECs)炎症介质表达的影响的研究,其结果显示,葡萄籽原花青素能够抑制促炎因子的表达并促进抗炎因子的表达。如图8 所示,LPS的诱导可以显著增加Caco-2细胞中EGFR mRNA的表达,经PPAs干预后,EGFR mRNA的相对表达量显著下降,并呈现出剂量依赖效应,但ERK1/2作为EGFR的下游基因,LPS的诱导并未显著促进其表达,而PPAs的干预显著抑制ERK1/2的表达,同样表现为剂量依赖效应;NF-κB在细胞炎症反应中发挥关键作用,LPS的诱导使其mRNA的表达有所提升,但与正常组相比,不存在显著性差异,PPAs的干预显著抑制其表达,表明PPAs通过抑制EGFR-ERK1/2-NF-κB通路而发挥改善细胞损伤的作用。
2.8 免疫荧光检测分析
ZO-1是一种紧密连接蛋白,是细胞膜上紧密连接的核心调控者,通过连接跨膜蛋白与细胞骨架,维持细胞膜的机械稳定性、通透性和极性,存在于细胞间接触的复合物中。与空白组和LPS诱导组相比,随着PPAs干预浓度的升高,绿色荧光明显增强(图9、图10),表明细胞膜上的ZO-1蛋白的表达明显增加,即PPAs促进了肠上皮细胞间紧密连接蛋白的表达,增强细胞屏障功能。同样的,张蕾等[24]通过免疫荧光研究发现,原花青素可以抑制宫颈癌细胞与上皮-间质转化相关的TGF-β1、E-钙黏蛋白的表达。
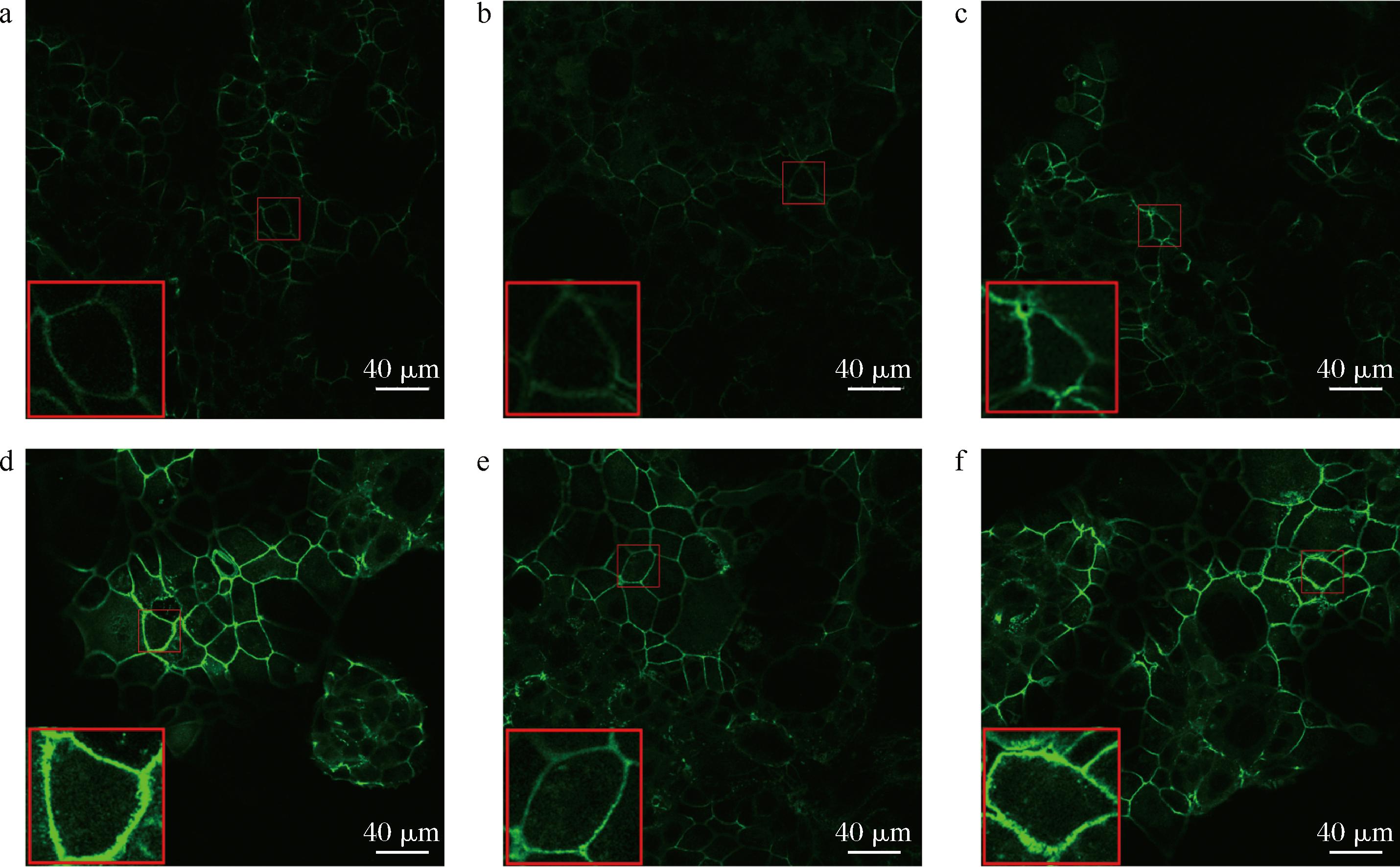
a-空白组;b-LPS诱导组;c-5 μg/mL的PPAs干预组;d-15 μg/mL的PPAs干预组;e-30 μg/mL的PPAs干预组;f-45 μg/mL的PPAs干预组
图9 PPAs对LPS诱导的Caco-2细胞ZO-1蛋白分布的影响(40×)
Fig.9 Effect of PPAs on ZO-1 protein distribution of Caco-2 cells induced by LPS (40×)
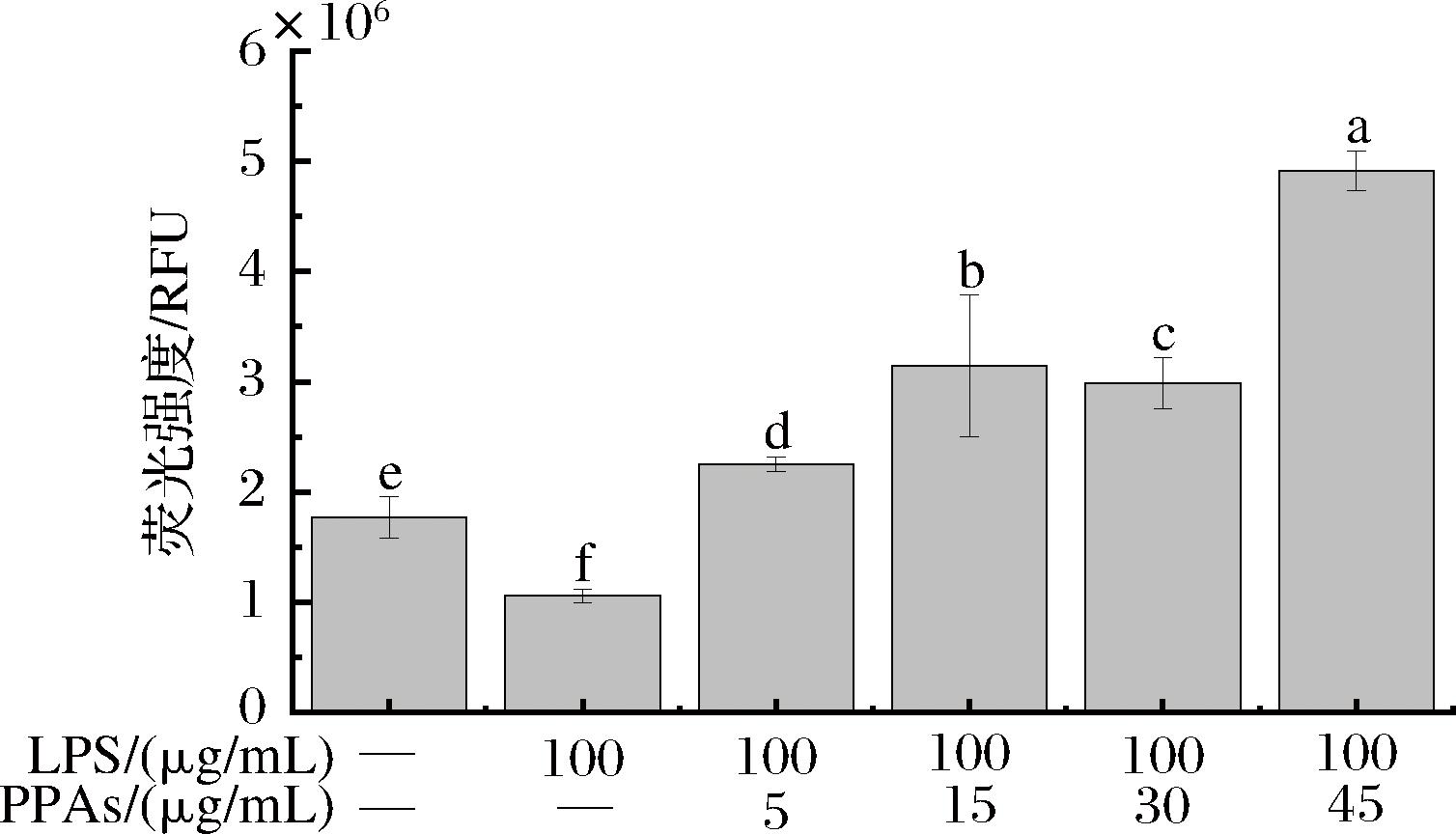
图10 PPAs对LPS诱导的Caco-2细胞ZO-1蛋白荧光强度的影响
Fig.10 Effect of PPAs on the fluorescence intensity of ZO-1 protein of Caco-2 cells induced by LPS
3 结论与讨论
借助LPS诱导Caco-2细胞损伤后,经PPAs干预,细胞培养液中LDH、AKP的活力均显著降低,即明显改善由LPS诱导的细胞通透性增加;SOD活力显著升高,MDA及NO含量显著减少,均呈现出剂量依赖效应;细胞流式仪结果表明PPAs的干预使得损伤细胞数量明显减少;EGFR、ERK1/2、NF-κB的mRNA表达明显受到抑制,细胞间隙的ZO-1紧密连接蛋白的表达明显增加。因此,PPAs的干预增加了Caco-2细胞抵抗氧化应激的能力,缓解LPS对Caco-2细胞的损伤作用。未来研究可深入解析PPAs调控EGFR-ERK1/2-NF-κB通路的分子机制,借助基因沉默技术等通过体内实验验证其对肠道屏障功能的保护作用,并基于抗氧化-抗炎-紧密连接修复的协同效应开发靶向肠道疾病的新型干预策略。
[1] WANG R F, SHI X, LI K K, et al.Activity and potential mechanisms of action of persimmon tannins according to their structures:A review[J].International Journal of Biological Macromolecules, 2023, 242:125120.
[2] ZHU W, WANG R F, KHALIFA I, et al.Understanding toward the biophysical interaction of polymeric proanthocyanidins (persimmon condensed tannins) with biomembranes:Relevance for biological effects[J].Journal of Agricultural and Food Chemistry, 2019, 67(40):11044-11052.
[3] AKAGI T, SUZUKI Y, IKEGAMI A, et al.Condensed tannin composition analysis in persimmon (Diospyros kaki Thunb.) fruit by acid catalysis in the presence of excess phloroglucinol[J].Journal of the Japanese Society for Horticultural Science, 2010, 79(3):275-281.
[4] ZOU B, GE Z Z, ZHANG Y, et al.Persimmon tannin accounts for hypolipidemic effects of persimmon through activating of AMPK and suppressing NF-κB activation and inflammatory responses in high-fat diet rats[J].Food &Function, 2014, 5(7):1536-1546.
[5] ZHU W, LIN K, LI K K, et al.Reshaped fecal gut microbiota composition by the intake of high molecular weight persimmon tannin in normal and high cholesterol diet-fed rats[J].Food &Function, 2018, 9(1):541-551.
[6] YAMAKOSHI J, SAITO M, KATAOKA S, et al.Safety evaluation of proanthocyanidin-rich extract from grape seeds[J].Food and Chemical Toxicology, 2002, 40(5):599-607.
[7] 孙雅望. 脂多糖引起奶牛乳腺和机体氧化应激损伤及蒲公英提取物对其阻断效果的研究[D].重庆:西南大学, 2021.SUN Y W.A study on the mammary and systematic oxidative stress induced by lipopolysaccharide in bovine and the blocking effect of dandelion extract[D].Chongqing:Southwest University, 2021.
[8] 任李梅. 人参根提取物及其有效成分对LPS诱导巨噬细胞炎症的缓解作用及其作用机制[D].长春:长春中医药大学, 2023.REN L M.Study on mechanism of ginseng root extract and its fractions related to the relieving effect on macrophage inflammation induced by LPS[D].Changchun:Changchun University of Traditional Chinese Medicine, 2023.
[9] AMARASIRI R P G S K, HYUN J, LEE S W, et al.Therapeutic potential of tryptophan metabolite indoleacrylic acid in inflammatory bowel disease:From cellular mechanisms to zebrafish stress-like behavior[J].International Immunopharmacology, 2025, 149:114207.
[10] BELLO M, SALDA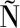 A-RIVERO L, CORREA-BASURTO J, et al.Structural and energetic basis for the molecular recognition of dual synthetic vs.natural inhibitors of EGFR/HER2[J].International Journal of Biological Macromolecules, 2018, 111:569-586.
A-RIVERO L, CORREA-BASURTO J, et al.Structural and energetic basis for the molecular recognition of dual synthetic vs.natural inhibitors of EGFR/HER2[J].International Journal of Biological Macromolecules, 2018, 111:569-586.
[11] WANG Z W, LITTERIO M C, MÜLLER M, et al.(-)-Epicatechin and NADPH oxidase inhibitors prevent bile acid-induced Caco-2 monolayer permeabilization through ERK1/2 modulation[J].Redox Biology, 2020, 28:101360.
[12] ZOU B, LI C M, CHEN J Y, et al.High molecular weight persimmon tannin is a potent hypolipidemic in high-cholesterol diet fed rats[J].Food Research International, 2012, 48(2):970-977.
[13] 于志辉, 袁斌, 诸葛祥真, 等.鸢尾素和鸢尾素-纳米脂质颗粒在非小细胞肺癌中的抗癌作用及其机制[J].现代肿瘤医学, 2024, 32(10):1792-1798.YU Z H, YUAN B, ZHUGE X Z et al.The anticancer effects and mechanism of Irisin and Irisin-liposomes in non-small cell lung cancer[J].Journal of Modern Oncology, 2024, 32(10):1792-1798.
[14] 慈小燕, 王泽, 李亚卓, 等.Caco-2细胞中药物转运蛋白的mRNA表达及活力评价[J].药物评价研究, 2018, 41(6):980-985.CI X Y, WANG Z, LI Y Z, et al.Expression of drug transporters mRNA in Caco-2 cells and its viability evaluation[J].Drug Evaluation Research, 2018, 41(6):980-985.
[15] 刘欢, 梁丽英, 刘显, 等.白花丹醌对人结肠腺癌Caco-2细胞凋亡、自噬及PI3K/Akt/mTOR信号通路的影响[J].中国病理生理杂志, 2021, 37(2):255-262.LIU H, LIANG L Y, LIU X, et al.Effects of plumbagin on apoptosis, autophagy and PI3K/Akt/mTOR signaling pathway in human colon adenocarcinoma Caco-2 cells[J].Chinese Journal of Pathophysiology, 2021, 37(2):255-262.
[16] 张林朴, 王冠华, 连小丽, 等.海藻酸钠/壳聚糖复合凝胶的制备与细胞毒性评价[J].中国组织工程研究, 2014,18(21):3310-3315.ZHANG L P, WANG G H, LIAN X L,et al.Preparation and cytotoxicity evaluation of chitosan-sodium alginate composite gel[J].Chinese Journal of Tissue Engineering Research, 2014,18(21):3310-3315.
[17] PAN F L, YANG W Z, ZHAO T, et al.Procyanidine alleviates bisphenol A-induced apoptosis in TM3 cells via the Nrf2 signaling pathway[J].Food and Chemical Toxicology, 2024, 192:114908.
[18] 江慧琼, 刘雅婷, 陈清华,等.超氧化物歧化酶的生理功能及其在动物生产中的应用前景[J].中国畜牧兽医, 2024, 51(3):945-954. JIANG H Q, LIU Y T, CHEN Q H,et al.Physiological function of superoxide dismutase and its application prospect in animal production[J].China Animal Husbandry &Veterinary Medicine, 2024, 51(3):945-954.
[19] 黄继义, 钟鸿斌, 逯富华, 等.肾小管上皮细胞线粒体氧化损伤在肾间质纤维化中的作用及机制[J].中国现代医生, 2016, 54(20):32-34.HUANG J Y, ZHONG H B, LU F H et al.Effect and mechanism of mitochondria oxidative damage in renal tubular epithelial cells on renal interstitial fibrosis[J].China Modern Doctor, 2016, 54(20):32-34.
[20] 陈素领, 周杰超, 张杰, 等.大黄素通过抑制FOXO1活性减轻NO对神经细胞的损伤[J].生物化学与生物物理进展, 2016, 43(11):1076-1085.CHEN S L, ZHOU J C, ZHANG J, et al.Emodin attenuates the neurotoxicity induced by nitric oxide through inhibiting FOXO1 transcriptional activity[J].Progress in Biochemistry and Biophysics, 2016, 43(11):1076-1085.
[21] BAAR M P, BRANDT R M C, PUTAVET D A, et al.Targeted apoptosis of senescent cells restores tissue homeostasis in response to chemotoxicity and aging[J].Cell, 2017, 169(1):132-147.e16.
[22] 张莲莲, 刘健彤, 韩在刚, 等.蓝莓原花青素抗氧化应激高血压血管损伤的研究[J].中国地方病防治杂志, 2017, 32(10):1087-1089.ZHANG L L, LIU J T, HAN Z G, et al.Study on antioxidation stress of blueberry proanthocyanidins in hypertensive vascular injury[J].Chinese Journal of Control of Endemic Diseases, 2017, 32(10):1087-1089.
[23] 张秀娟, 吴伟, 陈欣, 等.葡萄籽原花青素对牙龈上皮细胞炎症介质表达的影响[J].华西口腔医学杂志, 2022, 40(1):39-44.ZHANG X J, WU W, CHEN X, et al.Effects of grape seed proanthocyanidins on the expression of inflammatory mediators in gingival epithelial cells[J].West China Journal of Stomatology, 2022, 40(1):39-44.
[24] 张蕾, 黄华明, 周杰, 等.原花青素对宫颈癌HeLa细胞上皮间质转化的抑制作用[J].中成药, 2021, 43(7):1733-1740.ZHANG L, HUANG H M, ZHOU J, et al.Inhibitory effect of proanthocyanidins on epithelial mesenchymal transition of cervical cancer HeLa cells[J].Chinese Traditional Patent Medicine, 2021, 43(7):1733-1740.