米糠作为稻谷加工过程中的一种重要副产物,不仅产量丰富,而且由于其低廉的价格和广泛的获取途径,成为了极具应用潜力的副产物资源[1]。米糠多糖(rice bran polysaccharide,RBP)作为米糠的重要组成部分,具有显著的生物活性和广阔的应用前景。研究表明,米糠多糖具有抗氧化、降胆固醇、降血糖、抗肿瘤、抗炎、抗细菌感染和调节免疫功能等生理功效[2],可用于食品、保健品、医药等领域[3]。目前,米糠多糖已表现出满足不同领域应用要求的潜力。特别是,米糠多糖作为递送载体在制药领域引起了越来越多的关注[4]。然而,与其他使用的多糖相比,米糠多糖的有效利用率较低,关于米糠多糖在蛋白质中应用的报道较少[3]。
玉米醇溶蛋白是玉米中的主要蛋白质,具有很大比例的非极性氨基酸,有较强的疏水性并具有独特的自组装能力,这使得它被广泛应用于封装、保护和递送药物和生物活性分子[5]。玉米醇溶蛋白纳米颗粒(zein nanoparticles,ZNPs)作为药物载体,其疏水核心结构可显著改善难溶性药物的溶解特性及化学稳定性,延长药物的作用时间,还可以通过表面修饰调控实现器官靶向性,精准控制药物释放,减少毒性和不良反应[6]。但由于其自组装特性增加了溶剂的极性以及降低玉米醇溶蛋白的溶解度,从而导致其分子构象和聚集发生变化[7],使得由单一玉米醇溶蛋白构建的纳米颗粒不稳定且容易发生聚集。
多糖-蛋白质复合物构建的纳米载体可提高蛋白质纳米颗粒的稳定性,且多糖基纳米载体具有高表面积体积比和表面易修饰性,这增强了纳米载体在应用中的优势[8]。多糖的添加使得蛋白质的起泡性、乳化性、表面疏水性、溶解性等重要功能得到提升,天然多糖与蛋白可通过氢键、静电相互作用等形成稳定的纳米颗粒。LI等[9]将叶黄素包埋在玉米醇溶蛋白/可溶性大豆多糖复合纳米颗粒中,包封后,叶黄素的水溶性和化学稳定性均得到显著增强。ZHANG等[10]用玉米醇溶蛋白和桃胶多糖的复合纳米颗粒稳定用于姜黄素负载的Pickering乳液,纳米颗粒稳定乳液具有更小的液滴尺寸、更好的贮存和环境稳定性。YANG等[11]利用玉米醇溶蛋白和凉粉草多糖制备的复合纳米颗粒包埋姜黄素,包埋后的姜黄素具有更好的环境稳定性、更高的抗氧化活性和生物适应性,且纳米颗粒的多糖表面涂层使它们更容易被肠上皮细胞吸收。然而,目前尚无将米糠多糖与玉米醇溶蛋白进行复合作为纳米载体进行研究。
因此,本实验采用反溶剂沉淀法制备米糠多糖-玉米醇溶蛋白二元纳米颗粒,通过探究Zein-RBP纳米颗粒的相关性质,包括其表观形态、结构变化和理化性质等,以期得到一种具有优良功能特性和生物活性的Zein-RBP二元纳米颗粒,为米糠多糖的利用提供新的思路和方法,并有助于开发基于天然多糖和蛋白质的纳米递送载体。
1 材料与方法
1.1 材料与试剂
米糠多糖(纯度80%),陕西金润生物科技有限公司;玉米醇溶蛋白(纯度>98%),北京索莱宝科技有限公司;盐酸、无水乙醇等化学品均为分析纯,天津市天力化学试剂有限公司。
1.2 仪器与设备
Zetasizer nano ZS90 Plus型纳米粒度及zeta电位分析仪,英国马尔文公司;S-4800场发射扫描电子显微镜,日本株式会社日立高新技术;IRTracer-100傅里叶变换红外光谱仪,日本岛津公司;Rigaku Ultima Ⅳ型X射线粉末衍射仪,日本理学公司;STA8000热分析仪,美国珀金埃尔默公司;F-7000荧光光谱仪,日本日立公司;BSA124S电子分析天平,德国赛多利斯有限公司;HCJ-6E磁力搅拌水浴锅,常州恩培仪器制造有限公司;RE-3000旋转蒸发仪,上海亚荣生化仪器厂;DDS-11A型pH计,上海仪电科学仪器股份有限公司;SCIENTZ-18 N冷冻干燥机,宁波新芝生物科技股份有限公司。
1.3 实验方法
1.3.1 米糠多糖-玉米醇溶蛋白纳米颗粒制备
根据ZHANG等[12]方法进行修改,采用反溶剂沉淀法制备复合纳米颗粒。称取1 g Zein溶解在体积分数为80%的乙醇水溶液[V(乙醇)∶V(水)=4∶1]中,形成2.0%(质量分数)的Zein储备溶液。放置在磁力搅拌器上以850 r/min搅拌60 min后,静置24 h,以确保Zein完全溶解无沉淀。称取不同量的米糠多糖(25、50、100、200、400 mg)溶解在超纯水中,分别形成0.05%、0.1%、0.2%、0.4%、0.8%(质量分数)的米糠多糖储备溶液。用1 mol/L HCl将pH值调节到4.0。将5 mL的Zein乙醇水溶液用一次性注射器快速注射到在25 ℃水浴中50 mL不同浓度的多糖溶液中,同时以850 r/min搅拌90 min,使得反应完全。反应后溶液使用旋转蒸发仪除去溶液中的乙醇,再使用超纯水将溶液固定至50 mL。得到一部分分散液样品贮存在4 ℃下,另一部分样品冷冻干燥得到固态的冻干纳米颗粒,用于后续分析。将Zein与不同浓度米糠多糖形成的纳米颗粒分别标记为Zein NPs、0.05% Z-R NPs、0.1% Z-R NPs、0.2% Z-R NPs、0.4% Z-R NPs和0.8% Z-R NPs。
1.3.2 粒径、多分散性指数(polydispersity index,PDI)、zeta-电位的测定
参考CHEN等[13]方法,在25 ℃下,用纳米粒度及Zeta电位分析仪测量了纳米颗粒的粒度、PDI和Zeta-电位。在分析前,使用超纯水适当稀释纳米颗粒分散体。取2 mL样品放入样品池测量,稳定3 min,设定折射率为1.33,每个样品重复测定3次,最终取平均值作为实验结果。
1.3.3 纳米颗粒的微观形貌
取少许粉末样品,均匀撒在导电胶上,用洗耳球吹去表面未黏样品,喷金120 s左右。使用扫描电子显微镜(scanning electron microscopy,SEM)观察微观形态,其中加速电压为3 kV,拍摄倍数范围为50.0~100.0 k。
1.3.4 傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)的测定
参考前人方法[14],使用KBr压片法制备样品,取适量烘干后的样品,与干燥KBr粉末以质量比1∶100混合,研磨后压成薄片,扫描范围设定为400~4 000 cm-1,扫描次数32次,分辨率为4 cm-1。
1.3.5 X射线衍射(X-ray diffraction,XRD)的测定
使用XRD测定样品的晶体结构,将冷冻干燥后的粉末样品放置在样品凹槽中,用载玻片压平后,放入衍射仪中进行测量,加速电压设置为40 kV,管电流设置为40 mA,设置步长0.02°,扫描速度为7°/min,衍射角2θ范围为5°~50°。
1.3.6 荧光光谱的测定
利用F-7000荧光光谱仪对纳米颗粒的荧光光谱进行测定,参考WEI等[15]方法,测定纳米颗粒的内源荧光光谱,用超纯水稀释至适宜浓度,设置激发波长280 nm,发射波长290~450 nm,狭缝宽度5 nm,扫描速度1 200 nm/min。
1.3.7 热重(thermogravimetry,TG)分析
使用STA8000热分析仪对干燥样品进行热重分析,根据ZHANG等[16]的条件进行参数设置,测试温度设置为30~600 ℃,测量过程中的加热速率和氮气流速分别为10℃/min和20 mL/min。
1.3.8 乳化活性(emulsifying activity,EAI)和乳化稳定性(emulsifying stability,ESI)测定
不同样品的EAI和ESI通过经典比浊法并参考ZHANG等[17]方法进行测定。将不同样品分别配制成质量浓度为2 mg/mL的溶液,按照样品溶液与大豆油体积比3∶1制备乳液,使用均质机在10 000 r/min条件下搅打2 min。用SDS(1.0 g/L)将新鲜获得的乳剂等分试样稀释100倍,并在涡旋混合器中将混合物剧烈涡旋。并分别测定样品溶液在0、10 min时位于500 nm波长处的吸光度,样品的乳化性、乳化稳定性的计算如公式(1)和公式(2)所示:
(1)
(2)
式中:2是指常数,因为乳液的界面面积是其浊度的2倍;2.303是指ln10的值;N为稀释倍数;C为样品质量浓度,g/mL;φ为油相体积分数,%;A10和A0分别为10 min和0 min时的吸光度。
1.3.9 发泡能力(foam ability,FA)和泡沫稳定性(foam stability,FS)测定
根据王娜等[18]方法进行简单修改,准确称取0.5 g Zein-RBP纳米复合物,并将其溶解于50 mL去离子水中,然后搅拌均匀,并记录样品溶液体积V0(mL)。将高速分散器的搅拌头设置在容器中央,以10 000 r/min的速度发泡2 min,迅速移动至量筒中记录此时气泡体积V1(mL),静置30 min,记录此时气泡体积V30(mL),在25 ℃下重复3次。FA和FS的计算如公式(3)和公式(4)所示:
(3)
(4)
1.3.10 表面疏水性测定
参考WANG等[19]方法进行调整,采用ANS作为荧光探针测定表面疏水性。将复合物粉末分散至去离子水中,搅拌均匀,稀释成质量浓度为10~50 μg/mL。将4 mL Zein-RBP复合物溶液与50 μL 8.0 mmol/L ANS溶液混合,ANS溶液在避光条件下配制。利用荧光分光光度计F-7000在激发波长为360 nm和发射波长为490 nm时获得的荧光强度,设置狭缝宽度2.5 mm,测定3次取平均值。以样品质量浓度(μg/mL)为横坐标、荧光强度为纵坐标,表面疏水性通过计算荧光强度相对于样品浓度的初步斜率来确定。
1.4 数据统计方法
所有数据均为3次平行,采用IBM SPSS Statistics 26进行数据分析,使用邓肯检验确定各组间的统计差异(P<0.05为显著水平)。采用Origin 2024软件进行作图。
2 结果与分析
2.1 粒径、PDI和zeta电位
图1显示了不同浓度米糠多糖和玉米醇溶蛋白的复合纳米颗粒的粒径、PDI和zeta电位。单一的玉米醇溶蛋白纳米颗粒的平均粒径为95.43 nm,PDI为0.227,表明玉米醇溶蛋白能够发生自组装。在添加米糠多糖后,颗粒的粒径大小均显著增加,表明米糠多糖成功组装到玉米醇溶蛋白表面,形成复合颗粒。随着添加的米糠多糖进一步增加,表面电荷也逐渐增加,因此复杂颗粒之间的静电作用会增强导致粒径变小[20]。而米糠多糖质量分数为0.1%时,PDI值最小为0.204,此时纳米颗粒的稳定性与均一性最好。另外,在此形成条件下(pH=4),由于Zein低于等电点pH=6.2,因此Zein的Zeta电位为正(+30.69)[21]。随着米糠多糖的加入,电位值由正转负,表明米糠多糖通过静电相互作用吸附在Zein表面,且米糠多糖呈电位主导,由于米糠多糖浓度的增加致使电位值也逐渐增加。这一结果表明,用米糠多糖包覆Zein NPs的表面可以改变表面电荷的极性,并显著提高其颗粒稳定性[11]。
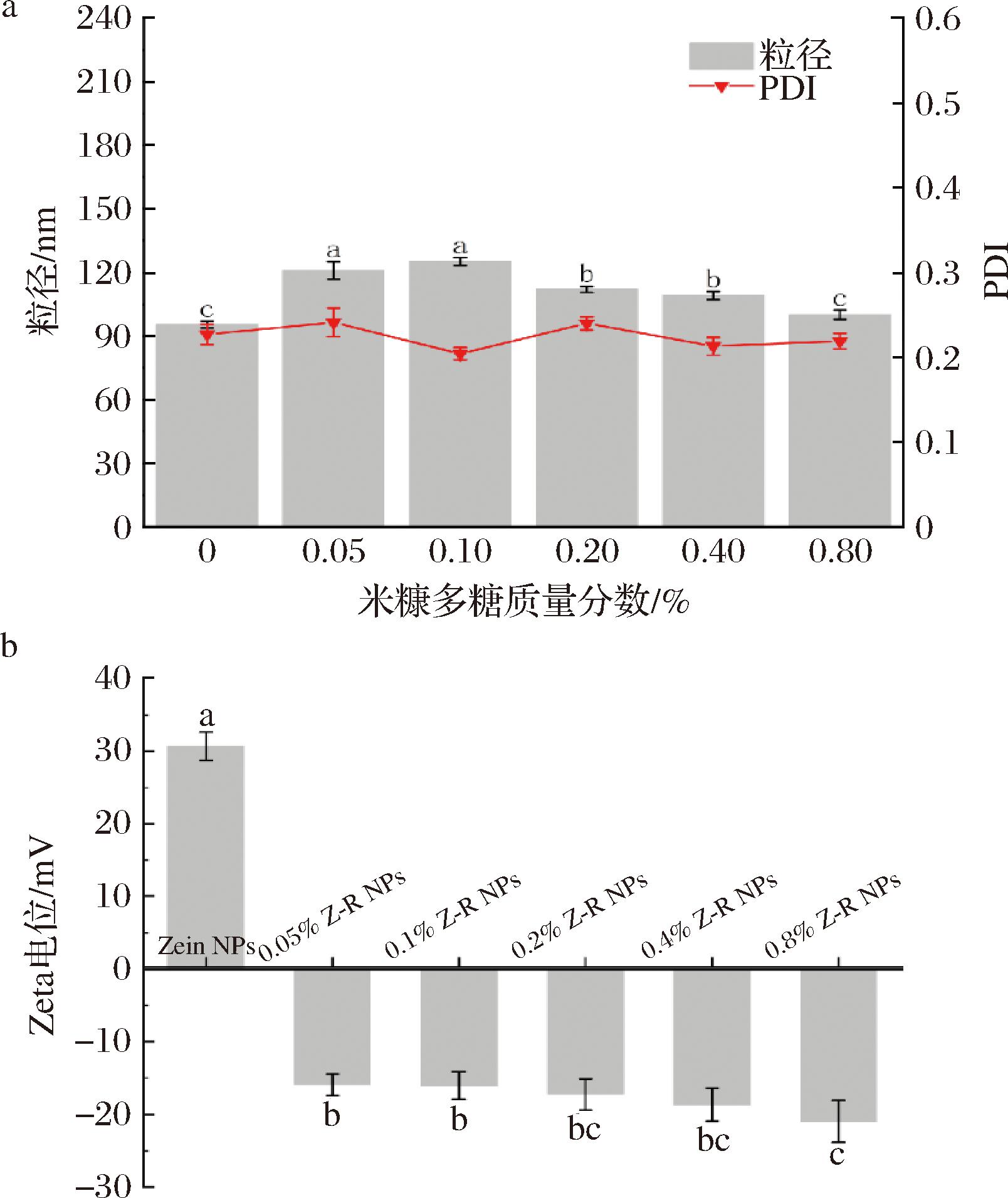
a-粒径图;b-电位图
图1 Zein-RBP复合颗粒粒径和电位图
Fig.1 Zein-RBP composite particle size and potential maps
注:同一指标不同字母表示差异显著(P<0.05)(下同)。
2.2 纳米颗粒微观形貌分析
复合纳米颗粒的微观结构如图2所示。单一Zein NPs的分布相对均匀,但由于颗粒间相互连接和Zein的高疏水性,导致颗粒表面有一定程度的黏连和聚集。当加入少量米糠多糖后,复合纳米颗粒呈现平滑且大小均匀的网状结构。当米糠多糖的添加量较高时(质量分数0.2%~0.8%),过量的多糖分子包裹在Zein颗粒表面,由于多糖分子间的相互作用力使得纳米颗粒相互黏附[22]。Z-R NPs在干燥过程中仍然保持球形,说明在添加了米糠多糖后,复合纳米颗粒显示出高均匀性,表明由Zein和米糠多糖结合形成的纳米颗粒具有更好的稳定性和均匀性[23]。此外,小而规则的球形纳米结构在细胞摄取和生物相容性方面也具有优势[24]。

图2 纳米粒子的微观形态
Fig.2 Microscopic morphology of nanoparticles
2.3 红外光谱分析
如图3所示,FTIR能够反映有关纳米粒子中Zein和米糠多糖的分子间相互作用。Zein的FTIR中有3个特征峰,与其他具有O—H键的化合物一样,Zein光谱显示3 325.4 cm-1对应于拉伸振动,1 661 cm-1处的(Zein的酰胺I)典型峰值代表C![]() O拉伸振动和1 543.1 cm-1处的(Zein的酰胺Ⅱ)吸收带对应于酰胺残基的平面弯曲振动中的N—H[25]。米糠多糖在3 403.6 cm-1处有呈现出O—H的拉伸振动,而C
O拉伸振动和1 543.1 cm-1处的(Zein的酰胺Ⅱ)吸收带对应于酰胺残基的平面弯曲振动中的N—H[25]。米糠多糖在3 403.6 cm-1处有呈现出O—H的拉伸振动,而C![]() O的不对称和对称拉伸振动峰值在1 635.3 cm-1处和1 455.5 cm-1[10]。与单独的Zein 的酰胺I和Ⅱ相比,Z-R NPs的吸收峰强度有所上升。此外,米糠多糖的不对称和对称C
O的不对称和对称拉伸振动峰值在1 635.3 cm-1处和1 455.5 cm-1[10]。与单独的Zein 的酰胺I和Ⅱ相比,Z-R NPs的吸收峰强度有所上升。此外,米糠多糖的不对称和对称C![]() O伸缩振动也明显减弱。这些结果表明,米糠多糖和Zein之间可能存在静电作用,通过米糠多糖链上的羧基和Zein链上的氨基发生反应。添加米糠多糖后,玉米醇溶蛋白NPs的羟基峰由3 325.4 cm-1红移至3 349.8 cm-1,归因于米糠多糖中的羧基或羟基与玉米醇溶蛋白中谷氨酰胺的酰胺基团之间形成氢键[26]。
O伸缩振动也明显减弱。这些结果表明,米糠多糖和Zein之间可能存在静电作用,通过米糠多糖链上的羧基和Zein链上的氨基发生反应。添加米糠多糖后,玉米醇溶蛋白NPs的羟基峰由3 325.4 cm-1红移至3 349.8 cm-1,归因于米糠多糖中的羧基或羟基与玉米醇溶蛋白中谷氨酰胺的酰胺基团之间形成氢键[26]。
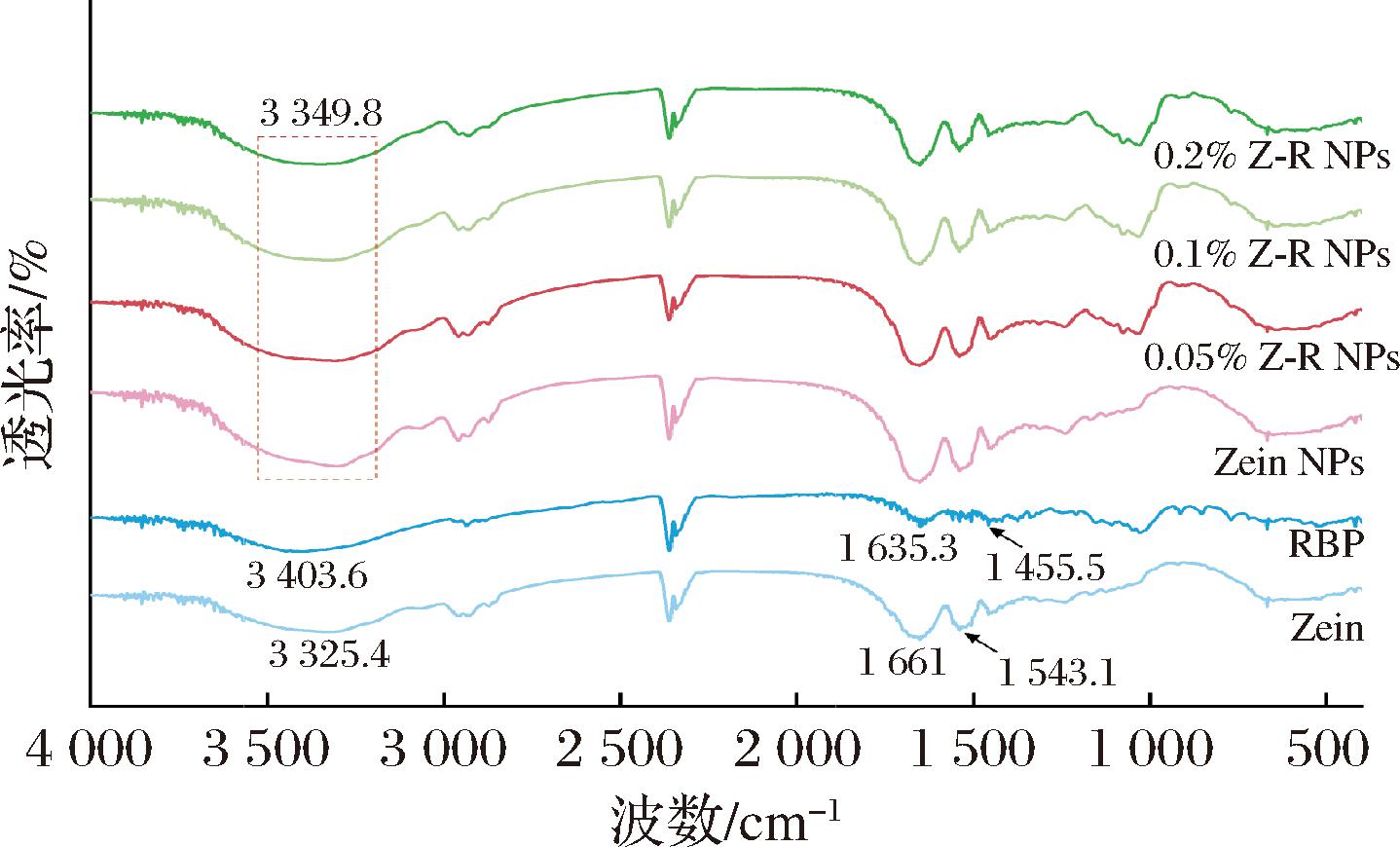
图3 Zein-RBP复合颗粒的FTIR图
Fig.3 Fourier-transform infrared spectrum of the Zein-RBP composite particles
2.4 XRD分析
XRD用于研究米糠多糖、Zein、Zein NPs和Z-R NPs的晶体结构或无定形结构的变化。如图4所示,其中米糠多糖在9.2°、18.4°、28.3°、30.9°和40.2°处存在尖锐吸收峰,表明米糠多糖呈晶体结构,而Zein在9.0°和20.1°处显示出明显的宽峰,证实了Zein以无定形形式存在[16]。在形成NPs后,Zein衍射峰的强度均有所下降,米糠多糖的尖峰消失,表明Zein与米糠多糖之间存在相互作用,并成功组装[27]。在不同浓度条件下形成的NPs的XRD图谱基本没有差异,表明米糠多糖浓度对NPs的晶体结构或无定形结构没有明显影响。
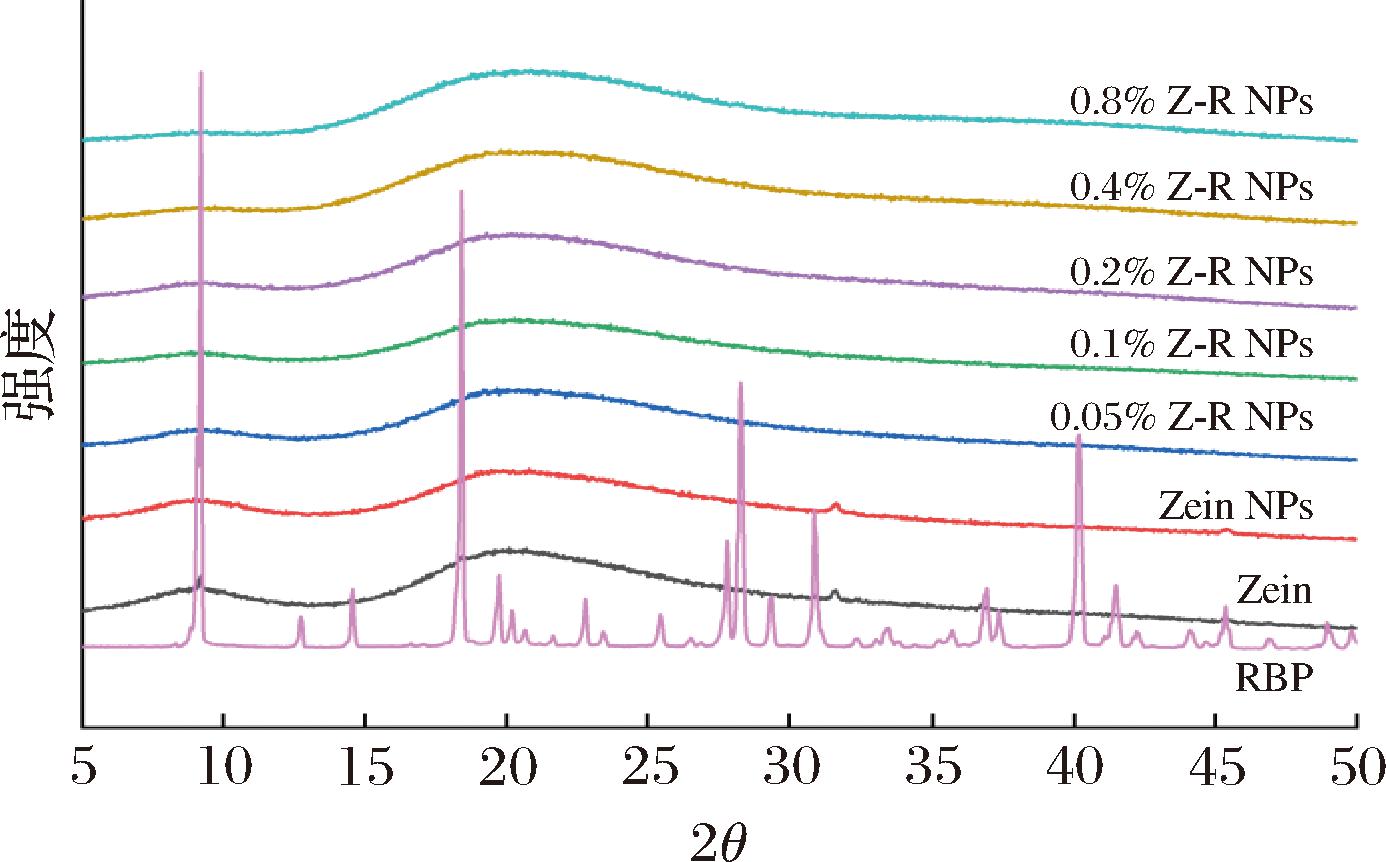
图4 Zein-RBP复合颗粒的XRD图
Fig.4 XRD pattern of the Zein-RBP composite particles
2.5 荧光光谱分析
玉米醇溶蛋白的荧光主要来源于酪氨酸(tyrosine,Tyr)、色氨酸(tryptophan,Trp)和苯丙氨酸(phenylalanine,Phe)残基,并且残基对于微环境变化敏感。如图5所示,Zein NPs的发射峰位于316 nm附近,这归因于Tyr和Trp残基的存在[28]。与Zein NPs相比,在添加米糠多糖后的复合颗粒最大荧光强度显著降低,发射带有轻微的蓝移。这些影响可能是由于Zein中带的负电荷与米糠多糖中带正电荷的氨基酸残基之间的相互作用,导致Zein上的疏水性氨基酸残基周围出现更亲水性的微环境[16]。随着米糠多糖添加量的增加,荧光强度逐渐降低,发生荧光淬灭,这可能是由于复合纳米颗粒内的米糠多糖和Zein之间发生的氢键和疏水相互作用造成的。
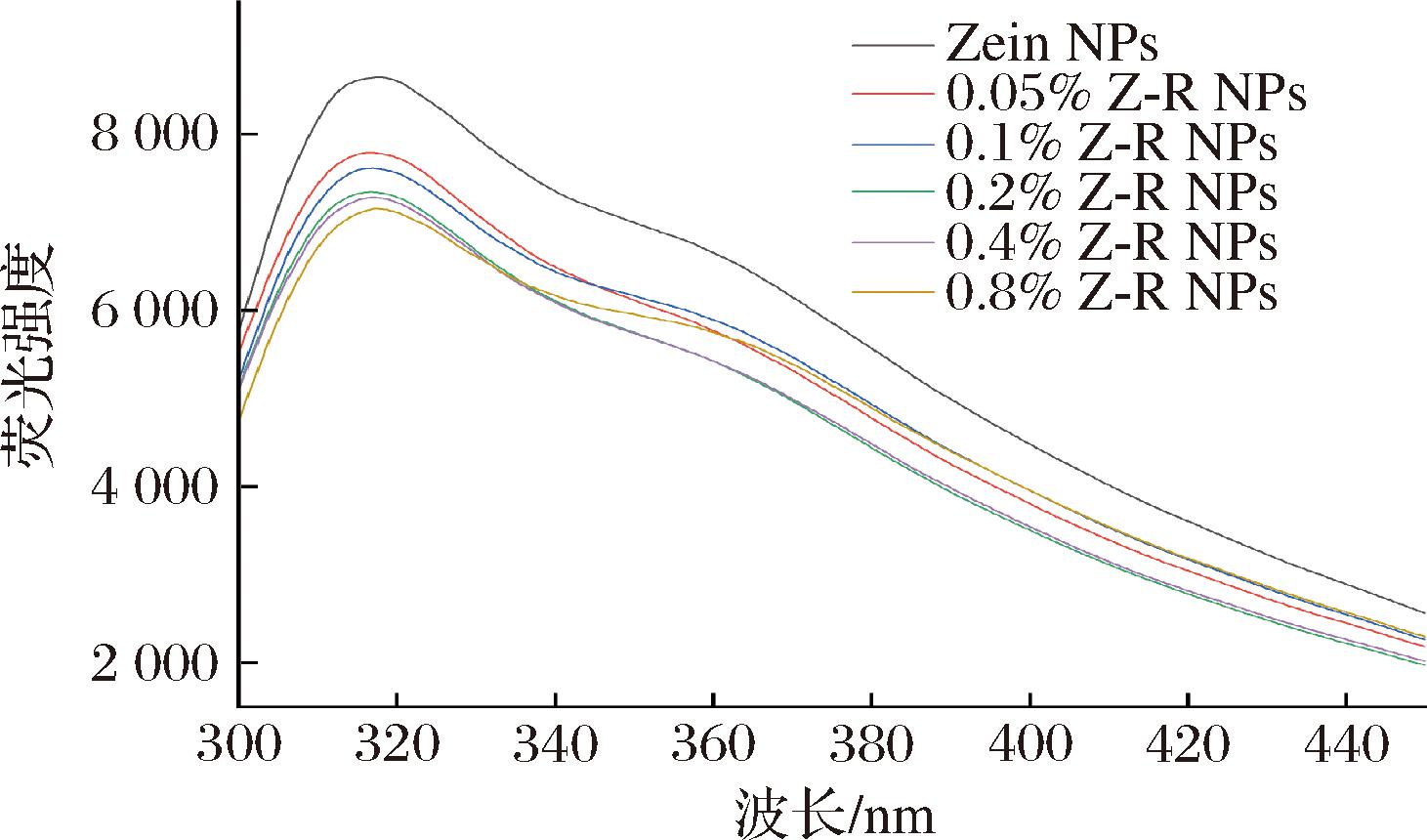
图5 Zein-RBP复合颗粒的内源荧光光谱图
Fig.5 Intrinsic fluorescence spectrum of the Zein-RBP composite particles
2.6 热重分析
TG分析通常通过测量样品以受控速率加热时质量的减少,以提供反映Zein、米糠多糖和Z-R NPs有关其热稳定性和成分的信息。如图6所示,在100 ℃时,米糠多糖的质量损失为4.4%,显著高于Zein,这可能是由于Zein具有很强的疏水性,因此游离水含量较低,而米糠多糖作为一种水溶性多糖,含有更多的游离水。100~200 ℃时的质量损失可能是由于结合水的释放而导致的质量损失[29]。在200~400 ℃,Zein和米糠多糖发生最显著的质量损失变化,分别为60.77%和64.98%这归因于肽键断裂、氨基酸分解以及碳水化合物的脱水和脱羧[25]。复合颗粒的显著的质量损失变化发生在170~500 ℃,在170 ℃时,Zein、0.05% Z-R NPs、0.1% Z-R NPs的米糠多糖损失率分别为1%、2%、4.4%、7.9%,质量损失率的变化是由于复合纳米颗粒中的结合水含量变化。500 ℃时,复合纳米颗粒的热损失率分别为61.7%、60.8%,显著低于玉米醇溶蛋白(70.5%)和米糠多糖(79.3%)。这些结果表明,蛋白与多糖之间的存在相互作用,形成复合颗粒后改变了它们原有的热稳定性[16,25]。
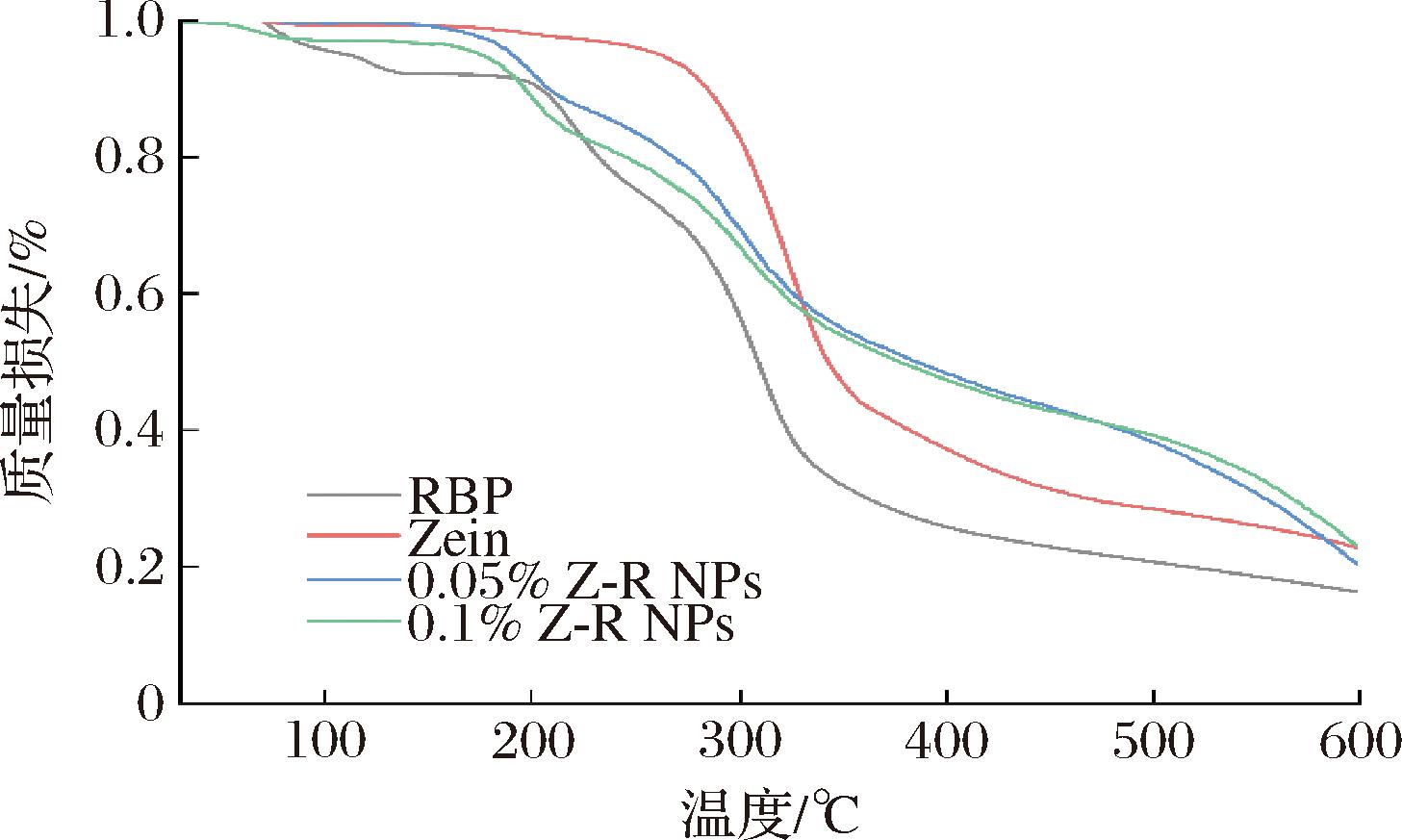
图6 Zein-RBP复合颗粒的热重分析图
Fig.6 Thermogravimetric analysis of Zein-RBP composite particles plots
2.7 EAI和ESI
复合颗粒的EAI和ESI变化如图7所示。EAI是指在乳液形成过程中,在水和油滴之间的界面处吸收蛋白质以防止重力分离、絮凝和聚结的能力。ESI是指复合颗粒在预定时间内保持乳化稳定性的能力[30]。相比于单一的Zein NPs,在加入米糠多糖形成复合颗粒后,EAI和ESI显著提升。Zein-RBP纳米颗粒的EAI,在米糠多糖质量分数为0%~0.2%时,随着米糠多糖比例的增加而提高,表明米糠多糖在乳化性能中起着决定性的作用[31]。在米糠多糖质量分数为0.1%~0.8%时,EAI和ESI值组间分别相差较小,这因为过量添加米糠多糖可能导致附着在复合颗粒表面的亲水基团增加引起聚集,从而破坏疏水性和亲水性之间的平衡[32]。此结果与表面疏水性得到的结果一致。
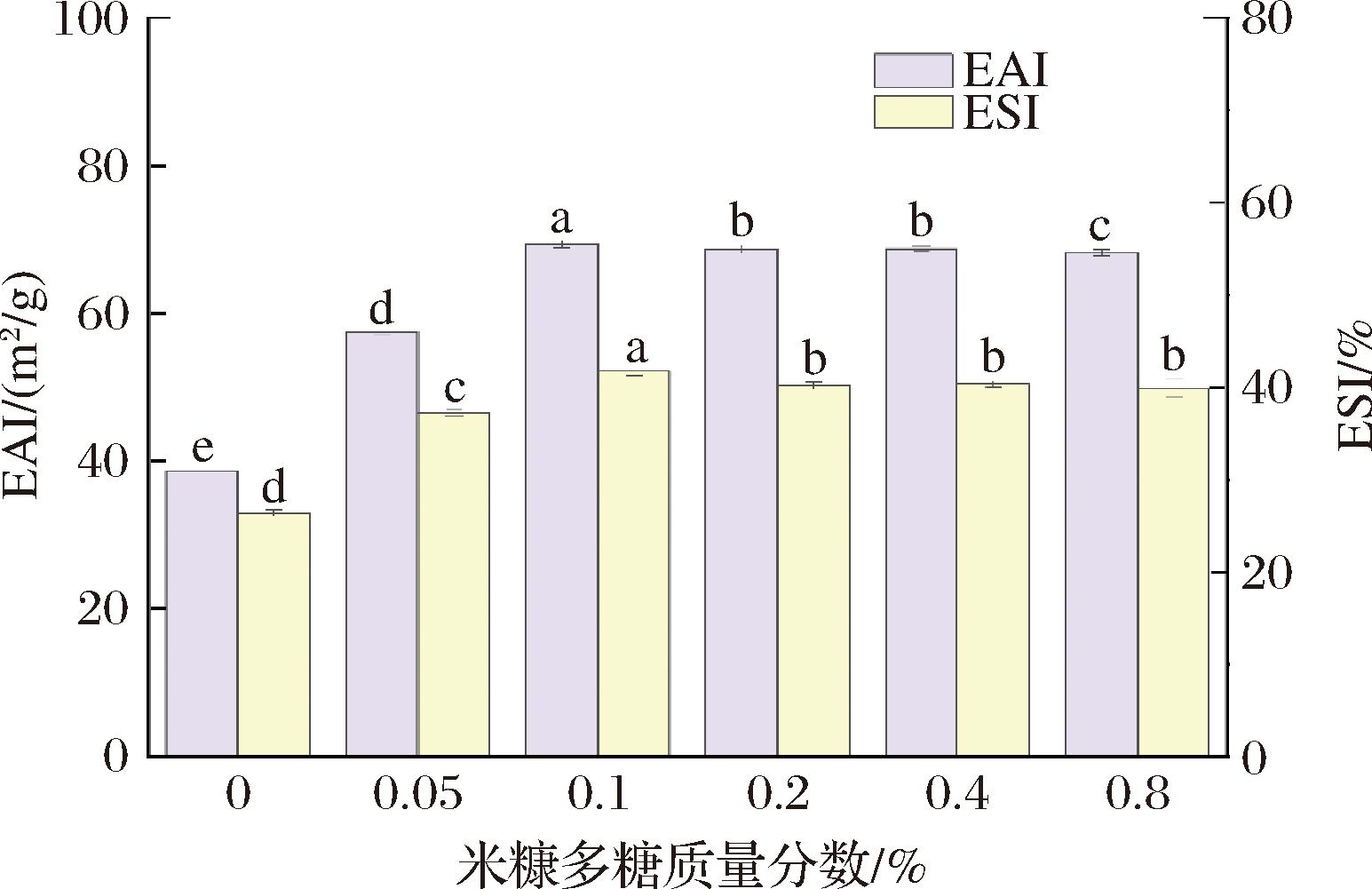
图7 Zein-RBP复合颗粒的乳化特性图
Fig.7 Plot of emulsification characteristics of Zein-RBP composite particles
2.8 发泡能力和泡沫稳定性
FA可量化纳米颗粒产生泡沫的效率,决定其作为起泡剂的基础性能,而FS则揭示其维持泡沫结构的机制强度,二者共同反映了纳米颗粒在泡沫应用中的实用性与可靠性。Zein-RBP复合颗粒的FA和FS如图8所示。由图8中观察到Zein NPs的FA最低为144.00%,在加入米糠多糖形成复合颗粒后,复合物的FA值均高于单独的玉米醇溶蛋白纳米颗粒,对于Zein-RBP复合颗粒,当米糠多糖质量分数为0.05%~0.2%时,FA几乎相同,而后随着添加量的增加,FA也小幅度提升。FA的增强可能是由于Zein-RBP复合颗粒降低界面张力的能力更强[33]。结果表明,由于泡沫的排水、粗化、絮凝和歧化,所有样品的泡沫体积随着时间的推移逐渐减少[34]。纳米颗粒的FS相差较小,反映了泡沫随时间推移的稳定性几乎相同。米糠多糖的添加对Z-R NPs的FS没有特别明显的影响。纳米颗粒的FA和FS受不同因素的影响,FA主要由其吸附速率决定,FS主要取决于界面膜的强度和刚度,以及气泡对聚结和歧化的抵抗力[35]。
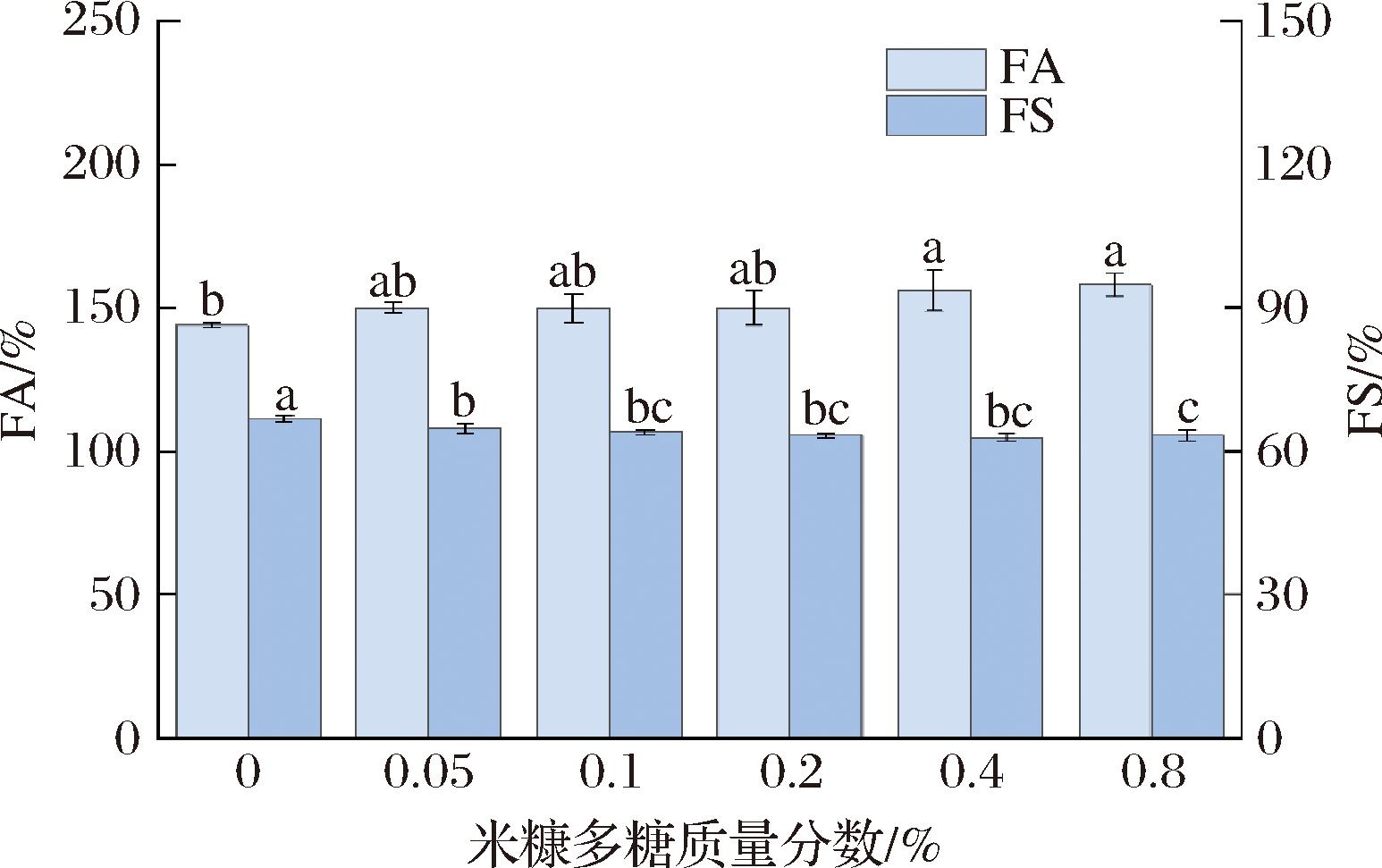
图8 Zein-RBP复合颗粒的起泡性图
Fig.8 Foamability graph of Zein-RBP composite particles
2.9 表面疏水性分析
蛋白质表面疏水性(H0)与暴露的疏水性氨基酸残基相关,表示蛋白质表面疏水基团的水平。H0不仅可以反映RBP-Zein复合物中蛋白质的结构变化,在油水界面的吸附中也起着至关重要的作用[36]。如图9所示,引入米糠多糖后,所有复合颗粒的H0显著高于Zein NPs,并且复合纳米颗粒在米糠多糖质量分数小于0.1%时,随着浓度的增加而增加。这可能是由于在该浓度下与Zein或米糠多糖相互作用后,蛋白质的空间结构更加拉伸,并且蛋白质疏水基团的暴露增加[35]。而质量分数为0.1%~0.8%时,H0值相差不大,可能是由于米糠多糖的亲水性基团会分布在颗粒表面,过多的米糠多糖可能会导致颗粒表面的多糖分子之间发生聚集,从而掩盖部分玉米醇溶蛋白的疏水区域。因此,米糠多糖的引入可以改变Zein的分子结构,有利于改善蛋白质的表面性质[19]。
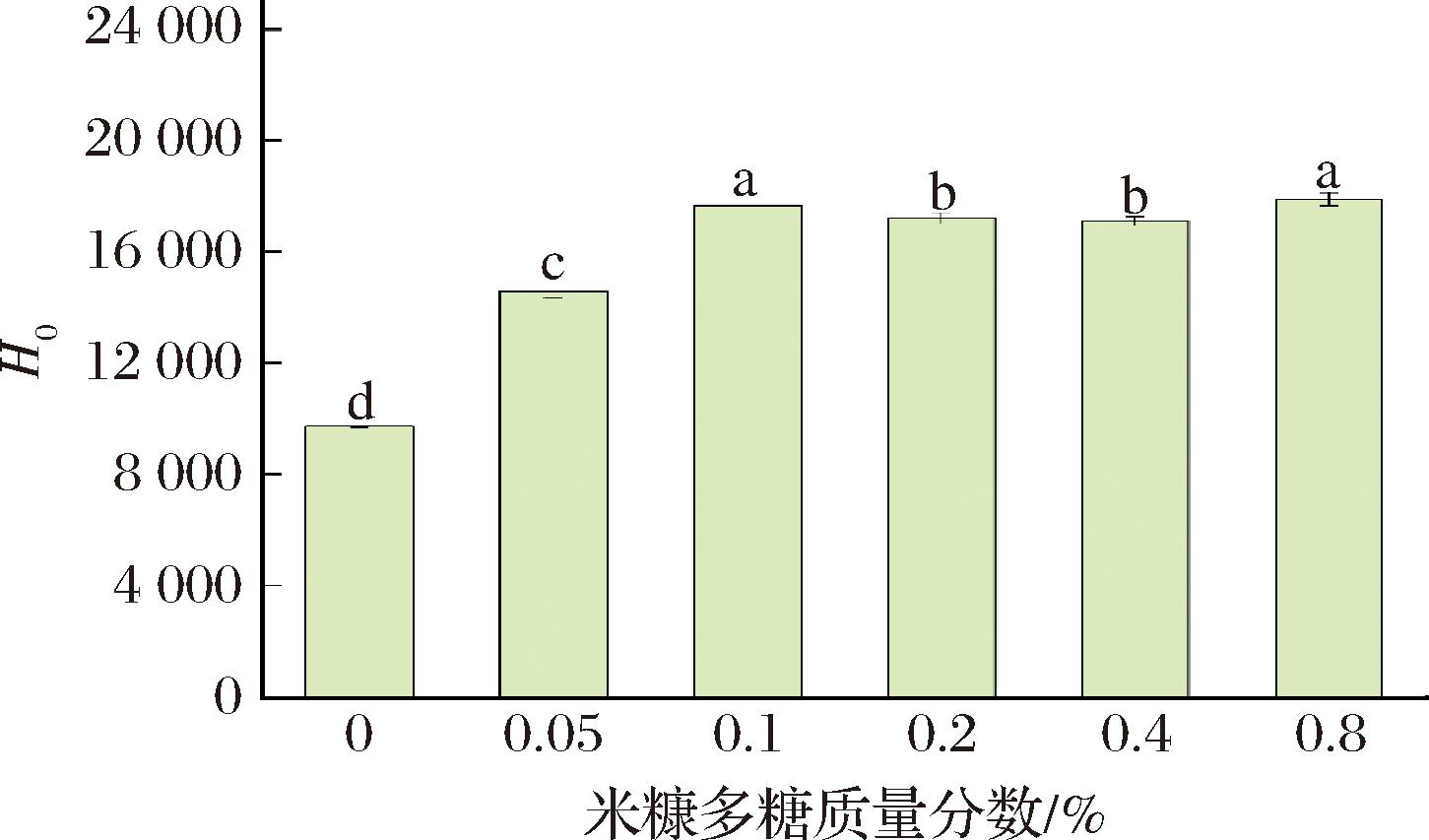
图9 Zein-RBP复合颗粒的表面疏水性图
Fig.9 Surface hydrophobicity map of Zein-RBP composite particles
3 结论
本实验以米糠多糖和玉米醇溶蛋白为原料,通过反溶液沉淀法制备了Zein-RBP复合纳米颗粒,探究了复合纳米颗粒的表观形态、结构特征、分子相互作用机制及功能特性。结果表明,Zein与米糠多糖质量比为2∶1时复合纳米颗粒平均粒径为(125.26±1.88) nm,电位为(-16.05±1.91) mV,PDI为0.204,具有较小的粒径和稳定的电位,并且有良好的乳化性、起泡性及表面疏水性。疏水相互作用、静电相互作用和氢键等非共价结合是复合纳米颗粒形成过程中的主要驱动力。与单独的Zein的酰胺I和Ⅱ相比,Z-R NPs的吸收峰强度有所上升。添加米糠多糖后,Zein NPs的宽峰由3 325.4 cm-1移至3 349.8 cm-1。荧光光谱中,在添加米糠多糖后的复合颗粒最大荧光强度显著降低,发射带有轻微的蓝移。随着米糠多糖添加量的增加,荧光强度逐渐降低,发生荧光淬灭。在形成NPs后,Zein衍射峰的强度均有所下降,米糠多糖的尖峰消失,表明Zein与米糠多糖之间存在相互作用,并成功组装。复合纳米颗粒的热损失率分别为61.7%、60.8%,显著低于玉米醇溶蛋白(70.5%)和米糠多糖(79.3%)。综上,本研究可为米糠多糖作为生物活性物质的递送载体,或用于绿色食品包装材料提供新思路。
[1] 纪雨青. 米糠多糖羧甲基化改性及其递送花青素的应用[D].武汉:武汉轻工大学, 2025.JI Y Q.Carboxymethylation modification of rice bran polysaccharides and their application in delivering anthocyanins[D].Wuhan:Wuhan University of Light Industry, 2025.
[2] SURIN S, SURAYOT U, SEESURIYACHAN P, et al.Antioxidant and immunomodulatory activities of sulphated polysaccharides from purple glutinous rice bran (Oryza sativa L.)[J].International Journal of Food Science &Technology, 2018, 53(4):994-1004.
[3] CHEN B J, QIAO Y J, WANG X, et al.Extraction, structural characterization, biological functions, and application of rice bran polysaccharides:A review[J].Foods, 2023, 12(3):639.
[4] LIU L, YAN Y J, NI D N, et al.TAT-functionalized PEI-grafting rice bran polysaccharides for safe and efficient gene delivery[J].International Journal of Biological Macromolecules, 2020, 146:1076-1086.
[5] YAN X J, LI M T, XU X F, et al.Zein-based nano-delivery systems for encapsulation and protection of hydrophobic bioactives:A review[J].Frontiers in Nutrition, 2022, 9:999373.
[6] SUN X X, PAN C Q, YING Z Y, et al.Stabilization of zein nanoparticles with k-carrageenan and tween 80 for encapsulation of curcumin[J].International Journal of Biological Macromolecules, 2020, 146:549-559.
[7] WEISSMUELLER N T, LU H D, HURLEY A, et al.Nanocarriers from GRAS zein proteins to encapsulate hydrophobic actives[J].Biomacromolecules, 2016, 17(11):3828-3837.
[8] 夏明杰, 杨立娜, 余科金, 等.天然多糖基纳米递送载体在功能性食品中的应用[J].中国食品学报, 2025, 25(1):442-454.XIA M J, YANG L N, YU K J et al.The application of natural polysaccharide-based nano-delivery carriers in functional foods[J].Journal of Chinese Institute of Food Science and Technology, 2025, 25(1):442-454.
[9] LI H, YUAN Y K, ZHU J X, et al.Zein/soluble soybean polysaccharide composite nanoparticles for encapsulation and oral delivery of lutein[J].Food Hydrocolloids, 2020, 103:105715.
[10] ZHANG R Y, LI L, MA C X, et al.Shape-controlled fabrication of zein and peach gum polysaccharide based complex nanoparticles by anti-solvent precipitation for curcumin-loaded Pickering emulsion stabilization[J].Sustainable Chemistry and Pharmacy, 2022, 25:100565.
[11] YANG J, LIN J Q, CHEN X X, et al.Mesona chinensis polysaccharide/zein nanoparticles to improve the bioaccesibility and in vitro bioactivities of curcumin[J].Carbohydrate Polymers, 2022, 295:119875.
[12] ZHANG Z H, LI X J, SANG S Y, et al.Preparation, properties and interaction of curcumin loaded zein/HP-β-CD nanoparticles based on electrostatic interactions by antisolvent co-precipitation[J].Food Chemistry, 2023, 403:134344.
[13] CHEN L, XU W, YANG Z Y, et al.Co-encapsulation of quercetin and resveratrol:Comparison in different layers of zein-carboxymethyl cellulose nanoparticles[J].International Journal of Biological Macromolecules, 2024, 278:134827.
[14] SUN C X, DAI L, GAO Y X.Interaction and formation mechanism of binary complex between zein and propylene glycol alginate[J].Carbohydrate Polymers, 2017, 157:1638-1649.
[15] WEI Y, GUO A X, LIU Z K, et al.Structural design of zein-cellulose nanocrystals core-shell microparticles for delivery of curcumin[J].Food Chemistry, 2021, 357:129849.
[16] ZHANG H, FENG H Z, LING J H, et al.Enhancing the stability of zein/fucoidan composite nanoparticles with calcium ions for quercetin delivery[J].International Journal of Biological Macromolecules, 2021, 193:2070-2078.
[17] ZHANG L T, PAN Z, SHEN K Q, et al.Influence of ultrasound-assisted alkali treatment on the structural properties and functionalities of rice protein[J].Journal of Cereal Science, 2018, 79:204-209.
[18] 王娜, 卜慧芳, 孙煜卓, 等.米糠蛋白水解物及其二元纳米颗粒的制备及结构表征[J].食品科学, 2025, 46(5):85-95.WANG N, BU H F, SUN Y Z, et al.Preparation and structural characterization of rice bran protein hydrolysates and their binary nanoparticles[J].Food Science, 2025, 46(5):85-95.
[19] WANG J G, YAN R, LIU T X, et al.The formation, interfacial, and foaming properties of complex constructed by caseinate and soy protein nanoparticle[J].Food Hydrocolloids, 2024, 151:109802.
[20] LIU Q Y, QIN Y, JIANG B, et al.Development of self-assembled zein-fucoidan complex nanoparticles as a delivery system for resveratrol[J].Colloids and Surfaces B:Biointerfaces, 2022, 216:112529.
[21] PATEL A R, BOUWENS E C M, VELIKOV K P.Sodium caseinate stabilized zein colloidal particles[J].Journal of Agricultural and Food Chemistry, 2010, 58(23):12497-12503.
[22] CHEN S, HAN Y H, WANG Y Q, et al.Zein-hyaluronic acid binary complex as a delivery vehicle of quercetagetin:Fabrication, structural characterization, physicochemical stability and in vitro release property[J].Food Chemistry, 2019, 276:322-332.
[23] YANG S F, LIU L, CHEN H Q, et al.Impact of different crosslinking agents on functional properties of curcumin-loaded gliadin-chitosan composite nanoparticles[J].Food Hydrocolloids, 2021, 112:106258.
[24] JINDAL A B.The effect of particle shape on cellular interaction and drug delivery applications of micro- and nanoparticles[J].International Journal of Pharmaceutics, 2017, 532(1):450-465.
[25] MENDOZA J, PE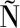 U
U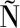 URI-MIRANDA O, VALDEZ-C
URI-MIRANDA O, VALDEZ-C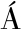 RDENAS M D C, et al.Encapsulation of anthocyanins from purple corn cob via antisolvent precipitation:Effect of pH and zein/gum arabic ratio on the antioxidant activity, particle size and thermal stability[J].Food Hydrocolloids for Health, 2025, 7:100197.
RDENAS M D C, et al.Encapsulation of anthocyanins from purple corn cob via antisolvent precipitation:Effect of pH and zein/gum arabic ratio on the antioxidant activity, particle size and thermal stability[J].Food Hydrocolloids for Health, 2025, 7:100197.
[26] 杨俊. 凉粉草多糖—玉米醇溶蛋白口服纳米递送体系的构建及其载膳食多酚肠道递送研究[D].南昌:南昌大学, 2024.YANG J.Construction of oral nano-delivery system of Mesona chinensis polysaccharide-zein and its intestinal delivery with dietary polyphenols[D].Nanchang:Nanchang University, 2024.
[27] 王伊, 郭睿阳, 沈万鑫, 等.玉米醇溶蛋白与冬凌草甲素的互作机制及其纳米颗粒制备与表征[J].食品工业科技, 2025,46(20):154-163.WANG Y, GUO R Y, SHEN W X, et al.Interaction mechanism of zein with oridonin and preparation and characterization of Zein-oridonin nanoparticles[J].Science and Technology of Food Industry, 2025,46(20):154-163.
[28] YANG S F, DAI L, MAO L K, et al.Effect of sodium tripolyphosphate incorporation on physical, structural, morphological and stability characteristics of zein and gliadin nanoparticles[J].International Journal of Biological Macromolecules, 2019, 136:653-660.
[29] REN M N, XIE T L, CHEN L, et al.Pickering emulsion stabilized by hollow Zein/SSPS nanoparticles loaded with Thymol:Formation, characterization, and application in fruit preservation[J].Food Research International, 2025, 201:115561.
[30] LI K, FU L, ZHAO Y Y, et al.Use of high-intensity ultrasound to improve emulsifying properties of chicken myofibrillar protein and enhance the rheological properties and stability of the emulsion[J].Food Hydrocolloids, 2020, 98:105275.
[31] ZHANG M, LI Z K, DAI M Q, et al.Fabrication and characterization of chitosan-pea protein isolate nanoparticles[J].Molecules, 2022, 27(20):6913.
[32] WANG Y, ZHANG P, LIN H W, et al.Pickering emulsions stabilized by β-lactoglobulin-rosmarinic acid-pectin nanoparticles:Influence of interfacial behavior and rheology performance[J].Food Hydrocolloids, 2024, 154:110084.
[33] GALUS S.Functional properties of soy protein isolate edible films as affected by rapeseed oil concentration[J].Food Hydrocolloids, 2018, 85:233-241.
[34] PENG D F, JIN W P, ZHOU P Y, et al.Foaming and surface rheological behaviors of gliadin particles:Effect of solvent and concentration of gliadin stock solution[J].Food Hydrocolloids, 2020, 106:105868.
[35] WU C, LIU W, ZHAO Z Q, et al.Interaction of alkyl gallate with gliadin and its effect on the surface and foaming properties of composite nanoparticles[J].Food Hydrocolloids, 2025, 163:111096.
[36] DENG L, LIAO J Q, LIU W Q, et al.Study of Zn2+ complexation driven zein-based W/O/W Pickering emulsions for enhancing curcumin bioaccessibility and fluorouracil bioactivity[J].Food Hydrocolloids, 2025, 164:111243.