苹果是人们喜食的水果之一,含有丰富的糖分、维生素、矿物质等营养成分以及膳食纤维、多酚等功效成分,可以增强人体免疫力,提高抗氧化能力[1]。苹果采收后通常进入冷库贮藏,以延长保鲜期,满足全年的市场供应。常见的苹果贮藏方式包括低温冷藏、自发气调包装贮藏、控制气调贮藏等,其中,相比于低温冷藏,气调贮藏可以维持更好的果实品质,抑制果实的呼吸和衰老,达到长期保鲜的目的[2]。然而,长期气调贮藏过程中,由于果实的呼吸代谢,苹果耐受气体的能力下降,可能遭受低氧气(O2)、高二氧化碳(CO2)的气体伤害,导致褐变、异味等生理病害的发生,降低商品价值[3-4]。
不同品种的苹果气调参数不同,“红富士”苹果的O2浓度通常控制在3~5 kPa,CO2浓度不超过3 kPa;“元帅”和“金冠”苹果的O2浓度不低于2 kPa,CO2浓度不超过5 kPa;而“金帅”苹果的最适气体成分为2 kPa O2和2 kPa CO2。当O2浓度过低、或CO2浓度过高时,苹果往往发生无氧呼吸和气体伤害的症状,研究发现相比于“金帅”苹果,“寒富”苹果对CO2更敏感[4],“富士”苹果在长期不适的气调环境中,果肉易发生褐变,总酚和抗坏血酸含量降低,而总酸及多酚氧化酶(polyphenol oxidase, PPO)活性升高,过氧化氢酶(catalase, CAT)、超氧化物歧化酶(superoxide dismutase,SOD)等抗氧化酶的活性受到抑制[5]。并且,富士苹果对CO2的敏感程度与品种、成熟度、贮藏条件和时间、气体种类和浓度等都有关系[6-7]。研究也发现,苹果自发气调包装贮藏期间,由于自身的呼吸作用和塑料袋的密封性,苹果更容易受到低O2、高浓度CO2的气体伤害[8]。研究表明,采用0、2、5、8 kPa CO2处理“富士”苹果可导致贮藏品质发生变化,2 kPa CO2处理可有效延缓果实硬度下降,提高可溶性固形物和总酸含量,维持较高的果实品质,而5 kPa 和8 kPa的CO2会导致果实生理代谢失调,造成果皮和果肉褐变症状,CO2浓度越高,伤害症状越严重[9]。目前,对于高浓度CO2伤害苹果的生理机制,一些研究表明,20 kPa 高CO2处理干扰了果实组织中的三羧酸循环,造成了丙酮酸的积累,从而引发了褐变[10-11],也有研究表明,CO2伤害与细胞内的抗氧化状态有关,高浓度CO2(10 kPa CO2)导致了苹果组织的氧化还原平衡失调,引起膜结构受到破坏,从而导致了CO2伤害[12]。最近通过转录组和代谢组的分析发现,“富士”苹果CO2伤害的发生与氧化还原过程、脂类代谢、激素信号转导和能量代谢等都有关,也与类黄酮代谢、有机酸代谢过程有关,是一个系统的调节过程[10]。然而,目前对于“秦脆”、“瑞雪”等新品种贮藏期间耐受CO2的差异还缺乏系统的研究。
因此,本文以“富士”苹果为参照,采用理化分析方法研究了“秦脆”和“瑞雪”苹果在高浓度CO2贮藏条件下的糖酸、维生素、挥发性气体成分等品质变化,考察了高CO2贮藏条件下苹果抗氧化相关酶及总酚、DPPH自由基清除率等相关指标的变化规律,以期为丰富苹果CO2伤害理论,开发苹果气调保鲜新技术提供参考。
1 材料与方法
1.1 材料与试剂
苹果,品种为“富士”、“秦脆”和“瑞雪”,于2024年11月份采摘,当天运回0 ℃冷库,挑选大小一致、颜色均匀,表面无机械伤、无病虫害的果实用于实验,果实在0 ℃下预冷3 d后置于气调箱。
邻菲咯啉(分析纯),上海麦克林生化科技有限公司;无水碳酸钠、无水乙醇、95%(体积分数)乙醇溶液、抗坏血酸、聚乙烯聚吡咯烷酮(polyvinylpyrrolidone,PVPP)、磷酸氢二钠、磷酸二氢钠、愈创木酚、邻苯二酚(均为分析纯),天津市凯通化学试剂有限公司;福林酚、EDTA、氧化型谷胱甘肽、NADPH(分析纯),北京索莱宝科技有限公司。
1.2 仪器与设备
CR-400色差计,柯尼卡美能达公司;AL204万分之一天平,瑞士梅特勒-托利多集团;PAL-1数字式糖度计折光仪,日本Atago公司;FW-80液氮研磨仪,北京市永光明医疗仪器有限公司;T6紫外可见分光光度计,北京普析通用仪器责任公司;UV-5100B紫外可见分光光度计,上海元析仪器有限公司;GL-20G-II高速冷冻离心机,长沙英泰有限公司;QP-2010-plus气相色谱-质谱联用仪,日本岛津公司。
1.3 实验方法
1.3.1 苹果样品的处理
设置空气对照(21.0 kPa O2+0.03 kPa CO2)、高浓度CO2(2 kPa O2+15 kPa CO2)2组处理,每组设置3个平行,每个平行用30个苹果。“富士”、“秦脆”、“瑞雪”的对照组和处理组分别标注为FS-CK、QC-CK、RX-CK,FS-CA、QC-CA和RX-CA。苹果贮藏条件为(0±1) ℃、90%相对湿度。分别在0、15、30、60、90 d取样,取样后进行拍照观察,并分别取果皮和果肉,测定颜色和可溶性固形物含量,其余样品液氮冷冻后放入-80 ℃备用,以测定其他指标。
1.3.2 果实颜色及CO2伤害发生率的测定
在果实赤道部位随机选取3个点,使用色差计测定苹果果实的颜色值(L*、a*、b*);果实CO2伤害发生率采用计数法测定,以果皮和果肉出现伤害的果实占总果实的百分比表示,计算如公式(1)所示:
CO2伤害发生率![]()
(1)
式中:发生伤害的果实数量,个;总果实数量,个。
1.3.3 果实糖酸品质及抗坏血酸含量的测定
利用PAL-1数显折光仪测定果实可溶性固形物含量(soluble solid content,SSC)。参考曹建康等[13]的方法,总酸度(total acid,TA)采用酸碱滴定法测定。参照曹建康等[13]的方法测定抗坏血酸(ascorbic acid,AsA)含量,称取0.5 g样品,加入1 mL 50 g/L三氯乙酸,定容至5 mL,于4 ℃下10 000 r/min离心10 min后过滤。取1.0 mL样品提取液,加入1.0 mL无水乙醇、0.5 mL 4 g/L磷酸-乙醇溶液,1.0 mL 5 g/L邻菲咯啉-乙醇溶液,0.5 mL 0.3 g/L FeCl3-乙醇溶液,测定在534 nm处吸光度。
1.3.4 果实挥发性香气成分的测定
将果肉样品和氯化钠固体按照10∶3的质量比装入20 mL样品瓶,利用萃取头在40 ℃加热条件下顶空吸附30 min后进样测定,解析3 min。色谱条件:Rtx-5MS毛细管色谱柱(30 m×0.25 mm,0.25 μm);进样口温度为250 ℃;升温程序:35 ℃保持2 min,然后以6 ℃/min升至120 ℃,再以10 ℃/min升至180 ℃,最后以20 ℃/min升至250 ℃保持5 min。载气为氦气,流速0.8 mL/min。质谱条件:电子电离方式;离子源温度为250 ℃;电子能量70 eV。
1.3.5 果实总酚含量和DPPH自由基清除率的测定
总酚含量的测定参考曹建康等[13]的方法,称取0.5 g样品,加入2 mL 70%(体积分数)丙酮,室温浸提1 h,于4 ℃下10 000 r/min离心20 min。取0.2 mL上清液加入0.5 mL福林酚试剂和10%(体积分数)的Na2CO3溶液,定容至10 mL,于25 ℃水浴1 h,765 nm条件下测定吸光度。DPPH自由基清除率的测定方法为称取0.5 g样品,加入2.5 mL的95%(体积分数)乙醇溶液,于4 ℃下10 000 r/min离心15 min。取上清液0.5 mL,加入2.5 mL、0.1 mmol/L的DPPH乙醇溶液,室温避光反应30 min后于517 nm下测定吸光值,计算如公式(2)所示:
DPPH自由基清除率![]()
(2)
式中:Ai,样品液的吸光度值,nm;At,对照的吸光度值,nm。
1.3.6 果实PPO活性的测定
称取1.0 g样品,加入0.05 g PVPP和3 mL的0.1 mol/L pH 6.8磷酸缓冲液,于4 ℃下10 000 r/min离心15 min,得到上清液。将1.5 mL的磷酸缓冲液和0.75 mL 0.1 mol/L的邻苯二酚混匀,并迅速加入0.75 mL粗酶液,于420 nm波长下测定吸光值,PPO活性以每分钟吸光度变化0.01为一个酶活力单位(U/g)。
1.3.7 果实过氧化物酶(peroxidase, POD)、CAT、SOD活性的测定
参考曹建康等[13]的方法,称取0.5 g样品、0.025 g PVPP,加入1.5 mL的0.1 mol/L pH 6.8磷酸缓冲液,于4 ℃下10 000 r/min离心15 min,得到上清液。将140 μL愈创木酚加入250 mL磷酸缓冲溶液中,加热溶解后加入95 μL 30%(体积分数)双氧水,取上述反应液2.6 mL,加入0.4 mL粗酶液,以磷酸缓冲液代替粗酶液为对照,于470 nm下测定吸光度值,POD活性以每分钟吸光值变化0.01为一个酶活力单位(U)。称取1.0 g样品、0.025 g PVPP加入2 mL的0.1 mol/L pH 7.0磷酸缓冲液,于4 ℃下10 000 r/min离心15 min,得到上清液。CAT反应液包括2 mL磷酸缓冲液、0.8 mL 0.3%(体积分数)H2O2溶液、0.2 mL 酶液,于240 nm波长下测定吸光值,CAT酶活以每分钟吸光值变化0.01为一个酶活力单位(U/g)。称取0.5 g样品、加入2 mL的0.05 mol/L pH 7.8磷酸缓冲液,于4 ℃下10 000 r/min离心15 min,得到上清液。反应体系包括1.5 mL磷酸缓冲液、0.3 mL 130 mmol/L甲硫氨酸,0.3 mL 0.75 mmol/L氯化硝基四氮唑蓝水溶液,0.3 mL 0.1 mmol/L EDTA-Na2,0.3 mL 0.1 mmol/L核黄素、0.5 mL待测上清液,于光照培养箱中反应30 min,于560 nm处测定吸光度。SOD活性以每分钟反应体系对氮蓝四唑反应抑制50%时的酶量为一个酶活力单位(U)。
1.3.8 果实抗坏血酸过氧化物酶(ascorbate peroxidase, APX)、谷胱甘肽还原酶(gluathione reductase,GR)活性的测定
参考曹建康等[13]的方法测定APX酶活,称取0.5 g 样品,加入2 mL提取缓冲液[含0.1 mmol/L EDTA、1 mmol/L抗坏血酸和2%(体积分数)PVPP],用0.1 mol/L pH 7.5磷酸钾缓冲液溶解,于4 ℃下10 000 r/min离心30 min,得到上清液。取2.5 mL反应缓冲液(含0.1 mmol/L EDTA、0.5 mmol/L抗坏血酸)加入0.2 mL酶提取液、0.3 mL 2 mmol/L H2O2溶液,于290 nm下测定吸光度值,APX活性以每克样品反应体系吸光度值降低0.01作为一个酶活力单位(U)。GR活性测定为称取0.5 g样品,加入2 mL的0.1 mol/L pH 7.5的磷酸缓冲液(含1 mmol/L EDTA),于4 ℃下10 000 r/min离心30 min,得到上清液。取2.7 mL上述磷酸缓冲液、0.1 mL的5 mmol/L氧化型谷胱甘肽溶液、0.2 mL酶液、40 μL的4 mmol/L NADPH溶液,于340 nm下测定吸光度值,GR活性以每克样品反应体系吸光度值降低0.01作为一个酶活力单位(U)。
1.4 数据处理
实验数据的分析及作图使用Excel 2019软件进行,以“平均值±标准差”表示,并使用IBM SPSS Statistics 26对数据进行统计分析,采用邓肯检验进行差异显著性分析(P<0.05表示差异显著)。
2 结果与分析
2.1 高浓度CO2处理对苹果外观及CO2伤害发生率的影响
如图1-a所示,新鲜的3种苹果果面平滑光洁、颜色分布均匀。随着贮藏时间的延长,相比于对照,CO2处理后“富士”苹果果皮和果肉颜色变化不大,而“秦脆”苹果的果肉、“瑞雪”苹果的果皮在CO2处理30 d之后均出现明显的褐变;并随贮藏时间的延长而加重。从CO2伤害发生率也可以看出(图1-b),实验期间富士苹果CO2伤害发生率仅1.00%,“瑞雪”苹果的CO2伤害发生率高于“秦脆”苹果,在贮藏30 d之后,“瑞雪”和“秦脆”苹果的CO2伤害发生率分别为45.00%和12.50%,贮藏90 d后,“瑞雪”苹果所有果实都发生了CO2伤害。综合来看,黄皮的“瑞雪”苹果更容易受到CO2伤害,这与在黄富士上的研究结果是一致的[14]。

a-苹果外观;b-CO2伤害发生率
图1 高浓度CO2处理对苹果外观及CO2伤害发生率的影响
Fig.1 Effect of high-concentration CO2 treatment on appearance and CO2 injury incidence rate of apple fruits
注:CK表示空气处理组;CA表示高CO2处理组,不同字母表示显著性差异(P<0.05)(下同)。
2.2 高浓度CO2处理对苹果果实相关品质指标的影响
2.2.1 对果皮和果肉颜色的影响
苹果果皮和果肉的颜色不仅是品种特征的表现,更与营养价值和人们的接受度密切相关。由图2-a~图2-f可知,“瑞雪”苹果果皮L*显著(P<0.05)高于“富士”和“秦脆”苹果,但三者果肉L*值差异不显著(P>0.05),随着贮藏时间的延长,3个苹果品种的果皮和果肉的L*值均呈下降趋势,a*值与b*值均呈上升趋势。相较于对照,CO2处理组的果皮和果肉L*值始终低于对照组,其中“瑞雪”苹果果皮L*下降最为迅速,贮藏30 d,“瑞雪”苹果CO2处理组的果皮L*仅为对照组的78.25%,贮藏90 d后仅为对照组的54.86%,而“秦脆”苹果果肉L*值下降最快,贮藏30 d后,CO2处理组果肉L*值仅为对照组的95.49%。
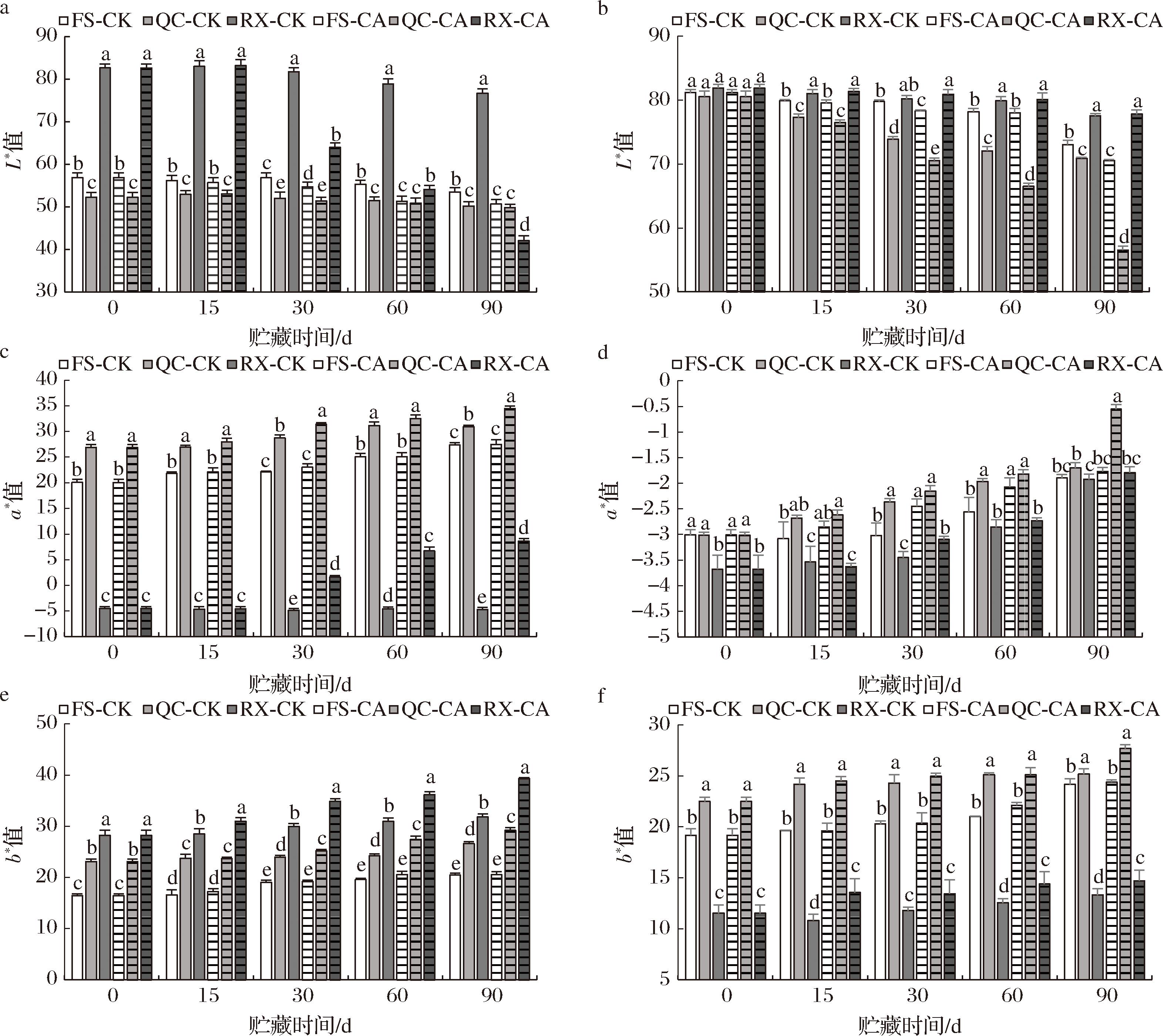
a-果皮L*值;b-果肉L*值;c-果皮a*值;d-果肉a*值;e-果皮b*值;f-果肉b*值
图2 高浓度CO2处理对“富士”、“秦脆”、“瑞雪”果实颜色的影响
Fig.2 Effect of high-concentration CO2 treatment on fruit color of ‘Fuji’, ‘Qincui’, and ‘Ruixue’ apple
从a*值来看,“秦脆”苹果果皮和果肉的a*值最高,而“瑞雪”苹果的a*值最小,与对照组相比,CO2处理均增加了果皮和果肉的a*值,特别是“瑞雪”苹果在贮藏30 d之后,a*值从-4.50 变为1.60。从b*值来看,“瑞雪”苹果果皮b*值最高,其次是“秦脆”和“富士”苹果,与对照相比,CO2处理增加了果皮和果肉的b*值,贮藏90 d后,“富士”、“秦脆”、“瑞雪”的果皮b*值分别比对照提高了0.44%、9.68%、23.50%,从果肉b*值来看,“秦脆”果肉的b*值最高,“瑞雪”苹果果肉b*值最小。许多研究表明,苹果颜色L*、a*和b*值的差异与其品种特性相一致,随着贮藏时间的延长,苹果果皮褪色变黄、亮度降低[15],这与本研究的结果一致,“瑞雪”苹果果皮黄色,b*值较高,而“富士”和“秦脆”苹果果皮红色,a*值较高。这种颜色差异的原因主要是由于苹果自身花青素、叶绿素、类胡萝卜素等色素共同作用造成的,也与可溶性固形物、总酸等品质指标及贮藏条件有关[16]。此外,研究也表明,高浓度CO2可以导致贮藏期间苹果果皮或果肉褐变,使果实颜色L*值下降和b*值增加,这可能由于CO2处理导致三羧酸循环无法正常运行,积累丙酮酸产生乙醛或乙醇所致,也可能与CO2导致氧化还原失衡、膜结构的破坏和酚类代谢异常有关[10,12]。
2.2.2 对果实糖酸品质及抗坏血酸含量的影响
可溶性固形物、总酸和抗坏血酸含量是苹果果实品质的核心指标,与果实的感官品质和商品价值密切相关[17]。由图3-a可知,“富士”、“秦脆”和“瑞雪”苹果果实的可溶性固形物含量在14.80%~15.80%,瑞雪苹果的可溶性固形物含量显著(P<0.05)高于富士和秦脆苹果,随着贮藏时间的延长,果实可溶性固形物含量略有增加,这可能与果实失水和后熟作用有关[18],与对照相比,高CO2处理抑制了果实可溶性固形物的变化,贮藏90 d后,“富士”、“秦脆”、“瑞雪”苹果可溶性固形物含量仅为对照组的97.54%、95.00%、95.02%。由图3-b可知,3种苹果的总酸均在0.25%左右,三者之间无显著差异(P>0.05),随着贮藏时间的延长,苹果总酸含量呈现逐渐下降的趋势,贮藏90 d之后,总酸含量仅为0.16%。与对照组相比,高CO2处理抑制了总酸含量的下降,特别是高CO2处理后的“秦脆”苹果总酸含量明显增加,30 d时达到顶峰,显著(P<0.05)高于其他处理组。由图3-c可知,“瑞雪”苹果的抗坏血酸含量显著(P<0.05)高于“富士”和“秦脆”苹果,随着贮藏时间的延长,对照组的苹果抗坏血酸含量均呈缓慢上升趋势,与对照组相比,高CO2处理抑制了抗坏血酸含量的增加,特别是在贮藏30 d后开始低于对照组,以“秦脆”苹果抗坏血酸含量下降最快,这也与“秦脆”苹果CO2处理后果肉褐变的趋势相一致,表明果实褐变与抗坏血酸的损失密切相关。研究表明,贮藏期间苹果的可溶性固形物、总酸、抗坏血酸含量一般呈下降趋势,主要是由于果实呼吸导致糖分被代谢、有机酸分解所致,但也受品种、果实成熟度和贮藏条件的影响而有所差异[19],而本研究中的可溶性固形物略有增加可能由于气调环境下果实容易失水及果实后熟作用导致的。研究也发现,在高CO2条件下,影响最大的差异代谢物是脂类和有机酸类,高CO2处理会导致苹果酸、琥珀酸等有机酸含量的下降[10,20],这与本研究的结果相一致,而有机酸含量下降的原因可能是CO2影响了三羧酸循环,导致有机酸代谢紊乱所致[10]。此外,苹果品种不同,对CO2敏感性不同,这也是导致3个苹果品种品质指标出现差异的原因之一。

a-可溶性固形物含量;b-总酸含量;c-抗坏血酸含量
图3 高浓度CO2处理对‘富士’、‘秦脆’和‘瑞雪’苹果果肉可溶性固形物、总酸和抗坏血酸含量的影响
Fig.3 Effect of high-concentration CO2 treatment on soluble solids content, total acid and ascorbic acid content in the flesh of ‘Fuji’, ‘Qincui’ and ‘Ruixue’ apple
2.2.3 对果实挥发性香气成分的影响
如图4-a所示,从3个苹果品种挥发性香气成分来看,“富士”苹果中主要的挥发性香气成分是酯类(60.66%)、醛类(13.40%)和醇类(9.63%),其中占比较高的是2-甲基丁基乙酸酯、乙酸己酯、2-己烯醛、乙酸丁酯、1-己醇等成分,这与其他研究富士苹果香气主要是酯类成分的结果相一致[20]。“秦脆”和“瑞雪”苹果主要以醛类为主,占比分别为41.47%和50.88%,以2-己烯醛含量最高。其中,“秦脆”苹果中酯类和醇类含量分别为26.87%和9.77%,包括乙酸丁酯、乙酸己酯、2-甲基丁基乙酸酯、1-己醇等成分。而“瑞雪”苹果中醇类含量高于酯类含量,主要包括2-甲基-1-丁醇、正己醛、丁酸己酯、1-己醇等成分,并且,“瑞雪”苹果的酸类和酮类物质含量高于“秦脆”和“富士”苹果主要成分列表见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043377)。研究表明苹果中主要特征香气成分为30~40种,因苹果品种和成熟度而有差异,可分为酯香型、清香型等类型[16]。“秦脆”由“富士”和蜜脆杂交而成,而“瑞雪”由“秦富1号”和“粉红女士”杂交选育而来,这可能是导致3种苹果香气成分差异的主要原因[21]。
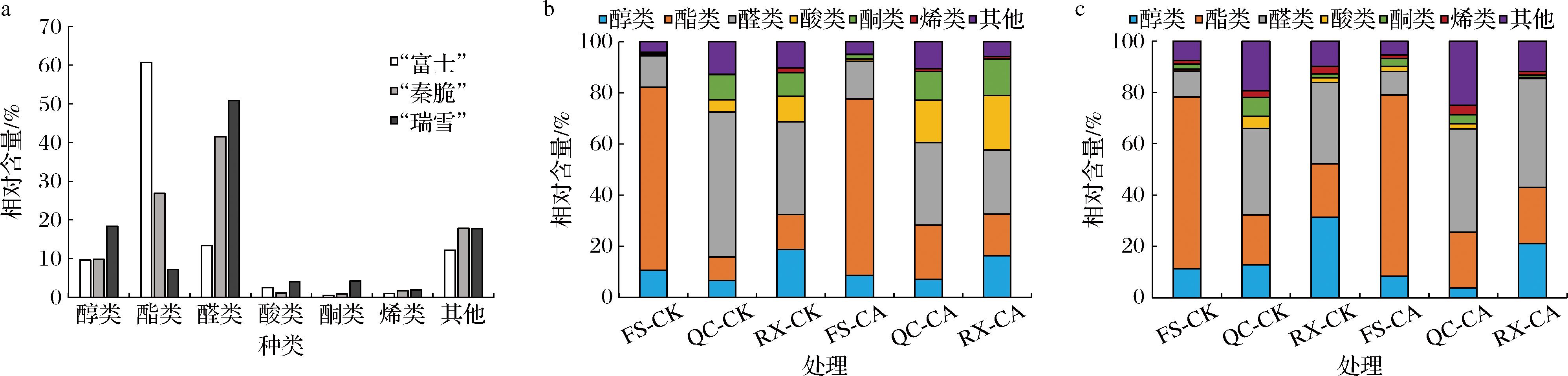
a-3种苹果主要挥发性香气成分;b-贮藏30 d后不同处理条件下的香气成分;c-贮藏60 d后不同处理条件下的香气成分
图4 高浓度CO2处理对“富士”、“秦脆”、“瑞雪”苹果挥发性香气成分的影响
Fig.4 Effect of high-concentration CO2 treatment on volatile aroma compounds in ‘Fuji’, ‘Qincui’ and ‘Ruixue’ apple
由图4-b和图4-c可知,贮藏30 d和60 d后,对照组“富士”苹果酯类、醇类等含量变化不大,但酮类、烯类、其他类物质含量增加,与对照组相比,CO2处理降低了富士苹果酯类和醇类的含量,但是增加了醛类、酸类、酮类等物质的含量。对于秦脆苹果,贮藏30 d后,对照组果实醇类和酯类为6.62%和9.15%,醛类物质达到56.79%,与对照组相比,CO2处理提升了“秦脆”苹果酯类和酸类物质含量,分别达到21.27% 和16.75%,但降低了醛类物质含量。贮藏60 d后,CO2处理组“秦脆”苹果果肉褐变严重,醇类物质明显下降,而其他类物质明显上升。对于“瑞雪”苹果,贮藏30 d后,对照组果实醛类占比为36.21%,醇类和酯类占比为18.69%和13.77%,贮藏60 d后,醛类占比变化不大,但醇类和酯类增加到31.26%和20.88%,与对照组相比,CO2处理提升了酯类物质含量,其他成分变化因贮藏时间和处理条件而不同。针对乙醇、乙醛、乙酸等指标来看,乙醇和乙醛很少被检测到,但与对照相比,贮藏30 d时,CO2处理显著提高了果实乙酸含量,但贮藏60 d后乙酸含量反而下降,这可能由于贮藏后期气体伤害严重所致。研究表明,贮藏温度、贮藏时间、处理手段等都会影响苹果挥发性香气成分的组成和含量[21],随着贮藏时间的延长,鲁丽苹果醛类物质呈下降趋势、酯类呈上升趋势,与本研究中“秦脆”和“瑞雪”的变化相似[16]。也有研究表明,高CO2条件下,“富士”苹果果实中的甲酯、乙酯含量会增加,但丁酯、己酯、丙酯等含量下降,其中,产生的乙醇可能代谢为乙酸乙酯等产物,这也可能是未检测到乙醛或乙醇的原因[22-23],并且,研究表明CO2可干扰苹果果实脂类、有机酸类、糖类、次生代谢等多种代谢过程,这可能是造成果实挥发性香气成分复杂多变的主要原因[10,22]。
2.3 高浓度CO2处理对苹果果实抗氧化相关指标的影响
2.3.1 对苹果果肉PPO和POD活性的影响
如图5-a所示,3个苹果品种以“富士”的PPO活性最高,其次是“秦脆”和“瑞雪”,PPO活性仅为“富士”苹果的79.01%和43.98%。整个贮藏期间,3个品种对照组的PPO活性均略有上升,与对照组相比,高CO2处理显著(P<0.05)抑制了“富士”和“秦脆”苹果的PPO活性,贮藏30 d后,“富士”和“秦脆”苹果的PPO活性分别为对照组的71.24%和80.56%,而CO2处理提高了“瑞雪”苹果果实贮藏期间的PPO活性。从POD活性来看(图5-b),3个苹果品种同样以“富士”苹果的POD活性最高,其次是“秦脆”和“瑞雪”。贮藏期间,POD活性呈现先下降后上升的趋势,与对照组相比,高CO2处理抑制了“富士”和“瑞雪”苹果POD活性的变化,但对“秦脆”苹果POD活性影响不大,在贮藏后期,处理组POD活性略有增加。研究表明,苹果果实CO2伤害的主要特征为果皮或果肉褐变,褐变主要由酶促褐变和非酶促褐变产生,也涉及果实体内的呼吸代谢、活性氧代谢和氧化还原平衡的调节作用[11,24],本实验中CO2处理抑制了PPO和POD的活性,表明CO2干扰了苹果褐变相关酶的活性,这与一些研究结果是一致的[25],但也有研究表明,CO2伤害导致的梨果心褐变、“寒富”苹果褐变与其PPO活性呈正相关,但CO2对“金冠”苹果PPO无显著影响,CO2伤害主要是导致了线粒体、质体和质膜等受到破坏,细胞膜透性增加,从而促使了褐变的发生[12,24]。
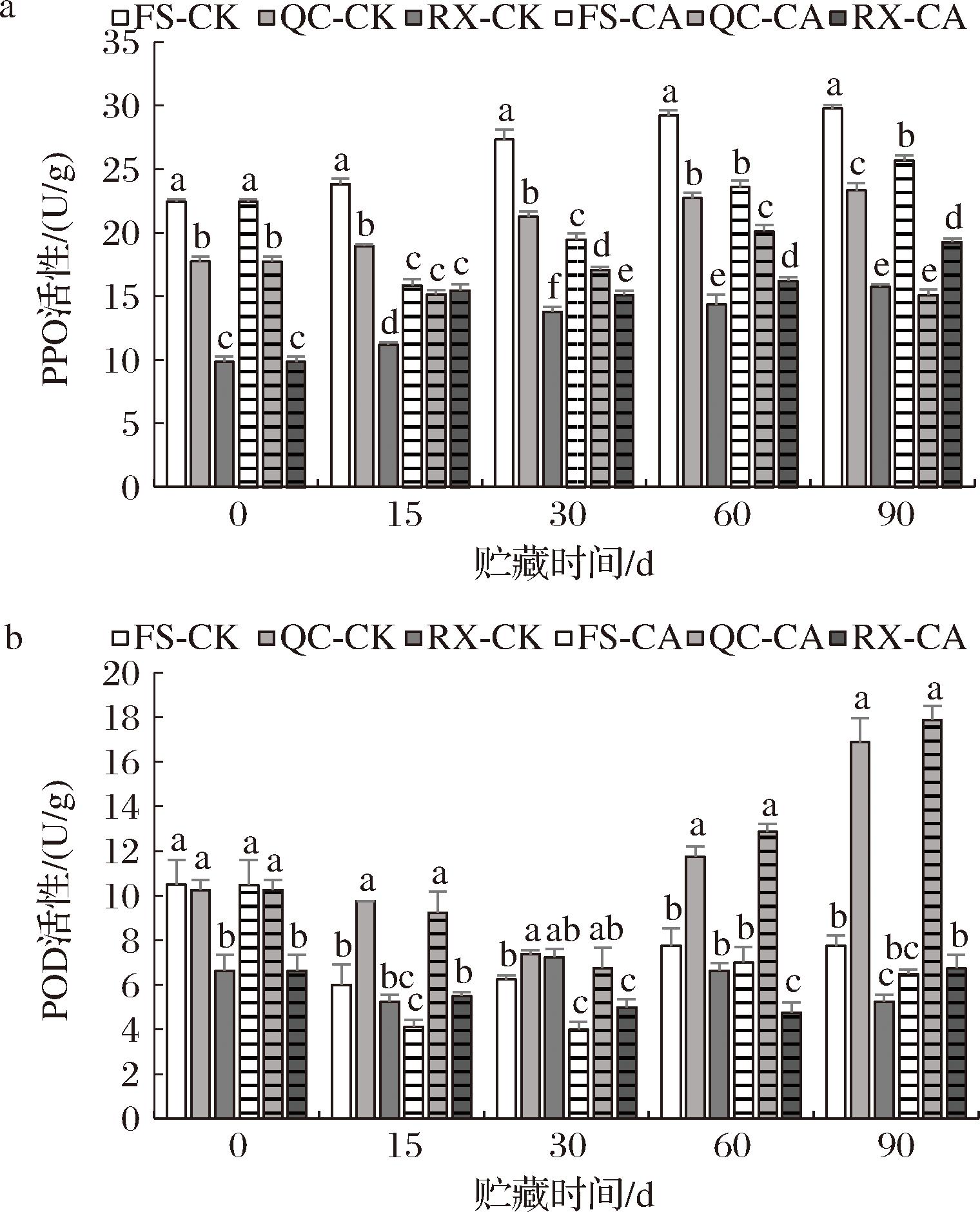
a-PPO活性;b-POD活性
图5 高浓度CO2处理对“富士”、“秦脆”、“瑞雪”苹果果肉PPO和POD活性的影响
Fig.5 Effect of high-concentration CO2 treatment on PPO and POD activities of ‘Fuji’, ‘Qincui’, and ‘Ruixue’ apple
2.3.2 对苹果果肉总酚含量和DPPH自由基清除率的影响
由图6-a可知,3个苹果品种中,以“富士”总酚含量最高,其次是“秦脆”和“瑞雪”。随着贮藏时间的延长,苹果总酚含量呈先降低后升高的趋势。与对照组相比,高浓度CO2处理促进了“富士”和“秦脆”苹果贮藏前期总酚含量的增加,但对“瑞雪”苹果影响不大。研究表明,苹果富含多酚类物质,不仅具有抗氧化防御作用,也在酶促褐变中作为底物起作用[26]。CO2处理促进贮藏前期酚类物质的增加,可能由于CO2促进了苹果的抗氧化防御反应导致的[27]。由图6-b所示,3个苹果品种的DPPH自由基清除率同样是“富士”最高,其次是“秦脆”和“瑞雪”。随着贮藏时间的延长,DPPH自由基清除率呈现逐渐升高的趋势,变化范围从50.00%左右到60.00%,这与陈宇航[25]在“富士”苹果上的研究结果是一致的,但与“鲁丽”苹果贮藏期间DPPH自由基清除率的变化不一致[16],可能与品种、贮藏条件和采收成熟度等因素有关。与对照相比,CO2处理在贮藏前30 d促进了“富士”和“瑞雪”苹果DPPH自由基清除率的升高,但在贮藏30 d后显著(P<0.05)抑制了DPPH自由基清除率的增加,特别是“秦脆”处理组,贮藏30 d和90 d后,DPPH自由基清除率仅为对照组的91.52%和80.91%,这与“秦脆”苹果果肉褐变和PPO活性的变化趋势一致,表明“秦脆”苹果耐受CO2的能力较差,在高CO2处理条件下,果实抗氧化系统被破坏,DPPH自由基清除率显著下降[14]。
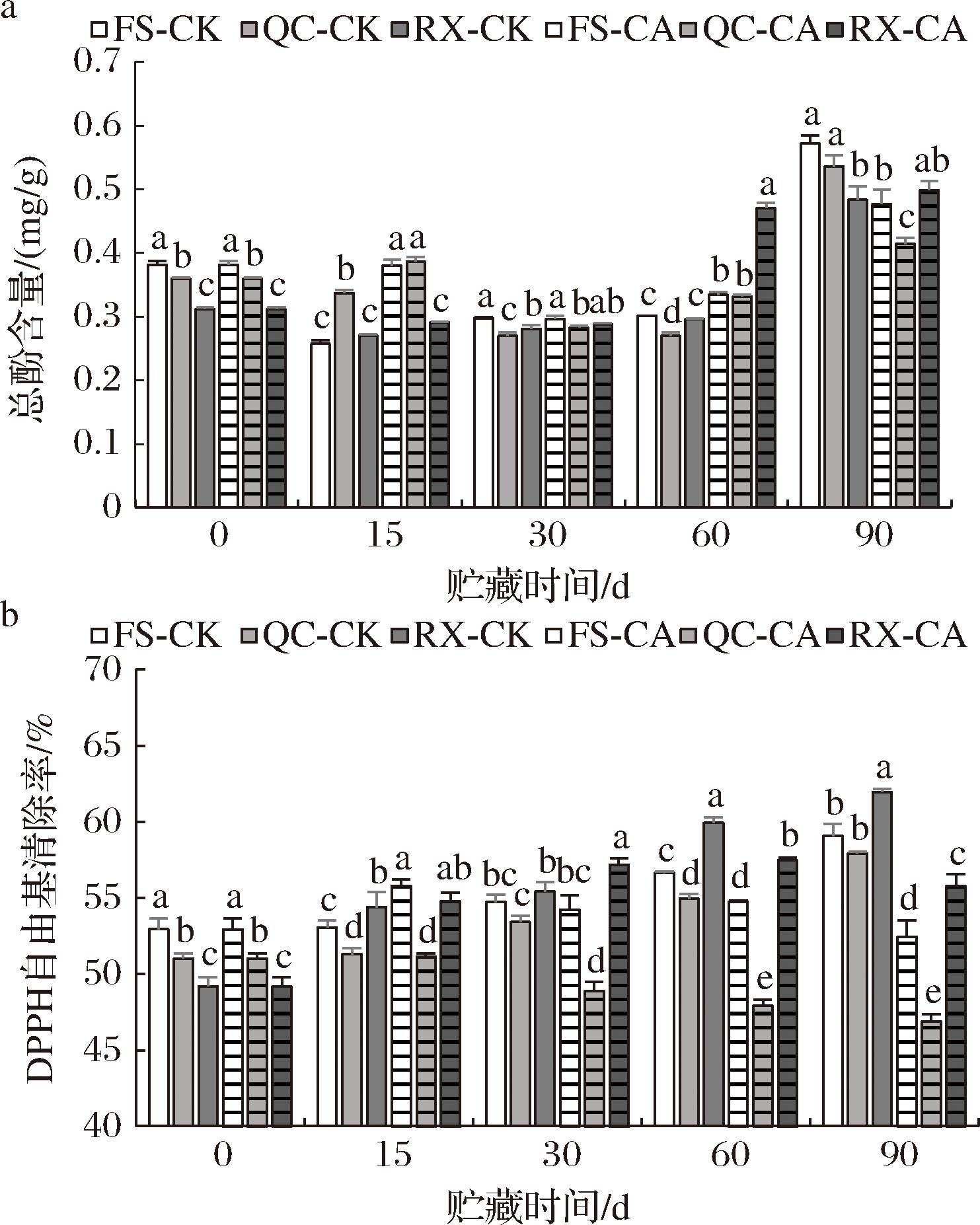
a-总酚含量;b-DPPH自由基清除率
图6 高浓度CO2处理对“富士”、“秦脆”、“瑞雪”苹果果肉总酚含量和DPPH自由基清除率的影响
Fig.6 Effect of high-concentration CO2 treatment on total phenolic content and DPPH radical scavenging activity of ‘Fuji’, ‘Qincui’, and ‘Ruixue’ apple
2.3.3 对苹果果肉抗氧化相关酶活性的影响
果实对外界胁迫的响应也与CAT、SOD、APX和GR等抗氧化相关酶的活性有关,如图7-a和图7-b所示,富士苹果的CAT或SOD活性高于秦脆和瑞雪苹果,整个贮藏期间,对照组CAT活性变化不大,而SOD活性略有上升。与对照相比,高CO2处理抑制了CAT和SOD活性的增加,特别是“秦脆”苹果,CO2处理对其CAT和SOD活性抑制最为明显。贮藏90 d后,CO2处理组的“富士”、“秦脆”和“瑞雪”苹果CAT活性分别为对照组的42.86%、34.48%、70.59%,SOD活性分别为对照组的72.87%、63.77%、75.51%。由图7-c和图7-d可知,3个苹果品种的APX和GR活性均以“瑞雪”苹果最高,其次是“秦脆”和“富士”,随着贮藏时间的延长,APX活性逐渐增加,而GR活性呈先增加后下降的趋势。与对照相比,除了15 d的“秦脆”处理组之外,高浓度CO2处理均抑制了APX活性的增加,贮藏90 d后,CO2处理组的“富士”、“秦脆”和“瑞雪”苹果APX活性分别为对照组的83.85%、43.97%、89.15%,同时,高浓度CO2也抑制了3个品种苹果的GR活性的变化。
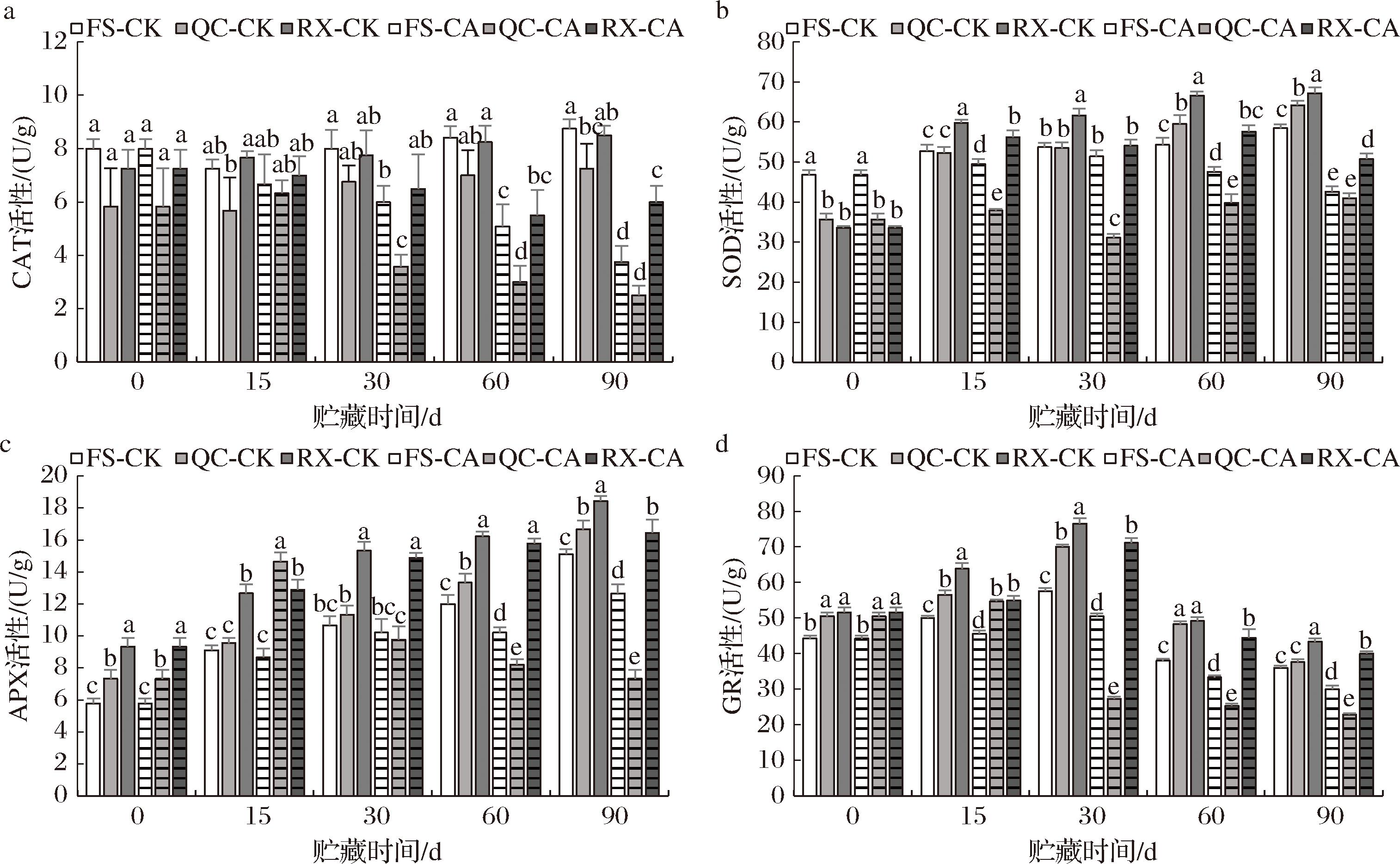
a-CAT活性;b-SOD活性;c-APX活性;d-GR活性
图7 高浓度CO2处理对“富士”、“秦脆”、“瑞雪”苹果果肉CAT、SOD、APX、GR活性影响
Fig.7 Effect of high-concentration CO2 treatment on CAT, SOD, APX and GR activities of ‘Fuji’, ‘Qincui’, and ‘Ruixue’ apple
研究表明,CAT可以将果实中积累的过氧化氢分解为水和氧气,SOD可以催化超氧阴离子转化为过氧化氢和氧气,从而保护细胞免受氧化损伤[28],因此,保持果实较高的CAT和SOD活性,可以减少氧化应激对果实的损害。研究也发现,高浓度CO2处理可以使“富士”苹果和西兰花的CAT和SOD活性下降[25,29],这与本研究结果一致,表明高浓度CO2导致了细胞中CAT和SOD活性的下降,加快了细胞膜的损伤。此外,APX和GR作为抗坏血酸-谷胱甘肽循环中的关键酶,能够催化抗坏血酸和过氧化氢反应,维持果实体内的氧化还原平衡[30],一旦果实受到外界非生物胁迫,APX和GR可以调节果实的抗氧化系统,避免受到氧化损伤。本研究发现CO2处理抑制了APX和GR活性,表明高浓度CO2降低了APX和GR的调控作用,这种调控作用的下降可能导致了CO2伤害症状的发生。但贮藏15 d的秦脆处理组果实APX活性明显上升,可能是秦脆苹果对于CO2抵抗力弱,表现出明显的防御反应所致,而这种反应随着时间的延长逐渐下降[22]。
3 结论
本实验系统研究了“富士”、“秦脆”和“瑞雪”3个品种耐受CO2的差异。结果表明,“富士”苹果对二氧化碳的抵抗力最强,贮藏期间未发现明显的CO2伤害症状,而“秦脆”苹果果肉、“瑞雪”苹果果皮都容易受到CO2伤害,0 ℃ 贮藏30 d出现明显症状。并且,相比于对照,CO2处理也降低了3种苹果果皮和果肉的L*值,增加了a*值和b*值,抑制了可溶性固形物的增加和总酸含量的下降。同时,CO2处理降低了富士苹果酯类和醇类的含量,增加了醛类、酸类、酮类等物质的含量;但CO2处理增加了“秦脆”和“瑞雪”苹果酯类物质含量,降低了醛类物质含量。从抗氧化能力来看,CO2处理抑制了贮藏期间“富士”和“秦脆”苹果的PPO活性,提高了“瑞雪”苹果的PPO活性。同时,CO2处理促进了贮藏前期“富士”和“秦脆”苹果总酚和DPPH自由基清除率的升高,但抑制了贮藏后期的变化,高浓度CO2处理也抑制了CAT、SOD、APX等抗氧化酶的活性。整体来看,CO2通过影响抗氧化酶及酚类物质干扰了苹果的抗氧化系统,影响了果实的糖酸品质和风味。本研究丰富了苹果CO2伤害的理论基础,为进一步探索苹果新品种耐受CO2的机制提供了参考。
[1] ELMANAWY A I, MARATAB A, GHAZAL A F, et al.Shelf-life assessment techniques for fruit and vegetables:Recent trends and future prospects[J].Postharvest Biology and Technology, 2025, 226:113521.
[2] AL SHOFFE Y, RUDELL D, PARK D, et al.Aroma volatiles and sensory quality of organically-grown apple cultivars after dynamic controlled atmosphere (DCA) storage and comparison with CA-stored fruit with and without 1-methylcyclopropene (1-MCP)[J].Postharvest Biology and Technology, 2024, 218:113162.
[3] JESENKO E, VIDRIH R, ![]() E, et al.Effect of long-term controlled atmosphere storage enriched with ethanol or hexanal vapour on primary and secondary aroma compounds of ‘Braeburn’ and ‘Granny Smith’ apples[J].Postharvest Biology and Technology, 2025, 226:113563.
E, et al.Effect of long-term controlled atmosphere storage enriched with ethanol or hexanal vapour on primary and secondary aroma compounds of ‘Braeburn’ and ‘Granny Smith’ apples[J].Postharvest Biology and Technology, 2025, 226:113563.
[4] BÜCHELE F, KHERA K, THEWES F R, et al.Dynamic control of atmosphere and temperature based on fruit CO2 production:Practical application in apple storage and effects on metabolism, quality, and volatile profiles[J].Food and Bioprocess Technology, 2023, 16(11):2497-2510.
[5] 高名月, 赵政阳, 王燕, 等.气调贮藏对瑞雪苹果的保鲜效果与果皮褐变机制的初探[J].食品与发酵工业, 2023, 49(4):123-129.GAO M Y, ZHAO Z Y, WANG Y, et al.Effects of controlled atmosphere on preservation of Ruixue apples and preliminary study on pericarp browning mechanism[J].Food and Fermentation Industries, 2023, 49(4):123-129.
[6] FAWBUSH F, NOCK J F, WATKINS C B, et al.External carbon dioxide injury and 1-methylcyclopropene (1-MCP) in the ‘Empire’ apple[J].Postharvest Biology and Technology, 2008, 48(1):92-98.
[7] ARGENTA L C, FAN X T, MATTHEIS J P, et al.Responses of ‘Fuji’ apples to short and long duration exposure to elevated CO2 concentration[J].Postharvest Biology and Technology, 2002, 24(1):13-24.
[8] 贾朝爽, 王志华, 王文辉, 等.包装袋对‘国光’苹果自发气调后货架期质地和品质的影响[J].中国果树, 2021(9):15-20.JIA C S, WANG Z H, WANG W H, et al.Effects of packaging bags on the shelf life texture and quality of ‘Ralls’ apple after modified atmosphere[J].China Fruits, 2021(9):15-20.
[9] 田蓉. 不同包装和不同CO2充气处理对红富士苹果保鲜效果及抗性生理的影响[D].杨凌:西北农林科技大学, 2015.TIAN R.Effects of different packaging and inflatable packaging at different CO2 concentrations on postharvest quality and resistance physiology of red Fuji apple[D].Yangling:Northwest A&F University, 2015.
[10] 徐晓艳, 刘港帅, 李泓利, 等.转录组和代谢组联合解析苹果采后高浓度CO2伤害机制[J].生物工程学报, 2021, 37(8):2856-2869.XU X Y, LIU G S, LI H L, et al.Analysis of apple postharvest damage under high CO2 concentration by transcriptome combined with metabolome[J].Chinese Journal of Biotechnology, 2021, 37(8):2856-2869.
[11] LUM G B, SHELP B J, DEELL J R, et al.Oxidative metabolism is associated with physiological disorders in fruits stored under multiple environmental stresses[J].Plant Science, 2016, 245:143-152.
[12] 陈昆松, 于樑, 周山涛, 等.鸭梨果实气调贮藏过程CO2伤害机理初探[J].中国农业科学, 1991,24(5):83-88.CHEN K S, YU L, ZHOU S T, et al.A preliminary study on possible mechanism of CO2 injury of ‘Ya-Li’ pear (Pyrus Bretscheideri Rend.) during CA storage[J].Scientia Agricultura Sinica, 1991,24(5):83-88.
[13] 曹建康, 姜微波, 赵玉梅, 等.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社, 2007.CAO J K, JIANG W B, ZHAO Y M, et al.Experiment Guidance of Postharvest Physiology and Biochemistry of Fruits and Vegetables[M].Beijing:China Light Industry Press, 2007.
[14] CHEN Y H, TAO N, MENG Z, et al.Preharvest debagging alleviates external CO2 injury of ‘Fuji’ apple during storage by improving antioxidant capacity and energy status[J].Postharvest Biology and Technology, 2023, 196:112180.
[15] 李秀芳. ‘红富士’苹果采后贮藏过程中色度及其色素成分变化的相关研究[D].杨凌:西北农林科技大学, 2014.LI X F.The changes in the chromaticity and pigment composition of ‘red fuji’ apple fruit during postharvest storage[D].Yangling:Northwest A&F University, 2014.
[16] 王震, 彭勇, 刘静润, 等.‘鲁丽’苹果低温贮藏和货架期间品质和生理变化[J].食品科学, 2023, 44(17):136-143.WANG Z, PENG Y, LIU J R, et al.Quality and physiological changes of ‘Luli’ apple during cold storage[J].Food Science, 2023, 44(17):136-143.
[17] 石建新, 赵猛, 赵迎丽, 等.气调贮藏对富士苹果采后生理及果肉褐变的影响[J].果树科学, 1999, 16(1):14-17.SHI J X, ZHAO M, ZHAO Y L, et al.Effect of CA storage on the postharvest physiology and the flesh browning of Fuji apples[J].Journal of Fruit Science, 1999, 16(1):14-17.
[18] 王雷, 田晓宁, 田雪婷, 等.‘富士’苹果不同O2/CO2简易气调贮藏的生理特性[J].果树学报, 2020, 37(6):909-919.WANG L, TIAN X N, TIAN X T, et al. Physiological characteristics of ‘fuji’ apple in different O2/CO2 simple controlled atmosphere storage[J]. Journal of Fruit Science, 2020, 37(6):909-919.
[19] ![]() -GASTÉLUM J, ALVAREZ-PARRILLA E, DE LA ROSA L, et al.Effect of harvest date and storage duration on chemical composition, sugar and phenolic profile of ‘Golden Delicious’ apples from northwest Mexico[J].New Zealand Journal of Crop and Horticultural Science, 2015, 43(3):214-221.
-GASTÉLUM J, ALVAREZ-PARRILLA E, DE LA ROSA L, et al.Effect of harvest date and storage duration on chemical composition, sugar and phenolic profile of ‘Golden Delicious’ apples from northwest Mexico[J].New Zealand Journal of Crop and Horticultural Science, 2015, 43(3):214-221.
[20] APREA E, COROLLARO M L, BETTA E, et al.Sensory and instrumental profiling of 18 apple cultivars to investigate the relation between perceived quality and odour and flavour[J].Food Research International, 2012, 49(2):677-686.
[21] THEWES F R, ARGENTA L C, DE OLIVERIA ANESE R, et al.The response of ‘Monalisa’ apples to high CO2 storage conditions, harvest maturity and 1-MCP treatment[J].Scientia Horticulturae, 2023, 317:112038.
[22] LI Y X, ZHENG C, WANG C, et al.Comparative transcriptome reveals molecular mechanism in apple genotypes differing in CO2 tolerance in CA storage[J].Postharvest Biology and Technology, 2022, 185:111807.
[23] LUMPKIN C, FELLMAN J K, RUDELL D R, et al.‘Fuji’ apple (Malus domestica Borkh.) volatile production during high pCO2 controlled atmosphere storage[J].Postharvest Biology and Technology, 2015, 100:234-243.
[24] 王超. 低O2、高CO2处理对寒富和金冠苹果采后贮藏褐变的影响[D].锦州:渤海大学, 2021.WANG C.Effects of low O2 and high CO2 treatment on postharvest browning of Hanfu and golden delicious apples[D].Jinzhou:Bohai University, 2021.
[25] 陈宇航. 苹果采前套袋影响采后果皮二氧化碳伤害的机理研究[D].泰安:山东农业大学, 2023.CHEN Y H.Study on the mechanism of preharvest bagging influencing postharvest external carbon dioxide injury of apples[D].Taian:Shandong Agricultural University, 2023.
[26] 高习习, 廖梓懿, 刘洪冲, 等.苹果采后处理与贮藏保鲜技术研究进展[J].保鲜与加工, 2021, 21(6):138-144.GAO X X, LIAO X Y, LIU H C, et al.Research progress on postharvest treatment and storage technology of apple[J].Storage and Process, 2021, 21(6):138-144.
[27] DU M J, LIU Z T, ZHANG X T, et al.Effect of pulsed controlled atmosphere with CO2 on the quality of watercored apple during storage[J].Scientia Horticulturae, 2021, 278:109854.
[28] 王晓慧, 李培培, 杜荣, 等.温度对采后阿克苏“红富士”苹果贮藏品质和活性氧代谢的影响[J].北方园艺, 2025(9):79-87.WANG X H, LI P P, DU R, et al.Effects of temperature on quality and active oxygen metabolism of Aksu ‘Red Fuji’ apple after harvest[J].Northern Horticulture, 2025(9):79-87.
[29] ZHU C R, LI H W, LI Q Q, et al.Increase of propionic acid production in broccoli florets influences the resistance to carbon dioxide injury[J].Postharvest Biology and Technology, 2024, 218:113129.
[30] 陈曦冉. 高浓度CO2对软枣猕猴桃伤害机制研究[D].沈阳:沈阳农业大学, 2022.CHEN X R.Study on the injury mechanism of high concentration of CO2 to Actinidia arguta[D].Shenyang:Shenyang Agricultural University, 2022.