吞咽困难是指与吞咽过程有关的器官,如:下颌骨、舌、咽部、食管等结构或功能受损,食物不能安全有效地运输到胃部的过程。吞咽困难会影响摄食及营养吸收,还会导致食物误吸入气管引发吸入性肺炎,严重者可危及生命[1]。各年龄段人群中都有吞咽困难患者,其中老年群体尤为突出。基础流行病学研究表明,成人吞咽困难的全球患病率约为60%,且患病率随着年龄增长显著上升。50岁以上人群的患病率约为8%~22%,65岁时则升至15%~30%,70岁以上人群更是高达40%[2]。造成该现象的原因是随着年龄的增长,人们出现咽喉肌肉萎缩、神经反射减弱、唾液分泌减少等生理性退化症状,使老年人吞咽协调功能下降[3]。在全球人口结构加速老化的背景下,老年群体规模持续增大,吞咽困难正成为一个日益严峻的社会问题,严重影响人类健康和生活质量[4]。
目前,仍没有治疗吞咽困难的有效方法。临床上,医护人员经常采用冷刺激法或让患者闲暇时咀嚼几块碎冰块,从而有效加强吞咽功能。此外,改变进食姿势或吞咽方式也可以改善吞咽功能[5]。然而,这些方法通常仅适用于吞咽困难患者的短期恢复。因此,为吞咽困难患者提供长期有效的饮食策略成为食品行业的一大挑战[6]。
吞咽困难治疗领域通常使用食品增稠剂来对黏度较低的流体食物进行增稠以提高其黏度,减缓其在吞咽过程中的流速,降低食物吸入气管的风险,从而达到治疗吞咽困难的目的[7]。常用的流体食品增稠剂可分为淀粉基增稠剂和胶基增稠剂两大类[6]。由于淀粉颗粒具有在液体中溶胀和部分溶解的性质,淀粉基增稠剂易造成糊状的口感,影响吞咽困难患者的接受程度,而且随着时间和温度的不同,其稠化液体的黏度也会有很大的变化,因此很难得到均匀稳定的稠化流体。此外,淀粉类增稠剂还会增加吞咽后的残留物,导致吞咽困难患者意外误吸的风险提高[8]。因此,淀粉基增稠剂可能被认为是不安全的选择。目前,商业化的增稠剂以胶基增稠剂为主。胶基增稠剂在人体口腔内不易被唾液淀粉酶分解,能在水溶液中形成缠结结构,并能在相对长的时间内保持稳定的黏稠度[9],故广泛应用于吞咽困难护理领域。
魔芋葡甘露聚糖(konjac glucomannan, KGM)是从魔芋块茎分离、纯化后得到的一种多糖。KGM作为一种非离子多糖,由D-葡萄糖和D-甘露糖按一定比例通过β-1,4-葡萄糖苷键连接[10]。KGM中含有少量的乙酰基,这不仅赋予KGM良好的水溶性,同时也使得KGM具有两亲性多糖的特性,可作为多糖乳化剂应用[11]。此外,由于其良好的溶解性、生物相容性和凝胶形成性能,KGM已作为优良的食品增稠剂在食品领域得到广泛应用[12]。透明质酸(hyaluronan, HA)是一种高分子线性糖胺聚糖,由N-乙酰氨基葡萄糖和D-葡萄糖醛酸通过β-1,4-糖苷键交替连接而成[11]。HA广泛存在于人体的各种组织中,具有保持水分、维持器官结构稳定、促进伤口愈合、润滑关节等特殊的生理功能,在组织工程、药物递送和免疫调节等方面得到了广泛的应用[13]。此外,HA还可以在水性介质中通过分子间作用力形成三维网状结构,显著提高溶液体系的黏度,展现出良好的增稠效果[14]。目前已有相关研究表明,KGM-HA复配体系在伤口闭合和治疗烧伤创面愈合、控制药物释放等领域具有较大应用潜力[15-16],但其在吞咽困难治疗领域仍缺乏研究。
基于此,本研究从流变学角度出发,以KGM-HA溶胶体系为研究对象,系统研究其微观网络结构、流变特性及吞咽安全性,旨在为吞咽困难患者开发安全稳定的食品增稠剂提供理论支撑。
1 材料与方法
1.1 材料与试剂
KGM,上海源叶生物科技有限公司;HA,上海麦克林生化科技有限公司;NaCl,国药集团化学试剂有限公司;去离子水,实验室提供。
1.2 仪器与设备
HR-1旋转流变仪,美国TA仪器公司;JB-2恒温数显磁力搅拌器,常州高德仪器制造有限公司;BSA224I-1CCN分析天平,塞多利斯科学仪器北京有限公司;DAWN/LC-20A多角度激光光散射-凝胶渗透色谱联用仪,岛津(上海)实验器材有限公司。
1.3 实验方法
1.3.1 KGM-HA溶胶体系的制备
分别称取KGM和HA于2个烧杯中,每个烧杯中分别加入50 mL 纯水,置于25 ℃恒温磁力搅拌器上持续搅拌2 h,使其充分溶解。将KGM溶液边搅拌边加入到HA溶液中,25 ℃条件下搅拌1 h。得到混合溶液的最终浓度为1.0 g/L,且KGM和HA的质量比分别为9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9,分别命名为K9H1,K8H2,K7H3,K6H4,K5H5,K4H6,K3H7,K2H8,K1H9。制备过程中保持烧杯密封环境,防止水分损失。制备完成后需要放冰箱冷藏24 h后才可进行下一步实验。
1.3.2 KGM-HA溶胶体系的微观结构
1.3.2.1 凝胶渗透色谱(gel permeation chromatography, GPC)
将样品溶解于纯水,质量浓度控制在0.5~1 mg/mL,静置过夜,用0.22 μm滤膜过滤后进样。以0.9 g/L NaCl水溶液为流动相(流速1.0 mL/min),联用多角度光散射检测器(波长660 nm)和示差折光检测器。根据校准曲线,采用ASTRA软件基于Zimm模型分析数据,手动划分色谱峰计算重均分子质量(weight average molecular weight,Mw)、数均分子质量(number-average molecular weight, Mn)及多分散指数(polydispersity index, PDI)。每组样品重复测定3次。
1.3.2.2 缠结特性
使用HR-1旋转流变仪探索KGM-HA溶胶体系的缠结特性。夹具选用夹角为1°的40 mm圆锥钢板,设置间隙为50 μm,振幅为1%,测量温度范围为0~50 ℃。设定角频率由0.1 rad/s以对数模式升至100 rad/s,测定期间的储能模量(storage modulus, G′)和损耗模量(loss modulus, G″)的角频率依赖性曲线的变化,根据时温等效原理获得较宽范围内的流变数据,得到平台模量(plateau modulus, ![]() 计算缠结分子质量(entanglement molecular weight, Me)[17],其计算如公式(1)所示:
计算缠结分子质量(entanglement molecular weight, Me)[17],其计算如公式(1)所示:
(1)
式中:Me,缠结分子质量,g/mol;c,质量浓度,kg/m3;R,理想气体常数,J/(mol·K);T,温度,![]() 平台模量,Pa。
平台模量,Pa。
计算得到的缠结分子质量结合凝胶渗透色谱测出的重均分子质量,可以计算出缠结数(number of entanglements, Z)、缠结密度(ν)、网格尺寸(a),其计算如公式(2)、公式(3)和公式(4)所示:
(2)
(3)
(4)
式中:Z,缠结数;Mw,重均分子质量,g/mol;Me,缠结分子质量,g/mol;ν,缠结密度,m-3;k,玻尔兹曼常数,J/K;T,温度,![]() 平台模量,Pa;a,网格尺寸,m。
平台模量,Pa;a,网格尺寸,m。
1.3.3 KGM-HA溶胶体系的流变特性测试
使用配备锥形几何系统(直径40 mm、1°锥角)的HR-1旋转流变仪探索KGM-HA溶胶体系的流变特性。所有测试至少一式三份进行。
1.3.3.1 KGM-HA溶胶体系的振荡剪切频率扫描测试
夹具选用夹角为1°的40 mm圆锥钢板,设置间隙为50 μm,在37 ℃条件下,扫描应变值为1%,设定角频率由0.1 rad/s以对数模式升至100 rad/s,测定期间的G′、G″和损耗角正切(tanδ)的变化。
1.3.3.2 KGM-HA溶胶体系的流动剪切稳态扫描测试
夹具选用夹角为1°的40 mm圆锥钢板,设置间隙为50 μm,在37 ℃条件下,选用稳态模式使剪切速率由0.001 s-1对数模式升至1 000 s-1,每个数量级取7个点,记录溶胶样品在流动剪切下的表观黏度变化。
为进一步比较流体黏度,分析溶胶样品的流动特性,以往研究常使用Carreau模型直接对黏度-剪切速率进行拟合以得到零剪切黏度(η0)参数[18]。为了更精确地拟合黏度曲线,凸显样品间差异,本研究在之前研究的基础上进一步优化了拟合方式。先利用黏度幂律模型对溶胶样品在流动剪切下的非牛顿线性区域进行拟合,得到非牛顿区流体指数(n)后再将其固定代入Carreau-Yasuda模型拟合得到KGM-HA溶胶体系的η0[19]。其中,Carreau模型如公式(5)所示:
(5)
黏度幂律模型如公式(6)所示:
(6)
Carreau-Yasuda模型如公式(7)所示:
(7)
式中:η,表观黏度,Pa·s;k,稠度系数;n,流体指数;η0,零剪切黏度,Pa·s;η∞,无穷剪切黏度,Pa·s;γ,剪切速率,s-1;λ,特征时间,s;α,无实际意义拟合参数。
1.3.3.3 KGM-HA溶胶体系的时间依赖性实验
夹具选用夹角为1°的40 mm圆锥钢板,设置间隙为50 μm,设置温度为37 ℃。分别在剪切速率为50、200 s-1的条件下剪切5 min,静置1 min,再剪切1 min,测试表观黏度随时间的变化情况。
1.3.4 KGM-HA溶胶体系的IDDSI分级评价
以IDDSI框架中的汤匙倾侧测试确定吞咽障碍食品等级[20]。用标准光滑的勺子盛起样品,观察样品在勺子上的状态,然后将勺子稳定地向侧面倾斜,观察样品的滑落状态,以及样品滑落后勺子表面状态。
1.4 数据统计与分析
所有实验重复3次,采用Microsoft Excel软件整理数据,利用Origin 2024软件绘图,使用IBM SPSS Statistics 27软件采用ANOVA进行数据分析,Duncan法进行差异显著性分析,以P<0.05表示差异显著。
2 结果与分析
2.1 KGM-HA溶胶体系的缠结特性
图1展示了浓度c=10.0 kg/m3的KGM-HA溶胶体系的G′和G″对角频率(ω)的依赖性曲线变化。在ωaT一定区间内,G′曲线上可以观察到一个倾斜的“橡胶态平台”,这是由于聚合物分子链间的缠结作用[21]。由图1可知,随着角频率增加,G′和G″逐渐增大,而G′的增速快于G″,导致当角频率增加到一定程度的时候G′会超过G″,出现交叉。该现象可能是由于角频率的增大促进了KGM和HA分子链的缠结作用,使样品由粘性主导向弹性主导过渡,体系的缠结网络结构越来越稳定。当KGM和HA的质量比为9∶1 时,平台模量最小,表明缠结网络松散化,这可能是由于KGM占比过高,分子链的竞争性聚集抑制缠结,而少量HA的添加可能影响了KGM的原始结构,使分子之间发生滑动[16]。
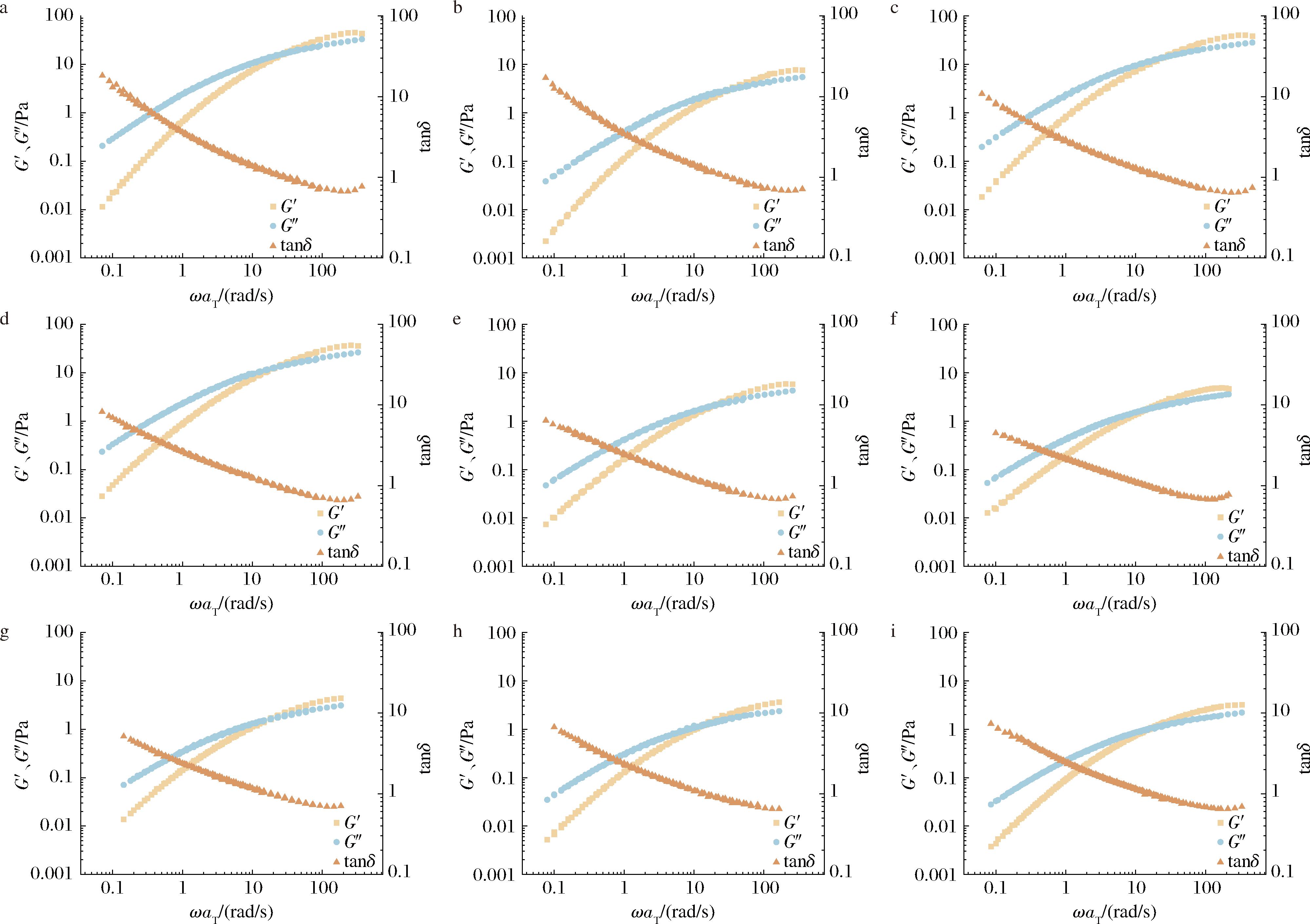
a-K1H9;b-K2H8;c-K3H7;d-K4H6;e-K5H5;f-K6H4;g-K7H3;h-K8H2;i-K9H1
图1 不同配比KGM-HA溶胶体系G′和G″对ω的依赖主曲线
Fig.1 The main curve of dependence of G′ and G″ on ω of KGM-HA sol system with different proportions
注:aT为水平偏移系数;c=10.0 kg/m3;Tr=40 ℃。
反映缠结特性的相关参数如表1所示,随着KGM比例增加,Me值出现波动变化,但整体呈现增加趋势。当KGM与HA的质量比为1∶9时,Me值最小为6.139×105 g/mol;当KGM与HA的质量比为9∶1 时,Me升高至最大8.203×106 g/mol,表明缠结点间的分子链段更长,ν值更低。出现这种波动变化可能与KGM和HA的分子间相互作用有关:随着HA比例的增加,KGM和HA之间的氢键相互作用使溶胶的网络结构更加稳定,这与之前WU等[15]的文献中报道的结果一致。他们通过FT-IR光谱观察发现,氧化透明质酸(oxidized hyaluronic acid, OHA)浓度不同的KGM/OHA水凝胶的光谱基本相似,但羟自由基(·OH)吸收峰(约3 406 cm-1附近)随OHA加入而发生移动,当OHA质量分数为0%、0.1%、0.3%、0.5%时,其峰位分别为3 396、3 406、3 420、3 404 cm-1。结果表明OHA质量分数从0%增加到0.3%,OH键拉伸使吸收峰位点逐渐向高波长偏移,这是由于KGM/OHA水凝胶间氢键相互作用随OHA含量增加而增强;而OHA质量分数为0.5%水凝胶的吸收峰位点与OHA质量分数为0.1%接近,表明OHA质量分数为0.5%时,该水凝胶的氢键相互作用减弱。羟基吸收峰位点逐渐向高波长偏移通常与氢键供体的电子云密度降低或氢键键长缩短有关,表明形成了更强的氢键作用。这种增强的氢键作用能够更有效地固定分子链,限制其运动,从而稳定网络结构。此外,本研究还发现当HA比例过高时,其可能会影响KGM的原始结构,使分子滑动,溶胶的网络结构强度减弱[22]。WU等[15]在研究魔芋葡甘露聚糖/氧化透明质酸水凝胶的构建过程中也发现在氧化透明质酸添加量较少的情况下,其对KGM水凝胶的主要作用是增强网络结构;而当氧化透明质酸的添加量超过了一定的限度,其会影响KGM水凝胶的原始结构,使分子滑动,导致水凝胶的黏度降低。此外,Z值在不同配比下也呈现波动变化。当KGM与HA的质量比为3∶7和 4∶6 时,Z值分别达到0.830和0.920,明显高于其他配比。这种差异可能与KGM和HA的分子链相互作用强度有关:在KGM和HA比例适中时,KGM和HA的相容性较好,分子链间形成的缠结点较多,导致Z值较高;而当HA或KGM占比过高时,分子链的竞争性聚集可能会抑制缠结,导致Z值降低[16]。a值随着HA比例增加整体呈现增大趋势。HA比例较高的溶胶体系对应的a值明显偏高,这可能与HA的分子特性有关,其长链结构和高分子质量导致缠结网络松散化,形成较大的网格[23];而KGM的短链或支链结构更易形成紧密的网格[11]。
表1 不同配比KGM-HA溶胶体系网络缠结参数
Table 1 Network entanglement parameters of KGM-HA sol systems with different ratios
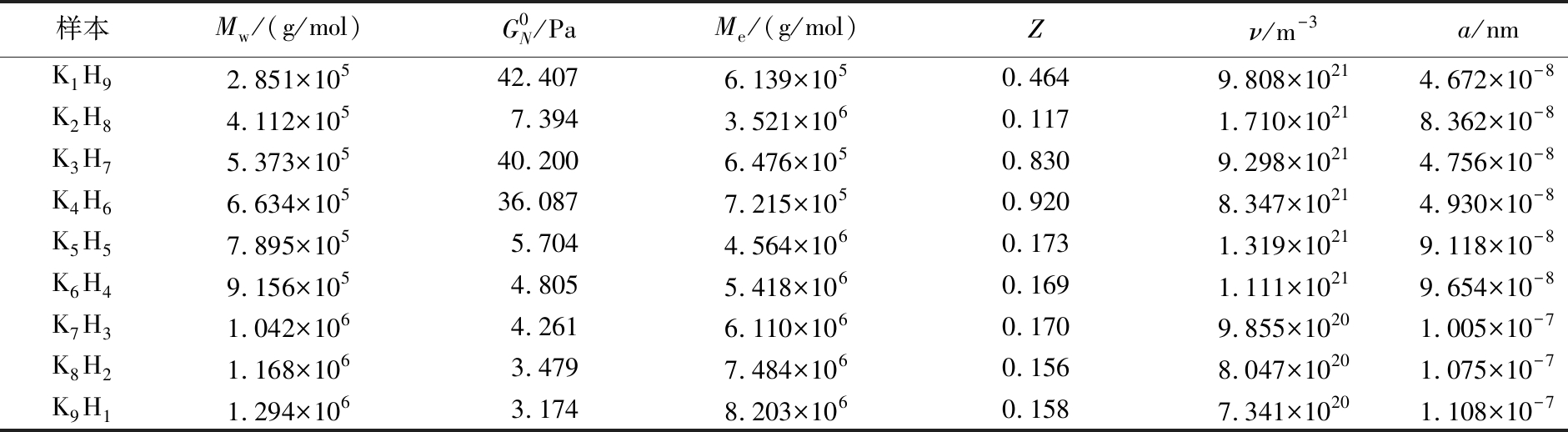
样本Mw/(g/mol)G0N/PaMe/(g/mol)Zν/m-3a/nmK1H92.851×10542.4076.139×1050.4649.808×10214.672×10-8K2H84.112×1057.3943.521×1060.1171.710×10218.362×10-8K3H75.373×10540.2006.476×1050.8309.298×10214.756×10-8K4H66.634×10536.0877.215×1050.9208.347×10214.930×10-8K5H57.895×1055.7044.564×1060.1731.319×10219.118×10-8K6H49.156×1054.8055.418×1060.1691.111×10219.654×10-8K7H31.042×1064.2616.110×1060.1709.855×10201.005×10-7K8H21.168×1063.4797.484×1060.1568.047×10201.075×10-7K9H11.294×1063.1748.203×1060.1587.341×10201.108×10-7
2.2 KGM-HA溶胶体系的流变特性
2.2.1 KGM-HA溶胶体系的频率扫描动态黏弹性
小振幅振荡剪切测试可以反映溶胶样品在频率变化下的动态黏弹性。动态黏弹性作为关键流变特性,既可衡量宏观力学性能,也能表征微观三维网络结构。G′与G″可以分别用来表示材料形变时的弹性大小与黏性大小。如图2所示,所有样品在角频率由0.1 rad/s增大到100 rad/s的过程中G″均高于G′,tanδ大于1,表现出类液体的性质,且随角频率的增大,tanδ趋向于1,样品的黏弹性上升。随着KGM比例的增加,KGM-HA溶胶体系的G′和G″均呈现出先增加后减小的趋势,出现这种情况与KGM和HA分子间氢键相互作用形成的网络结构的演变密切相关,在KGM与HA比例适中的范围内,氢键相互作用增强(表现为羟基吸收峰位点逐渐向高波长偏移),促进了更致密、稳定的分子间缠结网络的形成,从而显著提升了体系的G′和G″。而当KGM比例过高时,虽然氢键作用依然存在,但过量KGM可能会导致分子链竞争性聚集,抑制KGM与HA的缠结,使形成的网络结构强度减弱,宏观上表现为G′和G″的降低[22]。WANG等[24]在研究多糖对微凝胶颗粒重构大豆分离蛋白的影响中也发现HA可以通过静电相互作用、氢键和浓缩效应在增强凝胶性能方面表现出与蛋白质的协同作用。当KGM与HA的质量比为8∶2时,溶胶体系的G′值最大,表明KGM与HA在该质量比下弹性性能最强,说明KGM与HA在该质量比下分子间的网络交联程度增加。当KGM与HA的质量比为9∶1时,复配体系的G′值最小,表明KGM与HA在该质量比下弹性性能和结构强度减弱,进一步印证了前文纠缠特性中Me值较大的样品结构强度较弱,出现这种现象可能同样是由于KGM占比过高,分子链的竞争性聚集抑制缠结,而少量HA的添加影响了KGM的原始结构,使分子之间发生滑动,KGM与HA的交联程度下降而导致结构松散[15]。
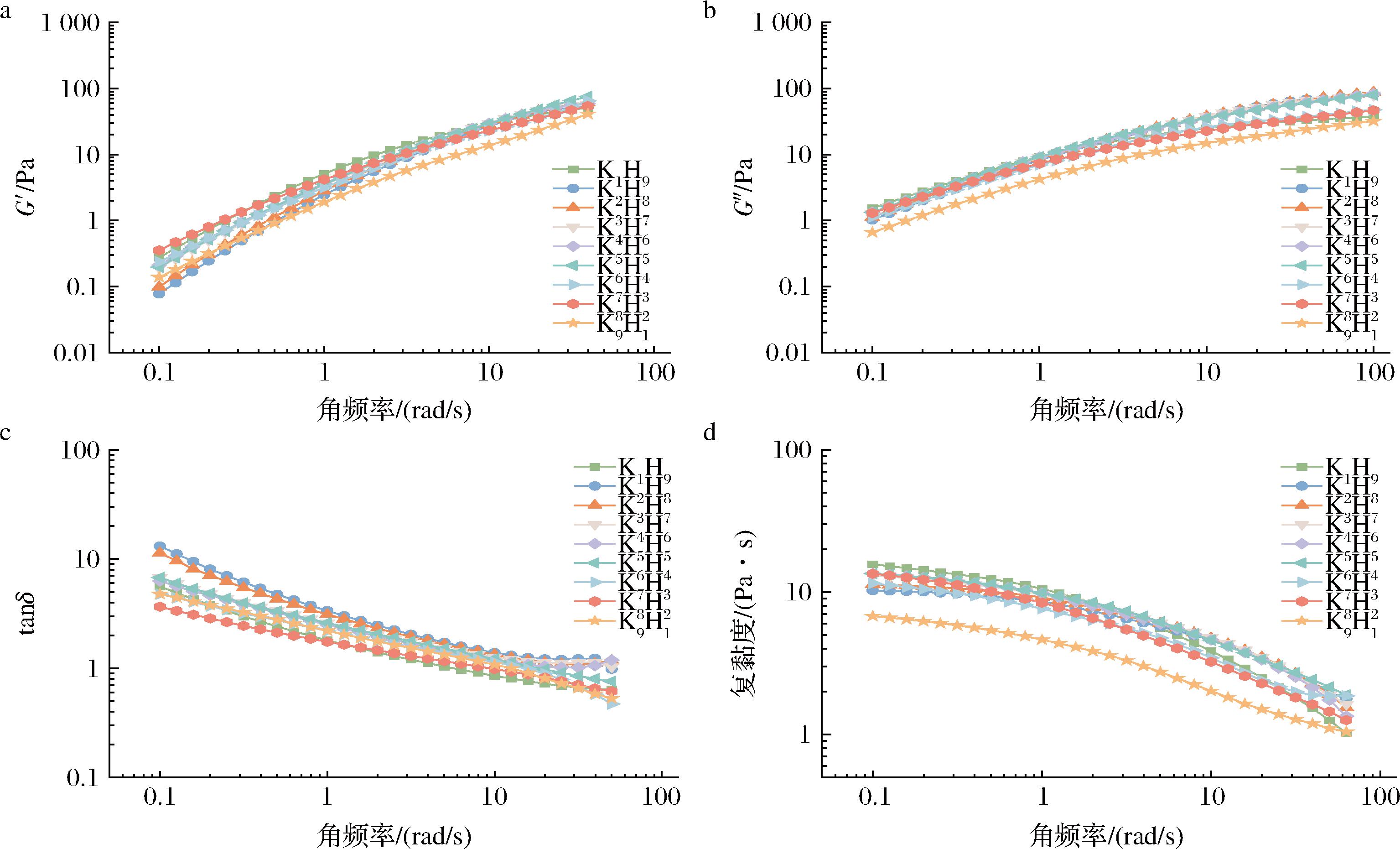
a-G′;b-G″;c-tanδ;d-复黏度
图2 不同配比KGM-HA溶胶体系的动态黏弹性
Fig.2 Dynamic viscoelasticity of KGM-HA sol systems with different proportions
2.2.2 KGM-HA溶胶体系的稳态扫描流动剪切黏度
图3展示了样品在稳态扫描流动剪切测试过程中的表观黏度变化。由图3可以看出,KGM-HA溶胶体系流动曲线在较低的剪切速率下呈现出明显的牛顿平台,而在较高的剪切速率下表现出剪切变稀的性质。KAYITMAZER等[25]在研究透明质酸/壳聚糖凝聚物的流变学和凝胶化过程中也发现透明质酸/壳聚糖凝聚物在高剪切速率下表现出显著的剪切稀化特性,表明其非常适合作为生物材料而进行应用。这种假塑性行为的产生是由于在较低剪切速率下,溶胶的三维网络结构没有被破坏,其黏度可以保持在较高的水平。然而,随着剪切速率的增加,分子链逐渐断裂,导致溶胶三维网络结构的破坏程度增加,溶胶的黏度降低[15]。比较不同质量比的KGM-HA溶胶体系,不难看出样品的整体黏度随着HA比例的增加而降低,表明提高HA的比例可以进一步降低溶胶的结构强度,增强其流动性。这与频率扫描测试中的结果趋势相同,可能同样是由于HA的添加可能影响了KGM的原始结构,使分子滑动[15]。为了进一步理解KGM-HA溶胶体系的黏度特征,对样品在流动剪切下的黏度变化行为进行拟合可以得到溶胶的零剪切黏度η0。在剪切速率变化范围足够大的情况下,可以观察到整个溶胶的双对数黏度曲线在中间及右侧区域呈现出线性变化。其曲线斜率与流体指数相关,本实验中所有样品在此区域内的黏度曲线斜率均小于零,意味着流体指数小于1,进一步印证了其剪切稀化特性。而在双对数图的左侧区域,曲线出现近乎平台的区间(曲线斜率趋近于0),表明此时流体指数接近1,溶胶样品展现出牛顿流体的黏度恒定性质,因此这个平台被称为牛顿平台[26]。
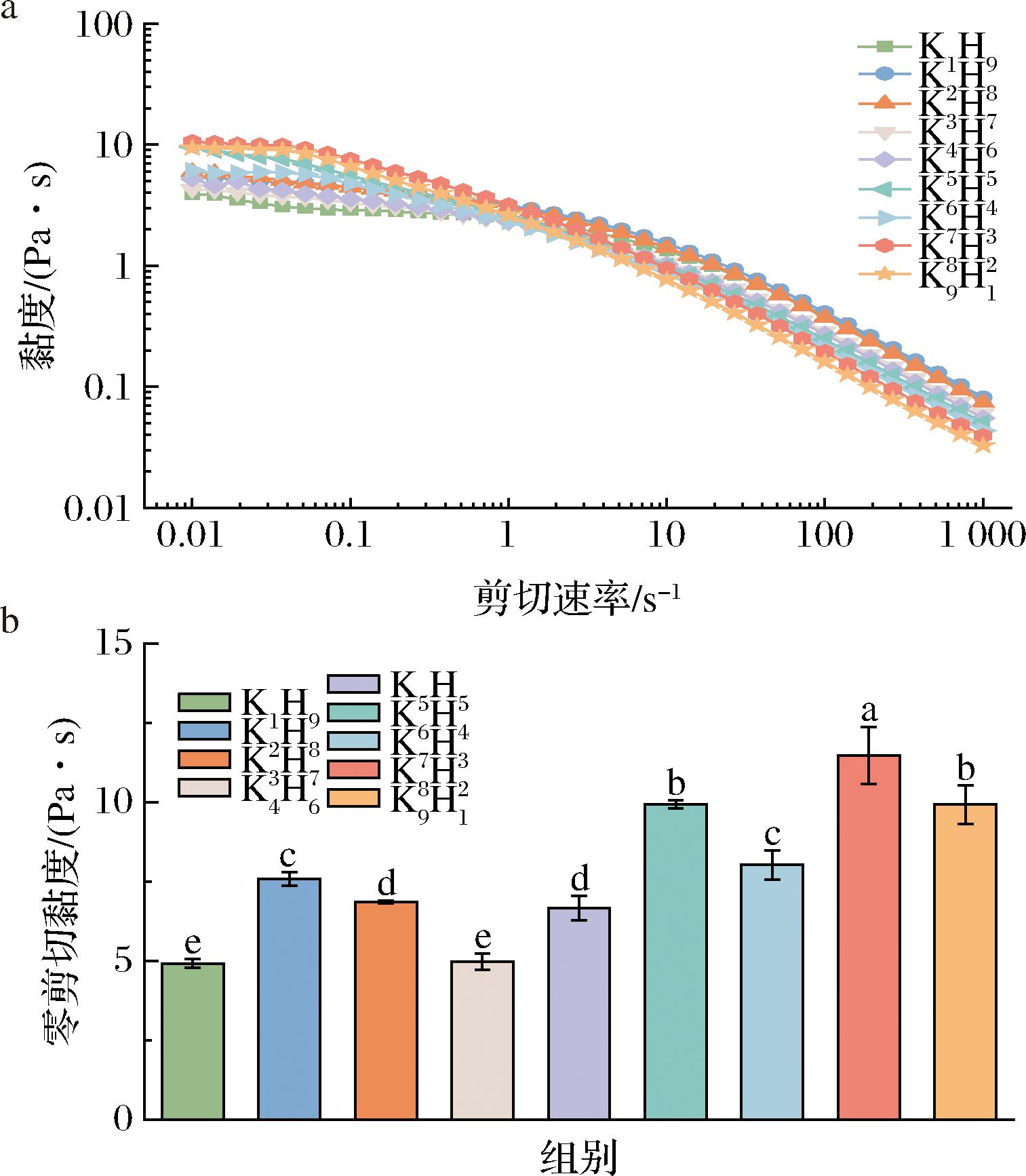
a-黏度曲线;b-零剪切黏度
图3 不同配比KGM-HA溶胶体系的流动剪切表观黏度
Fig.3 Flow shear apparent viscosity of KGM-HA sol system with different proportions
注:不同小写字母表示样品间差异显著(P<0.05)。
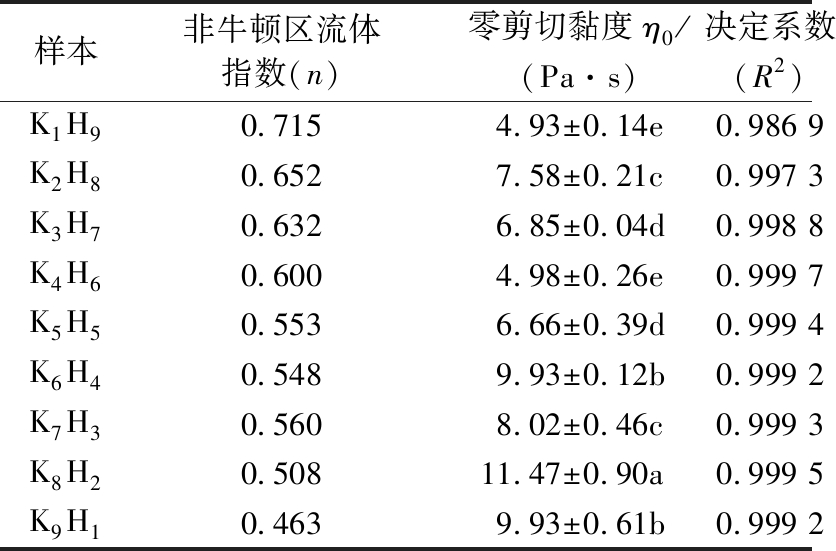
拟合得到的溶胶稳态流动参数如表2所示,随着KGM比例增加,KGM-HA溶胶体系表现出更高的η0,意味着KGM含量较高的样品在37 ℃下流动剪切时表现出更强的结构应力,而HA比例的增加能够降低KGM-HA溶胶体系的结构强度,从而减小其剪切应力。当KGM与HA的质量比为8∶2时,KGM-HA溶胶体系零剪切黏度最大,表明该配比下溶胶体系网络结构强度较高,这可能是因为KGM和HA之间的氢键相互作用增强了溶胶网络结构的稳定性[22]。此外,不同质量比的样品非牛顿区流体指数n也有所不同,KGM比例较高的样品表现出较低的n值。一般而言,非牛顿区的n值越远离1,则流体的非牛顿性越强,表明在流动剪切下样品内部的结构变化越大[27]。当KGM与HA的质量比为1∶9时,KGM-HA溶胶体系非牛顿区流体指数n最大,这表明该配比下的样品在非牛顿区的流动剪切下形变较大。
表2 不同配比KGM-HA溶胶体系的稳态流动参数
Table 2 Steady-state flow parameters of KGM-HA sol systems with different proportions
注:不同小写字母表示样品间差异显著(P<0.05)。
样本非牛顿区流体指数(n)零剪切黏度η0/(Pa·s)决定系数(R2)K1H90.7154.93±0.14e0.986 9K2H80.6527.58±0.21c0.997 3K3H70.6326.85±0.04d0.998 8K4H60.6004.98±0.26e0.999 7K5H50.5536.66±0.39d0.999 4K6H40.5489.93±0.12b0.999 2K7H30.5608.02±0.46c0.999 3K8H20.50811.47±0.90a0.999 5K9H10.4639.93±0.61b0.999 2
为了进一步定量描述和比较KGM-HA溶胶体系的剪切变稀性质,基于吞咽生理过程中的特征性剪切条件(约50 s-1),本研究选取剪切速率为10~100 s-1的流动曲线进行幂率拟合,得到相关参数。如表3所示,所有样品的幂律指数n均小于1,表明所有样品均具有剪切稀化的特性,这与前文结论一致。不同配比的KGM-HA溶胶体系具有不同的幂律指数,而幂律指数较低的增稠食物流体能为食用者带来更加愉悦的口感体验[27]。当KGM与HA的质量比为8∶2时,KGM-HA溶胶体系的n值最小,表明该配比下的KGM-HA溶胶体系具有更显著的剪切变稀效果,能为食用者带来更佳的口感体验。这进一步印证了KGM比例较高的样品的非牛顿性越强,在流动剪切下样品内部的结构变化越大。
表3 不同配比KGM-HA溶胶体系流动曲线的幂律方程拟合参数
Table 3 Power law equation fitting parameters of flow curves of KGM-HA sol system with different proportions
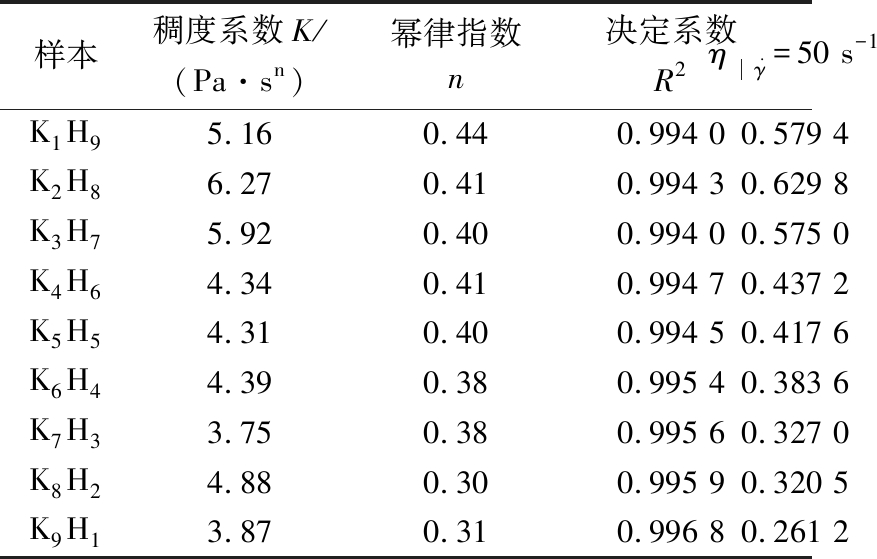
样本稠度系数K/(Pa·sn)幂律指数n决定系数R2 γ=50 s-1K1H95.160.440.994 00.579 4K2H86.270.410.994 30.629 8K3H75.920.400.994 00.575 0K4H64.340.410.994 70.437 2K5H54.310.400.994 50.417 6K6H44.390.380.995 40.383 6K7H33.750.380.995 60.327 0K8H24.880.300.995 90.320 5K9H13.870.310.996 80.261 2
2.2.3 KGM-HA溶胶体系的时间依赖性实验
用于吞咽困难治疗领域的流体食物增稠剂在保证增稠效果的同时,还应当具有稳定的黏度以满足患者对安全吞咽的需求[28]。因此探究增稠体系在动态剪切作用下的黏度时效特征尤为重要。本研究通过间歇施加恒定剪切速率的方式,监测黏度随剪切历史的变化规律,以此评估体系的触变特性[29]。如图4所示,在50、200 s-1 2种剪切速率条件下,样品依次经历5 min连续剪切、1 min静置及1 min再剪切过程。其中,50 s-1的剪切速率为吞咽生理过程中的特征性剪切条件;200 s-1的剪切速率代表高强度搅拌状态下流体所承受的剪切作用。通过上述测试方案,能够系统分析KGM-HA溶胶体系在不同的恒定剪切速率条件下黏度随时间的变化,并揭示配比差异对KGM-HA溶胶体系剪切敏感性的影响。由图4可知,对KGM-HA溶胶体系而言,表观黏度在二次剪切时与一次剪切后并无明显差异,且随着时间的延长,表观黏度也没有明显的改变,这表明依赖于剪切历史的动态微结构在溶胶体系中没有形成,其黏度不受剪切历史的影响,也没有明显的触变性。这说明了KGM-HA溶胶系统具有黏度稳定的特点,所以在其应用时能获得稳定的黏度以满足吞咽困难患者安全吞咽的需求。位元元等[30]在研究透明质酸流变学性质的过程中也发现HA增稠的营养制剂具有黏度稳定的特征,与本文研究结果一致。
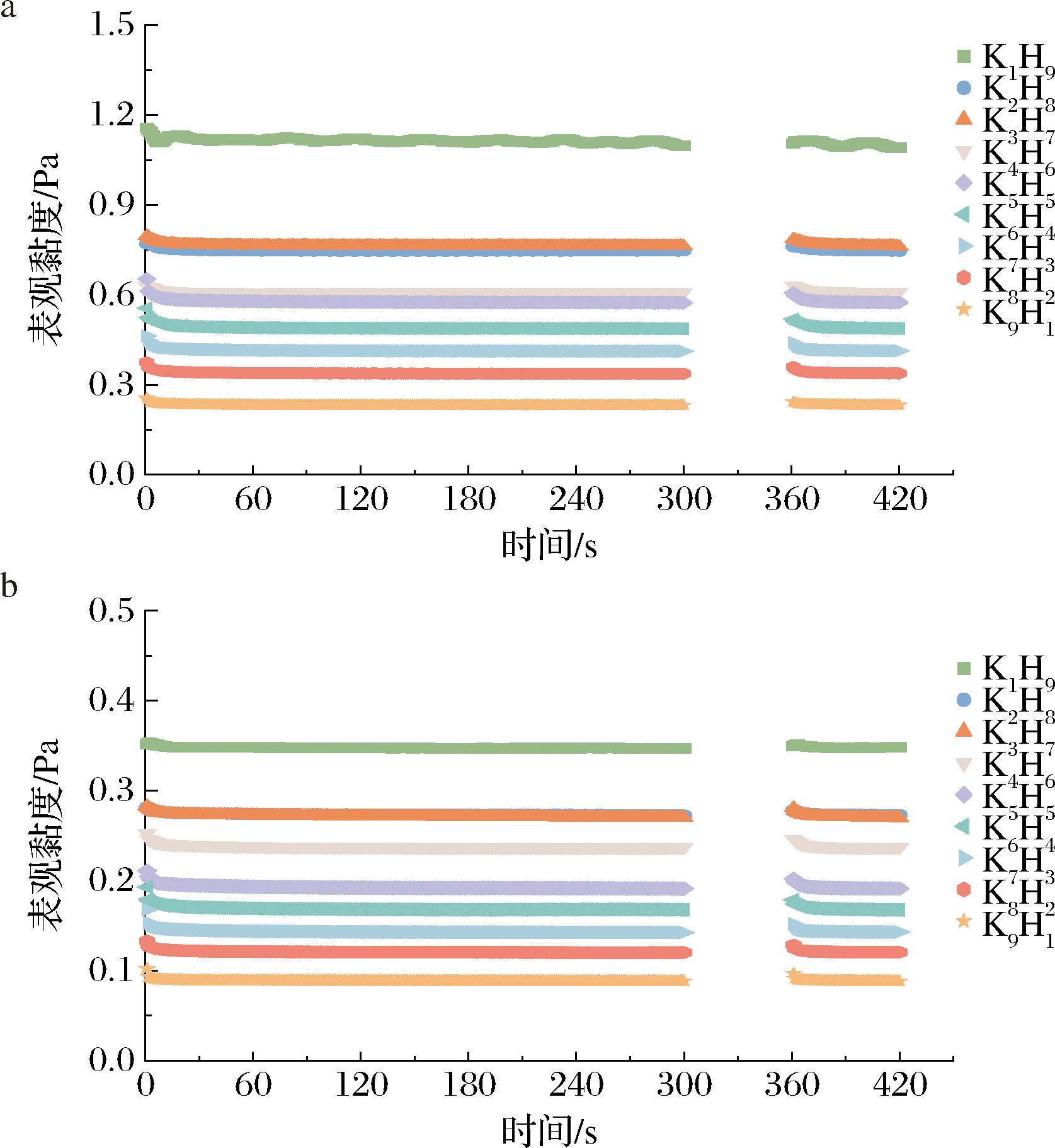
a-剪切速率50 s-1;b-剪切速率200 s-1
图4 不同配比KGM-HA溶胶体系在恒定剪切速率下表观粘度随时间的变化
Fig.4 Change of apparent viscosity with time of KGM-HA sol system with different ratio at constant shear rate
此外,通过综合分析剪切强度和剪切时间对KGM-HA溶胶体系黏度变化的影响,结合图4可以看出,KGM-HA溶胶体系在恒定剪切速率下,剪切时间的长短对其表观黏度影响较小。但不同的配比,高剪切速率相较于低剪切速率造成的表观黏度下降程度不同。如表4所示,当KGM和HA的质量比为1∶9时,表观黏度下降程度最大;当KGM和HA的质量比为4∶6时,表观黏度下降程度最小。因此,可以通过改变KGM和HA的比例来调节和控制黏度下降的程度,以满足不同的吞咽困难患者对黏度和口感的多方面需求。
表4 不同配比KGM-HA溶胶体系在恒定剪切速率下的表观黏度及变化
Table 4 The apparent viscosity of KGM-HA sol system with different ratio at constant shear rate and its change
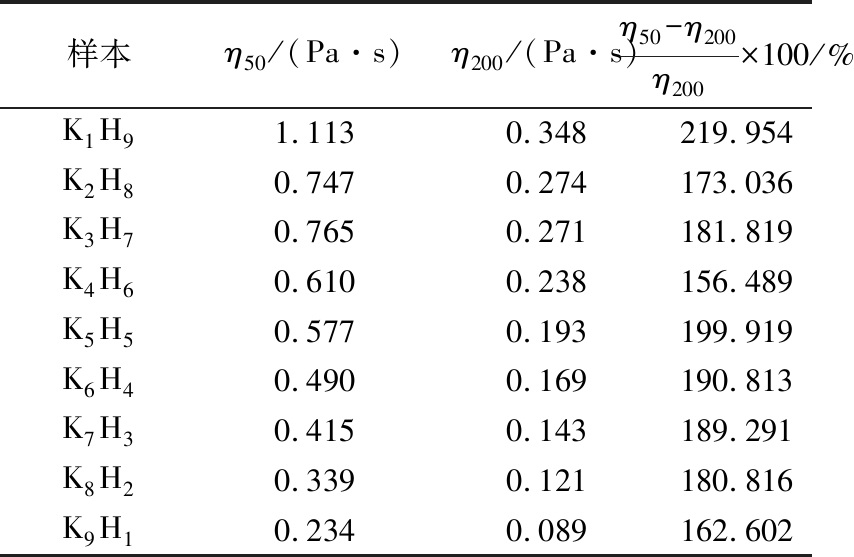
样本η50/(Pa·s)η200/(Pa·s)η50-η200η200×100/%K1H91.1130.348219.954K2H80.7470.274173.036K3H70.7650.271181.819K4H60.6100.238156.489K5H50.5770.193199.919K6H40.4900.169190.813K7H30.4150.143189.291K8H20.3390.121180.816K9H10.2340.089162.602
2.3 KGM-HA溶胶体系的IDDSI分级评价
根据国际吞咽障碍饮食标准化委员会制定的吞咽障碍食品分级标准[20],通过对KGM-HA溶胶体系进行系统性的汤匙倾斜测试得到图5所示实验结果,由图5可知所有样品在标准化测试条件下均展现出典型第3级流质食品的流动特性。当使用标准测试汤匙进行测试时,将盛有样品的汤匙以45°倾斜并保持10 s,观察到所有样品均呈现连续而稳定的滴状流动态势,且在倾斜过程中未见任何样品出现表面黏连或匙面残留现象,匙体表面仅形成完整液膜并迅速脱离,这一特性与IDDSI框架中第3级流质食品“中等稠度液体,可连续流动但不会快速流动”的定义高度吻合。第3级流质食品的黏稠度介于低稠与高稠之间,其流动性适中,且第3级流质食品质地均匀、无颗粒或团块,不会发生固液分离现象。这些特性减少了液体因流速过快导致的呛咳或误吸风险,降低了食物残渣掉入气道的风险,尤其适合咽部肌肉力量较弱或协调性差的患者[31]。KGM-HA溶胶体系IDDSI水平高,意味着其网络结构交联程度较好,这可能同样是由于KGM和HA之间的氢键相互作用使得多糖分子链相互缠结[15]。

图5 不同配比KGM-HA溶胶体系汤匙倾斜测试
Fig.5 Spoon tilt test of KGM-HA sol system with different ratio
3 结论
本研究以不同配比的KGM-HA溶胶体系为研究对象,系统探究了该体系的微观网络结构、流变学特性和吞咽安全性。结果表明,KGM和HA的比例过高都会导致溶胶体系网络结构松散;而中等质量比时,由于HA和KGM之间的氢键相互作用,溶胶体系的网络结构更加稳定。流变学测试发现,当KGM和HA的质量比为8∶2时,溶胶体系的储能模量最大,零剪切黏度最高,幂律指数最小,这表明其具有较好的弹性特性、更紧密的网络结构和更佳的口感体验,符合吞咽困难患者对食品增稠剂的要求。此外,KGM-HA溶胶体系在动态剪切下无明显触变性,黏度稳定性良好,表明其适用于长期吞咽护理。IDDSI分级评价测试表明所有配比的KGM-HA溶胶体系均符合第3级流质食品标准,具有适中的流动性和均匀的质地,可以降低误吸风险。因此,食品开发商可以通过调节KGM和HA的配比,精准调控KGM-HA溶胶体系的流变学特性和吞咽安全性,并根据不同吞咽困难患者的个性化需求,开发出不同类型的食品增稠剂。本研究为吞咽困难患者专用食品增稠剂的开发提供了理论依据,具有重要的社会价值与商业化潜力。
[1] WILKINSON J M, CODIPILLY D C, WILFAHRT R P.Dysphagia:Evaluation and collaborative management[J].American Family Physician, 2021, 103(2):97-106.
[2] CHU Y H, CHAO J C J.Effectiveness of diet modification on dietary nutrient intake, aspiration, and fluid intake for adults with dysphagia:A meta-analysis of randomized controlled trials[J].The Journal of Nutrition, Health And Aging, 2025, 29(4):100486.
[3] RODD B G, TAS A A, TAYLOR K D A.Dysphagia, texture modification, the elderly and micronutrient deficiency:A review[J].Critical Reviews in Food Science and Nutrition, 2022, 62(26):7354-7369.
[4] WANG K D, CHENG Z H, QIAO D L, et al.Polysaccharide-dextrin thickened fluids for individuals with dysphagia:Recent advances in flow behaviors and swallowing assessment methods[J].Critical Reviews in Food Science and Nutrition, 2025, 65(12):2236-2260.
[5] 冯晓瑜,叶慧玲,张咏军,等.脑卒中吞咽障碍病人精准摄食方案的构建及应用[J].循证护理,2025,11(8):1517-1522.FENG X Y, YE H L, ZHANG Y J, et al.Construction and application of precise feeding scheme for stroke patients with dysphagia[J].Chinese Evidence-Based Nursing, 2025, 11(8):1517-1522.
[6] YANG Y, XU J, SANG T T, et al.A review and evidence based recommendations on starch- and gum-based thickeners for dysphagic patients Proper thickeners for dysphagic patients[J].Journal of Food Measurement and Characterization, 2022, 16(4):3140-3152.
[7] MACKLEY M R, TOCK C, ANTHONY R, et al.The rheology and processing behavior of starch and gum-based dysphagia thickeners[J].Journal of Rheology, 2013, 57(6):1533-1553.
[8] WEI Y Y, GUO Y L, LI R Q, et al.Rheological characterization of polysaccharide thickeners oriented for dysphagia management:Carboxymethylated curdlan, konjac glucomannan and their mixtures compared to xanthan gum[J].Food Hydrocolloids, 2021, 110:106198.
[9] MORET-TATAY A, RODR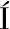 GUEZ-GARC
GUEZ-GARC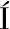 A J, MART
A J, MART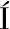 -BONMAT
-BONMAT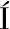 E, et al.Commercial thickeners used by patients with dysphagia:Rheological and structural behaviour in different food matrices[J].Food Hydrocolloids, 2015, 51:318-326.
E, et al.Commercial thickeners used by patients with dysphagia:Rheological and structural behaviour in different food matrices[J].Food Hydrocolloids, 2015, 51:318-326.
[10] WANG L, MU R J, LIN L Z, et al.Bioinspired aerogel based on konjac glucomannan and functionalized carbon nanotube for controlled drug release[J].International Journal of Biological Macromolecules, 2019, 133:693-701.
[11] SUN Y L, XU X W, ZHANG Q H, et al.Review of konjac glucomannan structure, properties, gelation mechanism, and application in medical biology[J].Polymers, 2023, 15(8):1852.
[12] CHEN W J, AN D, YE S X, et al.Interaction mechanism, fabrication strategies, and advanced applications of konjac glucomannan-based mixed polysaccharide systems[J].Food Chemistry, 2025, 468:142426.
[13] VALACHOV K, HASSAN M E,
K, HASSAN M E,  OLTÉS L.Hyaluronan:Sources, structure, features and applications[J].Molecules, 2024, 29(3):739.
OLTÉS L.Hyaluronan:Sources, structure, features and applications[J].Molecules, 2024, 29(3):739.
[14] DI MEO C, STELLAVATO A, D’AGOSTINO M, et al.Hyaluronan size and concentration:Effect on key biophysical and biochemical features[J].International Journal of Biological Macromolecules, 2024, 282:137125.
[15] WU H Y, BU N T, CHEN J, et al.Construction of konjac glucomannan/oxidized hyaluronic acid hydrogels for controlled drug release[J].Polymers, 2022, 14(5):927.
[16] HAO H Y, LI D.Facile fabrication of functional hyaluronic acid-/konjac glucomannan-based injectable hydrogel as wound closure and anti-microbial material for the treatment of burn wound healing[J].Journal of Materials Research, 2024, 39(16):2258-2271.
[17] HORINAKA J I, CHEN K, TAKIGAWA T.Entanglement properties of carboxymethyl cellulose and related polysaccharides[J].Rheologica Acta, 2018, 57(1):51-56.
[18] CARREAU P J.Rheological equations from molecular network theories[J].Transactions of the Society of Rheology, 1972, 16(1):99-127.
[19] YASUDA K, ARMSTRONG R C, COHEN R E.Shear flow properties of concentrated solutions of linear and star branched polystyrenes[J].Rheologica Acta, 1981, 20(2):163-178.
[20] CICHERO J A Y, LAM P T L, CHEN J S, et al.Release of updated international dysphagia diet standardisation initiative framework (IDDSI 2.0)[J].Journal of Texture Studies, 2020, 51(1):195-196.
[21] HORINAKA J I, YASUDA R, TAKIGAWA T.Entanglement properties of cellulose and amylose in an ionic liquid[J].Journal of Polymer Science Part B: Polymer Physics, 2011, 49(13):961-965.
[22] WANG N Z, HU J, ZHANG K D, et al.Development and characterization of a casein-hyaluronic acid emulsion gel with high water-holding capacity and excellent rheological properties for 3D printing[J].Food Hydrocolloids, 2023, 140:108632.
[23] BURDICK J A, PRESTWICH G D.Hyaluronic acid hydrogels for biomedical applications[J].Advanced Materials, 2011, 23(12):H41-H56.
[24] WANG Z X, LONG J, ZHANG C M, et al.Effect of polysaccharide on structures and gel properties of microgel particle reconstructed soybean protein isolate/polysaccharide complex emulsion gels as solid fat mimetic[J].Carbohydrate Polymers, 2025, 347:122759.
[25] KAYITMAZER A B, COMERT F, WINTER H H, et al.Rheology and gelation of hyaluronic acid/chitosan coacervates[J].Biomolecules, 2022, 12(12):1817.
[26] JIN L, SHANGGUAN Y G, YE T, et al.Shear induced self-thickening in chitosan-grafted polyacrylamide aqueous solution[J].Soft Matter, 2013, 9(6):1835-1843.
[27] BAYARRI S, TAYLOR A J, HORT J.The role of fat in flavor perception:Effect of partition and viscosity in model emulsions[J].Journal of Agricultural and Food Chemistry, 2006, 54(23):8862-8868.
[28] GARCIA J M, CHAMBERS E.Managing dysphagia through diet modifications[J].American Journal of Nursing, 2010, 110(11):26-33.
[29] DEWAR R J, JOYCE M J.The thixotropic and rheopectic behaviour of maize starch and maltodextrin thickeners used in dysphagia therapy[J].Carbohydrate Polymers, 2006, 65(3):296-305.
[30] 位元元,张洪斌,马爱勤,等.透明质酸多糖增稠适用于吞咽困难的肠内营养制剂及其流变学性质[J].食品科学,2019,40(1):50-55.WEI Y Y, ZHANG H B, MA A Q, et al.Rheological properties of hyaluronan thickened enteral nutritional preparations for dysphagia management[J].Food Science, 2019, 40(1):50-55.
[31] ONG J J, STEELE C M, DUIZER L M.Challenges to assumptions regarding oral shear rate during oral processing and swallowing based on sensory testing with thickened liquids[J].Food Hydrocolloids, 2018, 84:173-180.