番茄,又名西红柿,属于茄科番茄属,含有多种维生素和人体必备的矿物质。番茄既可作为水果直接食用,又可作为蔬菜煎炒蒸煮食用,还可经加工制成番茄蜜饯或番茄罐头等产品[1-3]。番茄罐头是一种较为普遍的番茄制品。影响番茄罐头品质的因素主要包含3方面:在番茄罐头生产工艺中,原料筛选、加工卫生及灭菌参数的协同控制构成产品质量保障的核心技术。原料筛选阶段需建立多级质控体系:初选时检测果实损伤度,选择合格的原料;若选择的原料已经受到微生物污染,甚至已经腐败变质,那么在产品杀菌前则可能已经出现气体堆积或具有恶臭味的现象,因此应选择无伤痕和未受到微生物污染的番茄果实进行加工,对于受到微生物污染的原料必须剔除[4-5]。加工卫生管理需执行卫生标准操作程序,仓储原料需及时完成分选,使用符合食品级卫生标准无菌水进行冲洗,以降低腐败微生物的初始载量[6]。针对灭菌工艺优化,需重点调控酸性环境与热处理的协同抑菌效应。研究表明,在酸性基质中,乳酸菌属及酵母菌仍能通过糖酵解途径代谢番茄红素等碳源,其代谢产生的乙酸、乳酸及CO2将导致番茄罐头腐败胀罐,因此,应选择合适的番茄罐头灭菌条件,以保证既不会破坏番茄本身的营养成分,又能降低番茄产品的微生物污染风险[7-10]。
由于番茄的罐藏食品pH<4.7,被称为酸性罐藏食品。通常情况下,对于酸性罐藏食品,产品中即使污染了产气荚膜梭菌、蜡样芽胞杆菌和致病性球菌等致病菌,这些菌株也无法在酸性条件下存活和生长;但腐败微生物则不然,其可在酸性环境下生存,酸性罐藏食品若受到腐败微生物污染,在一定条件下腐败微生物的存在有可能会引起罐头食品变质[11]。若酸性罐藏食品中混入了酵母菌或厌氧菌等腐败菌,既会大大增加罐藏食品腐败变质的风险[12]。国外有研究报道,桶装番茄制品中若混入了异型发酵乳酸菌,桶装浓缩番茄酱在贮藏过程中极有可能会利用产品进行发酵,同时产酸产气,损坏番茄酱的品质[13]。本研究采用多组学技术联用策略系统阐述番茄罐头生产链微生物风险:基于高通量测序平台,通过时间序列采样分析不同工艺节点(原料预处理→灌装→灭菌→贮藏)的细菌群落动态演替规律与功能菌群特征;同步实施培养组学方案,运用适宜培养基进行腐败菌的分离纯化,并采用分子生物学与基质辅助激光解析电离飞行时间质谱(matrix-assisted laser desorption/ionization time of flight mass spectrometry, MALDI-TOF MS)技术实现菌株精准鉴定。通过构建人工污染模型进行关键腐败细菌验证,建立腐败细菌的溯源分析流程。多维度研究框架可系统阐明加工链微生物污染路径,为建立定向抑菌策略提供理论依据。
1 材料与方法
1.1 材料与试剂
本研究所用材料与试剂如表1所示,其他试剂均为国产或进口分析纯。
表1 材料与试剂
Table 1 Materials and Reagents

胰蛋白胨大豆琼脂(tryptic soy agar,TSA)(g/L):胰蛋白胨15.0,大豆蛋白胨5.0,氯化钠5.0,琼脂15.0。
MRS琼脂培养基(g/L):蛋白胨10.0,牛肉浸粉8.0,酵母浸粉4.0,葡萄糖20.0,磷酸氢二钾2.0,柠檬酸氢二铵2.0,乙酸钠5.0,硫酸镁0.2,硫酸锰0.04,琼脂14.0,吐温80 1.0。
1.2 仪器与设备
本研究所用仪器与设备见表2。
表2 仪器与设备
Table 2 Instruments and Equipment
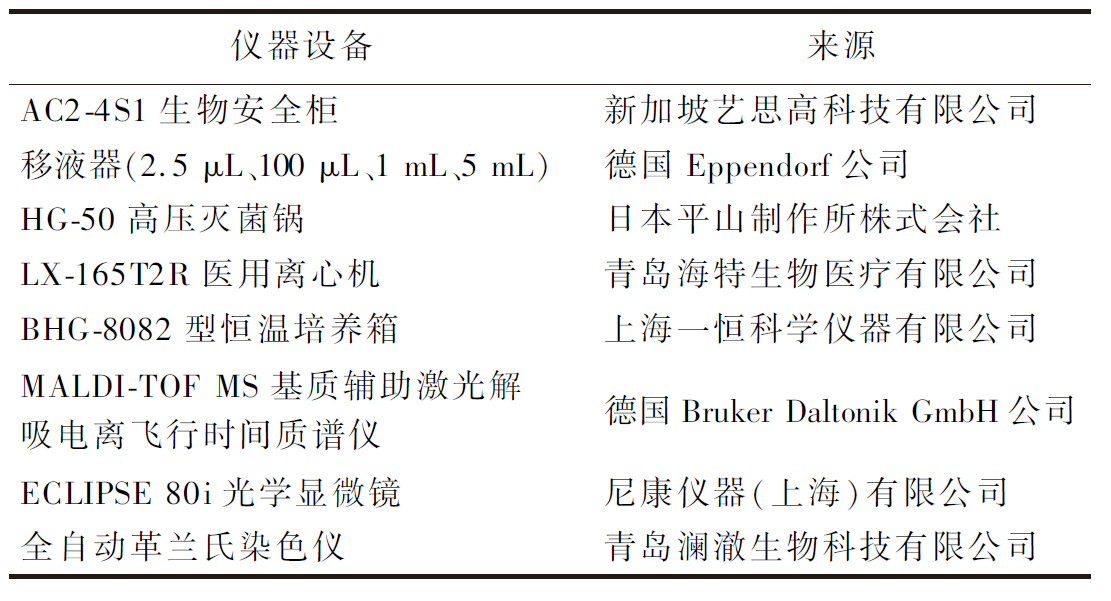
1.3 实验方法
1.3.1 样品采集
分别于7~9月对番茄罐头生产全流程(原料贮存、清洗、去蒂、烫皮、切丁、装罐、灭菌等环节)进行采样,采样后立即将棉拭子浸入无菌生理盐水中保存。9月设置热水清洗对照组;热水清洗后样品的采集方式为:使用 80 ℃热水对各环节传送带进行全面冲洗后立即采样。具体采样位点如表3所示。
表3 采样位点及缩写
Table 3 Sampling Sites and Abbreviations
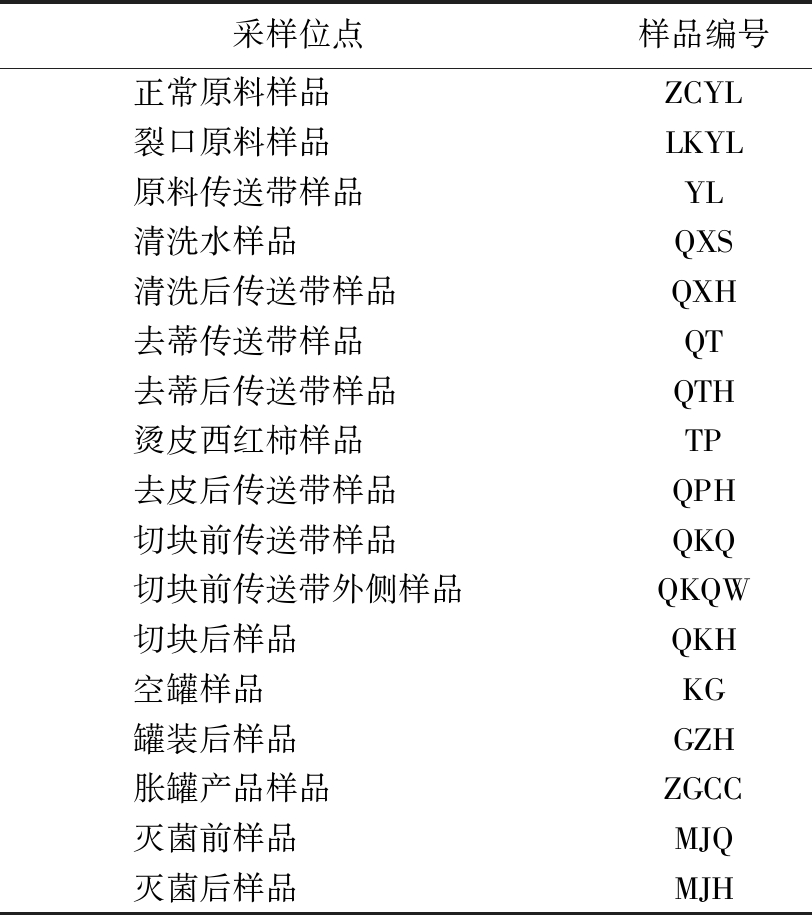
采样位点样品编号正常原料样品ZCYL裂口原料样品LKYL原料传送带样品YL清洗水样品QXS清洗后传送带样品QXH去蒂传送带样品QT去蒂后传送带样品QTH烫皮西红柿样品TP去皮后传送带样品QPH切块前传送带样品QKQ切块前传送带外侧样品QKQW切块后样品QKH空罐样品KG罐装后样品GZH胀罐产品样品ZGCC灭菌前样品MJQ灭菌后样品MJH
1.3.2 番茄罐头生产过程中细菌的分离与鉴定
采用梯度稀释法结合平板划线技术,使用 TSA 和 MRS 培养基进行菌株分离;利用MALDI-TOF MS的蛋白质指纹图谱分析,并结合16S rRNA基因全长测序及多位点序列分析,确定分离菌株的分类学地位。
1.3.2.1 细菌的分离纯化
将样品梯度稀释后,分别涂布于TSA和MRS培养基,30 ℃培养48~72 h,挑取形态差异菌落进行划线纯化,纯化菌株保存于-80 ℃甘油管[14]。
1.3.2.2 分离细菌的鉴定
通过MALDI-TOF MS获取菌株核糖体蛋白指纹图谱,结合数据库比对快速鉴定菌株。没有鉴定结果的菌株进一步扩增16S rRNA及持家基因pheS,经测序后比对NCBI数据库确认分类地位。
1.4 番茄罐头样品中的细菌群落结构分析
1.4.1 基因组DNA的提取、PCR扩增及测序
采用DNA提取试剂盒DNeasy PowerSoil Pro Kit(货号:47016,QIAGEN)提取样品的基因组DNA。取质控合格的基因组DNA各30 ng,使用16S rRNA基因通用引物338F和806R进行PCR扩增[15],PCR程序如下:95 ℃ 3 min;30个循环:95 ℃ 15 s,56 ℃ 15 s,72 ℃ 45 s;最后72 ℃ 延伸 5 min。终文库使用Agilent 2100 Bioanalyzer进行质控分析,质控合格后,利用MGISEQ-2000高通量测序平台进行测序。
1.4.2 数据分析
扩增子测序的数据分析流程主要包括原始数据质量控制、去除冗余序列、Tag拼接、操作分类单元(operational taxonomic units,OTU)分类、物种注释、Alpha多样性分析和Beta多样性分析等。利用fqcheck(v 0.25)软件[16]对下机数据进行质量控制,使用cutadapt (v 2.6)软件移除冗余序列、低质量reads和含N reads,得到高质量的Clean Data。使用FLASH(v1.2.11)软件[17]进行拼接,得到高变区的Tags。再利用USEARCH(v7.0.109 0)软件将已拼接好的Tags分类为OTU,从而获得每个样品的OTU丰度统计表。再通过 RDP classifer (v2.2)软件[18]将OTU代表序列和gold database数据库(v20 110 519)比对进行物种注释,设置置信度阈值为0.6,去除没有注释到的OTU以及注释结果明显不属于分析项目中的物种,并分别在界、门、纲、目、科、属和种的水平上统计分析各个样品中的细菌物种的组成。利用mothur(v.1.31.2)软件[19]进行样品Alpha多样性分析,主要包括Chao和Shannon指数,共同反映样品中菌落结构的丰富度和多样性。再用该软件分析各个物种在样品中的含量,从而计算出不同样品间的Beta 多样性值。最后选取丰度排名前10的细菌物种,通过R(v3.4.1)软件、Kruskal-Wallis(KW)和Wilcox检验分析方法分析该物种在各个分组中的平均相对丰度和差异显著性,探究不同样品中的关键细菌。
1.5 番茄罐头生产过程中优势细菌的溯源分析
1.5.1 优势细菌的菌株分型
为观察优势细菌菌株类型是否有差异,本研究采用随机扩增多态性DNA法(random amplified polymorphic DNA,RAPD)对生产过程中的优势细菌进行菌株分型。通过琼脂糖凝胶电泳中条带分散情况来反映基因组的多态性,进而实现优势菌株的分型。本研究从生产过程不同阶段样品中分离纯化得到的食物魏斯氏菌(Weissella cibaria)共17株,采用基因组DNA提取试剂盒DNeasy PowerSoil Pro Kit(货号:47016,QIAGEN)提取其基因组DNA,以引物M13(5′-GAGGGTGGCGGTTCT-3′)作为随机引物,以提取的基因组DNA作为模版进行PCR扩增。PCR扩增程序如下:94 ℃预变性5 min;94 ℃变性1 min,45 ℃退火20 s,72 ℃延伸2 min,共40个循环;72 ℃终延伸5 min。将扩增产物使用1.0%琼脂糖凝胶进行电泳检测,根据待检菌株凝胶电泳结果的条带数量、大小和位置来判断其RAPD分型图谱是否一致,从而实现菌株分型。
1.5.2 优势细菌的回接实验
选取不同采样周期得到的3株食物魏斯氏菌分别进行回接实验,观察菌株在番茄产品中的产酸产气能力。将冻存菌株接种于 5 mL MRS 液体培养基,30 ℃振荡培养至 OD600 值达 0.5,按2%接种量转接至 50 g 新鲜去皮番茄组织,密封于广口瓶中,30 ℃静置培养。分别于培养24、48和72 h后记录产气现象,并测定样品pH 值变化。
1.6 优势细菌的生产控制
基于微生物群落分析、菌株溯源及优势细菌的回接实验等结果进行综合分析,确定优势腐败菌主要来源于番茄原料和去蒂后的产品中。为提升番茄产品的合格率,本研究对番茄罐头生产工艺进行优化改良,具体控制方法为:采用80 ℃热水对原料处理至装罐前的全流程传送带进行全面冲洗,清洗后立即进行微生物采样。参照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》标准测定清洗前后各关键位点的菌落总数,通过lg值变化评估改良后的生产工艺对优势细菌去除效果。
2 结果与分析
2.1 番茄罐头生产过程中的细菌群落结构分析
对采集的不同时间和不同生产阶段的番茄罐头样品通过 MGISEQ-2000测序平台进行16S rRNA扩增子测序,系统阐明番茄罐头在生产过程中的细菌群落动态演变规律及物种差异。测序结果表明,在采集的50个样品中共获得3 886 160条Tags,单样品的Tags为76 749~78 842。50 个样品共获得19 756 OTUs,单个样品的OTUs数目为63~987。
2.1.1 番茄罐头生产过程中细菌的组成和丰度分析
基于跨生产周期的纵向研究设计,本研究对番茄罐头生产体系内4个不同时期样本进行微生物组多维度解析。采用V3~V4高变区通用引物338F/806R[扩增子长度(467±21) bp]进行16S rRNA基因靶向测序。该区段在属级分类分辨率达92.7%,显著优于种级分类效能,故选择属水平作为核心分析单元。样品的微生物组特征解析结果表明(图1),7月中原料处理环节呈现明显的高丰度特征菌属聚集现象,鉴定出6个丰度高于10%的优势菌属,包括明串珠菌属(Leuconostoc)、魏斯氏菌属(Weissella)、近魏斯氏菌属(Periweissella)、乳球菌属(Lactococcus)、泛菌属(Pantoea)和气单胞菌属(Aeromonas)。从整体上看,不同工艺节点样本菌群结构呈现明显差异,同时相邻位点间也表现出一定的相似性,其中灭菌后(MJQ_7)、灭菌前(MJH_7)、正常原料(ZCYL_7)和去蒂后传送带(QTH_7)的样品中明串珠菌属的丰度分别达到97%、96%、80%、34%;罐装后(GZH_7)、切块后(QKH_7)和去蒂传送带(QT_7)的样品以魏斯氏菌属为主,丰度分别为82%、72%、34%,而其丰度超过1%的有12个采样点,占比高达80%;近魏斯氏菌属是裂口原料(LKYL_7)和烫皮西红柿(TP_7)中的主要菌属,丰度分别为80%和22%;切块前传送带(QKQ_7)中乳球菌属是主要细菌,其丰度达到46%;泛菌属和气单胞菌属分别是去皮后传送带和清洗水样品中的特异性优势菌属,丰度分别为40%和28%,详细结果见图1-a。
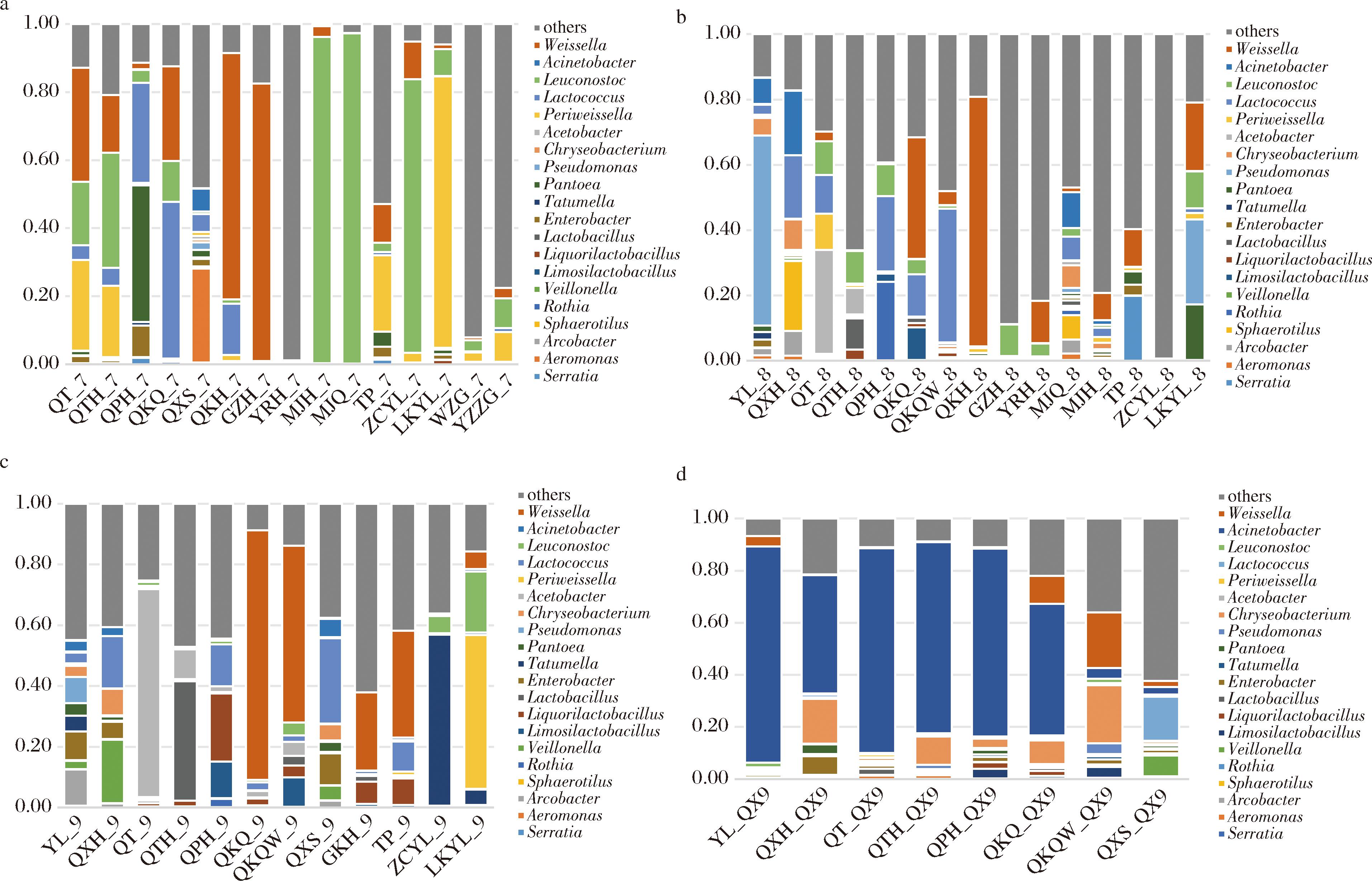
a-7月份样品;b-8月份样品;c-9月份样品;d-9月份清洗后样品
图1 番茄罐头不同时间和工艺样品中的细菌种类和丰度
Fig.1 Bacterial species and abundance in canned tomato samples at different times and processes
番茄罐头生产体系在时序性推进过程中呈现出微生物群落重构特征。随着环境温度上升及生物膜负载量累积,核心菌属有所不同,其中最大的变化就是明串珠菌属丰度明显下降,仅在裂口原料(LKYL_8)、去蒂传送带(QT_8)、去蒂后传送带(QTH_8)、去皮后传送带(QPH_8)和罐装后产品(GZH_8)样品中丰度达到10%~11%,而魏斯氏菌属逐渐成为各环节中优势细菌菌属,其丰度超过1%的有10个采样点,占比为67%,其中丰度超过10%的样品包括切块后产品(QKH_8)、切块前传送带(QKQ_8)、去蒂后传送带(QTH_8)、裂口原料(LKYL_8)、罐装预热后产品(YRH_8)、烫皮西红柿(TP_8)、灭菌后产品(MJH_8)、切块前传送带外侧(QKQW_8)、去蒂传送带产品(QT_8)和去皮后传送带产品(QPH_8),其中切块后产品(QKH_8)中的明串珠菌属菌株的占比最高,达到76%。8月份样品中出现了不同于7月份样品的优势菌属,假单胞菌属主要存在于原料传送带(YL_8)和裂口原料样品(LKYL_8),其丰度分别为58%和26%;乳球菌属、醋杆菌属(Acetobacter)、罗斯氏菌属(Rothia)、球衣菌属(Sphaerotilus)、沙雷氏菌属(Serratia)、不动杆菌属(Acinetobacter)分别是切块前传送带外侧(QKQW_8)、去蒂传送带(QT_8)、去皮后传送带(QPH_8)、清洗后传送带(QXH_8)和烫皮西红柿(TP_8)产品中的优势细菌。详细结果见图1-b。8月样品的动态演变规律在9月样品中仍有体现,魏斯氏菌属仍然是各环节的优势细菌菌属,有6个采样点的丰度大于1%,占比达到50%,有4个样品丰度大于10%,切块前传送带(QKQ_9)、切块前传送带外侧(QKQW_9)、烫皮西红柿(TP_9)和切块后产品(QKH_9)分别为82%、58%、35%、26%;此外,塔特姆氏菌属(Tatumella)被认为是9月份样品的特异性富集菌属,分布与7~8月有明显区别,其在正常原料(ZCYL_9)样品中的丰度为56%。详细结果见图1-c。
为阻断微生物沿生产链的持续累积,本研究在9月生产周期后段实施靶向热干预清洗方案:采用80 ℃ 热水对原料预处理至切丁装罐前全段传送带系统进行深度消毒,并于处理后完成采样。结果表明,清洗工艺使优势菌属更为明显,主要为不动杆菌属、魏斯氏菌属和金黄杆菌属(Chryseobacterium),分别分布在原料传送带-清洗后(YL_QX9)、切块前传送带外侧-清洗后(QKQW_QX9)和清洗水-清洗后(QXS_QX9),丰度在17%~83%。魏斯氏菌属菌种仍然属于优势细菌,其中,采样的5个样品中丰度均超过了1%,占比63%,其中清洗后的切块前传送带外侧-清洗后(QKQW_QX9)样品中魏斯氏菌属菌种丰度最高,达到21%;不动杆菌属菌种在清洗后的原料传送带-清洗后(YL_QX9)、去蒂传送带-清洗(QT_QX9)、去蒂后传送带-清洗(QTH_QX9)、去皮后传送带-清洗后(QPH_QX9)、切块前传送带-清洗后(QKQ_QX9)和清洗后传送带-清洗后(QXH_QX9)样品中的占比超过10%,丰度分别为83%、79%、73%、72%、51%、45%。此外,清洗后的切块前传送带外侧-清洗后(QKQW_QX9)、清洗后传送带-清洗后(QXH_QX9)和去蒂后传送带-清洗(QTH_QX9)样品中金黄杆菌属菌种为优势细菌,丰度分别为22%、17%、11%。详细结果见图1-d。
2.1.2 番茄罐头生产过程中细菌多样性研究
基于mothur(v.1.31.2)流程的多样性分析表明,番茄罐头生产时序样本以及优化后样本的微生物群落呈现显著动态演变特征。通过Chao指数(物种丰富度)与Shannon指数(多样性及均匀度)双维度评估发现,全周期样本Chao指数值域为113.14~1 178.69(图2-a),该指数越大表明丰富度越高,其中7月样本波动最小,提示初始工艺阶段群落结构稳定性较高,而9月非清洗样本呈现较大波动,表明污染菌随时间推移而积累。Shannon指数值域为0.14~4.49(图2-b),该指数越大表明物种多样性越高,分布越均匀,整体呈显著上升趋势,7月样本波动最大,8月样本中位数最高,且离散度最低,表明8月环境促进多菌属稳态共生,9月清洗后样本离散度较9月非清洗样本有明显下降,证实工艺优化对有害菌的选择性抑制。
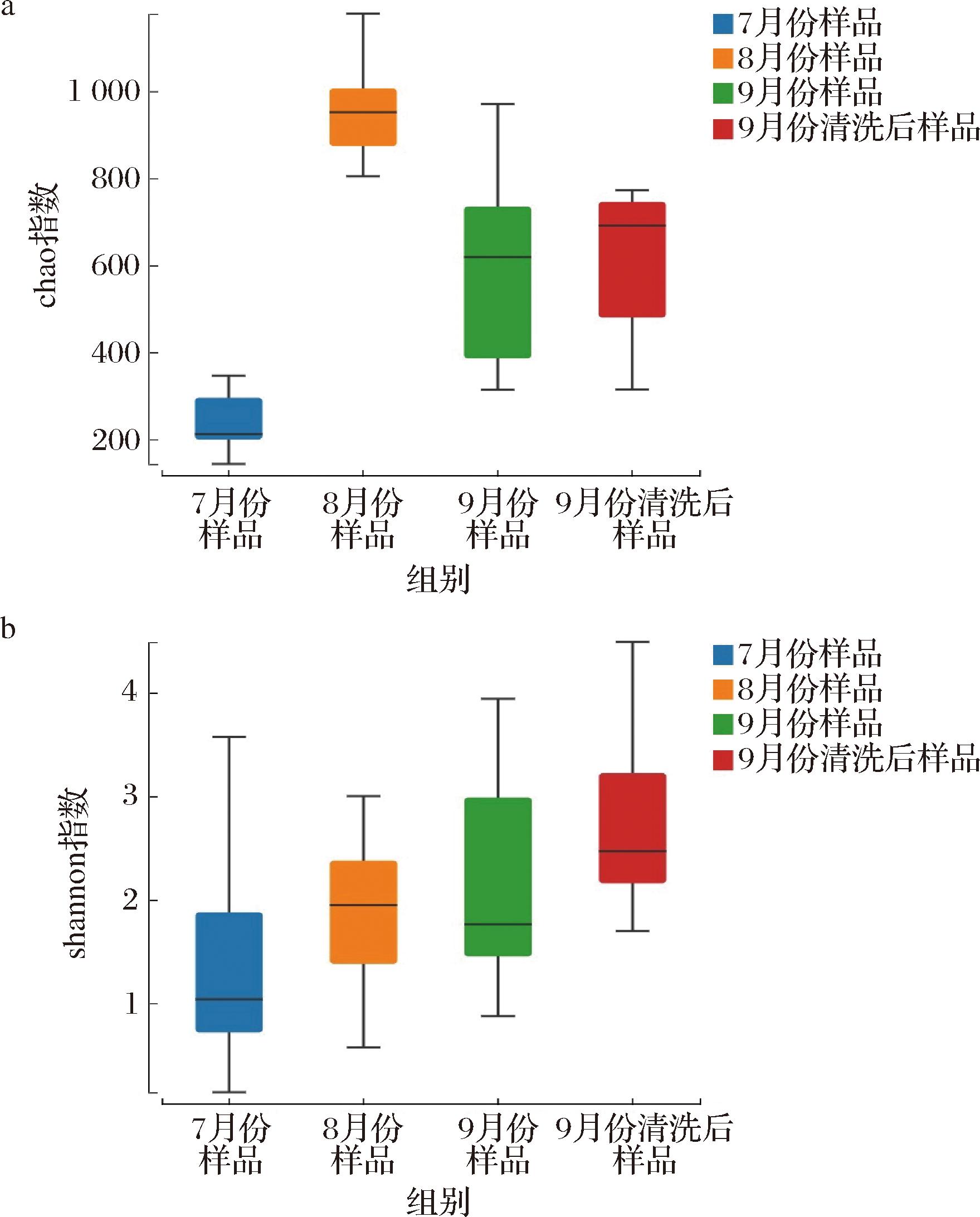
a-Chao指数;b-Shannon指数
图2 番茄罐头不同时间和工艺样品中的细菌多样性比较
Fig.2 Comparison of bacterial diversity in canned tomato samples at different times and processes
2.1.3 番茄罐头生产过程中的关键细菌分析
基于差异丰度特征菌筛选策略,通过R(v3.4.1)软件对番茄罐头全流程菌群进行多组学整合分析,分析结果显示,不动杆菌属、明串珠菌属、金黄杆菌属、醋杆菌属和假单胞菌属是不同时间样品中具有显著差异的关键细菌微生物。而魏斯氏菌属是贯穿7、8、9月份乃至9月份清洗后样品中的关键细菌,特别是在7、8、9月份样品中相对丰度均较高且较为稳定;7月样本中明串珠菌属、近魏斯氏菌属以及芽胞杆菌属(Bacillus)丰度显著高于其他阶段;而不动杆菌属为9月份清洗后样品的富集细菌(图3-a)。
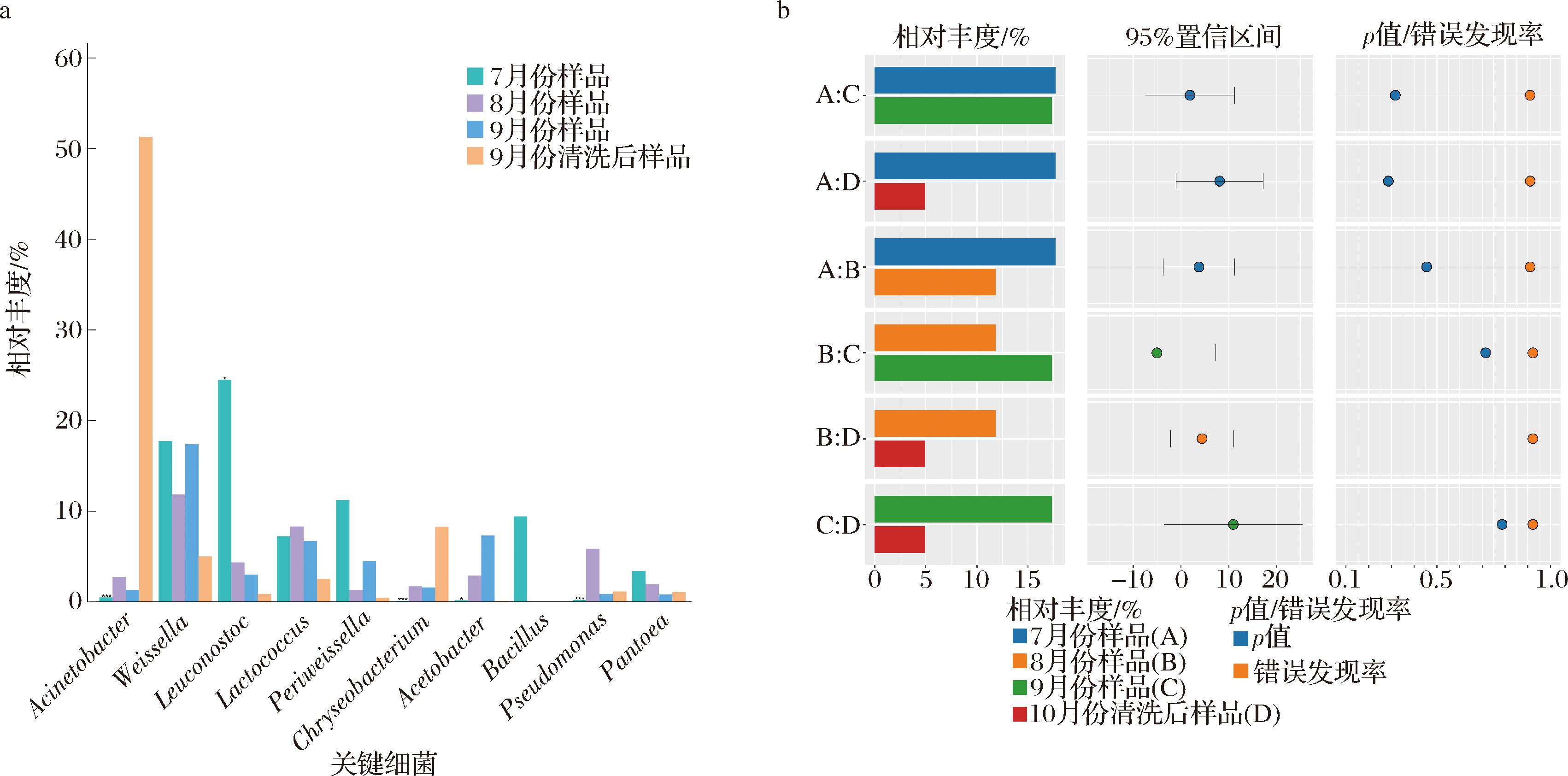
a-关键细菌分析;b-魏斯氏菌属分析
图3 番茄罐头样品中丰度前10的关键细菌及魏斯氏菌属差异分析
Fig.3 Analysis of the top 10 most abundant key bacteria in canned tomato samples and differential analysis of Weissellla
注:*表示即7月份样品与8月份样品、7月份样品与9月份样品、7月份样品与9月份清洗后样品两两相比的显著性差异; *代表P<0.05,**代表P<0.01,***代表P<0.001。
本研究进一步探究了魏斯氏菌属在不同时间和生产工艺样品中的分布情况,如图3-b所示,7、8、9月份样品中的魏斯氏菌属的平均相对丰度均显著高于9月份清洗后样品。其中,7月份、9月份样品中的魏斯氏菌属平均相对丰度最高,占比分别为27.7%和26.3%;8月份样品中魏斯氏菌属的占比为20.7%,均显著高于9月份清洗后样品5%。
上述分析结果表明,随着番茄罐头生产持续进行,优势细菌魏斯氏菌属菌株一直存在于整个生产过程中,这与番茄罐头容易出现的胀罐现象是息息相关的;从9月份清洗后样品中魏斯氏菌属平均相对丰度占比可看出,在进行工艺优化后,增加80 ℃热水清洗的工序能够在很大程度上降低魏斯氏菌属的平均相对丰度。
2.2 番茄罐头的生产过程中细菌分离结果
本研究通过分离纯化获得150株细菌纯培养物,经16S rRNA基因序列分析结合系统发育树构建,共鉴定出51个分类学属(电子版增强出版附表1,https://doi.org/10.13995/j.cnki.11-1802/ts.041980),主要包括魏斯氏菌属、芽胞杆菌属、不动杆菌属、明串珠菌属、肠杆菌属(Enterobacter)和泛菌属等。从分离的种属来看,在不同生产阶段的样品中共分离得到19株魏斯氏菌属,占总分离细菌的12.7%,其中有17株经鉴定确认为食物魏斯氏菌,占整个属的89.5%,在采集的裂口原料样品、原料传送带样品、清洗后传送带样品、去蒂传送带样品、去蒂后传送带样品、去皮后传送带样品、切块前传送带样品、切块前传送带外侧样品、清洗水样品、切丁传送带样品、灌装后产品样品、切块后样品和胀罐产品等采集的样品中均分离鉴定出食物魏斯氏菌,几乎贯穿整个生产工艺流程,因此推测食物魏斯氏菌是导致番茄罐头胀罐变质的潜在优势腐败细菌,这也和16S rRNA扩增子测序分析的结果是一致的。此外,芽胞杆菌属和不动杆菌属检出率相对较高,占比分别为8.7%和5.3%,其中芽胞杆菌属主要分布于裂口原料样品、原料传送带样品、去蒂传送带样品、烫皮西红柿样品、灭菌前产品和胀罐产品等5个阶段样品中,芽胞杆菌属分布较为广泛可能和其是环境中常见的细菌有关,并且部分芽胞可产生孢子,一般的杀菌工艺不能完全将其去除;不动杆菌属主要存在于裂口原料、原料传送带和去蒂传送带等西红柿烫皮前的采样位点,西红柿烫皮后几乎没有检出,推测对西红柿进行烫皮时可能将不动杆菌杀死或使其从生产设备上冲落。
从整体上看,原料传送带分离得到的细菌微生物种类较多,共有12种,主要包括魏斯氏菌属和芽胞杆菌属,推测原料传送带作为番茄原料直接接触的第一道工艺程序,此时未经过任何清洗处理,每个经过该程序的番茄原料表面所携带的细菌可能脱落在原料传送带上,导致该采样位点的细菌微生物种类较多;然而,在去皮后传送带和切块前传送带等产品灭菌前采样位点的样品分离到细菌微生物种类较少,主要包括魏斯氏菌属和沙雷氏菌属。推测该采样位点在经过番茄烫皮处理工艺后,原本附着在番茄表面和传送带上的细菌被热水冲走或者杀死,微量残留的细菌微生物还未来得及进行大量繁殖,从而造成这2个采样位点所分离的微生物种类较少。
比较优化工艺流程前后可发现,清洗后可分离的细菌种类和总数均大幅度降低,同位点较清洗前共分离得到72株细菌,涵盖34个属,主要集中在魏斯氏菌属、沙雷氏菌属和肠杆菌属,主要分布在与番茄原料直接接触的各个位点传送带等位置;热水清洗后样品共分离得到18株细菌,涵盖12个属,其中丰度较高的是魏斯氏菌属,主要分布在去蒂传送带样品、切块前传送带样品、清洗后传送带等样品中。
2.3 番茄罐头生产过程中的优势细菌的溯源分析结果
结合扩增子测序分析结果和分离鉴定结果发现,食物魏斯氏菌是番茄罐头不同生产时间和不同生产过程中的稳定优势细菌,几乎在所有生产工艺中均有该菌种检出,并且随着番茄罐头的持续生产其丰度也在逐渐增加。由于食物魏斯氏菌是一种常见的具有耐酸特性的细菌,在发酵时能产酸和产气,可引起罐装产品胀罐腐败,推测该菌种是引起番茄罐头胀罐和腐败变质的潜在优势细菌。
2.3.1 食物魏斯氏菌的菌株分型结果
将上述分离的17株食物魏斯氏菌为模版,通过预实验将M13作为RAPD随机引物进行扩增来进行食物魏斯氏菌的分型溯源。琼脂糖凝胶电泳的检测结果表明(图4),分离得到的17株食物魏斯氏菌可分为4种株型,株型1包括YL-M4、QT-1M1、TP-M3、QKQ-6M1、GZH-8M2、QKQ-QX-6T1、QKQW-QX-M4和ZGCC-M1,该株型分离菌株数量最多,几乎贯穿整个生产工艺,并且在胀罐产品中也分离出该株型;株型2包括LKYL-19M3和QTH-M1,该株型分离数量最少;株型3包括QTH-M1、QKQW-M1、QKH-6M-1和QT-QX-M3,清洗后的样品中也有该株型食物魏斯氏菌检出;株型4包括QXS-M2、QXH-M2和QPH-M1;由于株型1几乎贯穿整个生产工艺,并且该株型食物魏斯氏菌分离数量最多,因此,推测食物魏斯氏菌株型1是引起番茄罐头胀罐和腐败变质的关键细菌。
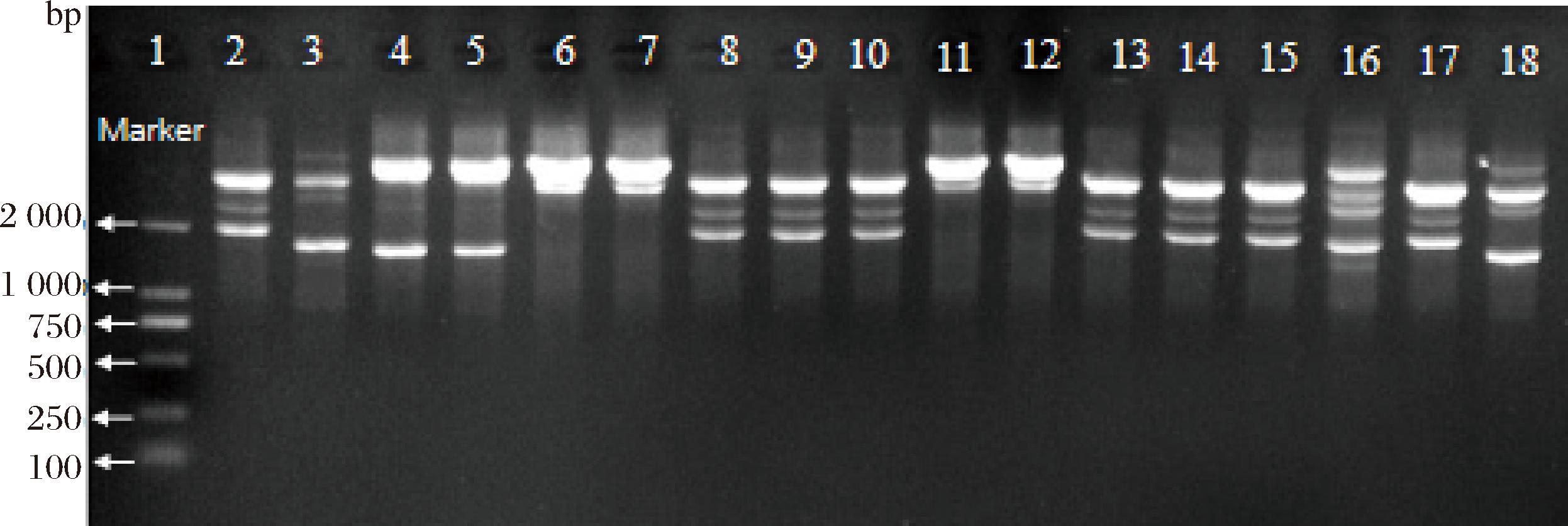
1-Marker;2-YL-M4;3-LKYL-19M3;4-QXS-M2;5-QXH-M2;6-QTH-M1;7-QKH-6M-1;8-QT-1M1;9-TP-M3;10-QKQ-6M1;11-QKQW-M1; 12-QT-QX-M3;13-QKQ-QX-6T1;14- QKQW-QX-M4;15-GZH-8M2;16-QKH-M9;17-ZGCC-M1;18-QPH-M1。
图4 17 株食物魏斯氏菌RAPD分型结果
Fig.4 RAPD results of 17 W.cibaria
2.3.2 食物魏斯氏菌回接实验结果
选取3株分离自番茄罐头关键工艺节点的食物魏斯氏菌构建人工污染模型。实验组采用直接接种法模拟原位腐败过程,对照组注入等体积无菌生理盐水。通过动态监测番茄基质中pH值变化及产气情况,验证回接菌株是否是引起样品腐败变质和胀罐腐败菌。
结果如图5所示,接种食物魏斯氏菌的番茄样品培养24 h后开始出现产气现象,并且pH值平均下降0.4,其中样品2下降幅度最大,pH值下降了0.5;培养48 h后接种食物魏斯氏菌样品产气最多,在广口瓶中明显观察到有较多的气泡,但该阶段产酸情况不太明显,pH值仅下降了0.1;在培养72 h后虽然产气能力有所下降,但是仍然能明显观察到有较小的气泡存在,但该阶段的pH值未下降,与培养48 h时结果一致;而空白对照组一直未观察到产气泡的产生,且pH值始终保持不变,这表明食物魏斯氏菌能够利用番茄中的营养物质进行代谢产生气体和少量酸,是造成番茄罐头腐败变质和胀气的优势细菌。

a-培养24 h;b-培养48 h;c-培养72 h
图5 食物魏斯氏菌回接实验结果
Fig.5 Reinoculation experiment results of W.cibaria
3 讨论与结论
基于番茄罐头生产流程时序性样本的细菌群落动态分析表明,物种丰度最高出现在8月份,而7月份最低。核心菌群的多样性随工艺流程,呈现梯度富集特征。在7月样本中检测到6个优势菌属(相对丰度>10%),其中魏斯氏菌属最高丰度可达82%。在7、8、9月份3阶段中,菌群多样性指数随环境等因素发生波动。值得注意的是,魏斯氏菌属在动态演替过程中展现出显著生态位保守性,始终为不同时间和阶段样品中的优势菌属。魏斯氏菌属在7~9月生产周期内呈现持续性定植特征:其相对丰度大于1%的样本占比分别为80%、67%、50%,证实该菌属为跨工序的核心腐败功能菌群,是导致罐头胀罐及风味劣变的关键驱动因子。基于全流程分离培养策略也证明这一点,在番茄罐头生产体系内共鉴定出51个菌属,其中食物魏斯氏菌呈现显著空间优势,共有17株分离株,占全部分离株的12.7%,并且在生产阶段中的裂口原料、原料传送带、清洗水、灌装后产品和胀罐产品等不同的生产阶段中均能分离出该物种,进一步证明了食物魏斯氏菌是导致番茄罐头腐败变质和胀罐的潜在的优势细菌。食物魏斯氏菌属于魏斯氏菌属,而魏斯氏菌属是乳酸菌科下的一个分支。常分离自分布于新鲜蔬菜、发酵制品、奶酪、青贮饲料和土壤中,由于其发酵过程中会产生葡萄糖、杂多糖、其他低聚糖等物质,并具有产细菌素能力和抗真菌性,被广泛应用于工农业、畜牧业、发酵食品和医药等领域[20-22]。此外,食物魏斯氏菌还具有降胆固醇、抗肿瘤和抗过敏等免疫调节功能[14]。当该菌存在于泡菜等腌制菜时,部分菌株具有良好的产酸、耐盐以及降解亚硝酸盐的能力,并且从泡菜中分离出的部分食物魏斯氏菌还具有良好的清除自由基功能,在延缓衰老方面起到积极作用,但其产品的脆性不良以及涩味较浓,造成泡菜口感不尽人意[23]。但若低温肉制品中含有食物魏斯氏菌,那么该菌便可通过发酵产生乳酸、乙酸、乙醇等,导致产品产生刺鼻酸味,并且由于其具有耐酸、耐盐、发酵产生有机酸、细菌素的特点,可在贮藏过程中有效抑制其他微生物的生长并大量繁殖,从而成为低温肉制品中的优势腐败细菌[24]。食物魏斯氏菌在糖代谢过程中可产生乳酸、乙酸和二氧化碳,是典型的异型发酵乳酸菌,当该菌存在于番茄罐头或水果罐头时,可通过发酵产二氧化碳造成产品胀罐甚至爆裂[25],这与本研究结果相对应。通过构建食物魏斯氏菌人工回接模型,系统解析其致腐动力学特征,实验组接种菌悬液后,代谢动态监测显示:1 d后检测到气泡和少量酸,2 d后检测到大量气泡的少量酸,3 d后仍能观察到气泡但pH值未发生改变;并且在接种2 d后的产气量达到峰值,这表明食物魏斯氏菌的存在确实是会导致番茄罐头腐败变质和胀罐。结合本研究的RAPD分型结果表明,分离的17株食物魏斯氏菌可分为4种株型,其中分离菌株中属于株型1的数量最多,广泛分布于生产过程中的原料传送带、去蒂传送带、烫皮西红柿、切块前传送带、切块前传送带外侧和胀罐样品等采样阶段,贯穿整个生产工序,这表明造成番茄罐头腐败变质和胀气的优势细菌在生产阶段中广泛存在,极大增加了番茄罐头腐败的风险。
对番茄罐头不同时间和不同生产阶段样品的细菌群落结构和关键物种差异进行综合分析,结合优势细菌的分离筛选及鉴定情况、回接验证以及RAPD分型结果分析,不仅表明食物魏斯氏菌是引起番茄罐头腐败变质和胀气的关键细菌,而且发现优势细菌主要来源于番茄原料和清洗去皮后的产品中,随着生产进行而逐步积累,在切块前传送带及传送带外侧、切块后产品和灌装后产品中丰度尤为明显。为提升番茄罐头货架稳定性,针对加工链微生物污染关键点,本研究通过强化生产环节微生物控制策略,对现有工艺进行系统性改进。建立了80 ℃热水清洗体系,采用分段式清洁方案对原料预处理至装罐前各环节传送带实施连续性冲洗。实验数据显示(表4),清洁前各关键节点微生物污染水平为3.1×106~4.3×108 CFU/mL,表明原料处理过程存在显著微生物累积现象;实施热水清洁后,对应位置样品菌落总数均呈现不同程度下降,清洁后污染水平控制在7~3×105 CFU/mL。其中原料传送带清洁前后菌落数降幅达7.1 lg CFU/mL,切块前传送带外侧降幅最低为2.2 lg CFU/mL。数据对比分析表明,该清洁工艺对生产流程中优势菌群的增殖具有显著抑制作用,可有效提升番茄罐头产品的微生物安全性,为工业化生产提供可靠的工艺优化方案。
表4 清洗前后细菌菌落总数
Table 4 Total colony count before and after cleaning
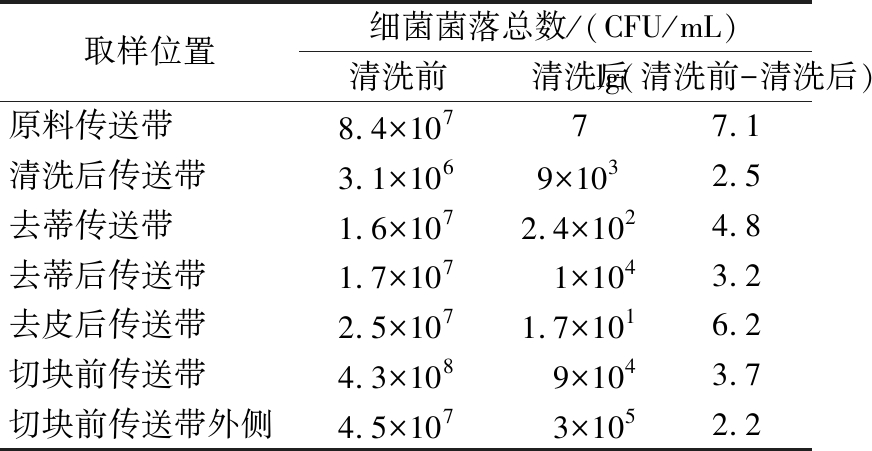
取样位置细菌菌落总数/(CFU/mL)清洗前清洗后lg(清洗前-清洗后)原料传送带8.4×10777.1清洗后传送带3.1×1069×1032.5去蒂传送带1.6×1072.4×1024.8去蒂后传送带1.7×107 1×1043.2去皮后传送带2.5×1071.7×1016.2 切块前传送带4.3×108 9×1043.7 切块前传送带外侧4.5×107 3×1052.2
为系统提升新疆番茄罐头产品品质,本研究聚焦生产过程微生物控制关键环节,构建了基于多组学技术的微生物溯源分析体系。首先通过扩增子测序技术解析全生产流程微生物群落演替规律,结合纯培养分离技术系统开展微生物分离培养,成功分离出优势腐败菌;通过回接验证实验与RAPD分子分型技术,明确魏斯氏菌为贯穿原料处理至装罐工序的关键优势腐败菌,对番茄罐头生产阶段中优势微生物的溯源建立了一套全面的分析策略。基于微生物溯源结果,本研究实施工艺优化,增加热水清洗工序,优化后各工序微生物污染水平较优化前下降趋势明显。本研究首次揭示魏斯氏菌在番茄罐头生产中的持续性污染特征,建立的多维度微生物控制技术体系,为解决同类加工食品微生物污染问题提供了创新方案,为工业化生产提供理论支撑。
[1] MATEVOSYAN L G, HARUTYUNYAN S S, GALSTYAN M H, et al.Balance and coefficients of usage of nitrogen, phosphorus and potassium from the soil and fertilizers by tomatoes and peppers in the conditions of Ararat Plain of Armenia[J].Agronomy Research, 2024, 22(1).
[2] ALANCAY M M, LOBO M O, SAMMAN N C.Physicochemical and structural characterization of whey protein concentrate-tomato pectin conjugates[J].Journal of the Science of Food and Agriculture, 2023, 103(11):5242-5252.
[3] 李静, 马自强, 柴岳, 等.新疆特色番茄制品深加工工艺技术研究[J].现代食品, 2023, 29(20):124-126.LI J, MA Z Q, CHAI Y, et al.Research on deep processing technology of Xinjiang characteristic tomato products[J].Modern Food, 2023, 29(20):124-126.
[4] 程明才. 水果类罐头在生产中产品质量控制措施探讨[J].食品安全导刊, 2015(6):59-61.CHENG M C.Discussion on product quality control measures of canned fruits in production[J].China Food Safety Magazine, 2015(6):59-61.
[5] 侯慧波, 张春玲, 蒋永衡.新疆番茄酱的加工工艺及品质控制[J].农产品加工(学刊), 2010(11):55-57.HOU H B, ZHANG C L, JIANG Y H.Processing technology and quality control of tomato paste in Xinjiang[J].Academic Periodical of Farm Products Processing, 2010(11):55-57.
[6] 王帅.新疆加工番茄生长及加工过程污染霉菌的分类与鉴定[D].乌鲁木齐:新疆农业大学, 2011.WANG S.Processing tomato growth and processing of classification and identification of mold[D].Urumqi:Xinjiang Agricultural University, 2011.
[7] 朱建飞,王琳琳.食品加工与保藏原理[M].北京:化学工业出版社:2023-10-01.ZHU J F, WANG L L.Principles of Food Processing and Preservation[M].Beijing:Chemical Industry Press, 2023-10-01.
[8] 马自强,柴娟,王陈强,等.3 kg番茄丁罐头食品杀菌工艺改进及品质分析[J].食品工程, 2024(2):30-33.MA Z Q, CHAI J, WANG C Q, et al.Sterilization process improvement and quality analysis of 3 kg canned tomato diced food [J].Food Engineering, 2024(2):30-33.
[9] 范力艺, 范群艳, 林佳馨, 等.燕窝罐头原料及生产中嗜热微生物分析[J].食品与生物技术学报, 2023, 42(11):88-97.FAN L Y, FAN Q Y, LIN J X, et al.Analysis of thermophilic microorganisms in canned bird’s nest production[J].Journal of Food Science and Biotechnology, 2023, 42(11):88-97.
[10] 李涛, 彭芳刚, 舒楠, 等.果汁型黄桃罐头感官与营养品质研究[J].中国食品学报, 2024, 24(2):160-168.LI T, PENG F G, SHU N, et al.Studies on sensory and nutritional quality of juice-type canned yellow peach[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(2):160-168.
[11] 刘欢. 食品变质微生物及其检测方法研究综述[J]. 工业微生物, 2024, 54(4):40-42.LIU H. A review of research on food spoilage microorganisms and their detection methods[J]. Industrial Microbiology, 2024, 54(4):40-42.
[12] 胡习祯, 杨玉新.微波杀菌技术在番茄制品中的应用[J].农产品加工, 2015(5):40-42.HU X Z, YANG Y X.The application of microwave sterilization in tomato products[J].Farm Products Processing, 2015(5):40-42
[13] BJORKROTH K J, KORKEALA H J. Lactobacillus fructivorans spoilage of tomato ketchup[J]. Journal of Food Protection, 1997, 60(5):505-509.
[14] 张健, 陈国辉, 高逸, 等. 番茄罐头生产过程中腐败真菌的溯源分析[J]. 食品与发酵工业, 2025, 51(17):184-194.ZHANG J, CHEN G H, GAO Y, et al. Traceability analysis of spoilage fungi in production process of tomato cans[J]. Food and Fermentation Industries, 2025, 51(17):184-194.
[15] 杨雨鑫, 朱基, 黄圣南, 等.海南红心火龙果根际微生物群落的季节性特征研究[J].热带作物学报, 2024, 45(12):2659-2669. YANG Y X, ZHU J, HUANG S N, et al.Seasonal characteristics of rhizosphere microbial communities in red pitaya in Hainan[J].Chinese Journal of Tropical Crops, 2024, 45(12):2659-2669.
[16] DROOP A P.Fqtools:An efficient software suite for modern FASTQ file manipulation[J].Bioinformatics.2016, 32(12):1883-1884.
[17] ![]() T, SALZBERG S L.FLASH:Fast length adjustment of short reads to improve genome assemblies[J].Bioinformatics, 2011, 27(21):2957-2963.
T, SALZBERG S L.FLASH:Fast length adjustment of short reads to improve genome assemblies[J].Bioinformatics, 2011, 27(21):2957-2963.
[18] EDGAR R C, HAAS B J, CLEMENTE J C, et al.UCHIME improves sensitivity and speed of Chimera detection[J].Bioinformatics, 2011, 27(16):2194-2200.
[19] SCHLOSS P D, WESTCOTT S L, RYABIN T, et al.Introducing mothur:Open-source, platform-independent, community-supported software for describing and comparing microbial communities[J].Applied and Environmental Microbiology, 2009, 75(23):7537-7541.
[20] 文宇萍, 金清.饲料提取物对食窦魏斯氏菌耐酸性的影响[J].延边大学农学学报, 2023, 45(3):45-50.WEN Y P, JIN Q.Effect of feed extract on acid resistance of Weissella cibaria[J].Agricultural Science Journal of Yanbian University, 2023, 45(3):45-50.
[21] 白霞, 崔梦含, 朱鹏程, 等.3株魏斯氏菌的分离鉴定与生物学特性研究[J].食品安全质量检测学报, 2023, 14(9):59-69.BAI X, CUI M H, ZHU P C, et al.Isolation, identification and biological characteristics of 3 strains of Weissella[J].Journal of Food Safety &Quality, 2023, 14(9):59-69.
[22] KLEPPEN H P, HOLO H, JEON S R, et al. Novel Podoviridae family bacteriophage infecting Weissella cibaria isolated from Kimchi[J]. Applied and Environmental Microbiology, 2012, 78(20):7299-7308.
[23] 张桂英, 李会霞, 姜龙波, 等.发芽-发酵联合处理对谷子淀粉结构和理化性质的影响[J].食品工业科技, 2024, 45(22):89-96.ZHANG G Y, LI H X, JIANG L B, et al.Effect of combined germination-fermentation treatment on the structure and physicochemical properties of foxtail millet starch[J].Science and Technology of Food Industry, 2024, 45(22):89-96.
[24] 刘长蕾, 文宇萍, 李冠洋, 等.魏斯氏菌的研究进展[J].食品与机械, 2022, 38(9):227-233.LIU C L, WEN Y P, LI G Y, et al.Recent progress of Weissella[J].Food &Machinery, 2022, 38(9):227-233.
[25] 文宇萍. 耐酸性食窦魏斯氏菌的诱变选育及特性研究[D].延吉:延边大学, 2020.WEN Y P.Mutation breeding and characteristic study of acid resistant Weissella cibaria[D].Yanji:Yanbian University, 2020.