常言道,“曲乃酒之骨”,“有美酒必备佳曲”。作为白酒生产中被广泛应用的糖化发酵剂和生香剂,酒曲含微生物和酶类,可直接影响白酒的产量和质量。尤其在酱香型白酒酿造过程中,酒曲与高粱总体比例可达1∶1,高温大曲不仅发挥糖化、发酵和生香的作用,也作为酿酒原料参与微生物代谢[1]。粉碎小麦混合母曲和水后被压制成曲坯,曲坯在曲房严格的保温保湿环境进行微生物网罗和发酵,最高培曲温度在60 ℃以上,发酵结束后再贮存3个月以上便得到可用于酿酒的高温大曲[2]。
在传统的高温大曲生产技艺中,常采用人工踩曲成型和“横三竖三”堆放培曲,此方法用人成本高且极度依靠工人经验,占地面积广且无法精准控制环境条件,最终导致大曲质量难以把控[3]。随着科技进步和工厂智能化的推进,在制曲板块,已经有浓香型白酒企业采用仿生压曲、仿生安曲和微机控制架式发酵等技术推动中温大曲自动化生产[4]。而高温大曲较难实现从粉碎、安曲、培曲等全步骤仿生化,原因之一是曲房堆积发酵过程中的温度和湿度较难调控[5]。传统高温大曲堆积发酵过程中必须保证较高的制曲温度和适宜的湿度以驯化芽孢杆菌等耐高温微生物。稻草由于疏松多孔的内部结构和独特的表面纤维具有较好的保温保湿性能,在传统工艺中常被用于覆盖曲坯保温保湿并隔离大曲防止黏连[5]。在探索仿生高温大曲生产的进程中,暂时没有合适的稻草替代材料。因此,寻找一种既能高效替代稻草保温保湿功能,又能适应仿生高温大曲生产需求的材料,显得尤为迫切。
本研究采用不同材料对仿生工艺高温大曲的发酵过程进行保温保湿,基于大曲的理化指标、特征风味物质和微生物群落结构对大曲发酵过程进行对比分析,旨在探究不同保温保湿材料对大曲发酵过程及成品质量的影响,以期为仿生高温大曲的保温保湿调控提供思路。本研究对于改进制曲工艺并推动高温大曲仿生化发展具有实际生产指导意义。
1 材料与方法
1.1 材料与试剂
高温大曲,四川省泸州市某酒厂;DNA提取试剂盒(货号175033914),QIAGEN公司;双链DNA荧光定量检测试剂盒(货号12640ES),翌圣生物科技(上海)股份有限公司;DNA标记物(货号G3363-01),武汉塞维尔生物科技有限公司。
1.2 仪器与设备
5403R冷冻离心机,德国Eppendorf公司;SI-0256(G560E)涡旋振荡仪,美国Scientific Industries公司;TUV-TOC/UF纯水仪,德国OmniaPure公司;SBL-10TD控温超声波清洗机,宁波新芝生物科技股份有限公司;HH-8数显恒温水浴锅,常州天瑞仪器有限公司;MS105DU电子天平,瑞士METTLER TOLEDO公司;PAL RTC-1600顶空固相微萃取多功能进样器,广州智达实验室科技有限公司;GCMS-QP2020气相色谱-质谱联用仪,日本Shimadzu Corporation公司;HP-INNOWAX色谱柱(60 m×0.25 mm×0.25 μm),美国Agilent公司。
1.3 实验方法
1.3.1 制曲
采用仿生工艺制备高温大曲。曲坯经压制成型后,放入曲架进行发酵。方案1:在曲架四周(除顶部和底部)覆盖稻草,样品以C表示。方案2:在曲架四周(除顶部和底部)覆盖其他保温保湿材料,样品以A表示。为保证实验结果的可靠性和重复性,每个方案均设置了10个以上的独立生物学重复(每组n≥10个独立曲架)。
1.3.2 取样
每天固定时间进行温度(湿度)数据的采集:针对环境温度(曲房外)和曲房温度(门口、窗户和中心),设置3个温度记录点;针对大曲的发酵温度,分别在每个独立曲架的上层(S)、中层(Z)、下层(X)设置3个温度记录点。在安曲(0 d)、翻曲(7 d)、拆曲(40 d)这3个关键时间点进行大曲样品采集。针对每个独立曲架,采用五点取样法分别从上层、中层、下层这3个垂直梯度采集样品。将同一曲架内每层的5个取样点样本分别粉碎并等质量混合均匀,形成该曲架对应的上层、中层、下层代表性样本,用于理化指标和风味物质检测。同一实验方案的10个曲架样品分层等质量混合均匀后的大曲样品用于微生物组检测。样品保存于-80 ℃用于微生物检测,保存于-20 ℃ 用于理化指标和风味检测。
1.3.3 理化指标检测
大曲样品的水分、酸度和淀粉均参考QB/T 4257—2011《酿酒大曲通用分析方法》;温度与湿度采用便携式数字温湿度计检测;还原糖的测定采用斐林试剂法[6]。每次检测均重复3次以上。
1.3.4 大曲微生物结构解析
采用试剂盒提取高温大曲DNA,通过荧光计和双链DNA荧光定量检测试剂盒检测DNA的浓度和纯度,利用1%琼脂糖凝胶电泳检测DNA完整性。PCR和测序等后续步骤交由上海美吉生物公司进行。使用Illumina NovaSeq/Hiseq Xten测序平台进行宏基因组测序,经过严格的数据质控、拼接组装、基因预测、非冗余基因集构建等步骤获得最终信息。进行物种注释时,选择最优匹配的结果作为最终的注释结果。
1.3.5 大曲风味物质检测
采用顶空固相微萃取气相色谱质谱联用技术(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)测定高温大曲中的挥发性风味物质含量,具体方法见参考文献[6]。
1.4 数据分析方法
采用DMSAS 1.0.2软件计算标准差,数据以“平均值±标准差”表示;所有统计过程均基于原始测量值的正态性(Shapiro-Wilk检验,P>0.05)和方差齐性假设验证(Levene检验,P>0.1);多重比较使用Tukey HSD(honestly significant difference)法,显著性阈值设为P<0.05;采用SciDAVis.2.7软件绘制折线图、柱状图、聚类热图;采用R语言进行正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA);采用联川生物云平台计算Spearman相关性系数并绘制相关性热图。
2 结果与分析
2.1 不同保温保湿材料高温大曲的理化指标分析
在大曲的发酵过程中,曲房的温度和湿度等非生物因素对大曲微生物群落的胁迫作用赋予大曲独特的风味和功能。较高的制曲温度是酱香大曲区别于其他大曲的关键点,发酵顶温通常高于60 ℃。由于曲架的空间异质性,同一曲架不同层的高温大曲的环境因子也并不完全相同,在发酵结束后可形成黑曲、白曲和黄曲。
大曲发酵周期为40 d,在7 d进行翻曲,在23 d对曲房进行开窗换气,曲块和环境的温度变化情况如图1所示。环境和曲房温度分别在22.0~34.5 ℃、29.3~56.0 ℃波动。大曲的发酵温度整体符合“前缓、中挺、后缓落”的变化规律。由图1可知,大曲的核心温度在0~7 d阶段迅速上升,在短时间内从接近室内温度上升到最高温度(62.0 ℃),升温趋势与李喆等[7]的研究结果相似。在大曲温度达到最高后进行翻曲可调节曲块与氧气的接触面从而促进微生物生长繁殖,有助于提升高温大曲的质量[8]。7~20 d大曲温度较高且平稳。在23 d曲房开窗通风之后,曲温整体上升后缓慢下降,可能是氧气骤增引起好氧菌产热,但发酵后期的微生物群落结构已经较稳定,因此温度短暂上升后逐渐回落到正常水平。C组和A组的上层温度变化趋势相似度极高,可能是曲架顶部与空气接触面积更大导致上层曲块与环境温度紧密相关。
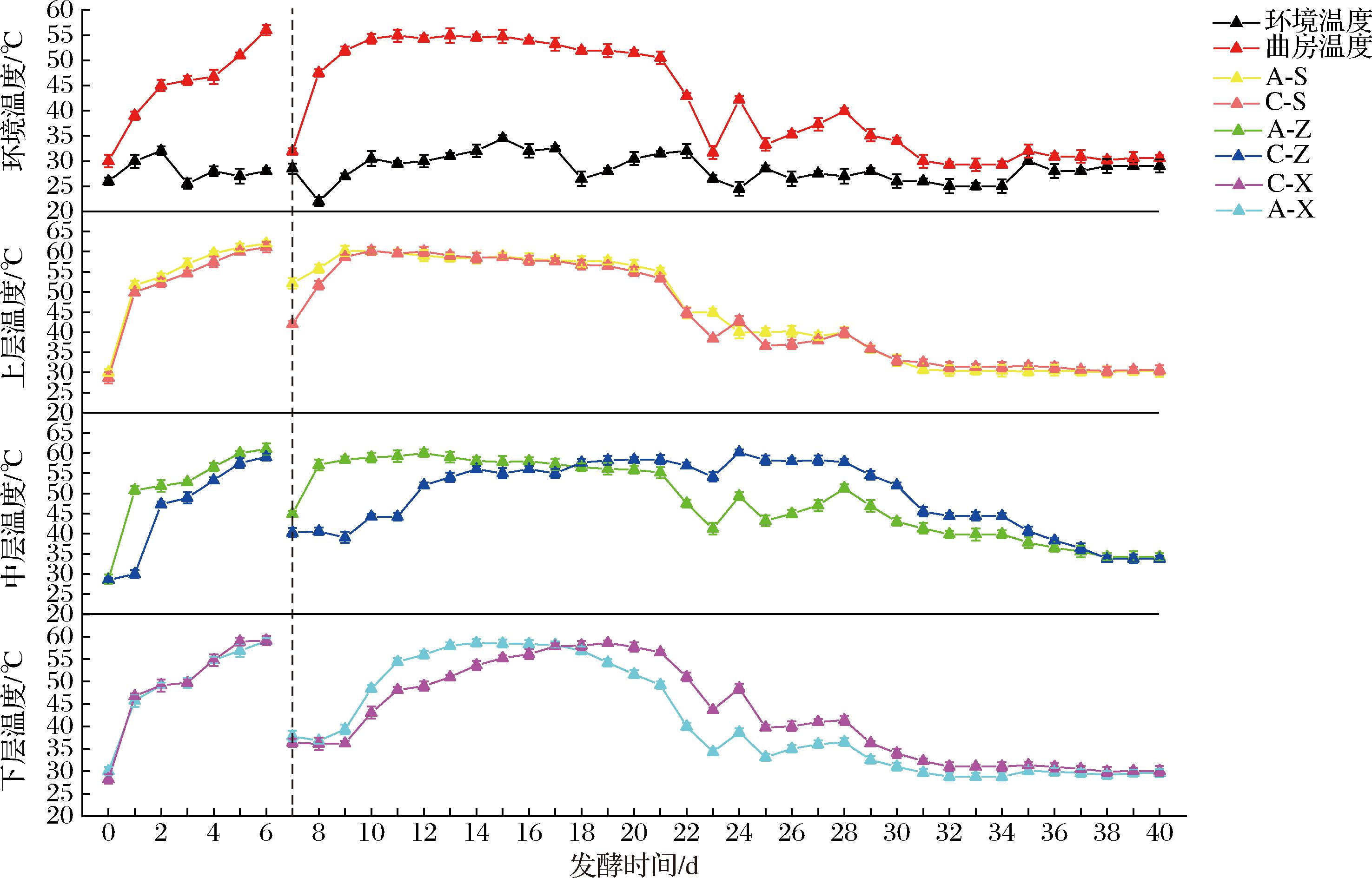
图1 高温大曲温度变化情况
Fig.1 The variation of temperature in high-temperature Daqu
注:7 d虚线表示翻曲。
在0~17 d,A组的中下层比C组更快地进入挺温期,而在发酵中后期(18~40 d),A组的中下层比C组的更快进入缓落期,据此可认为A组在高温大曲发酵中表现出更灵敏的温度响应特性,可能主要归因于其材料的物理特性与微生物活动的协同作用。由于材料A的透气性低于稻草,初期可能通过减少热量散失促进微生物(如芽孢杆菌)快速产热,加速核心温度升至62.0 ℃。发酵中期,材料A的低透气性形成微氧环境,抑制好氧菌活性,而弱吸湿性维持曲心湿度,促进耐湿菌繁殖。至后期,A组的内部水分梯度增大和氧限制效应会加速微生物代谢衰退,导致温度缓落更显著。
对高温大曲发酵过程的理化指标进行检测,如图2所示。随着发酵的进行,温度的升高和微生物活性的增加会促进水分挥发,曲块水分从(35.40±0.25)%下降到(12.37±0.94)%,符合生产高温大曲的水分变化规律[7]。在翻曲时,发酵温度已达到最高点,曲块水分迅速挥发并聚集在上部空间,因此翻曲阶段的水分呈现“上层>中层>下层”的趋势。同时,A组平均水分高于C组,说明材料A比稻草具有更好的保湿效果。淀粉是微生物生长繁殖的物质基础,传统工艺大曲在正常发酵时一般消耗6%~7%的淀粉[9]。本研究的仿生高温大曲从安曲到拆曲,淀粉含量从(72.19±0.90)%下降到(68.17±1.89)%,较传统工艺下降幅度更小。淀粉等物质在淀粉酶的催化作用下水解产生还原糖,能被微生物直接利用。仿生高温大曲的还原糖变化趋势与魏阳等[6]的研究结果相似,呈现先快速上升后缓慢下降的趋势。发酵初期,由于微生物快速繁殖会产生淀粉酶,分解小麦淀粉导致使还原糖含量上升,但至中后期,由于消耗速度超过产生速度导致还原糖含量逐渐下降[6]。从发酵初期到结束,酸度逐渐升高,拆曲时酸度最可达2.81 mmol/10 g。曲块中的微生物(特别是产酸微生物)进行有机酸代谢或三羧酸循环降解,有机物会使大曲的酸度增加[9]。
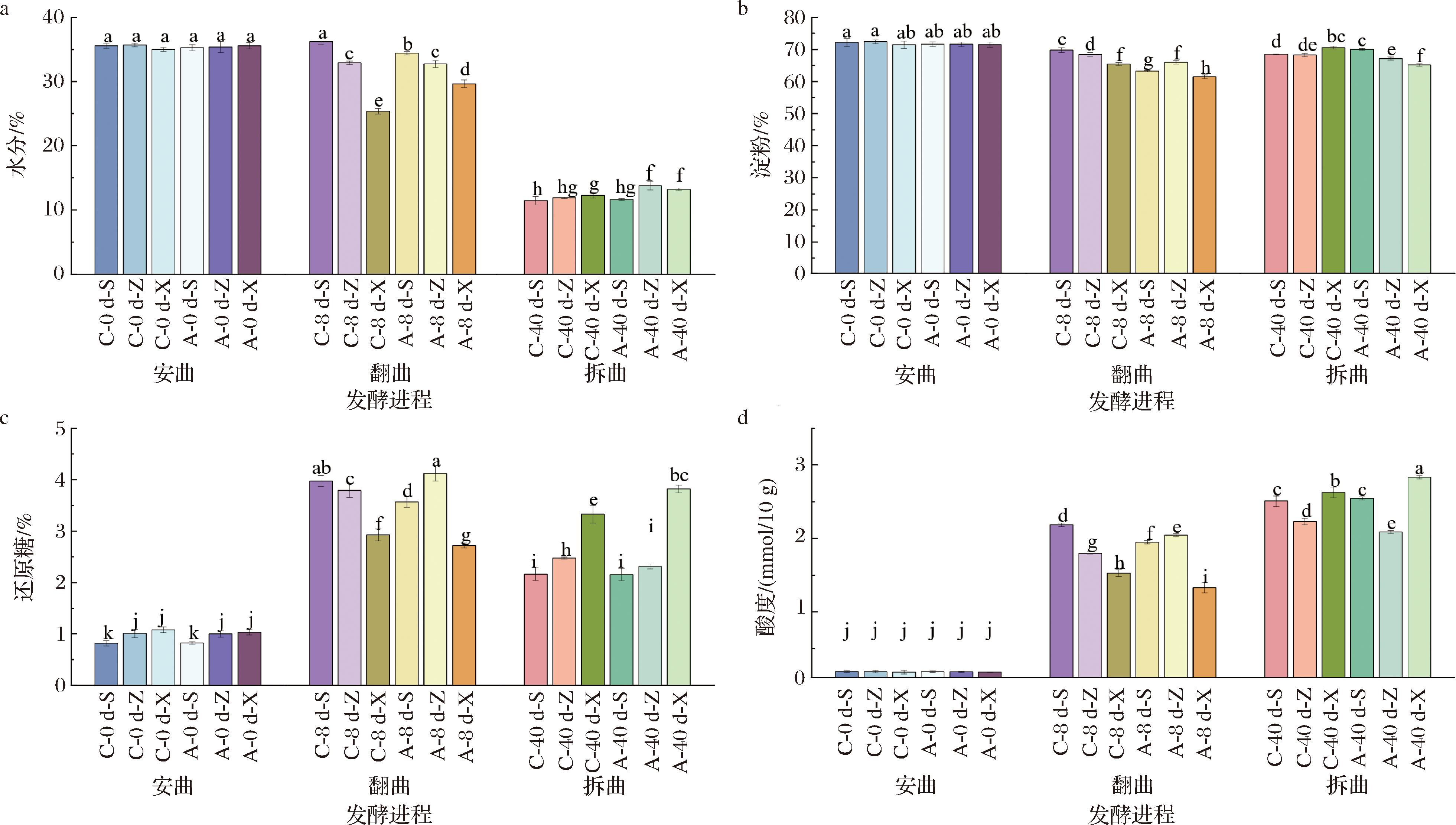
a-水分;b-淀粉;c-还原糖;d-酸度
图2 高温大曲的理化指标
Fig.2 Physicochemical indicators of high-temperature Daqu
注:凡有一个相同标记字母的即为差异不显著(P>0.05),凡具不同标记字母的即为差异显著(P<0.05)。
2.2 不同堆积发酵方式高温大曲的风味物质分析
2个方案高温大曲样本中共鉴定出76种挥发性化合物,其中22种酯类、17种醇类、11种醛类、10种吡嗪类、6种酸类、4种酮类、3种酚类、3种其余物质。
大曲中不同类型挥发性化合物组成如图3-a所示。对大曲挥发性化合物进行Z-score标准化并绘制聚类热图(图3-b)。随着发酵的进行,2组大曲的挥发性化合物总量逐渐增加,但按组分类的风味物质的增加趋势有较大差异:醇类和酮类含量逐渐增加,酸类和酯类含量先增加后降低。与之前的研究相似,醇类物质的总量在发酵中后期占据绝对优势,而酸类物质虽然种类少,但含量却高于酯类和醛酮类[10]。在翻曲时,A组的风味物质总量高于C组,同时2组均表现为下层物质的风味物质总量最高。但在拆曲时,C组风味物质总量高于A组,且C组中层的风味物质总量最高。结合大曲的发酵温度可推测:在前期阶段,A组的温度上升速率高于C组,可能归因于A组微生物的生长繁殖活动更为旺盛,在释放了大量热能的同时还促进了风味物质的大量生成。随着发酵时间的延长,A组比C组的发酵温度更快进入缓落期。此时,A组大曲的微生物活动逐渐进入了衰亡期导致风味化合物的生成速度也随之下降,而C组大曲在发酵后期微生物活动增强,为其风味物质的积累提供了更为有利的条件,从而使其在拆曲时表现出更为丰富的风味特性。这一现象不仅反映了2组大曲在发酵过程中微生物活动的差异,也揭示了不同发酵阶段对风味物质积累的影响。
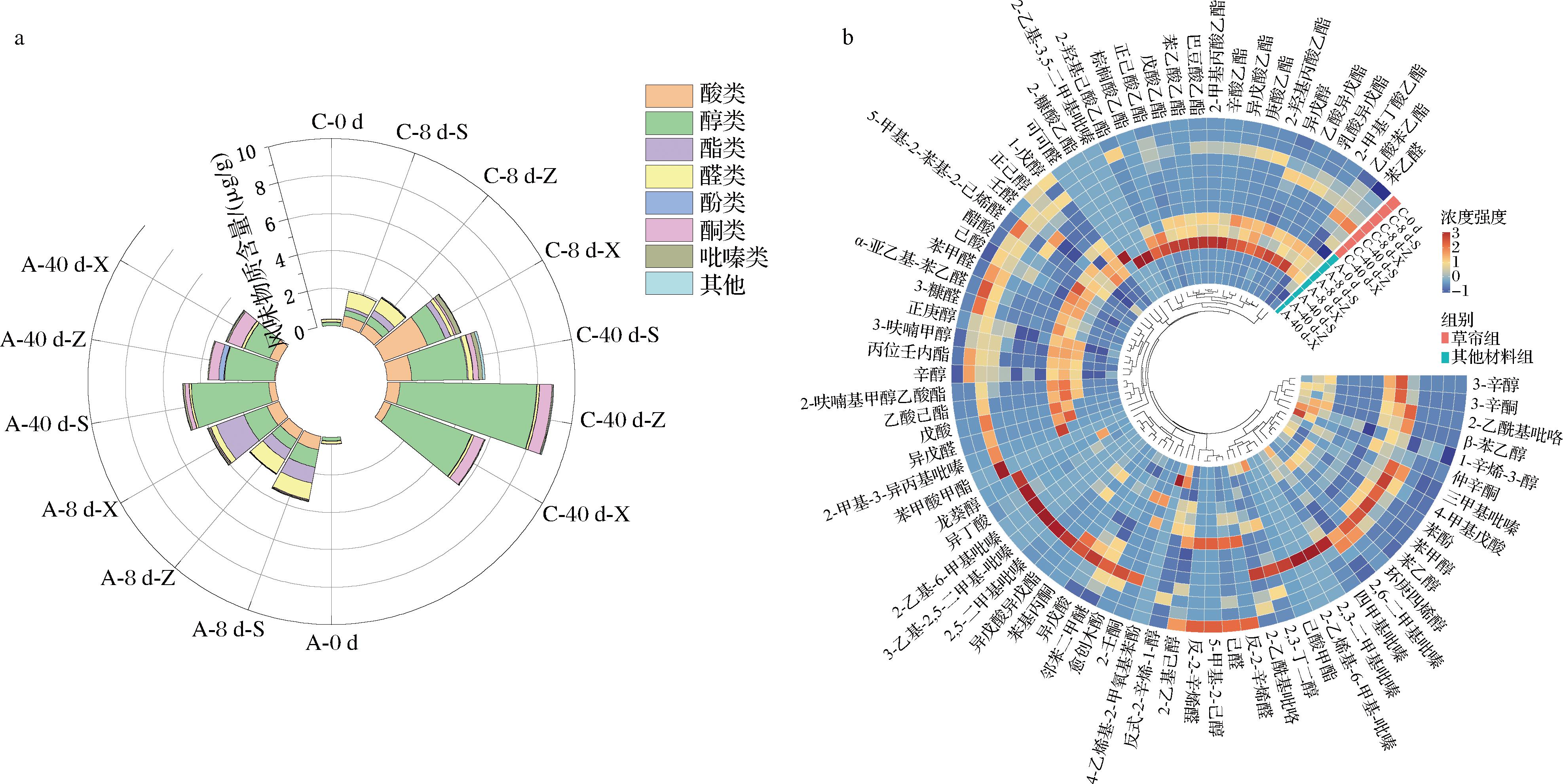
a-挥发性风味物质堆积柱状图;b-挥发性风味物质聚类热图
图3 高温大曲的挥发性风味物质组成
Fig.3 Composition of volatile flavor compounds in high-temperature Daqu
尽管每种挥发性风味物质总量不同且表现出不同的变化规律,但它们的挥发物的时间变化规律仍然具有可比性。部分风味物质的含量在翻曲时高于拆曲时,如A组的乳酸异戊酯、乙酸异戊酯、辛酸乙酯等物质,C组的异丁酸、2-乙基-6-甲基吡嗪、3-乙基-2,5-二甲基-吡嗪等物质,以及A组和C组共有的乙酸、已酸、正庚醇等物质。这种变化趋势可能是由于微生物代谢活动和物质间的相互作用:随着发酵的进行,部分微生物的活性可能先增加后减少,导致相关风味物质的产生量也呈现先增后减的趋势。同时,挥发性风味物质之间可能存在相互作用,如竞争、转化或抑制等,这些相互作用可能导致某些物质在发酵过程中的积累量受到限制,从而在达到峰值后逐渐下降[11]。部分物质含量随发酵时间延长呈现增加的趋势,在拆曲时达到最高值,如3-辛醇、3-辛酮、β-苯乙醇等。可能原因是微生物代谢产生的物质未被有效转化为其他物质,同时某些微生物在发酵后期仍然保持较高的活性,持续产生相关物质。
采用有监督的OPLS-DA揭示A组和C组高温大曲的香气特征差异物质,将不同保温保湿方案下不同时间采集的样品设为自变量X,香气物质的浓度设为响应变量Y,结果显示:R2X=0.894,R2Y=0.742,表明模型较好地拟合了数据[12]。OPLS-DA得分图(图4-a)显示,翻曲和拆曲时的样品在X轴上距离较远,说明这2个阶段的大曲在香气物质组成上存在显著差异。此外,200次置换实验的交叉验证表明,模型Q2的一元线性回归曲线在纵轴上的截距小于0,说明模型可靠,没有过度拟合[13]。
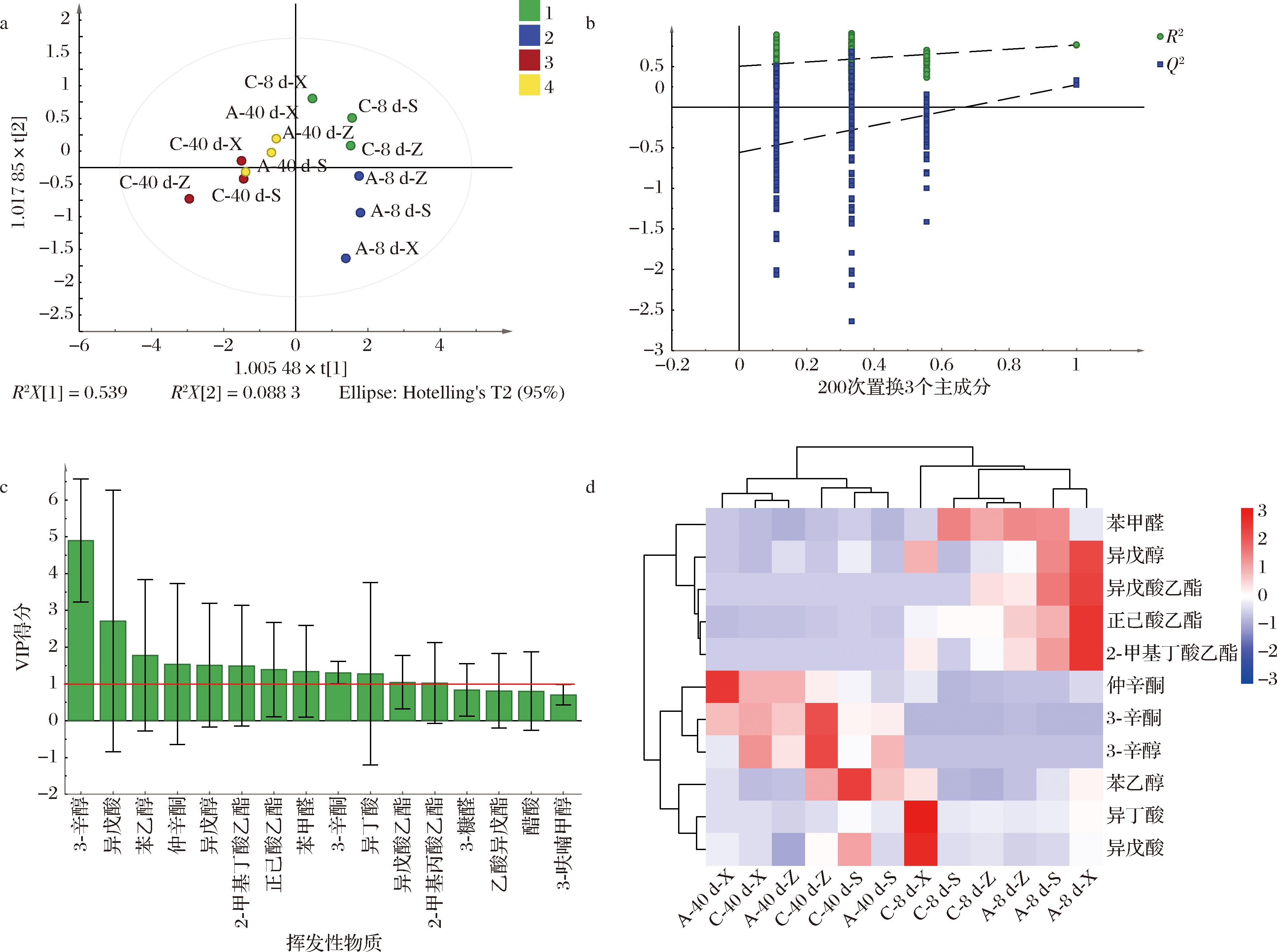
a-高温大曲香气成分的PLS-DA得分图;b-200次置换实验的交叉验证结果;c-挥发性物质的VIP得分;d-基于VIP风味物质的聚类热图
图4 高温大曲的挥发性风味物质分析
Fig.4 Analysis of Volatile Flavor Compounds in High-Temperature Daqu
基于变量投影重要性(variable importance in projection,VIP)值>1的条件筛选出对模型香气物质组成差异贡献最大的11种特征风味物质并绘制热图。如图4-d所示,发酵过程中挥发性物质的动态演变呈现显著阶段特异性:部分酯类与低分子质量醇类在翻曲时(7 d)达到峰值,而部分酮类及芳香醇类则在成熟期(40 d)显著富集。在翻曲时,A组下层样品中检测到某些酯类物质的特异性积累,其中异戊酸乙酯[(0.16±0.003) μg/g]、正己酸乙酯[(0.40±0.005 6) μg/g]和2-甲基丁酸乙酯[(0.42±0.004 1) μg/g]含量分别较C组同层高0.16、0.31、0.11 μg/g。这种现象可能与材料A较高的保湿性促进下层曲坯水分再分布,进而激活酯化酶系活性相关。但至成熟期(40 d),上述酯类物质含量下降0.034 μg/g至检测限以下,提示其可能作为前体物质参与后续美拉德反应或微生物转化过程。在拆曲时,仲辛酮、3-辛酮、3-辛醇在中层富集,而β-苯乙醇则在上层富集。这种空间分布特征可能源于发酵时上层温度高于下层,促进上层酵母菌的苯丙氨酸代谢及中层3-辛酮合成相关微生物的氧化过程。
2.3 不同堆积发酵方式高温大曲的微生物群落分析
2.3.1 α-多样性分析
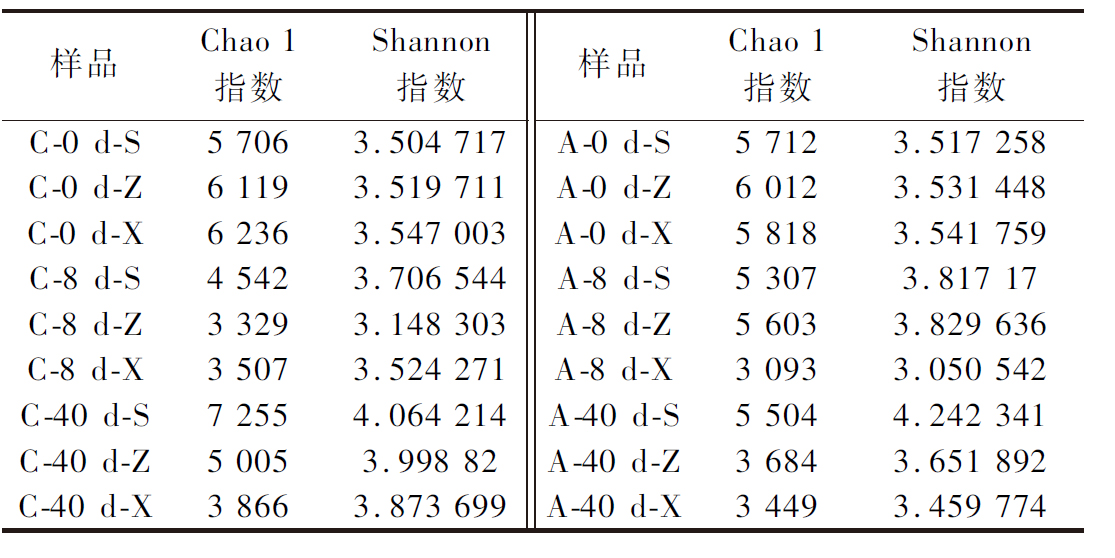
经过高通量测序,18个样品共得到5 524 151份非冗余基因集基因,总序列长度为1 938 706 008 bp。采用Chao 1指数反映不同保温保湿材料高温大曲的微生物物种丰富度,采用Shannon指数反映群落多样性。由表1可知,在0 d时,C组和A组的Chao 1和Shannon指数都不存在显著性差异(P>0.05)。在翻曲时,C组上层和A组中层的Chao 1和Shannon指数在2组方案中最高,表明此时A组和C组的微生物物种丰富度和群落多样性开始显示出细微区别。在拆曲时,无论是A组还是C组,中上层的微生物物种丰富度和群落多样性都高于下层。
表1 高温大曲的α-多样性指数
Table 1 α-Diversity indices of high-temperature Daqu
2.3.2 细菌和真菌微生物群落分析
如图5-a所示,进一步对A组和C组大曲样品微生物群落的结构进行比较分析,将平均相对丰度高于1.0%的细菌(真菌)门和属定义为优势细菌(真菌)门和属,对占比最高的前20个优势细菌(真菌)进行分析,其他菌属归类于“others”。经物种分类注释后,18个大曲样品共检测到6个优势物种门,其中芽孢杆菌门(Bacillota),子囊菌门(Ascomycota),假单胞菌门(Pseudomonadota)是平均含量最丰富的3个门。在安曲时,Pseudomonadota占据绝对优势,在C组和A组分别高达70.59%和70.53%;在翻曲时,Bacillota平均占比最高,在C组和A组分别高达97.71%和82.49%;在拆曲时,Ascomycota平均占比最高,在C组和A组分别高达90.22%和68.79%,其次是Bacillota,其他微生物总相对丰度较低。这与之前的研究结果一致:在高温大曲中Ascomycota、Bacillota等为绝对优势菌门,为高温大曲的风味形成贡献重要作用[14-15]。据报道,大曲中芽孢杆菌的数量与吡嗪类化合物的含量呈正相关,而吡嗪类化合物赋予了酱香型白酒的特征风味[16]。在拆曲时,A组相较于C组的Bacillota占比显著较高,暗示A组中可能含有更多能够产生吡嗪类化合物的微生物。
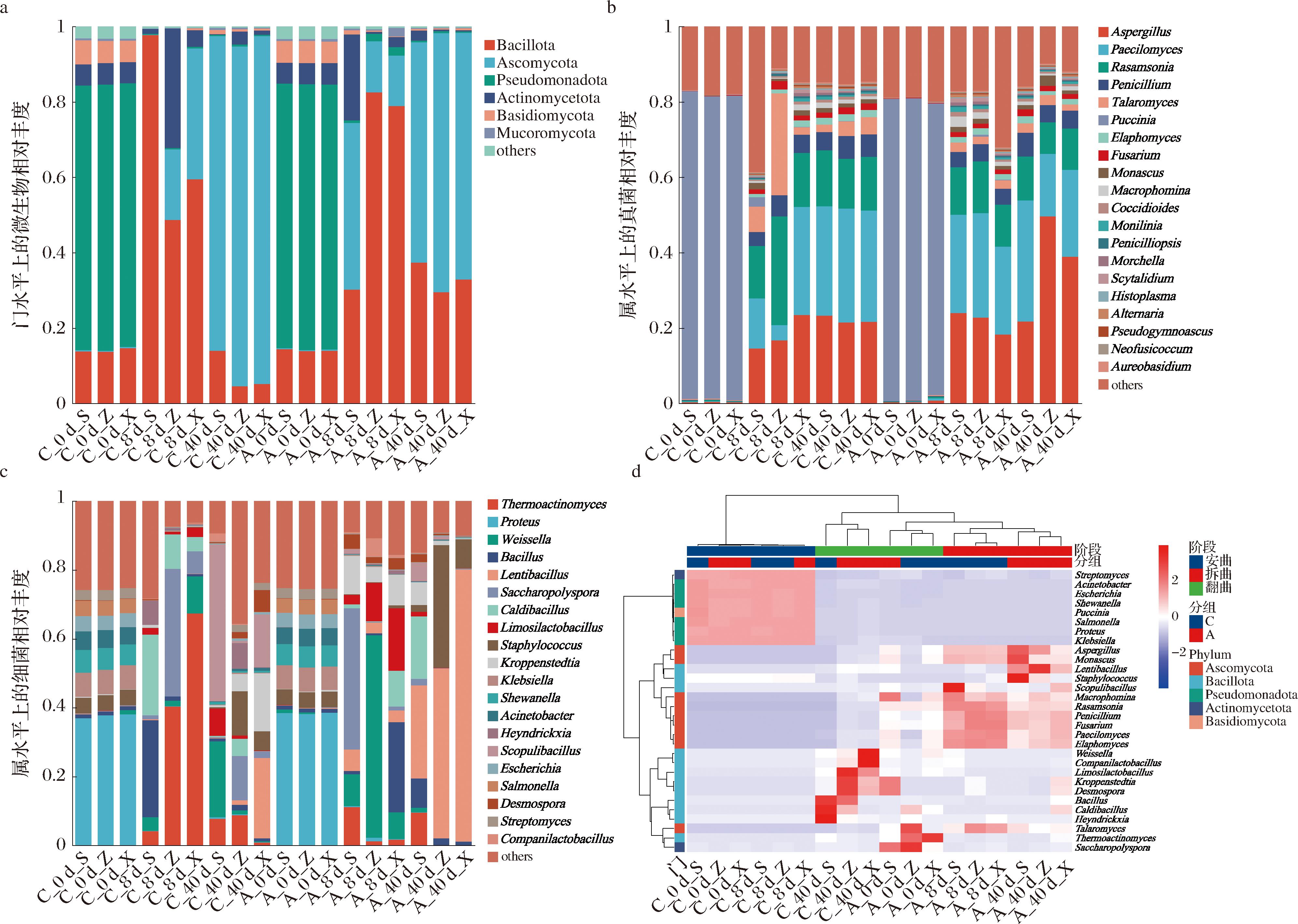
a-基于门水平的微生物相对丰度;b-基于属水平的真菌相对丰度;c-基于属水平的细菌相对丰度;d-基于属水平的真菌和细菌聚类热图
图5 高温大曲细菌和真菌的群落结构
Fig.5 Community structure of bacteria and fungi in high-temperature Daqu
进一步在属水平上对真菌进行分析。如图5-b所示,在2组大曲中一共观察到20种占比高于1%的真菌属。在安曲时,锈菌属(Puccinia)在A组和C组中都占绝对优势。在拆曲时,C组的上、中和下层的真菌群落结构差异较小,而A组差异较大。从翻曲到拆曲,平均相对丰度从高到低的真菌属依次是曲霉属(Aspergillus),淡紫拟青霉属(Paecilomyces),罗萨氏菌属(Rasamsonia)。这3种微生物在C组和A组的变化趋势基本一致,但具体变化幅度和起点有所不同:8~40 d,Rasamsonia的含量总体下降,且C组的下降幅度大于A组;Aspergillus的含量总体上升,且C组的增加幅度小于A组;Paecilomyces在C组中呈现增加趋势,在A组中呈现下降趋势。研究显示Aspergillus在中温大曲中平均相对含量显著偏高,是中温大曲中的优势真菌之一[17-18],而Rasamsonia、Aspergillus、丝衣霉属(Byssochlamys)也是黑曲中的常见微生物,在高温大曲中扮演着重要的角色[19]。霉菌能够产生淀粉酶、蛋白酶、纤维素酶、脂肪酶等多种酶类物质,这些酶类在白酒酿造前期对原料中淀粉等大分子物质的降解起到重要作用。此外,霉菌在代谢过程中还会分泌一些呈香物质,这些物质对大曲风味的形成起到重要作用[17]。
如图5-c所示,在高温大曲的发酵过程中,细菌群落结构经历了显著的动态变化,呈现出明显的阶段性特征。安曲阶段以变形杆菌属(Proteus)为主,第一次翻曲则以高温放线菌属(Thermoactinomyces,C组)和魏斯氏菌(Weissella,A组)等菌属为主,在拆曲时则以火山渣芽孢杆菌属(Scopulibacillus,C组上层)和慢生芽孢杆菌属(Lentibacillus,A组全层及C组下层)等菌属为主。虽然优势菌属在发酵过程中不断更替,但某些菌属(如Thermoactinomyces、Lentibacillus等)在不同阶段或不同组别中均有出现,显示出其一定的持续性和适应性。在安曲时,Proteus(36.87%~38.56%)是绝对优势菌属,其含量远高于其他细菌属。在翻曲时,在C组的中层和下层中,Thermoactinomyces成为绝对优势菌属,含量分别为40.42%和67.33%,显示出其在发酵中期C组中的主导地位。C-8 d-X的愈创木酚、2-壬酮、苯基丙酮的含量很高,可能与Thermoactinomyces的高占比相关[20]。A组的上、中、下层含量最高的细菌分别是糖多孢菌属(Saccharopolyspora,40.98%)、Weissella(58.74%)、Bacillus(26.22%)。Saccharopolyspora和Bacillus是酱香型大曲常见优势细菌,前者在白曲和黄曲中的占比分别可达59%和87%,后者在白曲、黑曲和红曲中的占比分别达到23%、29%、30%[21]。在拆曲时,C组的上、中、下层含量最高的细菌分别是Scopulibacillus(45.56%)、葡萄球菌属(Staphylococcus,12.83%)、Lentibacillus(23.37%),而A组上层、中层和下层中,Lentibacillus均占据绝对优势,含量分别为27.01%、49.35%、79.06%。在发酵后期,特别是A组中,Lentibacillus成为绝对优势菌属,表明其在高温大曲发酵后期具有重要的作用[22]。这可能与Lentibacillus的耐高温、耐酸碱等特性有关,使其能够在高温大曲的极端环境中生存并繁殖。Lentibacillus具有良好的淀粉酶、蛋白酶、纤维素酶产生能力,在45 ℃固态模拟发酵过程能够产生2,5-二甲基吡嗪、蘑菇醇、苯乙醇、2-甲基己酸等结构多样的代谢产物,是大曲曲香的重要组成成分[22]。Bacillus是高温大曲常见的细菌,主要分布在高温大曲的黑色部分,与吡嗪的含量呈正相关,能赋予酱香型白酒特有的风味[16]。
图5-d通过聚类热图的形式直观地展示了安曲、翻曲、拆曲时的优势细菌和真菌的分布情况。由图5-d可知,高温大曲在3个不同阶段的微生物群落结构存在着差异,每个阶段都拥有其独特的优势微生物种群。在安曲阶段,A组与C组的微生物群落结构高度相似。此阶段,链霉菌属(Streptomyces)、不动杆菌属(Acinetobacter)、埃希氏菌属(Escherichia)、Puccinia等微生物的丰度显著高于翻曲和拆曲时。在翻曲阶段,A组和C组的微生物群落结构虽然呈现出一定的差异,但尚未达到完全区分的程度。例如,C-8 d-S与A组的某些样本(如A-8 d-Z和A-8 d-X)聚为一组,而A-8 d-S则与C组的另一些样本(如C-8 d-Z和C-8 d-X)聚为一组,显示出一定的组间差异。到了拆曲时,A组与C组的微生物群落结构发生了显著变化,2组之间的差异变得尤为明显,且每组内部的上、中、下层之间差异相对较小。在这个阶段,壳球孢属(Macrophomina)、Rasamsonia、青霉属(Penicillium)、镰孢属(Fusarium)、Paecilomyces等微生物在A组的丰度更高,而Aspergillus、红曲霉属(Monascus)、Lentibacillus、Staphylococcus则在C组的丰度更高。
2.2.3 菌群代谢功能及其变化
微生物的群落结构发生改变可能导致其代谢功能发生变化。本研究将宏基因组测序结果与KEGG进行注释对比,以探究微生物代谢功能的偏好。大曲微生物的KEGG二级代谢通路信息如图6所示,随着发酵的进行,高温大曲的细菌二级代谢通路发现明显变化。全局和总览图主要包括次生代谢物的生物合成、不同环境中的微生物代谢和碳代谢等通路,它在每个阶段的占比都最高,说明微生物群落可能具有较强的生长代谢潜力和新老更替速率。参与神经退行性疾病、碳水化合物代谢、氨基酸代谢的基因占比也较高。以上结果表明,微生物处于活跃的生长繁殖与代谢活动中,其中对碳水化合物与氨基酸等物质的代谢较为旺盛[20]。碳水化合物通过微生物代谢生成还原糖,还原糖和氨基酸在被利用与转化过程中可能发生美拉德反应,从而伴生多种酸、醇和醛类物质,最终影响白酒的感官风味。
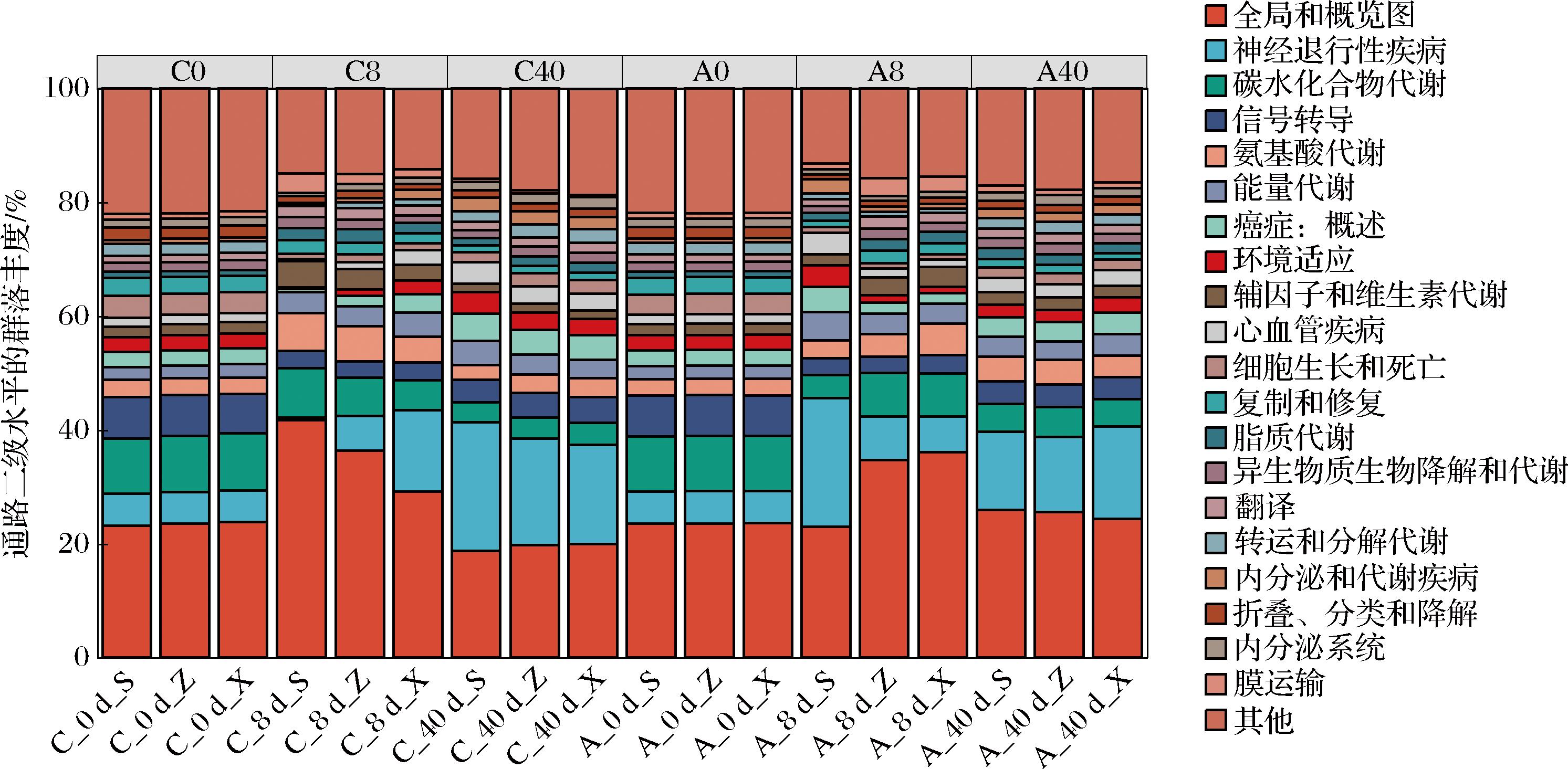
图6 高温大曲的微生物的KEGG二级代谢通路信息
Fig.6 KEGG level 2 metabolic pathway information of microorganisms in high-temperature Daqu
2.4 高温大曲微生物群落与风味物质关联性分析
酱香型白酒中酸类、醛酮类、酚类、呋喃类等物质的生成受到众多微生物的调控作用[23]。为了更深入地理解高温大曲中优势微生物与风味物质之间的关系,采用Spearman相关系数分析了前20种优势细菌与真菌分别与特征风味物质之间的相互作用[24]。设定当相关系数大于0.6且P<0.05时,认为两者之间存在显著相关性。如图7-a所示,Scopulibacillus与异戊酸乙酯、2-甲基丁酸乙酯、正己酸乙酯、异戊醇等多种风味物质呈显著正相关(P<0.05)。Scopulibacillus是高温大曲中常见的优势细菌,与4-羧基谷氨酸、3-羟基犬尿氨酸和反式乌头酸等物质的代谢相关,同时与戊酸的产生存在微弱的正相关关系[25-26]。此外,3-辛醇和3-辛酮的生成与Acinetobacter、Escherichia、Streptomyces等细菌显著相关(P<0.05)。3-辛醇具有油脂香和青草香,3-辛酮具有蘑菇香、奶酪香,并带有青香和蔬菜香,3-辛醇经过氧化反应后可生成3-辛酮。β-氧化途径是细菌脂肪酸降解的重要途径,而3-辛醇和3-辛酮作为烷基酮类化合物,其生成可能与Escherichia等细菌的β-氧化途径相关。如图7-b所示,部分真菌与部分风味物质存在正向关联:异戊醇和2-甲基丁酸乙酯等风味物质与Macrophomina、Monilinia、Morchella、柱顶孢属(Scytalidium)、链格孢属菌(Alternaria)等真菌属呈显著正相关(P<0.05)。同时,Scytalidium和Alternaria对正己酸乙酯、异戊酸乙酯的生成具有正向显著影响(P<0.01)。结合大曲的风味物质浓度数据可推测:微生物群落功能分化驱动可能会导致A组与C组的风味物质累积差异。翻曲时A组风味物质总量更高,源于其早期富集的Thermoactinomyces和快速增殖的Aspergillus等微生物协同代谢,加速淀粉、蛋白质水解,生成酯类及氨基酸衍生物。拆曲时C组的风味物质更高,可能是因为A组中后期Lentibacillus通过氧化作用消耗酯类,而C组中Scopulibacillus与Scytalidium可能形成共生体系:真菌合成萜烯类物质弥补氧化损失,细菌则稳定酯类代谢。

a-优势细菌与关键风味物质的相关性分析;b-优势真菌与关键风味物质的相关性分析
图7 关键风味化合物与优势微生物的关联分析
Fig.7 Correlation analysis between key flavor compounds and dominant microorganisms
在大曲发酵体系中,微生物以大曲所含的淀粉和蛋白质类物质作为底物,借助淀粉/纤维素降解、糖酵解、三羧酸循环、脂肪酸延伸等一系列关键代谢途径,实现了乙酯类化合物的生物合成。在这一复杂的代谢网络中,葡萄糖转化为丙酮酸,丙酮酸可进一步转化为乙酰辅酶A,而乙酰辅酶A是合成乙酸乙酯等小分子直链脂肪酸酯的重要前体物质。对于异戊酸乙酯、正己酸乙酯等特定酯类化合物,其生物合成主要涉及缬氨酸合成与代谢途径(ko00290)、丙酮酸代谢途径(ko00620)、脂肪酸生物合成途径(ko00061)以及脂肪酸代谢途径(ko01212)。然而,值得注意的是,由于微生物种类的多样性以及环境条件的复杂性,实际参与这些酯类化合物合成的代谢通路可能会存在一定差异。已有研究表明,Bacillus、Streptomyces、Kroppenstedtia等微生物在己酸和异戊醇生物合成的关键代谢途径上呈现出显著的遗传富集现象[27]。Scopulibacillus作为芽孢杆菌属的一员,在制曲发酵阶段能够分泌多种胞外酶,这些酶类可以有效地促进原料的水解过程,进而为酯类物质的合成提供充足的前体物质。尽管目前尚未有确凿的文献证据表明Scytalidium和Alternaria与酯类化合物的生成之间存在直接的正向因果关系,但基于其在次级代谢产物合成调控方面的潜在作用,这些真菌可能通过间接的方式影响酯类物质的多样性和组成。综上所述,Scopulibacillus、Scytalidium、Alternaria在酯类物质的生成过程中展现出协同作用,其中Scopulibacillus的相对丰度随发酵时间的延长而增加,这些微生物可能是高温大曲中的关键产酯功能菌群。为了进一步通过基因或代谢层面直接验证此记录,后续可基于宏基因组学靶向筛选酯酶基因,并结合体外纯培养实验验证菌株产酯能力。
3 结论
本研究针对仿生化高温大曲工艺的优化需求,系统解析了稻草(C组)与其他保温保湿材料(A组)对高温大曲发酵过程的影响机制。研究结果显示,A组在中下层大曲发酵中表现出更快的温度响应,能更快达到温度挺温期和缓落期,且曲块平均水分含量高于C组,显示出材料A在保温保湿方面的优势。在挥发性风味物质方面,虽然翻曲时A组总量较高,但拆曲时C组更高,且2组挥发性成分组成存在差异。在拆曲时,A组相较于C组含有更高占比的Bacillota和Lentibacillus,因此A组中可能产生更多吡嗪类以及大曲曲香相关化合物。本研究发现,不同保温材料对高温大曲中的微生物群落结构也有一定影响,主导微生物种类及其变化趋势存在差异,这些差异进一步影响了高温大曲中的风味物质含量和组成,导致部分风味物质随时间变化呈现不同的变化趋势。综上所述,在高温大曲的生产中运用材料A进行保温保湿可能是潜在的稻草保温替代法。本研究为改进制曲工艺并推动高温大曲仿生化发展提供了实际生产指导意义。未来研究可在此基础上进一步深化,例如,探究更多种类的保温保湿材料对高温大曲发酵过程的影响,以寻找更优的保温保湿解决方案。同时,还可将成品大曲应用酿酒生产,对不同保温保湿材料制成的高温大曲酿酒品质进行深度评估。
[1] 周晨曦, 郑福平, 李贺贺, 等.白酒大曲风味物质研究进展[J].中国酿造, 2019, 38(5):6-12.ZHOU C X, ZHENG F P, LI H H, et al.Research progress on flavor compounds of Baijiu Daqu[J].China Brewing, 2019, 38(5):6-12.
[2] YANG L, FAN W L, XU Y.GC×GC-TOF/MS and UPLC-Q-TOF/MS based untargeted metabolomics coupled with physicochemical properties to reveal the characteristics of different type Daqus for making soy sauce aroma and flavor type Baijiu[J].LWT, 2021,146:111416.
[3] 王凡, 卢君, 王丽, 等.白酒生产自动化技术应用研究进展[J].中国酿造, 2023,42(4):1-7.WANG F, LU J, WANG L, et al.Research progress on the application of automation technology for Baijiu production[J].China Brewing, 2023,42(4):1-7.
[4] 左乾程, 黄永光, 郭敏, 等.酱香型白酒机械化制曲发酵细菌群落的演替[J].食品科学, 2021,42(18):150-156.ZUO Q C, HUANG Y G, GUO M,et al.Succession of bacterial community during mechanized fermentation of Maotai-flavor Daqu[J].Food Science, 2021,42(18):150-156.
[5] 李声睿, 张立强, 魏阳, 等.不同堆积发酵方式高温大曲理化指标及微生物关联性研究[J].食品与发酵工业, 2025, 51(7):105-114.LI S R, ZHANG L Q, WEI Y, et al.Investigation of physicochemical indexes and microbial correlation of high-temperature Daqu in different fermentation methods[J].Food and Fermentation Industries, 2025, 51(7):105-114.
[6] 魏阳, 张芮, 张立强, 等.小麦粉碎度与成品高温大曲理化和风味组分的相关性研究[J].食品与发酵工业, 2024,50(20):181-189.WEI Y, ZHANG R, ZHANG L Q, et al.Correlation between wheat pulverization degree and physicochemical and flavor components of high-temperature Daqu[J].Food and Fermentation Industries, 2024,50(20):181-189.
[7] 李喆, 冯海燕, 吴德光, 等.高温大曲发酵过程中理化指标及风味变化规律的研究[J].酿酒科技, 2022(10):40-45.LI Z, FENG H Y, WU D G, et al.Changes of physicochemical indexes and flavor of high-temperature Daqu during fermentation[J].Liquor-Making Science &Technology, 2022(10):40-45.
[8] 王永辉, 张春香, 聂正东, 等.翻曲次数对酱香高温大曲品质的影响分析[J].酿酒科技, 2022(3):77-82.WANG Y H, ZHANG C X, NIE Z D, et al.Effect of Daqu-turning frequency on the quality of high-temperature Jiangxiang Daqu[J].Liquor-Making Science &Technology, 2022(3):77-82.
[9] 刘石雪, 武艳丽, 王秀菊, 等.中高温大曲发酵过程中理化指标及微生物消长规律研究[J].酿酒科技, 2024(8):25-29;37.LIU S X, WU Y L, WANG X J, et al.Study on physicochemical indexes and microbial succession law during fermentation of medium/high-temperature Daqu[J].Liquor-Making Science &Technology, 2024(8):25-29;37.
[10] 卢中明, 张祥, 叶光斌.不同生产月份中高温成品大曲理化指标、挥发性风味物质分析[J].食品与发酵工业, 2024,50(19):315-320.LU Z M, ZHANG X, YE G B.Physicochemical indexes and volatile flavor substances of medium-high temperature mature Daqu in different production months[J].Food and Fermentation Industries,2024,50(19):315-320.
[11] 张春林, 敖宗华, 炊伟强, 等.固相微萃取-气相色谱-质谱法分析中高温大曲发酵、贮存过程中挥发性风味成分的变化[J].食品与发酵工业, 2011, 37(4):198-203.ZHANG C L, AO Z H, CHUI W Q, et al.Changes in volatile compounds of Daqu during fermentation and storage by headspace solid phase microextraction combined with gas chromatography-mass spectrum[J].Food and Fermentation Industries, 2011, 37(4):198-203.
[12] HUANG P, JIN Y, LIU M M, et al.Exploring the successions in microbial community and flavor of Daqu during fermentation produced by different pressing patterns[J].Foods, 2023,12(13):2603.
[13] 周丽伟, 史乐怡, 宁井铭, 等.基于分子感官组学的不同产区茉莉花茶香气组成特征分析[J].安徽农业大学学报, 2024, 51(3):495-502.ZHOU L W, SHI L Y, NING J M, et al.Study on the characteristic aroma components of jasmine tea from different producing areas by molecular sensory genomics[J].Journal of Anhui Agricultural University, 2024, 51(3):495-502.
[14] 李彦涛, 梁红东, 尉军强, 等.不同种类高温大曲真菌群落多样性与结构分析[J].中国酿造, 2024,43(7):126-131.LI Y T, LIANG H D, WEI J Q, et al.Analysis of fungi community diversity and structure in different high-temperature Daqu[J].China Brewing, 2024,43(7):126-131.
[15] LI H, LIAN B, DING Y H, et al.Bacterial diversity in the central black component of Maotai Daqu and its flavor analysis[J].Annals of Microbiology, 2014,64(4):1659-1669.
[16] JIN Y, LI D Y, AI M, et al.Correlation between volatile profiles and microbial communities:A metabonomic approach to study Jiang-flavor liquor Daqu[J].Food Research International, 2019,121:422-432.
[17] 崔梦君, 王玉荣, 侯强川, 等.基于三代测序技术高温和中高温大曲真菌多样性解析及酵母菌的分离鉴定[J].食品工业科技, 2025,46(2):175-183.CUI M J, WANG Y R, HOU Q C, et al.Analysis of fungal diversity and isolation and identification of yeast in high-temperature and medium-high-temperature Daqu using three generation sequencing technology[J].Science and Technology of Food Industry, 2025, 46(2):175-183.
[18] 赵慧君, 王玉荣, 侯强川, 等.滨州地区高温和中温大曲真菌类群解析及其感官品质关联性分析[J].食品工业科技, 2025,46(11):163-173.ZHAO H J, WANG Y R, HOU Q C, et al.Analysis of fungal communities of high-temperature and medium-temperature Daqu in Binzhou region and their correlation with sensory quality[J].Science and Technology of Food Industry, 2025,46(11):163-173.
[19] 张芮, 刘文虎, 张立强, 等.基于宏基因组学解析高温大曲微生物群落与功能的异质性[J].酿酒科技, 2023(5):70-77.ZHANG R, LIU W H, ZHANG L Q, et al.Analysis of microbial community and functional heterogeneity of high-temperature Daqu based on metagenomics[J].Liquor-Making Science &Technology, 2023(5):70-77.
[20] WANG Y R, CAI W C, WANG W P, et al.Analysis of microbial diversity and functional differences in different types of high-temperature Daqu[J].Food Science &Nutrition, 2021,9(2):1003-1016.
[21] DENG L, MAO X, LIU D, et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Frontiers in Microbiology, 2020,11:588117.
[22] LIANG Y, LU Z M, SHI W, et al.Lentibacillus Daqui sp.nov., isolated from high-temperature Daqu, a starter for production of Chinese Jiang-flavour Baijiu[J].International Journal of Systematic and Evolutionary Microbiology, 2023,73(8):5962.
[23] DU Y K, XIN W, XIA Y, et al.Analysis of fermentation control factors on volatile compounds of primary microorganisms in Jiang-flavor Daqu[J].Journal of Food Biochemistry, 2022,46(10):e14277.
[24] 陈勇, 林涵瑞, 陈晓茹, 等.川派浓香型白酒大曲的典型产区差异性分析[J].中国酿造, 2024,43(11):34-40.CHEN Y, LIN H R, CHEN X R, et al.Difference analysis of Sichuan strong-flavor Baijiu Daqu in typical producing areas[J].China Brewing, 2024,43(11):34-40.
[25] REN H W, SUN Y F, YANG Y F, et al.Unraveling the correlations between microbial communities and metabolic profiles of strong-flavor Jinhui Daqu with different storage periods[J].Food Microbiology, 2024, 121:104497.
[26] ZHANG Y D, DING F, SHEN Y, et al.Characteristics of the microbiota and metabolic profile of high-temperature Daqu with different grades[J].World Journal of Microbiology and Biotechnology, 2022, 38(8):137.
[27] LI T, CAO W T, LI D N, et al.Metagenomic insights into quorum sensing-associated microbial profiling and its correlations with flavor compounds of Maotai-flavor liquor:A case study of stacking fermented grains[J].Food Research International, 2024,198:115324.