发酵肉制品是指在天然或人工调控的条件下,利用特定微生物或酶对生肉进行发酵而得到的产品[1],通过一系列的生化反应与物理变化使该产品具有独特的风味、较长的保质期、丰富的营养以及较高的益生菌含量,因此在全球范围内颇受消费者的喜爱[2]。发酵肉制品的传统生产工艺常受制于不可控的自然发酵条件,导致产品质量稳定性较差[3]。现代工业化生产中,通过添加发酵剂可有效改善这一问题。已有研究证实,乳酸菌、凝固酶阴性葡萄球菌、酿酒酵母及食用霉菌等已制成发酵剂被广泛应用于肉制品发酵[4-5]。值得注意的是,近年研究倾向于采用凝固酶阴性葡萄球菌与乳酸菌的协同发酵体系,通过分解脂肪促进风味的形成,还可以降低硝酸盐水平并产生过氧化氢酶,有助于产品形成诱人的色泽[6-7]。
为制备高质量的发酵剂,目前研究大多分为3步:探究发酵菌株适合的培养基构成;优化发酵条件达到高密度培养;利用真空冷冻干燥技术制备菌粉,最终形成高质量的发酵剂[8-11]。所在实验室前期已对清酒乳杆菌与肉葡萄球菌(Staphylococcus carnosus)复合发酵牛肉香肠进行了最佳制备工艺的探究,并对其进行了脂质代谢组学的分析[3]。目前关于乳酸菌的高密度培养及其冻干损伤的研究较多,而针对凝固酶阴性葡萄球菌的相关研究则相对不足。因此为制备目标菌株的发酵剂,以形成稳定的产品质量,本团队已完成对肉葡萄球菌最适培养基构成的探究工作。本研究的主要目的是优化肉葡萄球菌的培养条件及确定最适的发酵罐工艺,以此构建肉葡萄球菌的生长动力学模型,并对其抗冻能力进行初步的探究,明确菌株的冻干损伤,为后续采用相应的冻干保护剂降低菌株损伤提供参考,为制备高质量的发酵剂奠定理论基础。
1 材料与方法
1.1 菌株与试剂
1.1.1 菌株
肉葡萄球菌由河南农业大学肉品加工与质量控制实验室从云南腊肉中分离筛选得到,于-80 ℃条件下保藏。
1.1.2 试剂
氨水、氢氧化钠、氢氧化钾、磷酸氢二钾、葡萄糖、氯化钠、七水硫酸镁、无水乙醇,国药集团化学试剂有限公司;牛肉浸粉、大豆蛋白胨,青岛海博生物公司;微生物发酵用消泡剂,美仑生物公司;SYTO9绿色核酸染料、碘化丙啶红色荧光核酸染料,赛默飞世尔科技公司;Na+/K+-ATP酶活性检测试剂盒,南京建成生物工程研究所;电镜固定液,武汉赛维尔生物科技有限公司。
1.1.3 培养基
发酵培养基(g/L):葡萄糖3.21、大豆蛋白胨20.17、牛肉浸粉20.17、磷酸氢二钾5.63、氯化钠5、七水硫酸镁0.20。
平板计数琼脂(g/L):胰蛋白胨5.0、酵母浸粉2.5、葡萄糖1.0、琼脂15.0。
1.2 仪器与设备
BPG-9156A精密鼓风干燥箱,上海一恒科学仪器有限公司;KB240可编程低温培养箱,美国BINDER公司;LS-75LD高压灭菌锅,江阴滨江医疗设备有限公司;AE224电子分析天平,上海舜宇恒平有限公司;Synergy H1多功能微孔板检测仪,美国BioTek公司;Regulus8100超高分辨场发射扫描电子显微镜,日科学仪器有限公司;ZEISS SIGMA 300蔡司场发射扫描电镜,三本精密仪器有限公司;SP8 DIVE激光共聚焦显微镜,徕卡显微系统贸易有限公司;5 L发酵罐,保兴赛斯制药装备有限公司;SCIENTZ-30YG/A中试型硅油原位冻干机,宁波新芝冻干设备股份有限公司。
1.3 实验方法
1.3.1 菌种活化
将肉葡萄球菌接种于发酵培养基中,置于可编程低温培养箱中37 ℃恒温培养14 h。活化传代2次得到种子液用于后续实验。
1.3.2 活菌计数
将待测样品按10倍梯度系列稀释,选取合适的梯度区间,取0.1 mL该梯度下的菌液,滴加到平板计数培养基的表面,均匀涂布后置于37 ℃培养24 h,每一稀释度重复3皿,计活菌数(CFU/mL)。
1.3.3 培养条件优化
将种子液接种于含有125 mL发酵培养基的250 mL 锥形瓶中,在不同条件下分别培养14 h。考察温度(25、30、35、40、45 ℃)、初始pH(6、6.5、7、7.5、8)与接种量(1%、3%、5%、7%、9%,体积分数)对活菌数的影响。
1.3.4 发酵罐工艺优化
发酵罐装液量为50%,2.5 L;通入气体为无菌空气。发酵过程中,从0 h为起点,14 h为终点,每隔2 h取样,每次取样后立即平板计数。
转速优化:以已优化的培养条件为基础,在5 L发酵罐中,转速梯度设置为:100、200、300、400、500 r/min。
pH优化:以已优化的培养条件和参数为基础,在5 L发酵罐中,pH梯度设置为:7.0、7.5、8.0。
中和剂种类优化:以已优化的培养条件和参数为基础,在5 L发酵罐中,中和剂种类选取氨水、氢氧化钠、氢氧化钾。
1.3.5 非线性自回归(nonlinear autoregressive,NAR)神经网络构建菌体生长动力学模型
采用最优的发酵参数,同1.3.4节的取样方法。以取样数据为样本,首先使用Graphpad Prism 9软件,选用Fit spline/LOWESS中的Akima插值算法对样本数据进行补充,在相邻时间点间生成连续数据。再以扩充后的数据为训练样本,利用MATLAB R2022b的神经网络工具箱中NAR神经网络进行菌体生长动力学模型构建。设置训练数据占比为70%,测试数据和验证数据占比均为15%,隐藏层大小为10,时滞为2。
1.3.6 菌体抗冻干能力研究
1.3.6.1 预冻温度对肉葡萄球菌冻干存活率的影响
以预冻温度为-20、-30、-40、-80 ℃进行单因素试验,预冻时间为4 h,升华温度为-10 ℃。探究不同的预冻温度对肉葡萄球菌冻干存活率的影响。冻干存活率计算如公式(1)所示:
(1)
式中:A,冻干存活率,%;N前,冻干前的活菌数,CFU/mL;N后,冻干后的活菌数,CFU/mL。
1.3.6.2 形态学观察
采用GE等[12]的方法略作修改,首先使用1.5 mL离心管离心(10 000 r/min,10 min),弃上清液,并用无菌生理盐水洗涤2次。沿管壁缓缓注入电镜固定液直至注满离心管,在4 ℃下贮存过夜。固定后,离心去除上清液并洗涤,使用乙醇梯度脱水,然后进行临界点干燥。所有样品均喷金,通过场发射扫描电镜观察细菌样品的表面三维结构。
1.3.6.3 细胞膜完整性评价
采用TANG等[13]的方法并作修改,首先,将每种冻干细菌粉末在无菌生理盐水中再水化,洗涤2次,然后重悬于无菌生理盐水中。然后,将SYTO9绿色核酸染料和碘化丙啶红色荧光核酸染料等体积混合。向稀释的悬浮样品中加入总共10 μL混合染料,并在室温下孵育20 min。随后,将染色的细菌悬浮液滴添加到载玻片上,并使用激光共聚焦显微镜观察。
1.3.6.4 细胞膜流动性评价
采用LI等[14]的方法略作修改。将冻干菌粉复溶后,用无菌生理盐水清洗菌体2次,10 000 r/min离心10 min,重悬在无菌生理盐水中,加入Laurdan膜透性荧光探针至终浓度为10 μmol/L,30 ℃避光孵育30 min,以未用荧光染料处理的细胞作为对照,测定荧光强度,广义荧光偏振表征样细胞膜流动性。
1.3.6.5 Na+/K+-ATP酶活性
为分析评估冻干环境对菌株酶活性的影响,使用Na+/K+-ATP酶活性试剂盒检测酶活性。
1.4 数据处理
实验结果用“平均值±标准差”表示,所有实验重复3次。使用SPSS 26软件对试验数据进行显著性分析,P<0.05为显著。Origin 2024、MATLAB R2022b及Graphpad Prism 9软件用于绘制图表及模型构建。
2 结果与分析
2.1 培养条件对最大活菌数的影响
从图1可知,接种量、初始pH、温度对肉葡萄球菌的最大活菌数均有一定的影响,并且通过对比可以发现其中初始pH对活菌数的影响最为显著。不同菌株的生长速度以及对营养物质的利用效率不同,因此对菌株的接种量进行探究。当接种量过高时,菌体利用营养物质速度较快,代谢产物大量积累而抑制菌体的增殖[15]。而当接种量过低时,菌株可能生长较为缓慢。由图1可知,接种量1%为最佳,随着接种量的增加,最大活菌数逐步下降。显然这株肉葡萄球菌的生长速度较快,1%的接种量下可达最大活菌数。
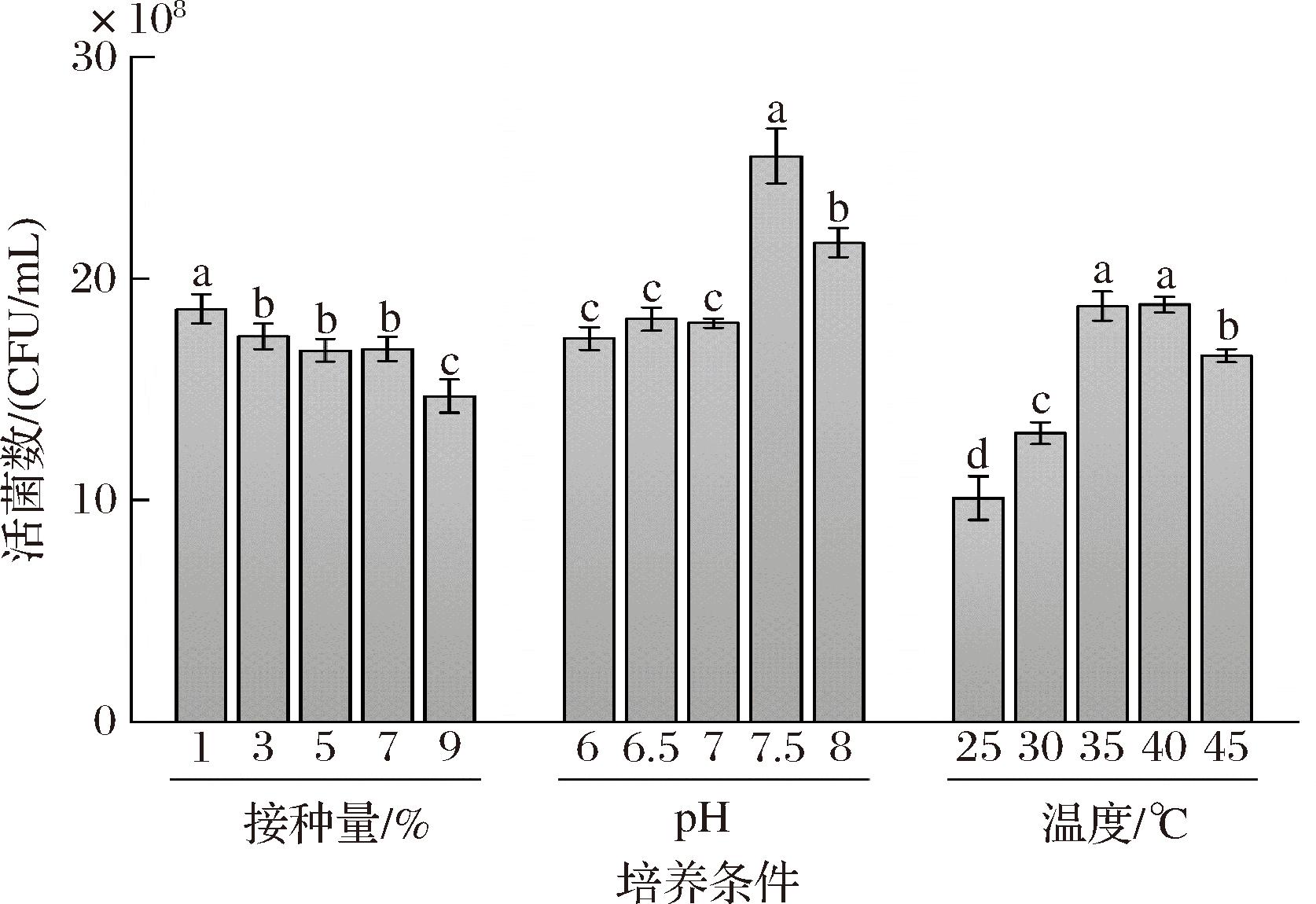
图1 培养条件对肉葡萄球菌活菌数的影响
Fig.1 Effect of culture conditions on the viable count of S.carnosus
注:不同小写字母表示差异显著(P<0.05)(下同)。
合适的pH有利于保持微生物细胞膜的完整性,过酸或过碱均会对菌体生长产生不利影响[8]。图1所示pH试验中,随着pH的升高,活菌数呈现先上升后下降趋势,初始pH值为7.5时活菌数最高,由此表明肉葡萄球菌在弱碱性的环境中生长良好。此外,不同温度下培养的菌株有不同的蛋白活力、酶活性以及细胞膜的流动性,影响着菌株的生长代谢[16]。由图1可知,在35和40 ℃时活菌数最高,且两者之间无显著性差异;当温度继续升高后,活菌数则呈现出下降的趋势。综上,肉葡萄球菌最佳培养条件为:接种量1%、初始pH值为7.5、温度35~40 ℃,优化后的最大活菌数可达2.53×109 CFU/mL。
2.2 发酵罐工艺优化对最大活菌数的影响
在对培养条件的优化的基础上,使用发酵罐对肉葡萄球菌进行扩大培养。分别对转速、恒定pH以及中和剂的种类进一步优化。MUSTAFA等[17]研究发现,适合目标菌株的转速可提高菌株的生长速率与营养物质的利用速率。当转速过低时,菌体无法充分利用罐中营养物质和氧气且易沉积在发酵罐底部[11];而转速过高则对菌体造成机械损伤[18],产生较大的消泡压力,在实际肉葡萄球菌发酵过程中,300 r/min时就需要消泡剂来应对罐中产生的气泡。由图2可知,随着转速的升高,最大活菌数逐步上升,在400 r/min为最大。当转速上升至500 r/min时,最大活菌数有所下降,虽与400 r/min无显著性差异,但可能因搅拌过快造成菌体机械损伤,且高转速下需多次添加消泡剂,增加了发酵成本。因此综合考虑选择转速400 r/min进行后续实验。
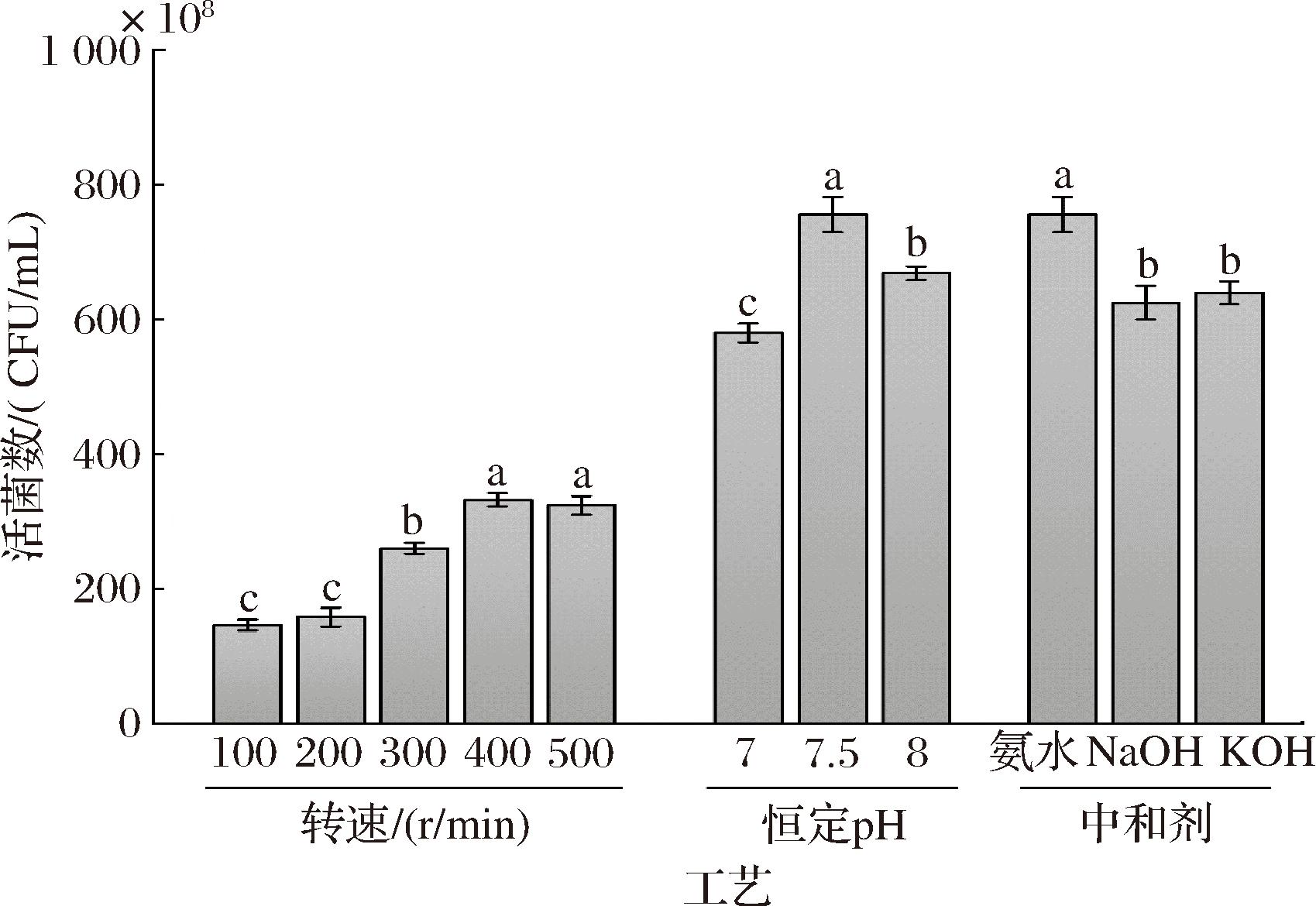
图2 发酵罐工艺对肉葡萄球菌活菌数的影响
Fig.2 Effect of fermentation tank technology on the viable count of S.carnosus
控制罐内pH可以为菌株生长代谢提供稳定的环境,降低酸抑制,延长对数生长期,从而使活菌数增高[19]。由图2可知,探究转速阶段并不控制pH,与其相比,恒定pH阶段整体最大活菌数明显上升。且在pH 7.5时肉葡萄球菌的活菌数最大,说明此时的pH最适合肉葡萄球菌的生长。工业发酵中常用氢氧化钠、氢氧化钾和氨水来作为中和剂,钠离子具有调节渗透压平衡等作用,钾离子与微生物体内磷的传递有关,而铵根离子又能够补充微生物生长所需的无机氮源[20]。氢氧化钠与氢氧化钾对肉葡萄球菌的最大活菌数来说并无显著性差异,氨水组活菌数最高。也印证了前期筛选肉葡萄球菌最适营养需求实验结果,该菌对氮源十分敏感,可能是氨水在发酵过程不仅作为中和剂,还起到了补充氮源作用。综上,肉葡萄球菌的最优发酵参数为转速400 r/min、恒定pH 7.5,中和剂为氨水,优化后最大活菌数可达7.56×1010 CFU/mL。经培养条件和发酵罐工艺优化后,活菌数是优化前的40倍。
2.3 NAR神经网络构建菌体生长动力学模型
微生物生长曲线通常是非线性的,可能包含多个阶段(如滞后期、对数期、稳定期和衰亡期),并且数据点可能稀疏或不均匀分布。Akima插值可以用于减少实验数据中的噪声、平滑曲线、填补缺失数据,或者在稀疏数据点之间生成更连续的曲线[21]。在实际的发酵过程中,本实验每隔2 h进行1次取样,所获得的数据样本数量无法满足神经网络训练的需求。由于数据量偏少,往往难以获得性能较优的模型。因此在对数据进行神经网络训练前,利用Akima插值算法对样本进行数据量扩充以达到较好的训练效果。
图3所示为肉葡萄球菌在最优的培养条件和发酵参数下所构建的菌体生长动力学模型。传统的微生物生长模型,如Logistic方程和Monod方程,也能够满足模型构建的需求[22]。然而,NAR神经网络具有自回归结构,它能够精准捕捉时间序列数据中的动态依赖关系,直接从实验数据中进行学习,无需预先假设具体的动力学方程。且多项研究证实神经网络所构建的模型均有较好的拟合能力和较高的预测精度[23]。由表1可知,本实验所拟合的模型相关系数R=1,模型对所有数据均有解释能力,测试集的均方误差(mean squared error,MSE)=0.091 9,具有较高的精度,说明此模型可以较好地解释肉葡萄球菌的活菌数随时间的变化情况。
表1 数据集分类及模型拟合效果
Table 1 Dataset classification and model fitting performance

数据集分类样本数据占比/%MSER训练700.044 51验证150.234 61测试150.091 91
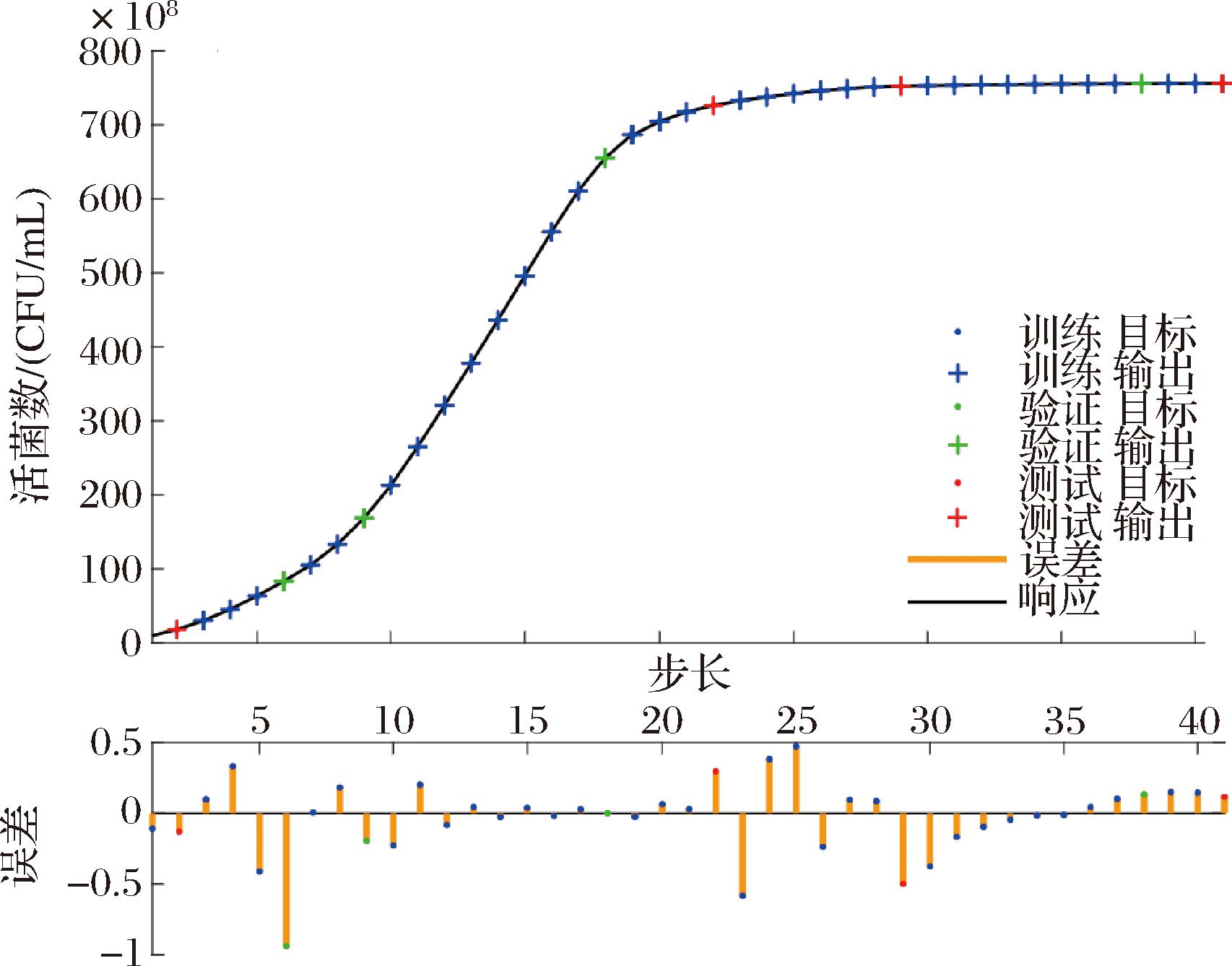
图3 NAR神经网络构建菌体生长动力学模型
Fig.3 NAR network for constructing microbial growth kinetic models
2.4 菌株的抗冻干能力检测
真空冷冻干燥对细胞的损伤主要体现在细胞膜破坏、酶活性改变以及DNA双螺旋结构受损[24](图4),进而造成菌株冻干存活率较低。冰晶的大小与冷却速率呈反比,决定着对菌株的损伤程度。当冷却速度过慢时,细胞可能因水分过度流失而发生收缩;相反,如果冷却速度过快,细胞内外的水分子可能会迅速结冰,形成冰晶。这些冰晶可能会穿透细胞结构,对细胞造成严重的物理性损伤[25]。为减小冰晶对菌体的损伤,需要对不同的预冻温度进行筛选,由图5可知,随着预冻温度的降低,肉葡萄球菌冻干存活率呈上升态势,-80 ℃下的冻干存活率最高为19.9%,可能是因为-80 ℃下的冰晶形成速度对肉葡萄球菌的损伤最小。但此时的冻干存活率无法满足商业发酵剂的要求。为了明确冻干对细胞造成的损伤位点和损伤程度,本文接下来对冻干前后细胞膜的完整性和流动性、酶活性进行了探究。同时,利用扫描电镜观察了菌体冻干前后表面的三维立体结构。研究结果可为后续选用相应冻干保护剂提供依据。
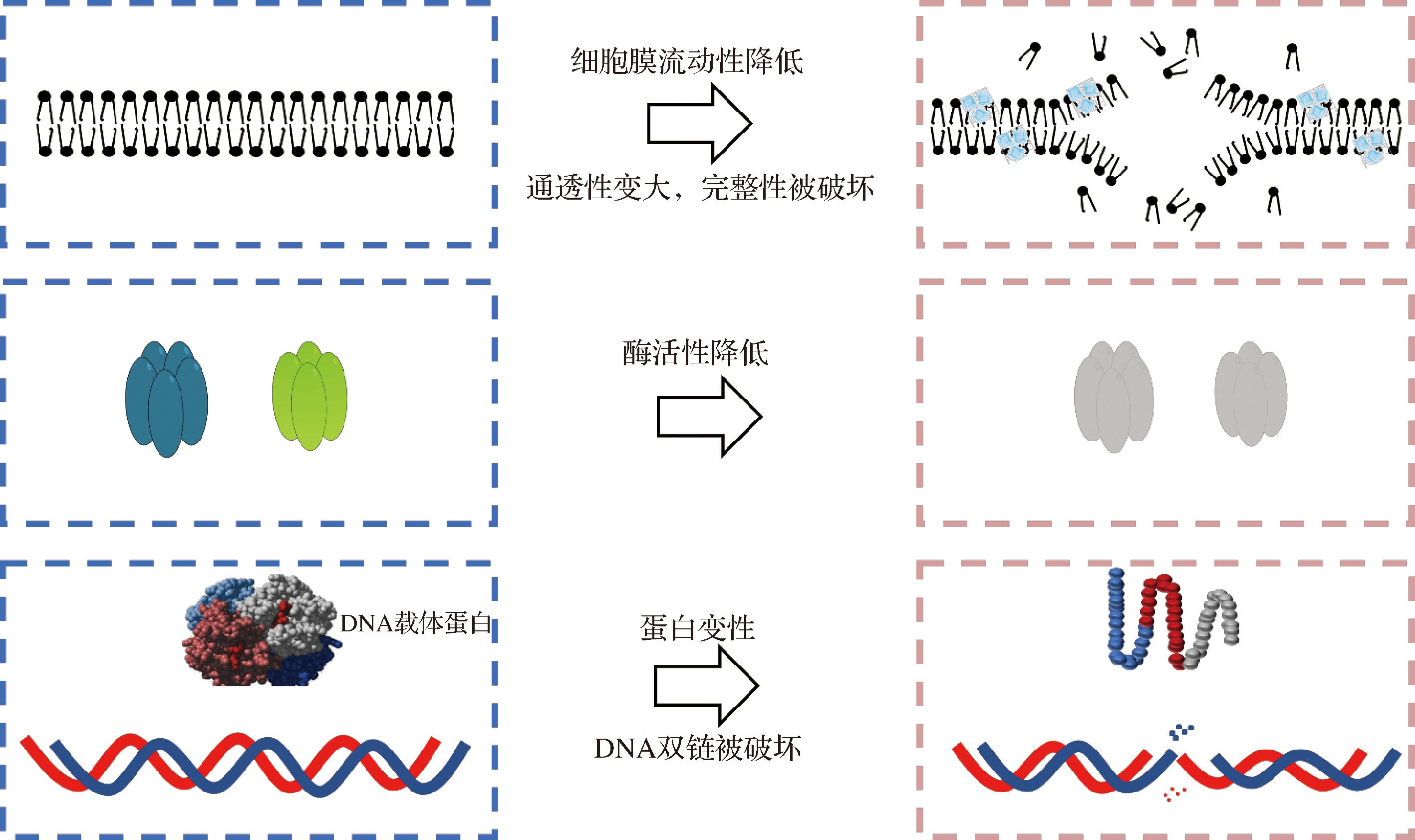
图4 冷冻干燥对细胞造成的损伤
Fig.4 Cell damage caused by freeze-drying
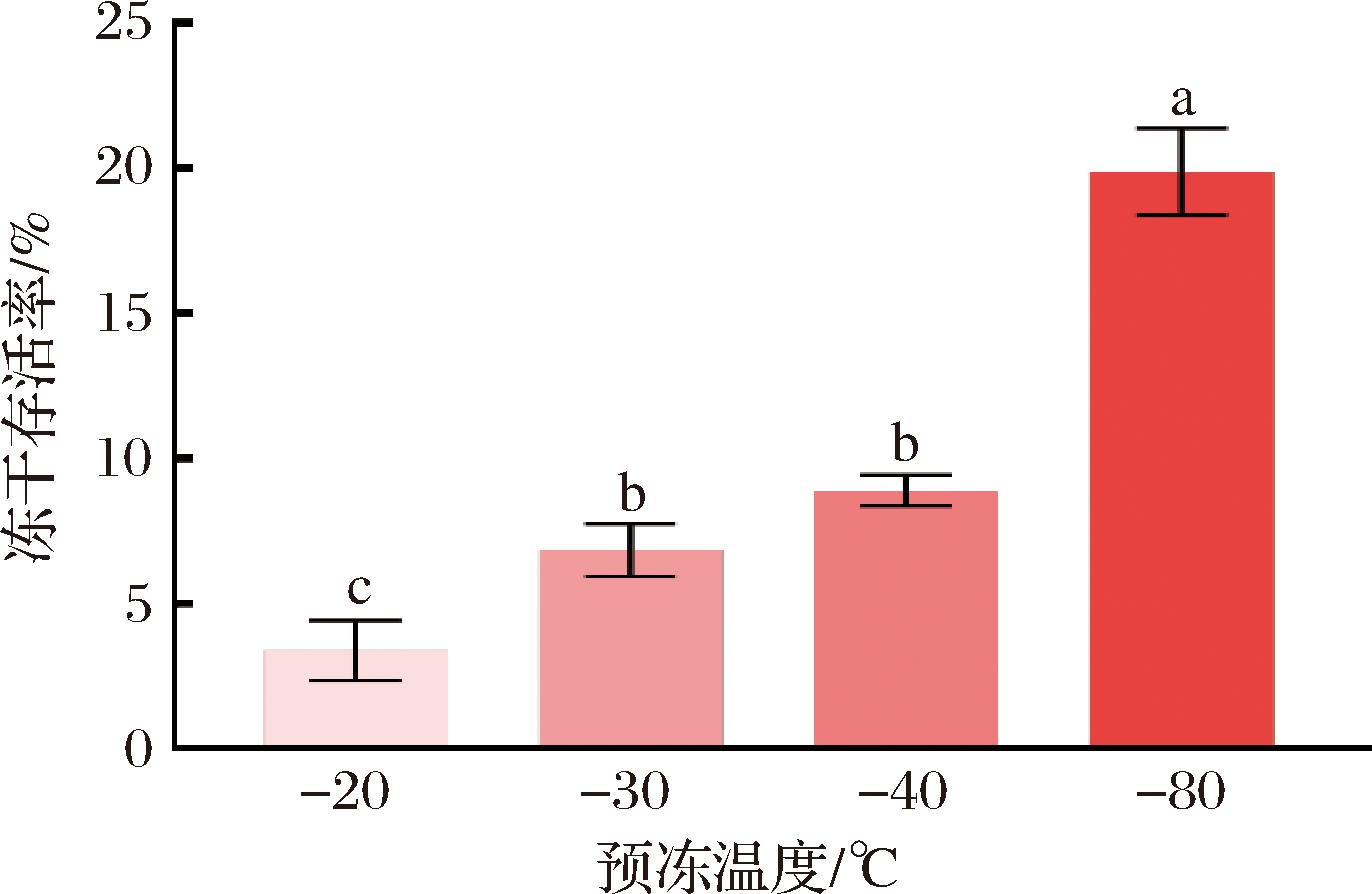
图5 预冻温度对肉葡萄球菌冻干存活率的影响
Fig.5 Effect of pre-freezing temperature on freeze-drying survival rate of S.carnosus
2.4.1 细胞膜完整性与流动性及膜上Na+/K+-ATP酶活性检测
细胞膜主要由磷脂、蛋白质和糖类等物质组成,可隔绝菌体与外部环境,是保护菌体的重要屏障。利用SYTO9绿色核酸和碘化丙啶红色荧光核酸混合染料对冻干前后的细胞进行染色,从染色原理可知绿色荧光代表细胞膜完整性较好,活力较强的细胞;红色荧光代表细胞膜完整性遭到破坏的细胞[12]。图6-a~图6-f显示正常状态下细胞呈明亮的绿色荧光且占绝大多数,只存在极少数的红色荧光,说明此时的肉葡萄球菌细胞膜完整,细胞活力较高。而冻干处理后的绿色荧光数量急剧下降,明显少于红色荧光的数量。图6-e显示,存活的细胞中只有极少部分呈现明亮的绿色荧光,大部分绿色荧光较微弱,说明存活的细胞可能活力也较弱。这些结果表明,真空冷冻干燥会破坏肉葡萄球菌细胞膜完整性,降低细胞活力。可能是预冻过程中游离水形成的冰晶对细胞膜造成溶质损伤和机械损伤[26]。通常情况下,细胞内外液体冰点不同,细胞外液先于内液冻结,造成胞内外溶质差升高,电解质浓缩,造成溶质损伤[27]。同时,水分冻结时产生的机械力会刺破细胞膜,破坏细胞膜完整性,降低细菌的生存能力[28-29]。
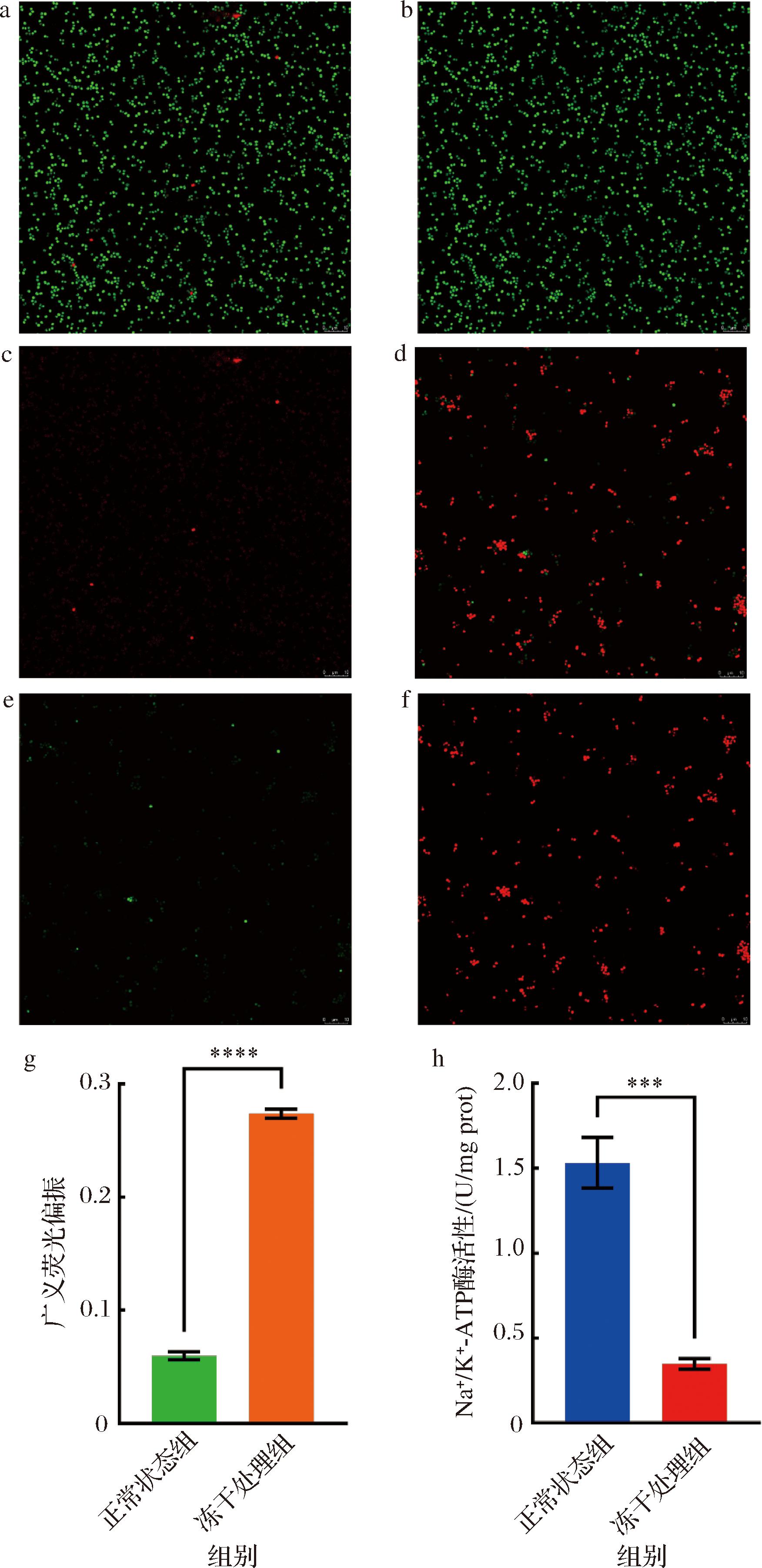
a-正常状态细菌活死染色图;b-正常状态活菌染色图;c-正常状态死菌染色图;d-冻干处理后细菌活死染色图;e-冻干处理后活菌染色图;f-冻干处理后死菌染色图;g-冻干前后菌体细胞膜广义荧光偏振;h-冻干前后菌体Na+/K+-ATP酶活性
图6 冻干对肉葡萄球菌细胞膜及Na+/K+-ATP酶活性的影响
Fig.6 Effect of freeze-drying on membrane and Na+/K+-ATPase activity of S.carnosus
注:绿色荧光代表活菌,红色荧光代表死菌;a~f图中细菌放大倍数为800倍;***表示P<0.001,****表示P<0.000 1。
磷脂双分子层的流动性是其关键生理特征之一,对温度敏感,受不饱和脂肪酸比例调控[30]。这种动态特性赋予细胞感知并响应外界环境变化的能力,这些变化涵盖温度波动、酸碱度改变以及渗透压平衡等物理化学参数方面。当环境信号被识别后,细胞可通过启动特定基因转录程序,诱导适应性代谢反应,从而实现对外界环境的动态适应[31]。有研究人员在对冻干后的微生物细胞膜进行检测时,观察到冻干后的微生物细胞膜1,6-二苯基-1,3,5-己三烯、荧光偏振、各向异性和微观黏度的值显著增加,表明细胞膜的流动性降低[32]。因此本文利用荧光偏振对细胞膜的流动性进行表征,如图6-g所示,2组之间的差异性极显著,冻干后细胞膜的荧光偏振增加,说明细胞膜流动性下降,可能是冻干环境使细胞膜中不饱和脂肪酸与饱和脂肪酸的比例降低所致。刘玥[33]利用GC-MS检测膜上脂肪酸变化,发现无保护剂状态下木糖葡萄球菌在真空冷冻干燥后,其不饱和脂肪酸/饱和脂肪酸比例较低。菌株处于正常状态下时,脂酰基链间可以进行布朗运动,此时分子排列较为疏松,磷脂双层保持相对无序的液晶态。而冷冻干燥时,细胞膜逐渐趋于凝胶态,这种刚性状态是由于低温环境造成磷脂分子酰基链间产生了疏水间力,导致细胞膜流动性下降,而不饱和脂肪酸含量增加有利于细胞膜对液晶态的维持,提高细胞膜的流动性,增强对恶劣环境的适应能力[24,27,34]。
冻干过程中的解析干燥涉及去除细胞中的结合水,可能会导致细胞某些组分功能的丧失[35]。Na+/K+-ATP酶广泛分布于细胞膜系统中,在产生跨膜电位和通过交换钾离子和氢离子维持pH梯度中起着至关重要的作用[24,36]。图6-h所示结果表明,冻干前菌株的酶活性为1.53 U/mg prot,冻干后菌株酶活性大幅度降低至仅为0.35 U/mg prot,酶活性降低77%,组间差异性显著。GE等[12]研究发现,真空冷冻干燥首先会破坏细胞膜的完整性和流动性,随之破坏细胞膜上酶的结构或活性,导致细胞代谢能力和活力下降而死亡。冻干导致肉葡萄球菌该酶活性大幅度降低,进而破坏其pH动态平衡,这可能也是导致该菌株死亡的原因之一。Na+/K+-ATP酶活性的维持或提高被认为是提高菌株细胞膜完整性和增强其抗冻干能力的重要因素[37]。
鉴于冻干环境对肉葡萄球菌的细胞膜和酶类造成了较为严重的损伤,后续实验中冻干保护剂可能采用海藻糖和脱脂乳,海藻糖可取代极性分子周围的水,显著抑制冰晶的形成,其特有的高黏度和低流动性保护了细胞膜和蛋白质结构[38]。脱脂乳可包裹菌体,形成对菌体的保护层,并且其中的钙离子固定酶类,可维持酶活性和降低冰晶刺穿细胞膜的风险[33]。
2.4.2 菌体冻干前后的微观结构
肉葡萄球菌冻干前后微观结构如图7所示,图7-a显示菌体呈球形,表面光滑平整,并无形态损伤迹象。图7-b可见,与图7-a中菌体形态相比,部分菌体出现褶皱或塌陷情况,细胞变形严重且相互堆叠,细胞内物质泄露。说明真空冷冻干燥对肉葡萄球菌造成严重的形态损伤。冻干保护剂可以在一定程度上维持菌体的形态,降低在冻干过程中的形态损伤[12]。后续试验可能还需要加入可以维持菌体结构的物质,如甘露醇,作为菌株常见的冻干保护剂,其既可以作为冰晶结晶的促进剂,又可以作为细菌结构的稳定剂,有效防止菌体应变坍塌[12]。

a-冻干前菌体形态;b-冻干后菌体形态
图7 菌体形态学观察
Fig.7 Bacterial morphological observation
3 结论
本研究对肉葡萄球菌培养条件和发酵工艺条件进行了优化,确定最佳培养条件为:接种量1%、初始pH 7.5、温度35~40 ℃,活菌数可达2.53×109 CFU/mL;发酵最佳工艺条件为转速400 r/min、恒定pH 7.5、中和剂种类为氨水,活菌数可达7.56×1010 CFU/mL。整体优化后活菌数是优化前的40倍。以最优条件为基础,利用NAR神经网络构建菌体生长动力学模型,该模型相关系数R=1,MSE=0.091 9,模型可以较好地解释肉葡萄球菌的生长动态情况。随后又对肉葡萄球菌的抗冻能力展开初步探索,菌株最优的预冻温度为-80 ℃,此温度下冻干存活率为19.9%,Na+/K+-ATP酶活性降低77%,激光共聚焦与荧光偏振结果表明细胞膜的完整性、流动性受到较大损伤,扫描电镜下菌体的三维立体结构遭到破坏。基于这些损伤位点,下一步可能采用冻干保护剂为脱脂乳、海藻糖、甘露醇,从而提高菌株冻干存活率,以期为高质量发酵剂的制备奠定基础。
[1] CAO Q F, FAN X K, XU J, et al.Insights into the molecular mechanisms of lipid metabolism of air-dried goose on the formation of flavor substances by co-inoculation of lactic acid bacteria and Staphylococcus based on GC-MS and lipidomics[J].Food Chemistry, 2025, 463:141388.
[2] ZHANG Q H, SHEN J L, MENG G G, et al.Selection of yeast strains in naturally fermented cured meat as promising starter cultures for fermented cured beef, a traditional fermented meat product of northern China[J].Journal of the Science of Food and Agriculture, 2024, 104(2):883-891.
[3] LI X, ZHAO G M, ZHENG Y Y, et al.Effects of single fermentation of Lactobacillus sakei and compound fermentation with Staphylococcus carnosus on the metabolomics of beef sausages[J].Food Chemistry, 2025, 464:141728.
[4] BINTSIS T.Lactic acid bacteria as starter cultures:An update in their metabolism and genetics[J].AIMS Microbiology, 2018, 4(4):665-684.
[5] KAVEH S, HASHEMI S M B, ABEDI E, et al.Bio-preservation of meat and fermented meat products by lactic acid bacteria strains and their antibacterial metabolites[J].Sustainability, 2023, 15(13):10154.
[6] ![]() I, MARKOV K,
I, MARKOV K, ![]() D, et al.Identification and characterization of potential autochthonous starter cultures from a Croatian “brand” product “Slavonski kulen”[J].Meat Science, 2011, 88(3):517-524.
D, et al.Identification and characterization of potential autochthonous starter cultures from a Croatian “brand” product “Slavonski kulen”[J].Meat Science, 2011, 88(3):517-524.
[7] WANG D B, ZHAO L H, SU R N, et al.Effects of different starter culture combinations on microbial counts and physico-chemical properties in dry fermented mutton sausages[J].Food Science &Nutrition, 2019, 7(6):1957-1968.
[8] 周宁萍, 蒋雪, 裴琪, 等.红酸汤源植物乳杆菌NCU001929的高密度培养条件研究[J].食品与发酵工业, 2024, 50(21):36-44.ZHOU N P, JIANG X, PEI Q, et al.High-density culture conditions of Lactobacillus plantarum NCU001929 isolated from red sour soup[J].Food and Fermentation Industries, 2024, 50(21):36-44.
[9] 陈娟, 康文丽, 侯爱香, 等.植物乳植杆菌高密度培养及菌粉制备技术研究进展[J].中国乳品工业, 2024, 52(10):64-68.CHEN J, KANG W L, HOU A X, et al.Research progress on high density culture and powder preparation technology of Lactiplantibacillus plantarum[J].China Dairy Industry, 2024, 52(10):64-68.
[10] 高欣伟, 崔树茂, 唐鑫, 等.长双歧杆菌的最适底物解析和高密度发酵工艺优化[J].食品与发酵工业, 2021, 47(19):12-20.GAO X W, CUI S M, TANG X, et al.Optimization of substrate in high-density fermentation of Bifidobacterium longum[J].Food and Fermentation Industries, 2021, 47(19):12-20.
[11] 马琳. 短双歧杆菌高密度发酵工艺的优化[D].呼和浩特:内蒙古农业大学, 2024.MA L.Optimization of high-density fermentation technology of Bifidobacterium brevis[D].Hohhot:Inner Mongolia Agricultural University, 2024.
[12] GE S T, HAN J R, SUN Q Y, et al.Optimization of cryoprotectants for improving the freeze-dried survival rate of potential probiotic Lactococcus lactis ZFM559 and evaluation of its storage stability[J].LWT, 2024, 198:116052.
[13] TANG M M, LIU F, WANG Q, et al.Physicochemical characteristics of ginger essential oil nanoemulsion encapsulated by zein/NaCas and antimicrobial control on chilled chicken[J].Food Chemistry, 2022, 374:131624.
[14] LI H P, ZHAO P, ZHANG S H, et al.Protective effect of polysaccharides from Pholiota nameko on Lactobacillus casei ATCC 334 subjected to freeze-drying[J].LWT, 2019, 115:108463.
[15] 李娜. 植物乳杆菌ZJ316的高密度发酵及高活性菌制剂的初步研究[D].南宁:广西大学, 2020.LI N.Preliminary study on high-density fermentation and high-activity bacterial preparation of Lactobacillus plantarum ZJ316[D].Nanning:Guangxi University, 2020.
[16] 左梦楠, 刘伟, 张菊华, 等.发酵乳杆菌BLHN3的高密度培养优化[J].食品与机械, 2022, 38(12):181-189.ZUO M N, LIU W, ZHANG J H, et al.Optimization of high density culture of Lactobacillus fermentum BLHN3[J].Food &Machinery, 2022, 38(12):181-189.
[17] MUSTAFA S M, CHUA L S, ALI EL-ENSHASY H, et al.Kinetic profile and anti-diabetic potential of fermented Punica granatum juice using Lactobacillus casei[J].Process Biochemistry, 2020, 92:224-231.
[18] IWANICKI N S, MASCARIN G M, MORENO S G, et al.Growth kinetic and nitrogen source optimization for liquid culture fermentation of Metarhizium robertsii blastospores and bioefficacy against the corn leafhopper Dalbulus maidis[J].World Journal of Microbiology &Biotechnology, 2020, 36(5):71.
[19] 吴军林,柏建玲,莫树平,等.乳酸菌R8高密度培养的发酵工艺研究[J].现代食品科技, 2018, 34(2):164-170, 251.WU J L, BAI J L, MO S P, et al.Optimization of culture conditions and medium of lactic acid bacteria R8 cultured in high density fermentation[J].Modern Food Science and Technology, 2018, 34(2):164-170, 251.
[20] CHEN X J, WU X F, JIANG S T, et al.Influence of pH and neutralizing agent on anaerobic succinic acid production by a Corynebacterium crenatum strain[J].Journal of Bioscience and Bioengineering, 2017, 124(4):439-444.
[21] AKIMA H.A new method of interpolation and smooth curve fitting based on local procedures[J].Journal of the ACM, 1970, 17(4):589-602.
[22] 赖长龙, 曹余, 杨玉, 等.植物乳杆菌发酵动力学及高密度培养研究[J].食品与发酵工业, 2022, 48(20):137-144.LAI C L, CAO Y, YANG Y, et al.Fermentation kinetics and high density culture studies of Lactobacillus plantarum[J].Food and Fermentation Industries, 2022, 48(20):137-144.
[23] 游云, 黄晓霞, 肖斯立, 等.反向传播-人工神经网络在辐照黑椒牛肉品质预测中的应用[J].食品科学, 2024, 45(8):228-237.YOU Y, HUANG X X, XIAO S L, et al.Application of backpropagation-artificial neural network in quality prediction of irradiated black pepper beef[J].Food Science, 2024, 45(8):228-237.
[24] GE S T, HAN J R, SUN Q Y, et al.Research progress on improving the freeze-drying resistance of probiotics:A review[J].Trends in Food Science &Technology, 2024, 147:104425.
[25] RAJU R, BRYANT S J, WILKINSON B L, et al.The need for novel cryoprotectants and cryopreservation protocols:Insights into the importance of biophysical investigation and cell permeability[J].Biochimica et Biophysica Acta (BBA)-General Subjects, 2021, 1865(1):129749.
[26] WANG H, DUAN X, DUAN L L, et al.Mutual transformation of the water binding state and moisture diffusion characteristics of Chinese yams during microwave freeze drying[J].Drying Technology, 2021, 39(1):66-76.
[27] 鄂晶晶.培养条件对植物乳植杆菌LIP-1冷冻干燥存活率的影响及其内在机制的研究[D].呼和浩特:内蒙古农业大学, 2022.E J J.Study on the effects of culture conditions on the survival rate of Lactiplantibacillus plantarum LIP-1 during freeze-drying and its intrinsic mechanisms[D].Hohhot:Inner Mongolia Agricultural University, 2022.
[28] WANG G Q, CHEN P Y, YU X Q, et al.C18:1 Improves the freeze-drying resistance of Lactobacillus plantarum by maintaining the cell membrane[J].ACS Applied Bio Materials, 2020, 3(8):4933-4940.
[29] CHENG Z Y, YAN X, WU J Y, et al.Effects of freeze drying in complex lyoprotectants on the survival, and membrane fatty acid composition of Lactobacillus plantarum L1 and Lactobacillus fermentum L2[J].Cryobiology, 2022, 105:1-9.
[30] 王昊乾, 张静雯, 杨雄洲, 等.抗氧化肽在真空冷冻干燥过程中对乳双歧杆菌Probio-M8的保护作用[J].中国食品学报, 2023, 23(10):32-40.WANG H Q, ZHANG J W, YANG X Z, et al.Protective effect of antioxidant peptides on Bifidobacterium animalis subsp. lactis Probio-M8 during vacuum freeze-drying[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(10):32-40.
[31] LOS D A, MURATA N.Membrane fluidity and its roles in the perception of environmental signals[J].Biochimica et Biophysica Acta (BBA)-Biomembranes, 2004, 1666(1-2):142-157.
[32] LI B K, TIAN F W, LIU X M, et al.Effects of cryoprotectants on viability of Lactobacillus reuteri CICC6226[J].Applied Microbiology and Biotechnology, 2011, 92(3):609-616.
[33] 刘玥. 木糖葡萄球菌干粉保护剂的研究及其在发酵香肠中的应用[D].扬州:扬州大学, 2020.LIU Y.Research on dry powder protective agent of Staphylococcus xylosus and its application in fermented sausage[D].Yangzhou:Yangzhou University, 2020.
[34] E J J, CHEN J, CHEN Z C, et al.Effects of different initial pH values on freeze-drying resistance of Lactiplantibacillus plantarum LIP-1 based on transcriptomics and proteomics[J].Food Research International, 2021, 149:110694.
[35] SCHWAB C, VOGEL R, G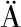 NZLE M G.Influence of oligosaccharides on the viability and membrane properties of Lactobacillus reuteri TMW1.106 during freeze-drying[J].Cryobiology, 2007, 55(2):108-114.
NZLE M G.Influence of oligosaccharides on the viability and membrane properties of Lactobacillus reuteri TMW1.106 during freeze-drying[J].Cryobiology, 2007, 55(2):108-114.
[36] ZHEN N, ZENG X Q, WANG H J, et al.Effects of heat shock treatment on the survival rate of Lactobacillus acidophilus after freeze-drying[J].Food Research International, 2020, 136:109507.
[37] CHEN B Y, WANG X Y, LI P Z, et al.Exploring the protective effects of freeze-dried Lactobacillus rhamnosus under optimized cryoprotectants formulation[J].LWT, 2023, 173:114295.
[38] CARVALHO A L, CARDOSO F S, BOHN A, et al.Engineering trehalose synthesis in Lactococcus lactis for improved stress tolerance[J].Applied and Environmental Microbiology, 2011, 77(12):4189-4199.