肝组织通常为肥胖导致的慢性炎症表现器官,并且非酒精性脂肪肝病(non-alcoholic fatty liver, NAFLD)的发展也常与肥胖相关[1]。现如今人们被过剩的营养所包围,因此与脂质异位积累相关的肥胖成为NAFLD的一个重要危险因素[2]。在肥胖NAFLD患者的肝脏中检测到肝脏3-羟基-3-甲基戊二酰单酰辅酶A(3-hydroxy-3-methylglutaryl monocoenzyme A,HMG-CoA)还原酶的信使核糖核酸(messenger RNA, mRNA)表达显著增加[3],在非肥胖的NAFLD患者中也发现胆固醇生物合成的增高。NAFLD在机体内受多条信号通路的调节,包括能量代谢、脂肪酸氧化、脂肪酸合成、胆固醇合成、氧化应激以及细胞凋亡等。腺苷酸活化蛋白激酶(AMP-activated protein kinase, AMPK)通路受细胞内单磷酸腺苷/三磷酸腺苷(adenosine monophosphate/adenosine triphosphate, AMP/ATP)比值变化影响,进而能够对能量产生、代谢起到控制作用,是维持能量稳态的关键传感器,是控制脂质和能量代谢的最重要信号之一[4]。
食物蛋白质的消化会产生链长较短的肽段,即为生物活性肽,其抗氧化、降血压等生理作用已经得到广泛研究。近年来,人们越来越关注食物蛋白质中提取的生物活性肽,并探索将其作为一种天然安全的NAFLD预防和管理策略。研究表明,生物活性肽可以防止脂质堆积,调节食欲和能量代谢,并具有抗炎和抗氧化特性,使其有希望成为替代化学药物的一种缓解和干预NAFLD的天然代替品[5]。新兴的天然蛋白质及其肽的降脂效应引起了许多研究者的重视,豌豆肽的抗糖尿病活性已在动物模型和临床试验中得到证明:WEI等[6]使用经诱导的2型糖尿病小鼠为模型、豌豆低聚肽为研究对象进行研究,结果表明豌豆低聚肽显著降低了模型动物的肝脏脂肪沉积、血脂和血糖。POWNALL等[7]发现豌豆蛋白抗氧化肽,并使用不同的酶对制备豌豆抗氧化肽的方法进行了优化,最终使用碱性酶、风味酶和胃蛋白酶制备的豌豆肽具有更好地清除自由基的能力,且小分子质量的肽效果更好[8]。
综上,本研究将豌豆蛋白作为研究对象,进行低聚肽制备及相关检测,通过对HMG-CoA还原酶抑制活性测定、细胞NAFLD模型的缓解作用评价探究豌豆低聚肽的NAFLD缓解活性,并通过Western blot检测研究豌豆低聚肽对NAFLD的缓解作用机制,为开发新型、安全有效的非酒精性脂肪肝缓解和干预替代物奠定理论基础。
1 材料与方法
1.1 材料与试剂
豌豆蛋白,烟台东方蛋白科技有限公司;HMG-CoA还原酶抑制剂筛选试剂盒,BioVision;人肝肿瘤细胞(HepG2细胞),中国医学科学院肿瘤医院(北京);总甘油三脂(triglyceride,TG)测定试剂盒、总胆固醇(total cholesterol,TC)测定试剂盒,南京建成生物工程研究所;Tris-甘氨酸转膜缓冲液(Tris-glycine transfer buffer)、Tris-甘氨酸SDS-PAGE电泳缓冲液,塞维尔公司;AMPK Alpha 1 Monoclonal antibody试剂、乙酰辅酶A羧化酶(acetyl-CoA carboxylases, ACC) Monoclonal antibody试剂等信号蛋白试剂,Affinity 公司。
1.2 仪器与设备
HERAcell150i-CO2细胞培养箱,美国Thermo Fisher Scientific公司;多功能酶标仪,Molecular Devics SpectraMax i3;Western-blot套装,美国伯乐(Bio- Rad Laboratories)公司;HPLC-MS/MS 8060高效液相色谱-串联质谱仪,日本Shimadzu公司。
1.3 实验方法
1.3.1 豌豆低聚肽的制备
豌豆蛋白(1 g)悬浮于5 mL蒸馏水中,50 ℃合并和乳化。使用碱性蛋白酶和中性蛋白酶在pH值为8的条件下,在50 ℃下启动酶解4 h,后95 ℃、15 min 终止水解。得到的水解产物以3 000 r/min离心15 min,上清液依次通过分子质量为10、1 kDa的陶瓷膜,得到含有低分子质量寡肽的渗透液[1]。用纳滤法去除液体中的微量盐和游离氨基酸。将纯化液进行低温浓缩,当浓度接近30 Brix时,进行30 min脱色,再进行喷雾干燥获得豌豆低聚肽。
1.3.2 豌豆低聚肽基础理化性质分析
1.3.2.1 基础理化成分测定
参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》、GB 5009.4—2016《食品安全国家标准 食品中灰分的测定》、GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》测定豌豆低聚肽中的水分、灰分和总蛋白质含量;酸溶蛋白含量和游离氨基酸的差值为肽含量的测定方法。
1.3.2.2 氨基酸组成测定
以豌豆低聚肽为原料,参照GB 5009.124—2016《食品安全国家标准 食品中氨基酸的测定》测定豌豆低聚肽中氨基酸组成。
1.3.2.3 分子质量分布测定
1 mg/mL豌豆低聚肽溶液经过滤膜(0.22 μm)后上样,凝胶过滤使用高效液相色谱仪,并使用紫外检测器检测,数据处理软件为GPC。校正曲线使用肽标准品溶液制作[9]。层析具体参数为:色谱柱(300 mm×7.8 mm),流动相为V(乙腈)∶V(水)∶V(三氟乙酸)为45∶55∶0.1,进样10 μL,0.5 mL/min流速,220 nm检测波长。
1.3.3 HMG-CoA还原酶抑制实验
HMG-CoA还原酶(EC 1.1.1.34)是甲羟戊酸途径的速率控制酶,甲羟戊酸途径是从乙酰-CoA产生胆固醇的代谢途径[10]。在NADPH的反应中,HMG-CoA还原酶将HMG-CoA还原生成甲羟戊酸盐和CoA,这种酶是他汀类降胆固醇药物的靶点。抑制HMG-CoA还原酶诱导肝脏中低密度脂蛋白(low-density lipoprotein, LDL)受体的表达,能够降低血浆中胆固醇的浓度。使用HMG-CoA还原酶抑制活性测定试剂盒可以通过吸光度降低(OD340nm值)来测量NADPH的利用率。使用公式(1)计算抑制率:
抑制率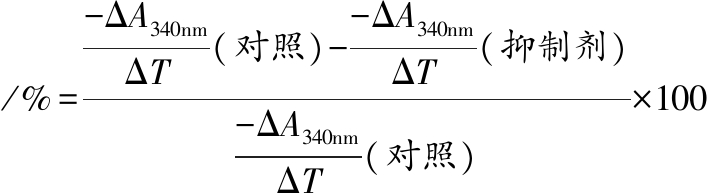
(1)
式中:ΔA340nm是2个时间点(T1和T2)在340 nm处的吸光度之差;ΔT是测定时间间隔,本实验测定时间为10 min。
1.3.4 NAFLD细胞模型评价
1.3.4.1 细胞培养
液氮中取出的HepG2细胞快速解冻后1 000 r/min下离心3 min,弃去上清液,加入1 mL含有10%(体积分数)胎牛血清和1%(体积分数)双抗的DMEM培养基,混匀后移至培养瓶,加培养基于37 ℃,5%(体积分数)CO2条件下培养复苏。细胞融合80%以上时,弃培养基并用PBS润洗,后加入1 mL胰酶细胞消化液消化至细胞收缩、间隙变大,弃去消化液并加入2 mL完全培养基终止消化,轻轻吹落细胞,混匀后分装2个培养瓶,添加培养基培养传代。待培养瓶中细胞融合达80%以上,重复上述步骤至吹落细胞并混匀,后将稀释的细胞悬液混匀吸取100 μL用流式细胞仪进行计数,按需要的铺板浓度(96孔板细胞浓度为1×104个/孔,6孔板细胞浓度为1×106个/孔),将细胞悬液稀释后加于培养板中,混匀后培养。
1.3.4.2 CCK8法检测样品的细胞毒性
取对数期生长的细胞接种(96孔板,1×104个细胞+100 μL细胞悬液/孔),培养24 h后弃去培养基用PBS润洗,每孔加入100 μL不同浓度的样品,豌豆低聚肽的质量浓度分别为50、100、200、400、600、800、1 000、1 500、2 000、4 000、6 000、8 000 μg/mL,游离脂肪酸的浓度为0、0.25、0.5、0.75、1、1.25、2 mmol/L,阿托伐他汀的浓度为0、1、5、10、20、30、40 μmol/L,培养24 h后丢弃培养基并用PBS润洗,将10 μL CCK8、100 μL新培养基加入培养孔,后于培养箱内孵育(1~3 h),使用酶标仪测定其在450 nm 处吸光度。细胞存活率计算如公式(2)所示:
细胞存活率![]()
(2)
式中:A样品组、A对照组和A空白组分别为样品组、对照组和空白组在450 nm处的吸光度。
1.3.4.3 油红O染色
取对数期生长的细胞接种至6孔培养板(1×106个/孔),每孔加入2 mL细胞悬液,培养24 h后弃培养基并润洗,设置4个实验组,空白组中加入含10 g/L BSA的DMEM培养基、游离脂肪酸组中加入0.5 mmol/L FFA、豌豆低聚组中加入0.5 mmol/L FFA和800 μg/mL豌豆低聚肽、阿托伐他汀组中0.5 mmol/L FFA和10 μmol/L阿托伐他汀,继续培养24 h。培养24 h后,弃培养液并润洗,加多聚甲醛固定液6 mL固定20 min并润洗。加入体积分数为60%的异丙醇覆盖细胞并弃去后,用油红O染色液染色,后加适量异丙醇静置30 s并洗去,再加适量PBS于显微镜下观察。每孔加入适量异丙醇孵育15 min 抽提,抽提液于490 nm波长处测吸光度。
1.3.4.4 细胞TG、TC检测
取对数期生长的细胞接种至6孔细胞培养板培养,设置6个实验组,空白组中加入含1%(体积分数)牛血清白蛋白(bovine serum albumin, BSA)的DMEM培养基、游离脂肪酸组中加入0.5 mmol/L 游离脂肪酸(free fatty acids, FFA)、豌豆低聚组中加入0.5 mmol/L FFA及分别加入400、600、800 μg/mL的豌豆低聚肽和、阿托伐他汀组中0.5 mmol/L FFA和10 μmol/L阿托伐他汀。培养24 h后弃培养液并洗涤,加细胞裂解液200 μL,裂解后收集液体。每个实验组的蛋白浓度使用二喹啉甲酸(bicinchoninic acid,BCA)法试剂盒检测。
a)TG含量测定
TG测定按照甘油三酯测试盒说明书进行加样操作,设置加蒸馏水的空白孔、加校准品的标准孔和加样本的样本孔,分别加2.5 μL,各孔再加入工作液250 μL振荡混匀并孵育10 min(37 ℃),酶标仪于500 nm处测定吸光度值。TG含量计算如公式(3)所示:
TG含量![]()
(3)
式中:A样本孔,样本在500 nm处的吸光度值;A标准孔,标准品在500 nm处的吸光度值;A空白孔,溶剂在500 nm处的吸光度值;C标准=2.39 mmol/L;Cpr,待测样本蛋白浓度,g prot/L。
b)TC含量测定
TC测定按照胆固醇测试盒说明书进行加样操作,同TG测定前准备步骤,使用酶标仪于500 nm处测定样品吸光度值。TC含量根据公式(4)计算:
TC含量![]()
(4)
式中:A样本孔,样本在500 nm处的吸光度值;A标准孔,标准品在500 nm处的吸光度值;A空白孔,溶剂在500 nm处的吸光度值;C标准=6.56 mmol/L,Cpr,待测样本蛋白浓度,gprot/L。
1.3.4.5 Western blot检测
取对数生长期的细胞接种至6孔细胞培养板(1×106个/孔),每孔加2 mL细胞悬液,培养24 h后丢弃完全培养基并用PBS润洗,设置4个实验组,分别为空白组(含1%BSA的DMEM)、游离脂肪酸组(0.5 mmol/L FFA)、豌豆低聚肽组(0.5 mmol/L FFA+800 μg/mL豌豆低聚肽)和阿托伐他汀组(0.5 mmol/L FFA+10 μmol/L阿托伐他汀),培养24 h。培养后缓慢吸去细胞培养液并润洗,加入已混合苯甲基磺酰氟(phenyl methane sulfonyl fluoride, PMSF)、蛋白酶抑制剂和磷酸酶抑制剂的200 μL细胞裂解液吹打混匀裂解,裂解液离心3~5 min(10 000~14 000 r/min),取上清液。每个实验组蛋白浓度检测同1.3.4.4节。用裂解液、蛋白溶液稀释样品,使得每个样品的蛋白质量浓度最终为4 μg/μL,置于沸水浴中煮沸5 min,再分装并于-80 ℃保存。
使用预制胶进行电泳设置为恒压模式先80 V运行30 min,再120 V运行60 min,电泳完成后进行湿法转膜,转膜结束后,将聚偏二氟乙烯(polyvinylidene fluoride, PVDF)膜放置于封闭液[含吐温20 的Tris缓冲盐水,TBST,含5%(体积分数)脱脂奶粉]封闭2 h,后用TBST洗膜,再将膜放置到稀释后的一抗中,4 ℃摇床孵育过夜。孵育结束后洗膜,再将膜放置稀释后的二抗中孵育2 h。孵育完成后洗膜,再将PVDF膜放置凝胶成像仪中,滴加增强型化学发光试剂(enhanced chemiluminescence, ECL)显影液显影。
1.4 数据处理
所有实验都进行3次重复,数据以“平均值±标准差”表示。方差分析(analysis of variance,ANOVA)用于评估平均值的显著差异。使用Origin 2021(OriginLab Corporation,美国)和GraphPad Prism 9(GraphPad Software,美国)绘制图表,使用ImageJ软件量化Western blot显影结果。
2 结果与分析
2.1 豌豆低聚肽的基础理化性质
通过高效液相色谱法分析了豌豆低聚肽的分子质量分布情况。由图1及表1可以看出,豌豆低聚肽中分子质量小于1 000 Da的组分占比87.89%,分子质量为150~1 000 Da的组分占比高达82.94%,分子质量在2 000 Da以上的组分仅占比12.08%,并且豌豆低聚肽的重均分子质量为559.10 Da。这与WEI等[6]酶解制备的豌豆低聚肽分子质量分布情况相似。此外,相关研究得出肽比游离氨基酸或完整的蛋白质更易有效运输和吸收[11],因此,对比于豌豆蛋白来说,豌豆低聚肽具有易消化吸收的特点。
表1 豌豆低聚肽的分子质量分布
Table 1 Molecular weight of pea oligopeptides
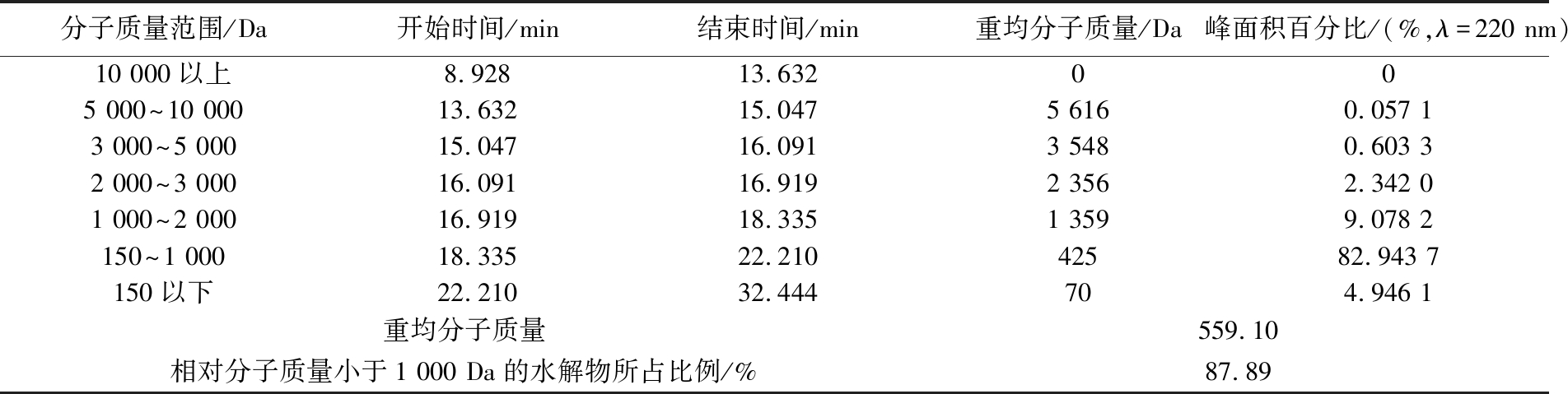
分子质量范围/Da开始时间/min结束时间/min重均分子质量/Da峰面积百分比/(%,λ=220 nm)10 000以上8.92813.632005 000^10 00013.63215.0475 6160.057 13 000^5 00015.04716.0913 5480.603 32 000^3 00016.09116.9192 3562.342 01 000^2 00016.91918.3351 3599.078 2150^1 00018.33522.21042582.943 7150以下22.21032.444704.946 1重均分子质量559.10相对分子质量小于1 000 Da的水解物所占比例/%87.89
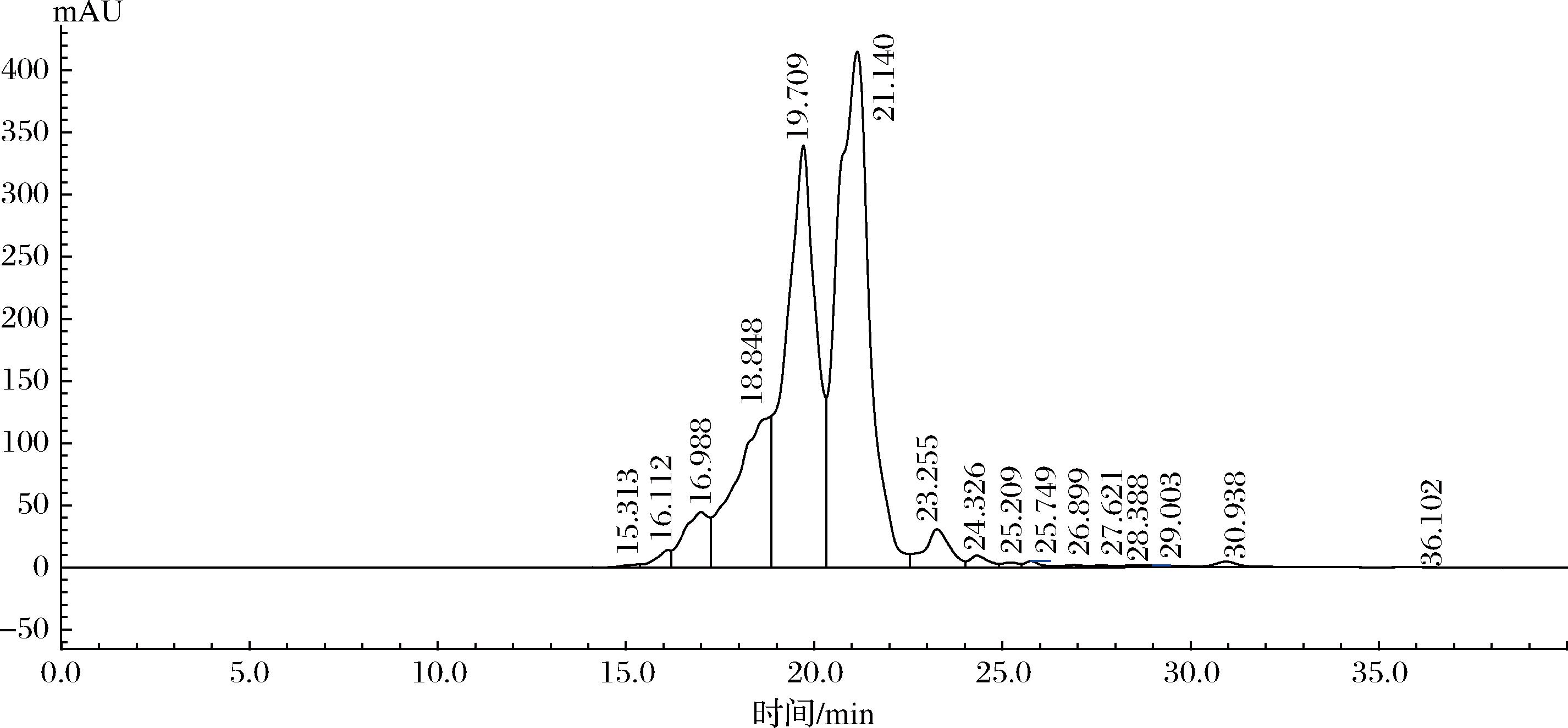
图1 豌豆低聚肽的高效液相色谱图
Fig.1 High performance liquid chromatography of pea oligopeptides
表2和表3列出了豌豆低聚肽的理化成分和氨基酸组成,从表中可以看出豌豆低聚肽的蛋白质和肽含量较高,分别为90.09、81.44 g/100 g。豌豆低聚肽中含有大量的谷氨酸(18.20 g/100 g)、天冬氨酸(10.77 g/100 g)、赖氨酸(6.56 g/100 g)等,且必需氨基酸含量丰富,含量达27.51 g/100 g。氨基酸是蛋白质的组成成分,在细胞生长过程的信号传递中发挥着重要的作用,丰富的氨基酸组成对人体生理功能的调节起着至关重要的作用[12]。此外,豌豆低聚肽的氨基酸组成中支链氨基酸含量也较高,包括亮氨酸(6.29 g/100 g)、异亮氨酸(3.36 g/100 g)和缬氨酸(4.07 g/100 g)。支链氨基酸是在脂肪侧链上有分支的氨基酸,它们可以通过多种信号通路在营养代谢和能量稳态中发挥重要作用,可以抑制脂肪堆积[13]。因此,豌豆低聚肽具有一定的降脂潜力。
表2 豌豆低聚肽的理化成分
Table 2 Chemical composition of pea oligopeptides

水分/(g/100 g)灰分/(g/100 g)蛋白质(干基)/(g/100 g)酸溶蛋白(干基)/(g/100 g)游离氨基酸/(g/100 g)肽含量(干基)/(g/100 g)分子质量小于1 000 Da所占比例/%4.785.4890.0983.942.3881.4487.89
表3 豌豆低聚肽的氨基酸组成
Table 3 Amino acid composition of pea oligopeptides
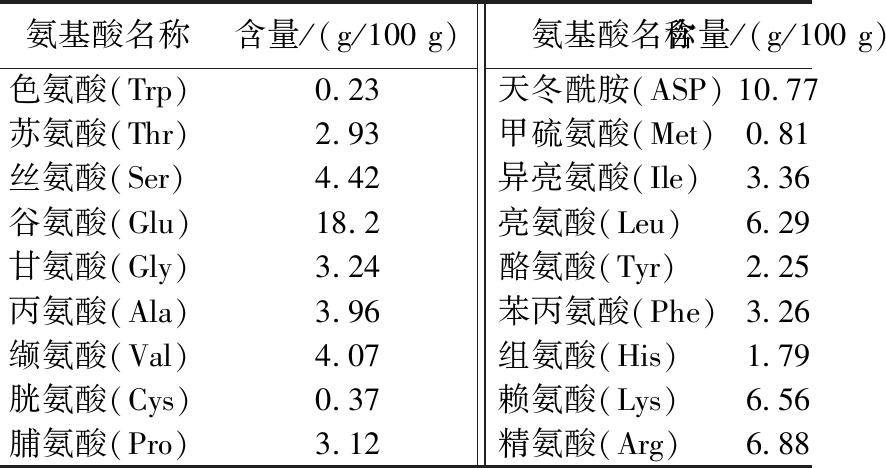
氨基酸名称含量/(g/100 g)氨基酸名称含量/(g/100 g)色氨酸(Trp)0.23天冬酰胺(ASP)10.77苏氨酸(Thr)2.93甲硫氨酸(Met)0.81丝氨酸(Ser)4.42异亮氨酸(Ile)3.36谷氨酸(Glu)18.2亮氨酸(Leu)6.29甘氨酸(Gly)3.24酪氨酸(Tyr)2.25丙氨酸(Ala)3.96苯丙氨酸(Phe)3.26缬氨酸(Val)4.07组氨酸(His)1.79胱氨酸(Cys)0.37赖氨酸(Lys)6.56脯氨酸(Pro)3.12精氨酸(Arg)6.88
2.2 豌豆低聚肽的HMG-CoA还原酶抑制能力
胆固醇稳态改变和肝脏游离胆固醇积累与NAFLD的发病机制有关,胆固醇生物合成途径中的限速酶为HMG-CoA还原酶,其能够催化HMG-CoA生成甲羟戊酸,其调节对于维持肝脏和血液循环中的胆固醇稳态至关重要[14]。因此,调控HMG-CoA还原酶活性是缓解非酒精性脂肪肝的主要途径之一。本研究测定了豌豆低聚肽对HMG-CoA还原酶的抑制能力,结果如图2所示,50、100 mg/mL豌豆低聚肽对HMG-CoA还原酶的抑制率分别为24.45%和56.62%,这表明豌豆低聚肽中具有抑制HMG-CoA还原酶活性的成分,存在调控HMG-CoA还原酶的潜力。
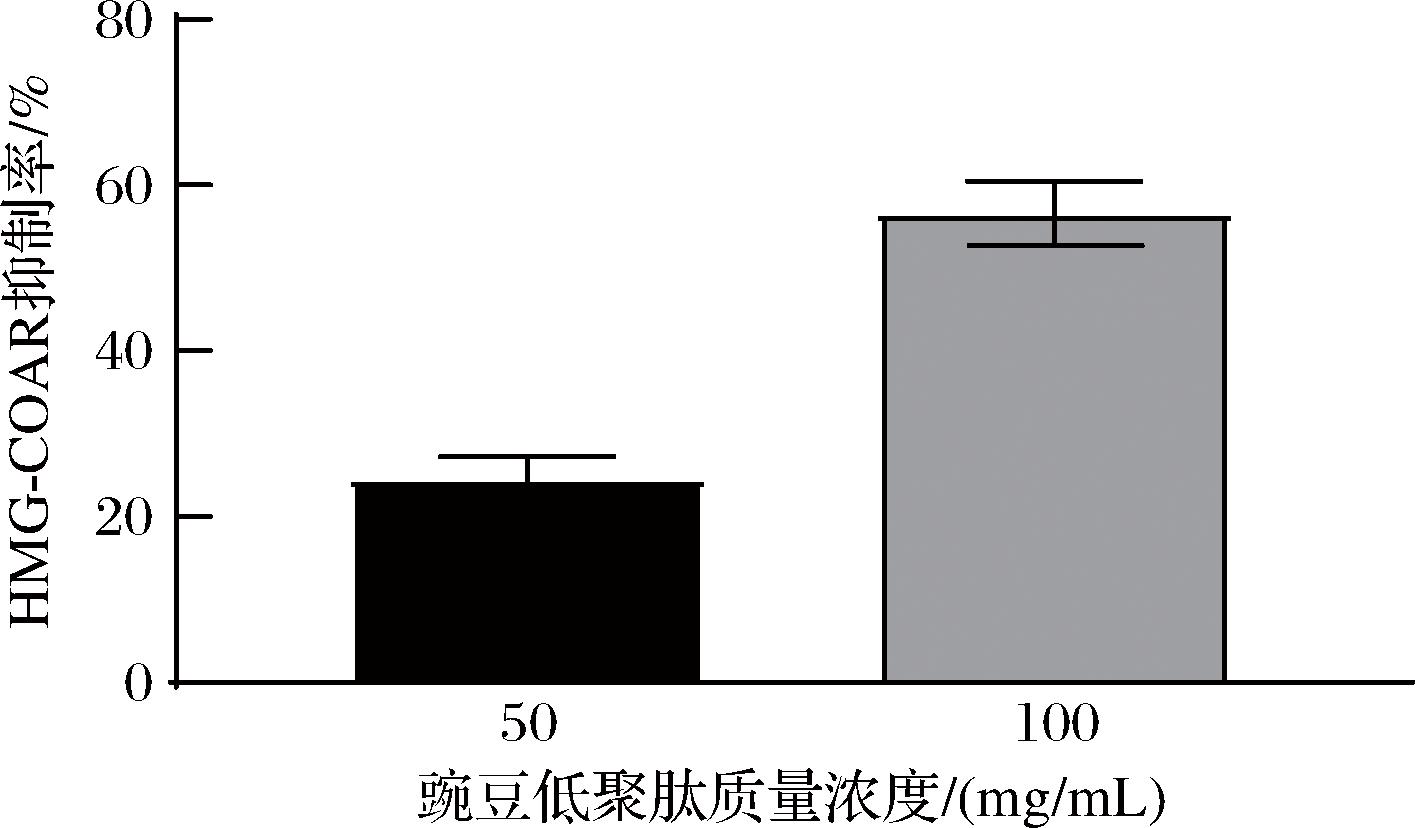
图2 豌豆低聚肽对HMG-CoA还原酶的抑制率
Fig.2 Inhibition rate of pea oligopeptides on HMG-CoA reductase
2.3 豌豆低聚肽对HepG2细胞活力的影响
人肝癌系HepG2细胞具有人肝脏组织的生理特性,且易于培养[15],现如今已被广泛用于研究肝脏脂肪变性、脂质过度沉积以及构建NAFLD细胞模型[16-17]。本研究以HepG2细胞构建NAFLD细胞模型,采用细胞计数试剂盒-8(Cell Counting Kit-8, CCK8)法评价了豌豆低聚肽对HepG2细胞存活率的影响,结果如图3-a所示,使用了不同浓度的豌豆低聚肽处理HepG2细胞24 h后,细胞存活率呈现明显的浓度依赖性下降趋势,当豌豆低聚肽质量浓度为1 000~8 000 μg/mL时,细胞存活率显著下降,影响了细胞的正常生存。因此,选择低于1 000 μg/mL的3个豌豆低聚肽质量浓度(200、400、800 μg/mL)进行后续试验,并按浓度梯度依次设置为豌豆低聚低剂量组、中剂量组和高剂量组。此外,阿托伐汀作为阳性对照,也采用CCK8法评价了其对细胞存活率的影响,结果如图3-b所示,发现不同浓度的阿托伐他汀处理HepG2细胞24 h后,细胞存活率也呈现浓度依赖性下降趋势,其中浓度为20 μmol/L的阿托伐他汀显著地影响了细胞存活率,10 μmol/L的阿托伐他汀对HepG2细胞存活率的影响较小,这与WILCOX等[18]报道的结果相似,因此,选择10 μmol/L的阿托伐他汀作为后续研究浓度。
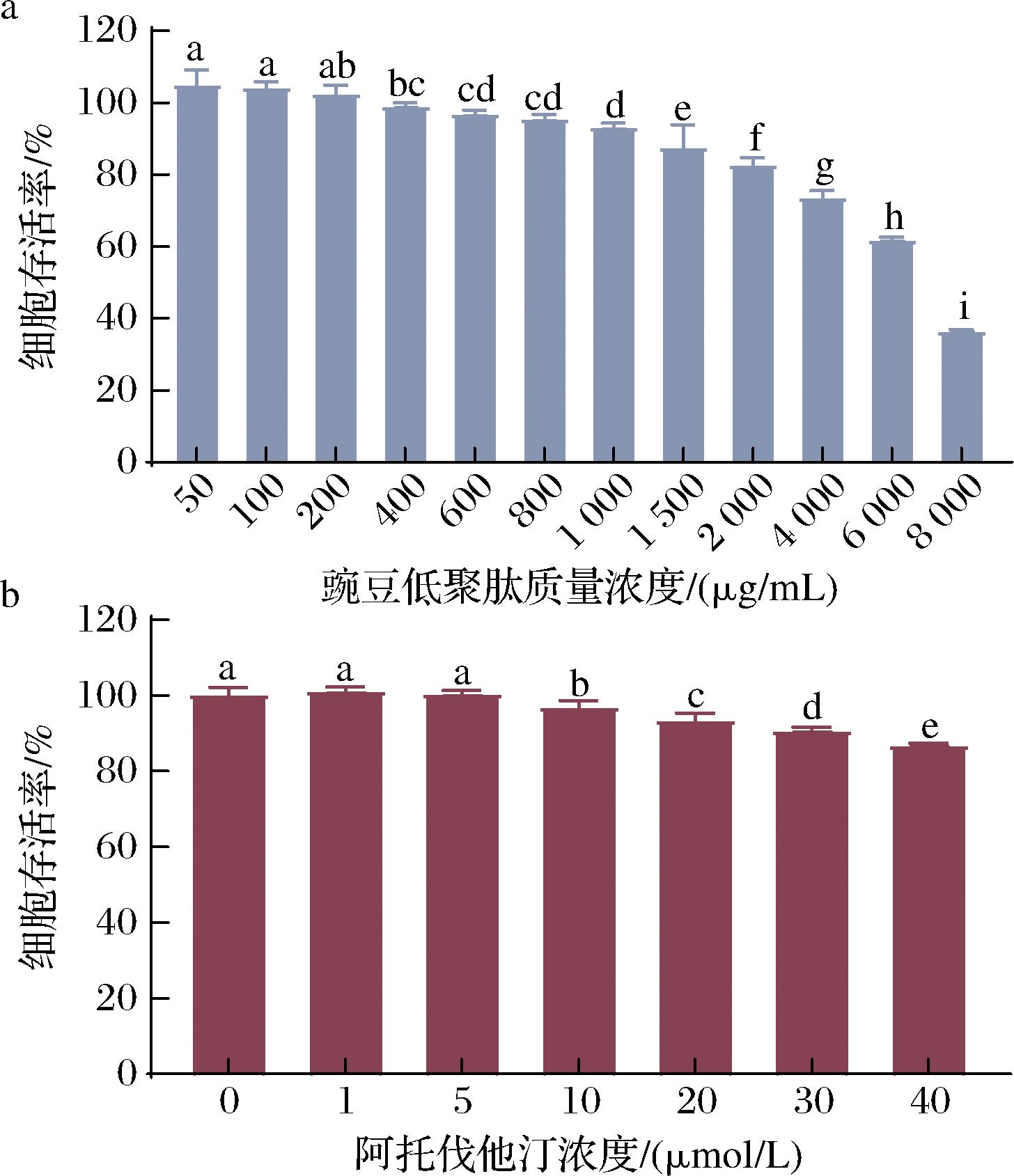
a-豌豆低聚肽质量浓度对细胞存活率的影响;b-阿托伐他汀浓度对细胞存活率的影响
图3 豌豆低聚肽和阿托伐他汀对HepG2细胞存活率的影响
Fig.3 Effect of pea oligopeptides and atorvastatin on HepG2 cells activity
注:不同字母表示组间存在显著差异(P<0.05)(下同)。
2.4 豌豆低聚肽对NAFLD细胞模型内脂质积累的影响
2.4.1 HepG2细胞的脂质沉积
相关研究已经证明FFA可用于诱导HepG2细胞内脂质沉积,在一定浓度范围内,FFA诱导HepG2细胞内脂质积累和脂毒性呈剂量依赖性,FFA已被广泛用于诱导HepG2细胞建立NAFLD细胞模型[19]。本研究将HepG2细胞与不同浓度的FFA(油酸∶棕榈酸=2∶1,物质的量浓度比)混合培养24 h,观察游离脂肪酸对肝细胞体外活力的影响,CCK8法检测FFA对HepG2细胞毒性。如图4所示,与对照组相比,随着FFA浓度的增加,细胞存活率呈现明显的浓度依赖性下降趋势,尤其是FFA浓度大于1 mmol/L时,细胞存活率显著下降,这与MA等[20]和JIN等[21]利用FFA诱导HepG2细胞建立NAFLD细胞模型研究中的结果相似,0.5 mmol/L FFA不影响HepG2细胞存活率,因此,选择0.5 mmol/L FFA来诱导HepG2细胞建立NAFLD细胞模型。
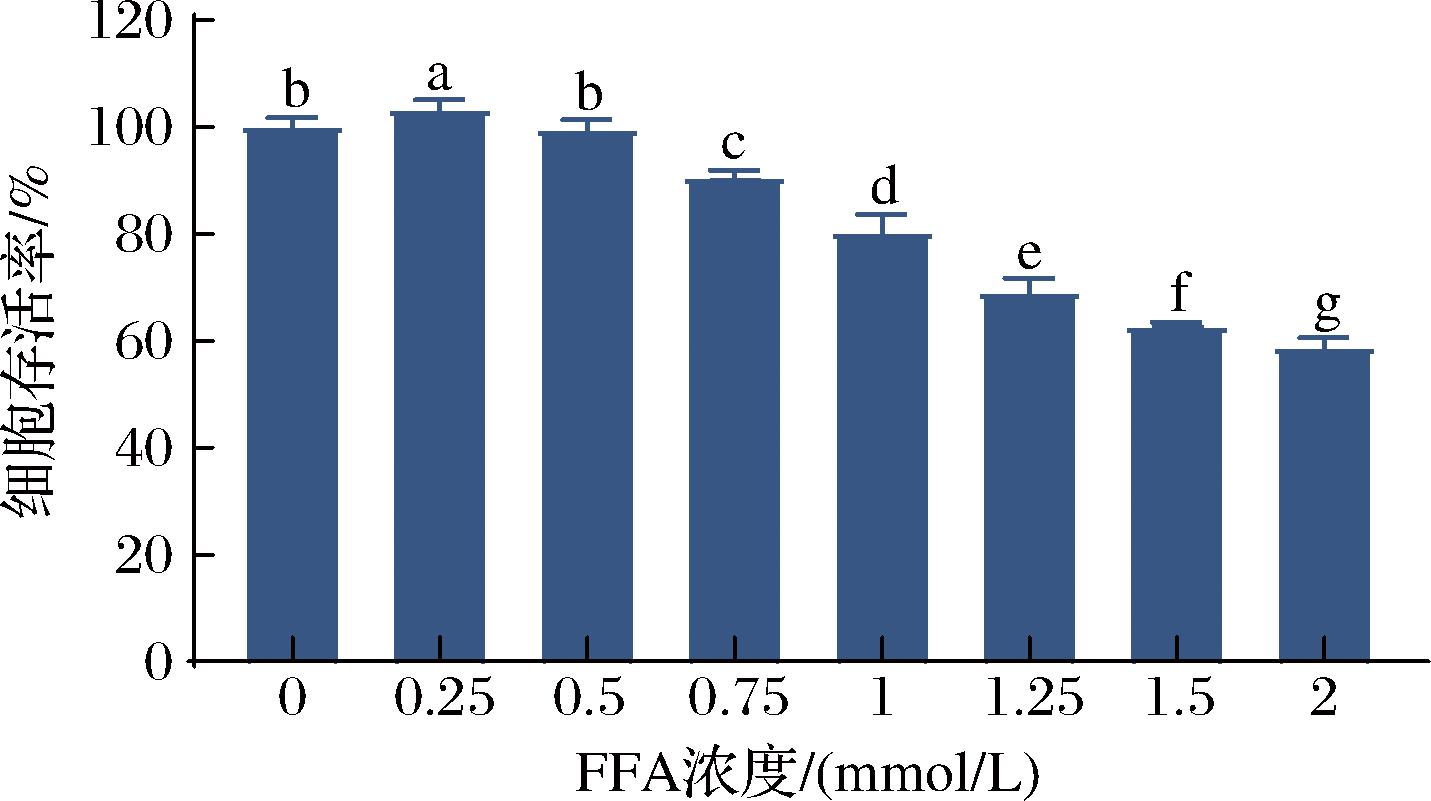
图4 FFA对HepG2细胞存活率的影响
Fig.4 Effect of FFA on the activity of HepG2 cells
2.4.2 豌豆低聚肽改善HepG2细胞脂质沉积
为了更加直观地评价豌豆低聚肽对FFA诱导的NAFLD细胞模型的影响情况,对正常的HepG2细胞、FFA诱导的NAFLD细胞模型、豌豆低聚肽和FFA共处理的HepG2细胞,以及阿托伐他汀和FFA共处理的HepG2细胞进行了油红O染色,结果如图5-a所示。与正常的HepG2细胞相比,FFA处理24 h后,细胞形态变圆,胞质中大量聚集红色脂滴。在豌豆低聚肽干预作用下,油红O染色的红色脂滴明显少于FFA诱导的NAFLD细胞模型组,并且阳性对照也出现了类似的现象。在波长500 nm下定量分析了油红O染色结果(5-b),检测结果与拍摄照片结果相同,与FFA诱导的NAFLD细胞模型相比,豌豆低聚肽与FFA共处理显著减轻了HepG2细胞中的脂质积累。此检测表明豌豆低聚肽可以改善HepG2细胞内的脂质积累。
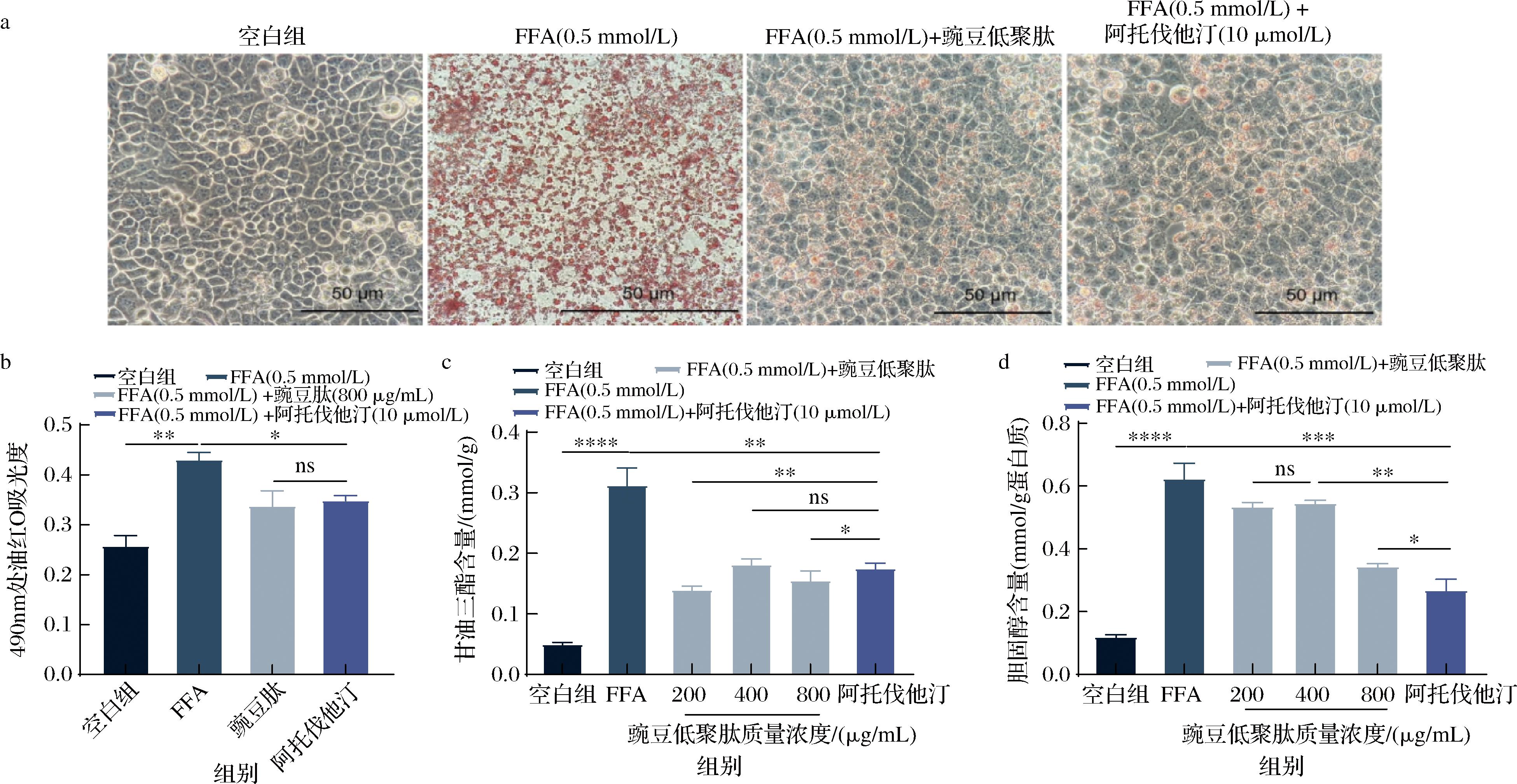
a-油红O染色结果;b-油红O染色定量结果;c-干预下对细胞内甘油三酯影响情况;d-干预下对细胞内胆固醇影响情况
图5 豌豆低聚肽对NAFLD细胞模型内脂质积累的影响
Fig.5 Effect of pea oligopeptides on lipid accumulation in NAFLD cell model
注:*表示P<0.05;**表示P<0.01;***表示P<0.001;****表示P<0.000 1;ns表示P>0.05。
为进一步确定豌豆低聚肽对NAFLD细胞模型内脂质积累的影响,测定了正常的HepG2细胞、FFA诱导的NAFLD细胞、豌豆低聚肽和FFA共处理的HepG2细胞以及阿托伐他汀和FFA共处理的HepG2细胞中TG、TC的含量,以证实油红O的染色结果。结果如图5-c、图5-d所示,与正常的HepG2细胞相比,FFA处理显著增加了细胞内TG、TC的含量,然而,200~800 μg/mL豌豆低聚肽的处理缓解了这一现象。与单独FFA处理相比,豌豆低聚肽和FFA共处理显著地减少了细胞内TG、TC的含量,但没有明显的浓度依赖性,阳性对照(阿托伐他汀和FFA共处理)出现了更为显著地缓解现象,这些现象均映证了油红O染色的结果。NAFLD中肝脏脂质代谢的改变促进了血脂的异常发展,尤其是TG和TC水平的升高,相关研究也观察到FFA诱导HepG2细胞TG、TC含量升高,与本研究中的结果一致[19]。综上结果表明,豌豆低聚肽可以改善NAFLD细胞模型内的脂质积累。
2.4.3 豌豆低聚肽对NAFLD细胞模型内脂质代谢相关信号蛋白表达水平的影响
为研究豌豆低聚肽缓解FFA诱导的NAFLD细胞模型脂质累积的机制,检测与脂肪酸代谢和胆固醇合成相关蛋白的表达。使用0.5 mmol/L FFA以及800 μg/mL的豌豆低聚肽处理HepG2细胞24 h,以阿托伐他汀干预作为阳性对照,提取各组细胞的蛋白进行Western blot分析,结果如图6所示。AMPK是细胞内能量代谢的重要能量探测器,可调节细胞甘油三酯和胆固醇的产生[22],AMPK的磷酸化减弱了游离脂肪酸介导的新生脂肪形成和肝脏脂质积累[17]。有研究报道,激活AMPK/ACC信号通路可以抑制TG的产生[23]。此外,在肝脏脂质过载的情况下,肉碱棕榈酰转移酶1(carnitine palmitoyltransferase1, CPT1)表达下调导致脂肪酸β-氧化过量,进一步导致肝脏脂肪变性和脂质过氧化[24]。
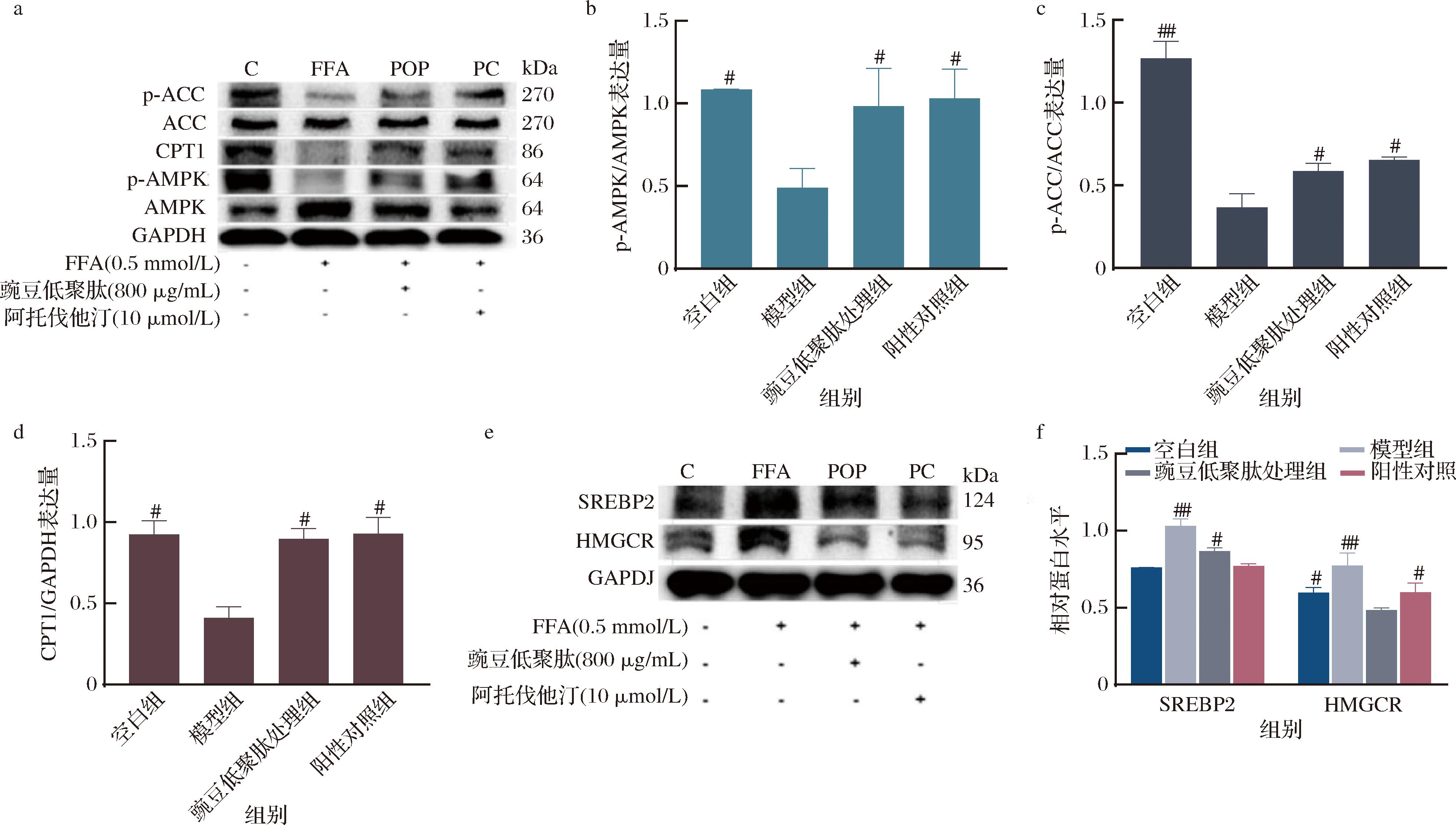
a-AMPK/ACC信号通路蛋白表达情况;b-p-AMPK/AMPK表达量;c-p-ACC/ACC表达量;d-CPT1/GAPDH表达量; e-SPEBP2/HMGCR信号通路蛋白表达情况;f-SREP2和HMGCR表达量
图6 豌豆低聚肽干预NAFLD细胞模型内脂质代谢相关信号蛋白的表达
Fig.6 Expression of signaling proteins related to lipid metabolism in a cell model of NAFLD treated with pea oligopeptides
注:#表示P<0.05,##表示P<0.01。
如图6-a~图6-d所示,研究结果表明,豌豆低聚肽的干预显著上调了磷酸化-AMPK(p-AMPK)、磷酸化-ACC(p-ACC)以及CPT1的表达量,因此可以推断豌豆低聚肽能通过激活AMPK磷酸化来抑制ACC活性,并促进CPT1A的表达,从而可能加强脂肪酸的β-氧化,减弱脂肪酸合成的过程,减少新生脂肪形成和肝脏脂质积累。甾醇调节元件结合蛋白2(sterol regulatory element-binding protein 2, SREBP2)是肝脏中的一种转录因子,其是调节胆固醇生物合成的关键转录调控因子和调节体内平衡的基因,能够激活甲羟戊酸途径基因和3-羟基-3-甲基戊二酰辅酶A还原酶(3-hydroxy-3-methylglutaryl-coenzyme A, HMGCR)的转录[17,25]。胆固醇合成增加导致游离胆固醇积累,及SREBP2、HMGCR表达增加,均是NAFLD的特征。图6-e~图6-f中,对比空白对照组,NAFLD模型组的SREBP2和HMGCR的表达量都显著升高,这表明NAFLD细胞模型构建成功。对比于FFA诱导的NAFLD细胞模型组,豌豆低聚肽处理组的SREBP2和HMGCR的表达量都显著下调,因此,豌豆低聚肽能够通过干预胆固醇合成途径的关键因子的表达来减少胆固醇的合成。此外,SREBP2受上游AMPK调节,AMPK的磷酸化会抑制SREBP2的表达,从而下调HMGCR的表达,弱化胆固醇的合成途径,减少胆固醇的累积[26]。
综上所述,豌豆低聚肽通过激活AMPK/ACC信号通路来调节NAFLD细胞模型中脂质的积累。具体是通过激活AMPK磷酸化来抑制ACC活性和SREBP2的表达,进一步促进CPT1A的表达和下调HMGCR的表达,从而加强了脂肪酸的β-氧化,减弱了脂肪酸和胆固醇的合成途径,最终降低了细胞内脂质积累。
3 结论
本研究首先通过酶解工艺制备了豌豆低聚肽,对豌豆低聚肽的分子质量分布、基础理化成分(蛋白质含量、肽含量、水分、灰分和氨基酸组成)进行了测定,并评价了豌豆低聚肽对HMG-CoA还原酶的抑制活性。此外,采用FFA诱导HepG2建立了NAFLD细胞模型,评价豌豆低聚肽对NAFLD细胞膜型内脂质累积和脂质代谢相关信号蛋白的影响。结果表明,酶解法制备的豌豆低聚肽分子质量小于1 000 Da的组分占比87.89%,其重均分子质量为559.10 Da。豌豆低聚肽的蛋白质和肽含量较高,其蛋白质含量为90.09 g/100 g,肽含量为81.44 g/100 g。豌豆低聚肽的氨基酸组成均衡,含有大量的谷氨酸(18.20 g/100 g)、天冬氨酸(10.77 g/100 g)、赖氨酸(6.56 g/100 g)等,必需氨基酸含量高达27.51 g/100 g。此外,豌豆低聚肽的氨基酸组成中支链氨基酸含量也较高。豌豆低聚肽对HMG-CoA还原酶显示出一定的抑制能力,50、100 mg/mL豌豆低聚肽对HMG-CoA还原酶的抑制率分别为24.45%和56.62%。豌豆低聚肽可以改善和干预FFA诱导的NAFLD细胞模型内脂质积累,主要表现为显著降低细胞内TG和TC水平。经研究发现,豌豆低聚肽是通过激活AMPK磷酸化来抑制ACC活性和SREBP-2的表达,进一步上调CPT1的表达和下调HMGCR的表达,从而加强了脂肪酸的β-氧化,减弱了胆固醇的合成途径,最终降低了细胞内脂质的积累。
本研究初步研究了豌豆低聚肽在体外细胞水平上干预和改善NAFLD的脂质沉积作用,未来可以进一步开展体内试验进行评价。本研究结果为以豌豆蛋白为原料开发干预NAFLD的产品提供理论基础,并为探寻天然安全有效的NAFLD缓解及干预产品提供了依据,为食源性生物活性肽的设计开发提供了有力支撑。
[1] YU R Y, GU Y P, ZHENG L Y, et al.Naringenin prevents NAFLD in the diet-induced C57BL/6 J obesity model by regulating the intestinal barrier function and microbiota[J].Journal of Functional Foods, 2023, 105:105578.
[2] JUNG E J, SUNG K W, BAE T H, et al.The N-degron pathway mediates lipophagy:The chemical modulation of lipophagy in obesity and NAFLD[J].Metabolism, 2023, 146:155644.
[3] ISMAIL B S, ABDEL-REHEIM E S, SOLIMAN H A, et al.Protective effect of gallic acid against nonalcoholic fatty liver disease induced by high fat diet[J].Journal of Pharmaceutical Research International, 2021, 33(44B):378-397.
[4] ZHANG J J, MA X X, FAN D D.Ginsenoside CK ameliorates hepatic lipid accumulation via activating the LKB1/AMPK pathway in vitro and in vivo[J].Food &Function, 2022, 13(3):1153-1167.
[5] SURYANINGTYAS I T, JE J Y.Bioactive peptides from food proteins as potential anti-obesity agents:Mechanisms of action and future perspectives[J].Trends in Food Science &Technology, 2023, 138:141-152.
[6] WEI Y, ZHANG R X, FANG L, et al.Hypoglycemic effects and biochemical mechanisms of pea oligopeptide on high-fat diet and streptozotocin-induced diabetic mice[J].Journal of Food Biochemistry, 2019, 43(12):e13055.
[7] POWNALL T L, UDENIGWE C C, ALUKO R E.Amino acid composition and antioxidant properties of pea seed (Pisum sativum L.) enzymatic protein hydrolysate fractions[J].Journal of Agricultural and Food Chemistry, 2010, 58(8):4712-4718.
[8] ASEN N D, ALUKO R E.Acetylcholinesterase and butyrylcholinesterase inhibitory activities of antioxidant peptides obtained from enzymatic pea protein hydrolysates and their ultrafiltration peptide fractions[J].Journal of Food Biochemistry, 2022, 46(11):e14289.
[9] LIU W Y, LU J, GAO F, et al.Preparation, characterization and identification of calcium-chelating Atlantic salmon (Salmo salar L.) ossein oligopeptides[J].European Food Research and Technology, 2015, 241(6):851-860.
[10] SANTOS-S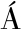 NCHEZ G,
NCHEZ G, 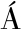 LVAREZ-L
LVAREZ-L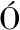 PEZ A I, PONCE-ESPA
PEZ A I, PONCE-ESPA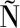 A E, et al.Food-derived peptides with inhibitory capacity for HMG-CoA reductase activity:A potential nutraceutical for hypercholesterolemia[J].Food Science and Human Wellness, 2024, 13(6):3083-3094.
A E, et al.Food-derived peptides with inhibitory capacity for HMG-CoA reductase activity:A potential nutraceutical for hypercholesterolemia[J].Food Science and Human Wellness, 2024, 13(6):3083-3094.
[11] 杨克炜, 关伟, 廖建平.白蛋白肽饮品在功能性食品中的应用[J].食品安全导刊, 2021(17):28-29.YANG K W, GUAN W, LIAO J P.The application of albumin peptide beverages in functional foods[J].China Food Safety Magazine, 2021(17):28-29.
[12] SANKANAGOUDAR S, SHUKLA R, SHUKLA K K, et al.Positive association of branched-chain amino acids with triglyceride and glycated haemoglobin in Indian patients with type 2 diabetes mellitus[J].Diabetes &Metabolic Syndrome:Clinical Research &Reviews, 2022, 16(4):102481.
[13] SAMMS R J, ZHANG G F, HE W T, et al.Tirzepatide induces a thermogenic-like amino acid signature in brown adipose tissue[J].Molecular Metabolism, 2022, 64:101550.
[14] GARC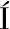 A-FERN
A-FERN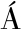 NDEZ-BRAVO I, TORRES-DO-REGO A, L
NDEZ-BRAVO I, TORRES-DO-REGO A, L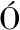 PEZ-FARRÉ A, et al.Undertreatment or overtreatment with statins:Where are we[J].Frontiers in Cardiovascular Medicine, 2022, 9:808712.
PEZ-FARRÉ A, et al.Undertreatment or overtreatment with statins:Where are we[J].Frontiers in Cardiovascular Medicine, 2022, 9:808712.
[15] ARZUMANIAN V A, KISELEVA O I, POVERENNAYA E V.The curious case of the HepG2 cell line:40 years of expertise[J].International Journal of Molecular Sciences, 2021, 22(23):13135.
[16] LIU H M, YAN J, GUAN F T, et al.Zeaxanthin prevents ferroptosis by promoting mitochondrial function and inhibiting the p53 pathway in free fatty acid-induced HepG2 cells[J].BBA - Molecular and Cell Biology of Lipids, 2023, 1868(4):159287.
[17] POORNIMA M S, SINDHU G, BILLU A, et al.Pretreatment of hydroethanolic extract of Dillenia indica L.attenuates oleic acid induced NAFLD in HepG2 cells via modulating SIRT-1/p-LKB-1/AMPK, HMGCR &PPAR-á signaling pathways[J].Journal of Ethnopharmacology, 2022, 292:115237.
[18] WILCOX L J, BARRETT P H R, HUFF M W.Differential regulation of apolipoprotein B secretion from HepG2 cells by two HMG-CoA reductase inhibitors, atorvastatin and simvastatin[J].Journal of Lipid Research, 1999, 40(6):1078-1089.
[19] WU M F, XI Q H, SHENG Y, et al.Antioxidant peptides from monkfish swim bladders:Ameliorating NAFLD in vitro by suppressing lipid accumulation and oxidative stress via regulating AMPK/Nrf2 pathway[J].Marine Drugs, 2023, 21(6):360.
[20] MA P, HUANG R R, OU Y.A soy glycinin derived octapeptide protects against MCD diet induced non-alcoholic fatty liver disease in mice[J].Food Science and Human Wellness, 2022, 11(6):1544-1554.
[21] JIN R T, JUVENTUS AWEYA J, LIN R, et al.The bioactive peptide VLATSGPG regulates the abnormal lipid accumulation and inflammation induced by free fatty acids in HepG2 cells via the PERK signaling pathway[J].Journal of Functional Foods, 2023, 104:105515.
[22] LI L S, DONG Y J, LIU X F, et al.Mangiferin for the management of liver diseases:A review[J].Foods, 2023, 12(13):2469.
[23] YE J N, ZHENG J W, TIAN X X, et al.Fucoxanthin attenuates free fatty acid-induced nonalcoholic fatty liver disease by regulating lipid metabolism/oxidative stress/inflammation via the AMPK/Nrf2/TLR4 signaling pathway[J].Marine Drugs, 2022, 20(4):225.
[24] YU S, LEE H M, LEE J, et al.Pennogenin 3-O-β-chacotrioside attenuates hypertrophied lipid accumulation by enhancing mitochondrial oxidative capacity[J].International Journal of Molecular Sciences, 2024, 25(5):2970.
[25] GUO J T, LI Y W, YUAN Y B, et al.Cholesterol-lowering activity of 10-gingerol in HepG2 cells is associated with enhancing LDL cholesterol uptake, cholesterol efflux and bile acid excretion[J].Journal of Functional Foods, 2022, 95:105174.
[26] LIN B Y, WAN H F, YANG J H, et al.Lipid regulation of protocatechualdehyde and hydroxysafflor yellow A via AMPK/SREBP2/PCSK9/LDLR signaling pathway in hyperlipidemic zebrafish[J].Heliyon, 2024, 10(3):e24908.