根据联合国粮食及农业组织(Food and Agriculture Organization of the United Nations,FAO)数据统计,中国作为全球主要农业生产国,其稻谷年产量约为2亿t[1]。米糠是稻谷在碾磨过程中从糙米外层分离的副产物,其质量占糙米总重的5%~8%[2]。米糠具有显著的营养特性,其组成包括14%~18%蛋白质、9%~12%水分、7%~9%灰分、34%~54%碳水化合物以及20%~30%膳食纤维(dietary fiber,DF),其中可溶性膳食纤维(soluble dietary fiber,SDF)占1.5%,不溶性膳食纤维(insoluble dietary fiber,IDF)占75.2%[3]。尽管米糠具有天然来源、可再生性以及富含生物活性成分等优势,但目前主要被用作动物饲料或直接废弃[4]。这不仅降低了资源综合利用率,还可能引发环境污染,使其潜在经济价值和营养功能未能得到充分挖掘。
研究表明,阿拉伯木聚糖(arabinoxylan,AX)是米糠膳食纤维的主要成分之一,属于非淀粉多糖的半纤维素类,主要是由阿拉伯糖和木糖构成,还含有少量的半乳糖和葡萄糖[5]。作为一种天然无毒的植物多糖,米糠阿拉伯木聚糖(rice bran arabinoxylan,RAX)具有多种生理功能特性。近年来,其在肠道菌群调节、抗氧化、糖尿病调控、心血管疾病预防及结肠癌防治等方面表现出良好的营养保健价值[6]。然而,可溶性AX在米糠中的含量较低,根据先前的报道,可通过碱法、酶法以及物理辅助法来提高AX提取率[7]。其中,碱法是最常用的方法,这是因为碱溶液能够破坏细胞壁结构,实现AX的高效溶出[8]。
蒸汽爆破(steam explosion,SE)作为一种新型原料预处理技术而得到广泛关注,利用高温高压蒸汽瞬间释放产生的机械力破坏植物细胞壁,可促进多糖溶出[9]。该方法具有处理时间短、能耗低、效率高和产业化适应性强等优势,符合绿色可持续的发展理念[10]。近年来,SE技术广泛应用在膳食纤维改性的研究中。TIAN等[11-12]通过SE处理米糠,其SDF含量提高了95.03%,且持水性、持油性和胆固醇吸附能力显著增强,其IDF热稳定性增强。MA等[13]发现SE处理可以促进黑米糠中IDF向SDF转化,显著降低SDF的分子质量。ZHOU等[14]证明了经SE处理的薏米麸皮SDF在体外发酵中可以促进有益菌的生长,抑制病原微生物的增殖,同时显示出很强的抗氧化特性。然而,当前关于SE处理对米糠中RAX精细结构的影响,以及分子结构变化如何调控其功能的研究尚不清晰。
基于此,本研究在课题组已经成熟的碱法提取阿拉伯木聚糖工艺的基础上,结合SE预处理,研究不同压强的SE预处理对米糠中RAX提取率、理化特性(化学组分、分子质量、分支度和官能团)、功能特性(溶解性和流变特性)和生物活性(抗氧化活性)的影响,并明确其构效关系,可为稻谷加工副产物的高值化利用提供参考依据和技术手段。
1 材料与方法
1.1 材料与试剂
米糠,安徽煜曦农产品经营部;T-系列葡聚糖标准品(10、40、70、500、2 000 kDa)、透析袋,北京索莱宝科技有限公司;单糖标准品(鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、葡萄糖醛酸、半乳糖醛酸),美国Sigma公司;α-淀粉酶、糖化酶和木瓜蛋白酶,上海源叶生物科技有限公司;没食子酸,上海麦克林生化科技有限公司;碘甲烷、重水和硼氘化钠,上海萨恩化学技术有限公司;二甲基亚砜,美国剑桥同位素实验室公司。除上述特殊说明外,实验过程中所使用的化学品和试剂均为分析纯,江天化工技术股份有限公司(天津)。
1.2 仪器与设备
QBS-200B蒸汽爆破设备,鹤壁正道生物能源有限公司;LC-20A示差高效凝胶排阻色谱(high-performance size exclusion chromatography,HPSEC),日本岛津公司;6890 N气质联用仪,安捷伦科技有限公司;Infinite 200 Pro酶标仪,TECAN公司;ICS-5000+离子色谱仪,Thermo Scientific公司;IS50傅里叶变换红外光谱仪(fourier transform infrared spectroscopy,FT-IR),尼高利公司;AVANCE Ⅲ 600核磁共振波谱仪(nuclear magnetic resonance spectroscopy,NMR),Bruker公司;MARS 60动态流变仪,Haake公司;SU1510扫描电子显微镜(scanning electron microscope,SEM),Hitachi公司。
1.3 实验方法
1.3.1 蒸汽爆破预处理
用自来水反复清洗米糠,70 ℃烘干。对蒸汽爆破设备进行加压,待压强达到目标值(0.5、0.8、1.2、1.5、2.0 MPa)后,将500.0 g米糠投入物料仓,处理120 s。收集样品,70 ℃干燥10 h,粉碎过60目筛网,贮存在4 ℃环境,供后续分析。
1.3.2 米糠微观结构测定
将米糠粉末均匀固定在样品架上,表面喷一层金膜,置于SEM下,加速电压设定为5 kV,分别选取放大倍数为250、1 000倍进行图像采集。
1.3.3 米糠阿拉伯木聚糖制备及其得率测定
将米糠与石油醚1∶5(g∶mL)在25 ℃连续搅拌4 h,8 000 r/min离心20 min,收集沉淀。将脱脂米糠和蒸馏水1∶20(g∶mL)充分混合,加入0.5%(质量分数)α-淀粉酶,95 ℃加热搅拌4 h,待降至60 ℃,加入0.5%(质量分数)糖化酶,搅拌1 h,进一步除去残留淀粉,煮沸15 min灭酶。溶液冷却后,添加1.0%(质量分数)木瓜蛋白酶,55 ℃保温搅拌4 h,灭酶,去除蛋白质。冷却至室温后,4 000 r/min离心30 min,收集沉淀,溶解、离心,重复2~3次,60 ℃烘干。加入0.5 mol/L NaOH溶液,在44.5 ℃萃取128 min[15]。上清液用4 mol/L HCl溶液调节pH值至4,进一步沉淀蛋白质,4 ℃静置12 h,离心。将上清液浓缩并加入3倍体积的无水乙醇,混匀,4 ℃静置12 h,收集沉淀,60 ℃复溶,透析72 h(截留分子质量为3.5 kDa)除去生成的盐和小分子组分。冷冻干燥后,获得RAX、RAX0.5(0.5 MPa)、RAX0.8(0.8 MPa)、RAX1.2(1.2 MPa)、RAX1.5(1.5 MPa)和RAX2.0(2.0 MPa)样品,根据公式(1)计算其得率:
(1)
式中:W1,得率,%;M,米糠质量,g;M1,RAX质量,g。
1.3.4 化学组成测定
根据苯酚-硫酸法[16],以木糖为标准品,测定RAX总糖含量。利用间羟基联苯比色法[17]测定RAX糖醛酸含量。根据福林酚法[18],以没食子酸为标准品,测定RAX总酚含量。使用Bradford法蛋白浓度测定试剂盒测定蛋白质含量。
1.3.5 分子质量分布测定
使用流动相(0.1 mol/L NaNO3溶液)作为溶剂,配制2 mg/mL的RAX溶液,60 ℃加热搅拌至完全溶解,利用HPSEC进行分子质量分布测定。色谱柱为Ultrahydrogel linear Column(7.8 mm×300 mm),检测温度为40 ℃,检测流速为0.6 mL/min。
1.3.6 单糖组成测定
用2 mol/L三氟乙酸溶液将RAX样品在120 ℃水解4 h,加入0.5 mL甲醇,干燥处理,重复操作5次,彻底去除三氟乙酸。将干燥后的水解产物溶解在超纯水中,利用离子色谱仪测定RAX的单糖组成[19]。色谱柱:CarboPacTM PA20保护柱(3 mm×150 mm)和CarboPacTM PA20分析柱(3 mm×150 mm),温度维持在30 ℃。流动相:A,超纯水溶液;B,0.2 mol/L NaOH溶液;C,0.1 mol/L CH3COONa溶液,流速为0.4 mL/min。
1.3.7 FT-IR测定
将1.0 mg干燥RAX样品和约150.0 mg KBr用研钵研磨并压片,利用FT-IR在4 000~500 cm-1波数扫描样品,扫描次数为16次,分辨率为4 cm-1。
1.3.8 甲基化分析
根据GUO等[20]报道的方法对SE预处理前后样品进行甲基化分析。将RAX样品用二甲基亚砜溶解,加入碘甲烷,将游离羟基甲基化,经4 mol/L三氟乙酸溶液水解、硼氘化钠还原和乙酰化处理,利用气质联用仪进行测定。色谱柱:HP-5毛细管色谱柱(30 m×0.32 mm×0.25 μm);升温程序:首先120 ℃维持3 min,然后以3 ℃/min速度升至210 ℃,最后210 ℃维持4 min;流速:10 mL/min;进样口温度:280 ℃。
1.3.9 1H NMR分析
将20.0 mg RAX加入到1.0 mL重水中,完全溶解后冷冻干燥,重复3次。将处理好的样品再次溶于重水,利用NMR进行扫描测定。
1.3.10 溶解度测定
配制10 g/L的RAX溶液,室温下搅拌3 h,10 000 r/min离心10 min,将沉淀在55 ℃下烘干至恒重,称量。RAX溶解度按照公式(2)计算:
(2)
式中:W2,溶解度,%;M,样品质量,mg;M1,样品加离心管质量,mg;M2,烘干后沉淀加离心管质量,mg。
1.3.11 流变学特性测定
制备80 g/L的RAX溶液,测试温度为25 ℃,使用直径35 mm椎板。在0.01~100 s-1剪切速率获得RAX表观黏度的流动曲线;固定应变为10%(线性黏弹性区内),在0.1~10 Hz频率测定RAX的储能模量(G′)和损耗模量(G″)[18]。
1.3.12 抗氧化活性测定
参考张秀敏等[21]报道方法评估RAX的DPPH自由基、ABTS阳离子自由基和羟自由基清除活性,稍有修改。以维生素C为阳性对照,以H2O为空白对照,试剂溶液分别为DPPH甲醇溶液、ABTS工作液及9 mmol/L FeSO4溶液、9 mmol/L水杨酸乙醇溶液和8.8 mmol/L H2O2溶液。通过梯度稀释制备RAX系列溶液,将样品溶液分别与试剂溶液在96孔板中充分混匀和反应,通过酶标仪测定吸光度,根据公式(3)计算RAX自由基清除率:
(3)
式中:W3,自由基清除率,%;A1,样品或阳性对照组吸光度;A2,试剂组吸光度;A0,空白对照组吸光度。
1.4 数据处理与统计分析
所有测量均重复3次或按说明进行,表示为“平均值±标准差”。使用SPSS 26.0软件和Duncan方法,对数据进行方差分析和多重测试分析,在P<0.05时表示处理的结果存在差异性显著。使用Origin 2021软件进行做图,采用MestReNova 15.0软件进行核磁谱图分析。
2 结果与分析
2.1 SE预处理对米糠微观结构的影响
未经SE处理(0 MPa)及经不同压强SE预处理(0.5~2.0 MPa,处理120 s)米糠微观结构变化如图1 所示。未经SE处理时,米糠的微观结构呈现较大的块状结构,表观形貌完整,紧凑平滑;而经SE处理后,表面粗糙,形成一些孔洞和褶皱,并伴有碎片颗粒产生。随着SE压强的增大,米糠表观形态破坏和孔隙特征愈发明显,这一现象与CHEN等[22]通过SE预处理大豆种皮的研究结论相吻合。米糠表面孔隙是由高压水蒸气渗透至内部形成的。在压力瞬间释放时,水蒸气迅速膨胀,产生的机械力破坏了米糠细胞壁紧密结构,使其表面呈现多孔特征[23],这为RAX提取创造了有利条件。

a-0 MPa,250×;b-0.5 MPa,250×;c-0.8 MPa,250×;d-1.2 MPa,250×;e-1.5 MPa,250×;f-2.0 MPa,250×;g-0 MPa,1 000×; h-0.5 MPa,1 000×;i-0.8 MPa,1 000×;j-1.2 MPa,1 000×;k-1.5 MPa,1 000×;l-2.0 MPa,1 000×
图1 SE预处理前后米糠的SEM图像
Fig.1 SEM images of rice bran before and after SE pretreatment
2.2 SE预处理对RAX得率的影响
利用不同压强SE预处理米糠,碱法萃取RAX并计算RAX得率,探究SE预处理对RAX得率的影响(表1)。SE预处理后,RAX得率显著升高,在1.5 MPa时,RAX得率(1.66%)达到峰值,与SE处理前相比,提高至1.80倍。SE预处理使米糠细胞壁紧密结构被破坏,分子间共价键断裂和相互作用减弱,促进了可溶性AX溶出,使RAX得率显著升高[24],这与先前所述的SEM观察结果一致。然而,当压强超过最大得率所对应值后,RAX得率降为1.31%。这可能是由于过高的SE压强使多糖降解为无法被乙醇沉淀的低聚糖和单糖[25],导致得率降低。上述结果表明,适宜的SE压强可以显著提高RAX得率,这为未来RAX产业化生产提供了重要参考依据。
表1 SE预处理对RAX得率、化学组成和分子质量的影响
Table 1 The effect of SE pretreatment on RAX yield, chemical composition and molecular weight
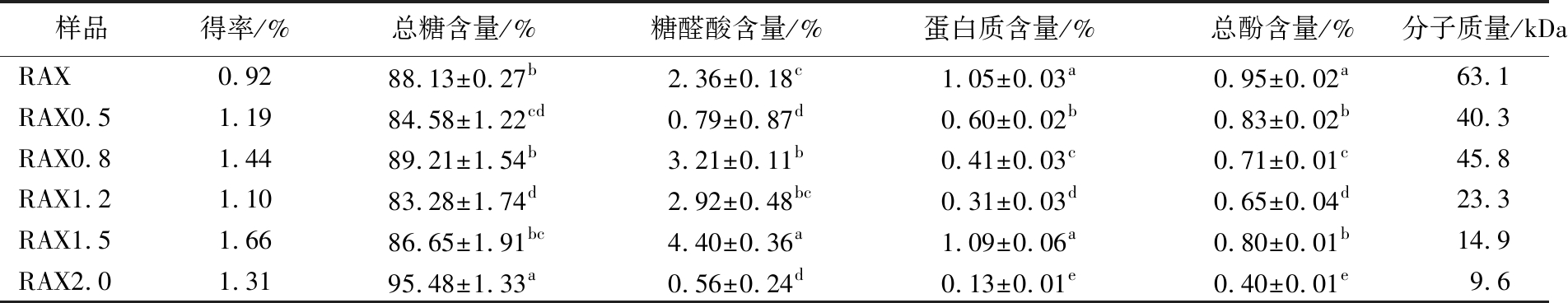
注:同一列中不同字母表示差异显著(P<0.05)。
样品得率/%总糖含量/%糖醛酸含量/%蛋白质含量/%总酚含量/%分子质量/kDaRAX0.9288.13±0.27b2.36±0.18c1.05±0.03a0.95±0.02a63.1RAX0.51.1984.58±1.22cd0.79±0.87d0.60±0.02b0.83±0.02b40.3RAX0.81.4489.21±1.54b3.21±0.11b0.41±0.03c0.71±0.01c45.8RAX1.21.1083.28±1.74d2.92±0.48bc0.31±0.03d0.65±0.04d23.3RAX1.51.6686.65±1.91bc4.40±0.36a1.09±0.06a0.80±0.01b14.9RAX2.01.3195.48±1.33a0.56±0.24d0.13±0.01e0.40±0.01e9.6
2.3 SE预处理对RAX化学组成和分子质量分布的影响
SE预处理前后RAX的化学组成如表1所示,RAX的总糖含量为88.13%,糖醛酸、蛋白质和总酚含量均低于3%,分别为2.36%、1.05%和0.95%,表明RAX是一种纯度较高的中性多糖。与未经SE处理样品相比,除RAX0.5(0.79%)和RAX2.0(0.56%)外,其余RAX样品的糖醛酸含量均有所增加。这可能是因为SE处理使木质素和糖醛酸之间酯键遭到破坏,导致糖醛酸基团释放,从而使糖醛酸含量增加[26]。此外,SE预处理使RAX中总酚含量显著降低(P<0.05),这可能是因为SE高温高压条件使米糠中部分酚类化合物被破坏和分解。
如表1和图2所示,SE预处理后,RAX分子质量显著下降(从63.1 kDa降至9.6 kDa),降低程度与SE压强呈正相关。这主要归因于在SE处理过程中产生强大的机械力和热效应,导致RAX中糖苷键断裂和结构解聚,促使其从大分子片段转变为小分子片段[27]。此外,分子质量的降低可以提高多糖的溶解度和生物利用度,可为其在食品、制药和生物医学领域的应用创造新的机会。
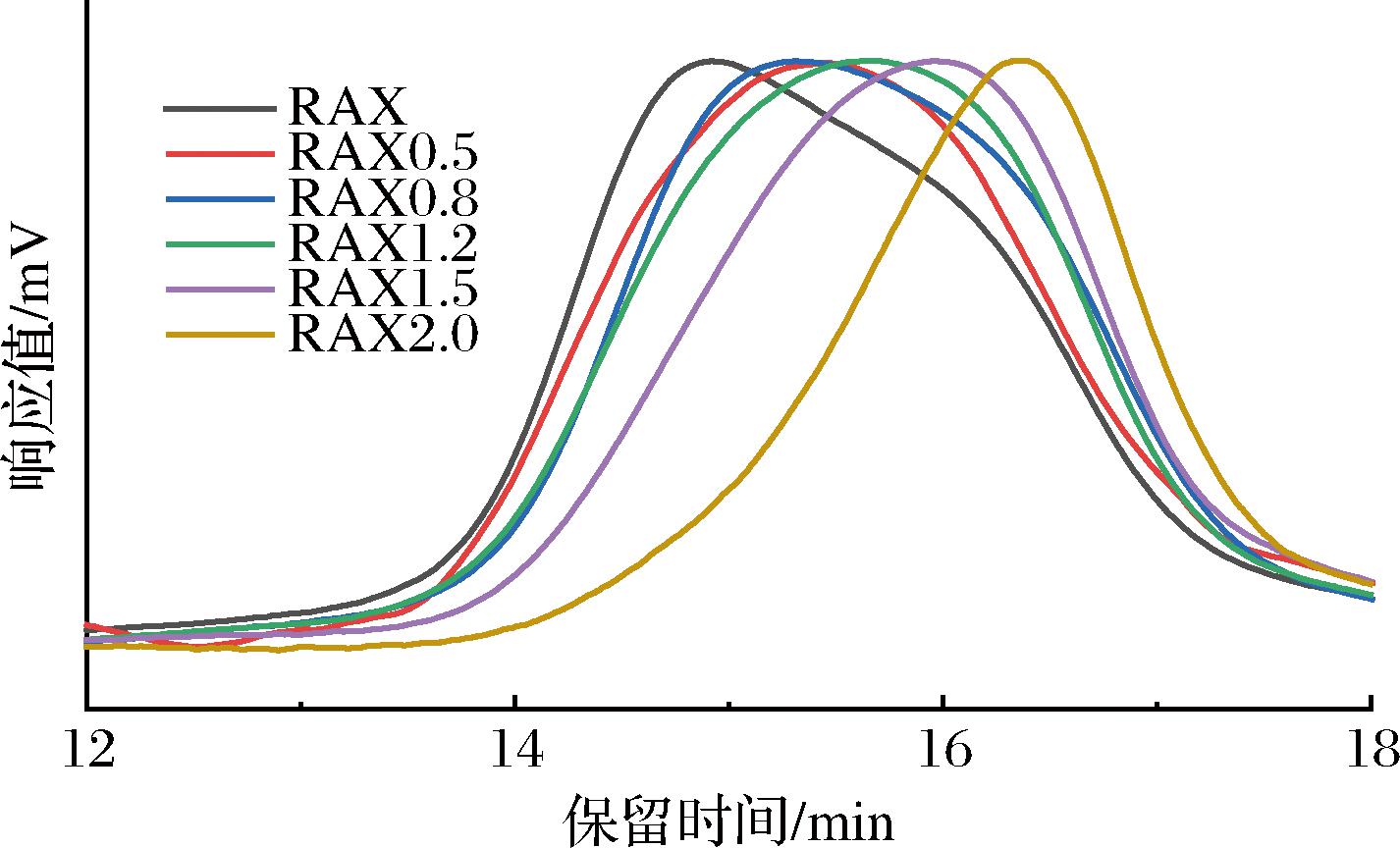
图2 RAX的分子质量分布
Fig.2 Molecular weight distribution of RAX
基于RAX得率、分子质量分布和总酚含量3个关键指标,综合分析后,分别选定RAX、RAX0.8和RAX1.2为代表样品,进行后续结构表征和生物活性研究。
2.4 SE预处理对RAX结构的影响
2.4.1 单糖组成分析
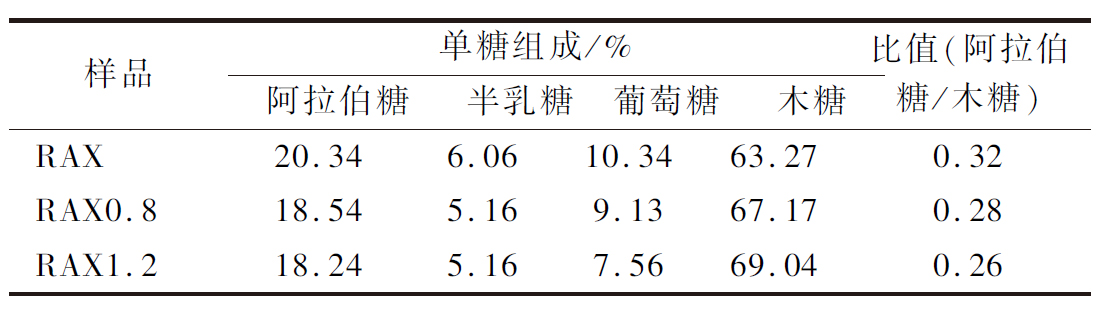
如表2所示,RAX主要由阿拉伯糖和木糖组成,还含有少量半乳糖和葡萄糖,这与GUO等[28]的研究结果一致。可以发现,SE预处理并未改变RAX单糖种类,但改变了各单糖组分的比例。阿拉伯糖/木糖值是表征AX支化程度的重要参数,与功能特性密切相关[29]。可以观察到,SE处理后RAX的阿拉伯糖/木糖值随着压强的增大而降低,分别为0.32(RAX)、0.28(RAX0.8)和0.26(RAX1.2),这可能是低压强下,在SE处理过程中的机械能和热能作用对RAX侧链的破坏所致。综上所述,SE处理能够有效降低RAX支化程度。
表2 SE预处理前后RAX的单糖组成
Table 2 Monosaccharide composition of RAX before and after SE pretreatment
2.4.2 FT-IR分析
SE预处理对RAX结构特征的影响可通过FT-IR光谱图进行评估,结果如图3所示。在3 426 cm-1处宽吸收带与—OH伸缩振动有关,而2 929 cm-1处则与C—H伸缩振动有关;1 640 cm-1处观察到的吸收峰是由C![]() O不对称拉伸振动所引起[28]。此外,1 200~800 cm-1的吸收峰为AX的典型特征区。其中,1 050 cm-1处振动信号表明,RAX中存在吡喃糖环结构,而894 cm-1处特征峰对应β糖苷键(C—O—C)的对称伸缩振动[9]。SE处理前后RAX的FT-IR光谱特征基本一致,无明显差异,这说明SE处理并未改变RAX主要官能团。
O不对称拉伸振动所引起[28]。此外,1 200~800 cm-1的吸收峰为AX的典型特征区。其中,1 050 cm-1处振动信号表明,RAX中存在吡喃糖环结构,而894 cm-1处特征峰对应β糖苷键(C—O—C)的对称伸缩振动[9]。SE处理前后RAX的FT-IR光谱特征基本一致,无明显差异,这说明SE处理并未改变RAX主要官能团。
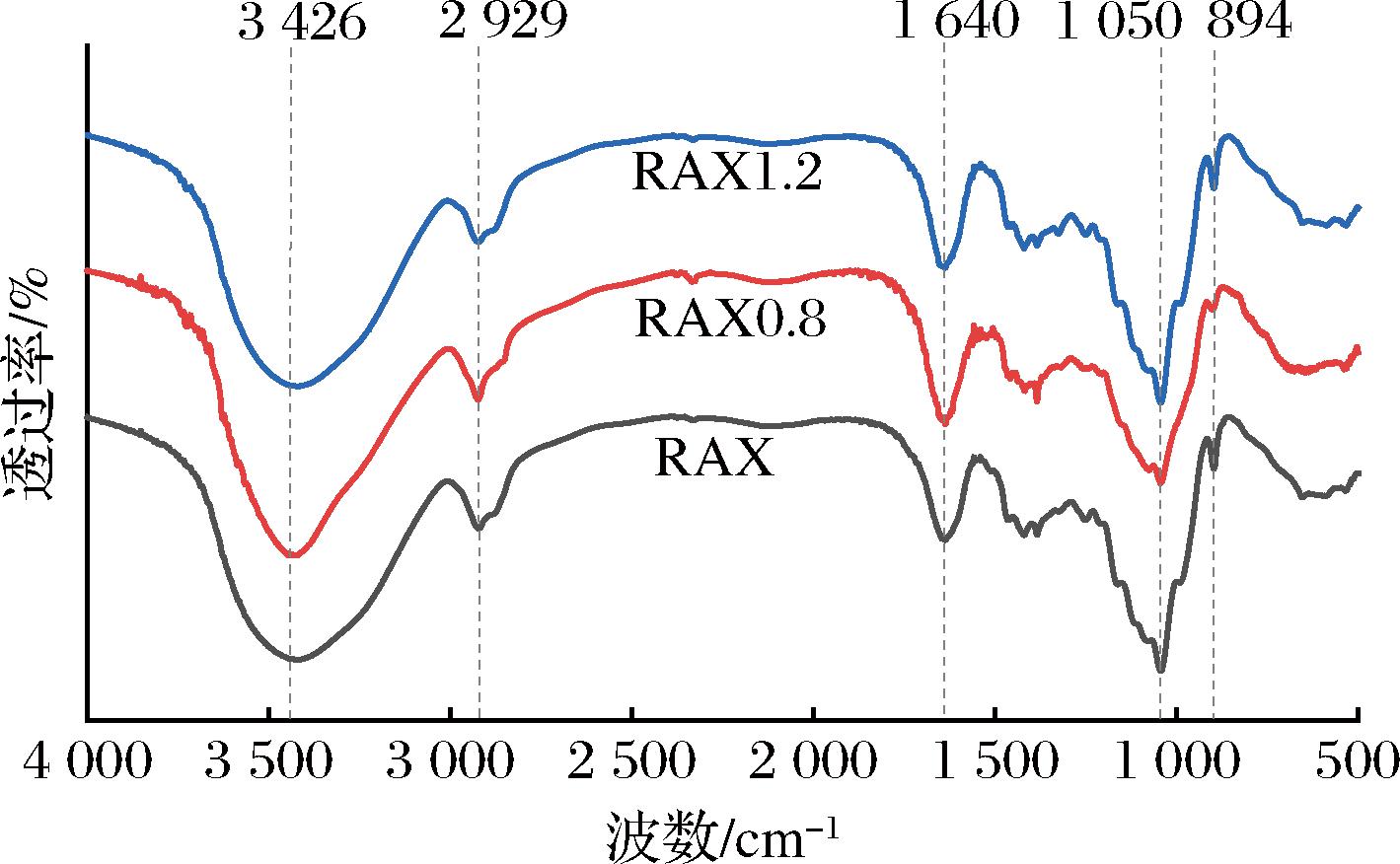
图3 RAX的FT-IR图谱
Fig.3 FT-IR spectra of RAX
2.4.3 甲基化分析
SE预处理对RAX糖苷键的影响可通过甲基化分析评估。如表3所示,RAX由木糖、阿拉伯糖、半乳糖和葡萄糖残基组成,这与上述单糖组成相同。可以观察到,RAX的木糖残基和阿拉伯糖残基均有4种类型,分别为T-Xylp、4-Xylp、3,4-Xylp和2,3,4-Xylp以及T-Araf、2-Araf、3-Araf和5-Araf,其中,T-Araf的含量在阿拉伯糖残基中居首位。这一结果与KANG等[18]报道的结果相似。RAX的木糖骨架中含有58.09%的未取代、16.46%的单取代、1.54%的双取代和4.16%的末端木糖残基,表明RAX的取代程度较低。
表3 RAX的甲基化分析
Table 3 Methylation analysis of RAX
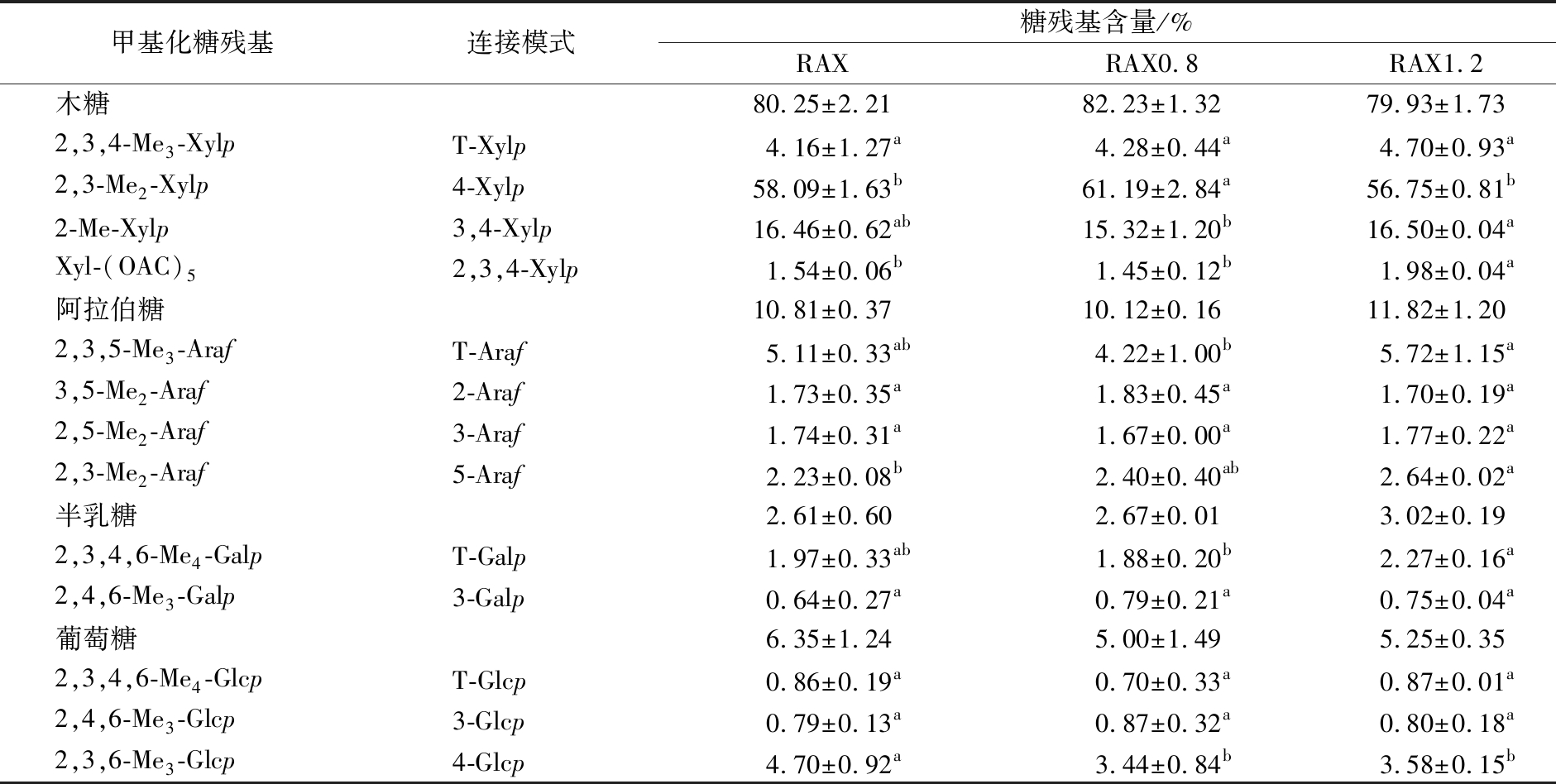
注:同一行中不同字母表示差异显著(P<0.05)。
甲基化糖残基连接模式糖残基含量/%RAXRAX0.8RAX1.2木糖80.25±2.2182.23±1.3279.93±1.732,3,4-Me3-XylpT-Xylp4.16±1.27a4.28±0.44a4.70±0.93a2,3-Me2-Xylp4-Xylp58.09±1.63b61.19±2.84a56.75±0.81b2-Me-Xylp3,4-Xylp16.46±0.62ab15.32±1.20b16.50±0.04aXyl-(OAC)52,3,4-Xylp1.54±0.06b1.45±0.12b1.98±0.04a阿拉伯糖10.81±0.3710.12±0.1611.82±1.202,3,5-Me3-ArafT-Araf5.11±0.33ab4.22±1.00b5.72±1.15a3,5-Me2-Araf2-Araf1.73±0.35a1.83±0.45a1.70±0.19a2,5-Me2-Araf3-Araf1.74±0.31a1.67±0.00a1.77±0.22a2,3-Me2-Araf5-Araf2.23±0.08b2.40±0.40ab2.64±0.02a半乳糖2.61±0.602.67±0.013.02±0.192,3,4,6-Me4-GalpT-Galp1.97±0.33ab1.88±0.20b2.27±0.16a2,4,6-Me3-Galp3-Galp0.64±0.27a0.79±0.21a0.75±0.04a葡萄糖6.35±1.245.00±1.495.25±0.352,3,4,6-Me4-GlcpT-Glcp0.86±0.19a0.70±0.33a0.87±0.01a2,4,6-Me3-Glcp3-Glcp0.79±0.13a0.87±0.32a0.80±0.18a2,3,6-Me3-Glcp4-Glcp4.70±0.92a3.44±0.84b3.58±0.15b
尽管RAX经SE处理前后,其糖残基种类未发生变化,但其糖残基含量存在差异。SE处理后,RAX的Araf残基含量先减少后增加,而Xylp残基含量先增加后减少,且T-Araf和4-Xylp含量变化分别与之相同。表明SE预处理在低压(0.8 MPa)时主要作用于RAX侧链的T-Araf,随着SE压强的增大,主要作用位点变为4-Xylp,进一步验证了上述单糖组成的结果。
2.4.4 1H NMR分析
如图4所示,分布在δ 5.6~5.0的质子信号归属于α-L-Araf[21],在δ 5.54、5.41、5.38、5.31、5.29和5.22处的信号分别代表A2(→2)-α-L-Araf-(1→)、AT(3 mX)(O-3单取代Xylp残基)、A5(→5)-α-L-Araf-(1→)、A3(→3)-α-L-Araf-(1→)、AT(3 dX)和AT(3 dX)(O-2,3双取代Xylp残基);而δ 4.7~4.3则归因于未取代、单取代和二取代的β-D-Xylp残基[18],包括X234(→2,3,4)-β-D-Xylp-(1→)、X34(→3,4)-β-D-Xylp-(1→)、XT(T-β-D-Xylp-(1→)和X4(→4)-β-D-Xylp-(1→),分别位于δ 4.64、4.54、4.49、4.47。
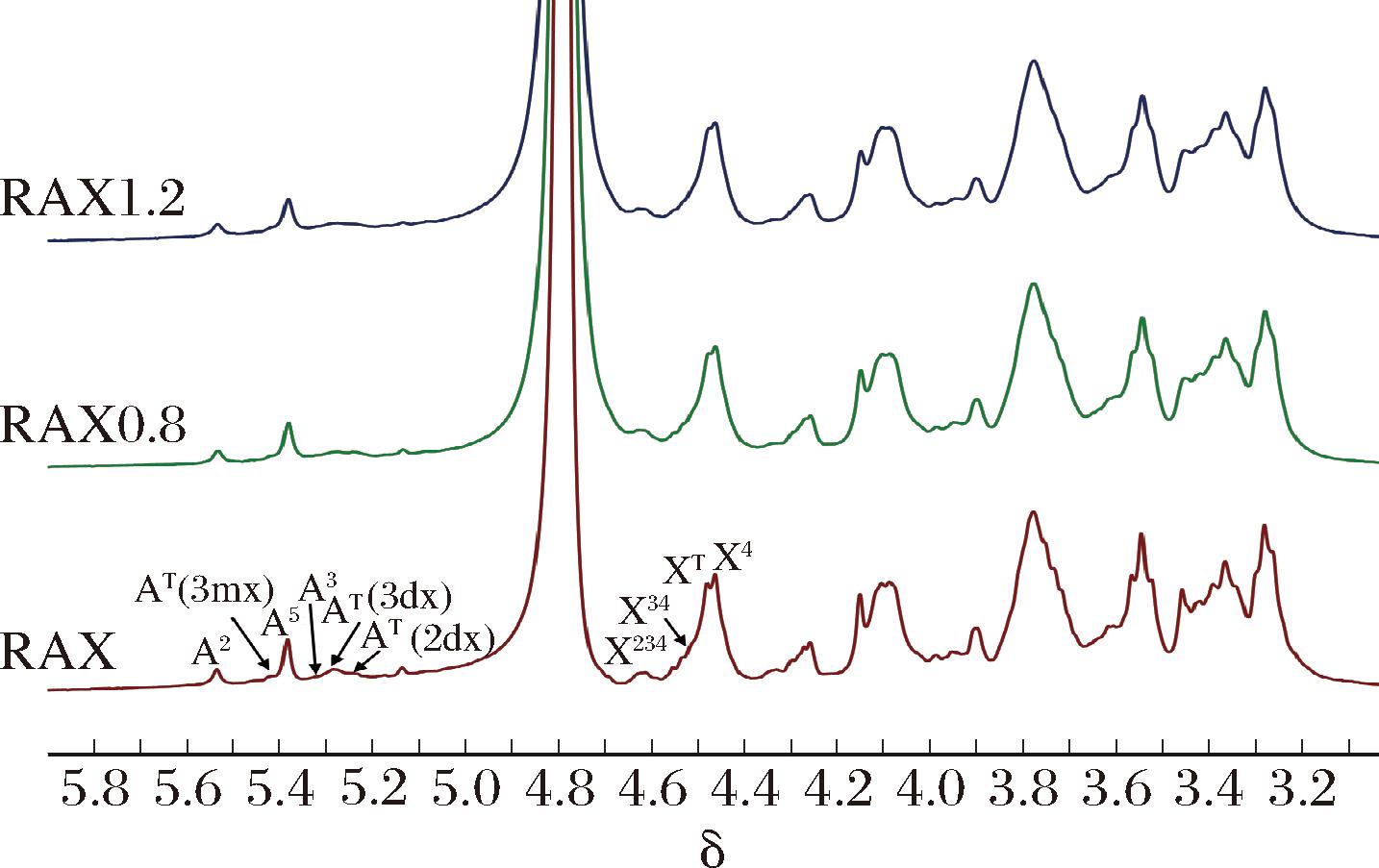
图4 RAX的1H NMR图谱
Fig.4 1H NMR spectra of RAX
此外,RAX中糖残基的化学位移和含量如表4所示,RAX0.8的α-L-Araf含量为23.37%,显著低于RAX(27.06%),表明SE处理在较低压强(0.8 MPa)时RAX侧链α-L-Araf连接断裂。与RAX和RAX0.8相比,RAX1.2的β-D-Xylp含量(71.95%)降低,并且X4变化趋势与之相同,表明在较高压强(1.2 MPa)时,SE处理对于RAX主链β-D-Xylp(X4)连接的破坏更为剧烈。1H NMR的分析结果与单糖和甲基化的结果相符。
表4 RAX的1H NMR分析
Table 4 1H NMR analysis of RAX
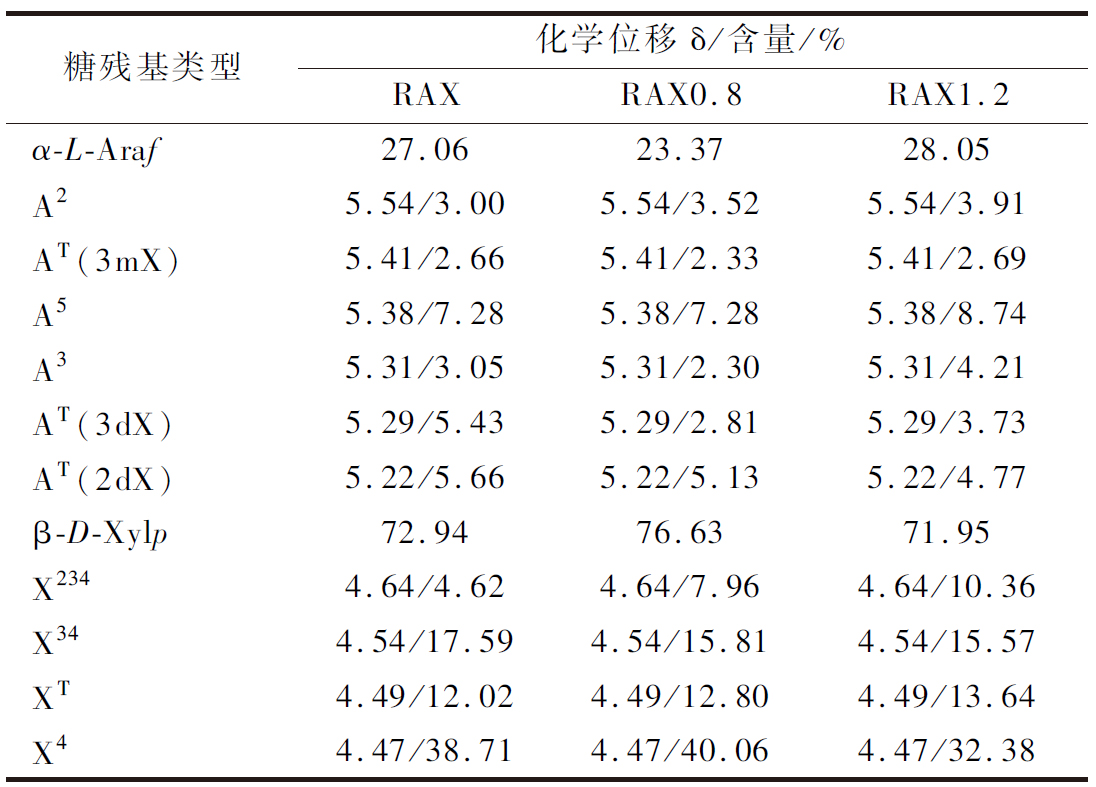
注:A2:→2)-α-L-Araf-(1→;AT(3 mX):连接在β-1,3,4-Xylp残基上的α-T-Araf;A5:→5)-α-L-Araf-(1→;A3:→3)-α-L-Araf-(1→;AT(3 dX)和AT(3 dX):连接在β-1,2,3,4-Xylp残基上的α-T-Araf;X234:→2,3,4)-β-D-Xylp-(1→;X34:→3,4)-β-D-Xylp-(1→;XT:T-β-D-Xylp-(1→;X4:→4)-β-D-Xylp-(1→。
糖残基类型化学位移δ/含量/%RAXRAX0.8RAX1.2α-L-Araf27.0623.3728.05A25.54/3.005.54/3.525.54/3.91AT(3mX)5.41/2.665.41/2.335.41/2.69A55.38/7.285.38/7.285.38/8.74A35.31/3.055.31/2.305.31/4.21AT(3dX)5.29/5.435.29/2.815.29/3.73AT(2dX)5.22/5.665.22/5.135.22/4.77β-D-Xylp72.9476.6371.95X2344.64/4.624.64/7.964.64/10.36X344.54/17.594.54/15.814.54/15.57XT4.49/12.024.49/12.804.49/13.64X44.47/38.714.47/40.064.47/32.38
2.5 SE预处理对RAX功能特性的影响
2.5.1 溶解度
如图5所示,SE预处理能够显著增加RAX的溶解度(P<0.05)。一般来说,RAX的溶解度与分子质量和阿魏酸含量呈负相关,与阿拉伯糖/木糖值呈正相关[30]。这是因为,高分子质量RAX能通过交联或聚合反应,增加分子链缠结和空间位阻,降低在水中的分散能力;较高阿魏酸含量会导致RAX链与链之间形成共价“双阿魏酸桥”交联,使RAX在水溶液中溶解度较低;阿拉伯糖/木糖值降低导致木糖主链的β-1,4糖苷键排列更规整,分子间氢键增强,结晶度提高,溶解性下降[31]。RAX0.8溶解性的增加可能是SE处理使其分子质量降低和酚酸含量降低的正向作用远大于阿拉伯糖/木糖值降低的负向作用。同时,RAX1.2的溶解度较RAX0.8显著降低的原因归于其较低的阿拉伯糖/木糖值导致多糖分子间氢键数量增加。总之,SE处理可以作为改善RAX溶解性的一种有效技术。
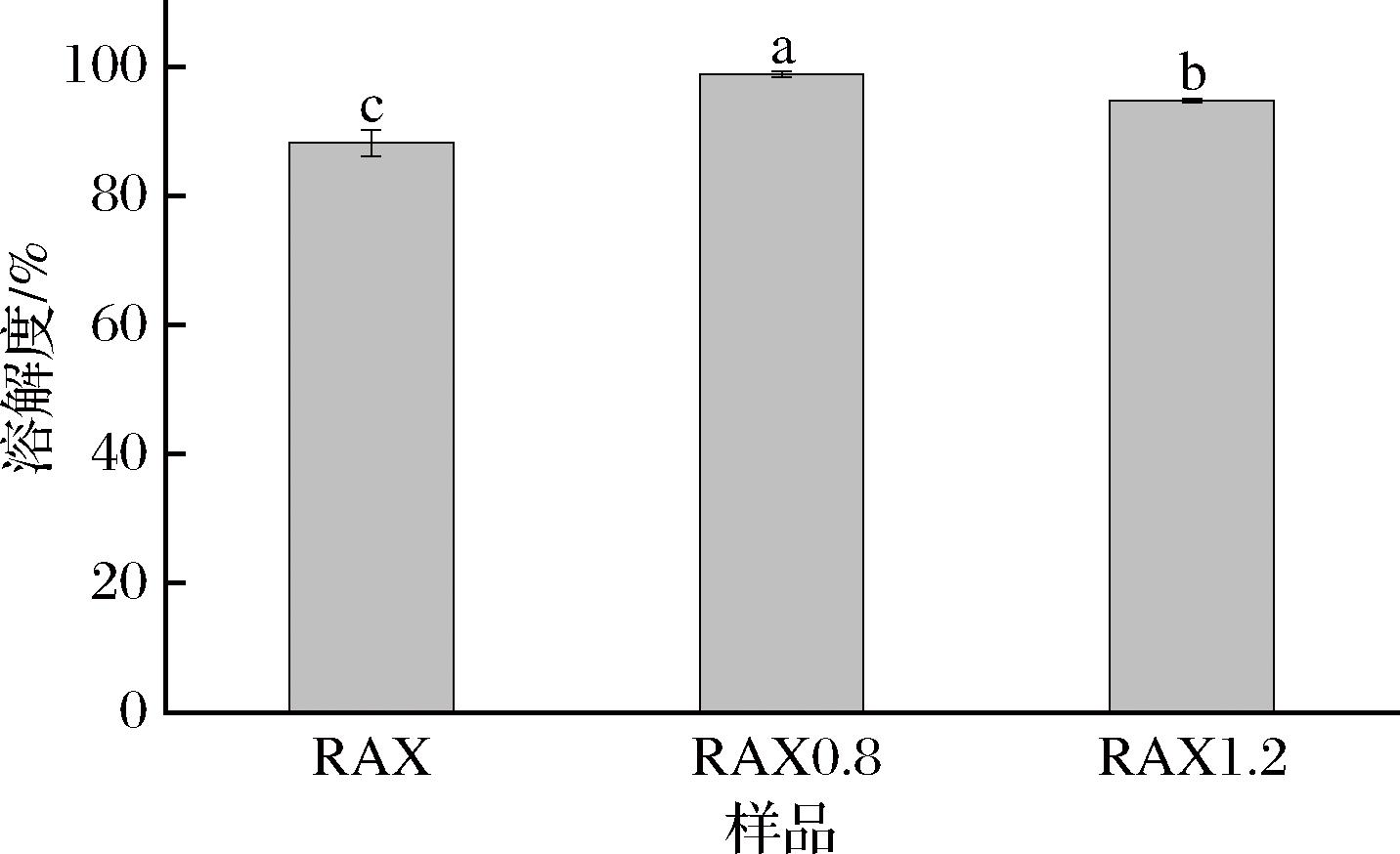
图5 SE预处理前后RAX的溶解度
Fig.5 Solubility of RAX before and after SE pretreatment
注:不同字母表示差异显著(P<0.05)。
2.5.2 流变学特性
2.5.2.1 表观黏度
如图6-a所示,所有RAX样品都表现出非牛顿流体的剪切稀化行为[19],即表观黏度随着剪切速率的增加而降低。此外,在相同剪切速率下,与RAX相比,SE预处理后的RAX0.8和RAX1.2溶液表现出较低的剪切黏度,且其表观黏度随着SE压强的增大而降低,与分子质量变化趋势一致。这种现象可能是由于SE处理后RAX分子质量和总酚含量显著降低,减少了链的缠结,使网状结构变得松散,最终表现为黏度的下降[27]。
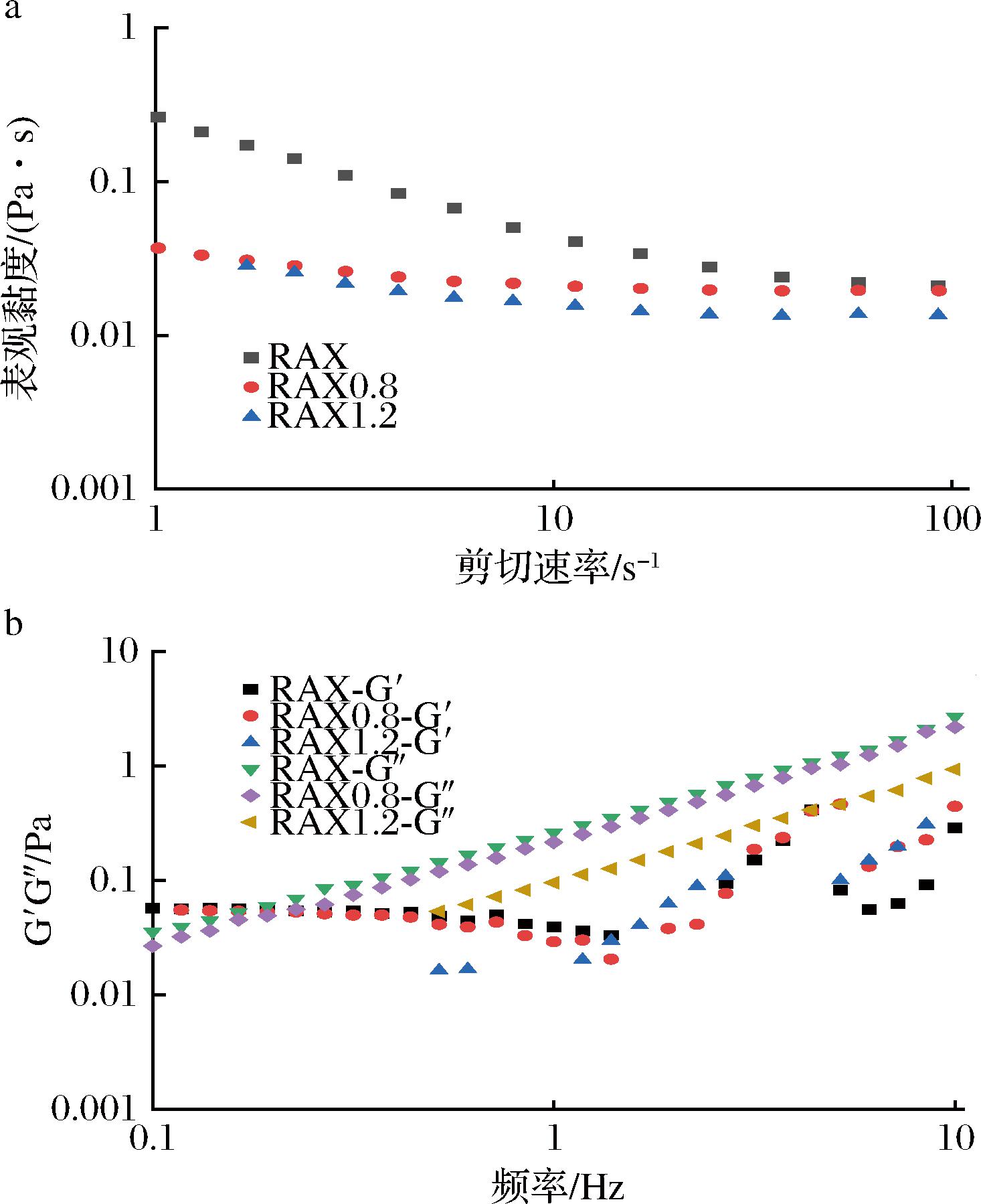
a-表观黏度;b-动态频率扫描
图6 SE预处理前后RAX的流变学特性
Fig.6 Rheological properties of RAX before and after SE pretreatment
2.5.2.2 动态黏弹性
如图6-b所示,随着振荡频率的增加,RAX溶液的G′和G″整体上呈现逐渐增加的趋势。可以观察到,RAX1.2的G″始终高于G′,表现出典型的类流体行为[19]。然而,RAX和RAX0.8的动态黏弹性显示出不同的现象,在低频率扫描条件下G′高于G″,表现出典型的类固体行为,表明其具有凝胶特性[32]。但在高扫描频率下G″高于G′,表现类流体行为,说明RAX和RAX0.8链结构间的相互作用力较弱,凝胶结构消失。特别是,与RAX溶液相比,RAX0.8溶液的G′和G″的交叉点向右移向更高的频率,说明其凝胶特性更好,这可能与RAX0.8存在更多的未取代木糖主链(61.19%)有关,从而赋予其更强的多糖分子间网络结构[33]。
2.6 SE预处理对RAX抗氧化活性的影响
2.6.1 DPPH自由基清除活性
如图7-a所示,在0.5~8 mg/mL,RAX、RAX0.8和RAX1.2的DPPH自由基清除活性随着质量浓度的增加无显著差异。在质量浓度为16 mg/mL时,其DPPH自由基清除率分别为21.84%、19.42%、15.47%,与其酚类含量的变化趋势一致,且RAX的DPPH自由基清除活性与总酚含量呈正相关。RAX的DPPH自由基清除活性较低,可能是因为其在环境温度下醇溶性差,影响与DPPH反应[34]。
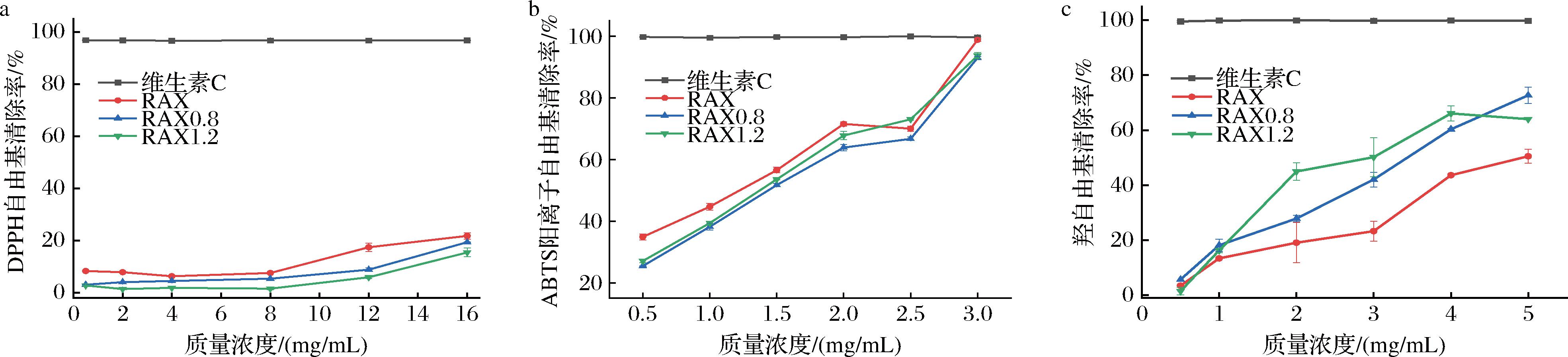
a-DPPH自由基清除活性;b-ABTS阳离子自由基清除活性;c-羟自由基清除活性
图7 SE预处理前后RAX的抗氧化活性
Fig.7 The antioxidant activity of RAX before and after SE pretreatment
2.6.2 ABTS阳离子自由基清除活性
如图7-b所示,RAX的ABTS阳离子自由基清除活性呈质量浓度依赖性,且大体上与总酚含量趋势一致。在质量浓度为3 mg/mL时,RAX的ABTS阳离子自由基清除率均达到90%以上,表明SE处理对于RAX的ABTS阳离子自由基清除能力的影响无显著差异。值得注意的是,RAX的ABTS阳离子自由基清除活性(3 mg/mL时)与阳性对照维生素C相当。
2.6.3 羟自由基清除活性
如图7-c所示,在质量浓度5 mg/mL时,对RAX的羟自由基清除率进行排序:RAX0.8>RAX1.2>RAX。但结果与预期不同,抗氧化活性并没有遵循与总酚含量相同的趋势。这可能是因为:a)SE预处理显著降低RAX分子质量,促进了还原性羟基末端的流动性和自由基的可及性;b)SE预处理可以改变酚类化合物的组成,并且取代基和空间构型的差异也可能导致不同的生物活性表现[24]。
3 结论
本研究表明,SE预处理能够破坏米糠细胞壁的紧密结构,使其表面呈现孔洞和褶皱,从而提高RAX得率。随着SE压强的增加,RAX分子质量和阿拉伯糖/木糖值降低,但不会改变RAX的主要官能团。甲基化和1H NMR结果显示,在低压强(0.8 MPa)时进行SE处理,主要作用于RAX侧链α-L-Araf,在较高压强(1.2 MPa)时主要作用点转变为主链β-4-Xylp。此外,SE预处理能够显著增加RAX的溶解度(P<0.05)和降低表观黏度,这被认为与分子质量和阿拉伯糖/木糖值的降低有关。SE预处理还能显著改变RAX的动态黏弹性行为,RAX0.8的凝胶性能优于RAX,这与其木糖主链较高的未取代程度有关。同时,SE预处理能够增加RAX的羟自由基的清除能力。综上所述,SE预处理能够改变RAX的理化特性(分子质量、化学组成和分支度)、功能特性(溶解性、表观黏度和黏弹性行为)和生理特性(抗氧化活性),在以上研究的基础上,可进一步探讨其作为一种有前景的谷物加工副产物高值化利用技术手段,拓宽其在食品工业中的应用领域。
[1] WANG Y H, LIANG H X, HU Z Y, et al.Evaluation of flavor properties in rice bran by solid-state fermentation with yeast[J].Food Chemistry:X, 2025, 28:102516.
[2] ABDUH M Y, ALYSSA S, BUTAR R A, et al.Effects of solid-state fermentation using Aspergillus niger on yield, total phenolic content, and antioxidant activity of defatted rice bran extract[J].Food Chemistry Advances, 2025, 7:100957.
[3] WEN Y, NIU M, ZHANG B J, et al.Structural characteristics and functional properties of rice bran dietary fiber modified by enzymatic and enzyme-micronization treatments[J].LWT, 2017, 75:344-351.
[4] 刘芳, 韩伟, 郭超, 等.米糠蛋白提取、改性及在食品加工中的应用[J].食品与发酵工业, 2025, 51(1):363-372.LIU F, HAN W, GUO C, et al.Research progress on extraction, modification and application of rice bran protein in food[J].Food and Fermentation Industries, 2025, 51(1):363-372.
[5] NOORMOHAMMADI M, GHORBANI Z, SHAHINFAR H, et al.Is there any hepatic impact associated with rice bran arabinoxylan compound supplementation? A systematic review and dose-response meta-analysis of randomized controlled trials[J].Clinical Nutrition ESPEN, 2023, 57:665-675.
[6] AYALA-SOTO F E, SERNA-SALD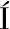 VAR S O, WELTI-CHANES J, et al.Phenolic compounds, antioxidant capacity and gelling properties of glucoarabinoxylans from three types of sorghum brans[J].Journal of Cereal Science, 2015, 65:277-284.
VAR S O, WELTI-CHANES J, et al.Phenolic compounds, antioxidant capacity and gelling properties of glucoarabinoxylans from three types of sorghum brans[J].Journal of Cereal Science, 2015, 65:277-284.
[7] 鄢宏浩, 蔡乔宇, 陈轩, 等.米糠多糖的提取纯化及生理功能活性研究进展[J].食品科技, 2020, 45(10):197-201.YAN H H, CAI Q Y, CHEN X, et al.Research progress in extraction, purification and physiological function activity of rice bran polysaccharide[J].Food Science and Technology, 2020, 45(10):197-201.
[8] PIETI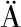 INEN S, MOLDIN A, STRÖM A, et al.Effect of physicochemical properties, pre-processing, and extraction on the functionality of wheat bran arabinoxylans in breadmaking—A review[J].Food Chemistry, 2022, 383:132584.
INEN S, MOLDIN A, STRÖM A, et al.Effect of physicochemical properties, pre-processing, and extraction on the functionality of wheat bran arabinoxylans in breadmaking—A review[J].Food Chemistry, 2022, 383:132584.
[9] XI H H, WANG A X, QIN W Y, et al.The structural and functional properties of dietary fibre extracts obtained from highland barley bran through different steam explosion-assisted treatments[J].Food Chemistry, 2023, 406:135025.
[10] KONG F, LI Y, QIU X R, et al.Modification of Tartary buckwheat flour via steam explosion and the quality characteristics of corresponding gluten-free whole-grain cookies[J].LWT, 2024, 213:117066.
[11] TIAN X Y, LIU J F, QIAO C C, et al.Functional properties and structure of soluble dietary fiber obtained from rice bran with steam explosion treatment[J].Journal of Cereal Science, 2024, 118:103938.
[12] TIAN X Y, LIU J F, CHENG Z, et al.Structure, thermal stability, physicochemical and functional characteristics of insoluble dietary fiber obtained from rice bran with steam explosion treatment:Effect of different steam pressure and particle size of rice bran[J].Food Research International, 2024, 187:114310.
[13] MA Q, WANG X, ZHANG R F, et al.Structural, physicochemical and functional properties of dietary fiber from black rice bran treated by different processing methods[J].Food Bioscience, 2025, 65:106025.
[14] ZHOU S X, TANG X J, HEGYI F, et al.In vitro digestion and fermentation characteristics of soluble dietary fiber from adlay (Coix lacryma-jobi L.var.ma-yuen Staft) bran modified by steam explosion[J].Food Research International, 2024, 192:114747.
[15] 姜元荣, 姚惠源, 陈正行, 等.碱溶性米糠多糖的提取及其免疫调节功能研究[J].中国粮油学报, 2004, 19(6):1-3;7.JIANG Y R, YAO H Y, CHEN Z X, et al.Extraction of alkali-soluble rice bran polysaccharide (ASRBP) and its immunity effect[J].Journal of the Chinese Cereals and Oils Association, 2004, 19(6):1-3;7.
[16] DUBOIS M, GILLES K A, HAMILTON J K, et al.Colorimetric method for determination of sugars and related substances[J].Analytical Chemistry, 1956, 28(3):350-356.
[17] BLUMENKRANTZ N, ASBOE-HANSEN G.New method for quantitative determination of uronic acids[J].Analytical Biochemistry, 1973, 54(2):484-489.
[18] KANG J, HUANG-FU Z Y, TIAN X N, et al.Arabinoxylan of varied structural features distinctively affects the functional and in vitro digestibility of wheat starch[J].Food Hydrocolloids, 2023, 140:108615.
[19] JIA X, XU Z Y, XIAO M, et al.Conformational and rheological property comparison for three exudates gums containing type II arabinogalactans[J].Food Hydrocolloids, 2025, 164:111163.
[20] GUO Q B, CUI S W, WANG Q, et al.Structural characterization of a low-molecular-weight heteropolysaccharide (glucomannan) isolated from Artemisia sphaerocephala Krasch[J].Carbohydrate Research, 2012, 350:31-39.
[21] 张秀敏, 周增超, 乔晋丽, 等.麦麸品种与提取方式对阿拉伯木聚糖结构及抗氧化性的影响[J].食品科学, 2023, 44(3):31-40.ZHANG X M, ZHOU Z C, QIAO J L, et al.Effects of wheat bran varieties and extraction methods on the structure and antioxidant activity of arabinoxylan[J].Food Science, 2023, 44(3):31-40.
[22] CHEN Y S, SHAN S R, CAO D M, et al.Steam flash explosion pretreatment enhances soybean seed coat phenolic profiles and antioxidant activity[J].Food Chemistry, 2020, 319:126552.
[23] PANG T R, WANG L, KONG F, et al.Steam explosion pretreatment:Dramatic reduction in energy consumption for wheat bran grinding[J].Journal of Cereal Science, 2024, 117:103893.
[24] WANG Z Y, DENG Z Y, YU C W, et al.Effects of steam explosion on raspberry leaf structure and the release of water-soluble nutrients and phenolics[J].Food Chemistry, 2024, 445:138708.
[25] GE Q, XIAO G M, WANG L Y, et al.Effect of steam explosion pretreatment on the fermentation characteristics of polysaccharides from tea residue[J].International Journal of Biological Macromolecules, 2024, 279:134920.
[26] YI J P, LI X, WANG S, et al.Steam explosion pretreatment of Achyranthis bidentatae Radix:Modified polysaccharide and its antioxidant activities[J].Food Chemistry, 2022, 375:131746.
[27] QIANG Y Y, HE M Y, ZHANG S Y, et al.Pressure-controlled steam explosion as pretreatment for efficient extraction of Tremella fuciformis polysaccharide:Structure and bioactivity[J].International Journal of Biological Macromolecules, 2024, 280:135766.
[28] GUO Q B, XIAO X Y, LI C R, et al.Catechin-grafted arabinoxylan conjugate:Preparation, structural characterization and property investigation[J].International Journal of Biological Macromolecules, 2021, 182:796-805.
[29] ZHANG X W, XIE J H, CHEN T T, et al.High arabinoxylan fine structure specificity to gut bacteria driven by corn genotypes but not environment[J].Carbohydrate Polymers, 2021, 257:117667.
[30] BILAL M, LI D D, XIE C, et al.Recent advances of wheat bran arabinoxylan exploitation as the functional dough additive[J].Food Chemistry, 2025, 463:141146.
[31] MATHEW S, KARLSSON E N, ADLERCREUTZ P.Extraction of soluble arabinoxylan from enzymatically pretreated wheat bran and production of short xylo-oligosaccharides and arabinoxylo-oligosaccharides from arabinoxylan by glycoside hydrolase family 10 and 11 endoxylanases[J].Journal of Biotechnology, 2017, 260:53-61.
[32] SHI S, FENG D, ZHANG T, et al.Characterization and rheological behavior of arabinoxylan extracted from reed straw by tetramethylammonium hydroxide aqueous solution[J].Industrial Crops and Products, 2024, 214:118524.
[33] IZYDORCZYK M S, BILIADERIS C G.Effect of molecular size on physical properties of wheat arabinoxylan[J].Journal of Agricultural and Food Chemistry, 1992, 40(4):561-568.
[34] LIU X F, HUANG L F, ZHANG X W, et al.Polysaccharides with antioxidant activity:Extraction, beneficial roles, biological mechanisms, structure-function relationships, and future perspectives:A review[J].International Journal of Biological Macromolecules, 2025, 300:140221.