衰老是生命进程中不可避免的自然规律,而且是一种不可逆的生命过程,在衰老过程中,会诱发多种疾病,如肿瘤[1]、神经退行性疾病、心血管疾病等[2]。研究发现,衰老可能由氧化损伤引起[3],氧化应激是自由基和反应性代谢物如氧化剂或活性氧的产生与其通过保护机制消除之间的不平衡[4]。这种不平衡会导致机体活性氧含量增多,从而加速细胞衰老。根据衰老的氧化应激理论,与年龄相关的功能损失是由于活性氧(reactive oxygen species,ROS)和NO对生物大分子的氧化损伤积累造成的结果[5]。因此,通过提高机体抗氧化能力延缓衰老具有重要意义。
天然植物多糖能够消除氧自由基,提高抗氧化能力[6]。羊肚菌是一种药食兼备食用菌,羊肚菌富含蛋白质、脂质、多糖、维生素及矿物质等多种营养成分,具有十分显著的食用、药用价值[7],主要表现为抗氧化、抗炎症、免疫调节、抗肿瘤、抗肥胖等多种生物学作用[8]。羊肚菌多糖(Morchella polysaccharide)作为羊肚菌主要活性成分之一,具有良好的保护肝脏[9]、调节脂质代谢[10]、调节肠道菌群[11]、降血糖等生物活性功能。国内对于羊肚菌多糖抗衰老化活性方面的相关研究已有报道,例如,BADSHAH等[12]从羊肚菌中提取羊肚菌多糖,且证明了羊肚菌多糖具有中等的体外自由基清除率。熊川等[13]研究结果表明,六妹羊肚菌多糖能够缓解过氧化氢作用的急性氧化损伤,抑制PC12细胞凋亡。闫永兰[14]的研究结果表明,羊肚菌多糖能够提高小白鼠的抗氧化和抗衰老能力。目前尚未见对于羊肚菌多糖抗衰老通路的探究。
秀丽隐杆线虫作为一种雌雄同体[15]动物,具有体积小、生长周期短、培养条件简单等特点。因其与人类高度相似的基因组而被认为是研究活性物质生物活性功能评价的首要模型动物[16]。
本研究以羊肚菌为实验材料,通过测定其对秀丽隐杆线虫模型寿命、生殖能力、体长、运动水平、抗热应激能力及抗氧化应激能力各项生理指标的影响,探究羊肚菌抗衰老的规律及机制,为羊肚菌产品的二度开发奠定理论基础。
1 材料与方法
1.1 材料与试剂
羊肚菌多糖,陕西天奇生物科技有限公司;尿嘧啶缺陷型大肠杆菌菌株OP50、野生型秀丽隐杆线虫N2、转基因型线虫DA1116(eat-2)、CB1876(clk-1)、CF1903(glp-1)和CB1370(daf-2)由实验室保存;超氧化物歧化酶(superoxide dismutase,SOD)试剂盒、微量丙二醛(malondialdehyde,MDA)试剂盒、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-PX)试剂盒、ROS试剂盒,南京建成生物公司研究所;胡桃醌(≥95%),山东科源生化有限公司;维生素E(≥98%),沪慧(上海)生物科技有限公司。
1.2 仪器与设备
SW-CJ-2D超净工作台,上海沪净医疗器械有限公司;ZS7045体式显微镜,余姚市晟达仪器有限公司;IBE2000荧光倒置显微镜,重庆奥特光学仪器有限公司;SpectraMax M3荧光酶标仪,Molecular Devices公司;H 1850 R高速冷冻离心机,湖南湘仪实验室仪器开发有限公司;LRHS-250-II恒温恒湿箱,上海跃进医疗器械有限公司。
1.3 实验方法
1.3.1 线虫的培养及同期化
线虫的培养如图1所示,N2野生型秀丽隐杆线虫、饮食限制信号通路基因缺陷型线虫DA1116(eat-2)、线粒体信号通路基因缺陷型线虫CB1876(clk-1)、生殖信号通路基因缺陷型线虫CF1903(glp-1)在涂有Escherichia coli OP50的线虫生长培养基(nematode growth medium,NGM)上于20 ℃恒温培养,胰岛素信号通路基因缺陷型线虫CB1370(daf-2)在涂有E.coli OP50的NGM培养基上于16 ℃恒温培养。同步化采用次氯酸钠法:用8%(体积分数)次氯酸钠裂解产卵期成虫,收集在离心管中离心,去除上清液,沉淀经M9缓冲液洗涤2~3次后,将虫卵转移至含有100 μL OP50的NGM培养基培养48 h,获得L4期同期化线虫[17]。
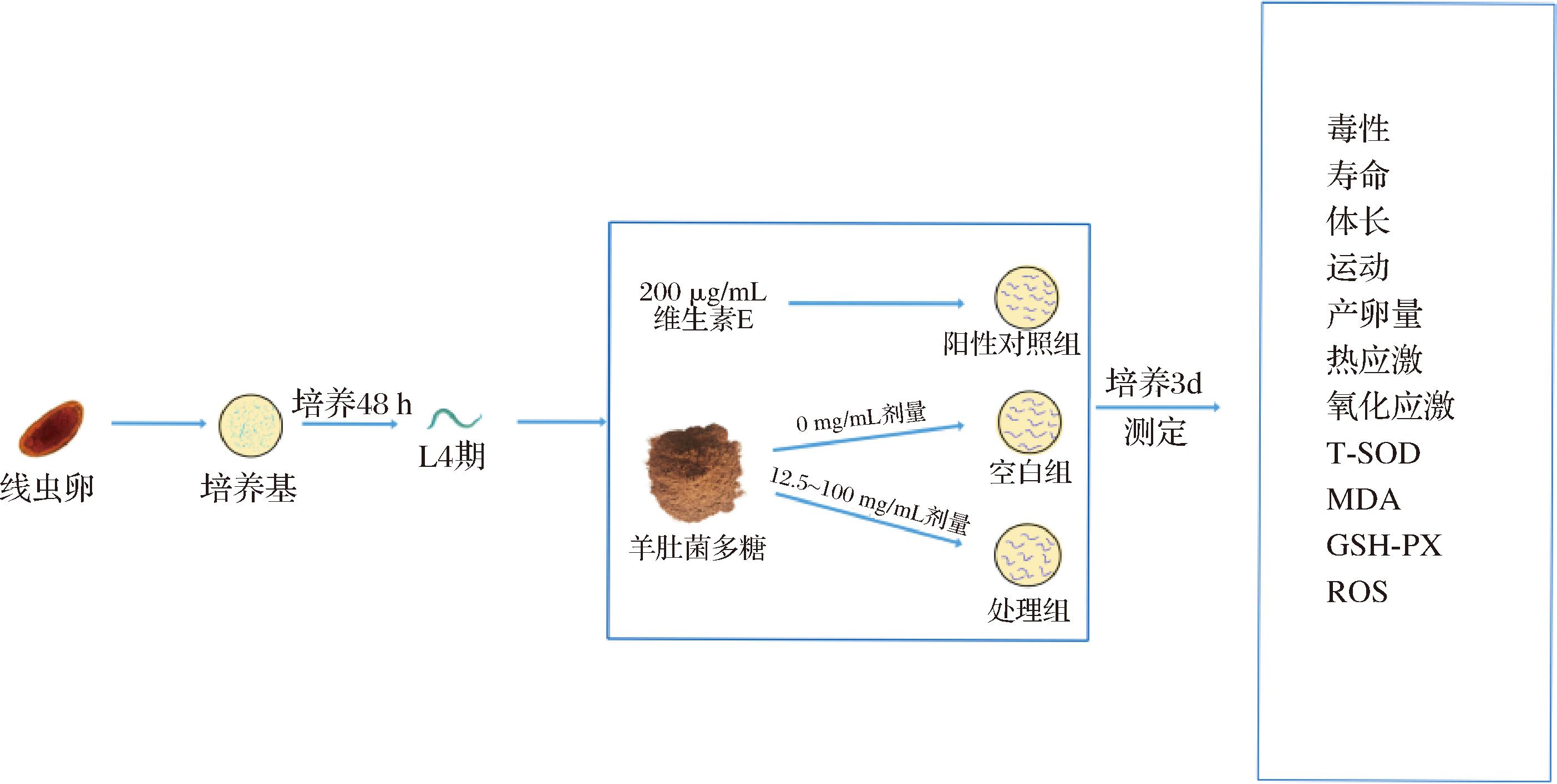
图1 实验流程示意图
Fig.1 Schematic diagram of test process
1.3.2 秀丽隐杆线虫毒性实验
取羊肚菌多糖溶于dd H2O中,配制成质量浓度分别为400、200、100、50、25、12.5、6.25、3.125 mg/mL的溶液,作为稀释OP50的稀释液。分别吸取上述8个不同质量浓度溶液200 μL,置于96孔板中,每个质量浓度8个平行。将同期化并生长至L4期的线虫置于每个质量浓度溶液中,每孔30只,24 h后计存活线虫数量。
1.3.3 实验分组
空白对照组:涂布有100 μL OP50 食物的NGM培养板。阳性对照组:涂布有100 μL质量浓度为200 μg/mL的维生素E和OP50混合物的NGM培养板。处理组:分别涂布有100 μL质量浓度为100、50、25、12.5 mg/mL的羊肚菌多糖和OP50混合物的NGM培养板。
1.3.4 寿命测定
参照LUO等[18]的方法稍作修改。将1.3.1节中生长至L4期的N2线虫挑入各组新平板上,每板30条线虫,每组3个平行,置于20 ℃培养箱中培养。每隔24 h将线虫转移至新板上,并记录线虫存活数量,直至线虫全部死亡。用挑针触碰线虫,未有反应则记为死亡。
1.3.5 运动能力测定
参照甘爱园等[19]的方法稍作修改。将1.3.1节中生长至L4期的N2线虫挑入各组新平板中,每板30条线虫,每组3个平行,置于20 ℃培养箱中培养。在给药的第6(早期)、10(中期)、14天(中晚期),测定其运动能力。秀丽隐杆线虫运动性被评估并分为三类:A、B和C。具有自发正弦运动的归为A类,不能进行正弦运动但仍有整体运动的线虫归为B类,仅在刺激头部和尾部时才显示运动的线虫归为C类。
1.3.6 产卵量测定
参照ZHANG等[20]的方法稍作修改。将1.3.1节中生长至L4期的N2线虫挑入各组新平板中,每板2条线虫,每组3个平行,置于20 ℃培养箱中培养。板中产卵期的线虫每天转至新的培养板中,直至线虫产卵期结束。
1.3.7 体长测定
参照WU等[21]的方法并稍做修改。将1.3.1节中生长至L4期的N2线虫挑入各组新平板上,每板10条线虫,每组3个平行,置于20 ℃培养箱。在给药的第3、6、14天,从平板中随机选取运动良好的线虫,并在麻醉后拍照。使用 ImageJ 中的分段线工具测量体长。
1.3.8 抗热应激能力测定
参照SHI等[22]的方法稍作修改。将1.3.1节中生长至L4期的N2线虫挑入各组新平板中,每板30条线虫,每组3个平行,置于20 ℃培养箱中培养48 h后,将线虫挑入不含OP50的新板中,置于37 ℃的培养箱中以实现热应激条件。显微镜下每1 h观察线虫的存活情况并计数,直至线虫全部死亡。用铂丝轻触线虫头部及尾部无反应的个体则视为死亡。
1.3.9 胡桃醌诱导N2线虫的氧化应激实验
参照王刚[23]的方法稍作修改。将1.3.1节中生长至L4期的N2线虫,分别挑入羊肚菌多糖含量为0、12.5、25、50、100 mg/mL的NGM培养基以及含有维生素E的NGM培养基上常规培养3 d,之后将线虫挑入含有胡桃醌(200 μg/mL)的培养基上,置于20 ℃培养箱培养,6 h时观察并记录线虫的存活情况,并计算生存率。每板30条线虫,每组3个平行。
1.3.10 体内ROS、MDA、T-SOD、GSH测定
野生型N2线虫培养同1.3.1节。将胡桃醌处理6 h后的线虫使用M9缓冲液将线虫冲洗并收集至EP管中,放入组织研磨机中研磨成浆,2 500 r/min 离心10 min,取上清液。参照南京建成生物工程研究所试剂盒说明书测定线虫体内ROS、MDA、T-SOD、GSH-PX。实验重复3次。
1.3.11 胡桃醌诱导基因缺陷型线虫的氧化应激实验
参照赵佳乐等[24]的方法稍作修改。将1.3.1节中生长至L4期的DA1116、CB1876、CF1903、CB1370线虫,分别挑入不同质量浓度羊肚菌多糖NGM培养基上常规培养3 d,之后将线虫挑入含有胡桃醌(200 μg/mL)的培养基上,DA1116(eat-2)、CB1876(clk-1)和CF1903(glp-1)置于20 ℃培养箱培养,CB1370(daf-2)置于16 ℃培养箱培养,之后每2 h计线虫死亡数量。每板30条线虫,每组3个平行。
1.4 数据处理
采用SPSS27软件单因素方差分析(ANOVA)对所有数据统计分析,P<0.05被认为具有显著差异。运用Origin 2021软件对数据进行作图。
2 结果与分析
2.1 羊肚菌多糖有效浓度筛选
结果如图2所示,24 h后400 mg/mL 羊肚菌多糖喂食线虫存活率为0%,200 mg/mL喂食线虫存活率为45.5%,100 mg/mL羊肚菌多糖喂食线虫存活率为95%,50、25、12.5、6.25、3.125 mg/mL羊肚菌多糖喂食线虫存活率均为100%。所以最终选取100、50、25、12.5 mg/mL 4个质量浓度进行后续实验。
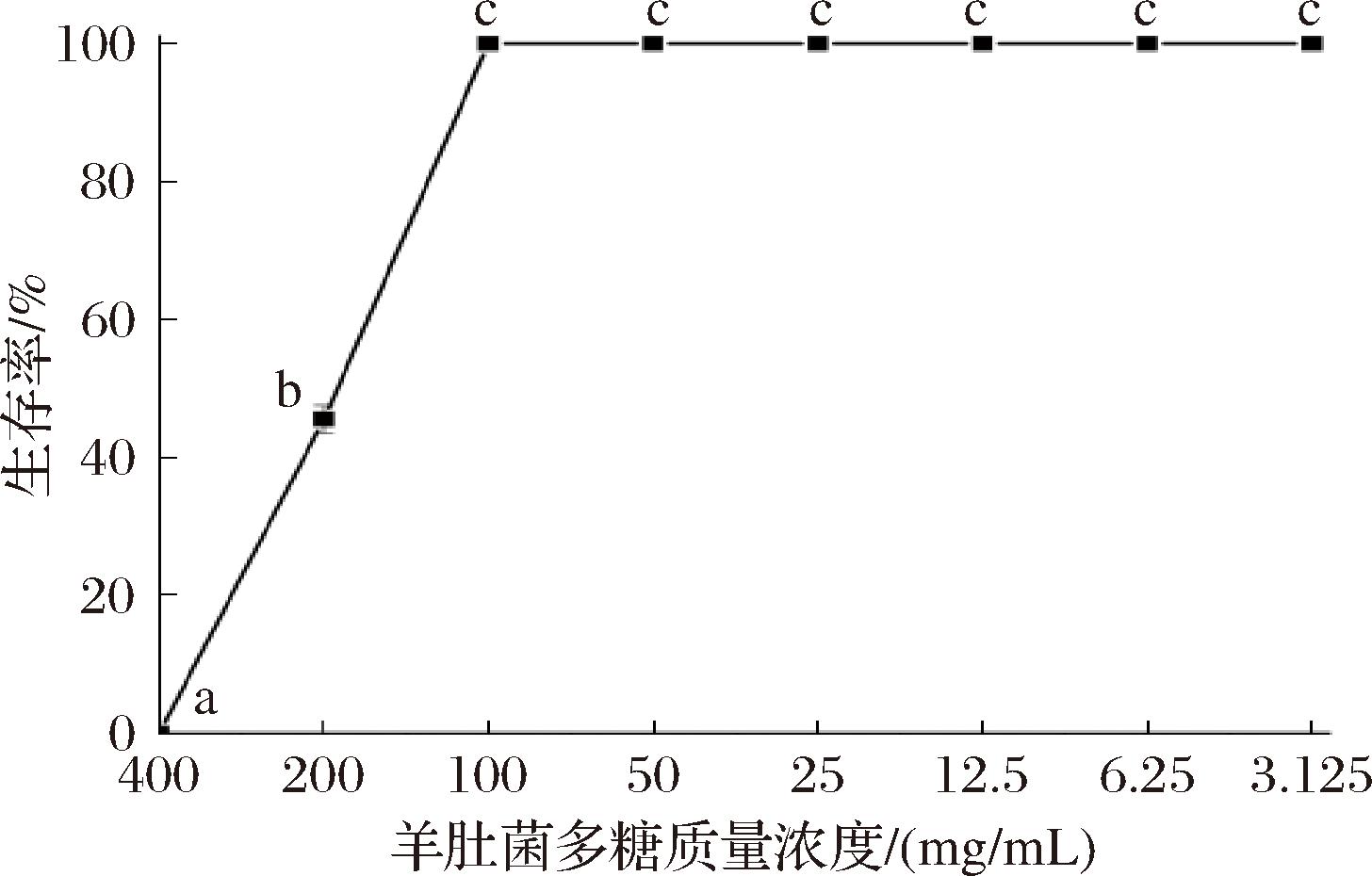
图2 不同浓度羊肚菌多糖对线虫存活率的影响
Fig.2 Effects of different concentrations of Morchella polysaccharide on the survival rate of nematodes
注:同一指标中,相同标记字母的为差异不显著(P>0.05),不同标记字母的为差异显著(P<0.05)(下同)。
2.2 羊肚菌多糖对线虫寿命及运动能力的影响
羊肚菌多糖能否延缓衰老的重要指标之一是寿命。由图3-a可知,空白对照组线虫的平均寿命为15.7 d,喂养100、50、25、12.5 mg/mL羊肚菌多糖的线虫平均寿命分别为18.17、16.83、16.63、16.87 d,相比于空白对照组,平均寿命分别延长了6.08%、15.86%、7.36%、6.08%、7.57%,具有显著性差异(P<0.05)。且与阳性对照组相比,经100 mg/mL羊肚菌多糖处理的线虫平均寿命显著延长了2%,该实验结果表明羊肚菌多糖能够延长线虫的寿命,且延寿效果能够接近阳性对照组的水平。这与WANG等[25]使用茶树菇多糖喂养线虫并延长寿命的结果相似。线虫的衰老与肌肉退化能力有关[26]。良好的运动能力使得线虫保持较高的摄食率,因此运动能力可反映线虫的健康状态[27]。由图3-b可知,不需外界刺激即可自发运动的线虫(A类)占比随着时间的延长逐渐下降,在第14天时,空白对照组A类线虫所占比例均低于羊肚菌多糖处理组。第5天时,处理组线虫运动能力良好,但空白对照组开始出现C类运动,这说明未经羊肚菌多糖处理的线虫已经开始出现衰老现象。在第10天时,处理组线虫运动能力均优于空白对照组。在第14天的时候,空白对照组C类运动占比35.29%,但羊肚菌多糖处理组A类运动占比分别为15.47%、9.93%、10%、19.28%,均低于空白对照组,且接近于阳性对照组的11.59%。这说明羊肚菌多糖在延缓线虫衰老、提高线虫的运动状态方面具有巨大的潜力。
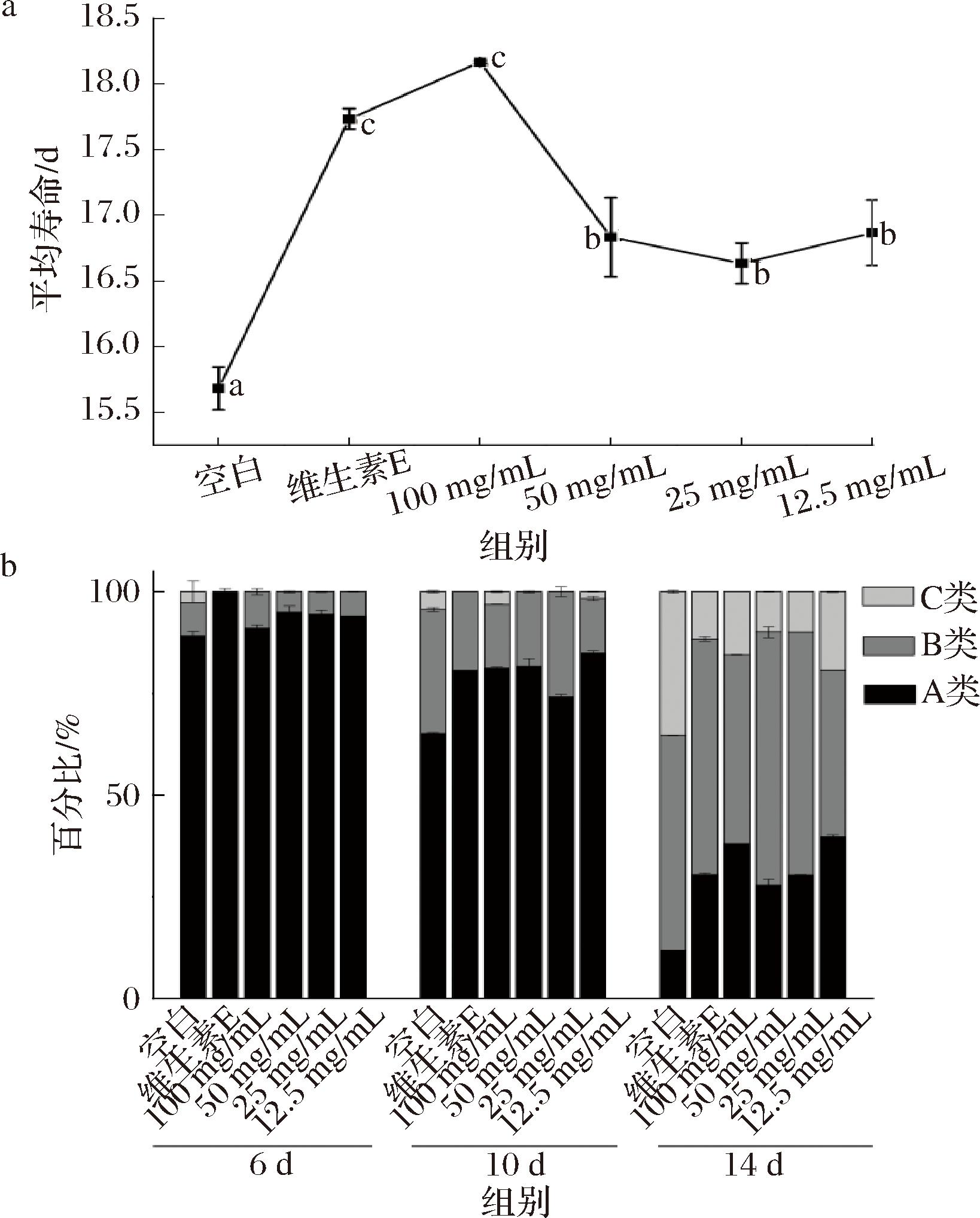
a-平均寿命;b-运动能力
图3 羊肚菌多糖对线虫平均寿命和运动能力的影响
Fig.3 Effects of Morchella polysaccharide on mean lifespan and locomotor activity of C.elegans
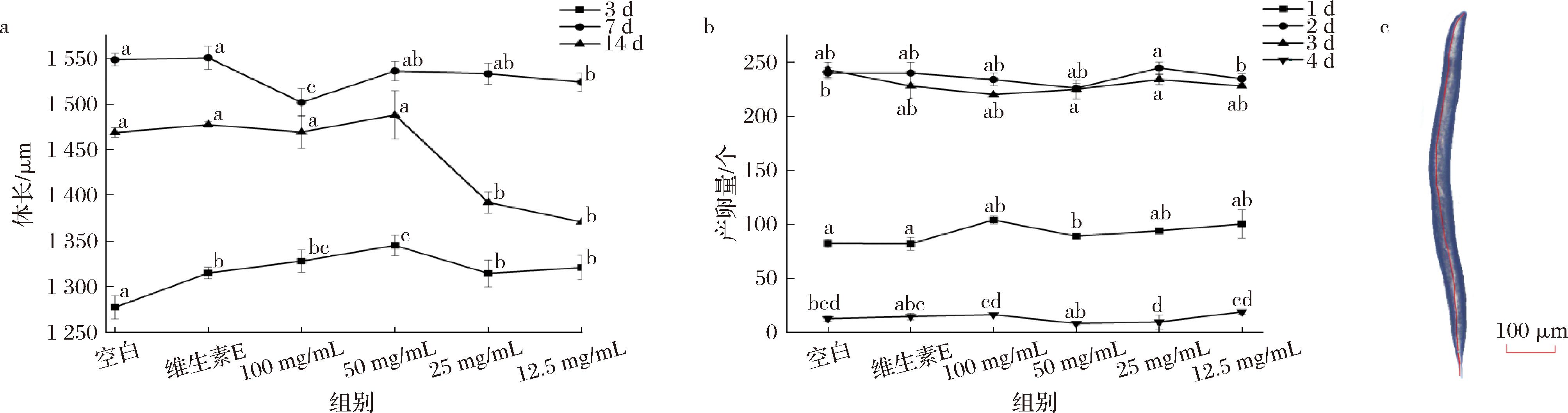
a-体长;b-产卵量;c-体长测量
图4 羊肚菌多糖对线虫体长和产卵量的影响
Fig.4 Effects of Morchella polysaccharide on body length and fecundity of C.elegans
2.3 羊肚菌多糖对线虫产卵量及体长的影响
由图4-b可知,不同质量浓度羊肚菌多糖对线虫的生殖能力没有显著影响。由图4-a可知,不同浓度羊肚菌多糖对线虫体长有显著影响。第3天时,处理组线虫体长显著高于空白对照组。第7天时,各组体长差异不显著。第14天时,与空白对照组相比,25、12.5 mg/mL羊肚菌多糖组体长分别显著降低(P<0.05)了5.2%和6.6%。因此,羊肚菌多糖对秀丽隐杆线虫生命周期的影响可能与“对有限资源的矛盾需求”理论有关,导致能量从生长发育转移到维持生存[28]。
2.4 羊肚菌多糖对线虫抗应激能力的影响
线虫抗压能力增强表明其寿命能随之延长。由图5-a可知,在37 ℃环境下,第11 h时,空白对照组生存率为0%,阳性对照组和12.5 mg/mL处理组生存率分别为6%和5%,生存率均高于空白对照组。且12.5 mg/mL处理组的生存率在第13天时趋近于0%,寿命显著高于空白组(P<0.05)。表明羊肚菌多糖处理能够增强线虫抗热应激能力。图5-b显示,在胡桃醌诱导的氧化应激条件下,阳性对照组和100、50、25、12.5 mg/mL处理组生存率分别为93.21%、96.50%、94.18%、93.03%、91.97%,与对照组相比分别显著升高了10.54%、14.44%、11.69%、10.32%、9.07%(P<0.05)。
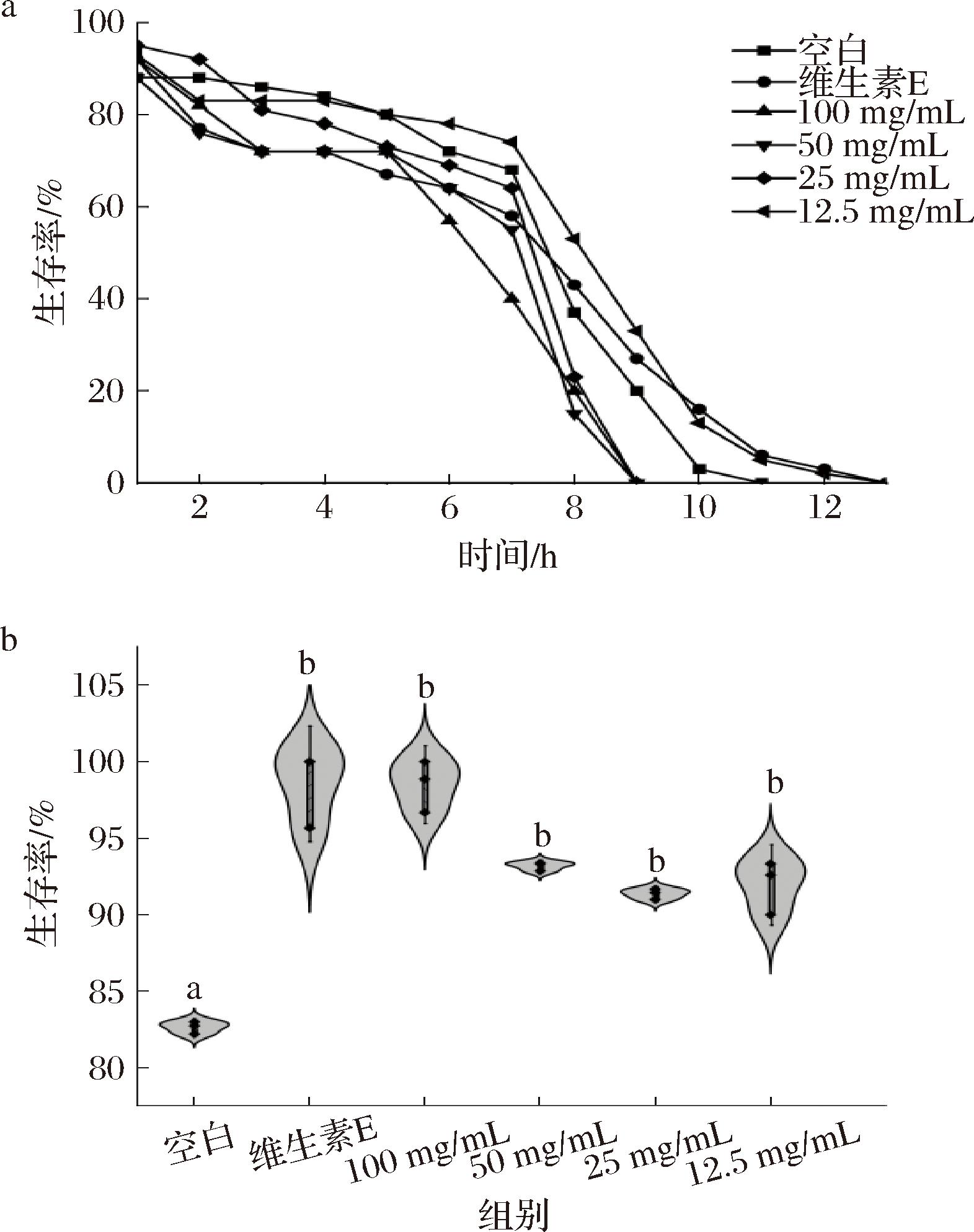
a-抗热应激能力;b-抗氧化应激能力
图5 羊肚菌多糖对线虫抗应激能力的影响
Fig.5 Effect of Morchella polysaccharide on anti-stress ability of nematodes
氧化应激发生时可导致错误折叠的蛋白累积,从而增加炎症和突变的发生率,因此氧化应激是导致线虫衰老的原因之一[29]。这也表明羊肚菌多糖能够提高胡桃醌胁迫的抗氧化应激能力,从而降低线虫衰老速率。
2.5 羊肚菌多糖对线虫体内T-SOD、MDA、GSH-PX和ROS的影响
为了减轻由衰老引起的氧化应激的影响,生物体会激活细胞内抗氧化酶系统,包括SOD和GSH-PX等[30]。ROS的过度产生会使氧化损伤加速,导致线粒体损伤、DNA突变等功能损害。并且当ROS对细胞脂质层造成损伤后,会生成脂质过氧化物MDA[31]。还原性谷胱甘肽(glutathione,GSH)可以与自由基结合加速自由基排泄[32],GSH-PX能够催化GSH对过氧化氢的还原反应,从而起到保护细胞膜结构等作用。
由图6可知,羊肚菌多糖处理组线虫与空白对照组相比,体内T-SOD活力提高了3.02~7.35倍,MDA含量降低了32%~79%。羊肚菌多糖处理的线虫体内GSH-PX活力显著升高(P<0.05)。经100、50、25 mg/mL羊肚菌多糖处理后线虫的荧光强度相较于空白对照和阳性对照组均显著下降(P<0.05)。上述结果也表明,羊肚菌多糖能够提高线虫体内抗氧化物酶水平和参与体内氧化还原反应,间接改善了氧化应激模型线虫的衰老现象。
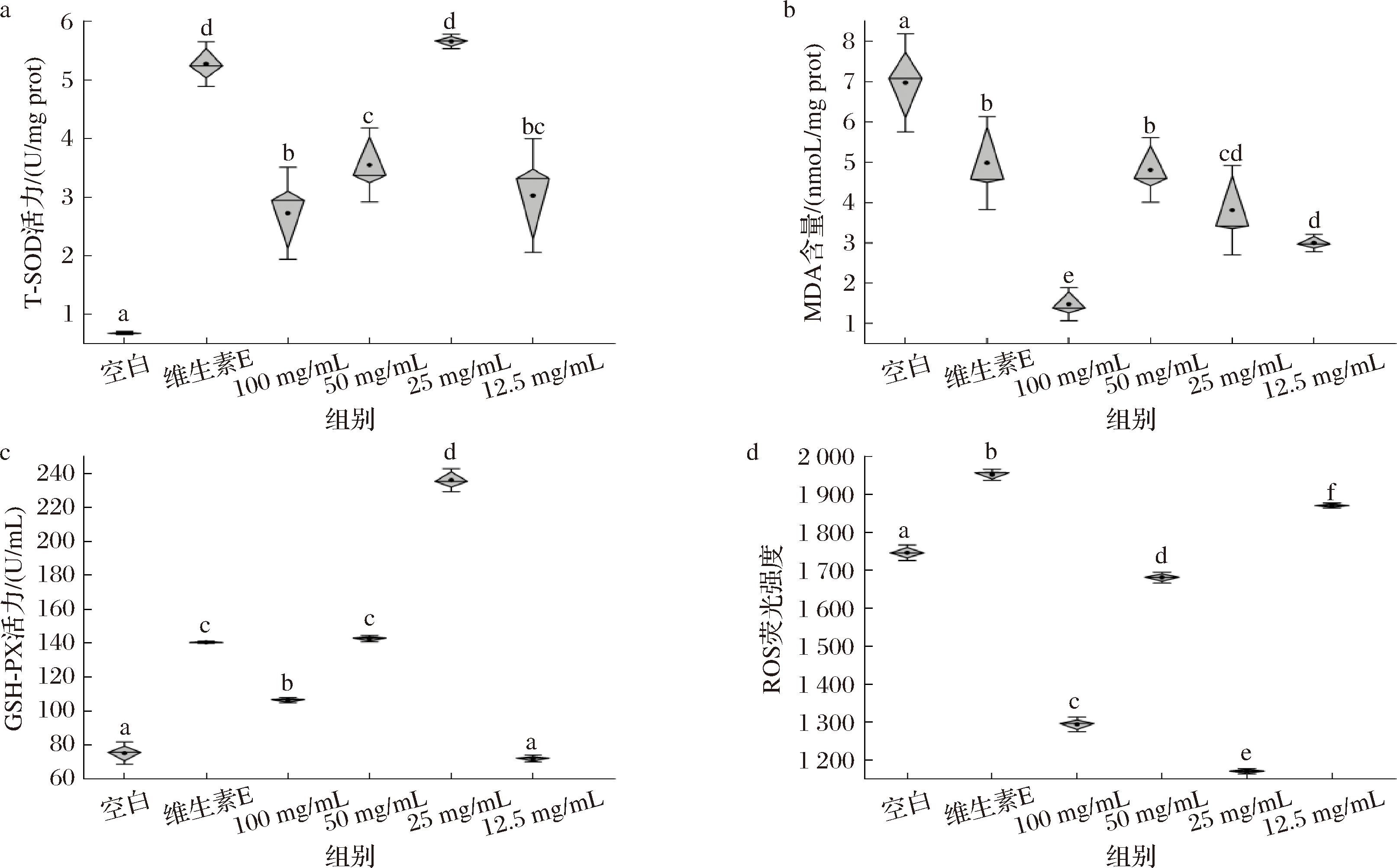
a-T-SOD水平;b-MDA 含量;c-GSH-PX水平;d-ROS含量
图6 羊肚菌多糖对线虫体内抗氧化酶活性及MDA和ROS含量的影响
Fig.6 Effects of Morchella polysaccharide on antioxidant enzyme activity, MDA and ROS content in nematodes
2.6 羊肚菌多糖对基因缺陷型线虫的抗氧化应激能力的影响
研究表明,线粒体呼吸过程、饮食限制、生殖系统和胰岛素/IGF-1信号是主要的衰老调节方案[33]。为了进一步确定羊肚菌多糖调节线虫急性氧化应激中的相关信号通路,本研究测定了各基因缺陷型线虫在胡桃醌(200 μg/mL)处理后的生存率。由图7-a~图7-f可知,DA1116(eat-2)、CB1876(clk-1)、CF1903(glp-1)和CB1370(daf-2)线虫在胡桃醌处理后的1 h时存活率均呈现急速下降趋势,随后下降速率降低,但在第7 h后,CB1370(daf-2)线虫存活率显著下降。在第9 h时CB1370(daf-2)线虫空白组、阳性对照组、100、50、25、12.5 mg/mL的生存率分别为0%、0%、1.67%、0%、1.67%和1.67%,均显著(P<0.05)低于DA1116(eat-2)、CB1876(clk-1)和CF1903(glp-1)3种线虫的生存率。由图7-g可知,第11 h时CB1370(daf-2)线虫各组存活率均为0,而DA1116(eat-2)、CB1876(clk-1)和CF1903(glp-1)3种线虫各处理组存活率均显著高于CB1370(daf-2)线虫(P<0.05)。以上结果表明,缺少daf-2基因的线虫会加快衰老速度。
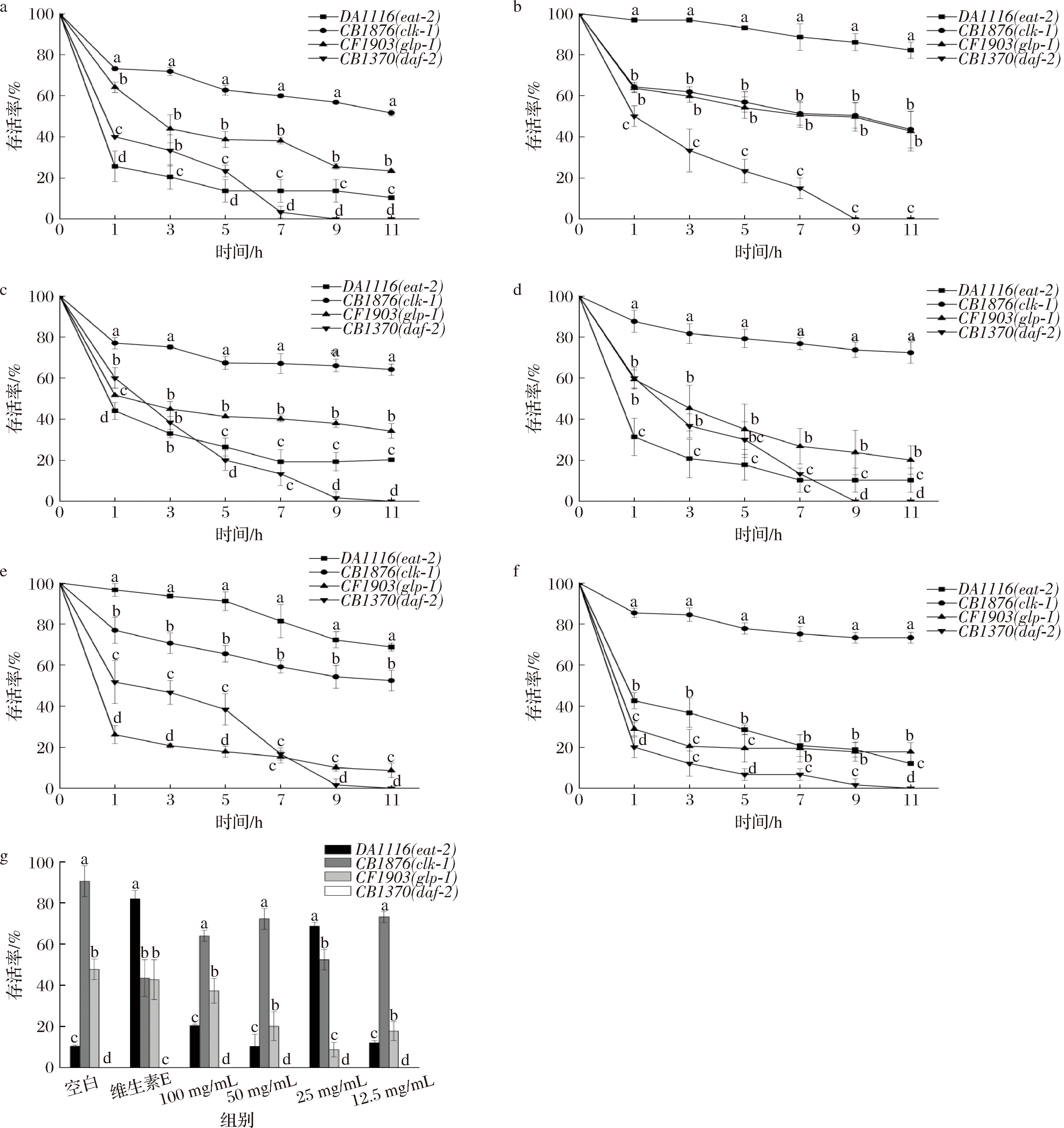
a-空白组;b-维生素E组;c~f-100、50、25、12.5 mg/mL羊肚菌多糖组;g-11 h时各基因缺陷型线虫存活率
图7 羊肚菌多糖对基因缺陷型线虫抗氧化应激能力的影响
Fig.7 Effect of Morchella polysaccharide on oxidative stress resistance of gene-deficient nematodes
daf-2是胰岛素信号通路中的关键基因,胰岛素信号通路是线虫体内新陈代谢的主要调控机制[34],当体内新陈代谢能力降低时,会引发ROS堆积,从而使线虫衰老速度加快。而CB1370(daf-2)为胰岛素信号降低的基因缺陷型线虫,因此胰岛素信号通路可能参与了羊肚菌多糖能够增强氧化应激抗性、延缓线虫衰老的过程。
3 结论
我国人口老龄化情况日益加重,延缓机体衰老实现健康老龄化,已成为燃眉之急。药食同源多糖能通过清除自由基及增加体内抗氧化酶等的活性而具有良好的抗氧化及抗衰老作用。据报道,灵芝多糖[35]、山药多糖[36]能够清除DPPH自由基、ABTS阳离子自由基、羟自由基、增强SOD及过氧化氢酶(catalase,CAT)的活力及降低ROS含量。
因此,本研究以秀丽隐杆线虫为研究对象,结果表明,所喂食的羊肚菌多糖具备安全性,在不损伤线虫生殖能力的前提下,延长了线虫的平均寿命、提高了线虫的运动能力、增强了线虫的抗热应激能力及抗氧化应激能力,并且使线虫体内T-SOD和GSH-PX活力升高并降低MDA及ROS的含量。并通过测定线粒体呼吸过程、饮食限制、生殖系统信号和胰岛素/IGF-1信号基因缺陷型线虫结果发现,羊肚菌多糖可能通过胰岛素信号通路调节自身代谢,从而抵抗应激环境,延长线虫寿命并减缓了其衰老速度。
但线虫是模式动物,其衰老特性与人类衰老特性过程存在一定差异,并且本研究只是对羊肚菌多糖抗衰老机制进行初步探究,因此本文的研究具有相对的局限性,羊肚菌多糖的抗衰老特性及作用机制需进一步使用哺乳动物进行验证。
[1] 王瑞淇, 杨杰良, 王子梅.酪蛋白激酶Ⅱ:衰老与衰老相关疾病调控[J].中国生物化学与分子生物学报, 2025, 41(3):333-343.WANG R Q, YANG J L, WANG Z M.Protein kinase CK2:Regulation of aging and aging-related diseases[J].Chinese Journal of Biochemistry and Molecular Biology, 2025, 41(3):333-343.
[2] LI Q, XIAO N Y, ZHANG H, et al.Systemic aging and aging-related diseases[J].The FASEB Journal, 2025, 39(5):e70430.
[3] 张惠琪. 发芽粟米活性肽对秀丽隐杆线虫氧化应激的影响及分子机制[D].南昌:南昌大学, 2024.ZhANG H Q.The effect of germinated millet active peptide on oxidative stress in Caenorhabditis elegans and its molecular mechanism [D].Nanchang:Nanchang University, 2024.
[4] REUTER S, GUPTA S C, CHATURVEDI M M, et al.Oxidative stress, inflammation, and cancer:How are they linked?[J].Free Radical Biology and Medicine, 2010, 49(11):1603-1616.
[5] LIGUORI I, RUSSO G, CURCIO F, et al.Oxidative stress, aging, and diseases[J].Clinical Interventions in Aging., 2018, 13:757-772.
[6] 栾雅格. 基于秀丽隐杆线虫的黄精炮制前后抗衰老作用比较及机制研究[D].北京:北京中医药大学, 2023.LUAN Y G.Comparison of anti-aging effects and mechanism of Polygonatum sibiricum before and after processing based on Caenorhabditis elegans [D].Beijing:Beijing University of Chinese Medicine, 2023.
[7] 陈茂原.羊肚菌脂质成分的研究[D].成都:电子科技大学,2023.CHEN M Y.Study on lipid components of Morchella esculenta [D].Chengdu:University of Electronic Science and Technology of China, 2023.
[8] 金琳山, 张睿, 刘永攀, 等.羊肚菌的化学成分和药理作用研究进展[J].特产研究, 2025, 47(1):161-166.JIN L S, ZHANG R, LIU Y P, et al.Research progress on chemical constituents and pharmacological action of Morchella esculenta L[J].Special Wild Economic Animal and Plant Research, 2025, 47 (1):161-166.
[9] WANG D D, ZHANG M L, ZHANG Y W, et al.Hepatoprotective effects of polysaccharide from Morchella esculenta are associated with activation of the AMPK/Sirt1 signaling pathway in mice with NAFLD[J].International Journal of Biological Macromolecules, 2025, 301:140444.
[10] ZHANG Z Y, CUI Y M, ZHANG X S, et al.Gut microbiota combined with serum metabolites to reveal the effect of Morchella esculenta polysaccharides on lipid metabolism disordered in high-fat diet mice[J].International Journal of Biological Macromolecules, 2024, 281:136380.
[11] ZHANG Y J, QIU R, ZHANG Z F, et al.Effect of Morchella esculenta polysaccharides on the rectal microbiota of mice challenged with lipopolysaccharides[J].Frontiers in Veterinary Science, 2024, 11:1446924.
[12] BADSHAH S L, RIAZ A, MUHAMMAD A, et al.Isolation, characterization, and medicinal potential of polysaccharides of Morchella esculenta[J].Molecules, 2021, 26(5):1459.
[13] 熊川, 罗强, 李强, 等.六妹羊肚菌多糖部分理化性质及抗氧化活性研究[J].天然产物研究与开发,2017,29(7):1182-1187;1153.XIONG C, LUO Q, LI Q, et al.Physical and chemical properties of polysaccharide isolated from the fruiting bodies of Morchella sextelata and its antioxidant effect[J].Nature Product Research and Development, 2017,29 (7):1182-1187;1153.
[14] 闫永兰. 酶提羊肚菌子实体多糖的抗氧化和抗衰老作用[J].中国食用菌, 2020, 39(1):42-45;60.YAN Y L.Antioxidation and anti-aging effects of polysaccharides from zymotic fruit bodies of Morchella[J].Edible Fungi of China, 2020,39(1):42-45;60.
[15] CORSI A K, WIGHTMAN B, CHALFIE M.A transparent window into biology:A primer on Caenorhabditis elegans[J].Genetics, 2015, 200(2):387-407.
[16] MARKAKI M, TAVERNARAKIS N.Caenorhabditis elegans as a model system for human diseases[J].Current Opinion in Biotechnology, 2020, 63:118-125.
[17] ZHOU L, LIU J, BU L L, et al.Curcumin acetylsalicylate extends the lifespan of Caenorhabditis elegans[J].Molecules, 2021, 26(21):6609.
[18] LUO X G, WANG J, CHEN H Q, et al.Identification of flavoanoids from finger citron and evaluation on their antioxidative and antiaging activities[J].Frontiers in Nutrition, 2020, 7:584900.
[19] 甘爱园, 汪卓, 尹欢, 等.羊栖菜速溶粉对秀丽隐杆线虫的抗氧化作用研究[J].食品与发酵工业,2025,51(7):177-184.GAN A Y, WANG Z, YIN H, et al.Antioxidant effect of Sargassum fusiforme instant powder on Caenorhabditis elegans [J].Food and Fermentation Industries, 2025,51 (7):177-184.
[20] ZHANG J Q, XUE X L, QIAO Y Q, et al.Astragaloside IV extends lifespan of Caenorhabditis elegans by improving age-related functional declines and triggering antioxidant responses.[J].Rejuvenation Research, 2021, 24(2):120-130.
[21] WU X Y, ZHANG C Y, ZHOU S W, et al.N.sphaeroides phycocyanin subunit Ns-α and Ns-β improve C.elegans antioxidative capacity via ROS-related regulation[J].PeerJ, 2025, 13:e18917.
[22] SHI L, YU X T, LI H, et al.D-chiro-inositol increases antioxidant capacity and longevity of Caenorhabditis elegans via activating Nrf-2/SKN-1 and FOXO/DAF-16[J].Experimental Gerontology, 2023, 175:112145.
[23] 王刚. 海红米皮糠神经酰胺的提取分离及其对秀丽隐杆线虫抗衰老作用的研究[D].湛江:广东海洋大学, 2023.WANG G.Extraction and separation of ceramide from sea red rice bran and its anti-aging effect on Caenorhabditis elegans [D].Zhanjiang:Guangdong Ocean University, 2023.
[24] 赵佳乐, 张鹏, 杨英, 等.列当水提物对秀丽隐杆线虫抗衰老作用研究[J].中国兽医科学, 2024, 54(1):124-133.ZHAO J L, ZHANG P, YANG Y, et al.Study on anti-aging effect of Orobanche cernua loefling extract on Caenorhabditis elegans[J].Chinese Veterinary Science, 2024,54 (1):124-133.
[25] WANG Y H, YANG J Y, LI X, et al.Optimization of the process of extracting polysaccharides from Agrocybe aegerita and in vitro antioxidant and anti-aging tests[J].Molecules, 2024, 29(21):4992.
[26] LIN C X, ZHANG X Y, XIAO J, et al.Effects on longevity extension and mechanism of action of carnosic acid in Caenorhabditis elegans[J].Food &Function, 2019,10(3):1398-1410.
[27] LEE Y, LEE H Y.Revisiting the bacterial Phylum composition in metabolic diseases focused on host energy metabolism[J].Diabetes &Metabolism Journal, 2020, 44(5):658-667.
[28] ZHANG K Z, ZHU J H, LIU P Y, et al.Petunidin-3-O-[rhamnopyranosyl-(trans-p-coumaroyl)]-5-O-(β-D-glucopyranoside), the main anthocyanin from the fruits of Lycium ruthenicum Murray, enhances the lifespan of Caenorhabditis elegans by activating DAF-16 and improving the gut microbiota[J].Food Bioscience, 2024, 61:104642.
[29] 叶海波, 夏琛, 张见明, 等.不同贮藏时间白茶对秀丽隐杆线虫抗衰老的作用及机制[J].浙江大学学报(农业与生命科学版), 2025,51(5):810-824.YE H B, XIA C, ZHANG J M, et al.Antiaging effects and mechanisms of white tea with different storage time on Caenorhabditis elegans[J].Journal of Zhejiang University (Agriculture and Life Sciences), 2025,51(5):810-824.
[30] ZHANG G W, JIANG W W,HU Q, et al.Characterization and anti-aging potency of phenolic compounds in Xianhu tea extracts[J].Foods, 2025, 14(5):737.
[31] LEE S A, LIM W H, VAN LE V, et al.Lifespan extension and anti-oxidant effects of carotenoid pigments in Caenorhabditis elegans[J].Bioresource Technology Reports, 2022, 17:100962-.
[32] 范欣悦, 何汶璐, 董丽, 等.金钗石斛提取物对秀丽隐杆线虫帕金森病模型的神经保护作用研究[J].中国比较医学杂志, 2025, 35 (4):31-42.FAN X Y, HE W L, DONG L, et al.Neuroprotective effect of Dendrobium nobile Lindl extract on Coenorhaditis elegans model of Parkinson’s disease[J].Chinese Journal of Comparative Medicine, 2025, 35 (4):31-42.
[33] 李雲凤. 鹿角多肽的制备、抗衰老活性及其机理研究[D].长春:长春工业大学, 2024.LI Y F.Preparation, anti-aging activity and mechanism of antler polypeptide [ D ].Changchun:Changchun University of Technology, 2024.
[34] 韩龙飞, 吴影, 樊秋霞, 等.凝结魏茨曼氏菌通过调节脂代谢通路改善高糖饮食诱导对秀丽线虫的损伤[J].食品工业科技,2025,46(14):430-440.HAN L F, WU Y, FAN Q X, et al.Weizmannia coagulans ameliorate high-sucrose diet-induced damage in Caenorhabditis elegans by regulating lipid metabolism pathways[J].Science and Technology of Food Industry,2025,46(14):430-440.
[35] 马慧秀, 戴德慧, 胡小康, 等.不同来源灵芝多糖的分离纯化、结构表征及抗衰老与应激活性研究[J/OL].中国食品学报, 2025.https://kns.cnki.net/kcms/detail/11.4528.ts.20250311.1746.004.html.MA H X, DAI D H, HU X K, et al.Purification, structural characterization and anti-aging and stress activities of Ganoderma lucidum polysaccharides from different sources[J/OL].Journal of Chinese Institute of Food Science and Technology, 2025.https://kns.cnki.net/kcms/detail/11.4528.ts.20250311.1746.004.html.
[36] 刘泽坤, 贺小芳, 洪颖, 等.山药多糖延缓秀丽隐杆线虫衰老的药效评价及作用机制研究[J].世界中医药, 2024, 19(4):473-480.LIU Z K, HE X F, HONG Y, et al.Pharmacodynamic evaluation and mechanism of Chinese yam polysaccharides in delaying senescence of Caenorhabditis elegans[J].World Chinese Medicine, 2024,19(4):473-480.