微生物在食品加工中发挥着重要作用,可用于发酵食品生产、充当天然防腐剂,还可通过添加益生菌提升食品的健康价值。然而,某些食品中的微生物会引起腐败变质,降低营养价值,甚至引发食源性疾病,严重威胁人体健康[1]。目前已知由食源性致病菌引起的疾病超过200种,常见致病菌包括肉毒梭菌、大肠杆菌(Escherichia coli)、沙门氏菌、李斯特菌和金黄色葡萄球菌(Staphylococcus aureus)等[2]。尽管我国在食品安全领域取得了显著进展,但食源性致病菌引发的微生物污染仍是食品安全的首要危险因素[3-4]。因此,开发高效、准确的食源性致病菌检测方法已成为当前的研究热点。
传统的微生物检测方法主要依赖微生物培养技术,也是国家标准中的常用方法。然而,该方法存在明显不足,如耗时长,无法快速鉴定病原菌;仅能检测活体微生物,无法识别已死亡的菌体;灵敏度较低,难以检出低含量的微生物;且依赖微生物的可培养性,无法检测不可培养的菌种[5-8]。
近年来,基因检测技术因其高效、准确的特点被广泛应用于食源性致病菌检测。其中,聚合酶链式反应(polymerase chain reaction, PCR)技术是应用最广泛的基因检测方法之一。PCR通过设计针对微生物高度保守基因序列的引物,利用DNA聚合酶扩增目标DNA片段,并对扩增产物进行分析,从而实现微生物的检测[9]。此外,自CHAMBERLAIN等[10]提出多重PCR技术以来,因该技术可同时扩增多种病原菌的目标序列,达到同时检测多种病原菌的目的,大幅提升检测效率,因此多重PCR在食源性致病菌的检测中有着广泛应用,且取得了良好成效。然而,多重PCR因同时存在多对引物,可能形成引物二聚体或是发生非特异性扩增,影响检测准确性[11]。为此,巢式PCR通过设计2对嵌套引物(第二对引物位于第一对引物扩增片段内部)增强扩增特异性(图1),第一轮扩增由外引物完成,若产生非目标片段,第二轮扩增的内引物仅结合目标片段,从而显著提高检测准确性[12]。
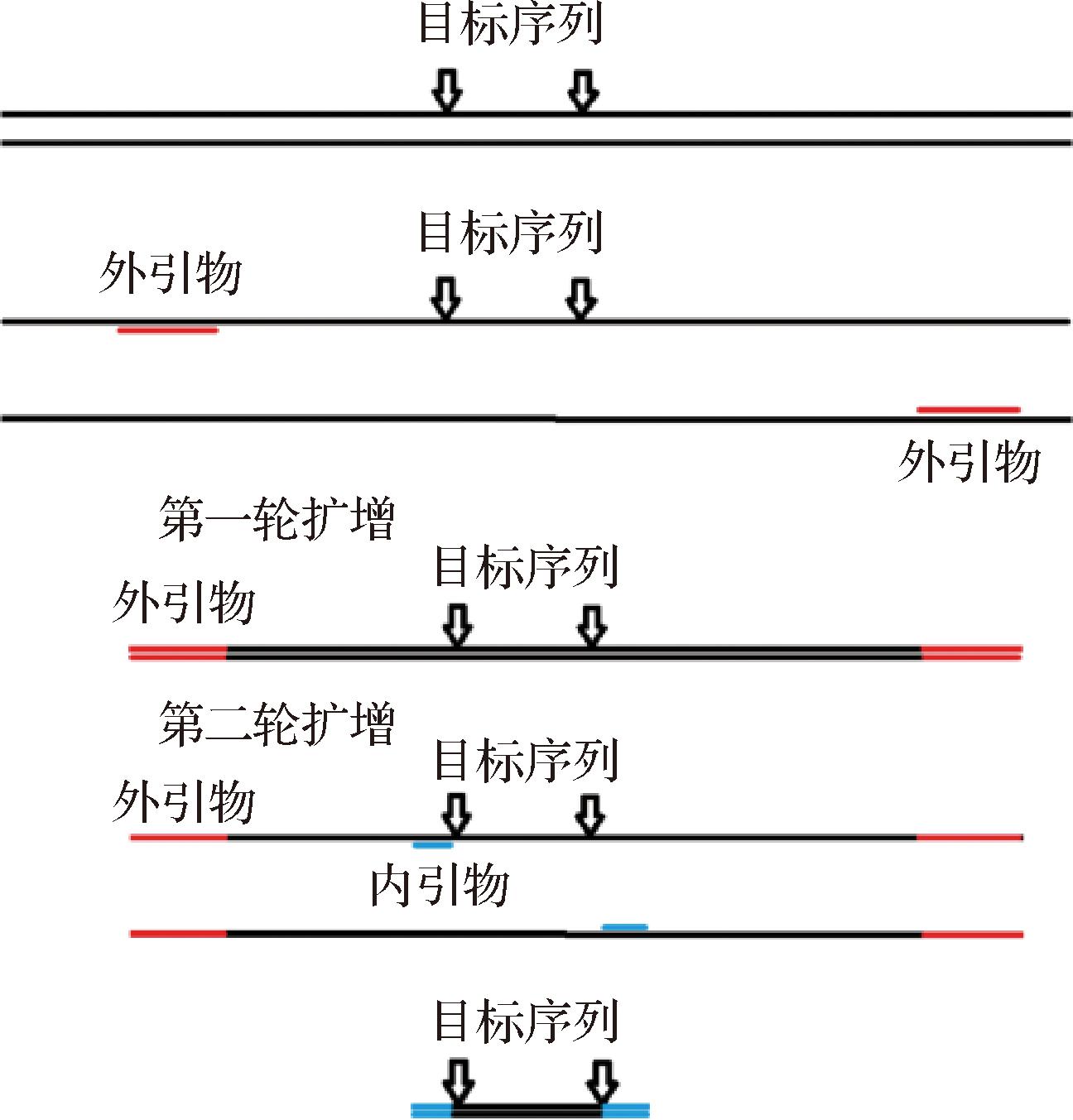
图1 巢式PCR扩增原理
Fig.1 The principle of nested PCR amplification
在PCR产物分析方面,传统琼脂糖凝胶电泳对DNA上样量要求较高,限制了其对微量微生物的检测,且分辨率较低,难以区分大小相近的DNA片段。相比之下,高效毛细管电泳技术具有高分辨率、高灵敏度和低上样量等优势,适用于微量微生物的检测[13]。对于微生物准确、灵敏的检测也可通过荧光定量PCR实现,然而染料法的荧光定量PCR单次只能检测一种目标基因,无法实现多种微生物的同时检测,荧光探针法虽能同时检测多种微生物,但其检测通量受限于荧光PCR仪的检测通道数,一般多为4通道,并且荧光探针的合成成本较高,是引物合成价格的20倍以上。本研究结合多重PCR与巢式PCR技术,针对大肠杆菌、沙门氏菌和金黄色葡萄球菌3种食源性致病菌的基因进行扩增;同时,采用毛细管电泳技术替代传统琼脂糖凝胶电泳分析PCR产物,以期以较低成本创建一种快速、准确和高灵敏的检测方法,以满足食品安全领域中对食源性致病菌的检测需求[14]。
1 材料与方法
1.1 材料与试剂
标准菌株共6株:鼠伤寒沙门氏菌(Salmonellatyphimurium, ATCC14028)、金黄色葡萄球菌(ATCC6538)、大肠埃希氏菌O157∶H7(ATCC35150)、单增李斯特氏菌(ATCC19114)、副溶血性弧菌(ATCC17802)、蜡样芽孢杆菌(ATCC11778),青岛海博生物技术有限公司。
CW0552S细菌基因组DNA提取试剂盒,康为世纪生物有限公司;N616-01 VAHTS HiFi Universal Amplification Mix、DC301-01 FastPure Gel DNA Extraction Mini Kit,南京诺唯赞生物科技股份有限公司;AM9932无核酸酶水(nuclease-free water,NF水),美国赛默飞科技公司。
1.2 仪器与设备
Qsep100全自动核酸蛋白分析系统,杭州厚泽生物科技有限公司;Applied Biosystems MiniAmp Plus热循环仪、Quibt 4.0荧光定量仪,美国赛默飞世尔科技公司;HE-120凝胶电泳槽、Tanon 1600全自动凝胶成像分析仪,上海天能科技有限公司。
1.3 实验方法
1.3.1 引物合成
在美国国家生物技术信息中心官网查询金黄色葡萄球菌nuc基因(登录号DQ507381.1)、鼠伤寒沙门氏菌hilA基因(登录号NC_003197.2)和大肠杆菌uidA基因(登录号NC_000913.3)3个基因的基因组序列,下载并用Primer Premier 5引物设计软件设计3组多重PCR引物(表1),委托苏州泓迅生物科技股份有限公司合成,使用NF水稀释至10 μmol/L[15]。
表1 三种目标菌及基因PCR引物信息
Table 1 Information of three target bacteria and gene PCR primers

注:out表示外引物,用于巢式PCR第一轮扩增;in表示内引物,是以out引物扩增产物为模板,用于巢式PCR第二轮扩增。
目标细菌及基因引物名称引物序列(5′-3′)产物大小/bp大肠埃希氏菌uidAuidA,out-FCGGGTGAAGGTTATCTCTAT779uidA,out-RGGTGATGATAATCGGCTGuidA,in-FCCTCGCATTACCCTTACGCT170uidA,in-RAGTTTCCCCGTTGACTGCCT鼠伤寒沙门氏菌hilAhilA,out-FGCATTACTCTATCGTGAAGG1 135hilA,out-RAACCAGCACTAACGGTAATAhilA,in-FGCTGGCAGAATGCTACCTCA141hilA,in-RTGTAGCCCCAGTAATCCTAAAGC金黄色葡萄球菌nucnuc,out-FGGGATGGCTATCAGTAATG478nuc,out-RCGTTTACCATTTTTCCATCnuc,in-FCGAAAGAACAATACGCAAAGAGG133nuc,in-RGAACCACTTCTATTTACGCCATT
1.3.2 核酸提取
按照DNA提取试剂盒说明书对鼠伤寒沙门氏菌、金黄色葡萄球菌、大肠埃希氏菌O157:H7、单增李斯特氏菌、副溶血性弧菌和蜡样芽孢杆菌进行DNA提取,并利用Quibt 4.0荧光定量仪测量DNA浓度,用NF水将各细菌DNA稀释至1.0 ng/μL备用。
1.3.3 单重巢式PCR与普通PCR对比
巢式PCR分为两轮扩增:第一轮以目标菌基因组DNA为模板,使用外引物进行扩增;第二轮以第一轮扩增产物的稀释液为模板,使用内引物进行扩增。同时,通过与直接使用内引物扩增目标菌DNA的普通PCR进行比较,评估巢式PCR的特异性。
1.3.3.1 第一轮扩增
以3种目标菌(大肠埃希氏菌、鼠伤寒沙门氏菌和金黄色葡萄球菌)的基因组DNA为模板,分为3组(uidA组、hilA组、nuc组)。各组加入对应目标基因的外引物(如uidA组加入uidA_out引物),在Applied Biosystems MiniAmp Plus热循环仪上进行单重PCR扩增。扩增体系和反应条件见表2,所得产物记为产物1。
表2 单重PCR组分与反应条件
Table 2 Single PCR components and reaction conditions
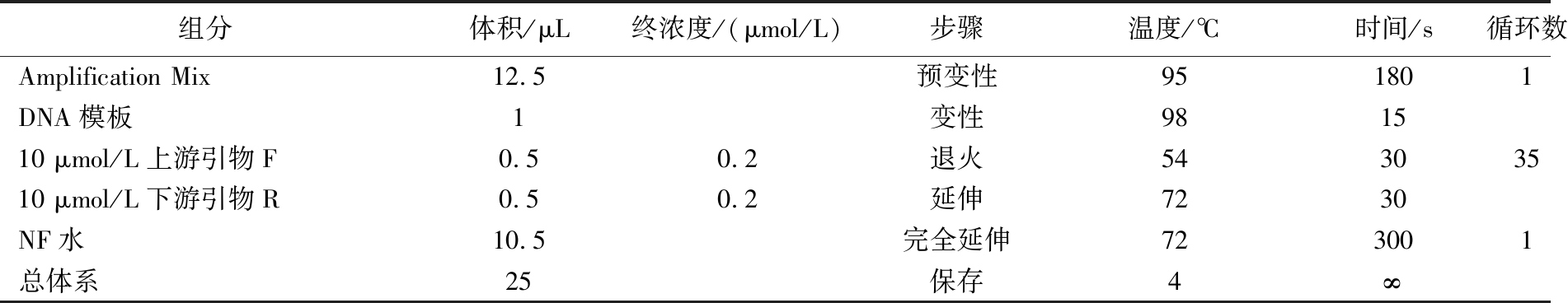
组分体积/μL终浓度/(μmol/L)步骤温度/℃时间/s循环数Amplification Mix12.5预变性951801DNA模板1变性981510 μmol/L上游引物F0.50.2退火54303510 μmol/L下游引物R0.50.2延伸7230NF水10.5完全延伸723001总体系25保存4∞
1.3.3.2 第二轮扩增
将产物1稀释100倍后,取1 μL加入对应目标基因的内引物(如在uidA组中加入uidA_in引物)。扩增体系及反应条件参考表2,退火温度调整为60 ℃,循环数设为20,其余条件不变。所得产物记为产物2。
1.3.3.3 普通PCR扩增
以3种目标菌的基因组DNA为模板,直接加入对应目标基因的内引物。扩增体系及反应条件参考表2,退火温度调整为60 ℃,其余条件不变。所得产物记为产物3。
分别取2 μL产物1~3进行琼脂糖凝胶电泳分析,以比较巢式PCR与普通PCR的特异性差异。电泳条件:0.01 g/mL琼脂糖凝胶,电压150 V,电流500 mA,运行20 min。
1.3.4 单重巢式PCR条件优化
1.3.4.1 第一轮扩增条件优化
在3组(uidA、hilA、nuc)DNA模版中加入对应目标基因的外引物,进行单重PCR扩增。扩增体系及反应条件参考表2,退火温度分别设为52、54、56、58 ℃,其余条件不变。所得产物记为产物4。取2 μL 产物4进行琼脂糖凝胶电泳分析。
1.3.4.2 第二轮扩增条件优化
将产物4稀释100倍,取1 μL加入对应目标基因的内引物。扩增体系及反应条件参考表2,退火温度分别设为56、58、60、62 ℃,循环数设为20,其余条件不变。所得产物记为产物5。取2 μL产物5进行琼脂糖凝胶电泳分析。
1.3.5 多重巢式PCR建立
根据上述优化结果,选用第一轮和第二轮扩增的最佳退火温度作为多重巢式PCR的退火温度。为避免扩增循环过多造成气溶胶污染,第一轮扩增循环数降至20,第二轮保持20循环。为确保扩增效果与普通PCR等效(35循环),第一轮产物稀释25倍,取0.78 μL(25/25≈0.78)进行第二轮扩增。
取3种目标菌的基因组DNA(1 ng/μL)等量混合,取3 μL作为模板,加入3对外引物(每对引物终浓度0.2 μmol/L)。扩增体系及反应条件参考表2,退火温度设为54 ℃,循环数设为20,其余条件不变。所得产物记为多重产物1。
取0.78 μL多重产物1,加入3对内引物(每对引物终浓度0.2 μmol/L)。扩增体系及反应条件参考表2,退火温度设为58 ℃和56 ℃,循环数设为20,其余条件不变。所得产物记为多重产物2。取2 μL产物2和多重产物2进行琼脂糖凝胶电泳分析。
取1 μL“多重产物2”加入99 μL NF水稀释100倍,使用Qsep100核酸蛋白分析系统进行毛细管电泳分析。仪器参数:进样电压4 kV,进样时间10 s;分离电压8 kV,分离时间160 s。
1.3.6 特异性验证
将3种非目标菌(单增李斯特氏菌、副溶血性弧菌和蜡样芽孢杆菌)的DNA等量混合,制备干扰DNA。将3种目标菌DNA与干扰DNA等量混合,制备混合DNA。采用1.3.5节建立的多重巢式PCR方法检测干扰DNA和混合DNA,验证该方法在存在其他食源性致病菌干扰时对3种目标菌检测的特异性。
1.3.7 灵敏度检测
按FastPure Gel DNA Extraction Mini Kit说明书操作,对1.3.3节中产物1的琼脂糖凝胶电泳条带进行胶回收,得到片段大小分别为779(uidA)、1 135(hilA)和478 bp(nuc)的单一DNA片段,作为阳性样本进行灵敏度检测。使用Qubit 4.0荧光定量仪测量阳性样本浓度,并将质量浓度(g/μL)换算为拷贝数浓度(copies/μL)。将样本稀释至105、104、103、102、101、100 copies/μL。按拷贝数等体积混合不同基因的阳性样本(如105copies/μL的3组等体积混合),制备阳性对照混合液。取3 μL(每基因1 μL)不同浓度的阳性对照混合液,加入1 ng干扰DNA(见1.3.6节)模拟真实样本DNA,采用1.3.5节的多重巢式PCR方法检测,确定检测限。其计算如公式(1)所示:
(1)
式中:C,质量浓度,g/μL;NA,阿伏伽德罗常数,6.022×1023;660,DNA碱基对平均分子质量;n,DNA链碱基对数。
1.3.8 食品基质中的检测
取3种目标菌干粉溶解在NF水中,配成每μL约含各细菌1×105个的混合菌液,在牛奶、牛肉、鸡肉、凉菜4种食品基质中加入1 μL菌液,每种基质取3份,随后对含菌液的食品基质进行提取并用以上方法进行检测,验证食品基质对该方法的影响。
1.4 数据处理
采用Tanon 1600软件处理凝胶电泳图像;毛细管电泳图由Qsep100采集后,将原始数据导出后用Origin 2021作图软件处理;采用WPS Office绘制表格。退火温度优化、灵敏度检测及食品基质检测实验重复3次。
2 结果与分析
2.1 单重巢式PCR扩增
2.1.1 第一轮扩增结果
3种目标细菌基因的第一轮扩增结果如图2-a所示,结果显示大肠埃希氏菌(uidA)、鼠伤寒沙门氏菌(hilA)和金黄色葡萄球菌(nuc)的DNA分别在779、1 135、478 bp处出现扩增条带,与设计引物的目标片段长度一致,表明第一轮扩增满足后续实验要求。
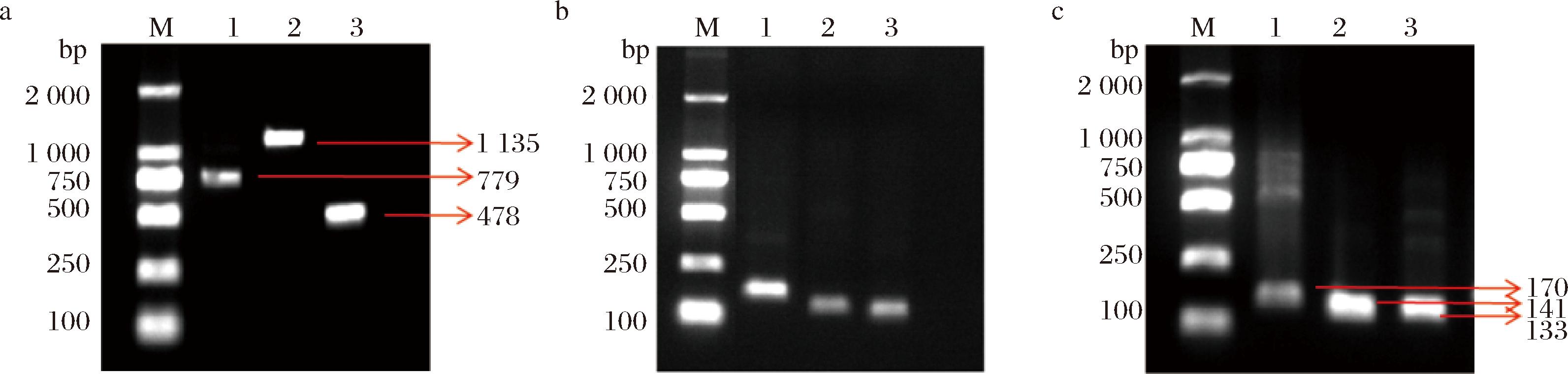
M:DM2 000;泳道1:uidA组(大肠埃希氏菌);泳道2:hilA组(鼠伤寒沙门氏菌);泳道3:nuc组(金黄色葡萄球菌)。
a-巢式PCR第一轮产物;b-巢式PCR第二轮产物;c-普通PCR产物
图2 巢式PCR和普通PCR扩增凝胶电泳结果
Fig.2 Results of gel electrophoresis amplified by nested PCR and conventional PCR
2.1.2 第二轮扩增结果
对“产物1”进行第二轮扩增的结果如图2-b所示,结果显示uidA、hilA和nuc的DNA分别在170、141、133 bp处出现扩增条带,与设计引物的目标片段长度相符,表明第二轮扩增成功。相比之下,普通PCR(内引物直接扩增,图2-c)虽在170、141、133 bp处有条带,但通道1中伴随大量非特异性条带,表明内引物特异性较差,易与非目标区域结合。而巢式PCR的产物无非特异性片段,表明两轮扩增能提升检测准确性。
2.2 单重巢式PCR条件优化
2.2.1 第一轮扩增条件优化结果
3种目标细菌DNA在不同退火温度下的第一轮PCR扩增(产物4)结果如图3-a所示。对于uidA组,在779 bp处均有扩增条带,54 ℃和56 ℃时条带亮度最高,扩增效率最佳。对于hilA组,在1 135 bp处均有扩增条带,58 ℃时条带亮度最低,52~56 ℃扩增效率较优。对于nuc组,在478 bp处均有扩增条带,54 ℃时条带亮度最高,58 ℃条带亮度最弱。因此选用54 ℃为第一轮扩增的退火温度。
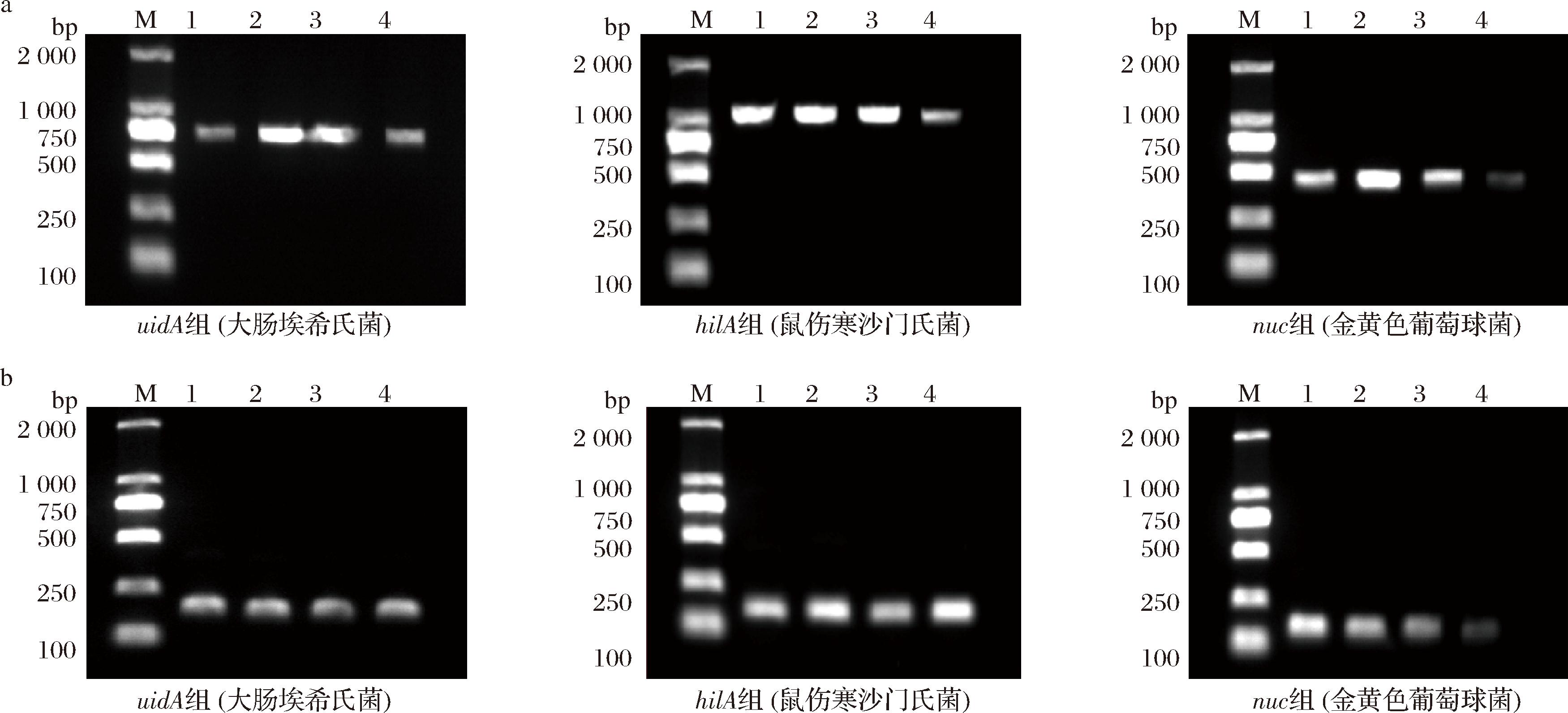
M:DM2 000;图a中泳道1~4依次为52、54、56、58 ℃;图b中泳道1~4依次为56、58、60、62 ℃。
a-第一轮产物;b-第二轮产物
图3 单重巢式PCR扩增条件优化结果
Fig.3 Optimization results of nested PCR amplification conditions
2.2.2 第二轮扩增条件优化结果
第二轮PCR在不同退火温度下的扩增(产物5)结果如图3-b所示。对于uidA组,4种温度在170 bp处均有扩增条带,且亮度无明显差异,表明该温度区间的扩增效率稳定。对于hilA组,在141 bp处均有扩增条带,58 ℃和62 ℃时亮度最高,此时扩增效率最佳。对于nuc组,在133 bp处均有扩增条带,56 ℃时亮度最高,此温度下的扩增效率最佳。因此确定56 ℃和58 ℃作为第二轮退火温度,具体选择需在多重巢式PCR中进一步验证。
2.3 多重巢式PCR建立
2.3.1 琼脂糖凝胶电泳结果
产物2和多重产物2的凝胶电泳结果如图4-a所示。单独扩增时,uidA、hilA和nuc的目标片段(170、141、133 bp)可区分。但多重巢式PCR(通道4、5)中,条带因片段大小相近(<37 bp)无法区分,表明凝胶电泳分辨率不足,需采用毛细管电泳。
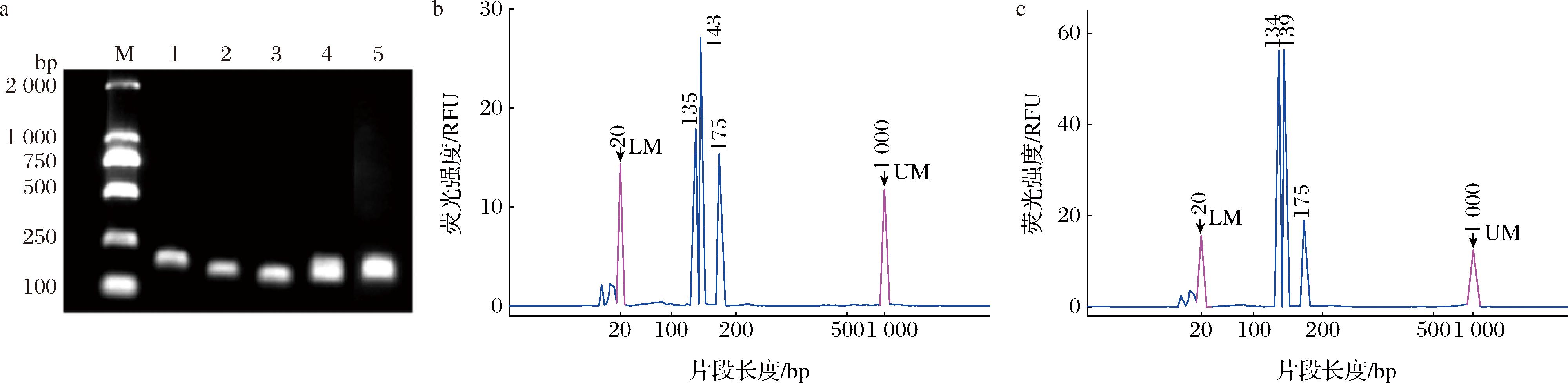
图a中M:DM2 000;泳道1~3依次为“产物2”中uidA组、hilA组、nuc组;泳道4~5为“多重产物2”中退火温度58 ℃和56 ℃。
a-凝胶电泳结果;b-58 ℃毛细管电泳结果;c-56 ℃毛细管电泳结果
图4 多重巢式PCR的电泳结果
Fig.4 Electrophoresis results of multiplex nested PCR
注:图中LM为Low Marker 20 bp,UM为Upper Marker 1 000 bp(下同)。
2.3.2 毛细管电泳结果
毛细管电泳可对微量DNA进行片段分析,实现对多重PCR产物的分离,具有快速、高分辨和高灵敏等特点[16]。毛细管电泳分析多重产物2的结果如图4所示。当退火温度为58 ℃时,检测到3个片段峰,长度分别为135、143、175 bp(Qsep100仪器S2卡夹检测DNA片段时有±5 bp的误差范围,所示片段峰在误差范围内即可视为目标片段),对应目标片段nuc_in(133 bp)、hilA_in(141 bp)和uidA_in(170 bp)。当退火温度为56 ℃时,检测到3个片段峰,长度分别为134、139、175 bp,同样对应nuc_in(133 bp)、hilA_in(141 bp)和uidA_in(170 bp)。由此可见,毛细管电泳可以区分大小差异仅为8 bp(133 bp和141 bp)的目标片段,大大提高了电泳检测的分辨率。相较于传统凝胶电泳,毛细管电泳在多重PCR应用中能够同时检测更多的目标基因,具有更高的检测效率。
在图4-b中,在退火温度为58 ℃时,nuc_in、hilA_in和uidA_in目标片段的荧光信号强度分别为(22.34±2.18) RFU、(31.26±3.88) RFU和(19.85±1.15) RFU;在图4-c中,在56 ℃时,三者的荧光信号强度分别增至(58.36±4.47) RFU、(58.32±3.87) RFU和(22.17±3.12) RFU。并且在图4-a中泳道5的亮度较泳道4更高。显然,56 ℃时3种目标片段的扩增效率更高。因此,第二轮PCR扩增的退火温度最终确定为56 ℃。
2.4 特异性验证
干扰DNA(单增李斯特氏菌、副溶血性弧菌、蜡样芽孢杆菌)和混合DNA(目标菌+干扰菌)的检测结果如图5所示。由图5可知,干扰DNA无目标片段峰,混合DNA仅出现133、141、170 bp峰,表明该方法可特异性检测大肠埃希氏菌、鼠伤寒沙门氏菌和金黄色葡萄球菌,不受非目标菌干扰,具有优异特异性。
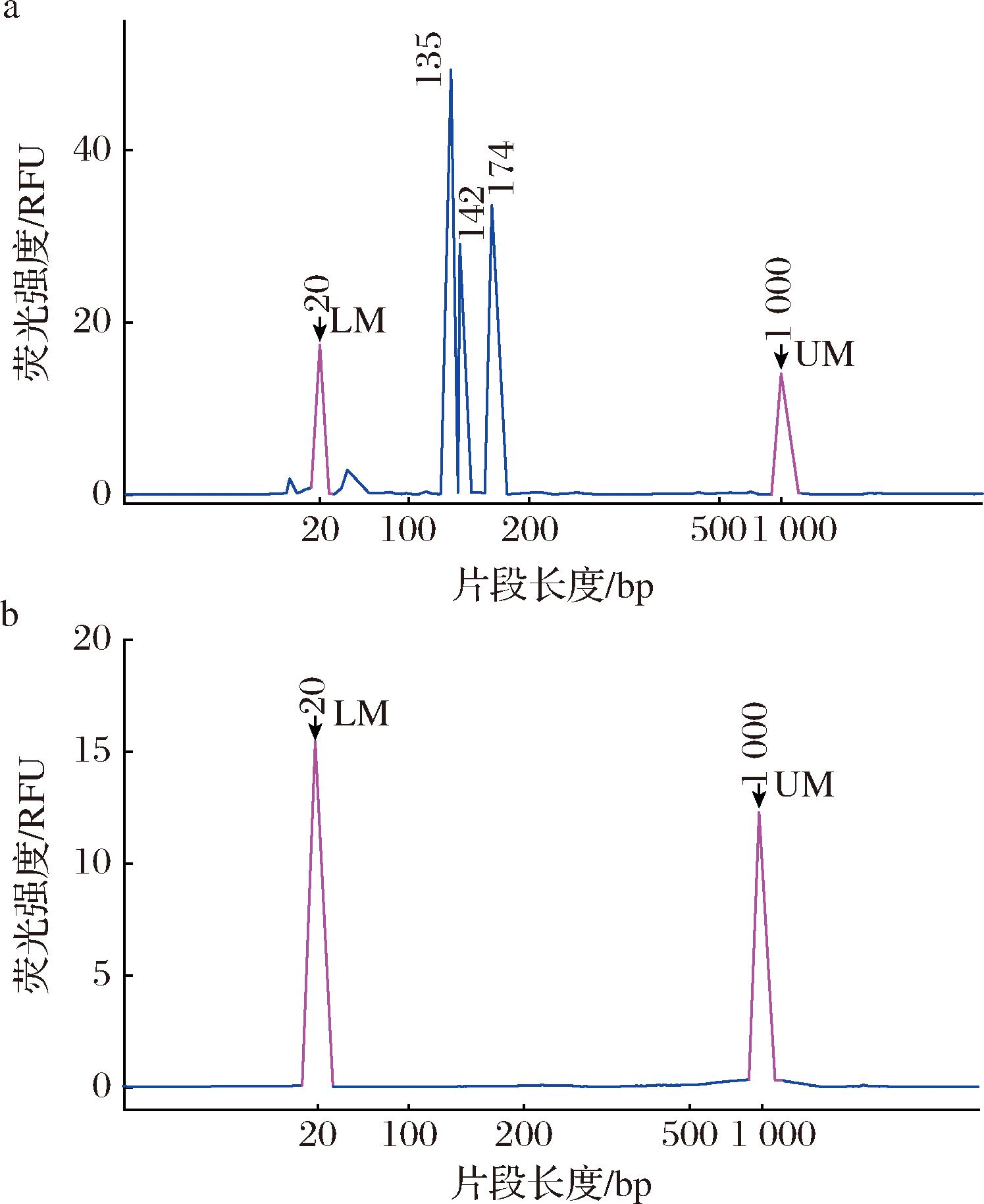
a-混合DNA;b-干扰DNA
图5 混合DNA与干扰DNA多重巢式PCR扩增结果
Fig.5 Multiplex nested PCR amplification results of mixed DNA and interfering DNA
2.5 灵敏度检测结果
2.5.1 阳性对照胶回收结果
3种目标基因的胶回收浓度如下:uidA(779 bp)质量浓度5.42 ng/μL、hilA(1 135 bp)质量浓度为3.23 ng/μL、nuc(478 bp)质量浓度为4.87 ng/μL。回收结果如图6所示,所得片段明亮且单一,说明仅含目标基因片段,可作为后续实验中的阳性对照。将以上所得阳性对照按照表3稀释至105 copies/μL,用于后续灵敏度检测。
表3 三种目标基因质量浓度与拷贝数浓度对应关系
Table 3 The corresponding relationships between the mass and copies concentrations of the three target genes
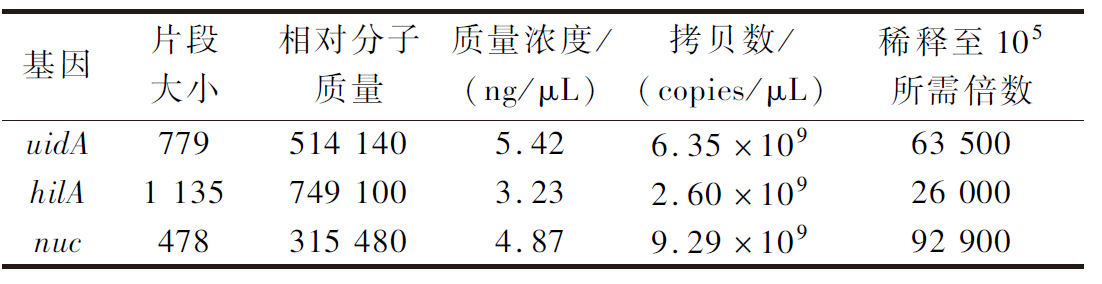
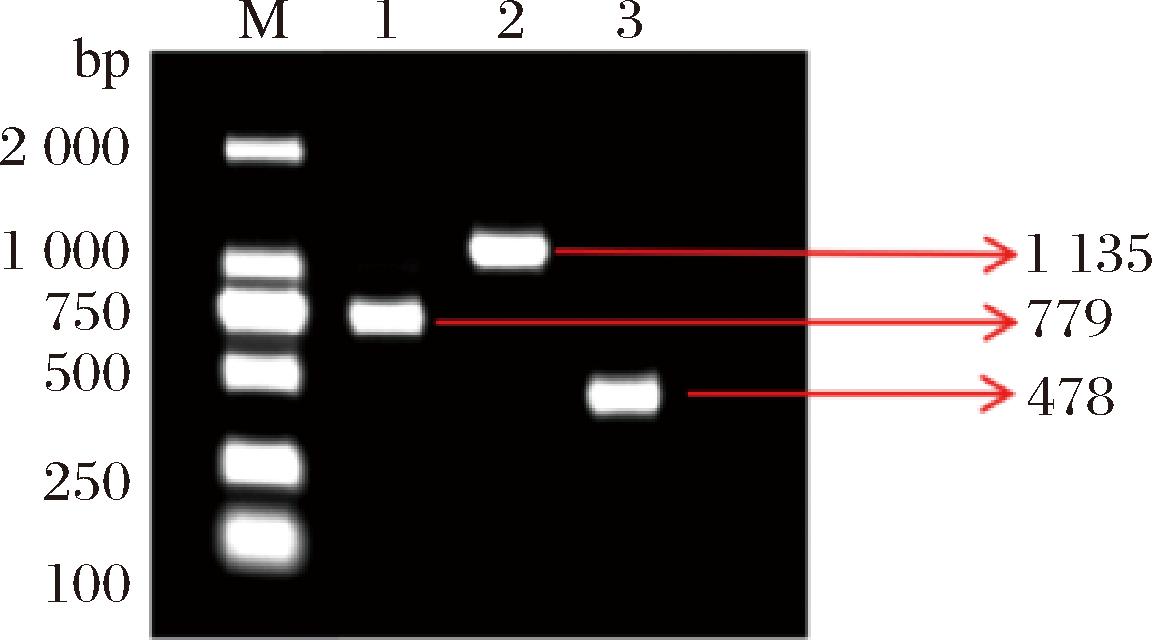
图6 三种目标基因胶回收结果
Fig.6 The recovery results of three target genes
2.5.2 检出限测定结果
不同浓度的“阳性对照混合液”检测结果如图7和表4所示。在体系含有105和104个拷贝时,检测结果在170、141、133 bp附近均有明显的峰,说明此时3种目标菌均能被检出。当拷贝数为103时,hilA基因(141)峰信号明显降低,而当拷贝数为102时,检测结果中无141左右的峰,说明该方法无法检测拷贝数低于103的hilA基因。当拷贝数为101时,uidA基因(170)和nuc基因(133)的峰信号都非常弱;拷贝数继续降低至100时,无任何峰信号。因此,该方法对大肠埃希氏菌uidA基因和金黄色葡萄球菌nuc基因的检测限为101copies;对鼠伤寒沙门氏菌hilA基因的检测限为103copies。马佳睿[17]的多重巢式PCR检测方法中,也出现了对鼠伤寒沙门氏菌(1.57 pg/μL)检测的灵敏度低于金黄色葡萄球菌(157 fg/μL)的现象,这可能是鼠伤寒沙门氏菌的基因扩增较为困难或是DNA聚合酶的偏好性造成的。
表4 三种目标基因的检测限结果
Table 4 The detection limit results of the three target genes
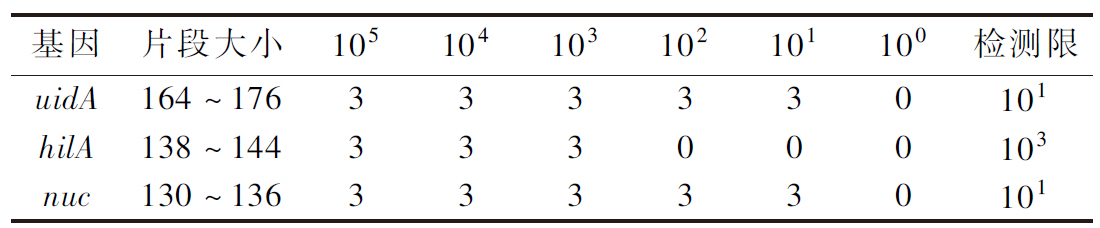
注:表中所示数字表示检出该基因的样本个数。
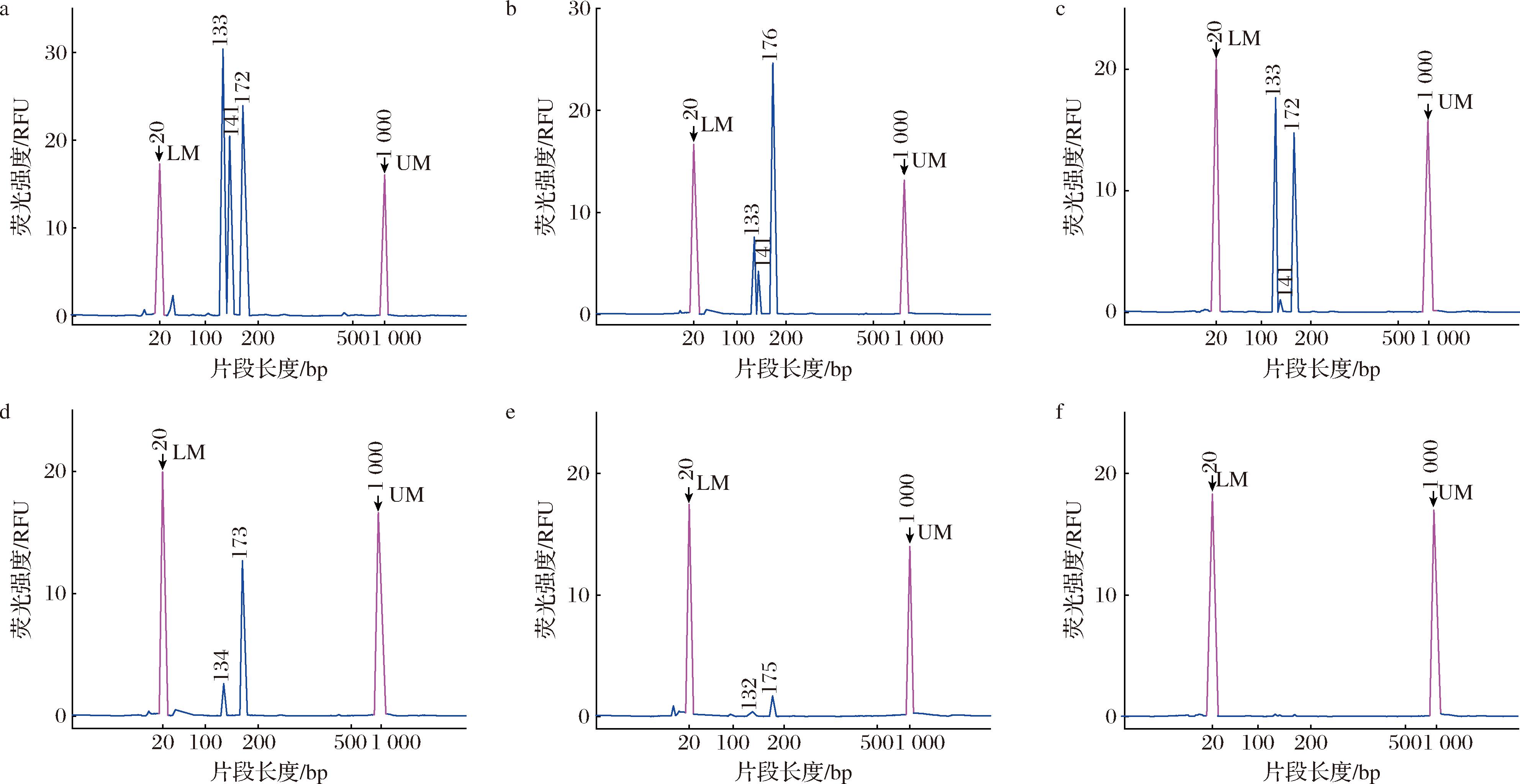
a-105;b-104;c-103;d-102;e-101;f-100
图7 不同拷贝数的多重巢式PCR检测结果
Fig.7 Results of multiplex nested PCR with different copies
2.5.3 食品基质中的检测结果
各含混合菌液的食品基质DNA提取及检测结果如表5所示,无食品基质样本提取得到(9.23±0.57) ng的DNA,其余样本提取量均高于无食品基质样本,说明除目标菌的DNA外,还提取到了食品基质本身所含有的DNA。检测结果显示,所有样本中均能检测到3种目标基因,表明该方法在面临真实食品样本时,仍有很好的检测效果。
表5 不同食品基质中的检测结果
Table 5 The detection results in various food matrices
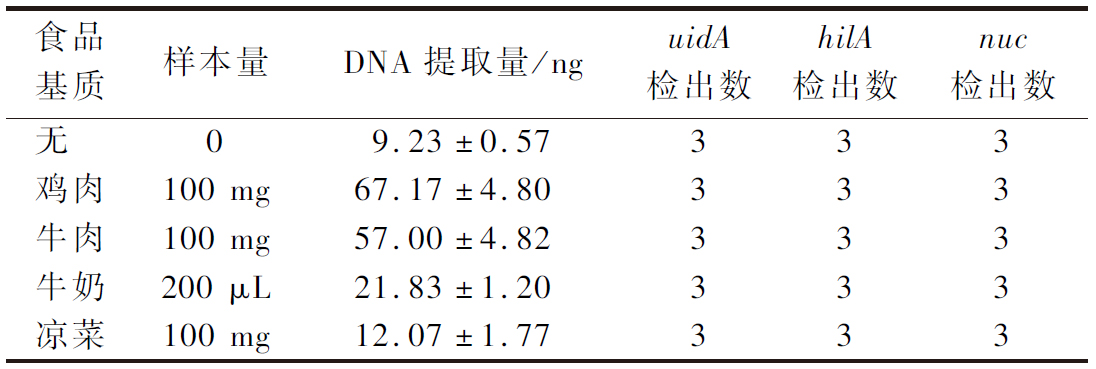
注:食品基质为“无”即为直接对混合菌液进行提取,提取DNA总体积为50 μL,检测用量为1 μL。
3 结论
食品安全事件的频繁发生严重影响着人类健康,食源性致病菌是影响食品安全的罪魁祸首。传统培养法在致病菌的检测中面临着越来越多的挑战,除培养周期长、灵敏度低、生物安全风险高和不能检测死细菌等缺点外,更有研究表明大部分食源性致病菌在食品加工过程中会进入活的非可培养状态,该状态下的细菌无法在常规培养条件中快速增殖,从而导致了假阴性结果的产生,这对传统培养法提出了新的挑战[18-19]。多重PCR可直接检测致病菌的基因,不受致病菌生长状态的限制,是一种更具优势的检测方法。多重PCR技术在替代传统培养检测食源性致病菌中已有广泛的应用,LEI等[20]同时利用多重PCR和传统培养检测食品中的6种致病菌,结果显示多重PCR法检出的阳性率更高;李雪艳等[7]也用多重PCR和国家标准中的方法对300份不同来源的食品样本进行检测,结果显示对于沙门氏菌、李斯特菌和金黄色葡萄球菌的阳性率,多重PCR也显著高于国家标准中的培养法(分别检出22例与6例),但检测限仍然停留在ng水平。提高对食源性致病菌检测的准确性和灵敏度是食品检测领域中的迫切需要。
本研究基于多重PCR技术,引入巢式扩增和毛细管电泳技术,旨在开发一种更加准确和灵敏的检测方法,用于同时检测3种常见食源性致病菌(大肠埃希氏菌、鼠伤寒沙门氏菌和金黄色葡萄球菌),以满足食品安全领域的需求[21]。本研究采用巢式PCR两步扩增技术,取代传统PCR一步扩增,显著增强了引物对短片段(<200 bp)目标基因的特异性,从而提高了检测准确性。利用毛细管电泳代替传统琼脂糖凝胶电泳分析后,对大肠埃希氏菌uidA基因和金黄色葡萄球菌nuc基因的检测灵敏度达到101 copies,对沙门氏菌hilA基因达到103 copies。范宏伟等[22]利用多重PCR-毛细管电泳检测大肠杆菌,其检测限达103 copies,本方法通过巢式扩增将检测限提升至101 copies,与朱安基等[23]采用荧光定量PCR的灵敏度相当,但试剂成本和设备需求更低。马佳睿[17]的多重巢式PCR方法对金黄色葡萄球菌和沙门氏菌检测限分别为157 fg/μL和1.57 pg/μL(约3×105 copies和1.33×106 copies),本方法引入毛细管电泳后,灵敏度分别提高了4个和3个数量级。此外,毛细管电泳将单样本检测时间从传统凝胶电泳的15~30 min缩短至5 min以内,显著提高了检测速度。为验证方法特异性,本研究以3种非目标食源性致病菌作为阴性对照进行干扰实验,结果表明即使在复杂背景下,仍能准确检测3种目标菌,充分证实了方法的特异性。值得注意的是,本研究中的方法需对PCR产物进行开盖处理,可能会造成气溶胶污染,因此需要严格遵守标准PCR实验室的要求,防止污染回流影响后续检测结果。
在实际食品样本检测中,DNA提取和纯化也是一个关键环节。复杂基质样本(如奶酪)中可能含有PCR抑制物,巢式PCR在第二轮扩增时对样本进行了稀释,降低了反应体系中食品基质的浓度以及PCR抑制物的浓度,往往比普通PCR具有更高的扩增效率,从而加大了其检测的灵敏度。因此,巢式PCR两轮扩增或许对一些基质复杂的食品样本的检测更具优越性[24-25]。
本研究结合多重和巢式PCR以及毛细管电泳技术,建立了一种对大肠埃希氏菌、鼠伤寒沙门氏菌和金黄色葡萄球菌的快速、准确和高灵敏的检测方法。多重扩增实现对3种目标菌的同时检测;巢式PCR通过两轮扩增显著提升了特异性;毛细管电泳将分辨率提高至8 bp的同时,灵敏度方面也得到了显著提升。经过巢式PCR两轮扩增退火温度的优化后,本方法对大肠埃希氏菌和金黄色葡萄球菌基因的检测限可达101 copies,鼠伤寒沙门氏菌基因可达103 copies,较文献报道的同类方法高出3~4个数量级,与荧光定量PCR相当,但成本更低。特异性测试表明,该方法不受非目标菌干扰,进一步验证了其检测的准确性。从DNA提取到检测总时长不超过4 h,为食源性致病菌快速检测提供了一种高效方案。
[1] SAUCIER L. Microbial spoilage, quality and safety within the context of meat sustainability[J]. Meat Science, 2016, 120:78-84.
[2] MEAD P S, SLUTSKER L, DIETZ V, et al. Food-related illness and death in the United States[J]. Emerging Infectious Diseases, 1999, 5(5):607-625.
[3] SUN F L, CAO Z S, QIU Z G, et al. Development of a simultaneous identification method for nine species of foodborne bacterial pathogens using real-time PCR assays and melting curve analysis[J]. Journal of Biotech Research, 2020, 11: 73-81.
[4] FODDAI A C G, GRANT I R. Methods for detection of viable foodborne pathogens: Current state-of-art and future prospects[J]. Applied Microbiology and Biotechnology, 2020, 104(10):4281-4288.
[5] ALTAYB H N, BADRI R M, CHAIEB K, et al. Detection and characterization of the most common foodborne pathogens by using multiplex PCR procedure[J]. Saudi Journal of Biological Sciences, 2023, 30(6):103653.
[6] 殷淑权. 多重PCR在食源性微生物快速检验中的效果分析[J]. 智慧健康, 2023, 9(27):207-210.YIN S Q. Effect analysis of multiplex PCR in rapid test of foodborne microorganisms[J]. Smart Healthcare, 2023, 9(27):207-210.
[7] 李雪艳, 魏彩姣, 王庄舒, 等. 多重PCR检测技术和传统培养法在食源性致病菌检测中的应用分析[J]. 质量与认证, 2025(1):96-98.LI X Y, WEI C J, WANG Z S, et al. Application analysis of multiplex PCR detection technology and traditional culture method in detection of food-borne pathogens[J]. China Quality Certification, 2025(1):96-98.
[8] LAW J W, AB MUTALIB N S, CHAN K G, et al. Rapid methods for the detection of foodborne bacterial pathogens: Principles, applications, advantages and limitations[J]. Frontiers in Microbiology, 2015, 5:770.
[9] 李聪, 刘健慧, 李志辉, 等. 4种食源性致病菌的多重PCR快速检测方法研究[J]. 食品研究与开发, 2019, 40(21):164-169.LI C, LIU J H, LI Z H, et al. Study on multiplex PCR of rapid detection method for four foodborne pathogens[J]. Food Research and Development, 2019, 40(21):164-169.
[10] CHAMBERLAIN J S, GIBBS R A, RANIER J E, et al. Deletion screening of the Duchenne muscular dystrophy locus via multiplex DNA amplification[J]. Nucleic Acids Research, 1988, 16(23):11141-11156.
[11] MARKOULATOS P, SIAFAKAS N, MONCANY M. Multiplex polymerase chain reaction: A practical approach[J]. Journal of Clinical Laboratory Analysis, 2002, 16(1):47-51.
[12] GOULART L R, COLOMBO B F M, LIMA M I S, et al. Expanded HPV genotyping by single-tube nested-multiplex PCR may explain HPV-related disease recurrence[J]. Microorganisms, 2024, 12(11):2326.
[13] 曾成鸣, 康格非. 高效毛细管电泳及其应用进展[J]. 国外医学.临床生物化学与检验学分册, 1995, 16(4):178-179.ZENG C M, KANG G F. High performance capillary electrophoresis and its application progress[J]. Foreign Medical Sciences, 1995, 16(4):178-179.
[14] 张明娟, 王娟, 袁磊, 等. 多重聚合酶链式反应技术在食源性致病菌检测上的应用研究进展[J]. 食品与发酵工业, 2021, 47(2):305-310.ZHANG M J, WANG J, YUAN L, et al. Application of multiplex polymerase chain reaction in detection of foodborne pathogens[J]. Food and Fermentation Industries, 2021, 47(2):305-310.
[15] 向婧姝, 周倩, 周藜, 等. 三种多重PCR技术检测食源性致病菌的对比研究[J]. 微量元素与健康研究, 2024, 41(5):59-62.XIANG J S, ZHOU Q, ZHOU L, et al. Comparative study on detection of food-borne pathogens by three multiplex PCR techniques[J]. Studies of Trace Elements and Health, 2024, 41(5):59-62.
[16] THALINGER B, PÜTZ Y, TRAUGOTT M. Endpoint PCR coupled with capillary electrophoresis (celPCR) provides sensitive and quantitative measures of environmental DNA in singleplex and multiplex reactions[J]. PLoS One, 2021, 16(7): e0254356.
[17] 马佳睿. 食源性金黄色葡萄球菌和沙门氏菌双重巢式PCR及双重LAMP检测方法的建立及应用[D]. 银川: 宁夏大学, 2021.MA J R. Establishment and application of double nested PCR and double LAMP detection methods to food-borne Staphylococcus aureus and Salmonella[D]. Yinchuan: Ningxia University, 2021.
[18] PODOLAK R, BLACK D G. Control of Salmonella and Other Bacterial Pathogens in Low Moisture Foods[M]. 1st ed. Hoboken, New Jersey: Wiley Blackwell, 2017.
[19] OLIVER J D. Recent findings on the viable but nonculturable state in pathogenic bacteria[J]. FEMS Microbiology Reviews, 2010, 34(4):415-425.
[20] LEI I F, ROFFEY P, BLANCHARD C, et al. Development of a multiplex PCR method for the detection of six common foodborne pathogens[J]. Journal of Food and Drug Analysis, 2008, 16(4): 6.
[21] SHARIFDINI M, MIRHENDI H, ASHRAFI K, et al. Comparison of nested polymerase chain reaction and real-time polymerase chain reaction with parasitological methods for detection of Strongyloides stercoralis in human fecal samples[J]. The American Journal of Tropical Medicine and Hygiene, 2015, 93(6):1285-1291.
[22] 范宏伟, 朱应飞, 翟平平, 等. 多重聚合酶链式反应-毛细管电泳技术检测5种食源性致病菌[J]. 食品安全质量检测学报, 2025, 16(1):180-186.FAN H W, ZHU Y F, ZHAI P P, et al. Detection of 5 kinds of foodborne pathogens by multiplex polymerase chain reaction and capillary electrophoresis technology[J]. Journal of Food Safety &Quality, 2025, 16(1):180-186.
[23] 朱安基, 李世宏, 徐浩, 等. 奶牛乳房炎大肠埃希氏菌和肺炎克雷伯菌及奇异变形杆菌三重TaqMan荧光定量PCR检测方法的建立[J]. 动物医学进展, 2024, 45(12): 19-25.ZHU A J, LI S H, XU H, et al. Establishment of a triple TaqMan fluorescence quantitative PCR method for detection of Escherichia coli, Klebsiella pneumoniae and Proteus mirabilis in dairy mastitis[J]. Progress in Veterinary Medicine, 2024, 45(12): 19-25.
[24] RUANO G, FENTON W, KIDD K K. Biphasic amplification of very dilute DNA samples via ‘booster’ PCR[J]. Nucleic Acids Research, 1989, 17(13):5407.
[25] ZBRUN M V, MORENO N, CAMUSSONE C M, et al. Comparison of real-time PCR and nested PCR based on the HlyA gene for the detection of Listeria monocytogenes. Application on cheese samples[J]. Brazilian Journal of Microbiology, 2024, 55(2):1783-1791.