食品安全是全球性重大挑战,对公共卫生和经济可持续发展构成严重威胁。据世界卫生组织统计,全球每年约10%的人口遭受食源性疾病困扰,导致42万人死亡,其发病率在全球总发病率中名列前茅[1]。食源性疾病主要由腐败食品中的致病性微生物引起。致病性微生物包括大肠杆菌(Escherichia coli)、沙门氏菌、金黄色葡萄球菌(Staphylococcus aureus)及单核细胞增生李斯特菌等[2]。目前广泛使用的化学防腐剂(如苯甲酸钠、山梨酸钾等)虽经食品药品监督管理局认证,但抗菌谱较窄,长期摄入存在致癌、致畸等健康风险,并可能导致耐药菌株出现[3]。因此,亟需开发新型生物防腐剂来应对这一现状。在抗生素耐药性问题日益突出的背景下,抗菌肽(antimicrobial peptides,AMPs)作为天然免疫效应分子,因其高效、低毒、安全、不易诱导耐药性,在解决致病性微生物污染方面展现出独特优势,已成为食品保鲜领域极具前景的候选生物防腐剂[4]。
然而,AMPs作为新型食品防腐剂在实际应用中面临合成成本高、抗菌活性不足、稳定性差、抗菌谱窄及具有潜在毒性等多重挑战[5-6]。为克服以上应用瓶颈,研究者们通过多种分子改造策略对AMPs进行结构优化,包括定点氨基酸替换、杂合肽设计及末端修饰等[7]。在众多改造策略中,杂合肽设计因能够整合不同AMPs的结构优势而备受关注。天蚕素(Cecropin)是最早被发现的AMPs之一,通常由31~39个氨基酸残基组成,具有广谱抗菌、抗肿瘤及抗病毒活性。但较长的肽链结构导致其化学合成成本较高,限制了其大规模应用[8]。研究证实,Cecropin A的N端1-8区域因其高度保守的α-螺旋结构,在与其他功能肽段杂交时能显著提升抗菌活性、细胞选择性及环境稳定性[9]。Aurein家族是从澳大利亚金铃蛙皮肤中分离得到的短α-螺旋AMPs。其中,Aurein 1.2抗菌谱窄,仅对革兰氏阳性菌具有较弱抗菌活性,这促使研究者们不断尝试对其进行结构优化[10]。基于此,本研究创新性地采用生物信息学工具系统分析了Aurein 1.2的结构特征、净电荷及疏水性等关键参数,进而鉴定出其核心功能片段Aurein 1.2(6-13)。通过分子杂合策略,将Cecropin A(1-8)与该核心片段进行拼接,成功构建杂合肽CA16。经验证该分子净电荷为+5,疏水性为0.414,符合典型AMPs的分子设计参数特征[11-12]。为进一步提升其生物相容性与应用潜力,依据疏水性预测结果,将CA16第2位的色氨酸(Trp, W)及第16位的苯丙氨酸(Phe, F)均替换为亮氨酸(Leu, L),最终获得疏水性为0.374的新型杂合肽CA16-L。随后,对其生物活性、环境稳定性、作用机制以及猪肉防腐保鲜效果进行了全面评估。本研究不仅为开发高效、稳定的肽类食品防腐剂提供了新的研究思路,同时也为深入理解AMPs的构效关系提供了重要的理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
大肠杆菌(E.coli ATCC25922、E.coli K88)、肺炎克雷伯菌(Klebsiella pneumonia CMCC46117)、鼠伤寒沙门氏菌(Salmonella typhimurium ATCC14028)、绿脓杆菌(Pseudomonas aeruginosa ATCC27853)、金黄色葡萄球菌(S.aureus ATCC25923、S.aureus ATCC29213)和粪链球菌(Enterococcus faecalis ATCC29212)、表皮葡萄球菌(Staphylococcus epidermidis ATCC12228)由吉林医药学院保存。
1.1.2 主要试剂
MH肉汤培养基(Mueller Hinton broth, MHB)、MH固体培养基(Mueller Hinton agar, MHA),北京奥博星生物技术有限公司;十二烷基硫酸钠(sodium dodecyl sulfate, SDS),北京索莱宝科技有限公司;三氟乙醇(2, 2, 2-trifluoroethanol, TFE)、N-苯基-1-萘胺(N-phenyl-1-naphthylamine, NPN)、邻硝基苯基-β-D-半乳糖苷(o-nitrophenyl-β-D-galactopyranoside, ONPG)、3, 3′-二丙基硫杂二羰花青碘化物(3, 3′-dipropylthiocarbocyanine iodide, DiSC3-5)、脂多糖(lipopolysaccharide, LPS),西格玛奥德里奇(上海)贸易有限公司;细菌基因组DNA抽提试剂盒,生工生物工程(上海)股份有限公司;乳酸链球菌肽(Nisin),上海麦克林生化科技有限公司。
1.2 仪器与设备
GENiso F129004酶标仪,奥地利Tecan公司;J-810圆二色谱仪,日本Jasco公司;F-4500荧光分光光度计,日本Hitachi公司;SU8100扫描电子显微镜,株式会社日立制作所;SW-CJ-1D超净工作台,苏州净化设备有限公司;DYY-8C电泳仪,北京六一生物科技有限公司;YT-04拍打式无菌均质器,上海叶拓科技有限公司。
1.3 实验方法
1.3.1 杂合肽的设计及合成
基于AMPs的构效关系,本研究将Cecropin A(1-8)与Aurein 1.2(6-13)片段杂合,获得了杂合肽CA16。为进一步提高其细胞选择性指数,将杂合肽CA16第2位的W和第16位的F均替换为L,成功构建了新型杂合肽CA16-L。此外,将2种杂合肽的C端进行酰胺化修饰来增强结构稳定性。上述序列均由生工生物工程(上海)股份有限公司采用固相合成法合成,经高效液相色谱法纯化(纯度>95%),并最终通过电喷雾质谱法进行分子量验证。本研究以蜂毒肽(Melittin)作为阳性对照。该肽是一种具有破膜杀菌作用的典型阳离子α-螺旋AMPs,在AMPs研究中已被广泛用作α-螺旋类AMPs的活性标准对照品[13-14]。
1.3.2 二级结构测定
采用圆二色谱仪测定多肽在模拟环境中的二级结构。将多肽分别溶解于10 mmol/L PBS、30 mmol/L SDS和50%(体积分数)TFE中,并使用1 mm光程的石英比色皿,以100 nm/min的扫描速度,在195~250 nm波长范围内对其圆二色性进行测定。每个样品重复扫描3次,数据取平均值,并计算平均残基椭圆率。
1.3.3 体外抗菌活性测定
采用改良的微量稀释法测定多肽对细菌的最小抑菌浓度(minimum inhibitory concentration,MIC)。首先将待测细菌培养至对数期,调整菌液浓度至OD600nm=0.05,并采用十倍梯度稀释法将菌液稀释至1×105 CFU/mL。接着,在96孔板中依次加入50 μL细菌悬浮液和50 μL含不同浓度多肽的MHB溶液,充分混匀后在37 ℃下恒温培养18~22 h。以未添加多肽组作为阳性对照,未添加菌液组作为阴性对照。本实验重复进行3次。
1.3.4 生物相容性分析
在溶血活性测定中,将抗凝的新鲜人类全血在4 ℃、1 000×g下离心10 min,使用PBS(pH 7.4)洗涤3次后,制备成2%(体积分数)的红细胞悬液。接着,取100 μL红细胞悬液分别与等体积不同浓度的多肽溶液混合,37 ℃下孵育1 h后,离心获取上清液,并在570 nm下测定其吸光度。以0.2%(体积分数)Triton X-100处理组作为阳性对照(100%溶血),PBS处理组作为阴性对照(0%溶血)。本实验重复进行3次。
采用CCK-8比色法检测多肽对人胚肾细胞HEK 293T的细胞毒性。将细胞以1~2×105个/孔的密度接种于96孔板,置于37 ℃、5%(体积分数)CO2培养箱中培养16 h。待细胞贴壁后,加入梯度稀释的多肽液继续培养16 h。接着,每孔加入10%(体积分数)CCK-8,37 ℃孵育2 h后,使用酶标仪测定450 nm处吸光度值。以未处理细胞为对照,计算细胞存活率。本实验重复进行3次。
1.3.5 稳定性评价
E.coli ATCC25922和S.aureus ATCC29213分别作为革兰氏阴性菌和革兰氏阳性菌的代表菌株。在盐离子稳定性测试中,将多肽分别置于不同盐离子溶液中(150 mmol/L NaCl、4.5 mmol/L KCl、6 μmol/L NH4Cl、1 mmol/L MgCl2、8 μmol/L ZnCl2、2 mmol/L CaCl2和4 μmol/L FeCl3)[13],测定其对测试菌的MIC值。在温度稳定性测试中,将多肽置于不同温度(4、37、60、100 ℃)条件下处理30 min,待其自然冷却至室温后,测定其对测试菌的MIC值。在pH稳定性测试中,将多肽置于不同pH(2、4、6、8、10、12)条件下,于37 ℃下孵育6 h后,测定其对测试菌的MIC值。
1.3.6 耐药性诱导实验
以E.coli ATCC25922 为代表菌株,采用连续亚抑菌浓度传代法评估其对多肽的耐药性发展。每代从前一培养周期的亚MIC孔中取菌,培养至对数生长期后,调整菌液浓度至1×105 CFU/mL,参照1.3.3节微量肉汤稀释法测定MIC值。本实验连续进行30代传代培养,并以黏菌素作为阳性对照,全程记录各代次MIC值变化,绘制耐药性发展曲线。
1.3.7 LPS绑定分析
采用鲎试剂(Limulus amebocyte lysate, LAL)显色法检测多肽的内毒素中和活性。将待测多肽溶液用无热原水进行2倍系列稀释,取100 μL该稀释液与等体积1 EU/mL LPS溶液混合,37 ℃水浴孵育60 min 完成中和反应。随后,依次加入100 μL LAL试剂和100 μL显色底物,反应终止后加入500 μL偶氮试剂(1、2、3)。使用酶标仪于545 nm波长下测定吸光度。以无热原水为阴性对照,1 EU/mL LPS为阳性对照,所有操作均在严格无热原条件下完成。本实验重复进行3次。
1.3.8 细胞外膜通透性测定
采用NPN荧光探针法检测细胞外膜通透性。使用5 mmol/L 4-羟乙基哌嗪乙磺酸[4-(2-hydroxyethyl) piperazine-1-ethanesulfonic acid,HEPES]缓冲液洗涤对数生长期的E.coli ATCC25922,调整菌悬液浓度至OD600nm=0.05。加入终浓度为10 μmol/L的NPN,于室温下避光孵育30 min。然后,将其与梯度稀释的待测多肽溶液混合,立即采用F4500荧光分光光度计(激发波长350 nm、发射波长420 nm)测定荧光强度变化。以10 μg/mL黏菌素作为阳性对照。本实验重复进行3次。
1.3.9 细胞质膜去极化
利用膜电位DiSC3-5的释放来评估细胞膜的去极化程度[14]。首先,将E.coli ATCC25922和S.aureus ATCC29213培养至对数期后,用HEPES缓冲液洗涤3次,并将菌液稀释至OD600nm=0.05。随后,加入终浓度为0.4 μmol/L的DiSC3-5,37 ℃下避光孵育1 h。待空白荧光强度稳定后,加入不同浓度的多肽(1×MIC~4×MIC),在622 nm的激发波长和670 nm 的发射波长下测定0~800 s内荧光强度的变化。本实验重复进行3次。
1.3.10 扫描电镜观察
收集对数生长期的E.coli ATCC25922和S.aureus ATCC29213菌体,用PBS缓冲液洗涤3次后调整菌液浓度至OD600nm=0.2~0.5。随后,分别加入MIC浓度的杂合肽溶液孵育1 h,以未经多肽处理的细菌悬浮液作为对照组。孵育结束后,用PBS洗涤菌体3次,加入2.5%(体积分数)的戊二醛后,于4 ℃条件下固定12 h。接着,依次进行乙醇梯度脱水(30%、50%、70%、90%、100%,体积分数),每次15 min。最后,将样品放置于冷冻干燥机内进行干燥,喷金处理后,使用扫描电镜进行观察。
1.3.11 DNA凝胶阻滞实验
采用细菌基因组DNA提取试剂盒分别提取对数生长期的E.coli ATCC25922和S.aureus ATCC29213基因组DNA。经紫外分光光度计检测,DNA样品OD260nm/OD28nm均大于1.8,符合实验要求。取300 ng基因组DNA与终浓度梯度为0.5~128 μmol/L的多肽混合于10 μL结合缓冲液中,37 ℃恒温孵育1 h后,进行琼脂糖凝胶电泳检测。利用ImageJ软件对不同浓度多肽处理后的基因组DNA条带进行灰度分析,从而定量评估多肽与DNA的结合能力。以无抗菌活性的杂合多肽CL16(序列为KWKLFKKIAHKVGHKL-NH2)作为阳性对照。本实验重复进行3次。
1.3.12 杂合抗菌肽在猪肉冷藏保鲜中的应用
将市售的新鲜猪肉迅速转运至实验室,称取1 g猪肉块样品保存于无菌试管中,接种浓度为105 CFU/g的S.aureus ATCC29213。随后,向每组样品(n=4)中分别添加4×MIC的杂合肽及乳酸链球菌肽,以PBS处理过的猪肉块作为对照组。将所有样品置于4 ℃下贮存5 d,每日用无菌PBS对样本进行均质处理,并将均质液涂布于MHA平板进行菌落计数。
1.4 数据统计与分析
所有数据经过SPSS 26.0统计,结果均用“平均数±标准差”表示,当P<0.05时具有统计学意义,并使用GraphPad Prism 10软件作图。
2 结果与分析
2.1 杂合肽的理化参数
杂合肽采用固相合成法进行合成,经质谱分析发现,其实际分子质量与理论值相符,表明合成成功。生物信息学分析结果显示(表1),杂合肽CA16和CA16-L的净电荷为+5,疏水性分别为0.414和0.374(CA>CA16-L)。螺旋轮结构示意图如1所示,杂合肽CA和CA16-L均呈现出典型的非完美两亲性结构特征,且具有明显的阳离子面(蓝色代表带正电荷的氨基酸)和疏水面(黄色代表疏水性氨基酸)。
表1 杂合肽的序列及其关键结构参数
Table 1 Sequences of hybrid peptides and their key structural parameters
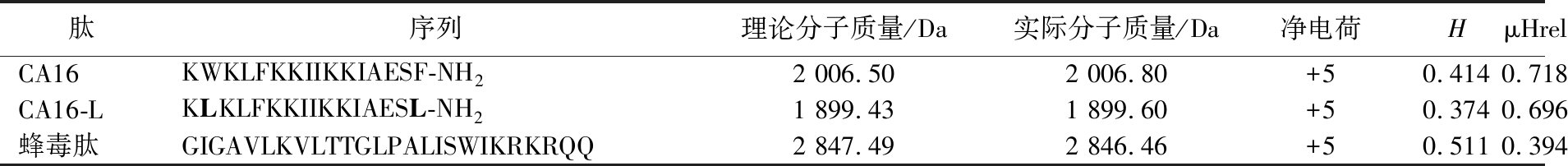
注:表中加粗的氨基酸为替换后的氨基酸;平均疏水性(H)和相对疏水力矩(μHrel)通过heliQuest在线分析平台进行计算。
肽序列理论分子质量/Da实际分子质量/Da净电荷HμHrelCA16KWKLFKKIIKKIAESF-NH22 006.502 006.80+50.4140.718CA16-LKLKLFKKIIKKIAESL-NH21 899.431 899.60+50.3740.696蜂毒肽GIGAVLKVLTTGLPALISWIKRKRQQ2 847.492 846.46+50.5110.394
2.2 二级结构测定
本研究采用圆二色谱技术分析了杂合肽CA16和CA16-L在多种模拟环境中二级结构的变化。其中,10 mmol/L PBS缓冲液用于模拟亲水环境,30 mmol/L SDS溶液用于模拟带负电荷的磷脂双分子层疏水环境,而50%(体积分数)TFE则用于模拟低极性、非聚集的疏水微环境。结果如图2所示,在亲水环境(10 mmol/L PBS)中,CA16和CA16-L均呈现无序构象;而在疏水环境[30 mmol/L SDS与50%(体积分数)TFE]中,二者均在208 nm和222 nm附近出现特征性负吸收峰,表明成功形成典型的α-螺旋结构。该结果与已有研究结论一致,部分AMPs在亲水环境中通常呈无规则或延伸构象,而在疏水环境(如模拟细胞膜条件)中则可发生构象转变,形成α-螺旋或β-折叠有序结构,从而显著影响其抗菌活性与作用特异性[15]。本研究中杂合肽的构象转变主要源于疏水环境中水分子对氢键的竞争作用减弱,肽链内部羰基氧与酰胺氢之间可形成稳定的分子内氢键,同时疏水侧链与周围低极性介质间的相互作用进一步促进了能量更低的α-螺旋构象的形成。相反,在PBS亲水环境中,水分子与肽链极性基团发生竞争性结合,破坏了内源氢键网络,导致肽链无法形成有序结构而维持无序状态。
2.3 体外抗菌活性测定
本研究采用微量稀释法测定了杂合肽CA16和CA16-L的抗菌活性。结果如图3所示,2种杂合肽均表现出广谱抗菌活性。尽管与临床常用抗生素黏菌素相比,CA16和CA16-L对革兰氏阴性菌的抗菌活性略弱,但其抗菌谱范围更广。此外,为了更好地评估杂合肽的抗菌效果,本研究计算了杂合肽对9种测试菌株的MIC的几何平均数(GMall),结果显示,CA16(GMall=2.16 μmol/L)和CA16-L(GMall=4.32 μmol/L)的抗菌效果均较好,略弱于对照蜂毒肽(GMall=1.71 μmol/L)(表2)。已有研究表明,AMPs的抗菌活性差异与其疏水性密切相关[12]。经生物信息学工具分析发现,上述3种肽的疏水性顺序为:蜂毒肽>CA16>CA16-L(表1)。总体而言,本研究设计的杂合肽对多种病原微生物显示出强效且广谱的抗菌能力,其效果优于仅对革兰氏阳性菌有效的商业肽类防腐剂乳酸链球菌肽。
表2 多肽的MHC10、GMMIC及SI值
Table 2 MHC10, GMMIC, and SI values of peptides
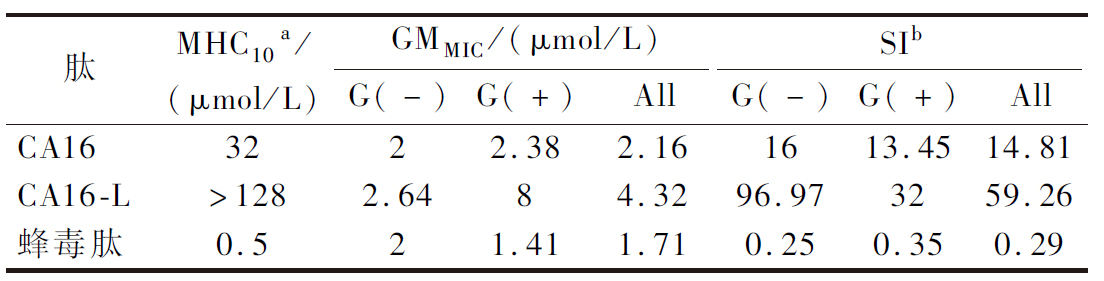
注:MHC10a是指导致人红细胞(hRBCs)溶血率大于10%的最小肽浓度;当在128 μmol/L时未检测到溶血活性时,则使用256 μmol/L的值来计算SI;SIb计算公式为MHC10/GMMIC;数值越大表明治疗潜力越高。
2.4 生物相容性分析
抗菌活性并非评估AMPs临床应用潜力的唯一标准, 生物相容性也是重要的限制因素[16]。因此,本研究通过建立溶血活性和细胞毒性双重评价体系,全面考察了多肽的安全性。溶血活性结果如图4-a所示,蜂毒肽和杂合肽CA16的10%溶血浓度(MHC10)分别为0.5 μmol/L和32 μmol/L;而疏水性相对较低的CA16-L即使在最大测定浓度128 μmol/L时,其溶血率仍低于10%。通过计算细胞选择性指数(selectivity index, SIall=MHC10/GMall)发现(表2),CA16-L(SIall=59.26)选择性指数较CA16(SIall=14.81)提高了约4倍,且明显高于蜂毒肽(SIall=0.29)。细胞毒性结果进一步证实CA16-L具有优异生物相容性,其在测定浓度下均保持80%以上的细胞存活率(图4-b)。基于上述实验,本研究开展了构效关系分析,结果表明,将杂合肽CA16中的W和F替换为L(疏水性顺序:W>F>L)后,CA16-L在维持原有抗菌活性的同时,还显著提高了生物相容性。这一结果证实,疏水性参数的精准调控是平衡多肽抗菌活性和生物安全性的有效策略[12,16]。本研究成果不仅为开发新型高效低毒的食品防腐保鲜剂提供了重要的理论支撑,同时也为其他功能性多肽的安全性优化提供了可借鉴的分子设计方式。
2.5 稳定性评价
尽管CA16-L展现出优异的细胞选择性,但其在复杂生理环境中的稳定性仍需系统评估。结果显示,在Na+、Mg2+和Ca2+溶液中,CA16和CA16-L对E.coliATCC25922 and S.aureus ATCC29213的MIC值均提高了2~8倍。已有研究证实高浓度阳离子可能通过不同的机制影响AMPs抗菌活性,对于革兰氏阳性菌,阳离子通过电荷屏蔽作用中和AMPs表面正电荷,从而减弱其与带负电细胞膜之间的静电吸附作用;对于革兰氏阴性菌,阳离子更可能与AMPs竞争结合LPS分子上的磷酸基团,进而干扰AMPs与细菌外膜的初始结合过程[17-18]。相比之下,![]() 和Fe3+对2种肽的抗菌活性影响较小(MIC变化不高于2倍),表明这些离子对肽与膜相互作用的干扰较弱。此外,经4、37、60 ℃处理后的CA16和CA16-L,对上述2种菌的MIC值未发生明显改变,表明其能耐受食品热处理过程。然而,经100 ℃处理后,2种肽的MIC值上升了4~8 倍。在极端pH环境下,CA16和CA16-L的抗菌活性表现出差异,在强酸性条件(pH 2.0)下两者的MIC值均增加了2~4倍;在强碱性条件(pH 12.0)下均增加了4~8倍;在中性环境及接近中性环境下,两者的MIC值基本维持在与对照组相当的水平或略微提高。上述结果与已有研究结论一致,稳定的α-螺旋结构是维持AMPs抗菌活性的结构基础。然而,在极端高温或极端pH条件下,二级结构可能遭到破坏,导致其抗菌活性降低[19]。总体而言,CA16-L表现出良好的盐离子适应性、温度稳定性以及宽pH耐受范围,这些特性为其作为天然食品防腐剂在食品保鲜领域的产业化应用提供了坚实的理论依据。
和Fe3+对2种肽的抗菌活性影响较小(MIC变化不高于2倍),表明这些离子对肽与膜相互作用的干扰较弱。此外,经4、37、60 ℃处理后的CA16和CA16-L,对上述2种菌的MIC值未发生明显改变,表明其能耐受食品热处理过程。然而,经100 ℃处理后,2种肽的MIC值上升了4~8 倍。在极端pH环境下,CA16和CA16-L的抗菌活性表现出差异,在强酸性条件(pH 2.0)下两者的MIC值均增加了2~4倍;在强碱性条件(pH 12.0)下均增加了4~8倍;在中性环境及接近中性环境下,两者的MIC值基本维持在与对照组相当的水平或略微提高。上述结果与已有研究结论一致,稳定的α-螺旋结构是维持AMPs抗菌活性的结构基础。然而,在极端高温或极端pH条件下,二级结构可能遭到破坏,导致其抗菌活性降低[19]。总体而言,CA16-L表现出良好的盐离子适应性、温度稳定性以及宽pH耐受范围,这些特性为其作为天然食品防腐剂在食品保鲜领域的产业化应用提供了坚实的理论依据。
2.6 诱导耐药实验
现有研究已明确揭示,靶位基因突变或耐药基因水平转移是细菌对抗生素产生耐药性的关键分子机制[20]。在此背景下,探究细菌是否会对CA16-L产生耐受性具有重要科学意义。本研究以E.coli ATCC 25922为代表菌株,系统评估了CA16-L的耐药性发展情况。结果如图6所示,在0.5×MIC浓度下持续传代培养30 d后,CA16-L处理组未观察到明显耐药性发展,而阳性对照黏菌素的MIC值则提升了32倍。上述结果充分证实,CA16-L不易诱导细菌耐药,其独特的物理性膜损伤作用,使其在食品防腐保鲜领域展现出良好应用前景。
2.7 LPS绑定能力分析
已有研究证实,阳离子AMPs对病原菌的杀灭作用主要依赖于其与细菌膜表面负电荷组分(如革兰氏阴性菌的LPS)的静电作用[14]。为深入阐明CA16-L的分子作用机制,本研究采用LAL显色法,系统评估了CA16-L与LPS的相互作用。结果如图7所示,CA16-L与LPS的结合呈浓度依赖性,随肽浓度的增加,其结合能力逐渐增强。在低浓度范围(1~8 μmol/L)内,CA16-L结合能力明显弱于阳性对照蜂毒肽;然而当浓度升高至16 μmol/L时,CA16-L展现出与蜂毒肽相当的强效结合能力。上述结果充分证明,CA16-L可通过特异性静电作用靶向识别病原菌膜表面的LPS分子,这一关键识别过程为其后续抗菌效应的发挥奠定了重要的基础。
2.8 细胞外膜通透性测定
革兰氏阴性菌的特征性外膜结构作为其关键的生理屏障,在维持菌体结构完整性和抵御外界刺激方面发挥重要作用[8]。本研究选用疏水性荧光探针NPN对外膜通透性进行定量分析,该探针在水相环境中呈现微弱荧光信号,而当其进入膜疏水区后荧光强度可显著提升。实验结果如图8所示,CA16-L作用于E.coli ATCC25922时,其外膜渗透率随肽浓度增加而增强,呈剂量依赖性。此外,阳性对照蜂毒肽在8 μmol/L浓度作用下即可使外膜渗透率达到80%,表现出快速且高效的膜穿透特性。而CA16-L需要达到16 μmol/L浓度才能实现相当的外膜渗透水平。虽然CA16-L的作用效率低于蜂毒肽,但其仍展现出较强的外膜穿透能力。
2.9 细胞质膜去极化
细菌质膜是维持细菌生命活动的关键结构。研究表明,当细菌的细胞壁受损时,其仍可保持存活状态。然而,一旦质膜结构完整性遭到破坏,将直接导致细菌死亡[19]。因此,本研究采用膜电位敏感探针DiSC3-5评估AMPs的膜去极化效应。该探针在完整膜中因淬灭而荧光微弱,一旦膜受损即可释放至胞外导致荧光增强。实验结果如图9所示,CA16-L可诱导E.coli ATCC25922和S.aureus ATCC29213产生时间及剂量依赖性膜去极化效应,但其去极化效率弱于阳性对照蜂毒肽。
2.10 扫描电镜观察
本研究采用扫描电镜直观观察了杂合肽CA16-L对细菌细胞膜的作用效果。结果如图10所示,对照组E.coli ATCC25922和S.aureus ATCC29213均呈现典型的完整形态,细胞表面光滑且结构完整。相比之下,经CA16-L处理1 h后,E.coli ATCC25922(图10-b)表面变得粗糙、出现囊泡样结构,部分细菌发生皱缩和变形。S.aureus ATCC29213(图10-d)则出现菌体聚集现象,部分细菌塌陷、变形,甚至发生裂解。上述电镜观察结果证实,CA16-L与已报道的α-螺旋AMPs的作用机制一致,其可通过破坏细菌细胞膜完整性而发挥抗菌作用[21]。
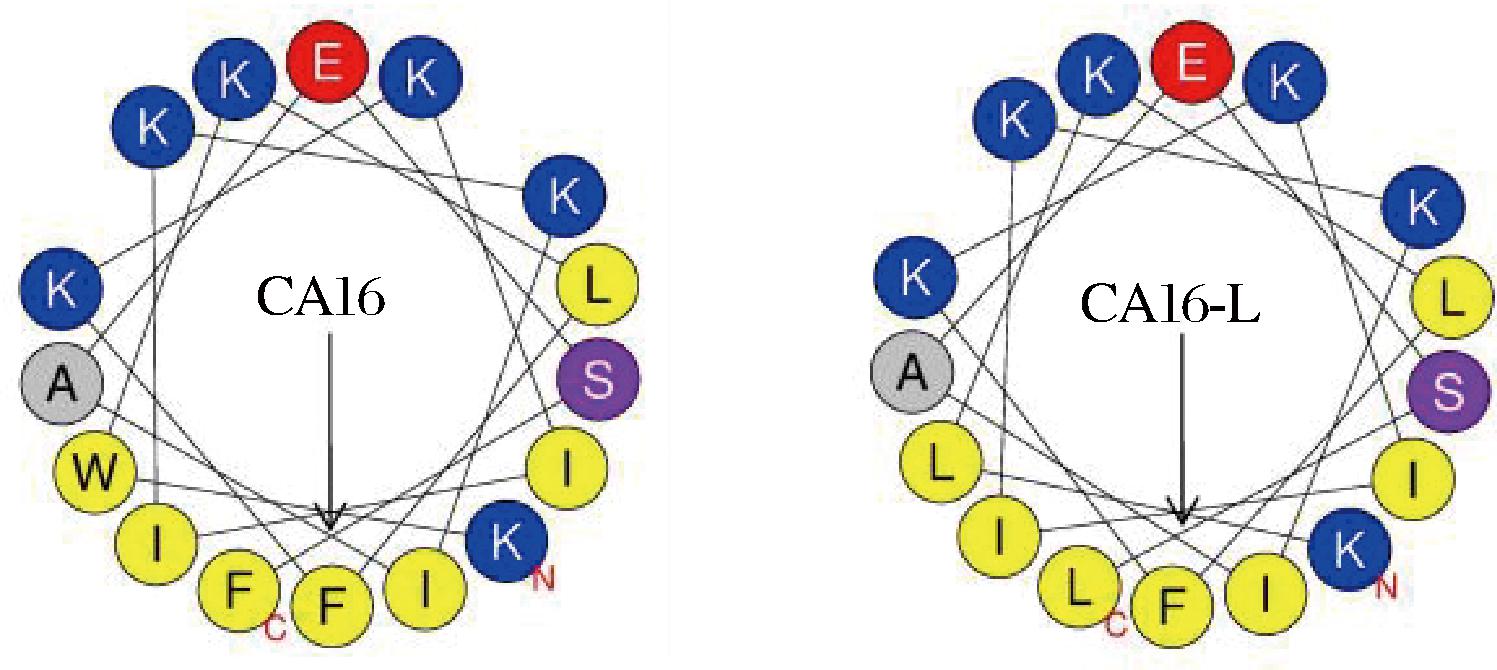
图1 杂合肽的螺旋轮结构示意图
Fig.1 Schematic diagram of the helical wheel structure of the hybrid peptides
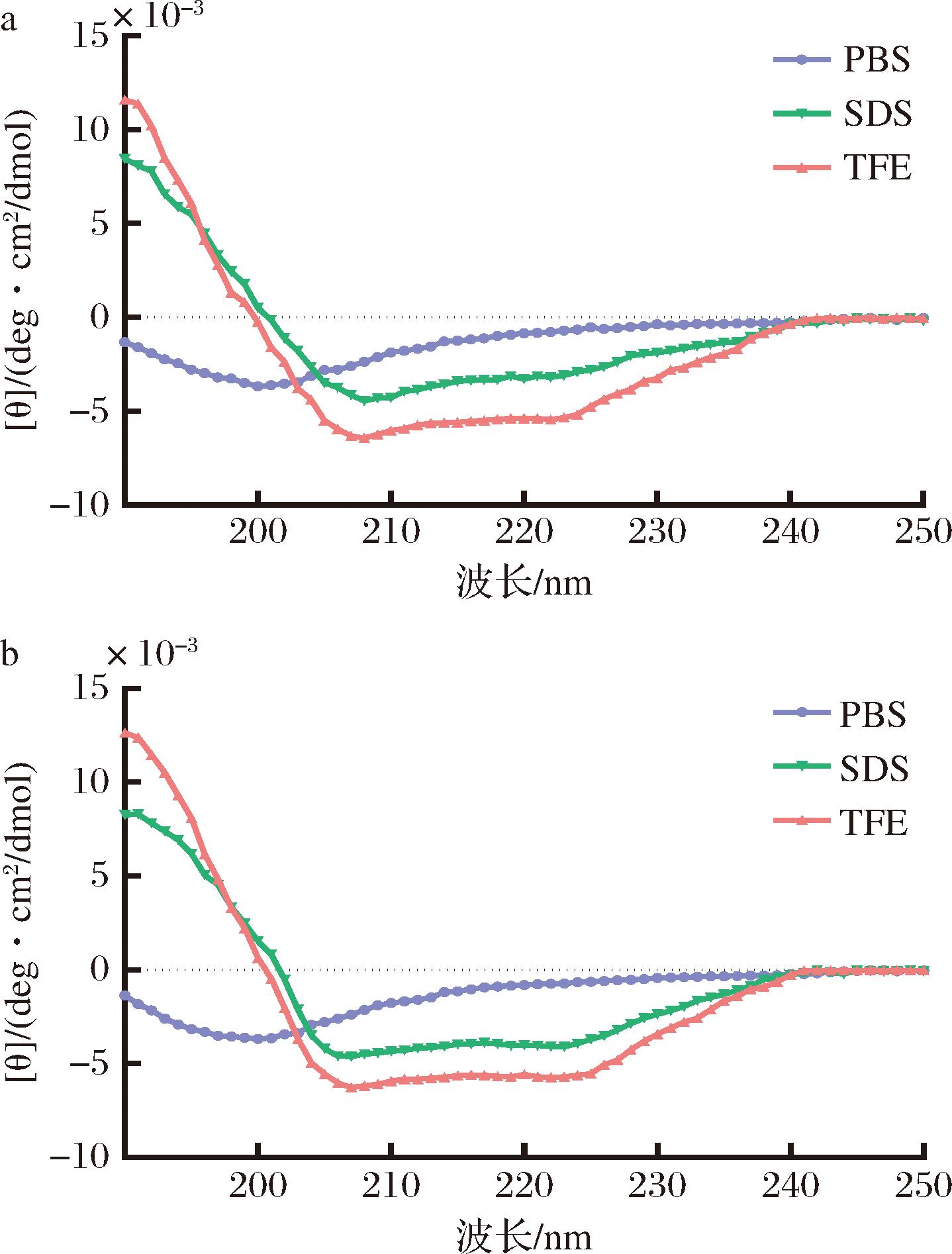
a-CA16;b-CA16-L
图2 杂合肽的CD光谱
Fig.2 CD spectrum of hybrid peptides
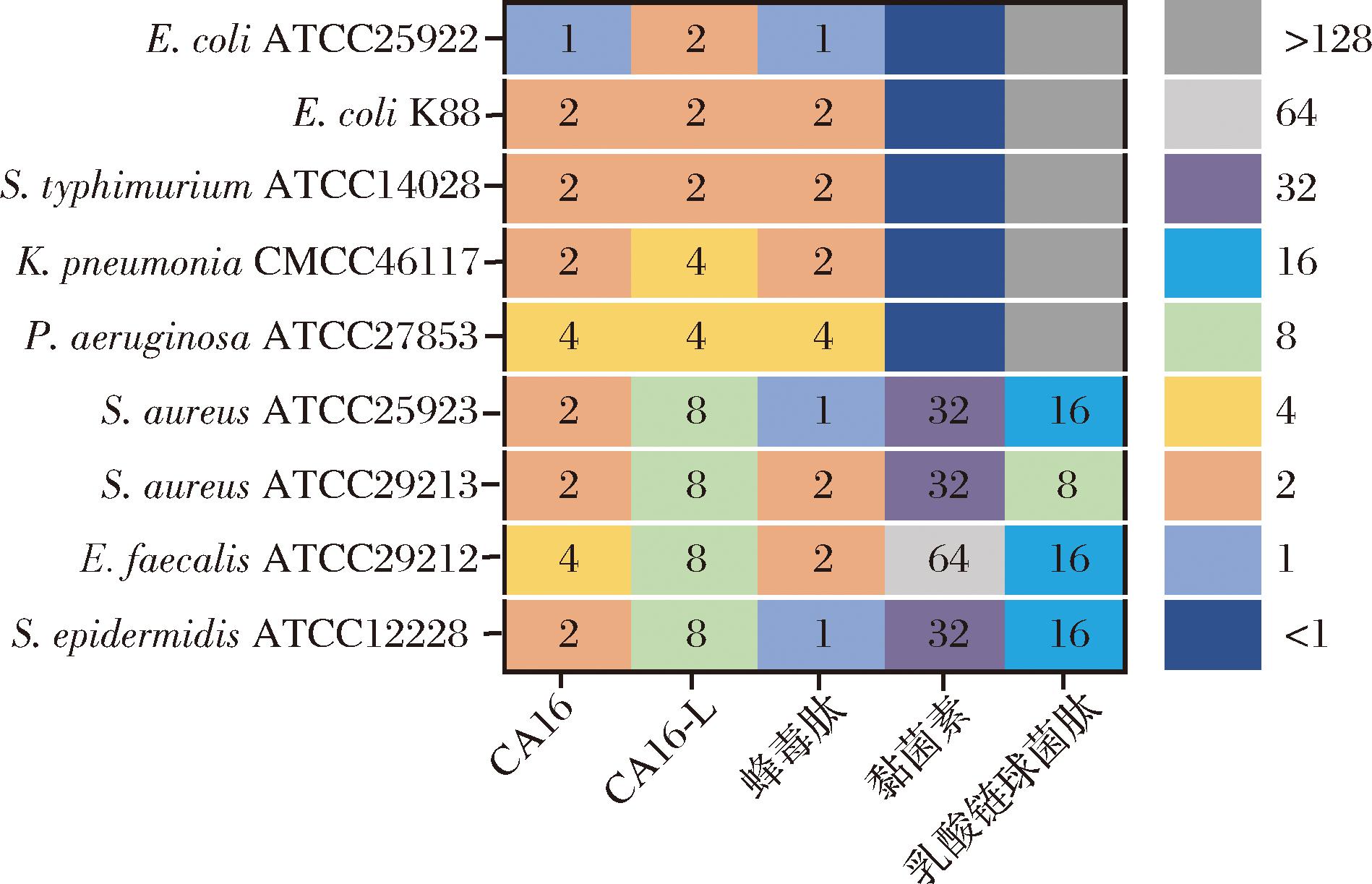
图3 多肽和黏菌素对测试菌株的MIC值
Fig.3 MIC values of the tested strains against peptides and colistin
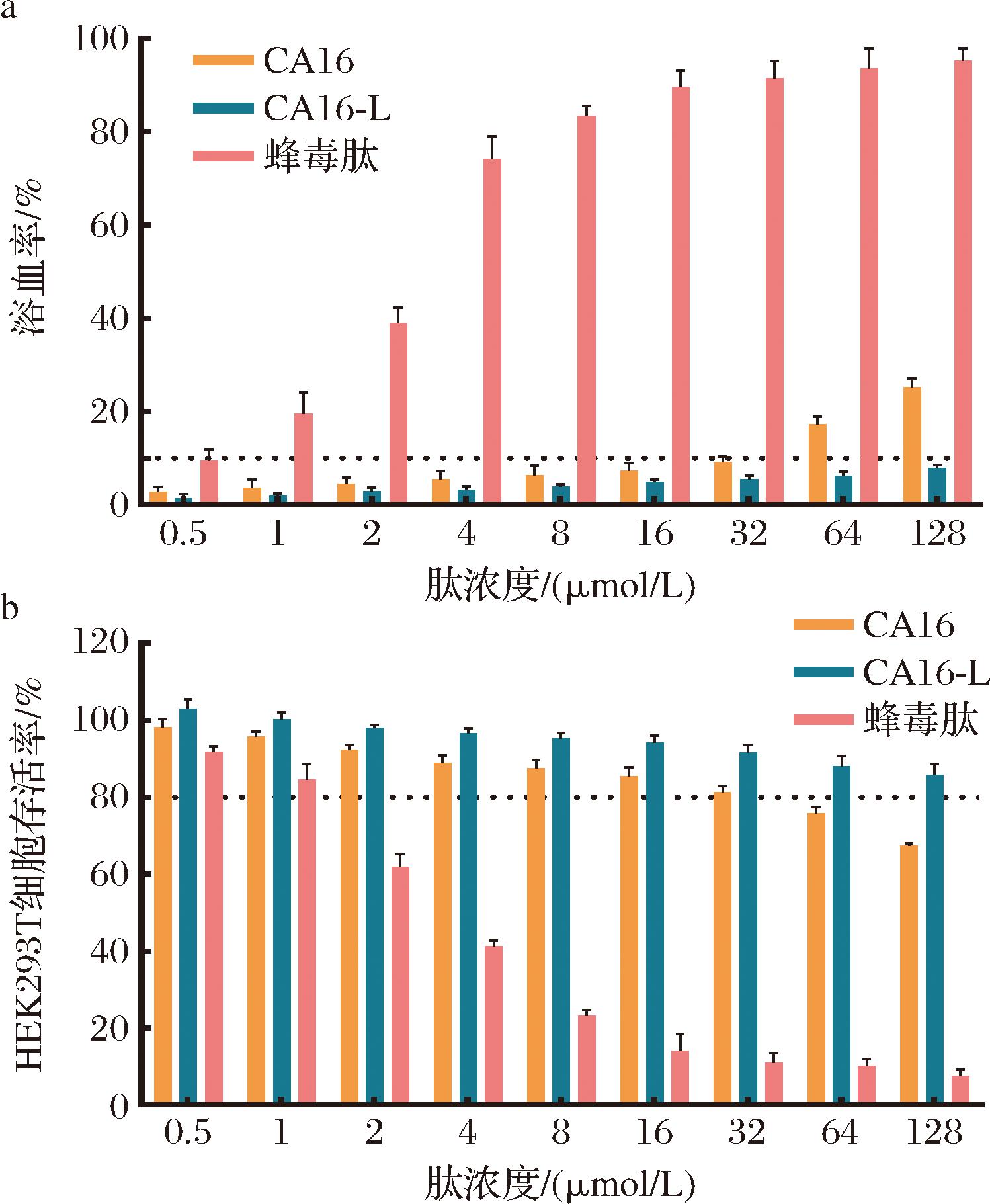
a-多肽对人红细胞的溶血活性;b-多肽对HEK293T 细胞的细胞毒性
图4 多肽的体外生物相容性
Fig.4 Biocompatibility in vitro of the peptides
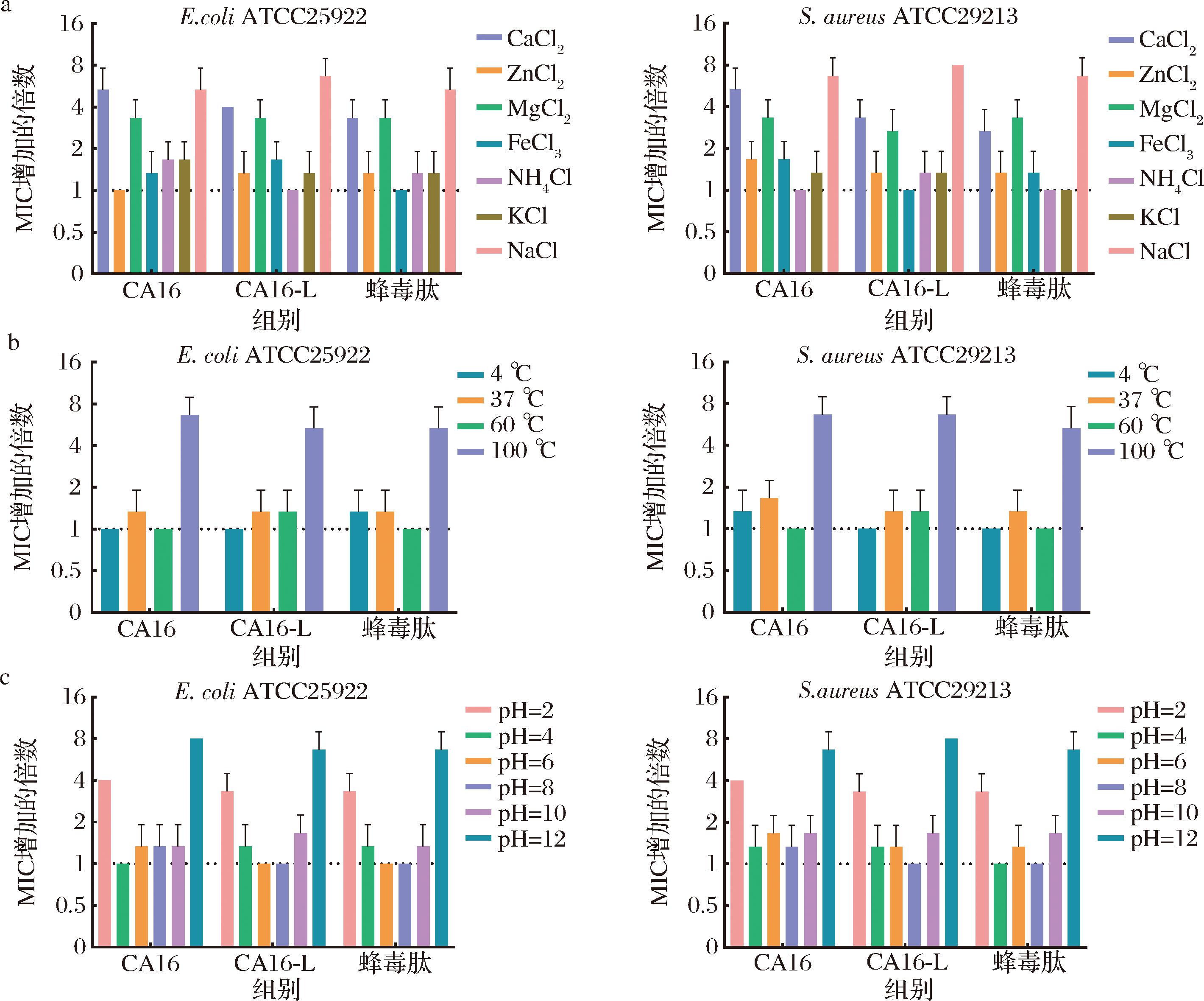
a-多肽在不同盐离子存在下的MIC值变化;b-温度对多肽抗菌活性的影响;c-pH对多肽抗菌活性的影响
图5 多肽的环境稳定性评估
Fig.5 Assessment of the environmental stability of peptides
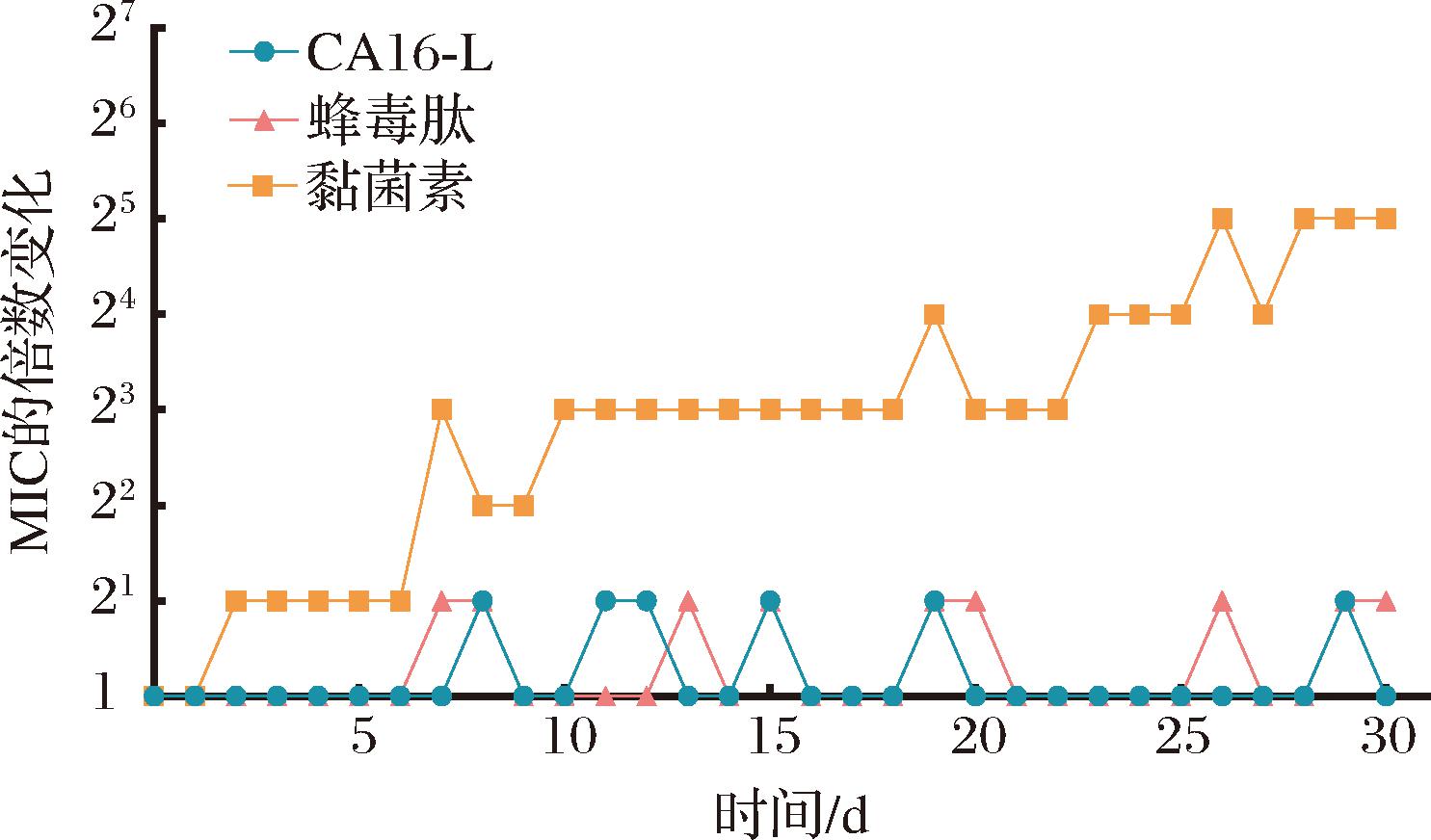
图6 多肽的耐药性发展
Fig.6 Development of resistance to peptides
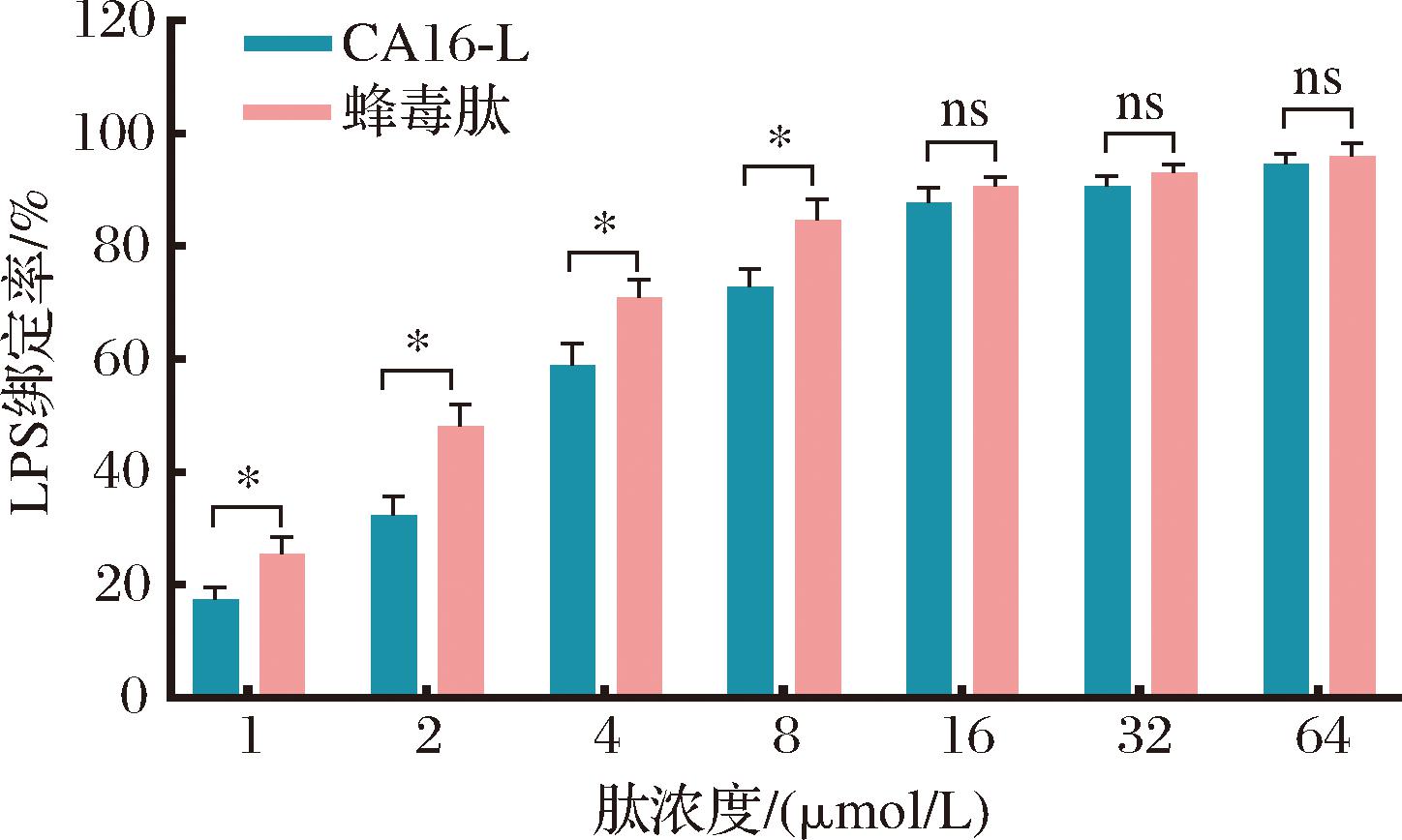
图7 多肽对LPS的结合能力
Fig.7 Binding capacity of peptides to LPS
注:*表示P<0.05;ns表示无统计学显著性(下同)。
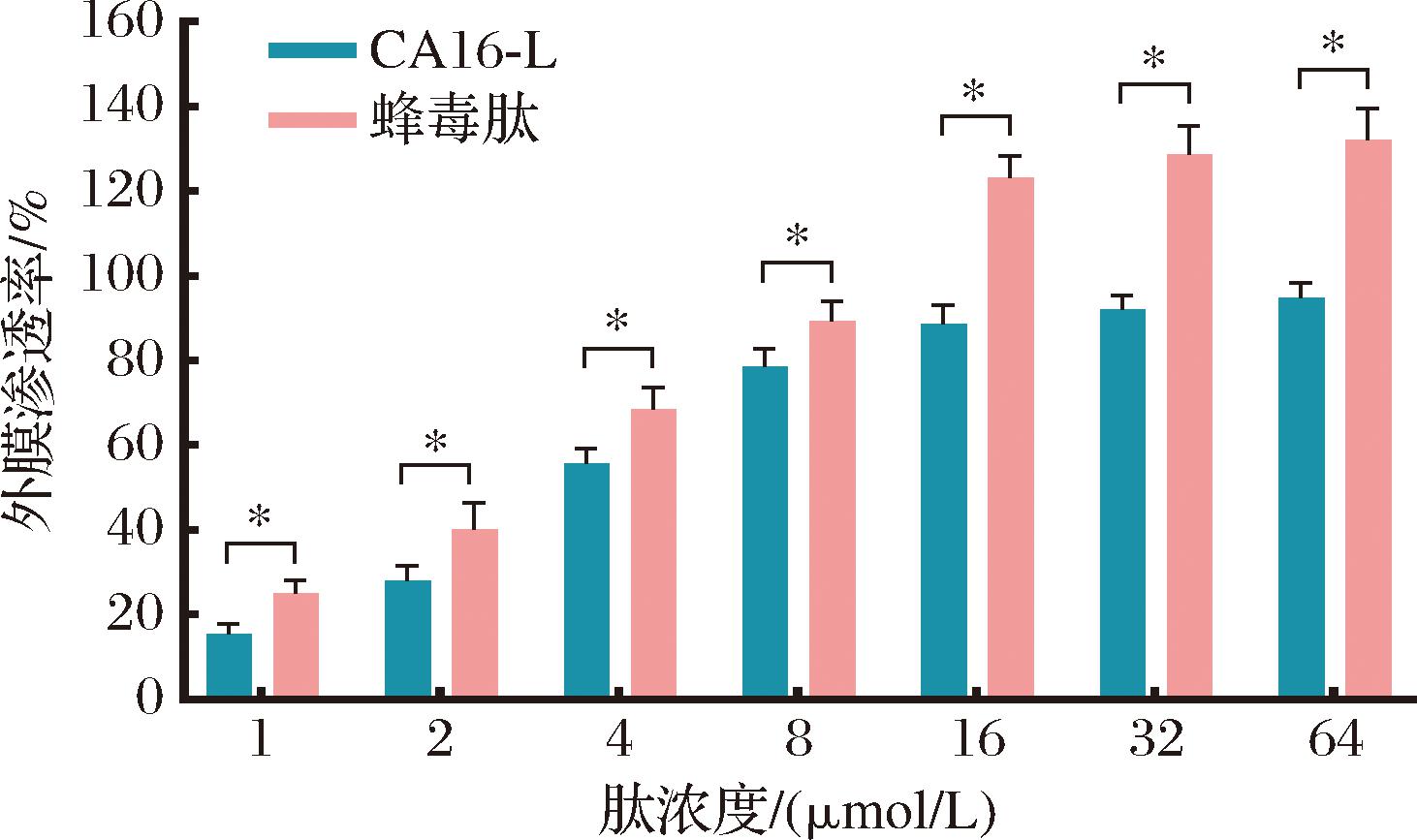
图8 多肽的外膜渗透率
Fig.8 The outer membrane permeabilization activity of peptides
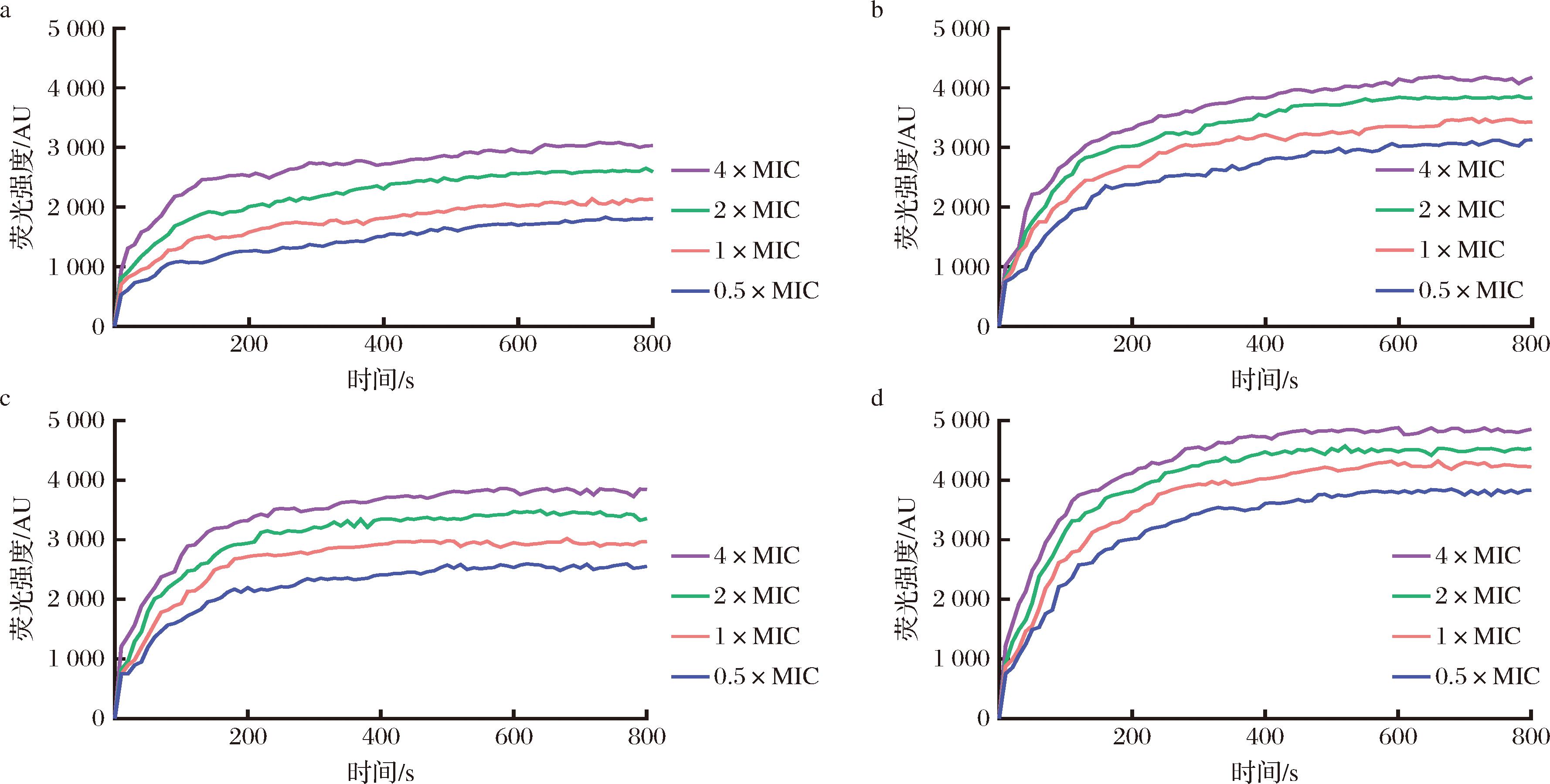
a-E.coli ATCC25922 CA16-L;b-E.coli ATCC25922 蜂毒肽;c-S.aureus ATCC29213 CA16-L;d-S.aureus ATCC29213 蜂毒肽
图9 E.coli ATCC25922和S.aureus ATCC29213的质膜电势变化
Fig.9 Cytoplasmic membrane depolarization of E.coli ATCC25922 and S.aureus ATCC29213

a-E.coli(对照);b-E.coli(CA16-L处理);c-S.aureus(对照);d-S.aureus(CA16-L处理)
图10 E.coli ATCC25922 和S.aureus ATCC25913的扫描电子显微镜图像
Fig.10 Scanning electron microscopy images of E.coli ATCC25922 and S.aureus ATCC29213
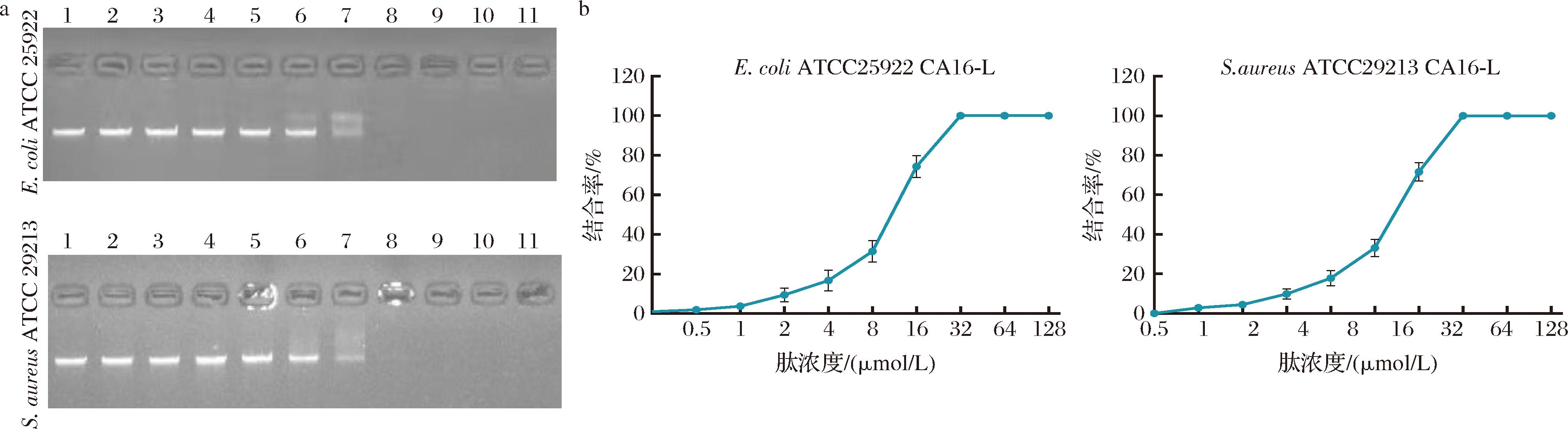
泳道1:基因组DNA;泳道2:经0.5 μmol/L CA16-L处理;泳道3:经1 μmol/L CA16-L处理;泳道4:经2 μmol/L CA16-L处理;泳道5:经4 μmol/L CA16-L处理;泳道6:经8 μmol/L CA16-L处理;泳道7:经16 μmol/L CA16-L处理;泳道8:经32 μmol/L CA16-L处理;泳道9:经64 μmol/LCA16-L处理;泳道10:经128 μmol/L CA16-L处理;泳道11:经32 μmol/L无抗菌活性的多肽CL16处理。
a-凝胶阻滞电泳图;b-多肽与DNA结合率分析
图11 细菌基因组DNA 绑定分析
Fig.11 Bacterial genomic DNA binding assay
2.11 DNA凝胶阻滞实验
基因组DNA因其磷酸骨架而带有强负电荷,可通过静电作用与带正电荷的多肽发生结合。已有研究表明,部分AMPs破坏细胞膜后可与遗传物质(如DNA和RNA)特异性结合,从而干扰细菌正常生理功能[22]。为探究CA16-L的抗菌机制,本研究采用凝胶阻滞实验检测了其与E.coli ATCC25922和S.aureus ATCC29213基因组DNA的结合能力。结果如图11所示,CA16-L能够通过静电作用与基因组DNA结合,且结合程度随多肽浓度升高而增强,表现出明显的剂量依赖性。当CA16-L浓度达到32 μmol/L时,可完全抑制DNA在凝胶中的迁移。无抗菌活性的多肽CL16(阳性对照)同样可通过静电作用与DNA结合,该现象主要归因于其阳离子特性,而与膜的穿透或破坏能力无关。此种以膜损伤为主、DNA结合为辅助的双重抗菌机制,不仅有助于CA16-L发挥高效抗菌活性,也可降低细菌耐药性的发展风险[23]。
2.12 杂合抗菌肽在猪肉冷藏保鲜中的应用
本研究针对肉类加工与贮藏过程中S.aureus ATCC29213污染问题展开研究。通过对比商业抗菌肽乳酸链球菌肽,系统评价了新型抗菌肽CA16-L在4 ℃冷藏条件下对污染猪肉的保鲜效果。结果如图12所示,经过5 d贮藏后,CA16-L处理组与乳酸链球菌肽处理组的菌落总数较对照组均显著降低。然而,商业肽类防腐剂乳酸链球菌肽仅对革兰氏阳性菌有效(图3),并且在碱性环境下抗菌活性会显著降低[24-25]。相比之下,广谱、高效、pH稳定性良好的新型肽类防腐剂CA16-L为食品安全保障和肉制品货架期延长提供了新的解决方案,具有重要的实际应用价值。
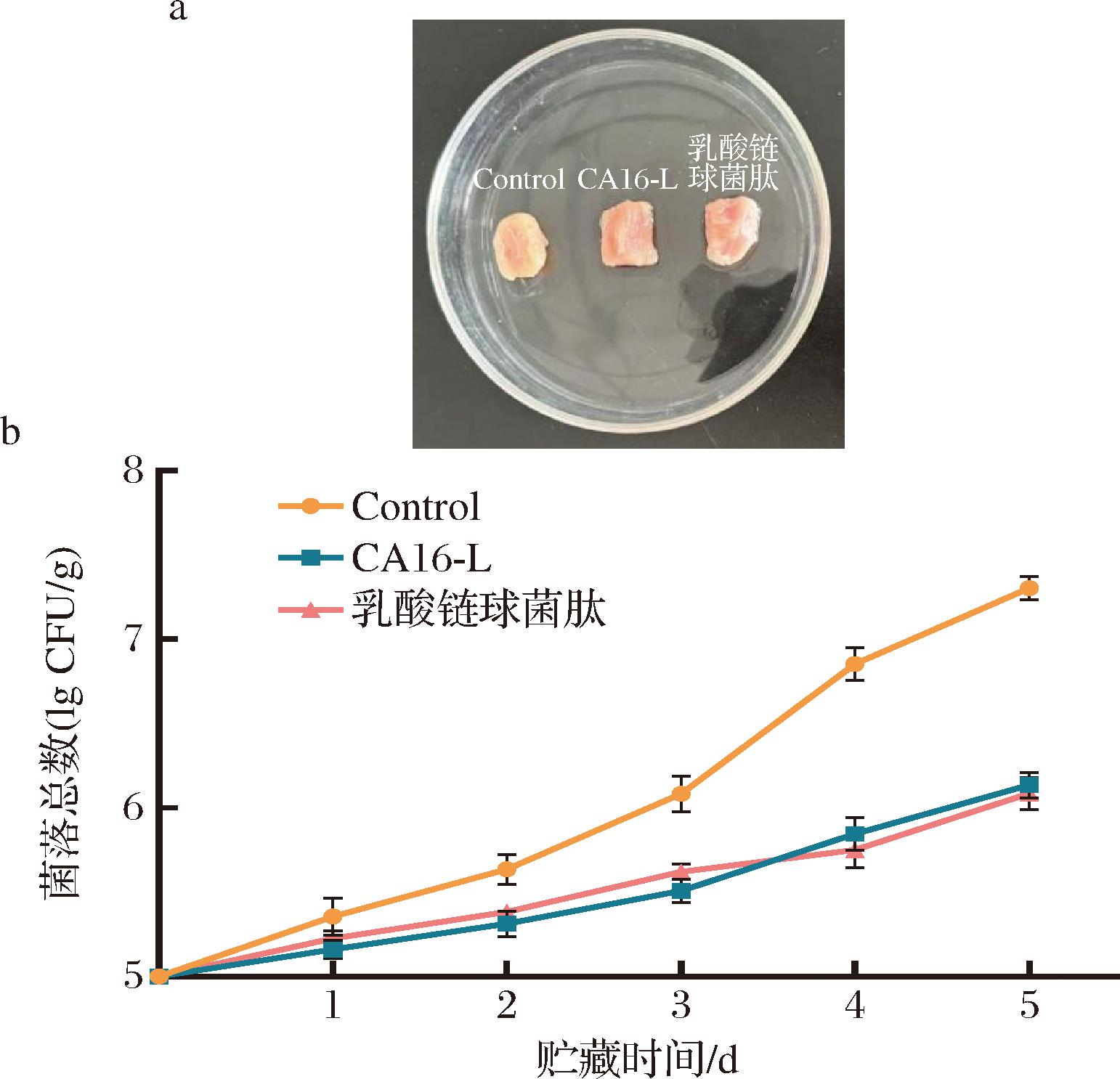
a-经CA16-L和乳酸链球菌肽处理5 d后的猪肉样品表观变化;b-CA16-L和乳酸链球菌肽对猪肉中S.aureus ATCC29213的 5 d抗菌效果
图12 CA16-L与Nisin对猪肉的保鲜效果
Fig.12 Preservation effects of CA16-L and Nisin on pork
3 结论
本研究基于生物信息学工具的分析结果,将天然抗菌肽Cecropin A(1-8)与Aurein 1.2(6-13)进行杂合,并通过氨基酸替换优化,成功构建了新型杂合抗菌肽CA16-L。随后系统评估了CA16-L的抗菌效果、生物相容性及稳定性,并利用荧光探针技术和扫描电子显微镜深入探究其抗菌机制。为进一步验证其实际应用价值,本研究还建立了鲜猪肉保鲜模型以考察其防腐性能。研究发现,CA16-L不仅保留了母体肽的关键功能域特征,更展现出广谱、高效的抗菌活性(GMall=4.32 μmol/L)和良好的生物安全性(SIall=59.26)。此外,该肽在不同盐离子环境、宽温度范围以及极端pH条件下均能维持稳定的抗菌活性,表现出良好的环境耐受性。抗菌机制研究表明,CA16-L首先通过静电作用特异性的识别细菌膜表面带负电的磷脂分子,继而引发膜结构破坏、通透性增加,随后穿透受损的细胞膜并与细菌基因组DNA结合,最终导致胞内物质泄漏和细菌死亡。此种协同作用机制在保证其抗菌能力的同时,有效规避传统抗生素的耐药性问题。在猪肉保鲜应用研究中,CA16-L表现出与商业化防腐剂乳酸链球菌肽相当的保鲜效果,能有效抑制细菌增殖并延缓食品腐败。本研究不仅为食品工业领域提供了广谱、高效、低毒、环境耐受性良好的新型AMPs候选分子,其设计策略也为功能性食品添加剂的开发提供了重要理论依据。
[1] HEYMICH M L, FRIEDLEIN U, TROLLMANN M, et al.Generation of antimicrobial peptides Leg1 and Leg2 from chickpea storage protein, active against food spoilage bacteria and foodborne pathogens[J].Food Chemistry, 2021, 347:128917.
[2] YANG S, LI J, AWEYA J J, et al.Antimicrobial mechanism of Larimichthys crocea whey acidic protein-derived peptide (LCWAP) against Staphylococcus aureus and its application in milk[J].International Journal of Food Microbiology, 2020, 335:108891.
[3] LENNERZ B S, VAFAI S B, DELANEY N F, et al.Effects of sodium benzoate, a widely used food preservative, on glucose homeostasis and metabolic profiles in humans[J].Molecular Genetics and Metabolism, 2015, 114(1):73-79.
[4] EL-SABER BATIHA G, HUSSEIN D E, ALGAMMAL A M, et al.Application of natural antimicrobials in food preservation:recent views[J].Food Control, 2021, 126:108066.
[5] 苏琰, 李融.抗菌肽的食品保鲜应用及生物合成研究进展[J].食品与机械, 2024, 40(7):208-215.SU Y, LI R. Advance on biosynthesis of antibacterial peptides and its application in food preservation[J]. Food &Machinery, 2024, 40(7):208-215.
[6] 李艳梅. 蜡样芽孢杆菌新型抗菌剂的设计、抗菌活性及机制研究[D].广州:华南理工大学, 2024.LI Y M.Design, antibacterial activity, and mechanism sstudy of a novel antibacterial agent from Bacillus cereus[D].Guangzhou: South China University of Technology, 2024.
[7] 徐浩然, 毕重朋, 王家俊, 等.人工设计及深度学习在抗菌肽改造策略上的研究进展[J].食品与发酵工业, 2025, 51(13):362-368;407. XU H R, BI C P, WANG J J, et al.Advances in artificial design and deep learning for antimicrobial peptide modification strategies[J].Food and Fermentation Industries, 2025, 51(13):362-368;407.
[8] 杨红艳. 天然抗菌肽Cecropin衍生物的设计及抗菌活性研究[D].郑州:河南工业大学, 2024.YANG H Y.Design and antibacterial activity study of Cecropin derivatives as natural antimicrobial peptides[D].Zhengzhou:Henan Technology University, 2024.
[9] YANG Y, WU D, WANG C X, et al.Hybridization with insect Cecropin A(1-8) improve the stability and selectivity of naturally occurring peptides[J].International Journal of Molecular Sciences, 2020, 21(4):1470.
[10] RAMEZANZADEH M, SAEEDI N, MESBAHFAR E, et al.Design and characterization of new antimicrobial peptides derived from aurein 1.2 with enhanced antibacterial activity[J].Biochimie, 2021, 181:42-51.
[11] VERMA D P, TRIPATHI A K, THAKUR A K.Innovative strategies and methodologies in antimicrobial peptide design[J].Journal of Functional Biomaterials, 2024,15(11):320.
[12] WANG J J, DOU X J, SONG J, et al.Antimicrobial peptides:Promising alternatives in the post feeding antibiotic era[J].Medicinal Research Reviews, 2019, 39(3):831-859.
[13] 李毓雯, 胡明阳, 赵璐, 等.抗菌肽MALK杀菌活性、生物相容性与作用机制[J].东北农业大学学报, 2025, 56(2):89-99.LI Y W, HU M Y, ZHAO L, et al.Investigation of bactericidal activity, biocompatibility and mechanism of action for antimicrobial peptide MALK[J].Journal of Northeast Agricultural University, 2025, 56(2):89-99.
[14] WANG J J, SONG J, YANG Z Y, et al.Antimicrobial peptides with high proteolytic resistance for combating gram-negative bacteria[J].Journal of Medicinal Chemistry, 2019, 62(5):2286-2304.
[15] MA Z, WEI D D, YAN P, et al.Characterization of cell selectivity, physiological stability and endotoxin neutralization capabilities of α-helix-based peptide amphiphiles[J].Biomaterials, 2015, 52:517-530.
[16] TAN P, FU H Y, MA X.Design, optimization, and nanotechnology of antimicrobial peptides:From exploration to applications[J].Nano Today, 2021, 39:101229.
[17] DESLOUCHES B, PHADKE S M, LAZAREVIC V, et al.De novo generation of cationic antimicrobial peptides:Influence of length and tryptophan substitution on antimicrobial activity[J].Antimicrobial Agents and Chemotherapy, 2005, 49(1):316-322.
[18] HUANG J F, HAO D M, CHEN Y, et al.Inhibitory effects and mechanisms of physiological conditions on the activity of enantiomeric forms of an α-helical antibacterial peptide against bacteria[J].Peptides, 2011, 32(7):1488-1495.
[19] JIA B Y, WANG Y M, ZHANG Y, et al.High cell selectivity and bactericidal mechanism of symmetric peptides centered on d-Pro-Gly pairs[J].International Journal of Molecular Sciences, 2020, 21(3):1140.
[20] FISHER R A, GOLLAN B, HELAINE S.Persistent bacterial infections and persister cells[J].Nature Reviews Microbiology, 2017, 15(8):453-464.
[21] WANG Z H, LI Q K, LI J Z, et al.The Trp-rich antimicrobial amphiphiles with intramolecular aromatic interactions for the treatment of bacterial infection[J].Frontiers in Microbiology, 2021, 12:733441.
[22] LIANG X L, YAN J X, LU Y W, et al.The antimicrobial peptide melectin shows both antimicrobial and antitumor activity via membrane interference and DNA binding[J].Drug Design, Development and Therapy, 2021, 15, 1261-1273.
[23] ZHANG R, XU L J, DONG C M.Antimicrobial peptides:An overview of their structure, function and mechanism of action[J].Protein &Peptide Letters, 2022, 29(8):641-650.
[24] THOMAS L V, WIMPENNY J W.Investigation of the effect of combined variations in temperature, pH, and NaCl concentration on nisin inhibition of Listeria monocytogenes and Staphylococcus aureus[J].Applied and Environmental Microbiology, 1996, 62(6):2006-2012.
[25] KHAN A, VU K D, RIEDL B, et al.Optimization of the antimicrobial activity of nisin, Na-EDTA and pH against gram-negative and gram-positive bacteria[J].LWT-Food Science and Technology, 2015, 61(1):124-129.