金黄色葡萄球菌(Staphylococcus aureus)是一种常见的人畜共患病原菌,可引起动物细菌性饲料中毒、牛羊乳腺炎感染及败血症等严重的疾病,其耐药菌株(如耐甲氧西林金黄色葡萄球菌)的全球性扩散已成为公共卫生领域的重大挑战[1]。由于细菌耐药性的增强导致传统抗生素的治疗效果逐渐减弱,因此寻找安全有效的替抗产品迫在眉睫。益生菌作为一种新型抑菌制剂,凭借产品种类丰富、成本低、无毒副作用、安全无污染等显著优势[2-5],在畜牧养殖领域逐步替代传统抗生素应用。近年来,因其通过分泌细菌素、短链脂肪酸酸等抗菌活性物质,并协同调节宿主肠道免疫等多重机制抑制病原菌的特性备受关注[6-8]。
沙克乳酸杆菌(Latilactobacillus sakei)具有乳酸菌特有的益生特性和抗菌潜力。已有研究表明从海洋鱼的肠道内容物[5]、香肠[9]和泡菜[10]中获得的L.sakei 分离菌株均对金黄色葡萄球菌展现出高效的抗菌作用。本课题组前期从藏羊胃肠道分离获得的L.sakei分离株具有广谱的抑菌性,且对极端环境具有较强的耐受性、生长速度和产酸能力优良,是制备藏羊源微生态制剂的良好菌株[11]。
目前关于L.sakei抑制金黄色葡萄球菌的机制尚未完全明确,为进一步探究L.sakei对病原菌的抑菌机理,本研究利用转录组学分析金黄色葡萄球菌在无细胞上清液(cell-free supernatant, CFS)共培养处理12 h后的差异表达基因(differentially expressed gene, DEG),结合代谢组学解析其代谢产物变化,挖掘关键抑菌靶点及相关代谢通路,从而为揭示L.sakei CFS对金黄色葡萄球菌的抑菌机理提供多维证据,同时也可为基于益生菌的新型抑菌剂开发及耐药性防控策略提供理论数据。
1 材料与方法
1.1 材料与试剂
藏羊源L.sakei、金黄色葡萄球菌均由青海大学农牧学院动物医学实验中心保存。
MRS肉汤培养基、普通肉汤培养基,青岛海博生物技术有限公司;PBS缓冲液,北京索莱宝科技有限公司;细菌总RNA提取试剂盒、琼脂糖,TIANGEN BIOTECH (BEIJING)公司;反转录试剂盒、TB Green® Premix Ex TaqTM (Tli RNaseH Plus),TaKaRa Bio公司;甲醇,Thermo Fisher Scientific公司。
1.2 仪器与设备
THZ-100B恒温摇床,上海一恒科学仪器有限公司;3-18K低温高速离心机,湖南凯达科学技术有限公司;0.22 μm滤膜,Sigma公司;LightCycler® 480 实时荧光定量PCR仪,Roche公司;微量分光光度计,GENE公司。
1.3 实验方法
1.3.1 L.sakei CFS制备
以1%(体积分数)的比例将L.sakei接入100 mL新鲜MRS肉汤培养基,34 ℃、170 r/min恒温摇床振荡培养24 h。发酵液于4 ℃、12 000 r/min离心10 min,收集上清液,用0.22 μm滤膜过滤,除去菌体,将得到的CFS分装,-80 ℃冰箱保存备用,用于后续实验。
1.3.2 样品制备
将活化的金黄色葡萄球菌液按1%(体积分数)接种到100 mL普通肉汤培养基,于37 ℃、170 r/min恒温摇床培养至对数生长期,借助前期实验确定CFS对金黄色葡萄球菌最小抑菌体积(minimum inhibitory volume, MIV)为40%(体积分数)的实验结果。此时处理组加入CFS并使其终浓度为1/2 MIV,对照组添加等量的新鲜MRS肉汤培养基。于37 ℃、170 r/min 恒温摇床继续共培养12 h,4 ℃、12 000 r/min离心10 min 弃上清液,收集菌体沉淀。1×PBS清洗3次后,吸干残留溶液后,迅速转移至-80 ℃冰箱保存,备用。
1.3.3 转录组学分析
将制备好的样品送生物公司进行转录组学测序。以Padj≤0.05,|log2 Fold Change|>0.0为筛选DEGs标准,利用DESeq软件筛选DEGs。将得到的DEGs注释到GO(Gene Ontology)、KEGG(Kyoto Encyclopedia of Genes and Genomes)数据库中,获得DEGs的GO功能注释和代谢通路富集分析。
1.3.3.1 提取金黄色葡萄球菌总RNA及质量检测
用试剂盒提取细菌总RNA,使用1%(质量分数)琼脂糖凝胶电泳和微量分光光度计检测RNA浓度和纯度以及完整性,用反转录试剂盒将RNA反转为cDNA,于-80 ℃保存cDNA样品。
1.3.3.2 实时荧光定量PCR(real time-qPCR,RT-qPCR)验证
选取15个DEGs进行RT-qPCR验证转录组学数据的可靠性。根据转录组学得到的基因序列设计荧光定量引物,引物序列如表1所示。PCR反应体系(25 μL):TB Green Premix Ex TaqⅡ 12.5 μL,上、下游引物各1 μL(终浓度为10 μmol/L),cDNA溶液2 μL,RNase free ddH2O 8.5 μL。PCR反应条件:预变性95 ℃ 30 s;循环反应95 ℃ 5 s,55 ℃ 30 s,72 ℃ 10 s,40个循环;以ropA为内参基因,采用2-ΔΔCT法计算相对表达量。
表1 RT-PCR引物序列
Table 1 Sequences of RT-PCR primers

基因/基因ID引物序列 (5′→3′)产物长度/bprpoAF-GCACCAAAGAAGGCGTTCAGR-ATATCGGCTGCAGTCACAGG125>N1060_RS03040F-GCAACGGCGCTTATATGTATCR-CCATTTCTTACGATGCTCTTCTC134>N1060_RS05220F-CCTTTGTTACTTCAGGTGGTAGAR-CGCAATGTCATGACGATAGAATAAA134>N1060_RS06560F-GACGGTGAAGCACCTGATATTR-TTTCGGCAATTGTGATCCTTTAG114>N1060_RS10130F-GCTTCAGGTCAAGCACGTAATAR-TTCGATACACCACCGCAAAG146>N1060_RS10135F-GACACTAAGAGACGGTGAACAAR-GCAGGAAATCCAGCTTCAATAAC117>N1060_RS05075F-TGGCGATGATACAAGTCACAAR-GATGACGTTTGCATGAGGATATG147>N1060_RS10145F-CTATCGAAGGTGGTGCCAAATAR-ATCGCGTCGTCATCAGAATATAG139>N1060_RS00720F-GTCATAAAGTACGCCCGGATAAR-CAACGGTTACTGAACCAATGC123>N1060_RS00650F-GATGCGTTAGTTGAAGCGTTAGR-ACCTGAATAGTGAACCGTCATAG135>N1060_RS11710F-AAGAAGATGGTACACTAGCATCAAR-ATTGTTCAGGCCAAGTGATAGT150>N1060_RS03705F-CACCTGTTAAATATGCGAGTAGTGR-CTTTACCTTCTTGCAGTCGTTG138>N1060_RS10575F-AGCAAGCCAATATGTAGACGAATTAR-GAGTAACCTTTCGCAGCTTCTT120>N1060_RS03550F-TTGACTATCGTCCTGATGTATTAGAR-GTTGCCCAGTAATTGGACATAAT114>N1060_RS03770F-GGTTCTGGTCAACAATGGTATTCR-CGTTCAGGTATAGGTGCAGTT122>N1060_RS10335F-CTCCCGAAGAAGCTGAAGAATR-AGCTACAGGGTCAAATACAATAGG149>N1060_RS03570F-CTCAAATGTGGGTTGAAACAGAAR-GCCTGTTAAACCAGCTAATGC113>N1060_RS08805F-CTGGCATCGTTGAAGAAATAGGR-AACACTGATGGAATCACCAATATG122>N1060_RS00320F-TCACCAGGTACGGTGATACAR-GGGCAGCACCAGTCAATAA118
1.3.4 非靶向代谢组学分析
样本制备同1.3节。样本置于EP管中,加入300 μL的80%(体积分数)甲醇水溶液,放入液氮速冻5 min,冰上融化后涡旋30 s,超声6 min,5 000 r/min、4 ℃ 离心1 min,取上清液至新离心管中,冻干成干粉,按所取样本体积加入相应的10%(体积分数)甲醇溶液溶解,每个样品3个生物学重复。送生物公司进行LC-MS/MS分析。
1.4 代谢物定性定量分析及差异代谢物注释
用XCMS数据处理软件,对样本中检测到的色谱峰进行积分,其中每个特征峰的峰面积表示一个代谢物的相对定量值,使用总峰面积对定量结果进行标准化,最后得到代谢物的定量结果。
2 结果与分析
2.1 转录组学分析
2.1.1 DEGs分析
与对照组相比,CFS处理组共检测到1 109个DEGs,其中502个上调表达基因,607个下调表达基因(图1)。
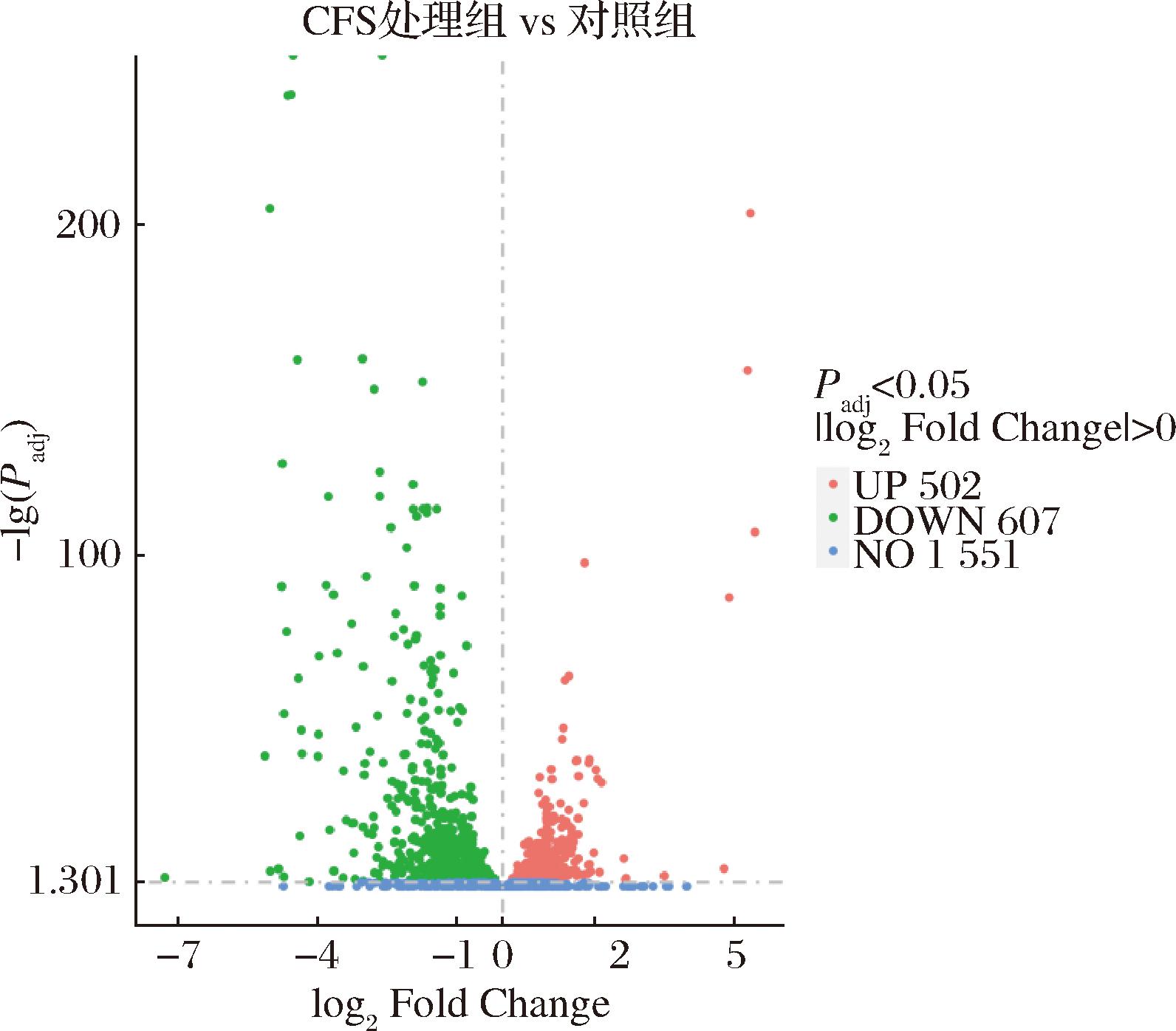
图1 差异表达基因火山图
Fig.1 Volcano map of differentially expressed genes
注:Padj为校正后P值;log2 Fold Change为表达倍数变化;UP表示基因上调表达;DOWN表示基因下调表达;NO表示无变化(图5同)。
2.1.2 转录组测序数据RT-qPCR验证
随机选取15个DEGs(8个上调基因和7个下调基因)进行RT-qPCR,结果表明所选基因mRNA表达趋势与RNA-seq结果一致(图2),说明本批样本转录组学测序数据可靠。
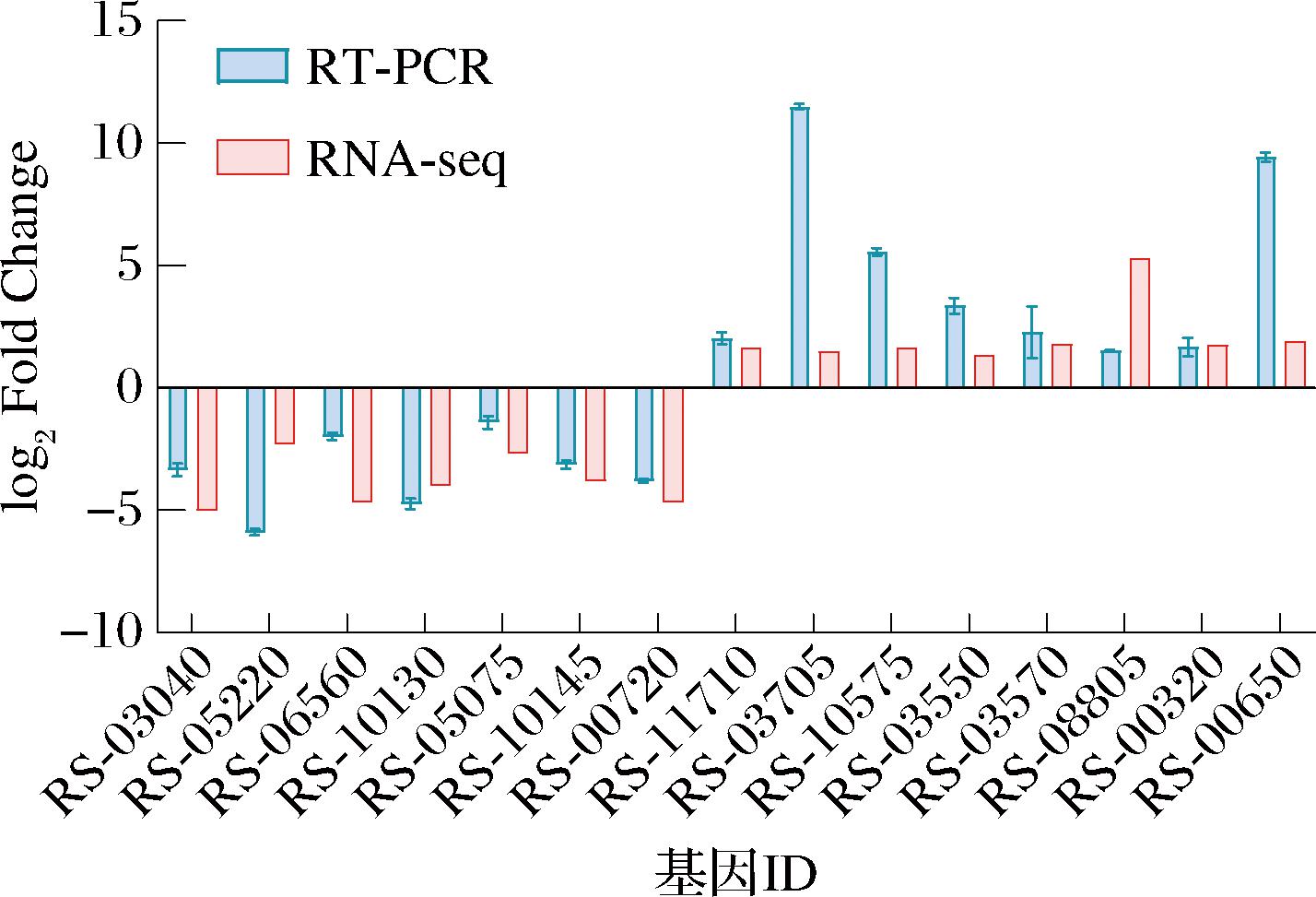
图2 样本转录组测序数据与RT-PCR结果比对
Fig.2 Comparison of transcriptome sequencing data with RT-PCR results
2.1.3 GO功能富集分析
对DEGs进行GO功能富集分析,结果显示有360个DEGs注释到GO功能富集上(P<0.05),包括生物过程(biological process, BP)、细胞组成(cellular component, CC)和分子功能(molecular function, MF)3个部分。其中BP部分包含214个DEGs,CC部分包含23个DEGs,MF部分包含123个DEGs。由图3可知,DEGs主要引起MF生物进程中离子结合、核苷酸结合、小分子结合、有机环化合物和杂环化合物等代谢过程,引起BP生物过程中细胞代谢、大分子代谢、生物合成、氧化还原过程的改变。由此推测,L. sakei CFS可能对金黄色葡萄球菌生长、蛋白表达等生物过程和细胞结构组成发挥作用。
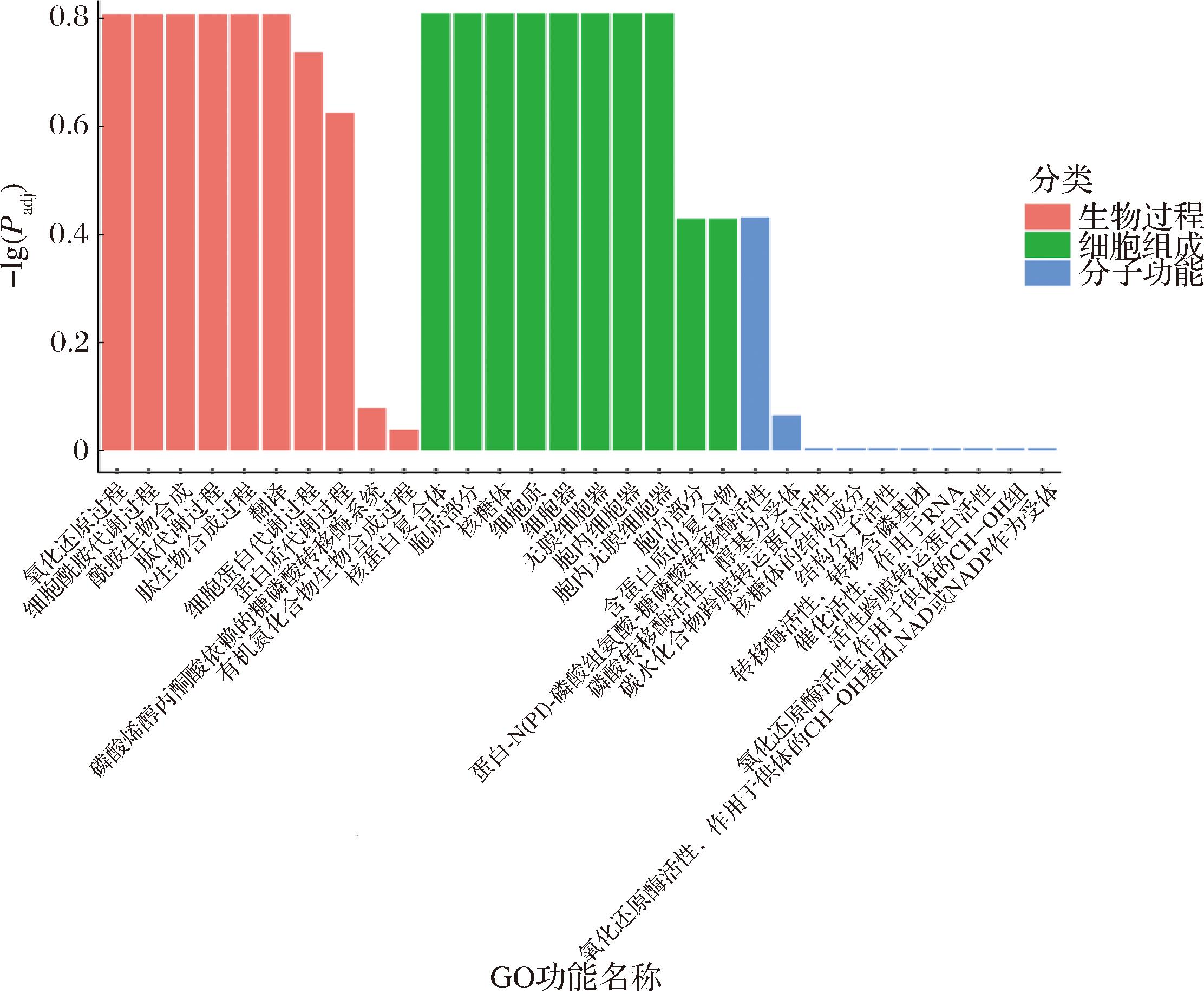
图3 各分类前10个组间差异表达基因GO功能富集
Fig.3 Functional enrichment of differentially expressed genes GO among the top 10 groups in each classification
2.1.4 KEGG通路富集分析
CFS作用后金黄色葡萄球菌有509个DEGs注释到74条KEGG代谢通路(图4)。主要涉及氨基酸代谢、糖代谢、脂代谢以及碳代谢等能量代谢通路以及双组分信号系统和群体感应系统的变化。KEGG注释结果显示CFS作用后氨基酸合成和代谢相关途径有32个基因表达显著上调,102个基因表达显著下调,其中编码支链氨基酸合成途径重要催化酶的leuB、leuC、ilvC、lysA、lysM表达下调,表明CFS抑制氨基酸合成的相关生物过程,其中可能涉及功能蛋白的表达抑制。糖合成和代谢相关途径有88个基因表达显著上调,101个基因表达显著下调,其中编码三羧酸循环的关键酶(α-酮戊二酸脱氢酶复合物)的sucA、sucB和lpdA以及编码三羧酸循环的关键限速酶的pckA均被显著下调,表明CFS可能通过抑制糖代谢过程中的关键酶活性,从而抑制细菌能量供应,最终抑制金黄色葡萄球菌的生长发育。CFS处理后氧化磷酸化等能量代谢相关通路有41个基因表达显著上调,74个基因表达显著下调,其中与氧化磷酸化途径相关的qoxA、qoxB、qoxC、qoxD、shdA、shdB、qtpB表达显著下调,揭示CFS处理后细菌产能受到一定程度的阻滞,从而影响了细菌正常的生命活动。脂质代谢有12个基因显著上调,19个基因显著下调,表明CFS处理后抑制了金黄色葡萄球菌脂类相关的代谢通路。双组分信号系统有14个基因表达显著上调,26个基因表达显著下调,群体感应有5个基因表达显著上调,18个基因表达显著下调,揭示CFS处理后金黄色葡萄球菌感知外界刺激的能力受到抑制。由此推测,CFS能下调金黄色葡萄球菌氨基酸、糖类、脂类以及能量代谢途径和群体感应系统等途径,阻抑金黄色葡萄球菌能量供应,降低对外界环境刺激的感知力,从而发挥抑菌作用。
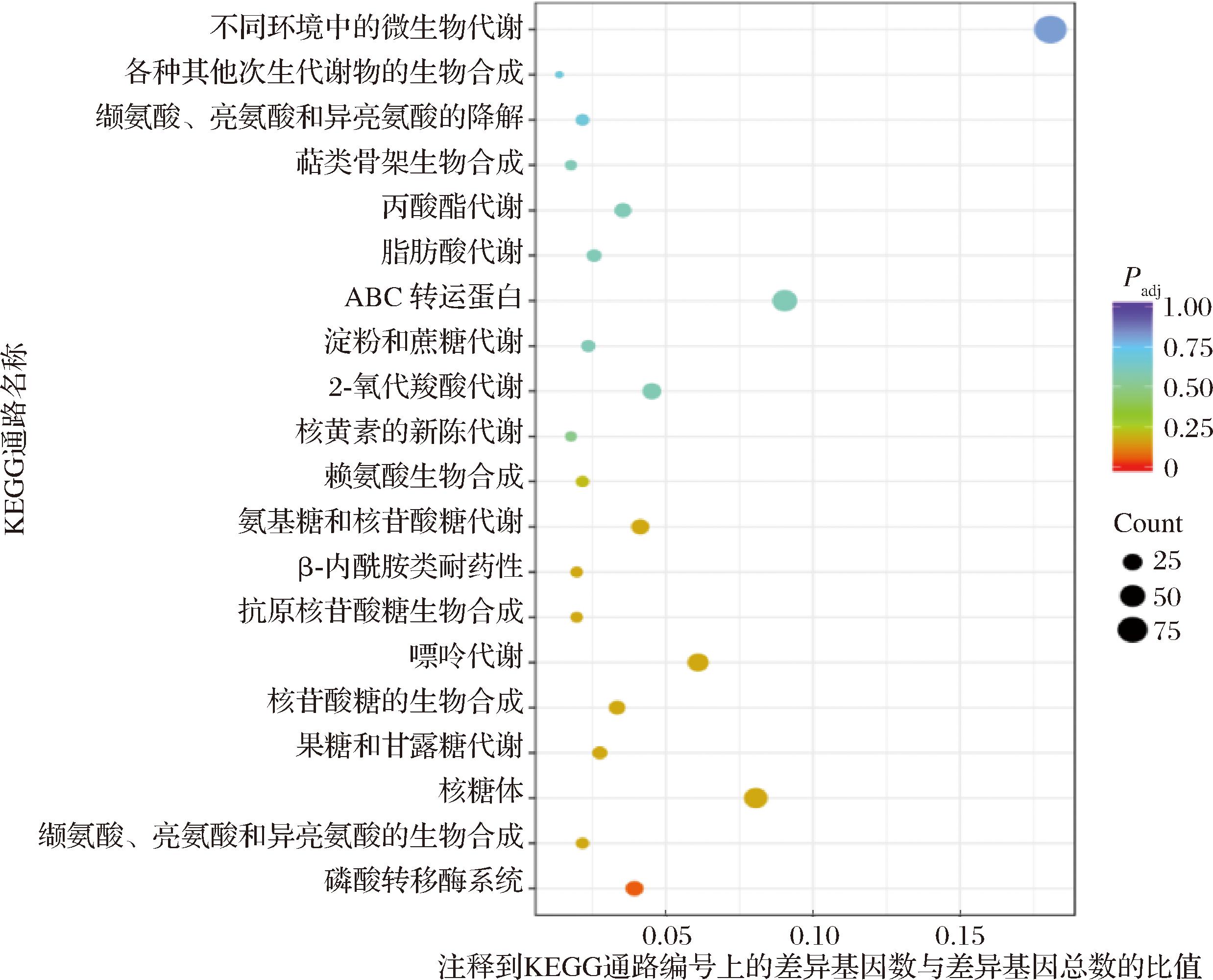
图4 前20个组间差异表达基因KEGG通路富集分析
Fig.4 KEGG pathway enrichment analysis of differentially expressed genes among the top 20 groups
2.2 非靶向代谢组学分析
2.2.1 差异代谢物分析
以P≤0.05,|log2 Fold Change|≥0.58,变量投影重要性(variable importance in projection, VIP)≥1为筛选差异代谢物阈值。与对照组相比,CFS处理组共筛选出1 685种差异代谢物,其中704种差异代谢物显著上调,981种差异代谢物显著下调(图5)。通过KEGG富集通路分析发现所有差异代谢物在39个代谢途径富集(图6)(P<0.05),主要涉及有机酸及其衍生物代谢合成、辅助因子和维生素代谢合成、核苷酸代谢、能量代谢、碳水化合物代谢等次生代谢物代谢途径。
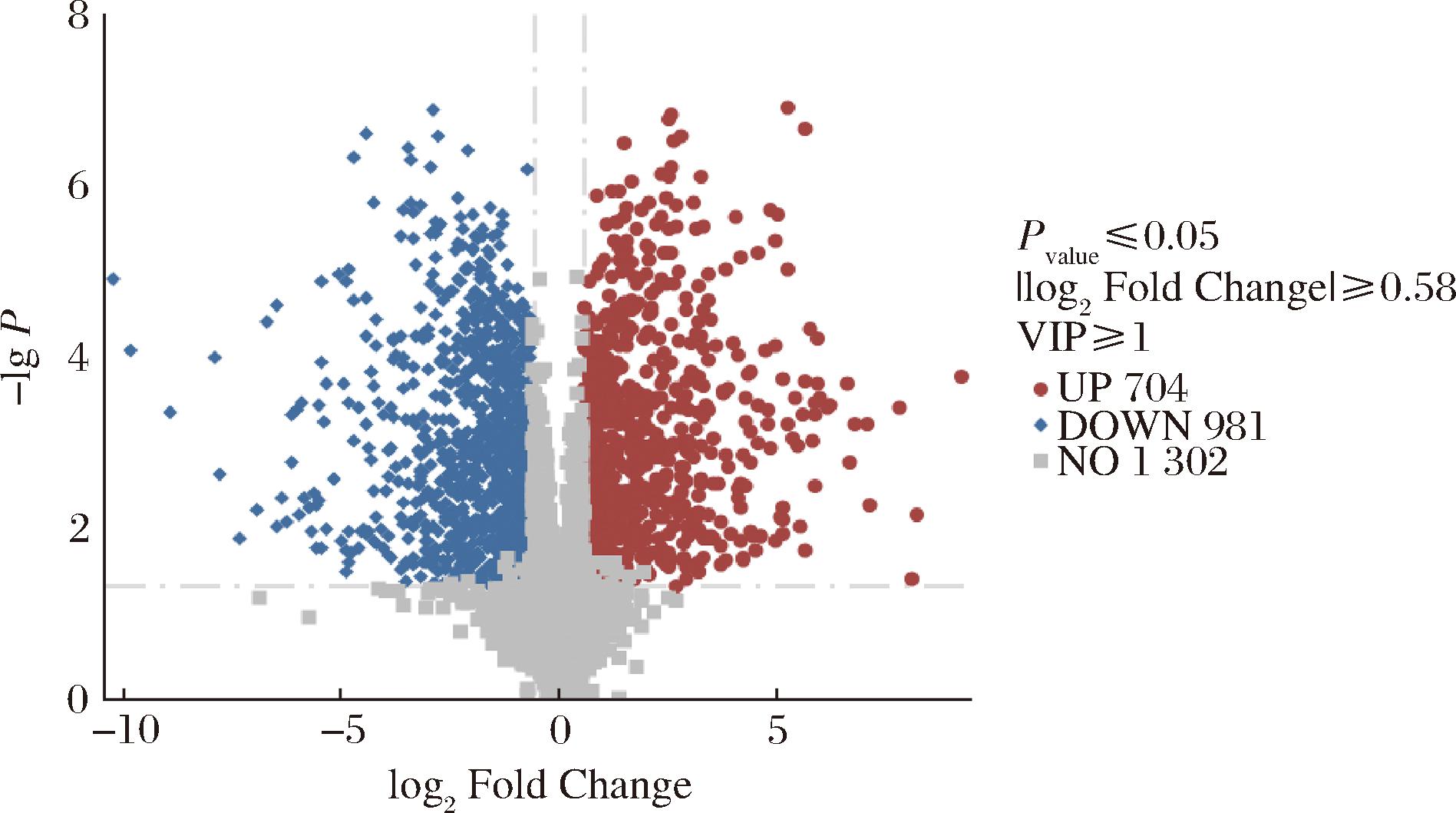
图5 组间差异代谢物火山图
Fig.5 Volcano map of differential metabolites between groups
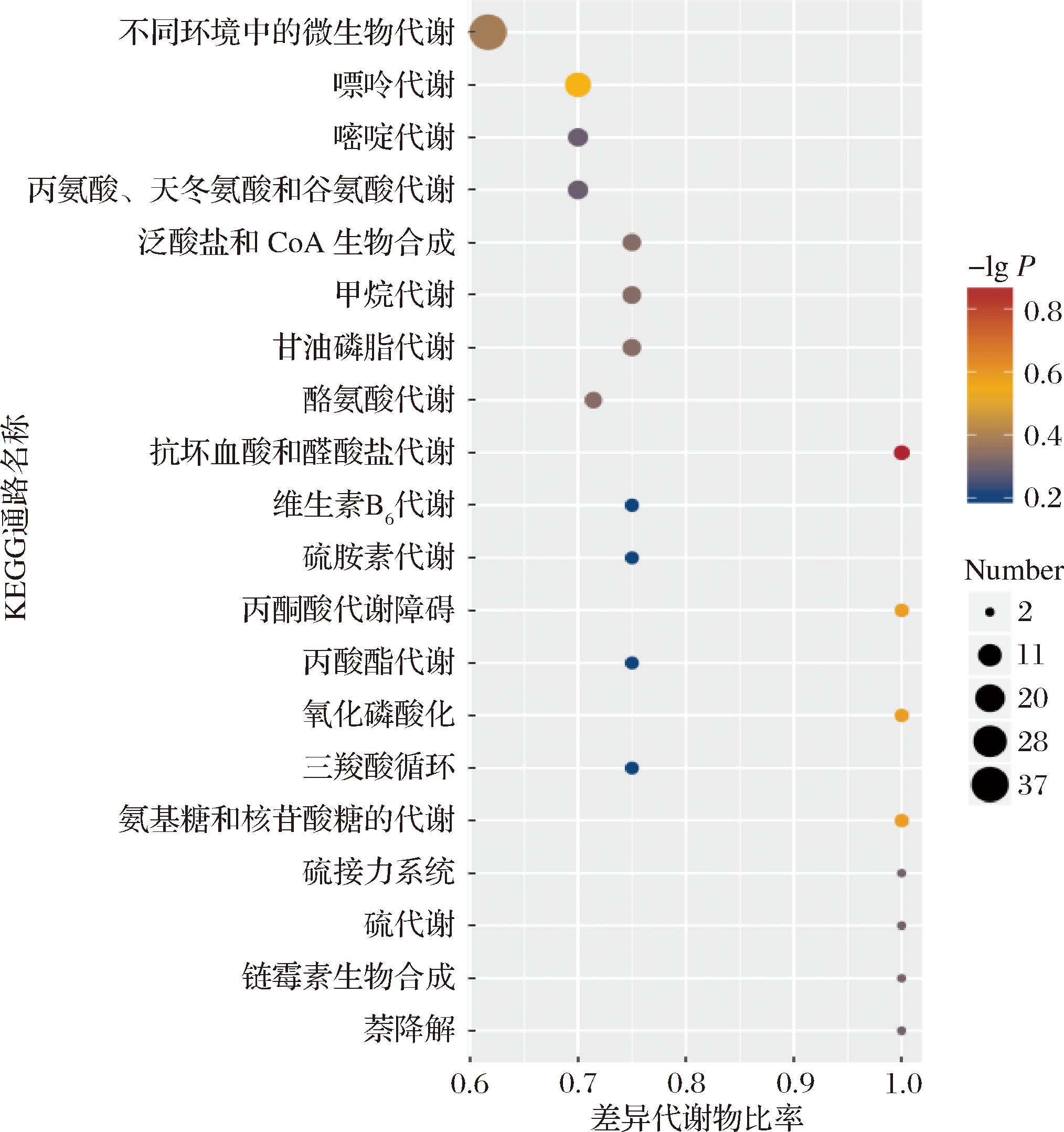
图6 差异代谢物前20 KEGG富集通路富集图
Fig.6 Enrichment map of the top 20 KEGG pathways enrichment
2.2.2 KEGG分类分析
对差异代谢物进行KEGG分类分析发现,代谢物的差异主要由53种有机酸及其衍生物17.73%(氨基酸、多肽和类似物;酮酸及其衍生物;三羧酸及其衍生物等);22种辅助因子和维生素的代谢物(吡啶及其衍生物;嘧啶和嘧啶衍生物等)7.36%;16种脂类和类脂分子5.35%(4.01%脂肪酸及其衍生物;1.34%萜类和多酮类);21种核苷酸和类似物7.02%(嘧啶核苷;嘌呤核苷);16种有机氧化合物5.35%(羰基化合物;醇和多元醇等)等组成(图7)。此外,全局概览图代谢物数量最多,说明差异代谢物广泛参与细菌多个相互联系基础代谢途径。
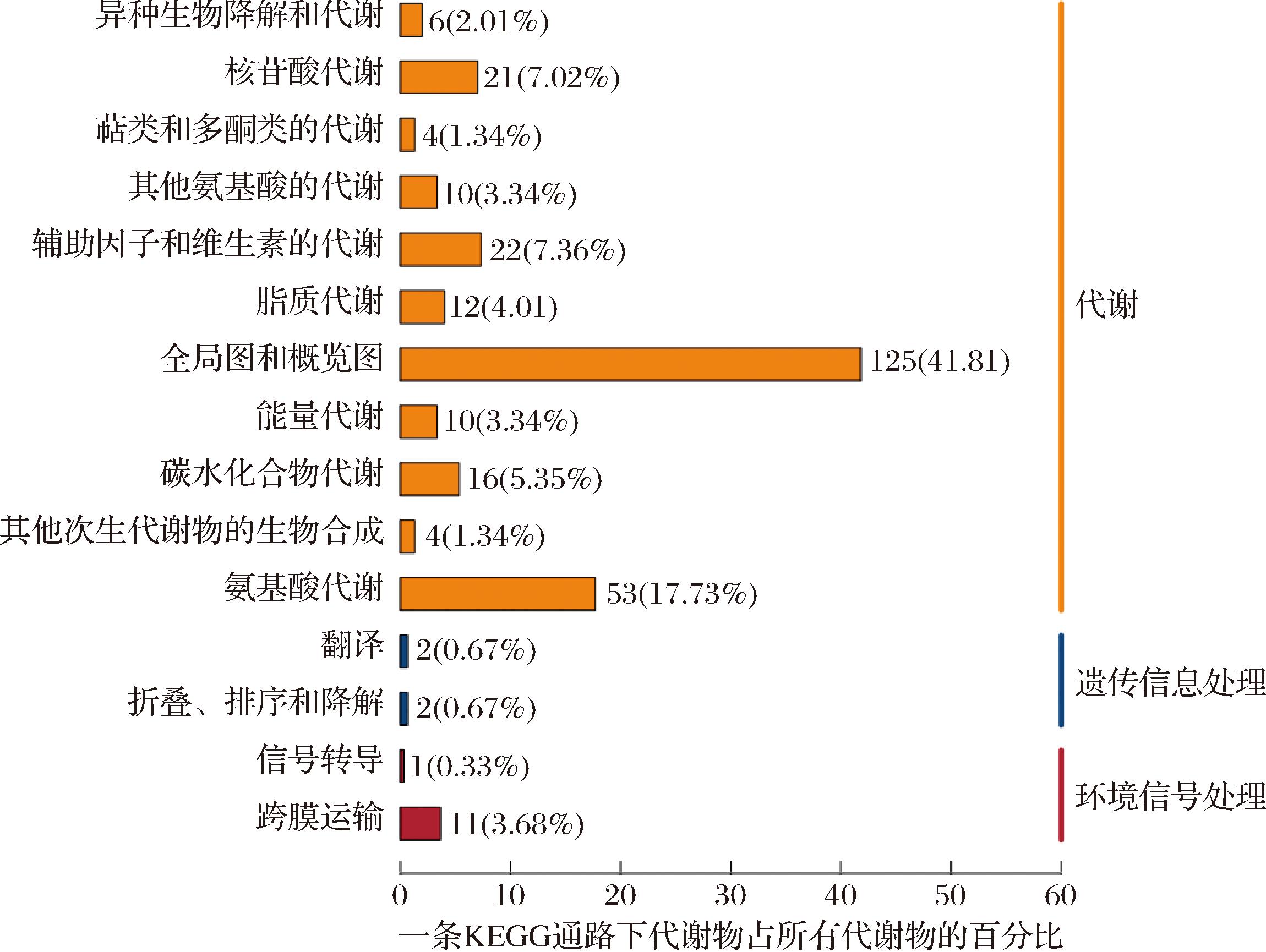
图7 组间代谢物KEGG富集分类
Fig.7 KEGG enrichment classification of metabolites among groups
注:图中横坐标表示KEGG某一条通路下注释到的代谢物数量占所有注释到的代谢物数量的百分比;右侧纵坐标为KEGG Pathway一级分类, 左侧纵坐标为KEGG Pathway二级分类。
2.3 转录组学和代谢组学联合分析
转录组学和代谢组学联合分析表明(图8),DEGs和差异代谢物在氧化磷酸化生物过程、磷酸转移酶系统(phosphotransferase system,PTS)、三羧酸循环等过程共富集,以上代谢途径是生物体内能量产生的重要来源。DEGs(Arg、Arc)和差异代谢物(N-alpha-乙酰基-L-鸟氨酸)在精氨酸生物合成中共富集,精氨酸生物合成可以通过三羧酸循环调节与糖酵解活性相关的生物过程。DEGs(sph、tagD、pgsA)和差异代谢物(O-磷酸乙醇胺、甘油磷酰胆碱)在甘油磷酸酯代谢通路发生共富集,甘油磷酸脂代谢涉及合成和降解一系列酶的催化反应,且O-磷酸乙醇可能通过细胞间信号转导影响细胞生长、分裂。CFS处理后金黄色葡萄菌甘油-3-磷酸胆碱代谢显著下调,进一步说明L.sakei CFS能破坏金黄色葡萄球菌的细胞结构从而导致金黄色葡萄球菌死亡。
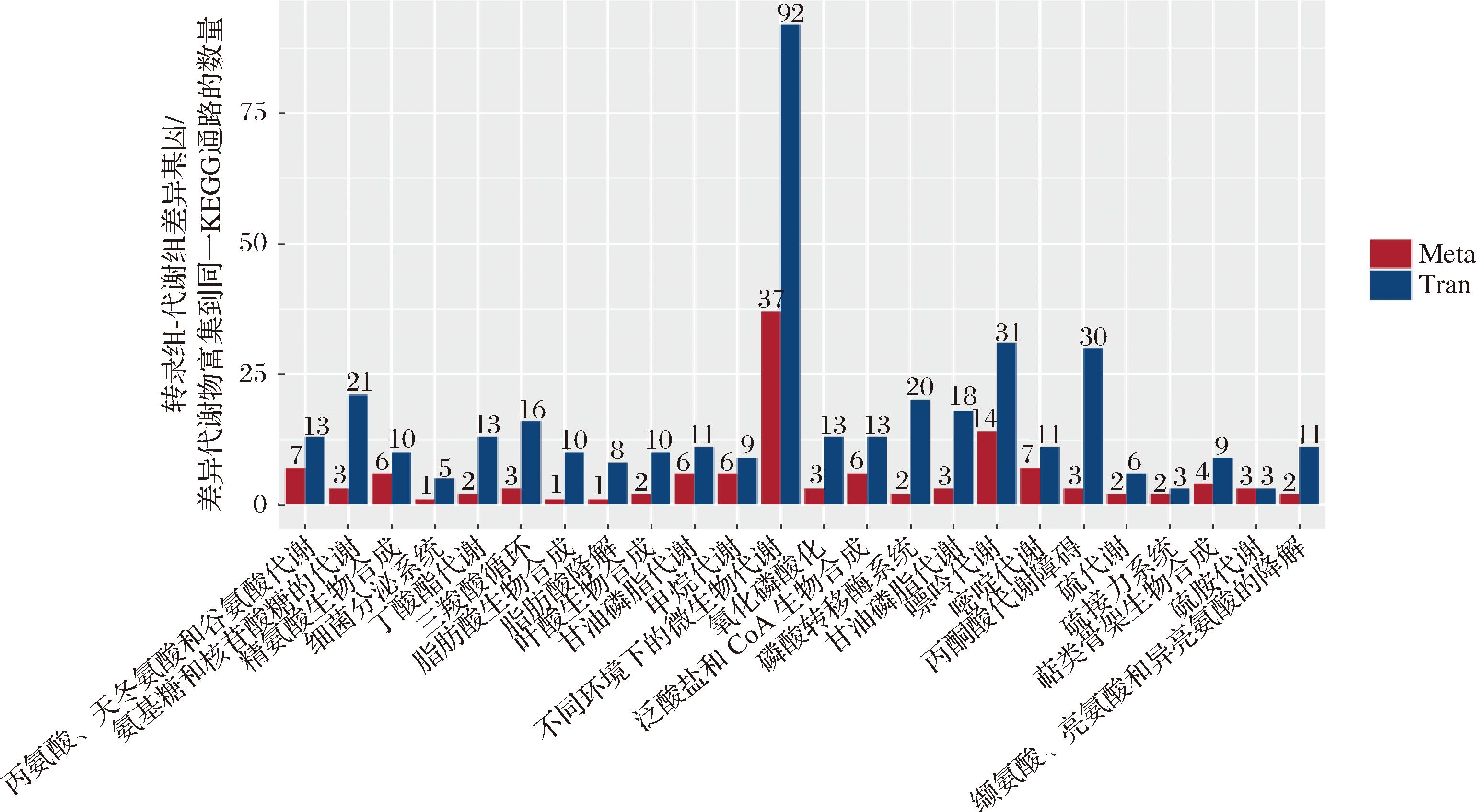
图8 DEGs和差异代谢物KEGG分布
Fig.8 KEGG distribution of differentially expressed genes and differentially metabolites
3 结论与讨论
本研究转录组和代谢组联合分析表明L.sakei CFS会影响金黄色葡萄球菌脂肪酸生物合成和降解、氨基酸代谢、ABC转运系统关键蛋白、细胞膜和细胞膜固有成分、氧化磷酸化等生化过程的基因的表达或代谢物产生。Fab基因家族是细菌脂肪酸生物合成的关键酶,FabF编码β-酮酰基-(acyl carrier protein, ACP)合成酶催化丙二酰-酰基载体蛋白ACP与酰基-ACP的缩合反应,是脂肪酸从头合成途径碳链延长阶段的核心酶[12]。FabI编码烯酰-ACP还原酶催化反式-2,3-烯酰基-ACP还原为饱和酰基-ACP,完成一轮脂肪酸链的延长循环,是脂肪酸从头合成途径中最后一步还原反应的关键酶[13]。CFS可能下调了金黄色葡萄球菌的FabF、FabI的表达,导致脂代谢受阻,这可能是CFS抑制金黄色葡萄球菌生长的原因之一。氨基酸合成代谢不仅提供蛋白质合成的原料,还会参与调控能量代谢、细胞壁合成和应激反应。leuB、leuC、ilvC低表达可能会减少支链氨基酸(branched-chain amino acids,BCAA)的产生和积累,导致核糖体功能障碍,触发mRNA降解和生长停滞,且氨基酸的合成受CodY转录调控因子的精细调控[14],如赖氨酸合成基因lysA受转录调控因子CodY蛋白调控,该基因表达受到抑制时细菌生长减缓。另外,CodY通过感知支链氨基酸浓度抑制hla、agr、icaADBC等毒力基因表达,降低细菌致病性[15-16],表明金黄色葡萄球菌CFS可能通过下调BCAA的合成基因,从而减少BCAA积累,进而对金黄色葡萄球菌的细胞存活造成损害。此外,CFS抑制了赖氨酸编码基因lysA、lysM的表达,导致赖氨酸合成代谢紊乱。赖氨酸的合成中间产物L-2,3-二氨基庚二酸是细菌肽聚糖交联的关键组分,赖氨酸缺乏时直接导致肽聚糖结构缺陷,进而引发细菌细胞壁结构缺陷甚至导致细菌裂解。综上,CFS可能同时抑制金黄色葡萄球菌BCAA和赖氨酸代谢,实现对其抑菌作用。转录组测序结果还表明ABC转运系统相关基因(adcA、gmpC、cntA、opp3C、opp3B、opp1C、tagG、tagH等)均下调表达,这些基因编码Ni2+、Zn2+转运、肽摄取、磷壁酸合成相关蛋白以及对细菌细胞壁完整性相关[14,17-20],综上所述,CFS整体表现出抑制金黄色葡萄球菌的生长。另外,有研究表明乳酸杆菌CFS通过抑制金黄色葡萄球菌生物被膜相关的疏水性、运动性、eDNA和多糖细胞间黏附素等生理特性从而降低细菌致病性和耐药性[21]。因此,可以基于金黄色葡萄球菌生物被膜对L.sakei CFS的抑菌机理展开更为深入的研究。
本研究以藏羊源L.sakei CFS为抑菌剂,通过多组学分析其抑制金黄色葡萄球菌的潜在机理。结果表明CFS处理可显著调控金黄色葡萄球菌1 109个DEGs和1 685种差异代谢物表达。将DEGs和差异代谢物共同注释到KEGG、GO功能富集通路发现DEGs和差异代谢物富集到缬氨酸、亮氨酸和异亮氨酸的降解、精氨酸生物合成等24条重要生化途径,涉及氧化磷酸化、丙酮酸代谢障碍和脂肪酸代谢等基本生长代谢途径。说明L.sakei CFS通过降低金黄色葡萄球菌代谢活性,减少能量的产生或直接对金黄色葡萄球菌的结构造成损伤,从而抑制金黄色葡萄球菌生长繁殖,表明CFS具有预防或治疗金黄色葡萄球菌感染的潜力。研究初步揭示了L.sakei CFS抑制金黄色葡萄球菌的作用靶点,为研发新型微生态制剂提供理论依据。
[1] 刘保光, 谢苗, 董颖, 等.金黄色葡萄球菌研究现状[J].动物医学进展, 2021, 42(4):128-130.LIU B G, XIE M, DONG Y, et al.Research status of Staphylococcus aureus[J].Progress in Veterinary Medicine, 2021, 42(4):128-130.
[2] 徐玲燕, 潘秋月, 聂小华, 等.产叶酸菌株的筛选及其发酵条件的优化[J].食品工业科技, 2012, 33(13):158-162.XU L Y, PAN Q Y, NIE X H, et al.Screening of folic acid producing strains and optimization of fermentation conditions[J].Science and Technology of Food Industry, 2012, 33(13):158-162.
[3] WU Z, WU J, CAO P, et al.Characterization of probiotic bacteria involved in fermented milk processing enriched with folic acid[J].Journal of Dairy Science, 2017, 100(6):4223-4229.
[4] 薛艳蓉, 靳光, 王呈, 等.自制泡菜中高产胞外多糖乳酸菌的筛选与鉴定[J].现代食品, 2019(11): 165-168.XUE Y R, JIN G, WANG C, et al.Screening and identification of lactic acid bacteria producing extracellular polysaccharides in homemade pickles[J].Modern Food, 2019(11):165-168.
[5] LV C, KONG Q, YU Z Y, et al.Medium optimization of three marine probiotics and their application in the culture of Sebastes schlegelii[J].Microbial Pathogenesis, 2025, 204:107599.
[6] ZOU X, PAN L, XU M, et al.Probiotic potential of Lactobacillus sakei L-7 in regulating gut microbiota and metabolism[J].Microbiological Research,2023, 274:127438.
[7] DINCER E, KIVANC M.Evaluation of metabolic activities and probiotic characteristics of two Latilactobacillus sakei strains isolated from past rma[J].World Journal of Microbiology and Biotechnology, 2022, 38(12):237.
rma[J].World Journal of Microbiology and Biotechnology, 2022, 38(12):237.
[8] 张舒玥, 唐鑫, 毛丙永, 等.罗伊氏粘液乳杆菌CCFM1453胞外多糖对胃炎的修复作用及机制[J].食品与发酵工业, 2025,51(24):322-330.ZHANG S Y, TANG X, MAO B Y, et al.Reparative effects and mechanisms of exopolysaccharides from Limosilactobacillus reuteri CCFM1453 on gastritis[J].Food and Fermentation Industries, 2025,51(24):322-330.
[9] BARBOSA M S, TODOROV S D, BELGUESMIA Y, et al.Purification and characterization of the bacteriocin produced by Lactobacillus sakei MBSa1 isolated from Brazilian salami[J].Journal of Applied Microbiology,2014, 116(5):1195-1208.
[10] PARK J M, MOON J W, ZHANG B Z, et al.Antioxidant activity and other characteristics of lactic acid bacteria isolated from Korean traditional sweet potato stalk kimchi[J].Foods, 2024, 13(20):3261.
[11] 马祥兆, 徐淑琴, 陈晓慧, 等.藏羊源沙克乳酸杆菌的分离、鉴定及体外益生特性研究[J].饲料研究, 2021, 44(23):69-72.MA X Z, XU S Q, CHEN X H, et al.Isolation,identification and probiotic properties in vitro of Lactobacillus sakei from Tibetan sheep[J].Feed Research, 2021, 44(23):69-72.
[12] MORGAN-KISS R M, CRONAN J E.The Lactococcus lactis FabF fatty acid synthetic enzyme can functionally replace both the FabB and FabF proteins of Escherichia coli and the FabH protein of Lactococcus lactis[J].Archives of Microbiology, 2008, 190(4):427-437.
[13] 周甲申, 张琳, 张良.Ⅱ型脂肪酸生物合成途径机制和药物发现研究进展[J].化学学报, 2020, 78(12):1383-1398.ZHOU J S, ZHANG L, ZHANG L.Advances on mechanism and drug discovery of type-Ⅱ fatty acid biosynthesis pathway[J].Acta Chimica Sinica, 2020, 78(12):1383-1398.
[14] HALSEY C R, LEI S L, WAX J K, et al.Amino acid catabolism in Staphylococcus aureus and the function of carbon catabolite repression[J].mBio, 2017, 8(1):e01434-e01416.
[15] MAJERCZYK C D, SADYKOV M R, LUONG T T, et al.Staphylococcus aureus CodY negatively regulates virulence gene expression[J].Journal of Bacteriology, 2008, 190(7):2257-2265.
[16] GAO Y, POUDEL S, SEIF Y, et al.Elucidating the CodY regulon in Staphylococcus aureus USA300 substrains TCH1516 and LAC[J].mSystems, 2023, 8(4):e00279-e00223.
[17] SALAZAR N, YAMAMOTO B B, DE SOUZA M C L, et al.The C-terminal domain of Staphylococcus aureus zinc transport protein AdcA binds plasminogen and factor H in vitro[J].Pathogens, 2022, 11(2):240.
[18] SONG L Q, ZHANG Y F, CHEN W Z, et al.Mechanistic insights into staphylopine-mediated metal acquisition[J].Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(15):3942-3947.
[19] WILLIAMS W A, ZHANG R G, ZHOU M, et al.The membrane-associated lipoprotein-9 GmpC from Staphylococcus aureus binds the dipeptide GlyMet via side chain interactions[J].Biochemistry, 2004, 43(51):16193-16202.
[20] WINSTEL V, SANCHEZ-CARBALLO P, HOLST O, et al.Biosynthesis of the unique wall teichoic acid of Staphylococcus aureus lineage ST395[J].mBio, 2014, 5(2):e00869-e00814.
[21] MAO Y N, WANG Y X, LUO X F, et al.Impact of cell-free supernatant of lactic acid bacteria on Staphylococcus aureus biofilm and its metabolites[J].Frontiers in Veterinary Science, 2023, 10:1184989.