黄刺,其学名为直穗小檗(Berberis dasystachya Maxim.),属于小檗科、是一类落叶灌木植物,作为青海省特色植物资源,其种类繁多,资源量丰富,开发利用前景广阔。研究表明,直穗小檗果实可药食两用且含有多种化学有效成分,如小檗碱(又称黄连素)[1]、多酚、多糖、黄酮等,不仅具健脾、滋补、治疗消化不良等功效,还能消炎抗菌、抗心律失常和抗癌[2]。
研究表明活性多糖是黄刺果实的主要功效成分,提取物中多糖含量约为60%~95%。黄刺多糖具有良好的降血糖、抗氧化、抗肿瘤增殖等生物学功能,可升高胰岛素含量,且对活性氧(reactive oxygen species,ROS)代谢相关酶活性具有一定的调控作用[3-5]。此外,研究表明,提取方法对多糖的化学组成、提取率、生物活性等均有不同程度的影响[6]。如今由于植物多糖分离鉴定技术的快速发展,超声辅助、酶辅助和超声酶辅助提取等提取方法逐渐崭露头角[7-9]。从时间、成本、操作简便性等多方面考虑,每种技术都有自己的优势。然而对于黄刺多糖的提取,文献报道主要有水提法,对于不同提取方法的研究还未报道。
因此,本研究通过6种不同提取方法获得的黄刺多糖(Berberis dasystachya polysaccharides,BDPs)的得率、化学组成、抗氧化活性和降血糖活性进行对比研究。其抗氧化活性以DPPH自由基和ABTS阳离子自由基清除能力来评价,其降血糖活性以α-淀粉酶和α-葡萄糖苷酶抑制活性评价。以期寻找最佳的提取方法,为有效提高BDPs的提取效果,增大BDPs的开发利用范围提供理论依据。
1 材料与方法
1.1 材料与试剂
实验原料:采自青海省大通县新鲜黄刺浆果。采摘后挑选无腐烂、损坏的黄刺浆果进行清洗,于55 ℃条件烘干贮存于4 ℃冰箱备用。
石油醚、无水乙醇、正丁醇、氯仿等均选自国产分析纯化学试剂;抗坏血酸、DPPH、ABTS、α-葡萄糖苷酶(≥50 U/mg),南京都莱生物技术有限公司;阿卡波糖,拜尔医药保健有限公司。
1.2 仪器与设备
FA2104电子分析天平,上海良平仪器仪表有限公司;PHSJ-4A型pH计,上海仪电科学仪器股份有限公司;R-1001VN旋转蒸发仪,郑州长城科工贸有限公司;Cool Scofe 55-9冷冻干燥机,Gene Company Limited基因有限公司;UV-1780紫外分光光度计,岛津仪器(苏州)有限公司;TH2-82恒温振荡器,常州国华电器有限公司;Epoch T2酶标仪,美国伯腾仪器有限公司;S-3400扫描电子显微镜,日立科学仪器有限公司;ICS5000高效液相色谱仪、U3000高效液相色谱仪,美国赛默飞世尔科技有限公司;Agilent 1260 Infinity II凝胶渗透色谱仪,美国安捷伦公司;Spectrum 3红外光谱仪、TGA 8000热重分析仪,美国珀金埃尔默股份有限公司。
1.3 实验方法
1.3.1 不同方法提取黄刺多糖的工艺流程及操作要点
1.3.1.1 黄刺果粉预处理
石油醚与黄刺果粉混合(料液比1∶5,g∶mL,下同),40 ℃水浴2 h。脱脂残渣与85%乙醇(料液比1∶3)混合,50 ℃水浴1 h。最后烘干备用。
1.3.1.2 不同提取方法制备BDPs
a)热水浸提法(hot water extraction, HWE):将预处理后的黄刺果粉与蒸馏水混合(料液比1∶30),80 ℃ 水浴提取0.5 h,重复提取2~3次收集滤液并富集;
b)超声波辅助热水浸提法(ultrasonic auxiliary hot water extraction, HUE):将预处理后的黄刺果粉与蒸馏水混合(料液比1∶30),在台式机械超声波清洗器中80 ℃提取0.5 h,重复提取2~3次收集滤液并富集[4];
c)微波辅助热水浸提法(microwave auxiliary hot water extraction, HME):将预处理后的黄刺果粉与蒸馏水混合,在动力微波辅助提取机中提取(提取功率:430 W;提取时间:10 min),重复提取2~3次收集滤液并富集[3];
d)热水协同酶法(hot water coenzyme method, HEE):将预处理后的黄刺果粉与含有果胶酶(酶的用量为原料质量的0.68%)的预热蒸馏水(料液比1∶30)混合,调整溶液的pH值为4.5~5.0,50 ℃水浴120 min。完成提取后,酶悬浮液在95 ℃灭活10 min,然后冷却至室温。通过离心10 min收集上清液,并进行2~3次富集[10];
e)超声波协同酶法(ultrasonic synergy enzymatic, UEE):将预处理后的黄刺果粉与蒸馏水混合(料液比1∶30),在台式机械超声波清洗器中80 ℃提取0.5 h,调节混合液的温度50 ℃,加入果胶酶(酶的用量为原料质量的0.68%)混合,立即用盐酸或氢氧化钠对溶液的酸碱度进行调节,确保其pH值为4.5~5.0,随后用水浴锅在50 ℃的温度下水浴120 min。完成提取后,酶悬浮液在95 ℃灭活10 min,然后冷却至室温。通过以离心10 min收集上清液,并继续进行多糖富集[10];
f)微波协同酶法(microwave synergy enzymatic, MEE):已除单糖黄刺果实残渣与纯水混合(料液比1∶30),在动力微波辅助提取机提取(提取功率:430 W;提取时间:10 min)[11],调节混合液的温度50 ℃,加入果胶酶(酶的用量为原料质量的0.68%)混合,随即采用盐酸、氢氧化钠来调整溶液的酸碱度,使溶液的pH值为4.5~5.0,而后在50 ℃的水浴锅中进行120 min的水浴。完成提取后,酶悬浮液在95 ℃灭活10 min,然后冷却至室温。通过离心10 min收集上清液,并继续进行多糖富集[10];
将上述6种提取方法得到的粗多糖提取液分别进行Savege法除去蛋白质[11]、大孔树脂进行脱色、透析纯化处理[12],最后用3倍体积无水乙醇溶液于4 ℃ 下醇沉24 h经真空冷冻干燥制得BDPs。
1.3.2 不同方法提取所得BDPs化学组成测定
在对BDPs的成分分析中,分别运用特定的检测方法对其各类物质含量予以测定:采用苯酚-硫酸显色原理测定BDPs内多糖的含量、硫酸咔唑反应体系量化BDPs中糖醛酸的占比[13]、DNS试剂与还原糖的特异性反应来计算还原糖含量[14]、依据考马斯亮蓝G-250与蛋白质结合后的吸光特性测定蛋白质含量[15]。
1.3.3 不同提取方法所得BDPs初级结构表征
1.3.3.1 不同提取方法制备BDPs分子质量测定
样品溶液配制:精密称取样品10 mg,溶解于1 mL 的流动相溶液中,配制成5 mg/mL溶液,涡旋至样品溶解后,12 000 r/min离心10 min。吸取上清液,用0.22 μm的水系微孔滤膜过滤,然后将样品转置于1.8 mL进样小瓶中上机检测。色谱系统采用的是凝胶色谱-示差-多角度激光光散射系统,采用凝胶排阻色谱柱SB-805-804-803(8 mm×300 mm);流速1 mL/min;柱温40 ℃;进样量50 μL;分析时间40 min。
1.3.3.2 不同提取方法制备BDPs单糖组成测定
a)样品前处理
精准称取(5 ± 0.05) mg的BDPs样品,置于色谱瓶内,随后加入1 mL浓度为2 mol/L的三氟乙酸(trifluoroacetic acid,TFA)溶液,将其置于121 ℃的环境下持续加热2 h。加热完毕后,采用氮气气流将溶液吹干,接着再次加入甲醇进行清洗并吹干,如此重复循环操作2~3次,最后加入无菌水使样品充分溶解,以便进行后续的检测。
b)色谱条件
实验所采用离子色谱系统ICS5000,配备DionexTM CarboPacTM PA20型色谱柱(150 mm×3.0 mm,10 μm),进样体积设定为5 μL。流动相选用A相(0.1 mol/L氢氧化钠溶液)与B相(由0.1 mol/L氢氧化钠和0.2 mol/L醋酸钠混合而成),以0.5 mL/min的流速通过色谱柱,柱温恒定控制在30 ℃,以此确保色谱分离过程的精准性与稳定性;
洗脱梯度程序如下:0 min A相/B相(95∶5,体积比),30 min A相/B相(80∶20,体积比),30.1 min A相/B相(60∶40,体积比),45 min A相/B相(60∶40,体积比),45.1 min A相/B相(95∶5,体积比),60 min A相/B相(95∶5,体积比)。
c)单糖含量测定
采用外标法定量,通过配制不同浓度标样来制定标准曲线。线性关系信息如表1所示,再以样品中各单糖对应的峰面积代入标曲计算浓度,进一步计算各单糖含量(mg/g)。计算如公式(1)所示:
单糖含量![]()
(1)
表1 单糖含量标准曲线
Table 1 Standard curve of monosaccharide content
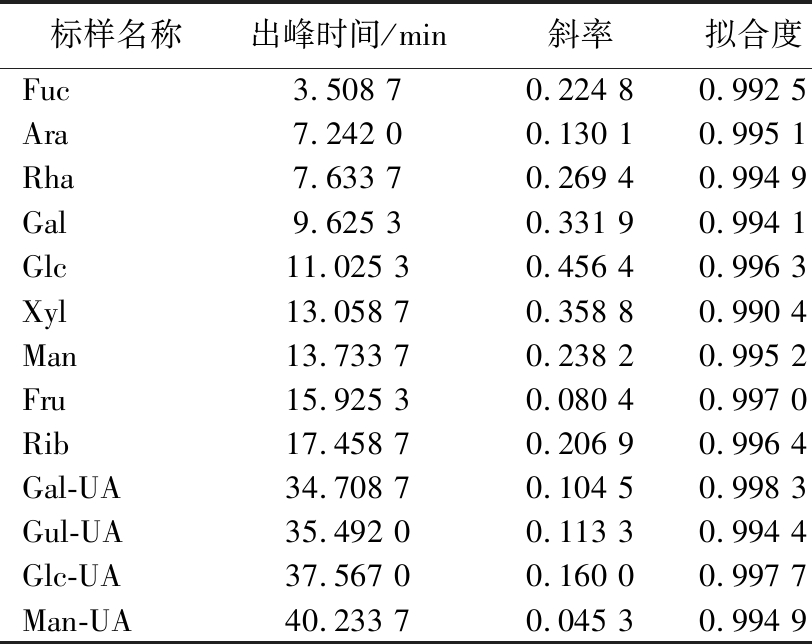
标样名称出峰时间/min斜率拟合度Fuc3.508 70.224 80.992 5Ara7.242 00.130 10.995 1Rha7.633 70.269 40.994 9Gal9.625 30.331 90.994 1Glc11.025 30.456 40.996 3Xyl13.058 70.358 80.990 4Man13.733 70.238 20.995 2Fru15.925 30.080 40.997 0Rib17.458 70.206 90.996 4Gal-UA34.708 70.104 50.998 3Gul-UA35.492 00.113 30.994 4Glc-UA37.567 00.160 00.997 7Man-UA40.233 70.045 30.994 9
式中:C为仪器读取质量浓度,μg/mL;V为样品提取液体积,mL;F为稀释因子;M为样品称取总质量,mg。
1.3.3.3 不同提取方法制备BDPs紫外光谱分析(ultraviolet spectroscopy,UV)
将粗多糖配制为1 mg/mL的溶液,用紫外可见分光光度计在200~800 nm进行全波长扫描[16]。
1.3.3.4 不同提取方法制备BDPs红外光谱分析(Fourier transform infrared spectroscopy,FT-IR)
借助傅里叶变换红外光谱仪,运用KBr压片法,于400~4 000 cm-1波数区间开展扫描测定,以获取样品的红外光谱信息。
1.3.3.5 不同提取方法制备BDPs电镜扫描观察(scanning electron microscope,SEM)
利用扫描电子显微镜观察BDPs样品粉末表观结构[17]。
1.3.3.6 不同提取方法制备BDPs刚果红分析
配制标准浓度(0.2 mmol/L)刚果红溶液和1 mol/L的NaOH溶液,测定BDPs在不同浓度下NaOH溶液最大吸光度对应的吸收波长。
1.3.4 不同提取方法制备BDPs热稳定性分析
精确称取一定量的BDPs多糖样品,置于热重仪内,在氮气保护氛围下,将样品从起始温度25 ℃以每分钟10 ℃的升温速率逐步加热至900 ℃,进而开展热重分析测试,以获取多糖在升温过程中的质量变化特性的关键数据。
1.3.5 不同提取方法所得BDPs体外抗氧化活性测定
1.3.5.1 不同提取方法制备BDPs对DPPH自由基清除活性测定
参照WANG等[18]的方法,稍作改动。精准称取6种不同提取方法所得到的粗多糖各64 mg,分别配制质量浓度为16、8、4、2、1、0.5、0.25、0.125 mg/mL的多糖溶液,以维生素C为对照,于517 nm波长处采用酶标仪检测吸光度,DPPH自由基清除率根据公式(2)计算:
DPPH自由基清除率![]()
(2)
式中:A0为样品溶液加DPPH溶液的吸光度;A1为样品溶液加乙醇溶液的吸光度;A2为乙醇溶液加DPPH溶液的吸光度。
1.3.5.2 不同提取方法制备BDPs对ABTS阳离子自由基清除活性测定
参照WANG等[18]的方法,稍作改动。精准称取6种不同提取方法所得粗多糖各64 mg,配制质量浓度分别16、8、4、2、1、0.5 mg/mL的多糖溶液,以维生素C为对照,于732 nm波长下用酶标仪测定吸光度,ABTS阳离子自由基清除率根据公式(3)计算:
ABTS阳离子自由基清除率![]()
(3)
式中:A0为样品溶液加ABTS溶液的吸光度;A1为样品溶液加去离子水的吸光度;A2为去离子水加ABTS溶液的吸光度。
1.3.6 不同提取方法所得BDPs体外降血糖活性测定
1.3.6.1 不同提取方法制备BDPs抑制α-葡萄糖苷酶活性分析
参考文献[19],略作改动。精准称取6种不同提取方法所得粗多糖各80 mg,配制质量浓度分别4、2、1、0.5、0.25 mg/mL的多糖溶液,于波长405 nm下用酶标仪测吸光度,阿卡波糖作对照,α-葡萄糖苷酶抑制率按公式(4)计算:
抑制率![]()
(4)
式中:A1为样品组;A2为样品对照组;A3为空白组;A4为空白对照组。
1.4.6.2 不同提取方法制备BDPs抑制α-淀粉酶活性的分析
参考文献[19],略作改动。精准称取6种不同提取方法所得粗多糖各80 mg,配制质量浓度分别4、2、1、0.5、0.25、0.125 mg/mL的多糖溶液,于波长540 nm 下用酶标仪测吸光度,阿卡波糖作对照,α-淀粉酶抑制率按公式(5)计算:
抑制率![]()
(5)
式中:A1为样品组;A2为样品对照组;A3为空白组;A4为空白对照组。
1.4 数据处理
全部试验数据进行3次平行测定,以“平均值±标准差”表示,数据分析由Excel软件及SPSS软件完成,图片由Origin 2022软件处理,P<0.05表示差异显著。
2 结果与分析
2.1 不同提取方法所得BDPs化学组成分析
不同提取方法所得BDPs中的多糖得率及化学组成结果如表2所示,BDPs-UEE的多糖得率最高,可达0.90%,其余提取方法多所得多糖得率均在0.5% 以上。BDPs-UEE的多糖含量和糖醛酸含量均显著高于其他提取方法所得BDPs,其含量分别高达(75.26±0.7)%(P<0.05)和(15.58±1.73)%(P<0.05),这可能是由于超声空化效应及机械剪切效应破坏了细胞壁,促使提取剂将水溶性多糖溶出[20]。BDPs-MEE的还原糖含量最高,达到了9.47%,HEE法和UEE法次之、三者均与HWE、HUE、HME法提取所得还原糖含量差异显著(P<0.05),对于还原糖含量的变化,原因可能是由于酶切割位点以及酶解环境的不同导致所得多糖结构不同,从而使还原糖含量存在差异,热水辅助所得还原糖含量显著低于酶辅助法,因此未来可进一步探究不同酶辅助的作用效果。蛋白质含量最低的为BDPs-HEE,达到(1.10±0.44)%,与BDPs-HWE相比差异不显著(P>0.05),与其余方法相比差异显著(P<0.05)说明酶在适宜的环境条件下具有较好的水解能力,降低了蛋白质的残留量。上述结果表明,不同提取方法制得多糖其得率及化学组成具有较大差异。
表2 不同提取方法所得BDPs的得率及化学成分
Table 2 The yield and chemical composition of BDPs by different extraction methods
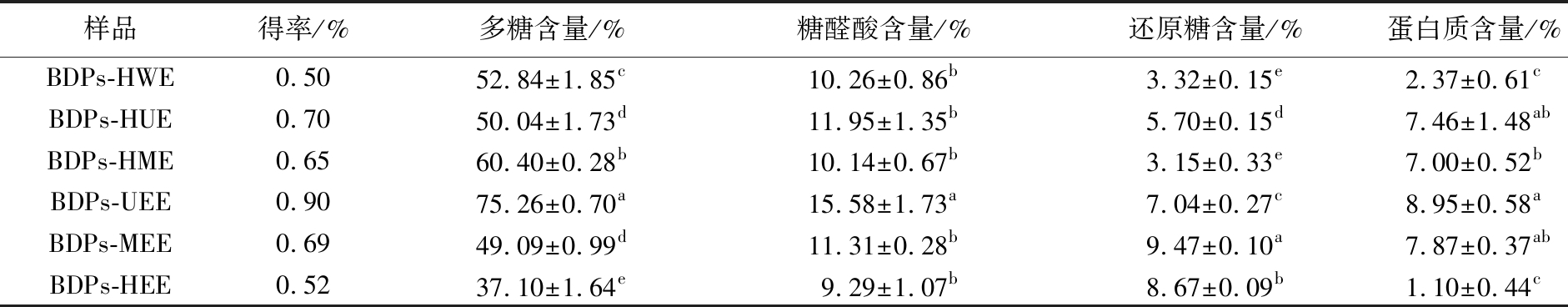
注:同列小写字母不同表示差异显著(P<0.05)。
样品得率/%多糖含量/%糖醛酸含量/%还原糖含量/%蛋白质含量/%BDPs-HWE0.5052.84±1.85c10.26±0.86b3.32±0.15e2.37±0.61cBDPs-HUE0.7050.04±1.73d11.95±1.35b5.70±0.15d7.46±1.48abBDPs-HME0.6560.40±0.28b10.14±0.67b3.15±0.33e7.00±0.52bBDPs-UEE0.9075.26±0.70a15.58±1.73a7.04±0.27c8.95±0.58aBDPs-MEE0.6949.09±0.99d11.31±0.28b9.47±0.10a7.87±0.37abBDPs-HEE0.5237.10±1.64e9.29±1.07b8.67±0.09b1.10±0.44c
2.2 不同提取方法所得BDPs初级结构表征
2.2.1 不同提取方法所得BDPs分子质量分析
由图1和表3可知,BDPs的分子质量受不同提取方法的影响较大。6种提取方法中,BDPs-HWE的重均分子质量最高,为1 361.926 kDa;BDPs-MEE的重均分子质量最低,为282.266 kDa。BDPs-HEE的峰值分子质量最大,为1 237.464 kDa;BDPs-MEE的峰值分子质量最小,仅96.04 kDa。BDPs-HWE的数均分子质量为890.354 kDa,在6种提取方法中相对较高;BDPs-MEE的数均分子质量最低,为85.472 kDa。此结果可能是由于普通的热水浸提因其较高的温度和较长时间的处理导致提取制备的多糖分子之间容易出现聚集现象,导致分子质量较大。
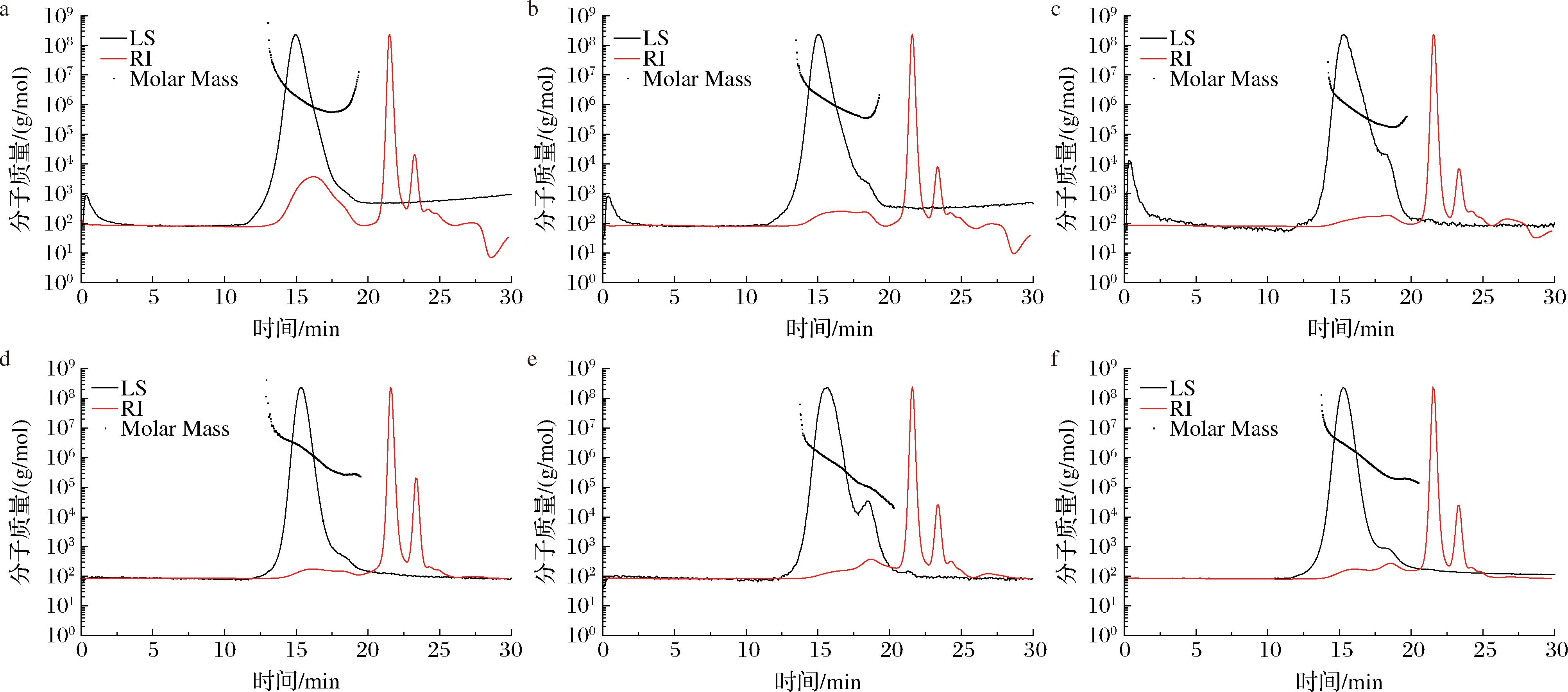
a-BDPs-HWE;b-BDPs-HEE;c-BDPs-HUE;d-BDPs-UEE;e-BDPs-MEE;f-BDPs-HME
图1 不同提取方法所得BDPs分子质量分析图
Fig.1 Molecular weight analysis diagram of BDPs obtained by different extraction methods
表3 不同提取方法所得BDPs的分子质量表
Table 3 Molecular weight of BDPs from different extraction methods
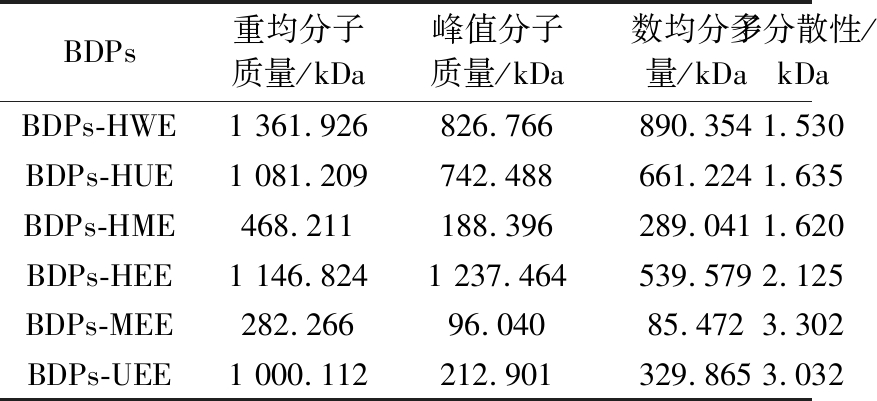
BDPs重均分子质量/kDa峰值分子质量/kDa数均分子量/kDa多分散性/kDaBDPs-HWE1 361.926826.766890.3541.530BDPs-HUE1 081.209742.488661.2241.635BDPs-HME468.211188.396289.0411.620BDPs-HEE1 146.8241 237.464539.5792.125BDPs-MEE282.26696.04085.4723.302BDPs-UEE1 000.112212.901329.8653.032
微波协同酶法提取一定程度上降低了多糖的分子质量,这可能是因为酶破坏了细胞结构增加了多糖的溶出,同时也破坏了多糖本身的链结构,而且微波效应可以在短时间内提高温度,迅速破坏组织结构,从而使高分子质量组分降低,中分子质量和小分子质量组分增加[21]。超声波的空化作用、机械效应和热效应也可以裂解多糖的糖苷键,对多糖的分子结构造成破坏,使BDPs-UEE的分子质量处于适宜范围。
2.2.2 不同提取方法所得BDPs单糖组成分析
检测BDPs单糖组成时,使用Thermo IC5000离子色谱系统,电化学检测器进行分析。图2所示的BDPs单糖组成离子色谱图中共有峰含有8种,分别是岩藻糖、阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、半乳糖醛酸、葡萄糖醛酸。其中BDPs-HUE单糖组成中相比其他样品多含有古罗糖醛酸,这可能是因为超声辅助条件下,空化效应优先断裂连接古罗糖醛酸的糖苷键,释放出游离的Gul-A或其寡糖片段。而其他提取方法的剪切力较弱,可能无法有效破坏这些键。因此不同提取方法BDPs中多糖组成存在差异。
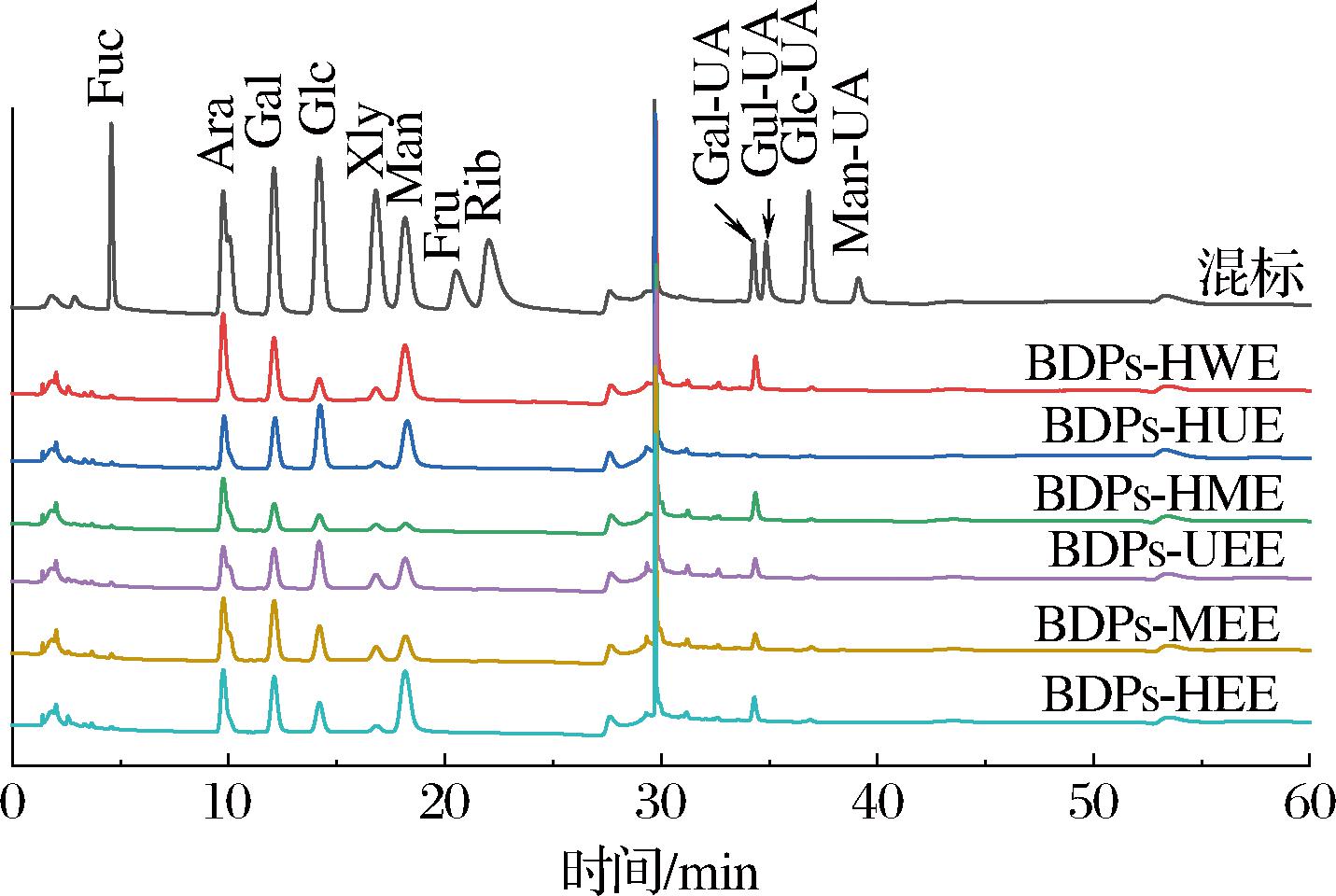
图2 不同提取方法BDPs单糖组成离子色谱图
Fig.2 Different regions BDPs monosaccharide composition of ion chromatograms
注:Fuc:岩藻糖,Ara:阿拉比糖,Rha:鼠李糖,Gal:半乳糖,Glc:葡萄糖, Xyl:木糖,Man:甘露糖,Fru:果糖,Rib:核糖,Gal-UA:半乳糖醛酸, Gul-UA:古罗糖醛酸,Glc-UA:葡萄糖醛酸,Man-UA:甘露糖醛酸(下同)。
不同提取方法所得BDPs中各单糖含量百分比如表4所示,6种提取方法所制备的BDPs样品,其单糖组成均为Fuc、Ara、Gal、Glc、Xly、Man、Gal-UA、Glc-UA;各单糖组分所占百分比分别为:BDPs-HWE:0.36∶26.91∶12.83∶3.96∶2.69∶23.68∶28.14∶1.42;BDPs-HME:0.48∶32.02∶10.11∶5.32∶2.75∶4.94∶43.14∶1.25;BDPs-MEE:0.87∶32.10∶17.80∶9.30∶4.42∶13.8∶19.35∶2.37;BDPs-UEE:0.73∶23.87∶12.42∶13.64∶4.75∶18.48∶24.55∶1.56;BDPs-HEE:0.35∶22.18∶13.36∶6.47∶1.64∶30.60∶24.08∶1.32;这5种多糖样品中单糖组成一致,单个单糖组分含量所占百分比却大相径庭。通过比较其他5种多糖样品发现,古罗糖醛酸只存在于BDPs-HUE中,其百分含量为1.57%。通过表3分析,不同提取方法所得BDPs中主要由岩藻糖、阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、半乳糖醛酸、葡萄糖醛酸这8种单糖组成。由此可知BDPs不同的提取方法致使粗多糖中单糖含量也呈现出较大差异。JI等[22]对红枣果实的研究也发现多糖的单糖组成存在差异,这可归因于提取方法的不同。猜测可能是不同提取工艺对细胞壁的降解机制及作用强度存在差异。热水浸提主要靠热作用使细胞膨胀破裂,释放多糖,但对细胞壁破坏有限;超声辅助提取利用超声空化效应,机械力较强,可能使部分多糖链断裂,影响单糖溶出;酶辅助提取通过酶特异性水解细胞壁成分,释放多糖,不同酶作用位点和效率不同,导致单糖溶出量有差异;酶-超声辅助提取结合两者优势,可能使多糖释放更充分,单糖含量也会不同。BDPs-MEE中阿拉伯糖、半乳糖、半乳糖醛酸的含量较高,可能的原因是微波协同果胶酶的提取条件下,果胶酶能特异性地降解细胞壁结构,水解不溶性的细胞壁纤维,而阿拉伯糖是细胞壁纤维的重要组成部分,酶的作用促进了阿拉伯糖的溶解和释放[23]。
表4 不同提取方法所得BDPs单糖含量测定 单位:μg/mg
Table 4 Determination of monosaccharide content of BDPs from different producing areas
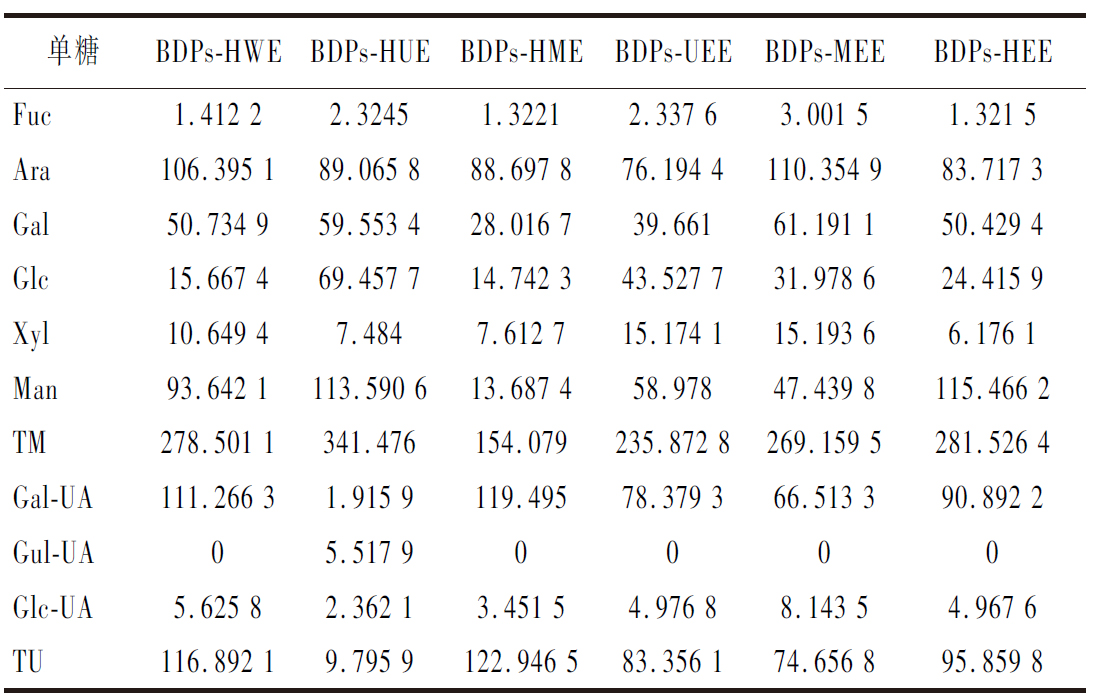
注:TM为多糖中各单糖含量总和;TU为多糖中各糖醛酸含量总和。
2.2.3 不同提取方法所得BDPs(UV)分析
由图3可知,6种不同提取方法所得BDPs在260、280 nm处均存在凸起峰,由此判断6种不同提取方法制备的多糖样品中存在核酸和蛋白质等物质[16]。由此说明多糖可能不是一种单一的糖类物质,而可能是以复合糖蛋白的形式存在。其次,说明多糖中含有未除干净的蛋白质杂质,这也与蛋白质含量测定的结果相吻合。
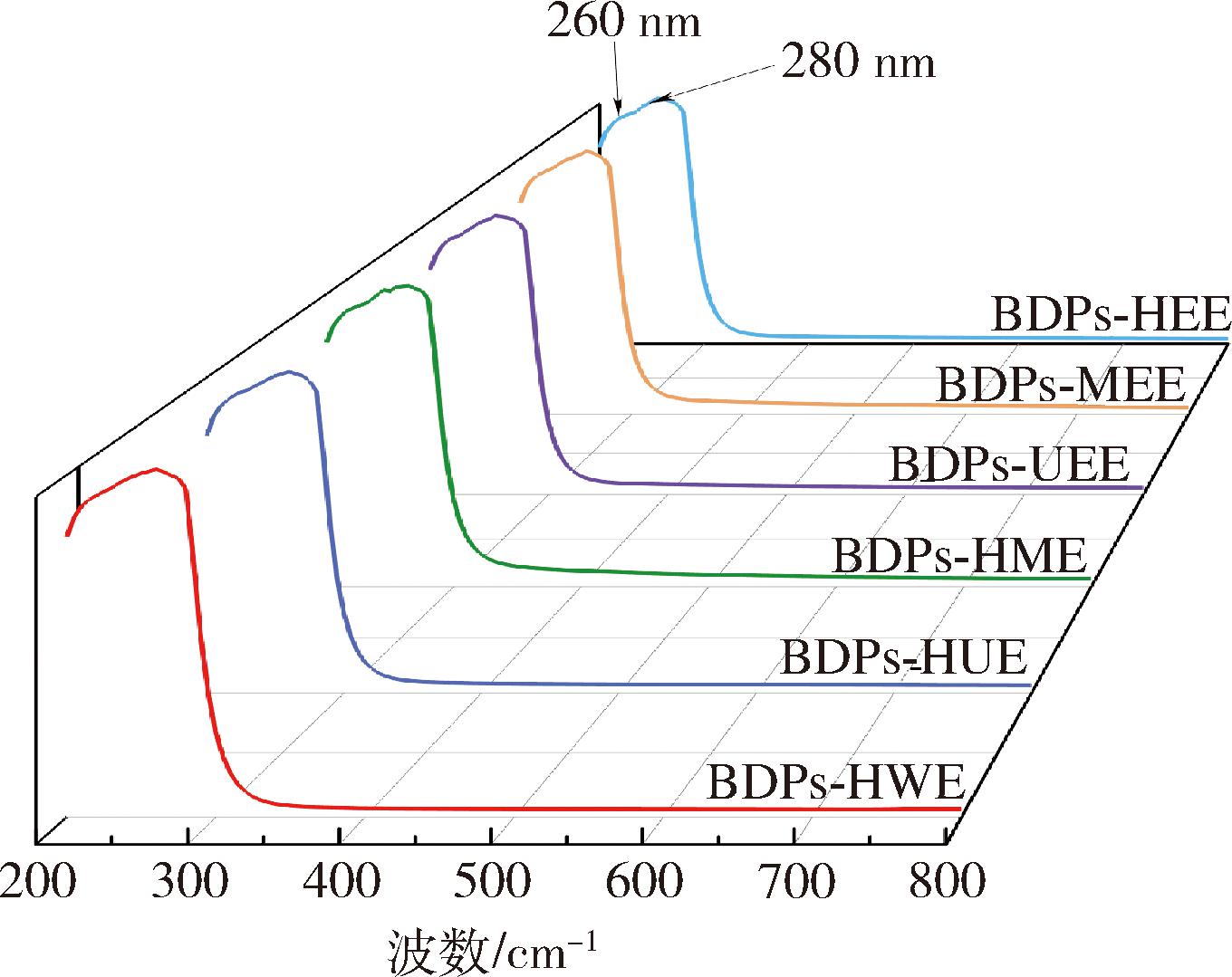
图3 不同提取方法所得BDPs的紫外光谱图
Fig.3 Ultraviolet spectra of BDPs by different extraction methods
2.2.4 不同提取方法所得BDPs(FT-IR)分析
由图4可知,在不同提取方法所得BDPs的红外光谱中,强振动特征吸收峰出现在3 600~3 000 cm-1,该范围内主要出现NH—和OH—官能团伸缩振动现象,为多糖分子间游离羟基与氨基的特征吸收峰,特征吸收峰出现于3 438 cm-1附近,即为—OH伸缩振动峰,说明不同提取方法所得的多糖均形成了分子间氢键[24];位于2 929 cm-1附近的特征峰是糖链烃基中C—H键振动所致,表征存在亚甲基;1 618 cm-1附近出现的吸收峰对应醛酸—COOH中C![]() O的非对称伸缩振动,表明不同提取方法所得的BDPs中均有糖醛酸的存在,此发现与化学组成分析所获糖醛酸含量结果相符。此外,1 417 cm-1附近的特征峰对应—COOH的对称伸缩振动[25];而在1 161~988 cm-1呈现的特征峰,则为多糖呈吡喃环型结构提供了证据;927~875 cm-1附近出现特征吸收峰属于α-糖苷键和β-糖苷的特征吸收峰[24]。由此说明,6种不同提取方法所得多糖结构均相似,具有典型的多糖伸缩振动峰,都由α-糖苷键和β-糖苷键共同连接而成的,且均为吡喃糖构型的杂多糖。
O的非对称伸缩振动,表明不同提取方法所得的BDPs中均有糖醛酸的存在,此发现与化学组成分析所获糖醛酸含量结果相符。此外,1 417 cm-1附近的特征峰对应—COOH的对称伸缩振动[25];而在1 161~988 cm-1呈现的特征峰,则为多糖呈吡喃环型结构提供了证据;927~875 cm-1附近出现特征吸收峰属于α-糖苷键和β-糖苷的特征吸收峰[24]。由此说明,6种不同提取方法所得多糖结构均相似,具有典型的多糖伸缩振动峰,都由α-糖苷键和β-糖苷键共同连接而成的,且均为吡喃糖构型的杂多糖。
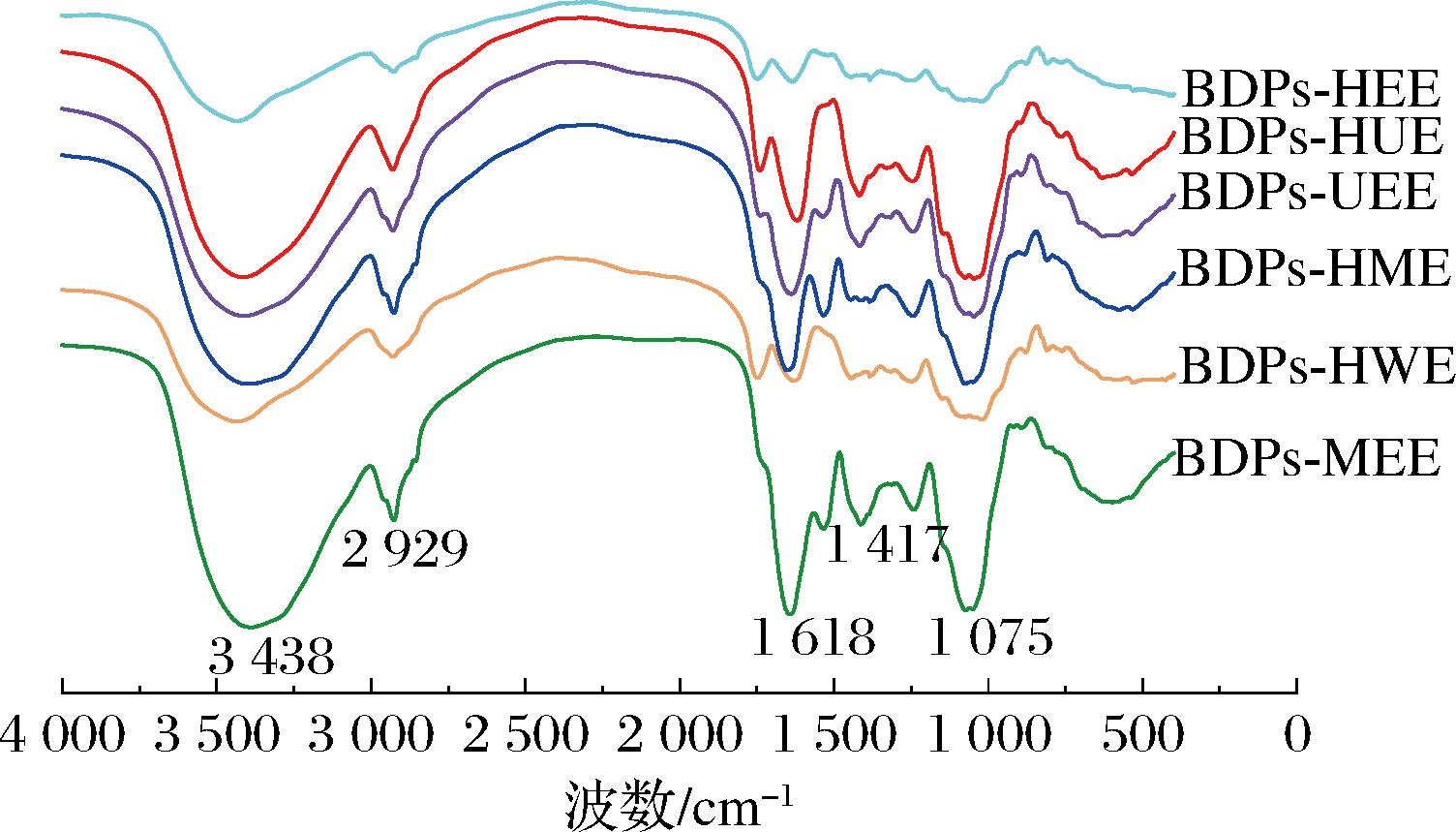
图4 不同提取方法所得BDPs的红外光谱
Fig.4 Infrared spectra of BDPs for different extraction methods
2.2.5 不同提取方法所得BDPs扫描电镜分析
由图5可知,HWE法(图5-a)所得多糖呈岩洞形,表面多孔洞,部分结构呈现似瀑布的形态,具有立体的层次感,这可能是由于热水浸提法相对温和,在提取过程中对多糖分子的结构破坏较小,能够较好地保留多糖分子的天然结构和性质,有利于形成相对完整的层状结构。通过HEE法(图5-b)与HUE法(图5-c)所制备的多糖,结构具有相似性,其表面平整光滑,呈现漩涡状形貌,且分子间结合较为致密,但后者表面纹路更加复杂多样,呈现流线型,与河流分布较相似。UEE法(图5-d)和MEE法(图5-e)所得多糖整体结构布局比较相似,均呈现不规则的块状,其中UEE法所得多糖表面相对光滑,结构相对致密,可能是由于超声波的空化作用增加了BDPs与果胶酶的接触机会,加速多糖分子链的断裂,使半乳糖醛酸溶出,从而出现BDPs-UEE的单糖组成中半乳糖醛酸含量较高的结果,此现象与罗世博等[26]对樱桃李纯化多糖微观结构的研究结果较为相似而略有不同。MEE法(图5-e)所得多糖表面比较粗糙,层次不一,可见圆球状颗粒的堆积,这可能是由于微波作用使糖苷键断裂,进而使大分子多糖中的葡萄糖、半乳糖溶出,同时微波的快速加热可能导致多糖局部高温,使还原糖与蛋白质和氨基酸在高温下结合,发生美拉德反应生成了聚合物,从而表现出了颗粒的堆积。HME法(图5-f)所得多糖表面呈现平整,可见大小不一的孔洞,这可能是因为在微波辐射作用下,极性物质选择性吸收电磁能并转化为热能,引起胞内温度上升产生了热效应导致细胞膜脂质双分子层发生相变,同时使细胞壁多糖结构发生局部降解,在亚细胞层面形成了孔隙结构[27]。

a-BDPs-HWE;b-BDPs-HEE;c-BDPs-HUE;d-BDPs-UEE;e-BDPs-MEE;f-BDPs-HME
图5 不同提取方法所得BDPs电镜扫描图
Fig.5 Electron microscopy scans of BDPs obtained by different extraction methods
通过SEM分析可知,由于提取方法的不同使得BDPs中的糖苷键及氢键的损伤程度有所差异,对BDPs表面微观结构造成较大影响,从而赋予BDPs不同的表面形貌和外观。
2.2.6 不同提取方法所得BDPs刚果红分析
由图6可知,随着NaOH浓度升高,BDPs-HUE、BDPs-HME、BDPs-HWE与刚果红试剂作用所产生络合物的最大吸收波长呈连续下降趋势,这表明BDPs均无三螺旋结构。出现该结果,可能是由于超声产生的空化效应会形成局部的高温、高压和强烈的冲击波,可能会使多糖分子的三螺旋结构发生解旋,同时微波产生的热效应也可能会导致三螺旋结构的破坏。此外,BDPs-MEE、BDPs-HEE、BDPs-UEE在较高的NaOH浓度下,刚果红络合物的最大吸收波长没有红移,无明显上升趋势,说明这3种提取方法所得的BDPs也没有三螺旋结构,猜测可能的原因是酶的特异性作用可能会降解多糖的某些特定区域,影响三螺旋结构的形成。总的来说,6种不同提取方法所得的BDPs与刚果红试剂作用所产生络合物的最大吸收波长有所不同,BDPs结构复杂且分子质量较大,碱性环境促使多糖分子内的氢键断裂,进而致使多糖分子在水溶液中呈现出无规则卷曲的空间构象。
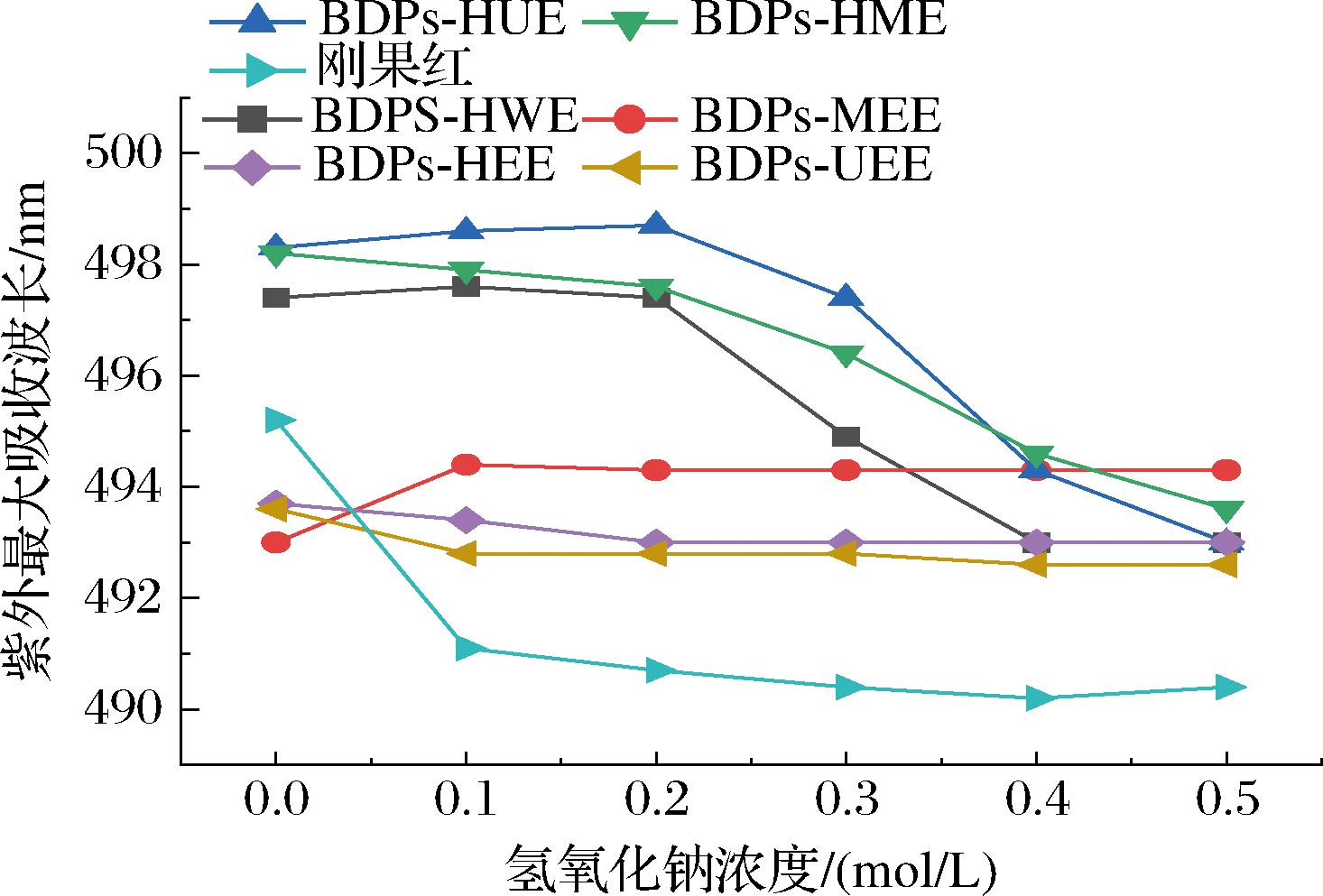
图6 不同NaOH浓度下BDPs与刚果红络合物的最大吸收波长λmax
Fig.6 The maximum absorption wavelength λmax of BDPs and Congo red complex at different NaOH concentrations
2.3 不同提取方法所得BDPs热稳定性分析
由图7中热重(thermogravimetry,TG)分析和微商热重(derivative thermogravimetry,DTG)分析曲线可知,在40~850 ℃的温度跨度内,BDPs热稳定性效果表现出较大差异。在整个温度区间内,BDPs的热降解过程可划分为2个阶段。6种不同提取方法所制备的BDPs样品发生热解第一阶段依次分别为:49.04~185.79 ℃、49.02~176.97 ℃、49.01~181.27 ℃、48.95~179.10 ℃、48.97~180.26 ℃、49.02~188.98 ℃,该阶段样品质量损失率依次为10.55%、10.74%、8.44%、11.10%、10.84%、10.19%,第一阶段最大失重率分别出现在96.64、87.91、85.82、94.91、104.92、116.01 ℃。此阶段样品质量的减少源于其内部水分的散失,这显示样品中不但含有结合水,而且存在一定比例的吸附水[4]。进一步分析印证了多糖于49~200 ℃的温度区间内能够维持稳定状态,说明此温度范围内实施的热处理并不会引发多糖的热分解反应。鉴于此特性,BDPs具备应用于巴氏杀菌食品以及药品等需高温加工领域的潜力[28]。在这一阶段BDPs-HME的质量损失率处于最低水平,为8.44%,这表明在第一阶段中BDPs-HME所含的水分相对较少,稳定性更佳。
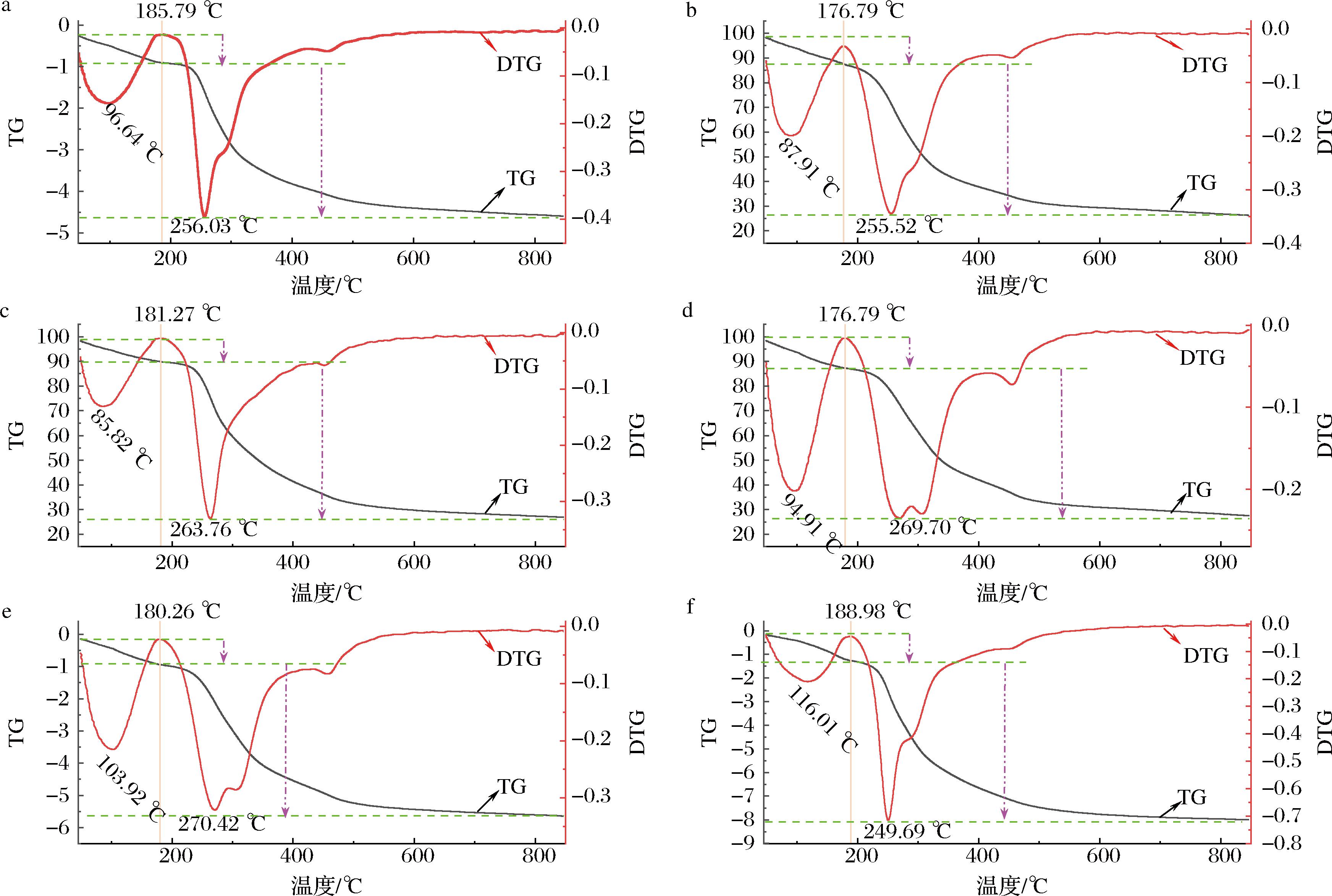
a-BDPs-HWE;b-BDPs-HUE;c-BDPs-HME;d-BDPs-UEE;e-BDPs-MEE;f-BDPs-HEE
图7 不同提取方法BDPs热稳定性
Fig.7 Thermal stability of BDPs of different extraction methods
第二阶段中不同提取方法所得的BDPs样品在以下温度范围内发生热解,分别是184.40~845.78 ℃、177.94~254.11 ℃、184.64~258.82 ℃、194.80~256.12 ℃、189.61~264.76 ℃、198.87~246.07 ℃,该阶段样品质量损失率依次为60.25%、61.24%、62.97%、59.74%、64.81%、59.70%,该阶段最大失重率分别出现在:BDPs-HWE:256.04 ℃,BDPs-HUE:255.52 ℃,BDPs-HME:264.76 ℃,BDPs-UEE:269.70 ℃,BDPs-MEE:270.42 ℃,BDPs-HEE:249.69 ℃,该结果表明,不同提取方法制备的BDPs样品在第二阶段发生热解的起始温度点各有差别,温度跨度介于100~200 ℃。该阶段内,样品质量大幅下降,可能是是由于高温促使BDPs样品中多糖糖苷键断裂,引发分子结构的分解与重组。
6种不同提取方法所得的BDPs样品在第三阶段发生热解的温度范围分别是284.56~617.74 ℃、176.70~845.76 ℃、181.27~845.99 ℃、179.08~845.97 ℃、180.94~845.84 ℃、188.98~845.69 ℃。在高温阶段,6种不同提取方法所得的BDPs样品的DTG曲线无明显峰值,说明样品的剩余质量基本稳定,质量损失较少,不同的提取方法对BSPs的热稳定性影响不显著。
2.4 不同提取方法所得BDPs体外抗氧化活性的分析
2.4.1 不同提取方法所得BDPs清除DPPH自由基的结果与分析
由图8可知,采用6种不同提取方式所得到的BDPs在特定浓度区间内,均展现出对DPPH自由基的有效清除能力。当处于高浓度条件下,即质量浓度达到8 mg/mL时,6种多糖样品对DPPH自由基的清除率均可超过80%,此清除能力与抗坏血酸(维生素C)相近。其中,由超声辅助酶法提取得到的BDPs对DPPH自由基的清除率更是高达89.61%,相较于阳性对照虽略低,但经统计学检验,两者差异无显著性意义(P>0.05),BDPs-UEE在这些多糖样本中展现出最优的抗氧化性能。猜测出现这种结果的潜在原因可能是酶解条件下,反应条件较为温和,且由于超声波辅助提取使多糖与蛋白等杂质的链接键被破坏,多糖结构中暴露出了更多的活性基团,从而提升了粗多糖的纯度和抗氧化能力[29]。许多研究表明,多糖的生物活性与其化学组成和结构特征,包括分子质量(Mw)、单糖组成、糖苷键、链构象等密切相关。JI等[30]对枣果实多糖的结构特征及抗氧化活性比较发现,植物多糖中存在大量半乳糖醛酸可能导致更高水平的DPPH自由基清除率。杨金涛等[31]对榆黄蘑多糖的构效关系研究发现,Ara、Rib、Man和Glc 4种单糖对多糖的抗氧化活性具有积极的促进作用。这与本研究结果中BDPs-UEE的Xyl、Glc、Man、Gal-UA含量相对较高大致吻合。在实验所设定的质量浓度范围(0.125~8 mg/mL)内,不同提取方法制备的多糖样品对DPPH自由基的清除率呈现出剂量依赖性变化,整体而言,它们的抗氧化效果均低于维生素C。猜测可能是因为不同提取方法对多糖中杂质的去除程度不同,某些杂质可能会与自由基反应,或者干扰多糖与自由基的结合,从而影响多糖的抗氧化活性。
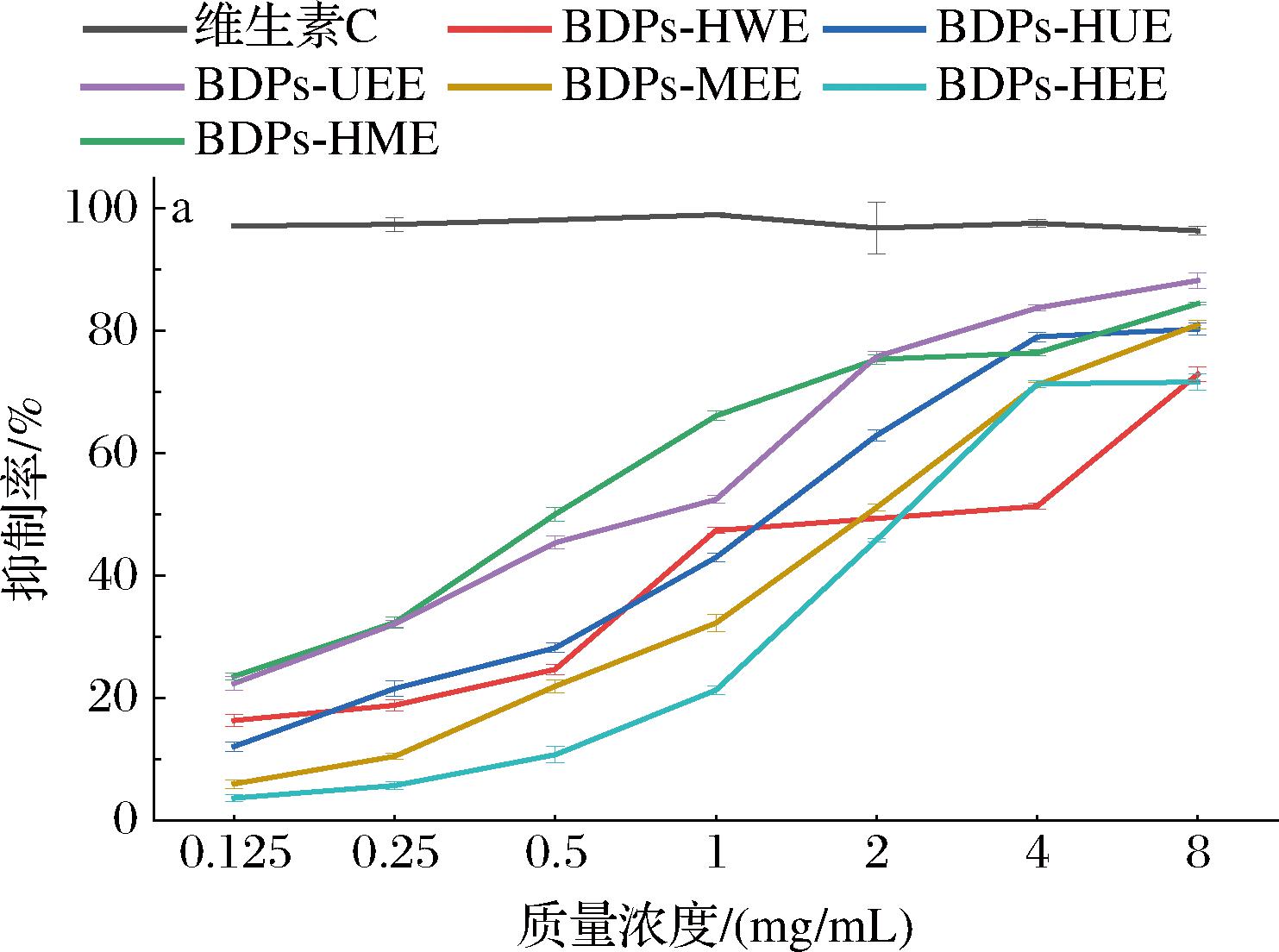
图8 不同提取方法所得BDPs及维生素C对DPPH自由基清除率比较
Fig.8 Comparison of DPPH free radical scavenging rate between vitamin C and BDPs obtained by different extraction methods
2.4.2 不同提取方法所得BDPs清除ABTS阳离子自由基的结果与分析
由图9可知,BDPs能有效地清除ABTS阳离子自由基,ABTS阳离子自由基的清除率和不同提取方法得到的多糖样品在给定浓度范围下的浓度呈正相关趋势。在高质量浓度(8 mg/mL)时BDPs对ABTS阳离子自由基的清除率最佳,其中BDPs-UEE对ABTS阳离子自由基的清除率最高,达到了98.44%,抗氧化效果接近于维生素C对照组。上述实验结果的产生或许归因于超声波提取BDPs的过程中,其机械性断键作用和空化效应使大分子多糖较敏感的化学键断裂,引起构象的改变,降低其分子质量,增加多糖的水溶性,使多糖中各单糖比例发生了改变,从而使其抗氧化能力显著增强[32]。分子质量较高的多糖分子含有较多的结构功能单元,这有助于维持其复杂的构象结构,但分子质量过大的多糖容易产生较大的分子体积,从而增加其跨膜阻力进而影响其发挥生物活性。分子质量较低的多糖通常具有更多的游离羟基和更高的还原糖含量,但分子质量过小的多糖不能拥有有效活性的寡糖片段,也会使具有强活性的高级结构(如三螺旋)无法形成。因此,适当分子质量的多糖可以很容易地穿过多个细胞膜屏障,并表现出最佳的生物活性[33],这可能是BDPs-UEE表现出对ABTS阳离子自由基清除率最高的原因之一。
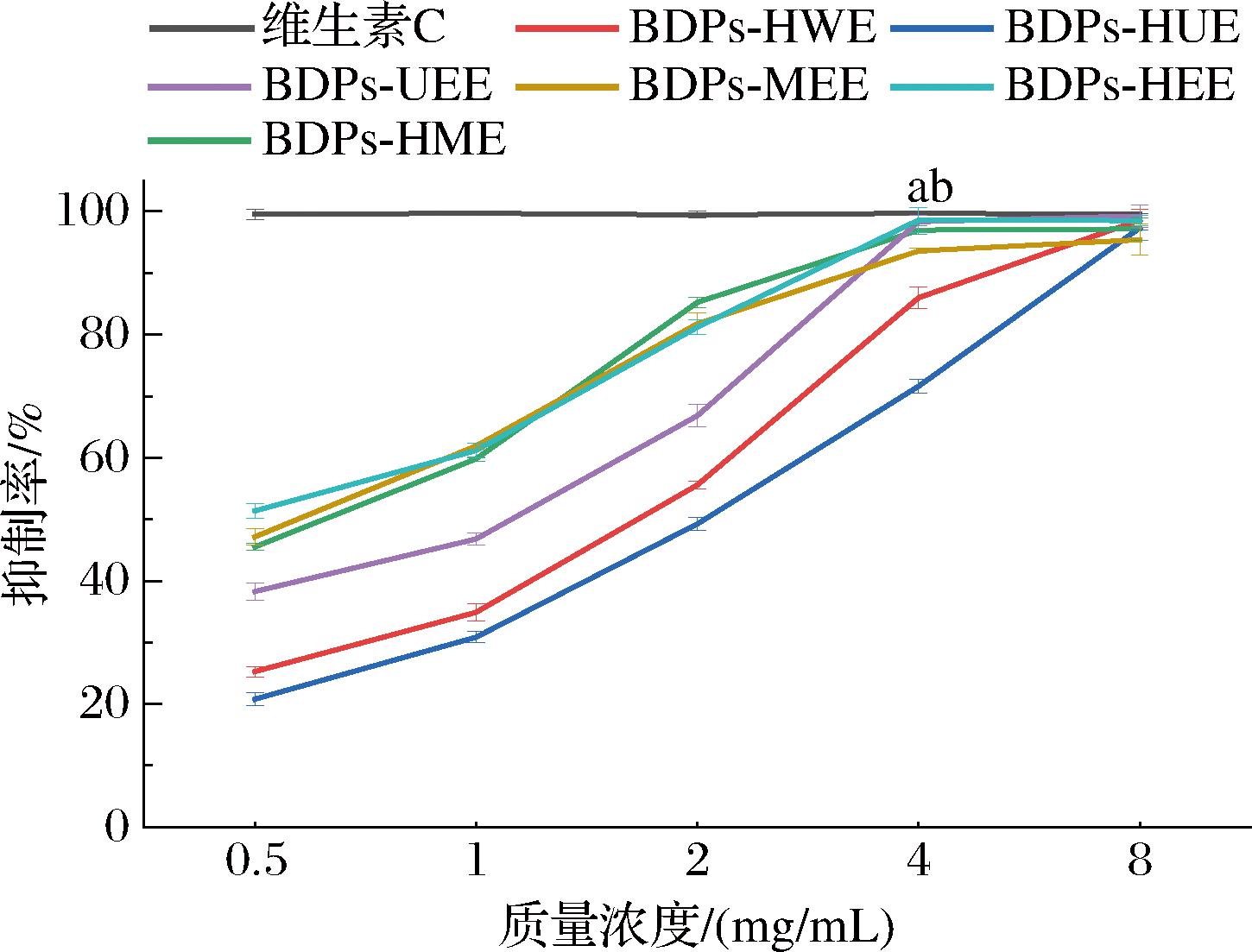
图9 不同提取方法所得BDPs及维生素C对ABTS阳离子自由基清除率比较
Fig.9 Comparison of ABTS cationic radicals scavenging rate between vitamin C and BDPs obtained by different extraction methods
2.5 不同提取方法所得BDPs对体外降血糖活性的影响
2.5.1 不同提取方法所得BDPs对α-葡萄糖苷酶抑制率的影响
由图10可知,经不同提取方法制得BDPs对α-葡萄糖苷酶有明显抑制作用,其抑制率均与浓度呈正相关且均低于阿卡波糖的抑制率(P < 0.05)。在最大质量浓度(4 mg/mL)条件下,6种BDPs对α-葡萄糖苷酶抑制均达到最优效果,其中BDPs-UEE抑制能力显著强于其余BDPs,其抑制率高达81.92%。在高质量浓度条件下(4 mg/mL)BDPs对α-葡萄糖苷酶抑制能力大小顺序为:BDPs-UEE>BDPs-HME>BDPs-HUE>BDPs-HWE>BDPs-HEE>BDPs-MEE。提取BDPs方法的不同使得其α-葡萄糖苷酶的抑制效果存在较大差异,猜测BDPs-UEE抑制效果较强的可能原因是由于超声波破坏植物细胞壁并加以酶辅助,促使细胞内容物渗出,同时加入的果胶酶能够促进BDPs的糖苷键断裂,使羟基、羧基等活性基团充分暴露。这些游离的基团能够与糖苷酶的氨基酸残基发生相互作用,竞争性地占据酶的活性位点,形成可逆性结合,从而抑制糖苷酶的催化活性,有助于降低血糖水平[34]。
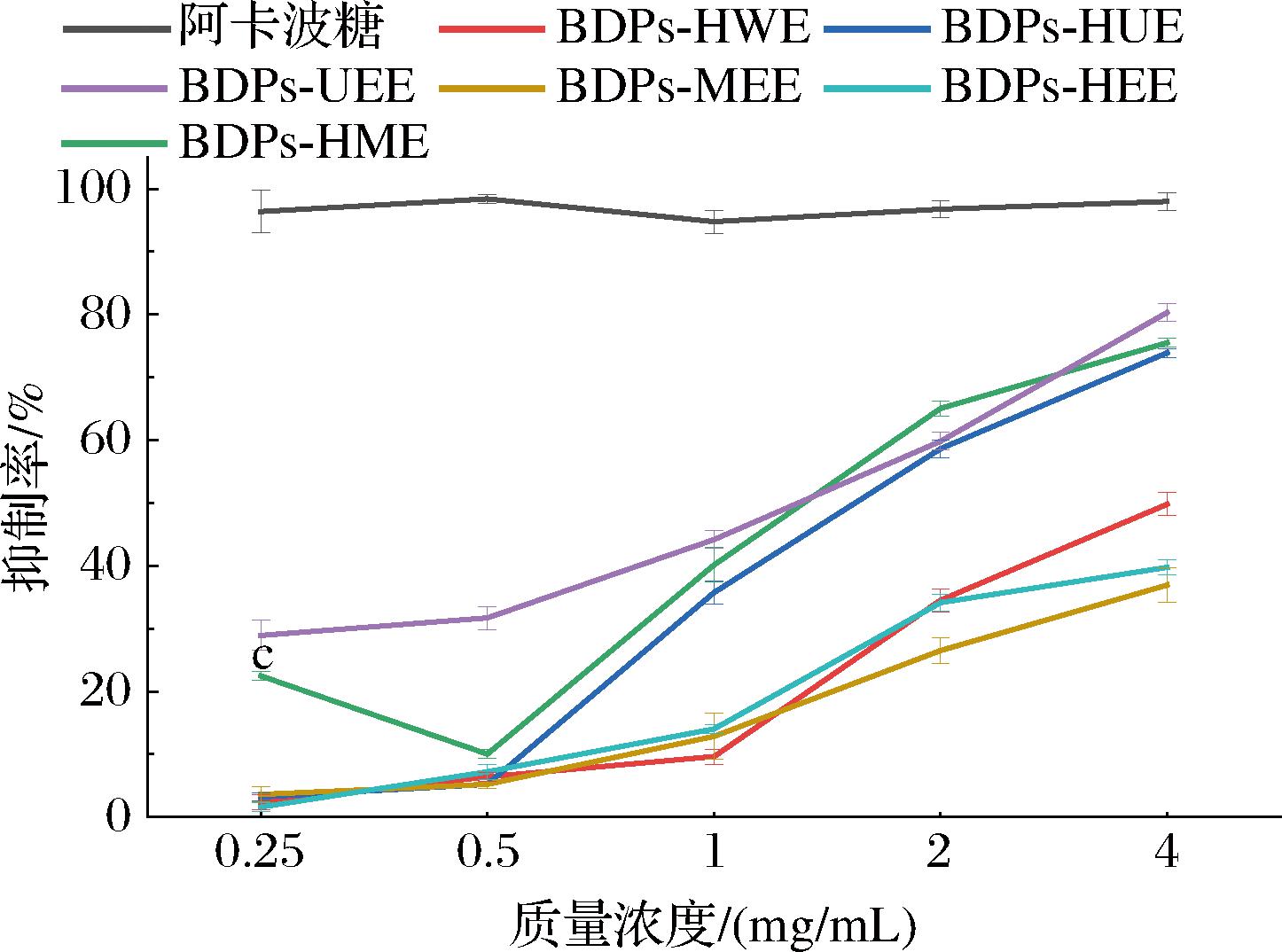
图10 不同提取方法所得BDPs及阿卡波糖对α-葡萄糖苷酶抑制率比较
Fig.10 Comparison of inhibition rate of α-glucosidase between acarbose and BDPs obtained by different extraction methods
2.5.2 不同提取方法所得BDPs对α-淀粉酶抑制率的影响
由图11可知,不同提取方法所得BDPs对α-淀粉酶存在明显抑制,整体呈现先升后降的趋势。在质量浓度处于0.125~1 mg/mL时,多糖对α-淀粉酶的抑制率呈现出随浓度升高而逐步增强的趋势。具体而言,当多糖质量浓度达到1 mg/mL时,抑制率达到峰值,其中运用超声辅助酶法提取的BDPs对α-淀粉酶的抑制率可达48.66%。随后,当质量浓度增加到1~4 mg/mL时,随着浓度的持续递增,多糖对α-淀粉酶的抑制率却转为逐渐下降的趋势。因此,判断抑制α-淀粉酶的最优多糖质量浓度为1 mg/mL。在此浓度下,BDPs-UEE抑制率最高,其次为BDPs-HUE和BDPs-HME,这三者之间差异不显著(P>0.05),且抑制率明显低于阳性对照阿卡波糖的抑制率(P<0.05),BDPs-MEE、BDPs-HEE和BDPs-HWE的抑制率依次减小,三者间差异不显著(P>0.05)。因此,采用超声并加以酶辅助提取所得多糖其降血糖效果较优。有研究表明,多糖的降血糖活性与多糖分子质量大小和单糖组成的复杂程度有着直接关系,多糖能够发挥最佳生物活性的前提是它的相对分子质量在合适的范围内,单糖组成种类越多会使得多糖具有更高降血糖活性[35],这也可能是BDPs-UEE拥有较高的降血糖活性的原因之一。
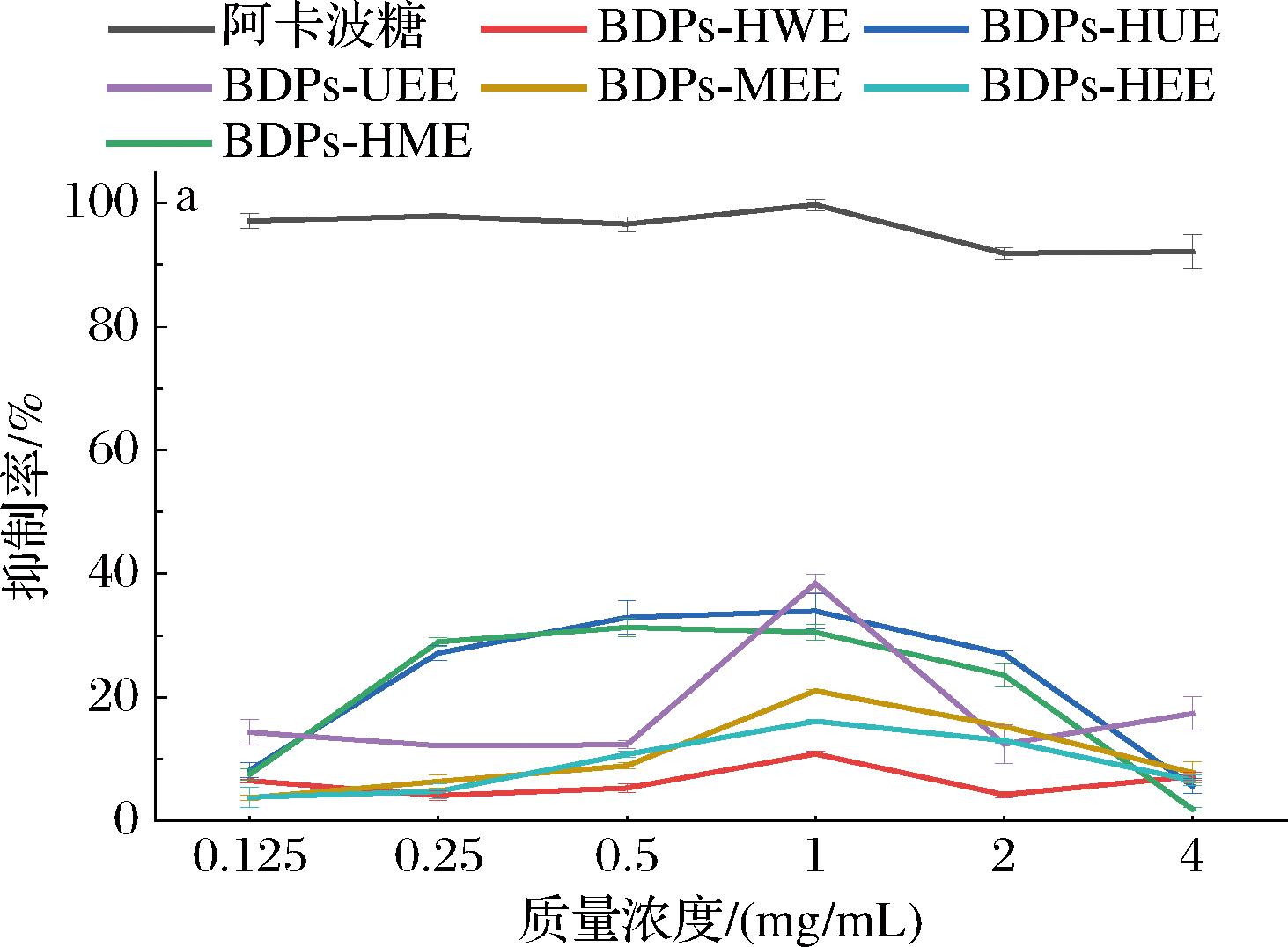
图11 不同提取方法所得BDPs及阿卡波糖对α-淀粉酶抑制率比较
Fig.11 Comparison of inhibition rate of α-amylase between acarbose and BDPs obtained by different extraction methods
3 结论
通过不同提取方法:热水浸提、超声波辅助热水浸提、微波辅助热水浸提、微波协同酶法、超声波协同酶法、热水协同酶法提取黄刺中的多糖,分别得到BDPs-HWE、BDPs-HUE、BDPs-HME、BDPs-MEE、BDPs-UEE、BDPs-HEE 6种多糖。不同提取方法对BDPs得率有显著影响(P<0.05),其中超声波协同酶法提取的BDPs得率最高,且多糖含量高达75.26%。单糖组成分析表明,6种多糖样品的单糖组成均为Fuc、Ara、Rha、Gal、Glc、Xly、Man、Glc-UA,但不同样品所含的单糖比例略有不同。红外光谱显示,6种BDPs均含有多糖的关键官能团,且多糖是以α和β糖苷键共同链接的吡喃糖构型。扫描电镜显示不同提取方法所得多糖的表观结构存在差异。抗氧化结果表明,BDPs均具有较强的自由基清除能力,呈现剂量依赖型。其中超声波协同酶法提取的BDPs具有较好的抗氧化活性,对DPPH自由基和ABTS阳离子自由基的清除率分别为89.61%和98.44%。体外降血糖实验也表明,超声波协同酶法制备的BDPs对α-葡萄糖苷酶和α-淀粉酶的活性均具有较好的抑制作用,抑制率分别为81.92%和48.66%。基于上述实验结果表明,不同提取方法对BDPs结构及生物活性有显著影响,经综合比较得出超声波协同酶法是提取BDPs的最佳方法。研究不同提取方法对BDPs理化性质及生物活性影响对于其在青藏高原特色资源的开发利用方面具有一定的参考价值,未来可进一步对该方法进行工艺优化。
[1] 邓永蓉, 韩丽娟, 岳庆明, 等.黄刺多糖工艺优化及其对过氧化氢损伤的胰岛β细胞的保护作用[J].食品与发酵工业, 2023, 49(3):146-156.DENG Y R, HAN L J, YUE Q M, et al.Optimization of extracting Berberi dasystachya polysaccharides and its protection against H2O2-induced pancreatic β cell injury[J].Food and Fermentation Industries, 2023, 49(3):146-156.
[2] 马娜娜, 韩丽娟, 杨永晶, 等.黄刺多糖对STZ诱导的Ⅰ型糖尿病大鼠糖脂代谢的调节作用[J].食品工业科技, 2024, 45(16):348-357.MA N N, HAN L J, YANG Y J, et al.Effect of Berberis dasystachya polysaccharide on glucose and lipid metabolisms in STZ-induced type Ⅰ diabetic rats[J].Science and Technology of Food Industry, 2024, 45(16):348-357.
[3] HAN L J, SUO Y R, YANG Y J, et al.Optimization, characterization, and biological activity of polysaccharides from Berberis dasystachya Maxim[J].International Journal of Biological Macromolecules, 2016, 85:655-666.
[4] 周雯, 韩丽娟, 马娜娜, 等.黄刺浆果不同组分多糖理化性质及生物活性的比较[J].食品与发酵工业, 2022, 48(2):189-197.ZHOU W, HAN L J, MA N N, et al.Comparative study on the physicochemical properties and biological activities of polysaccharides from different components in the berry of Berberi dasystachya[J].Food and Fermentation Industries, 2022,48(2):189-197.
[5] 韩丽娟, 乔杨波, 索有瑞, 等.直穗小檗果粉对STZ诱导的Ⅰ型糖尿病大鼠糖脂代谢的调节作用[J].食品工业科技, 2020, 41(4):298-306.HAN L J, QIAO Y B, SUO Y R, et al.Effect of Berberis dasystachya Maxim.fruit powder on glucose and lipid metabolisms in STZ-induced type Ⅰ diabetic rats[J].Science and Technology of Food Industry, 2020, 41(4):298-306.
[6] LIANG H Y, MA Y R, ZHAO Y, et al.A review on the extraction, structural analysis, and antitumor mechanisms of Sanghuangporus polysaccharides[J].Foods, 2025, 14(4):707.
[7] JIANG S, WU X T, SHI X P, et al.Extraction of Sanguisorba officinalis L.polysaccharide by ultrasound-assisted extraction:Structural characterization, antioxidant, hemostatic and immunological activity[J].Ultrasonics Sonochemistry, 2025, 115:107292.
[8] CHOUDHARY B, PATEL J, MISHRA A.Physicochemical, radical-scavenging, and anti-proliferative analyses of enzyme-assisted extracted polysaccharides unravel the potential of tropical green seaweeds[J].Algal Research, 2025, 87:103973.
[9] LI X Y, ZHU J S, WANG T Y, et al.Antidiabetic activity of Armillaria mellea polysaccharides:Joint ultrasonic and enzyme assisted extraction[J].Ultrasonics Sonochemistry, 2023, 95:106370.
[10] ZHAI X C, ZHU C P, LI Y, et al.Optimization for pectinase-assisted extraction of polysaccharides from pomegranate peel with chemical composition and antioxidant activity[J].International Journal of Biological Macromolecules, 2018, 109:244-253.
[11] CHEN S H, HUANG H L, HUANG G L.Extraction, derivatization and antioxidant activity of cucumber polysaccharide[J].International Journal of Biological Macromolecules, 2019, 140:1047-1053.
[12] DOU Z M, CHEN C, HUANG Q, et al.Comparative study on the effect of extraction solvent on the physicochemical properties and bioactivity of blackberry fruit polysaccharides[J].International Journal of Biological Macromolecules, 2021, 183:1548-1559.
[13] BLUMENKRANTZ N, ASBOE-HANSEN G.New method for quantitative determination of uronic acids[J].Analytical Biochemistry, 1973, 54(2):484-489.
[14] 高文军, 李卫红, 王喜明, 等.3,5-二硝基水杨酸法测定蔓菁中还原糖和总糖含量[J].中国药业, 2020, 29(9):113-116.GAO W J, LI W H, WANG X M, et al.Determination of reducing sugar and total sugar in turnip by 3,5-dinitrosalicylic acid colorimetry[J].China Pharmaceuticals, 2020, 29(9):113-116.
[15] GUO Q W, CHEN Z Q, SANTHANAM R K, et al.Hypoglycemic effects of polysaccharides from corn silk (Maydis stigma) and their beneficial roles via regulating the PI3K/Akt signaling pathway in L6 skeletal muscle myotubes[J].International Journal of Biological Macromolecules, 2019, 121:981-988.
[16] SHEN S W, ZHOU C, ZENG Y B, et al.Structures, physicochemical and bioactive properties of polysaccharides extracted from Panax notoginseng using ultrasonic/microwave-assisted extraction[J].LWT, 2022, 154:112446.
[17] TAN J Q, CUI P S, GE S Q, et al.Ultrasound assisted aqueous two-phase extraction of polysaccharides from Cornus officinalis fruit:Modeling, optimization, purification, and characterization[J].Ultrasonics Sonochemistry, 2022, 84:105966.
[18] WANG Y, LI X, ZHAO P, et al.Physicochemical characterizations of polysaccharides from Angelica Sinensis Radix under different drying methods for various applications[J].International Journal of Biological Macromolecules, 2019, 121:381-389.
[19] LYU Q Q, CAO J J, LIU R, et al.Structural characterization, α-amylase and α-glucosidase inhibitory activities of polysaccharides from wheat bran[J].Food Chemistry, 2021, 341:128218.
[20] LI J, NIU D B, ZHANG Y, et al.Physicochemical properties, antioxidant and antiproliferative activities of polysaccharides from Morinda citrifolia L.(Noni) based on different extraction methods[J].International Journal of Biological Macromolecules, 2020, 150:114-121.
[21] 方嘉沁, 郑青松, 文雨欣, 等.不同提取方法的莲子心多糖结构与理化性质比较[J].现代食品科技, 2023, 39(1):92-103.FANG J Q, ZHENG Q S, WEN Y X, et al.Comparison of the structures and physiochemical properties of polysaccharides extracted from Plumula nelumbinis by different methods[J].Modern Food Science and Technology, 2023, 39(1):92-103.
[22] JI X L, YAN Y Z, HOU C Y, et al.Structural characterization of a galacturonic acid-rich polysaccharide from Ziziphus jujuba cv.Muzao[J].International Journal of Biological Macromolecules, 2020, 147:844-852.
[23] YUAN S H, LI G L, DUAN J N, et al.Effects of five extraction methods on the physicochemical properties, antioxidant, and α-glucosidase inhibitory activities of polysaccharides from wild jujube flesh[J].Applied Food Research, 2024, 4(2):100609.
[24] 张燕. 沙棘叶多糖的酶解工艺优化、体外生物活性及理化性质研究[D].呼和浩特:内蒙古农业大学, 2024.ZHANG Y.Optimization of enzymatic hydrolysis process, functional properties and physicochemical properties of polysaccharide from Hippophae rhamnoides L. leaves[D].Hohhot:Inner Mongolia Agricultural University, 2024.
[25] DONG X D, LIU Y N, YU S S, et al.Extraction, optimization, and biological activities of a low molecular weight polysaccharide from Platycodon grandiflorus[J].Industrial Crops and Products, 2021, 165:113427.
[26] 罗世博, 热合巴提·努尔夏提, 王俊龙, 等.樱桃李多糖提取工艺优化及单糖组成与抗氧化活性测定[J].食品研究与开发, 2024, 45(20):100-107.LUO S B, NUERXIATI·R, WANG J L, et al.Optimization of polysaccharide extraction process and analysis of monosaccharide composition and antioxidant activity of Prunus cerasifera[J].Food Research and Development, 2024, 45(20):100-107.
[27] 闫晓慧, 姜思亮, 刘雪晴, 等.灵芝多糖的构效关系、提取工艺及药理作用研究进展[J].中医药学报, 2024, 52(4):117-122.YAN X H, JIANG S L, LIU X Q, et al.Research progress on structure-activity relationship, extraction technology and pharmacological action of Ganoderma lucidum polysaccharide[J].Acta Chinese Medicine and Pharmacology, 2024, 52(4):117-122.
[28] CHEN H Y, ZENG J S, WANG B, et al.Structural characterization and antioxidant activities of Bletilla striata polysaccharide extracted by different methods[J].Carbohydrate Polymers, 2021, 266:118149.
[29] 王荣琨, 王钦, 罗欣, 等.不同提取方法对竹荪多糖提取率及抗氧化性影响[J].中国食用菌, 2020, 39(3):24-28.WANG R K, WANG Q, LUO X, et al.Effects of different extraction methods on the extraction rate and antioxidant properties of Dictyophora indusiata polysaccharide[J].Edible Fungi of China, 2020, 39(3):24-28.
[30] JI X L, HOU C Y, YAN Y Z, et al.Comparison of structural characterization and antioxidant activity of polysaccharides from jujube (Ziziphus jujuba Mill.) fruit[J].International Journal of Biological Macromolecules, 2020, 149:1008-1018.
[31] 杨金涛, 信传鑫, 戴晓婧, 等.基于不同提取方法的榆黄蘑多糖构效关系[J].菌物研究, 2022, 20(3):190-197.YANG J T, XIN C X, DAI X J, et al.The relationship of Pleurotus citrinopileatus polysaccharides’ structure and activity based on different extraction methods[J].Journal of Fungal Research, 2022, 20(3):190-197.
[32] 冀晓龙, 郭建行, 田静源, 等.植物多糖降解方法及降解产物特性研究进展[J].轻工学报, 2023, 38(3):55-62.JI X L, GUO J H, TIAN J Y, et al.Research progress on degradation methods and product properties of plant polysaccharides[J].Journal of Light Industry, 2023, 38(3):55-62.
[33] ZHANG J S, CHEN X, ZHAN Q P, et al.Studying on the structure-activity relationship of Flammulina velutipes polysaccharides via ultrasonic degradation:Insights into molecular weight, chain conformation, and anti-inflammatory activity[J].International Journal of Biological Macromolecules, 2025, 302:140480.
[34] 覃引, 徐文慧, 吴凯, 等.不同提取方法对黄精多糖理化特性和生物活性的影响[J].现代食品科技, 2024, 40(3):142-152.QIN Y, XU W H, WU K, et al.Effects of the physicochemical properties and biological activities of Polygonatum sibiricum polysaccharides extracted by different extraction methods[J].Modern Food Science and Technology, 2024, 40(3):142-152.
[35] 王彤羽, 车环宇, 王欢, 等.天然多糖结构与降血糖活性作用关系的研究进展[J].粮食与食品工业, 2025, 32(2):23-28.WANG T Y, CHE H Y, WANG H, et al.Research progress on the relationship between the structure of natural polysaccharides and their hypoglycemic activity[J].Cereal &Food Industry, 2025, 32(2):23-28.