桑黄(Phellinus igniarius)作为珍贵的药用真菌,有“深林黄金”之美誉,含有多糖、黄酮、萜类、多肽等活性物质,在多种疾病的治疗中发挥着重要的药用价值[1]。桑黄多糖是桑黄的主要活性物质,具有免疫调节、抗肿瘤、降血糖、调血脂、抗炎、抗氧化、降血压、抗衰老等药理作用,受到研究者的关注[2-4]。从现有文献来看,关于桑黄多糖的研究主要集中在多糖的分离提取方法、结构鉴定、抗肿瘤、免疫调节、降血糖、抗氧化、降尿酸、抗疲劳等生物活性方面[2, 5-8]。而关于桑黄多糖的抗衰老方面的研究较少,国内只见少数几篇文献[9-14]。桑黄多糖的提取方法目前主要是热水浸提、酶解、超声和微波辅助等[15]。已有研究表明桑黄多糖的组成比较复杂,一般是由葡萄糖、半乳糖、甘露糖、鼠李糖、木糖、岩藻糖、阿拉伯糖等多种不同的单糖按照不同的摩尔比,以α-糖苷键、β-糖苷键等多种形式链接而成的具有不同空间结构和分子量的多糖分子[16-17]。由于多糖的组成和糖苷键不同使其空间结构和生物活性产生差异[17]。桑黄有效成分的提取方法和提取工艺技术条件等因素的改变,会直接影响有效成分的组成,进而影响提取物的生物活性[17]。衰老是生物体随着时间推移而逐渐发生的一系列生理功能衰退和结构改变的过程,抗衰老是减缓或阻止机体功能和结构的改变过程。自由基是导致衰老的原因之一,而清除自由基的抗氧化作用是防止生物损害的有效途径[2]。桑黄多糖的抗衰老作用主要是通过多糖自身的活性基团或通过调节细胞内超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)、谷胱甘肽过氧化物酶等抗氧化酶的合成与活性,降低丙二醛(malondialdehyde,MDA)含量,有效清除体内过多的自由基,减少自由基对细胞的破坏而延缓衰老[10]。果蝇作为一种重要的模式生物,因其培养简单,繁殖周期短等特点,已被广泛用于抗衰老研究的常用模型[10]。本文采用酶法、微波法、超声协同纤维素酶法提取桑黄多糖,通过喂饲和培养果蝇,测定不同组别果蝇组织内SOD、CAT、总抗氧化能力(total antioxidant capacity, T-AOC)、MDA等理化指标以及果蝇平均寿命、半数死亡时间和最高寿命,通过测定果蝇的抗氧化能力和果蝇寿命来评价不同方法提取的桑黄多糖的抗衰老效果,为进一步研究和开发桑黄多糖抗衰老产品提供理论依据。
1 材料与方法
1.1 材料与试剂
P.igniarius,通化十月细润生物科技有限公司;黑腹果蝇(Drosophila melanogaster),厦门慧嘉生物科技有限公司;氯仿、乙醇、乙醚、酒石酸钾钠,国药集团化学试剂有限公司;正丁醇,天津市科密欧化学试剂有限公司;苯酚,天津市福晨化学试剂厂;3,5 -二硝基水杨酸,上海源叶生物科技有限公司;NaOH,天津市光复科技发展有限公司;无水亚硫酸钠,济南世纪通达化工有限公司;葡萄糖,山东保龄宝生物股份有限公司;丙酸,南通润丰石油化工有限公司;琼脂,青岛海之林生物科技开发有限公司;蔗糖,中粮糖业控股股份有限公司;酵母粉,安琪酵母股份有限公司;玉米粉,山东鲁花集团有限公司;纤维素酶(酶活性>15 U/mg),上海源叶生物科技有限公司;木瓜蛋白酶(6×105 U/g),南宁庞博生物工程有限公司;蛋白质含量检测试剂盒,上海索桥生物有限公司;SOD检测试剂盒、T-AOC检测试剂盒、CAT检测试剂盒、MDA检测试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
L550低速离心机,常州国华电器有限公司;RE-201D 旋转蒸发仪,上海岐耀仪器设备有限公司;NAI-SYs-WBL微波炉,上海那艾精密仪器有限公司;752 N紫外可见分光光度计,上海精密科学仪器有限公司;TH-80智能恒温恒湿培养箱,广东艾思荔检测仪器有限公司;Multiskan FC酶标仪,北京澎昆博远科贸发展有限责任公司;HH.S电热恒温水浴锅,江苏省医疗器械厂;GT-2300S超声波萃取仪,深圳市固特宏业机械设备有限公司。
1.3 实验方法
1.3.1 桑黄多糖的提取与测定
1.3.1.1 酶法提取桑黄多糖
取桑黄子实体,洗净,置于烘箱内70 ℃干燥后,粉碎过40目筛,得桑黄粉末。称取1 g桑黄粉末,加水40 mL,添加木瓜蛋白酶至质量浓度为0.003 g/mL,50 ℃酶解 40 min 后,100 ℃,10 min灭酶,减压抽滤,获得滤液[18],然后浓缩至1/4体积,采用Sevage法除蛋白[V(氯仿)∶V(正丁醇)=4∶1,V(Sevage试剂)∶V(糖溶液)=1∶5],置于分液漏斗中振荡20 min后,静置15 min,放入离心机内以3 000 r/min离心10 min,取水相,重复操作2次,以1∶4体积比加入体积分数为95%的乙醇,置于4 ℃冰箱内静置过夜。次日取出后以5 000 r/min离心10 min,弃掉上清液,取得沉淀物,用无水乙醇洗至淡黄色,挥发掉乙醇,然后用蒸馏水定容至100 mL,待测。
1.3.1.2 微波法提取桑黄多糖
称取1 g桑黄粉末,加水(料液比为1∶30,g∶mL),置于480 W的微波炉内、微波处理8 min(采用微波间歇操作,微波30 s,间歇30 s)后,以3 000 r/min离心10 min得滤液,滤渣重复上述操作,合并滤液,于旋转蒸发仪中浓缩至1/4体积[19],后续处理同1.3.1.1节。
1.3.1.3 超声协同纤维素酶法提取桑黄多糖
称取1 g桑黄粉末,加水(液料比为30∶1,mL∶g),纤维素酶添加至质量浓度为0.01 g/mL,调节pH值为5.1,酶解温度50 ℃,超声波功率350 W,超声40 min后,于100 ℃水浴锅中灭酶10 min,在3 000 r/min下,离心10 min抽滤,获得滤液[20-21],后续处理同1.3.1.1节。
1.3.1.4 多糖含量测定
采用硫酸-苯酚法进行总糖含量测定,还原糖含量采用DNS法测定[18],按公式(1)计算多糖含量:
多糖含量/(mg/mL)=W总糖-W还原糖
(1)
式中:W总糖,待测样品经测定所得的多糖和还原糖含量之和,mg/mL;W还原糖,样品经测定所得的还原糖含量,mg/mL。
1.3.1.5 桑黄多糖得率测定
取1 mL提取的桑黄多糖溶液,置于15 mL具塞试管中按照多糖测定方法测定,按公式(2)计算桑黄多糖得率:
桑黄多糖得率![]()
(2)
式中:ρ,多糖样品质量浓度,mg/mL;V,多糖样品体积,mL;W,桑黄粉末质量,mg。
1.3.2 果蝇寿命及半数死亡时间测定
将羽化10 h内的果蝇用乙醚麻醉后分成4组,即空白对照组(A)、酶法多糖组(B)、微波法多糖组(C)与超声协同纤维素酶法多糖组(D),每组均设雌雄2个小组,雌雄分别30只,各做3个重复。空白对照组饲养在基本培养基内,其他3组分别向100 mL基础培养基中加入20 g采用不同提取方法提取到的桑黄多糖粉末。置于25 ℃,相对湿度50%~60%的恒温培养箱中培养,每3 d 换1次培养基。每天统计果蝇的死亡数,直至果蝇全部死亡为止,计算每组平均寿命。
半数死亡时间:每组中前半数果蝇存活时间的平均数为半数死亡时间。
最高寿命:每组最后死亡的10只果蝇的寿命。
1.3.3 抗衰老能力的测定
按1.3.2节方法,将4个组的果蝇培养30 d后,将果蝇先饥饿处理2 h,再用乙醚麻醉,按1∶49的体积比加入生理盐水,在冰浴下匀浆后,4 ℃,3 500 r/min 离心15 min取上清液,制得匀浆,移至新管中,在-80 ℃冰箱中,冷冻保存。采用二喹啉甲酸(bicinchoninic acid,BCA)法测定蛋白质含量,羟胺法测定SOD活性,钼酸铵法测CAT活性,铁还原抗氧化能力(ferric reducing antioxidant power,FRAP)法测定T-AOC,硫代巴比妥酸(thiobarbituric acid,TBA)法测定MDA的含量,具体方法根据试剂盒的操作说明完成,每组设置3次重复。
1.3.3.1 蛋白质含量测定
在碱性环境下,蛋白质分子中的肽键结构会与Cu2+络合,将Cu2+还原成Cu+。BCA能够特异地与Cu+结合,形成稳定的紫蓝色复合物,在562 nm处有最大的光吸收值A,颜色的深浅与蛋白质的含量成正比,可以根据吸收值测定蛋白质浓度,按公式(3)计算蛋白质含量:
蛋白质含量![]()
(3)
式中:A测定管,含有样品的溶液的吸光度值;A空白管,以蒸馏水替代样品的溶液的吸光度值;A标准管,含有标准品蛋白的溶液的吸光度值;C标,蛋白标准品的溶液质量浓度,mg/mL。
1.3.3.2 SOD活性测定
通过黄嘌呤及黄嘌呤氧化酶反应系统产生超氧阴离子自由基![]() 后者氧化羟胺形成亚硝酸盐,在显色剂的作用下呈现紫红色,在波长530 nm处有最大吸收峰,用分光光度计测其吸光值。通过公式(4)计算,可求出被测样品中的SOD活性。
后者氧化羟胺形成亚硝酸盐,在显色剂的作用下呈现紫红色,在波长530 nm处有最大吸收峰,用分光光度计测其吸光值。通过公式(4)计算,可求出被测样品中的SOD活性。
SOD活性定义:每毫克组织蛋白在1 mL反应液中SOD抑制率达50%时所对应的SOD量为1个SOD活性单位,单位U/mg prot。
组织匀浆中SOD活性![]()
(4)
式中:A测定管,含样品的溶液的吸光度值;A对照管,以等量蒸馏水替代样品的溶液的吸光度值;V总,反应液总体积,按试剂盒说明书添加各试剂后的溶液总体积,mL;V样,样品添加到反应体系中的体积量,mL;C样蛋白,待测样品的蛋白浓度,毫克蛋白数(mg prot/mL)。
1.3.3.3 CAT活性测定
过氧化氢酶分解H2O2的反应可通过加入钼酸铵而迅速中止,剩余的H2O2与钼酸铵作用产生一种淡黄色络合物,在405 nm处有吸收峰,测定其吸光值,可按公式(5)计算出CAT的活性。
CAT活性定义:每毫克组织蛋白每秒种分解1 μmol 的H2O2的量为一个活力单位,单位U/mg prot。
组织匀浆中CAT活性/(U/mg prot)
(5)
式中:A测定管,含样品的溶液的吸光度值;A对照管,以等量蒸馏水替代样品的溶液的吸光度值;271,斜率的倒数;V样,样品添加到反应体系中的体积量,mL;C样蛋白,待测样品的蛋白浓度,毫克蛋白数(mg prot/mL)。
1.3.3.4 T-AOC测定
生物体中有许多抗氧化物质能使Fe3+还原成Fe2+,后者可与菲啉类物质形成稳定的螯合物,在520 nm处有吸收峰,通过测定其吸光值,可以按公式(6)计算其抗氧化能力的高低。
单位定义:样本的抗氧化能力以达到同样吸光度变化值(ΔA)所需的标准液离子浓度(μmol/mL)表示,单位μmol/mg prot。
总抗氧化能力![]()
(6)
式中:C,待测样品的Fe2+的浓度,按照试剂盒说明书根据测定的吸光度值从标准曲线测得;V反总,添加各试剂后的溶液总体积,mL;V样,样品添加到反应体系中的量,mL;Cpr,待测样品蛋白浓度,mg/mL。
1.3.3.5 MDA含量测定
在酸性和高温的条件下,MDA可与TBA反应生成红棕色的3,5,5-三甲基恶唑-2,4-二酮,在532 nm处有最大吸光值,根据公式(7)计算出MDA含量:
组织匀浆中MDA含量/(nmol/mg prot)
(7)
式中:A测定管,按说明书添加样品和试剂一、二、三的试管中的溶液的吸光度值;A测定空白管,不加试剂三溶液,其他试剂成分与测定管试剂相同的试管中溶液的吸光度值;A标准管,加标准品和试剂一、二、三的试管中的溶液的吸光度值;A标准空白管,以无水乙醇替代标准品,其他试剂与标准管试剂相同的试管中的溶液的吸光度值;C标,标准品蛋白浓度,nmol/mL;C样,待测样品蛋白浓度,毫克蛋白数(mg prot/mL)。
1.4 数据处理
使用SPSS软件及Excel软件对实验数据进行统计学分析,实验结果采用“平均值±标准差”方式记录。
2 结果与分析
2.1 不同方法提取的桑黄多糖得率
经测定得葡萄糖标准曲线回归方程为:Y=14.181X+0.004 7,R2=0.999 4,葡萄糖浓度与吸光值呈良好的线性关系,测得酶法、微波法及超声协同纤维素酶法3种不同提取方法提取到的桑黄多糖得率分别为1.5%、3.2%、5.1%,多糖得率之间存在显著差异(P<0.01),超声协同纤维素酶法提取的桑黄多糖得率最高。
2.2 不同方法提取的桑黄多糖对果蝇寿命的影响
不同方法提取的桑黄多糖对果蝇寿命的影响实验结果如表1所示。
表1 不同方法提取的桑黄多糖对果蝇寿命的影响 单位:d
Table 1 Effects of polysaccharides extracted by different methods on the lifespan of D.melanogaster
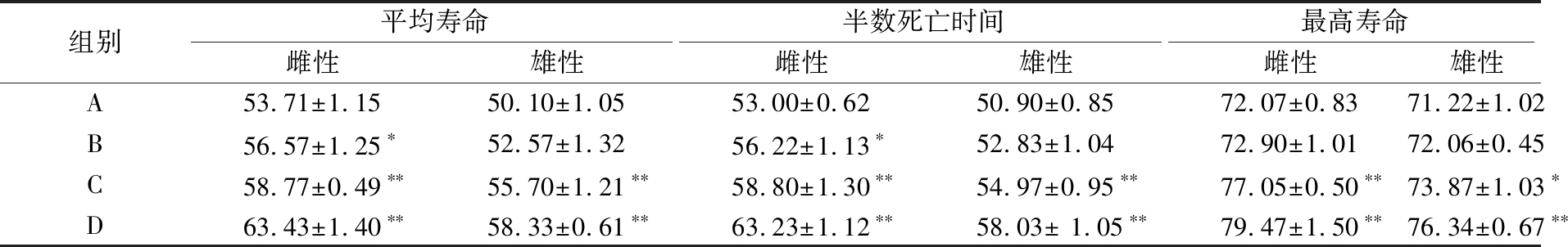
注:P<0.05为差异显著,以*表示;P<0.01为差异极显著,以**表示(下同)。
组别平均寿命半数死亡时间最高寿命雌性雄性雌性雄性雌性雄性A53.71±1.1550.10±1.0553.00±0.6250.90±0.8572.07±0.8371.22±1.02B56.57±1.25∗52.57±1.3256.22±1.13∗52.83±1.0472.90±1.0172.06±0.45C58.77±0.49∗∗55.70±1.21∗∗58.80±1.30∗∗54.97±0.95∗∗77.05±0.50∗∗73.87±1.03∗D63.43±1.40∗∗58.33±0.61∗∗63.23±1.12∗∗58.03± 1.05∗∗79.47±1.50∗∗76.34±0.67∗∗
由表1可知,由酶法、微波法及超声协同纤维素酶法分别提取到的桑黄多糖喂养的B、C、D三组果蝇与对照组A相比,它们的雌性果蝇的平均寿命分别延长了5.32%、9.42%、18.09%,雄性果蝇的平均寿命分别延长了4.93%、11.17%、16.42%;雌性果蝇的半数死亡时间比对照组A分别延长了6.07%、10.94%、19.30%,雄性果蝇的半数死亡时间比对照组A分别延长了3.79%、7.80%、14.00%;雌蝇的最高寿命比对照组A分别延长了1.15%、6.9%、10.27%,雄蝇的最高寿命比对照组A分别延长了1.18%、3.72%、7.19%。其中微波法和超声协同纤维素酶法提取到的桑黄多糖喂养的C、D两组果蝇,与对照组A相比,其延长雌、雄性果蝇的平均寿命,半数死亡时间及最高寿命的效果均有显著或极显著差异(P<0.05或P<0.01)。
用酶法提取到的桑黄多糖喂养的B组果蝇,其延长雌性果蝇的平均寿命和半数死亡时间效果显著(P<0.05),而对于雄性果蝇的平均寿命、半数死亡时间及最高寿命的延长效果不明显。3种不同方法提取到的桑黄多糖都可以不同程度地提高果蝇寿命,且对雌性果蝇的效果较好,其中超声协同纤维素酶法效果最佳。
2.3 不同方法提取的桑黄多糖对果蝇抗衰老指标的影响
2.3.1 不同方法提取的桑黄多糖对果蝇组织内SOD活性的影响
不同方法提取的桑黄多糖对果蝇组织内SOD活性影响的实验结果如表2所示。
表2 不同方法提取的桑黄多糖对果蝇SOD活性的影响 单位:U/mg prot
Table 2 Effects of polysaccharides extracted by different methods on SOD activity of D.melanogaster
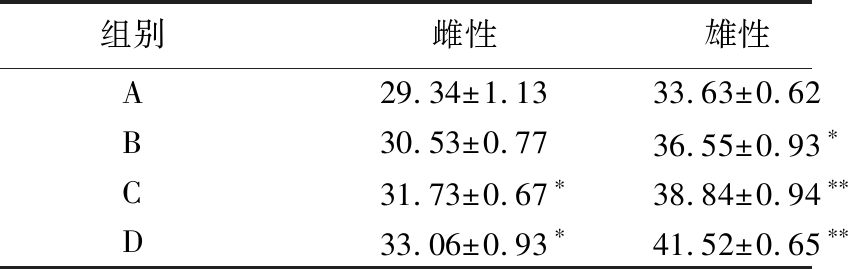
组别雌性雄性A29.34±1.1333.63±0.62B30.53±0.7736.55±0.93∗C31.73±0.67∗38.84±0.94∗∗D33.06±0.93∗41.52±0.65∗∗
由表2可知,由酶法、微波法及超声协同纤维素酶法提取到的桑黄多糖喂养的B、C、D三组果蝇,雌性果蝇组织内SOD活性比照组A分别提高了4.06%、8.15%、12.68%;雄性果蝇组织内SOD活性与对照组A相比分别提高了8.68%、15.49%、23.46%。其中,用酶法提取的桑黄多糖喂养的B组雌性果蝇组织内的SOD活性与对照组A相比,无显著差异。采用微波法及超声协同纤维素酶法提取到的桑黄多糖喂养的C、D两组雌蝇组织内SOD活性与对照组A相比差异显著(P<0.05);用酶法提取的桑黄多糖喂养的B组雄性果蝇,组织内的SOD活性与对照组A相比差异显著(P<0.05);微波辅助法及超声协同纤维素酶法提取的桑黄多糖喂养的C、D两组雄性果蝇,组织内SOD活性与对照组A相比,差异极显著(P<0.01)。3种方法提取的桑黄多糖都能提高果蝇组织内的SOD活性,其中超声协同纤维素酶法效果最佳。
2.3.2 不同方法提取的桑黄多糖对果蝇组织内CAT活性的影响
不同方法提取的桑黄多糖对果蝇组织内CAT活性的影响实验结果如表3所示。
表3 不同方法提取的桑黄多糖对果蝇CAT活性的影响 单位:U/mg prot
Table 3 Effects of polysaccharides extracted by different methods on CAT activity of D.melanogaster
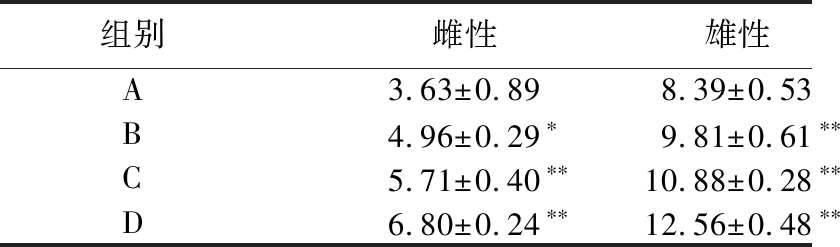
组别雌性雄性A3.63±0.898.39±0.53B4.96±0.29∗9.81±0.61∗∗C5.71±0.40∗∗10.88±0.28∗∗D6.80±0.24∗∗12.56±0.48∗∗
由表3可知,由酶法、微波法及超声协同纤维素酶法提取的桑黄多糖喂养的B、C、D三组果蝇的CAT活性与对照组A相比,雌性果蝇组织内CAT活性分别提高了36.64%、57.3%、87.32%;雄性果蝇组织内CAT活性比对照组A分别提高了16.92%、29.68%、49.7%。其中用酶法提取的桑黄多糖喂养的B组雌性果蝇组织内的CAT活性与对照组A有显著差异(P<0.05),用微波法及超声波协同纤维素酶法提取的桑黄多糖喂养的C、D两组雌性果蝇组织内CAT活性与对照组A相比,差异极显著(P<0.01);用3种不同方法提取的桑黄多糖喂养的B、C、D三组雄性果蝇组织内CAT活性与对照组A相比,均有极显著差异(P<0.01)。3种方法提取的桑黄多糖都能提高果蝇组织内的CAT活性,其中超声协同纤维素酶法效果最佳。
2.3.3 不同方法提取的桑黄多糖对果蝇组织内T-AOC的影响
不同方法提取的桑黄多糖对果蝇组织内T-AOC影响的实验结果如表4所示。
表4 不同方法提取的桑黄多糖对果蝇T-AOC的影响 单位:μmol/mg prot
Table 4 Effects of different extraction methods on T-AOC of D.melanogaster
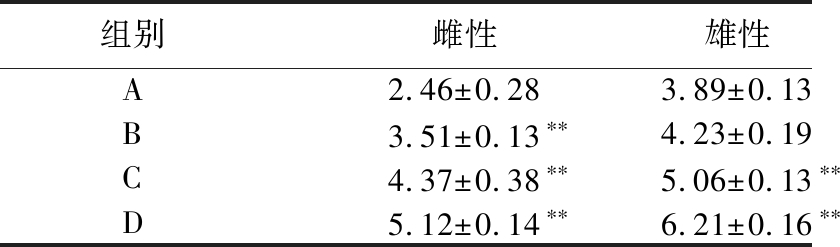
组别雌性雄性A2.46±0.283.89±0.13B3.51±0.13∗∗4.23±0.19C4.37±0.38∗∗5.06±0.13∗∗D5.12±0.14∗∗6.21±0.16∗∗
由表4可知,由酶法、微波法及超声协同纤维素酶法提取的桑黄多糖喂养的B、C、D三组果蝇,雌性果蝇组织内T-AOC与对照A组相比分别提高了42.68%、77.64%、108.12%;雄性果蝇组织内T-AOC与对照组A相比分别提高了8.74%、30.08%、59.64%。其中,3种不同方法提取的桑黄多糖喂养的B、C、D三组雌性果蝇,组织内T-AOC与对照组A相比,均有极显著差异(P<0.01);用酶法提取的桑黄多糖喂养的B组雄性果蝇,组织内的T-AOC与对照组A相比,无显著差异;用微波法及超声波协同纤维素酶法提取到的桑黄多糖喂养的C、D两组雄性果蝇组织内T-AOC与对照组A相比,存在极显著差异(P<0.01);用酶法、微波法及超声协同纤维素酶法提取的桑黄多糖都能提高果蝇组织内T-AOC,其中超声协同纤维素酶法效果最佳。
2.3.4 不同方法提取的桑黄多糖对果蝇组织内MDA含量的影响
不同方法提取的桑黄多糖对果蝇体内MDA含量影响的实验结果如表5所示。
表5 不同方法提取的桑黄多糖对果蝇MDA含量的影响 单位:nmol/mg prot
Table 5 Effects of polysaccharides extracted by different methods on MDA content of D.melanogaster
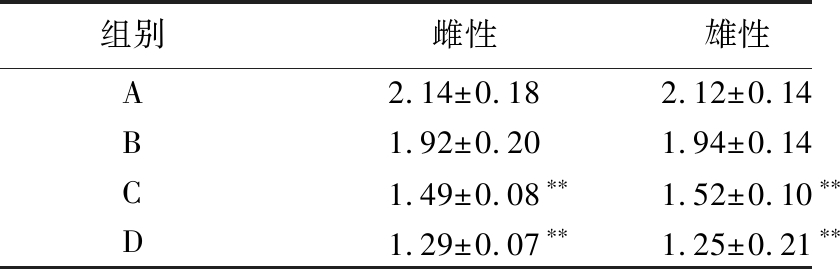
组别雌性雄性A2.14±0.182.12±0.14B1.92±0.201.94±0.14C1.49±0.08∗∗1.52±0.10∗∗D1.29±0.07∗∗1.25±0.21∗∗
由表5可知,由酶法、微波法及超声协同纤维素酶法提取的桑黄多糖喂养的B、C、D三组果蝇,雌性果蝇组织内MDA含量分别降低了10.28%、30.37%、39.71%;雄性果蝇组织内MDA含量与对照A相比分别降低了8.49%、28.30%、41.04%。其中用酶法提取的桑黄多糖喂养的B组雌、雄果蝇组织内的MDA含量与对照组A相比,无显著差异;用微波法及超声协同纤维素酶法提取的桑黄多糖喂养的C、D两组雌雄性果蝇组织内MDA含量与对照组相比,存在极显著差异(P<0.01);用微波法及超声协同纤维素酶法提取的桑黄多糖均能降低组织内MDA含量,其中超声协同纤维素酶法效果最佳。
3 讨论
衰老是机体在发育成熟后,随年龄增加由多种因素引起的体内各项功能活动进行性下降,内环境稳定能力与应激能力下降,结构、组分逐步退行性变,趋向死亡的不可逆转的复杂生物学过程,是必然的生命现象[9, 22]。关于衰老的机制目前尚未完全清楚,能够解释衰老的学说很多,其中最主要的学说是自由基学说。自由基学说认为正常机体内的自由基是处于平衡的状态,过量自由基可造成机体细胞非特异性氧化损伤,加速衰老,进一步发展会导致多种疾病和癌变发生[23-24]。如果机体的抗氧化能力较弱,会导致组成体内细胞受到自由基的攻击,从而引起细胞损伤,并导致机体快速衰老[9]。研究发现桑黄多糖具有较好的清除超氧阴离子自由基、羟自由基和DPPH自由基的能力,主要是桑黄多糖可以通过提高体内的SOD、CAT的活性、T-AOC,减少MAD含量来促进活性氧的产生,以增强抗氧化能力和延缓衰老[1,7,24]。桑黄多糖结构较为复杂,受限于生长环境、品种的特性、提取方法及介质等诸多因素的影响[17],由于桑黄多糖一般是由葡萄糖、半乳糖、甘露糖等单糖通过α-糖苷键和β-糖苷键按照不同方式链接成具有独特空间结构和不同分子量及不同支链或直链的糖分子,因此具有不同的生物活性。一般情况是α-糖苷键对酸性和热环境不够稳定,而β-糖苷键对酸性和热环境有较好的稳定性。同时组成多糖的不同糖苷键对不同的酶也有不同的敏感度。由于多糖的糖苷键、聚合度、空间结构不同等原因,使之对冷热、酸碱、酶解、压力等环境的耐受力不同,因此,不同的提取方法会导致多糖结构和生物活性产生差异[7,25-26]。本研究结果显示,超声协同纤维素酶法提取的多糖喂饲的果蝇平均寿命、半数死亡时间和最高寿命都是最高的,其SOD、CAT活性、T-AOC最高,MDA含量最少,与对照组有显著差异。在实验的3种多糖提取方法中,超声协同纤维素酶法提取的多糖的抗氧化、抗衰老能力最佳,其他2种提取方法获得的多糖也有一定的抗氧化、抗衰老作用。这可能是由于酶法和微波法在提取多糖过程中多糖本身的空间结构或单体的聚合度受到了一定程度的影响,导致生物活性降低。但对多糖结构是如何受到影响的,还需要进一步深入研究。本文研究结果验证了文献[7]不同提取方法的多糖抗氧化能力不同的观点,研究结果与文献[1,7,24]报道的研究结果一致,桑黄多糖可以增加生物体内的SOD、CAT活性,降低MDA含量,具有明显的抗氧化和抗衰老能力。本研究结果显示,尽管桑黄多糖对雌、雄性果蝇体内的SOD活性、CAT活性、T-AOC及MDA水平不均衡,但桑黄多糖对果蝇寿命的影响表现出性别差异,多糖对雌性果蝇的平均寿命、半数死亡时间和最高寿命指标的增加优于雄性果蝇。这可能是由于机体内激素种类不同、机体组织脂质过氧化成分差异、性别基因等原因导致。衰老是一个多因素参与的复杂过程,抗氧化酶和MDA水平的高低并不能完全决定寿命的长短,而体内自由基的平衡被打破才是影响寿命的重要因素[27]。REGAN等[28]的研究结果也证实了衰老的性别差异性,雌性果蝇的寿命长于雄性。
4 结论
桑黄多糖具有较好的抗氧化、抗衰老能力,但其活性大小因提取方法的不同而不同。酶法、微波法和超声协同纤维素酶法提取的桑黄多糖都具有一定的抗氧化、延长果蝇衰老的作用,其中超声协同纤维素酶法提取的桑黄多糖的抗衰老能力是3种方法中最有效的。桑黄多糖可以延长果蝇寿命,其延长雌性果蝇的寿命优于雄性果蝇。本研究为进一步开发具有抗氧化、抗衰老能力的桑黄多糖产品提供了理论依据。
[1] 荣丹, 唐梦瑜, 么越, 等.桑黄活性物质提取分离及药理作用研究进展[J].中国食用菌, 2022,41(6):1-6.RONG D, TANG M Y, YAO Y, et al.Research progress on extraction, separation and pharmacological action of the active substances from Sanghuang[J].Edible Fungi of China, 2022,41(6):1-6.
[2] 石河, 梅景晨, 李荣雪, 等. 桑黄多糖的提取分离及药理作用研究进展[J]. 2023(6):1360-1368.SHI H, MEI J C, LI R X, et al. Research progress on extraction, separation and pharmacological action of Phellinus igniarius polysaccharide[J]. Drug Evaluation Research, 2023(6):1360-1368.
[3] CHEN H, TIAN T, MIAO H, et al.Traditional uses, fermentation, phytochemistry and pharmacology of Phellinus linteus:A review[J].Fitoterapia, 2016,113:6-26.
[4] 杨焱, 陈晓华, 戴玉成, 等.我国桑黄产业发展现状、问题及展望:桑黄产业发展千岛湖宣言[J].菌物学报, 2023,42(4):855-873.YANG Y, CHEN X H, DAI Y C, et al.Sanghuang industry in China:Current status, challenges and perspectives:The Qiandao Lake declaration for Sanghuang industry development[J].Mycosystema, 2023,42(4):855-873.
[5] 谢存一, 周禹佳, 张疏雨, 等.桑黄活性成分研究及行业发展分析[J].食用菌, 2023,45(3):1-5.XIE C Y, ZHOU Y J, ZHANG S Y, et al.Study on active ingredients of Phellinus igniarius and analysis of its industry development[J].Edible Fungi, 2023,45(3):1-5.
[6] 刘锦程, 弓志青, 杨鹏, 等.桑黄营养成分、活性成分及多糖性质分析[J].食品工业科技, 2023,44(22):241-248.LIU J C, GONG Z Q, YANG P, et al.Analysis of nutritional components, active components and polysaccharide properties of Phellinus igniarius[J].Science and Technology of Food Industry, 2023,44(22):241-248.
[7] 范祺, 吴茂玉, 张博华, 等.桑黄的主要活性成分及国内外研究进展[J].中国果菜, 2022,42(11):50-55.FAN Q, WU M Y, ZHANG B H, et al.Main active components of Phellinus linteus and its domestic and international research progress[J].China Fruit &Vegetable, 2022,42(11):50-55.
[8] 于秋菊. 桑黄多糖提取、分离、结构解析及药理作用研究进展[J].山东化工, 2022,51(13):68-69;72.YU Q J.Research progress in extraction, isolation, structure analysis and pharmacological action of polysaccharide from Phellinus igniarius[J].Shandong Chemical Industry, 2022,51(13):68-69;72.
[9] 汪雯翰, 张劲松, 杨焱, 等.桑黄等十种食药用菌抗氧化和延缓衰老功效的比较研究[J].天然产物研究与开发, 2013,25(8):1027-1032.WANG W H, ZHANG J S, YANG Y, et al.A comparative study on antioxidant and anti-aging activities of ten edible/medicinal fungi[J].Natural Product Research and Development, 2013,25(8):1027-1032.
[10] 郑媛, 沈业寿.桑黄胞内多糖抗衰老作用的研究[J].中国食用菌, 2006,25(3):38-41.ZHENG Y, SHEN Y S.Study on the effect of anti- senility of intracellular polysaccharide from Phellinus igniarius[J].Edible Fungi of China, 2006,25(3):38-41.
[11] 吴娜. 桑黄子实体中抗衰老化合物的筛选及作用机制的初步探究[D].上海:上海师范大学, 2013.WU N.Screening the anti-aging active compounds from the fruiting of Phellinus baumii and study on their mechanism of active compounds[D].Shanghai:Shanghai Normal University,2013.
[12] 谷丽丽, 蔡为明, 金群力, 等.桑黄水煎液对D-半乳糖衰老模型小鼠的抗氧化作用[J].中国现代应用药学, 2019,36(17):2144-2148.GU L L, CAI W M, JIN Q L,et al.Effect of Sanghuang decoction on oxidative damage induced by D-galactose in mice[J].Chinese Journal of Modern Applied Pharmacy, 2019,36(17):2144-2148.
[13] 葛斌,许爱霞,杨社华.黄芪多糖抗衰老作用机制的研究[J].中国医院药学杂志, 2004,24(10):610-612.GE B, XU A X, YANG S H.Study on the effect and its mechanism of action of anti-senility of PRASH[J].Chinese Journal of Hospital Pharmacy, 2004,24(10):610-612.
[14] 侯立娟, 卯明娟, 刘迪, 等.杨树桑黄水提液对果蝇寿命和繁殖力及寿命相关基因的影响[J].食用菌学报, 2023,30(6):86-91.HOU L J MAO M J, LIU D, et al.Effect of Sanghuangporus vaninii water extract on life span, fecundity and life span-related genes of Drosophila melanogaster[J].Acta Edulis Fungi, 2023,30(6):86-91.
[15] 于秋菊, 孙科, 耿凤英.超声辅助低共熔溶剂提取桑黄多糖及其抗氧化活性[J].食品研究与开发, 2023,44(5):81-88;105.U Q J,SUN K,GENG F Y.Ultrasound-assisted deep eutectic solvent-based extraction of polysaccharides from Phellinus igniarius and its antioxidant activities[J].Food Research and Development, 2023,44(5):81-88;105.
[16] 李彦颖,张祺, 陈晓华, 等.桑黄多糖的分离纯化、生物活性及其产品开发研究进展[J].食药用菌, 2022,30(1):26-31;61.LI Y Y, ZHANG Q, CHEN X H, et al.Research progress in purification, bio-activity and product development of polysaccharides from Sanghuangporus[J].Edible and Medicinal Mushrooms, 2022,30(1):26-31;61.
[17] 徐雯雯, 陆春霞, 肖潇, 等.桑黄多糖的提取纯化技术及药理作用研究进展[J].蚕学通讯, 2022,42(3):20-30.XU W W, LU C X, XIAO X, et al.Research progress on the extraction and purification technology and pharmacological effects of polysaccharides from Sanghuangporus[J].Newsletter of Sericultural Science, 2022,42(3):20-30.
[18] 史玉宝, 白卫东, 赵文红, 等.酶解辅助提取桑黄粗多糖的工艺优化[J].农产品加工, 2019(18):29-32;35.SHI Y B, BAI W D, ZHAO W H, et al.Optimization of enzymatic hydrolysis-assisted extraction of polysaccharides from Phellinus igniarius[J].Farm Products Processing, 2019(18):29-32;35.
[19] 郭树凡, 蔡天革, 李辉, 等.微波辅助提取桑黄多糖的工艺研究[J].特产研究, 2008,30(1):22-25.GUO S F, CAI T G,LI H, et al.Microwave-assisted technology for extracting polysaccharide from Phellinus igniarius FruitBodys[J].Special Wild Economic Animal and Plant Research, 2008,30(1):22-25.
[20] 程俊文, 贺亮, 魏海龙, 等. 超声波协同复合酶法提取桑黄多糖工艺优化[J]. 2017(4):33-38.CHENG J W, HE L, WEI H L, et al. Optimization of extraction technology of Phellinus igniarius polysaccharide by ultrasonic wave combined with compound enzyme method[J]. Journal of Zhejiang Forestry Science and Technology, 2017(4):33-38.
[21] 刘安军, 陈伟伟, 王稳航, 等.桑黄(Phellinus linteus)水溶多糖提取技术研究[J].食品研究与开发, 2006, 27(10):32-35.LIU A J, CHEN W W, WANG W H, et al.Optimization extraction of polysaccharide from Phellinus linteus[J].Food Research and Development, 2006, 27(10):32-35.
[22] 苏路路, 管博文, 樊飞跃, 等.衰老细胞清除剂研究进展[J].中国药理学通报, 2019,35(10):1333-1337.SU L L, GUAN B W, FAN F Y, et al.Development of senolytics for selectively elimination of senescent cells[J].Chinese Pharmacological Bulletin, 2019,35(10):1333-1337.
[23] 薛立英, 高丽, 秦雪梅, 等. 药食同源中药抗衰老研究进展[J]. 食品科学, 2017, 38(15):302-309.XUE L Y, GAO L, QIN X M, et al. Research progress on anti-aging of traditional Chinese medicine with homology of medicine and food[J]. Food Science, 2017, 38(15):302-309.
[24] 王豪, 钱坤, 司静, 等.桑黄类真菌多糖研究进展[J].菌物学报, 2021,40(4):895-911.WANG H, QIAN K, SI J, et al.Research advances on polysaccharides from Sanghuang[J].Mycosystema, 2021,40(4):895-911.
[25] KOZARSKI M, KLAUS A, NIKSIC M, et al.Antioxidative and immunomodulating activities of polysaccharide extracts of the medicinal mushrooms Agaricus bisporus, Agaricus brasiliensis, Ganoderma lucidum and Phellinus linteus[J].Food Chemistry, 2011,129(4):1667-1675.
[26] 于艳杰, 王芳芳, 马红红, 等.桑黄生物活性成分及药理作用研究进展[J].特种经济动植物, 2022,25(10):94-99.YU Y J,WANG F F, MA H H, et al.Research progress on bioactive components and pharmacological effects of Phellinus igniarius[J].Special Economic Animals and Plants, 2022,25(10):94-99.
[27] 张欣文, 徐思红, 厉曙光.果蝇体内SOD和MDA随增龄变化及其与寿命的关系[J].中国公共卫生, 2000,16(3):222-223.ZANG X W, XU S H, LI S G.Effect of age-dependent variation of superoxide dismutse activity and malonaldehyde contents on life-span in Drosophila[J].China Public Health,2000,16(3):222-223.
[28] REGAN J C, LU Y X, URE A E, et al.Sexual identity of enterocytes regulates autophagy to determine intestinal health, lifespan and responses to rapamycin[J].Nature Aging,2022, 2(12):1145-1158.
A E, et al.Sexual identity of enterocytes regulates autophagy to determine intestinal health, lifespan and responses to rapamycin[J].Nature Aging,2022, 2(12):1145-1158.