枸杞(Lycium barbarum)是茄科的一个属[1],主要种植于我国西北地区,分为红枸杞、黑枸杞和黄枸杞。枸杞作为一种药用和食用水果,含有多酚、生物碱和多糖等各种生物活性成分[2],使枸杞具有多种健康益处,如抗氧化、抗炎、抗菌、免疫刺激、抗糖尿病、神经保护、抗癌、益生元和抗肥胖作用等[3]。成熟、新鲜的枸杞果实含水率高达80%左右,果实含糖量高,对微生物变质敏感,在采收和贮藏过程中易腐烂[4-5]。因此,收获后的新鲜枸杞必须及时加工或脱水至安全含水量,方便后续的运输、贮存和加工。枸杞产品种类丰富,广泛应用于食品、保健品、药品和化妆品等领域,主要包括枸杞原浆、枸杞酒、枸杞果糕、枸杞面膜等,但枸杞干仍然是最受欢迎的产品,目前市场上80%的枸杞仍以干果进行销售[6]。
食品所含营养成分的质量及其对健康的促进作用一直受消费者和研究人员的高度关注,而这些特性受食品加工方法的影响较大。我国枸杞的干制方式主要为自然晾晒、热风干燥、冷冻干燥、微波干燥、热泵干燥、脉冲真空干燥、红外干燥、电流体动力干燥和联合技术干燥等[7],而热风干燥技术由于干燥效率高、成本低,因此是枸杞干燥过程中应用最广泛的技术[5]。研究表明,枸杞预处理方式、干燥温度、干燥时间和干燥方式对枸杞产品的物理化学性质、营养品质和安全性具有极大的影响[8]。美拉德反应是一种通过蛋白质和糖类发生的非酶促褐变反应[9],食品在热加工过程中发生美拉德反应会伴随生成有害物质[10],其中食源性晚期糖基化产物(advanced glycation end-products, AGEs)和反应性α-二羰基化合物在热加工食品中的含量相对较高[11]。
AGEs分为内源性和食源性两类,内源性AGEs是由还原糖与蛋白质或氨基之间的相互作用导致它们在组织和体液中积累,食源性AGEs是在食品加工过程中形成的[12]。AGEs的产生不仅与食品自身成分有关,如蛋白质、脂肪和碳水化合物等[13];还与加工条件密切相关,如加工温度、加工时间和加工方式等,其中AGEs的形成受加工温度的影响较大[14-15]。唐晓敏[16]通过热风干燥、微波干燥和真空冷冻干燥处理枸杞,发现在干制过程中产热的热风干燥和微波干燥比真空冷冻干燥具有更高水平的荧光性AGEs。ZHANG等[17]研究了红茶在90、120、150 ℃干燥过程中AGEs的形成,发现在150 ℃的干燥过程中,每种AGEs的含量均显著高于90 ℃和120 ℃,且精氨嘧啶仅在150 ℃被检测到。因此,选择适宜的热风干制工艺可以减少加工过程中有害因子AGEs的产生。本研究选择40、50、60 ℃的热风条件对枸杞进行干制,目的是探究枸杞在干制过程中AGEs的形成规律以及与生物活性成分变化之间的联系。
1 材料与方法
1.1 材料与试剂
枸杞于2024年7月采自宁夏中宁县,将刚采摘的新鲜枸杞冷藏运输至实验室马上进行干制实验。碳酸钠(食品级)、甲酸(色谱纯)、甲醇(色谱纯)、乙腈(色谱纯),美国Millipore公司;乙酸铵,美国Sigma公司;氨水,美国Merck公司。
1.2 仪器与设备
DHG-9140A电热恒温鼓风干燥箱,上海精宏实验设备有限公司;Bioruptor超声波系统,Diagenode公司;Concentrator plu真空离心浓缩仪,Eppendorf公司;5430R、Eppendorf Centrifug、QTRAP 5500质谱仪,AB SCIEX公司;Nexera X2 LC-30AD超高压液相色谱仪,Shimadzu公司;Waters Acquity UPLC HSS T3色谱柱,美国Waters公司。
1.3 实验方法
1.3.1 枸杞干制过程
选择色泽均匀、颗粒饱满的优质枸杞,将枸杞用质量分数为30 g/L的Na2CO3溶液处理2 min,目的是为了除去枸杞表皮蜡质层,提高干制效率[18]。每份称取300 g采用热风处理至恒重,采用等时取样,选择40、50、60 ℃进行干制,以探究干制温度和干制时间对枸杞中的AGEs形成以及其它代谢物的影响。如图1所示,L-0 h:鲜枸杞;L40-14 h、L40-26 h、L40-38 h:在40 ℃下分别干制14、26、38 h的枸杞样品;L50-10 h、L50-20 h、L50-30 h:在50 ℃下分别干制10、20 h和30 h的枸杞样品;L60-6 h、L60-12 h、L60-18 h:在60 ℃下分别干制6、12 h和18 h的枸杞样品。本次实验为了进行质量控制(quality control,QC)同时制备了QC样本,QC样本为所有样品等量混合的样本。
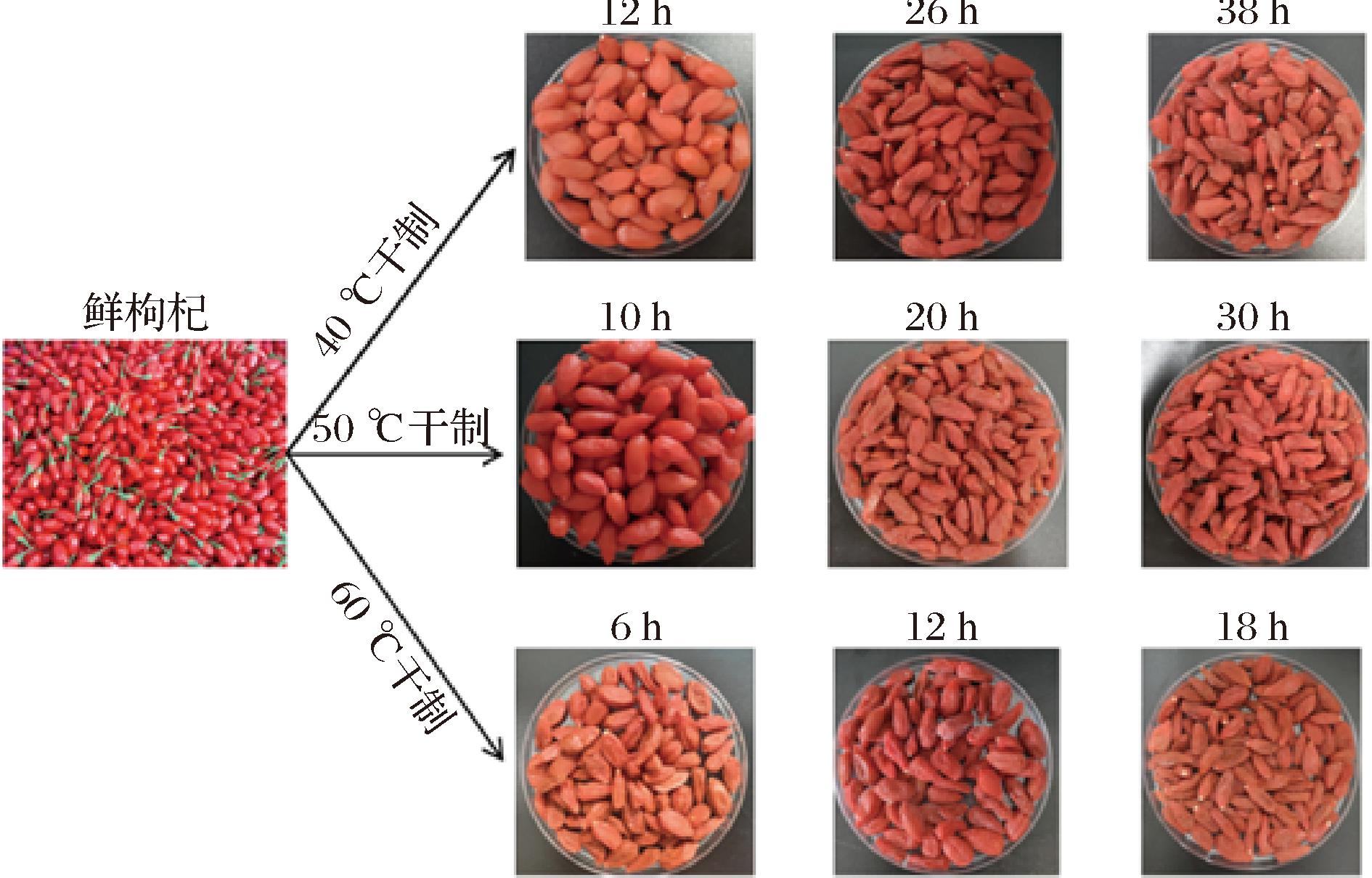
图1 枸杞的外观形态
Fig.1 Appearance of Lycium barbarum
1.3.2 代谢组学样品制备
每个样品称重50 mg,各加入400 μL预冷的80%甲醇水(体积比),加3颗钢珠,在组织破碎仪中低温匀浆破碎,再加入600 μL预冷的80%甲醇水(体积比),涡旋混匀,冰浴中超声20 min,-20 ℃静置1 h,16 000×g 4 ℃离心20 min,取上清液在高速真空浓缩离心机挥干[19]。样本复溶于100 μL预冷的QMT1000工作液(内标∶体积分数为50%的甲醇水=1∶9,体积比)中,20 000×g 4 ℃离心15 min,取上清液以备质谱进样分析。
1.3.3 LC-MS/MS分析
超高效液相色谱条件[20]:整个分析过程中样品置于4 ℃自动进样器中。HSS T3色谱柱(100 mm×2.1 mm,1.8 μm);进样量:5 μL,柱温:40 ℃,流速:0.2 mL/min;色谱流动相A:0.1%甲酸水溶液(体积比),B:乙腈。正离子模式液相梯度洗脱程序:0~2.5 min,0% B;2.5~9 min,30% B;9~10 min,100% B;10~15.4 min,B维持在100%;15.4~15.5 min,0% B。负离子模式液相梯度洗脱程序:0~2 min,0% B;2~2.5 min,20% B;2.5~3.5 min,40% B;3.5~4.5 min,50% B;4.5~10 min,100% B;10~15.4 min,B维持在100%;15.4~18.0 min,0% B。样本队列中插入QC样品,用于监测和评价系统的稳定性及实验数据的可靠性。
质谱条件[21]:电喷雾电离(electrospray ionization,ESI);样品采用正负离子模式检测;正离子模式,离子源温度:550 ℃;离子源气体Ⅰ(ion source gas1,GAS1):40 psi;离子源气体Ⅱ(ion source gas2,GAS2):50 psi;帘气(curtain gas,CUR):35 psi;离子喷雾电压(ion spray voltage floating,ISVF):5 500 V。负离子模式,离子源温度:550 ℃;离子源气体Ⅰ(ion source gas1,GAS1):40 psi;离子源气体Ⅱ(ion source gas2,GAS2):50 psi;帘气(curtain gas,CUR):35 psi;离子喷雾电压(ion spray voltage floating,ISVF):-4 500 V。采用MRM模式检测待测离子对。
1.4 数据处理
采用MultiQuant 3.0.2软件对检测到的代谢物进行提取,得到各代谢物的峰面积及保留时间。利用混标、保留时间、Q1/Q3离子对、二级质谱等相关条件进行代谢物鉴定。首先,对包括QC在内的所有样本数据进行主成分分析(principal component analysis,PCA),以评估其总体和组间差异,总的主成分为原始变量经正交变换生成的新的综合指标。选择同时具有多维统计分析变量投影重要性(variable importance in project, VIP)>1和单变量统计分析P<0.05的代谢物,作为具有显著性差异的代谢物。每组实验3次平行,结果以“平均值±标准差”的方式表示,采用IBM SPSS Statistics 27软件分析不同样本间的显著性。
2 结果与分析
2.1 实验质量控制评价
将所有样品等量混合制备QC样本,通过QC样本对数据的稳定性和重复性进行评价。所有检出代谢物的相对标准偏差(relative standard deviation,RSD)均小于30%,表明样本测试中数据稳定可靠。如图2-a所示,第一主成分(PC1)和第二主成分(PC2)分别解释了20.00%和13.71%的方差,并且所有QC样本紧密聚集在一起,表明本实验重复性较好。4个QC样本之间的相关性非常显著,确定了数据的质量和可靠性(图2-b)。
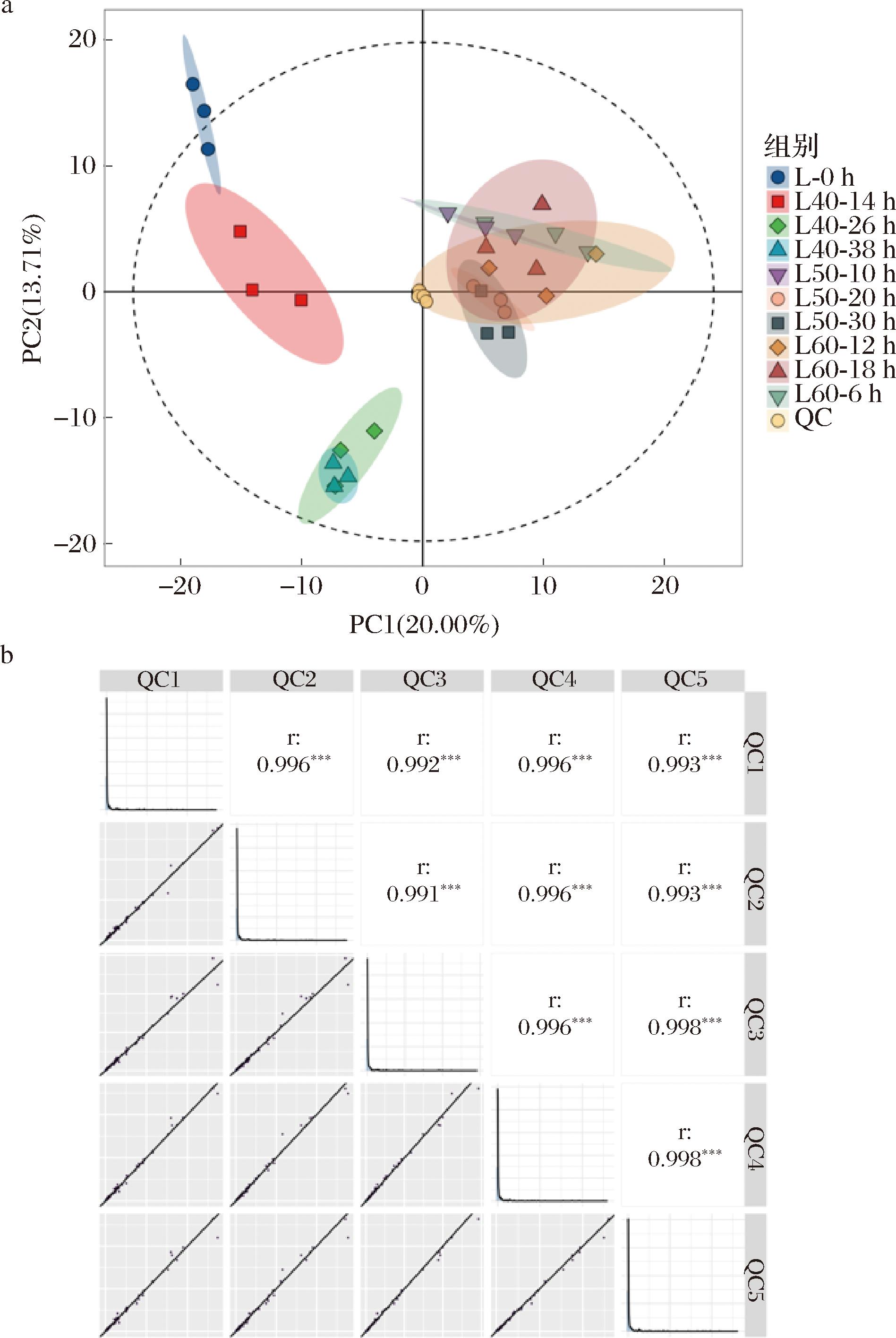
a-代谢物PCA得分图;b-4个QC样本的相关性
图2 分析系统概况
Fig.2 Analysis system overview
注:***表示极显著(P<0.001)。
2.2 代谢物分布情况
通过UHPLC-Q-Trap 5500 -MS靶向代谢组学在枸杞样品中共鉴定到了436种代谢物,正离子模式下有259种代谢物,负离子模式下有177种代谢物,分为18类。如图3所示,这些代谢产物为37种氨基酸、肽和类似物,28种有机酸及其衍生物,22种核苷、核苷酸和类似物,14种鞘脂类等。其中AGEs有8种,占比4.42%,说明AGEs是枸杞中较为重要的一类代谢产物。由图4可知,在50 ℃制干的枸杞中上调AGEs的数量最多,而在40 ℃制干枸杞中上调AGEs数量最少,且40 ℃的枸杞中没有下调AGEs。因此,为了探究枸杞在热风干制过程中AGEs的变化规律,以及与AGEs相关代谢物的变化,在下文进行了详细的分析。
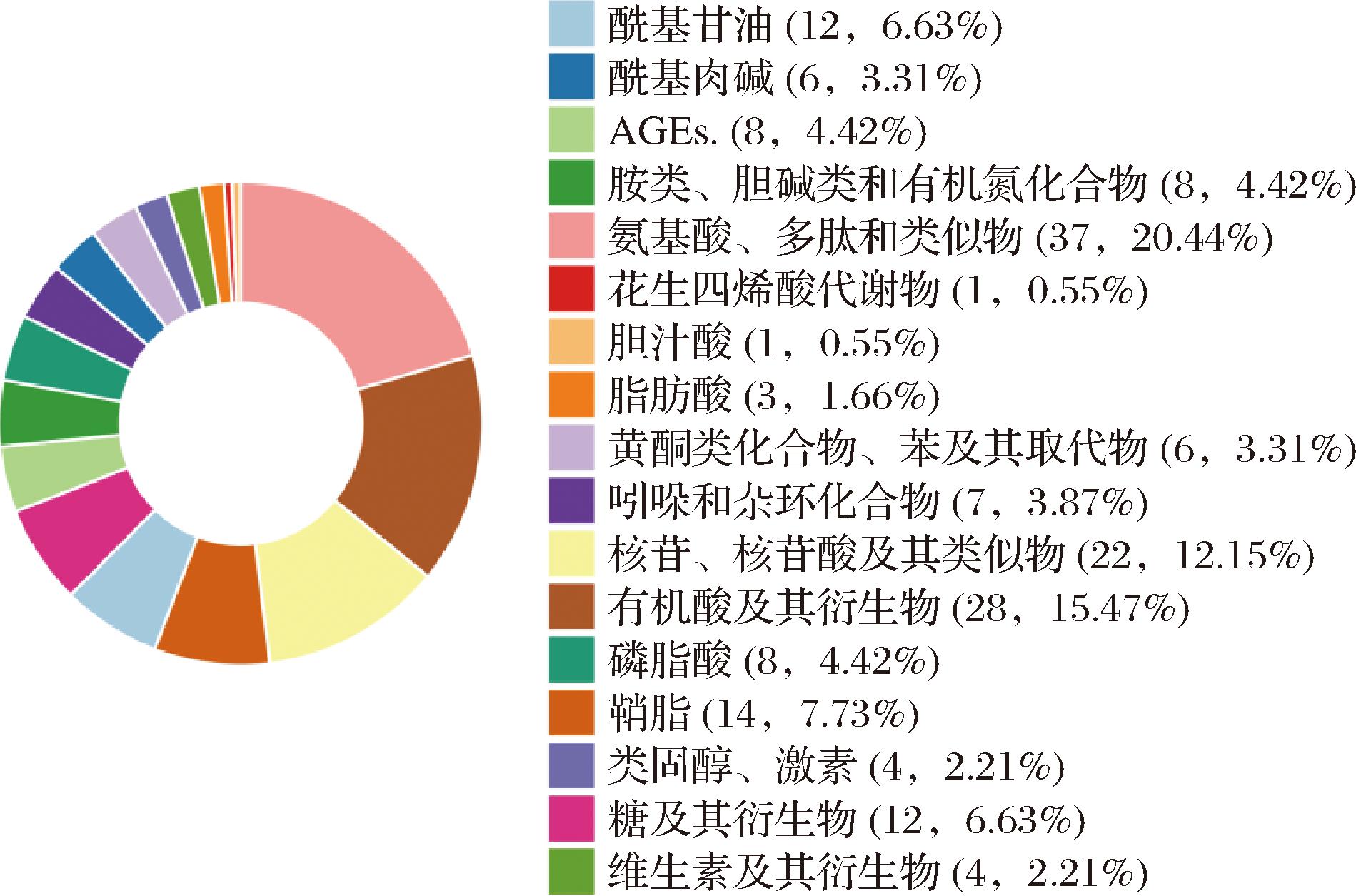
图3 代谢物类别及其数量总体分布
Fig.3 Overall distribution of metabolite classes and their quantities
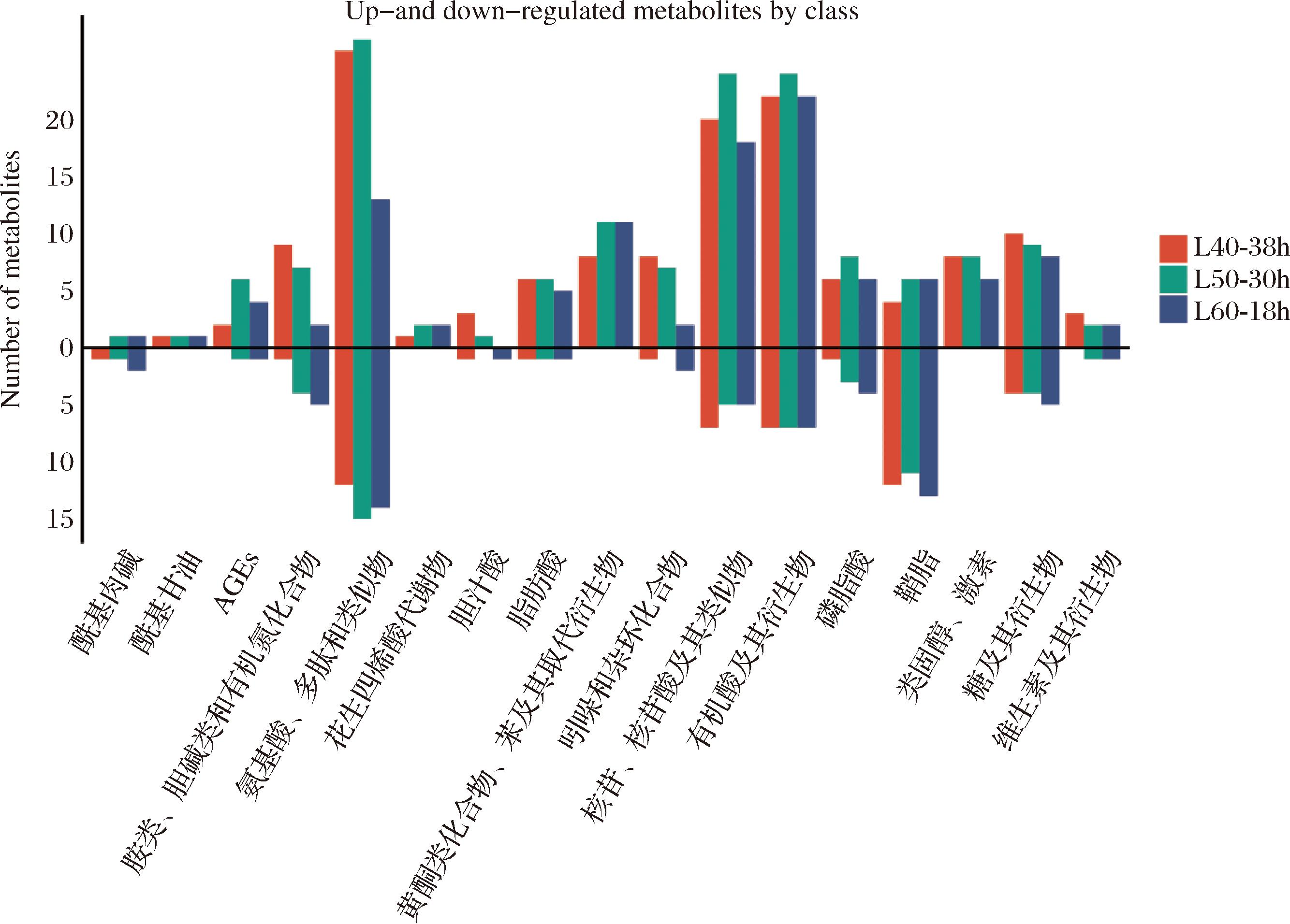
图4 差异代谢物分类
Fig.4 The classification of differential metabolites
2.3 枸杞干制中AGEs的形成规律
食源性AGEs主要指从食物中摄入的AGEs,是食物成分中的还原糖和含氮基团通过非酶促反应形成的。α-二羰基化合物是AGEs的前体,如甲基乙二醛(methylglyoxal,MGO)和乙二醛(glyoxal,GO)[22]。由表1和表2可知,本研究共鉴定出了8种AGEs,其中MGO会与赖氨酸残基交联生成羧乙基赖氨酸[Nε-(carboxyethyl)lysine, CEL],与精氨酸残基生成羧乙基精氨酸[Nε-(carboxyethyl)arginine, CEA]和甲基乙二醛-羟基咪唑酮异构体(methylglyoxal-hydroimidazolones, MG-H1);GO会与赖氨酸残基交联生成羧甲基赖氨酸[Nε-(carboxymethyl)lysine, CML],与精氨酸残基生成羧甲基精氨酸[Nε-(carboxymethyl)arginine, CMA]。而N6-苏氨酰、N6-草酰和N6-乳酰基也是由赖氨酸残基通过非酶促反应形成的,因此枸杞中赖氨酸衍生的AGEs比精氨酸衍生的AGEs高得多。在枸杞中鉴定出的AGEs中,N6-苏氨酰的含量最多,其次是CMA、N6-乳酰基、MG-H1、N6-草酰、CML和CEL。因此,可以将N6-苏氨酰和CMA作为枸杞中的代表性AGEs,用来评估枸杞中AGEs总量。而先前的研究是将CML和CEL作为评估食品中AGEs的指标,因此可能会影响对AGEs总量的评估。此外,N6-苏氨酰、N6-乳酰基和N6-草酰是食品中首次鉴定出的AGEs,从而丰富了食品在热加工过程中产生AGEs的种类。
表1 精氨酸衍生AGEs的变化
Table 1 Changes of arginine-derived AGEs
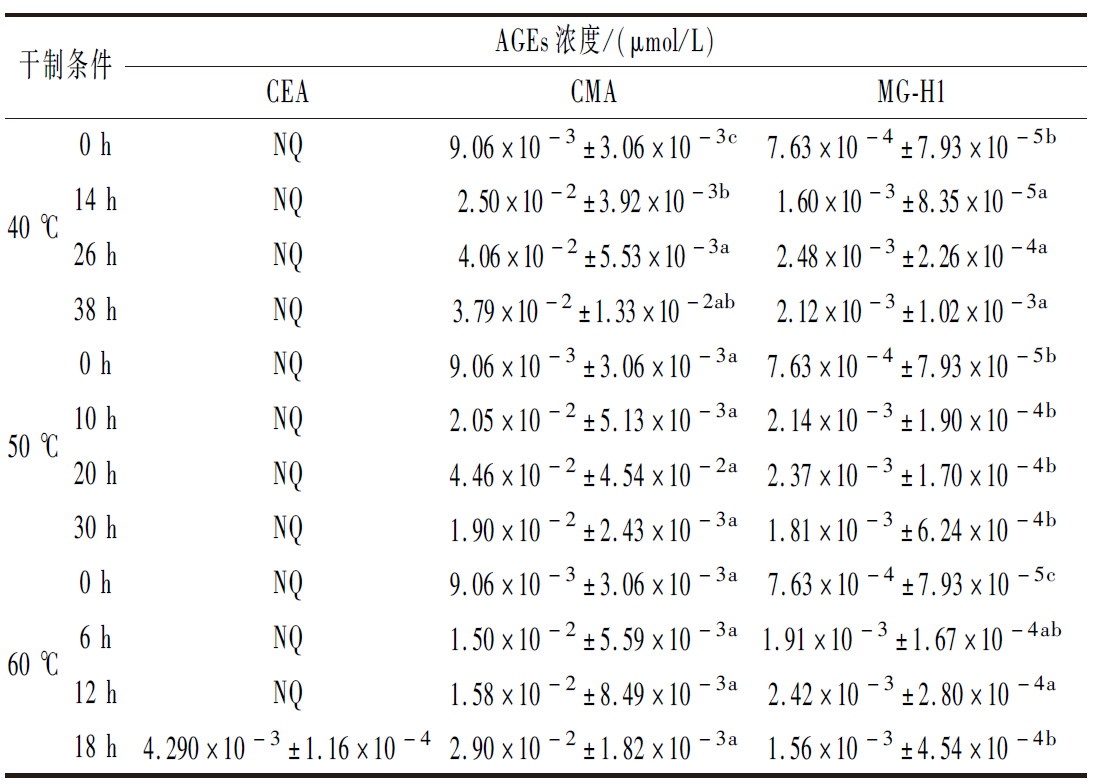
注:NQ表示最低检测限;不同的上标字母表示在相同温度、不同时间的干制条件下,样品之间存在显著差异(P < 0.05)(下同)。
表2 赖氨酸衍生AGEs的变化
Table 2 Changes of lysine-derived AGEs
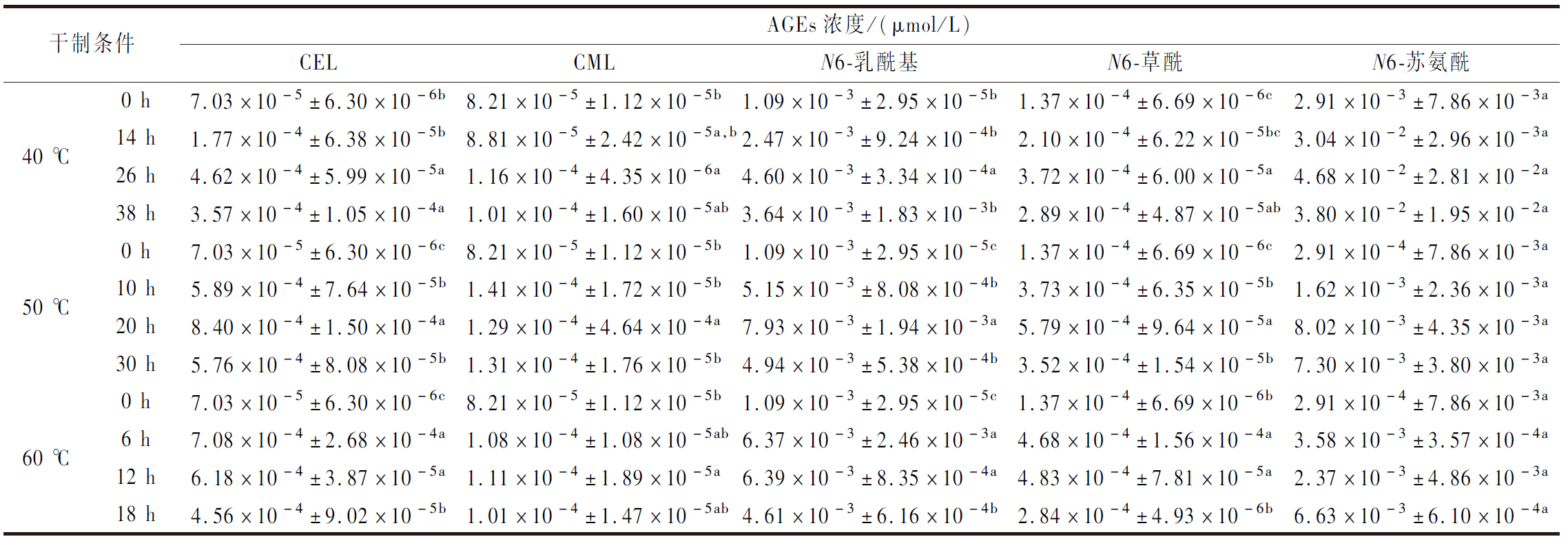
CEA在40 ℃和50 ℃的干制过程中其含量低于最低检测线,在60 ℃干制完成时CEA为4.290×10-3 μmol/L。鲜枸杞中存在一定含量的AGEs,随着干制时间的延长,AGEs的浓度显著增加。当结束干制时,AGEs的浓度有所下降,这与刘文婷[23]的研究结果一致。ZHANG等[24]研究发现:在湿热模式下,CML和CEL浓度在最初的90 min内增加,然后在120 min后下降;而吡咯啉浓度在30 min后增加,在60 min后又降低。此外,在50 ℃制干的枸杞中,赖氨酸衍生的AGEs普遍高于40 ℃和60 ℃干制处理的,这可能与40 ℃的干制温度较低,而60 ℃的干制时间较短有关。LIU等[25]发现油炸时间延长大大增加了AGEs的产生,而油炸时间较短时CML和CEL的形成受油炸温度的影响较小,这与本研究的结果一致。实验结果表明,枸杞在不同热风温度的干制过程中AGEs呈先上升后下降的变化趋势,且干制温度和干制时间都会影响AGEs的产生。
2.4 氨基酸与AGEs的联系
枸杞果实的营养价值归因于糖、有机酸、脂肪酸、类胡萝卜素、氨基酸和蛋白质、维生素和必需元素[26]。赖氨酸和精氨酸是AGEs的2种主要前体,它们可以与α-二羰基化合物交联生成的各种AGEs。赖氨酸和精氨酸衍生的AGEs普遍存在于食品中,尤其是热加工食品中[27],本研究通过热图可视化分析了枸杞干制过程中氨基酸含量的变化。如图5所示,鲜枸杞中的赖氨酸含量最高,随着干制时间的延长,赖氨酸的含量逐渐减少。且在50 ℃和60 ℃的干制过程中,赖氨酸减少的趋势更加明显,精氨酸在干制过程中呈现出与赖氨酸相似的变化趋势。由表1、表2结果可知,AGEs在50 ℃和60 ℃的枸杞样品中含量较高,这与赖氨酸和精氨酸的变化趋势相反,说明赖氨酸和精氨酸参与了AGEs的形成。赖氨酸和精氨酸不仅可以在美拉德反应的初始阶段与还原糖缩合,还可以通过参与氧化、缩合和Streker降解形成挥发性醛,这些美拉德反应将会不可避免地造成赖氨酸和精氨酸的损失[17]。随着干制时间的延长,枸杞中的各种氨基酸呈现下降的趋势,而氨基酸的减少会使枸杞的营养价值降低。且温度越高,氨基酸下降的趋势更加明显。
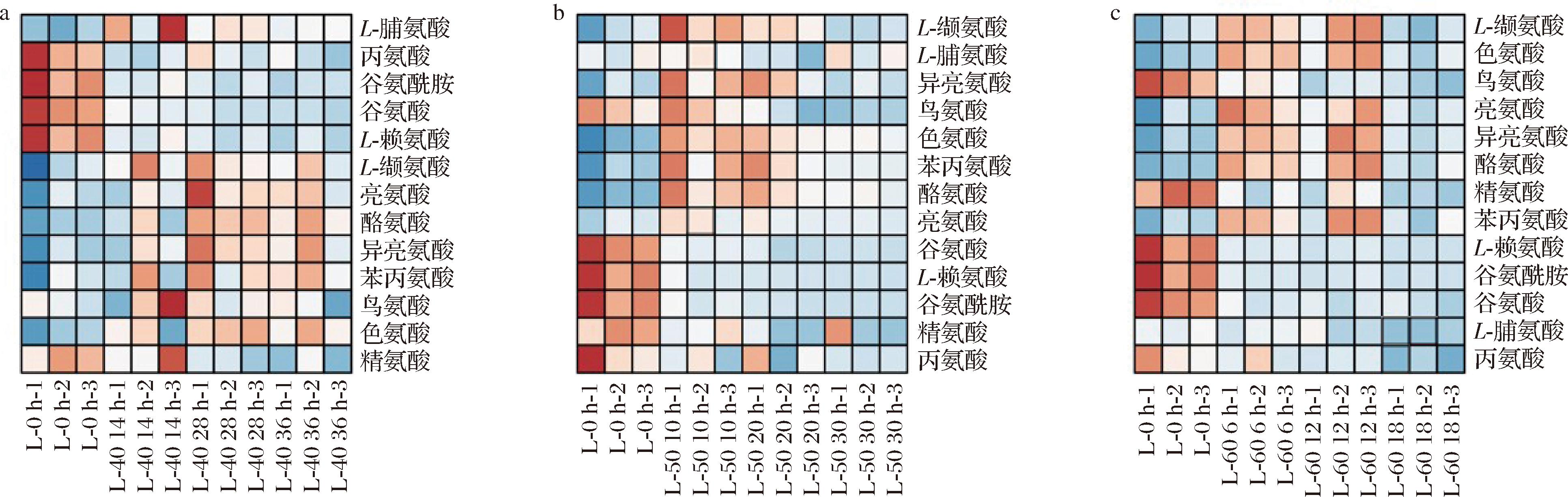
a-40 ℃干制枸杞;b-50 ℃干制枸杞;c-60 ℃干制枸杞
图5 枸杞干制过程中氨基酸含量变化热图
Fig.5 Heat map of amino acid content change during the drying process of Lycium barbarum
2.5 维生素与AGEs的联系
维生素是维持人体正常生理功能所必需的有机物质,在新陈代谢中起着重要作用。如图6所示,鲜枸杞中维生素的含量普遍较低,这可能与鲜枸杞水分含量较高有关。如图6-b和图6-c所示,在50 ℃和60 ℃的干制条件下,随着干制时间的延长,维生素B6的含量先上升后下降。枸杞在干制过程中大多数AGEs的含量也呈现先上升后下降的变化趋势,说明维生素B6的变化与AGEs有关。而硫胺素和烟酰胺在不同温度下随着干制时间的延长而增加,这可能是因为它们会参与抑制AGEs的形成。不同维生素的水平变化有所差异,这可能与它们参与抑制AGEs的方式有关。大多数维生素体可以抑制AGEs的形成,其中维生素B6是通过清除自由基和螯合金属离子来减少AGEs的形成[28]。维生素D对AGEs及其受体具有改善作用[29],并且维生素D的代谢物也可以减少糖基化修饰。而抗坏血酸是通过与葡萄糖竞争结合蛋白质,从而减少体外AGEs的产生[30]。
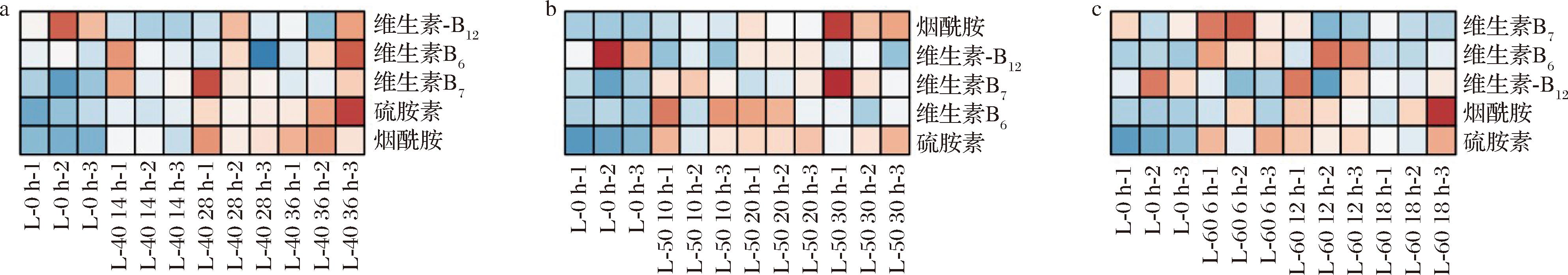
a-40 ℃干制枸杞;b-50 ℃干制枸杞;c-60 ℃干制枸杞
图6 枸杞干制过程中维生素含量变化热图
Fig.6 Heat map of vitamin content change during the drying process of Lycium barbarum
2.6 碳水化合物与AGEs的联系
糖类约占枸杞干果的40%,对枸杞的口感、品质和加工具有重要的影响[31]。如图7所示,枸杞在干制过程中葡萄糖、蔗糖、果糖和甘露糖发生了显著的变化,它们的水平有升高的趋势,但不同糖型有所差异,这可能是因为不同种类的糖对美拉德反应的影响不同。枸杞在干制过程中AGEs呈先上升后下降或者持续增加的变化趋势,而碳水化合物的水平也呈现相似的变化,说明碳水化合物对AGEs的形成有促进作用。TSAI等[32]研究发现,商业烘焙产品中总AGEs含量与总糖含量之间也存在显著的正相关。反应温度、反应时间和糖型都会促进CML的形成,其中糖型对CML的影响顺序为乳糖>葡萄糖>蔗糖[33]。
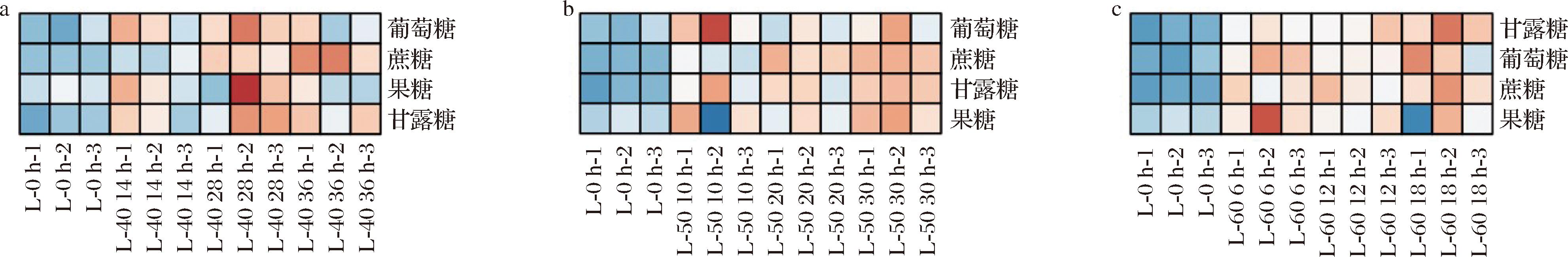
a-40 ℃干制枸杞;b-50 ℃干制枸杞;c-60 ℃干制枸杞
图7 枸杞干制过程中碳水化合物含量变化热图
Fig.7 Heat map of carbohydrate content change during the drying process of Lycium barbarum
2.7 脂肪酸与AGEs的联系
在加工富含不饱和脂肪酸的食品时,脂质和脂质氧化是导致AGEs形成的主要因素[34]。脂质是通过影响Amadori产物和α-二羰基化合物的生成来促进赖氨酸衍生AGEs的形成[35]。如图8所示,饱和脂肪酸[FA(4:0)和FA(8:0)]的水平在枸杞干制过程中有下降的趋势,但不饱和脂肪酸[FA(18:2)、FA(22:4)和13S-羟基十八碳二烯酸]的水平上升较为明显。这可能是因为饱和脂肪酸参与了美拉德反应,因此对食品中的AGEs有明显的抑制作用;而对于不饱和脂肪酸,其不饱和度与AGEs水平呈正相关。PEAKE等[36]研究发现,饱和脂肪酸降低了CML和CEL,同时增加了MG-H1;而花生四烯酸、二十碳五烯酸和二十二碳六烯酸对CEL和MG-H1没有影响,但会显著降低CML的产生。
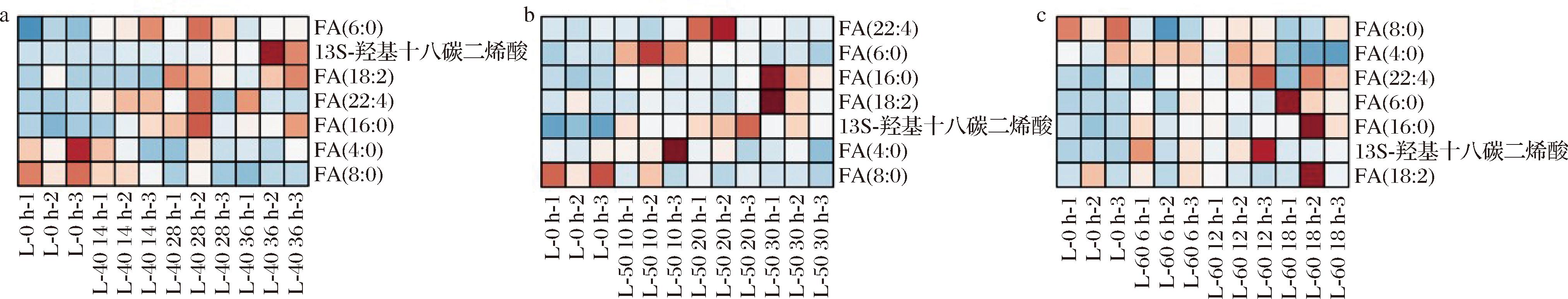
a-40 ℃干制枸杞;b-50 ℃干制枸杞;c-60 ℃干制枸杞
图8 枸杞干制过程中脂肪酸含量变化热图
Fig.8 Heat map of fatty acid content change during the drying process of Lycium barbarum
3 结论
本研究分析了干制温度和干制时间对枸杞中AGEs形成的影响,以及氨基酸、维生素、碳水化合物和脂肪酸与AGEs之间的联系。在枸杞中鉴定出了8种AGEs,由赖氨酸衍生的AGEs分别是CML、CEL、N6-苏氨酰、N6-草酰和N6-乳酰基,由精氨酸衍生的AGEs分别是CMA、CEA和MG-H1,因此赖氨酸衍生的AGEs高于精氨酸衍生的AGEs。实验结果表明,鲜枸杞中具有一定含量的AGEs,但在不同热风温度的干制过程中,AGEs的含量随着干制时间的延长而增加,当干制结束时,AGEs的含量有所下降。与干制时间相比,干制温度对AGEs形成的影响更大。此外,枸杞中的赖氨酸和精氨酸参与了AGEs的形成,维生素和饱和脂肪酸对AGEs表现出一定的抑制作用,而碳水化合物和不饱和脂肪酸与AGEs的水平有关。因此,通过探究枸杞在热风干制过程中AGEs的形成规律,从而为控制AGEs的形成提供理论参考。
[1] GONG H G, REHMAN F, MA Y, et al.Germplasm resources and strategy for genetic breeding of Lycium species:A review[J].Frontiers in Plant Science, 2022, 13:802936.
[2] LU J X, XIANG X Q, ZHANG Z F, et al.Nutritional compositions, phytochemical components, functional activities, and food applications of Lycium ruthenicum Murr.:A comprehensive review[J].Journal of Food Composition and Analysis, 2025, 140:107301.
[3] ![]() B B,
B B, ![]() M D, et al.Health benefits and applications of goji berries in functional food products development:A review[J].Antioxidants, 2022, 11(2):248.
M D, et al.Health benefits and applications of goji berries in functional food products development:A review[J].Antioxidants, 2022, 11(2):248.
[4] ZENG T, LIU B, BI L S, et al.Effects of different drying methods on quality and water distribution of Lycium barbarum[J].Journal of Food Process Engineering, 2023, 46(12):e14482.
[5] 王兆凯, 任广跃, 段续, 等.预处理与干燥方式对枸杞干燥特性及品质影响的研究进展[J].食品与发酵工业, 2023, 49(19):367-375.WANG Z K, REN G Y, DUAN X, et al.Research progress on influence of pretreatment and drying methods on drying characteristics and quality of goji[J].Food and Fermentation Industries, 2023, 49(19):367-375.
[6] 张琦, 朱绚绚, 熊佳丽, 等.枸杞营养功能特性及其产品开发现状[J].食品与发酵工业, 2024, 50(15):398-408.ZHANG Q, ZHU X X, XIONG J L, et al.Research progress of functional properties of wolfberry and development of its products[J].Food and Fermentation Industries, 2024, 50(15):398-408.
[7] CUI C J, ZHAO D D, HUANG J, et al.Progress on research and development of goji berry drying:A review[J].International Journal of Food Properties, 2022, 25(1):435-449.
[8] 王庆惠, 罗燕, 杨莉玲, 等. 不同干燥条件对枸杞热风干燥特性和品质的影响[J]. 食品工业科技, 2025, 46(8):202-210.WANG Q H, LUO Y, YANG L L, et al. Effects of drying conditions on hot-air drying characteristics and quality of goji berries[J]. Science and Technology of Food Industry, 2025, 46(8):202-210.
[9] SHENGBU M, AI L, SHI Q, et al. Research progress of Maillard reaction and its application in processing of traditional Chinese medicine[J]. Natural Product Communications, 2024, 19(11):1934578X241290620.
[10] LIU Y, LU L, YUAN S F, et al.Formation of advanced glycation end-products and α-dicarbonyl compounds through Maillard reaction:Solutions from natural polyphenols[J].Journal of Food Composition and Analysis, 2023, 120:105350.
[11] 于小慧. 焙烤花生中糖基化终产物和杂环胺的形成与控制[D].河南:河南工业大学, 2022.YU X H.Formation and control of advanced glycation end products and heterocyclic aromatic amines in roasted peanut[D].Henan:Henan University of Technology, 2022.
[12] PATEL S S, BAINS A, SHARMA M, et al.Recent trends in advanced glycation end products in foods:Formation, toxicity, and innovative strategies for extraction, detection, and inhibition[J].Foods, 2024, 13(24):4045.
[13] GU M J, LEE Y R, KIM D, et al.Comprehensive research on the properties of advanced glycation end products in food and biological samples and their harmful role in inducing metabolic diseases[J].Comprehensive Reviews in Food Science and Food Safety, 2024, 23(5):e13412.
[14] LU J N, LI M Y, SHEN M Y, et al.Advanced glycation end products and nitrosamines in sausages influenced by processing parameters, food additives and fat during thermal processing[J].Foods, 2023, 12(2):394.
[15] 宫瑞泽. 煮炸鹿茸中晚期糖基化终产物的生成规律及调控机制研究[D].北京:中国农业科学院, 2020.GONG R Z.Study on the formation regularity and regulation mechanism of advanced glycosylation end products in boiled velvet antler[D].Beijing:Chinese Academy of Agricultural Sciences, 2020.
[16] 唐晓敏. 干燥技术对枸杞多糖理化性质及美拉德反应产物的影响[D].北京:北京林业大学, 2022.TANG X M.Effect of drying technologies on physicochemical characteristics of polysaccharides and Maillard reaction products in dried goji berries[D].Beijing:Beijing Forestry University, 2022.
[17] ZHANG W, ZHANG B B, YE Y, et al. Corrigendum to “Methylglyoxal-hydroimidazolones (MG-Hs) instead of Nε-(carboxymethyl)-l-lysine (CML) is the major advanced glycation end-product during drying process in black tea”[Food Chem. 333(2020)127499[J]. Food Chemistry, 2021, 350:129326.
[18] 马奇虎, 郭雨桐, 唐辉, 等.不同干燥方式枸杞干果微观结构与营养成分对比分析[J].农产品加工,2022(17):72-74;78.MA Q H, GUO Y T, TANG H, et al.Comparative analysis of microstructure and nutrient composition of dried fruits of Lycium barbarum by different drying methods[J].Farm Products Processing, 2022(17):72-74;78.
[19] 奉综涛, 田梦乐, 买地那·帕尔哈提, 等.西藏三种枸杞基本营养成分及代谢物差异分析[J].食品与发酵工业, 2025,51(16):351-362. FENG Z T, TIAN M L, PAERHATI M D N, et al.Differences in basic nutrients and metabolites in three types of Lycium chinense in Tibet[J].Food and Fermentation Industries,2025,51(16):351-362.
[20] SANG S M, WANG W X, ZHAO Y T, et al.Quantitative analysis of a panel of advanced glycation end products through the integration of enzymatic hydrolysis and targeted metabolomics[J].Current Developments in Nutrition, 2024, 8:103162.
[21] 潘鑫. 香豆素抑制藜麦籽粒及穗发芽的作用研究[D].成都:成都大学, 2024.PAN X.Study on the inhibitory effect of coumarin on quinoa grain and pre-harvest sprouting[D].Chengdu:Chengdu University, 2024.
[22] 郭鸿阳. 半胱氨酸对油炸薯片中二羰基化合物、晚期糖基化终产物及其品质的影响[D].广州:暨南大学, 2021.GUO H Y.Effect of cysteine on the contents of dicarbonyl compounds, advanced glycation end products, and other quality parameters in fried potato chips[D].Guangzhou:Jinan University, 2021.
[23] 刘文婷. 加工条件和加工辅料对烘烤葵花籽中伴生危害物生成的影响[D].南昌:南昌大学, 2023.LIU W T.Effects of processing conditions and ingredients on heatinduced hazards in sunflower seeds processing[D].Nanchang:Nanchang University, 2023.
[24] ZHANG C Y, GUO Y R, HOU T Y, et al.Formation of advanced glycation end products in glucose-amino acid models of Maillard reaction under dry- and wet-heating conditions[J].Journal of the Science of Food and Agriculture, 2025, 105(4):2342-2351.
[25] LIU Q Y, WANG S, WANG X Y, et al.The relationship between the formation of advanced glycation end products and quality attributes of fried sturgeon fillets[J].LWT, 2022, 159:113161.
[26] ![]() A Ž, KAMILOGLU S, et al. Chemical composition, nutritional and health related properties of the medlar (Mespilus germanica L.): From medieval glory to underutilized fruit[J]. Phytochemistry Reviews, 2023, 22(6):1663-1690.
A Ž, KAMILOGLU S, et al. Chemical composition, nutritional and health related properties of the medlar (Mespilus germanica L.): From medieval glory to underutilized fruit[J]. Phytochemistry Reviews, 2023, 22(6):1663-1690.
[27] LIN Y Y, HUANG S F, LIAO K W, et al.Quantitation of α-dicarbonyls, lysine- and arginine-derived advanced glycation end products, in commercial canned meat and seafood products[J].Journal of Agricultural and Food Chemistry, 2023, 71(17):6727-6737.
[28] VERN F.Vitamin B6 and diabetes and its role in counteracting advanced glycation end products[J].Vitamins and Hormones, 2024, 125:401-438.
F.Vitamin B6 and diabetes and its role in counteracting advanced glycation end products[J].Vitamins and Hormones, 2024, 125:401-438.
[29] KHEIROURI S, ALIZADEH M.Vitamin D and advanced glycation end products and their receptors[J].Pharmacological Research, 2020, 158:104879.
[30] SONG Q H, LIU J J, DONG L Y, et al.Novel advances in inhibiting advanced glycation end product formation using natural compounds[J].Biomedicine &Pharmacotherapy, 2021, 140:111750.
[31] 罗群, 王莹, 李耀磊, 等.枸杞子化学成分及质量评价研究进展[J].中国药事, 2024, 38(11):1323-1337.LUO Q, WANG Y, LI Y L, et al.Progress of chemical composition and quality evaluation of Lycium barbarum L[J].Chinese Pharmaceutical Affairs, 2024, 38(11):1323-1337.
[32] TSAI C Y, LIAO K W, HSIA S M, et al.Key factors influencing the formation of α-dicarbonyls and dietary advanced glycation end products in bread and commercial bakery products:Impacts of sugar, lipid and gluten protein[J].Food Chemistry:X, 2025, 26:102286.
[33] LI L, HAN L P, FU Q Y, et al.Formation and inhibition of Nε-(carboxymethyl)lysine in saccharide-lysine model systems during microwave heating[J].Molecules, 2012, 17(11):12758-12770.
[34] ZHAO X, YUE L, LIU X C, et al.Contribution of linoleic acid to the formation of advanced glycation end products in model systems during heat treatment[J].Czech Journal of Food Sciences, 2017, 35(5):367-375.
[35] WANG Y T, HU H Y, MCCLEMENTS D J, et al.Effect of fatty acids and triglycerides on the formation of lysine-derived advanced glycation end-products in model systems exposed to frying temperature[J].RSC Advances, 2019, 9(27):15162-15170.
[36] PEAKE B, GHETIA M, GERBER C, et al.Role of saturated and unsaturated fatty acids on dicarbonyl-albumin derived advanced glycation end products in vitro[J].Amino Acids, 2022, 54(5):721-732.